Свинец (произносится как «led») — химический элемент ; его символ Pb (от латинского plumbum ) и атомный номер 82. Это тяжелый металл , который плотнее большинства обычных материалов. Свинец мягкий и ковкий , а также имеет относительно низкую температуру плавления . В свежем виде свинец имеет блестящий серый цвет с оттенком синего. Он тускнеет до тускло-серого цвета при контакте с воздухом. Свинец имеет самый высокий атомный номер среди всех стабильных элементов , и три его изотопа являются конечными точками основных цепочек ядерного распада более тяжелых элементов.
Свинец является относительно инертным постпереходным металлом . Его слабый металлический характер иллюстрируется его амфотерной природой; свинец и оксиды свинца реагируют с кислотами и основаниями , и он имеет тенденцию образовывать ковалентные связи . Соединения свинца обычно находятся в степени окисления +2 , а не в состоянии +4, обычном для более легких членов углеродной группы . Исключения в основном ограничиваются свинцовоорганическими соединениями . Как и более легкие члены группы, свинец имеет тенденцию связываться сам с собой ; он может образовывать цепи и полиэдрические структуры.
Поскольку свинец легко извлекается из руд , доисторические люди на Ближнем Востоке знали о нем . Галенит является основной рудой свинца, которая часто содержит серебро. Интерес к серебру помог инициировать широкомасштабную добычу и использование свинца в Древнем Риме . Производство свинца снизилось после падения Рима и не достигало сопоставимых уровней до промышленной революции . Свинец сыграл решающую роль в развитии печатного станка , поскольку подвижные литеры можно было относительно легко отливать из свинцовых сплавов. [9] В 2014 году ежегодное мировое производство свинца составляло около десяти миллионов тонн, более половины из которых приходилось на переработку. Высокая плотность свинца, низкая температура плавления, пластичность и относительная инертность к окислению делают его полезным. Эти свойства в сочетании с его относительной распространенностью и низкой стоимостью привели к его широкому использованию в строительстве , сантехнике , аккумуляторах , пулях , дробях , грузиках , припоях , оловянной посуде , легкоплавких сплавах , свинцовых красках , этилированном бензине и радиационной защите .
Свинец — нейротоксин , который накапливается в мягких тканях и костях. Он повреждает нервную систему и нарушает работу биологических ферментов , вызывая неврологические расстройства от проблем с поведением до повреждения мозга, а также влияет на общее состояние здоровья, сердечно-сосудистую и почечную системы. Токсичность свинца была впервые задокументирована древнегреческими и римскими писателями, которые отметили некоторые симптомы отравления свинцом , но широкое признание в Европе получило в конце 19 века нашей эры.
Атом свинца имеет 82 электрона , расположенных в электронной конфигурации [ Xe ]4f 14 5d 10 6s 2 6p 2 . Сумма первой и второй энергий ионизации свинца — полная энергия, необходимая для удаления двух 6p-электронов — близка к таковой у олова , верхнего соседа свинца в группе углерода . Это необычно; энергии ионизации обычно падают по мере спуска по группе, поскольку внешние электроны элемента становятся более удаленными от ядра и более экранированными меньшими орбиталями.
Сумма первых четырех энергий ионизации свинца превышает таковую у олова, [10] вопреки тому, что предсказывают периодические тенденции . Это объясняется релятивистскими эффектами , которые становятся значительными в более тяжелых атомах, [11] которые сжимают s- и p-орбитали таким образом, что 6s-электроны свинца имеют большую энергию связи, чем его 5s-электроны. [12] Следствием этого является так называемый эффект инертной пары : 6s-электроны свинца неохотно участвуют в связывании, стабилизируя состояние окисления +2 и делая расстояние между ближайшими атомами в кристаллическом свинце необычно большим. [13]
Более легкие конгенеры углеродной группы свинца образуют стабильные или метастабильные аллотропы с тетраэдрически координированной и ковалентно связанной алмазной кубической структурой. Энергетические уровни их внешних s- и p-орбиталей достаточно близки, чтобы позволить смешивание в четыре гибридные sp 3 -орбитали. В свинце эффект инертной пары увеличивает разделение между его s- и p-орбиталями, и зазор не может быть преодолен энергией, которая высвободилась бы дополнительными связями после гибридизации. [14] Вместо того, чтобы иметь алмазную кубическую структуру, свинец образует металлические связи , в которых только p-электроны делокализованы и разделены между ионами Pb 2+ . Следовательно, свинец имеет гранецентрированную кубическую структуру [15], как и двухвалентные металлы аналогичного размера [16] кальций и стронций . [17] [a] [b] [c]
Чистый свинец имеет яркий, блестящий серый цвет с оттенком синего. [22] Он тускнеет при контакте с влажным воздухом и приобретает тусклый вид, оттенок которого зависит от преобладающих условий. Характерные свойства свинца включают высокую плотность , ковкость, пластичность и высокую устойчивость к коррозии из-за пассивации . [23]

Плотноупакованная гранецентрированная кубическая структура свинца и высокий атомный вес приводят к плотности [24] 11,34 г/см 3 , что больше, чем у обычных металлов, таких как железо (7,87 г/см 3 ), медь (8,93 г/см 3 ) и цинк (7,14 г/см 3 ). [25] Эта плотность является источником идиомы « пролететь как свинцовый шар» . [26] [27] [d] Некоторые более редкие металлы плотнее: вольфрам и золото оба имеют плотность 19,3 г/см 3 , а осмий — самый плотный известный металл — имеет плотность 22,59 г/см 3 , что почти вдвое больше, чем у свинца. [28]
Свинец — очень мягкий металл с твердостью по шкале Мооса 1,5; его можно поцарапать ногтем. [29] Он довольно ковкий и несколько пластичный. [30] [e] Объемный модуль упругости свинца — мера его легкости сжимаемости — составляет 45,8 ГПа . Для сравнения, у алюминия он составляет 75,2 ГПа; у меди — 137,8 ГПа; у мягкой стали — 160–169 ГПа. [31] Прочность свинца на растяжение составляет 12–17 МПа, что является низким показателем (у алюминия он в 6 раз выше, у меди — в 10 раз, а у мягкой стали — в 15 раз выше); его можно усилить, добавив небольшое количество меди или сурьмы . [32]
Температура плавления свинца — 327,5 °C (621,5 °F) [33] — очень низкая по сравнению с большинством металлов. [24] [f] Его температура кипения 1749 °C (3180 °F) [33] является самой низкой среди элементов углеродной группы. Электрическое сопротивление свинца при 20 °C составляет 192 наноом -метра, что почти на порядок выше, чем у других промышленных металлов (меди при15,43 нОм·м ; золото20,51 нОм·м ; и алюминий на24,15 нОм·м ). [35] Свинец является сверхпроводником при температурах ниже 7,19 К ; [36] это самая высокая критическая температура среди всех сверхпроводников I типа и третья по величине среди элементарных сверхпроводников. [37]
Природный свинец состоит из четырех стабильных изотопов с массовыми числами 204, 206, 207 и 208, [38] и следов шести короткоживущих радиоизотопов с массовыми числами 209–214 включительно. Большое количество изотопов согласуется с четным атомным числом свинца. [g] Свинец имеет магическое число протонов (82), для которого модель ядерной оболочки точно предсказывает особенно стабильное ядро. [39] Свинец-208 имеет 126 нейтронов, еще одно магическое число, которое может объяснить, почему свинец-208 необычайно стабилен. [39]
Благодаря своему высокому атомному числу свинец является самым тяжелым элементом, естественные изотопы которого считаются стабильными; свинец-208 является самым тяжелым стабильным ядром. (Ранее это различие принадлежало висмуту с атомным числом 83, пока в 2003 году не было обнаружено, что его единственный первичный изотоп , висмут-209, распадается очень медленно.) [h] Четыре стабильных изотопа свинца теоретически могут подвергаться альфа-распаду до изотопов ртути с выделением энергии, но этого не наблюдалось ни для одного из них; их прогнозируемые периоды полураспада составляют от 10 35 до 10 189 лет [42] (по крайней мере, в 10 25 раз больше текущего возраста Вселенной).
Три стабильных изотопа обнаружены в трех из четырех основных цепочек распада : свинец-206, свинец-207 и свинец-208 являются конечными продуктами распада урана-238 , урана-235 и тория-232 соответственно. [43] Эти цепочки распада называются урановой цепочкой , актиниевой цепочкой и ториевой цепочкой . [44] Их изотопные концентрации в образце природной породы в значительной степени зависят от присутствия этих трех родительских изотопов урана и тория. Например, относительное содержание свинца-208 может варьироваться от 52% в обычных образцах до 90% в ториевых рудах; [45] по этой причине стандартный атомный вес свинца указан только с точностью до одного десятичного знака. [46] С течением времени отношение свинца-206 и свинца-207 к свинцу-204 увеличивается, поскольку первые два дополняются радиоактивным распадом более тяжелых элементов, а последний — нет; это позволяет проводить датирование свинцом-свинцом . По мере распада урана на свинец их относительные количества изменяются; это основа для датирования ураном-свинцом . [47] Свинец-207 проявляет ядерный магнитный резонанс , свойство, которое использовалось для изучения его соединений в растворе и твердом состоянии, [48] [49] в том числе в организме человека. [50]

Помимо стабильных изотопов, которые составляют почти весь свинец, существующий в природе, существуют следовые количества нескольких радиоактивных изотопов. Одним из них является свинец-210; хотя его период полураспада составляет всего 22,2 года, [38] небольшие количества встречаются в природе, поскольку свинец-210 образуется в результате длинной серии распада, которая начинается с урана-238 (который присутствует на Земле миллиарды лет). Свинец-211, -212 и -214 присутствуют в цепочках распада урана-235, тория-232 и урана-238 соответственно, поэтому следы всех трех этих изотопов свинца обнаруживаются в природе. Небольшие следы свинца-209 возникают в результате очень редкого кластерного распада радия-223, одного из дочерних продуктов природного урана-235, и цепочки распада нептуния-237, следы которого образуются при захвате нейтронов в урановых рудах. Свинец-213 также встречается в цепочке распада нептуния-237. Свинец-210 особенно полезен для определения возраста образцов путем измерения его отношения к свинцу-206 (оба изотопа присутствуют в одной цепочке распада). [51]
Всего было синтезировано 43 изотопа свинца с массовыми числами 178–220. [38] Свинец-205 является наиболее стабильным радиоизотопом с периодом полураспада около 1,70 × 107 лет. [7] [i] Вторым по стабильности является свинец-202, период полураспада которого составляет около 52 500 лет, что дольше, чем у любого из естественных следовых радиоизотопов. [38]

Массовый свинец, подвергающийся воздействию влажного воздуха, образует защитный слой различного состава. Карбонат свинца (II) является распространенным компонентом; [53] [54] [55] сульфат или хлорид также могут присутствовать в городских или морских условиях. [56] Этот слой делает массовый свинец фактически химически инертным на воздухе. [56] Мелко измельченный свинец, как и многие металлы, является пирофорным , [57] и горит голубовато-белым пламенем. [58]
Фтор реагирует со свинцом при комнатной температуре, образуя фторид свинца(II) . Реакция с хлором похожа, но требует нагревания, так как образующийся слой хлорида снижает реакционную способность элементов. [56] Расплавленный свинец реагирует с халькогенами, образуя халькогениды свинца(II). [59]
Металлический свинец устойчив к серной и фосфорной кислоте , но не к соляной или азотной кислоте ; результат зависит от нерастворимости и последующей пассивации соли продукта. [60] Органические кислоты, такие как уксусная кислота , растворяют свинец в присутствии кислорода. [56] Концентрированные щелочи растворяют свинец и образуют плюмбиты . [61]
Свинец показывает две основные степени окисления: +4 и +2. Четырехвалентное состояние является общим для группы углерода. Двухвалентное состояние редко встречается у углерода и кремния , второстепенно у германия, важно (но не преобладает) для олова и является более важным из двух степеней окисления для свинца. [56] Это объясняется релятивистскими эффектами , в частности эффектом инертной пары , который проявляется, когда существует большая разница в электроотрицательности между свинцом и оксидными , галогенидными или нитридными анионами, что приводит к значительному частичному положительному заряду на свинце. Результатом является более сильное сокращение 6s-орбитали свинца, чем в случае 6p-орбитали, что делает ее довольно инертной в ионных соединениях. Эффект инертной пары менее применим к соединениям, в которых свинец образует ковалентные связи с элементами со схожей электроотрицательностью, такими как углерод в свинцовоорганических соединениях. В них 6s- и 6p-орбитали остаются одинакового размера, а sp 3- гибридизация по-прежнему энергетически выгодна. Свинец, как и углерод, в таких соединениях преимущественно четырехвалентен. [62]
Существует относительно большая разница в электроотрицательности свинца (II) — 1,87 и свинца (IV) — 2,33. Эта разница отмечает изменение тенденции к повышению стабильности степени окисления +4 по мере спуска по углеродной группе; олово, для сравнения, имеет значения 1,80 в степени окисления +2 и 1,96 в степени окисления +4. [63]

Соединения свинца(II) характерны для неорганической химии свинца. Даже сильные окислители, такие как фтор и хлор, реагируют со свинцом, давая только PbF 2 и PbCl 2 . [56] Ионы свинца(II) обычно бесцветны в растворе, [64] и частично гидролизуются с образованием Pb(OH) + и, наконец, [Pb 4 (OH) 4 ] 4+ (в котором гидроксильные ионы действуют как мостиковые лиганды ), [65] [66] но не являются восстановителями, как ионы олова(II). Методы определения наличия иона Pb 2+ в воде обычно основаны на осаждении хлорида свинца(II) с использованием разбавленной соляной кислоты. Поскольку хлоридная соль плохо растворима в воде, в очень разбавленных растворах осаждение сульфида свинца(II) вместо этого достигается путем барботирования сероводорода через раствор. [67]
Монооксид свинца существует в двух полиморфных модификациях : глет α-PbO (красный) и массикот β-PbO (желтый), причем последний стабилен только при температуре выше 488 °C. Глет является наиболее часто используемым неорганическим соединением свинца. [68] Гидроксида свинца (II) не существует; увеличение pH растворов солей свинца (II) приводит к гидролизу и конденсации. [69] Свинец обычно реагирует с более тяжелыми халькогенами. Сульфид свинца является полупроводником , фотопроводником и чрезвычайно чувствительным детектором инфракрасного излучения . Два других халькогенида, селенид свинца и теллурид свинца , также являются фотопроводниками. Они необычны тем, что их цвет становится светлее по мере продвижения вниз по группе. [70]

Дигалогениды свинца хорошо охарактеризованы; они включают диастатид [71] и смешанные галогениды, такие как PbFCl. Относительная нерастворимость последнего образует полезную основу для гравиметрического определения фтора. Дифторид был первым твердым ионнопроводящим соединением, которое было открыто (в 1834 году Майклом Фарадеем ). [72] Другие дигалогениды разлагаются под воздействием ультрафиолетового или видимого света, особенно дииодид . [73] Известно много псевдогалогенидов свинца(II) , таких как цианид, цианат и тиоцианат . [70] [74] Свинец(II) образует большое разнообразие координационных комплексов галогенидов , таких как [PbCl 4 ] 2− , [PbCl 6 ] 4− , и цепочечный анион [Pb 2 Cl 9 ] n 5 n − . [73]
Сульфат свинца(II) нерастворим в воде, как и сульфаты других тяжелых двухвалентных катионов . Нитрат свинца(II) и ацетат свинца(II) очень хорошо растворимы, и это используется в синтезе других соединений свинца. [75]
Известно немного неорганических соединений свинца(IV). Они образуются только в сильно окислительных растворах и обычно не существуют в стандартных условиях. [76] Оксид свинца(II) дает смешанный оксид при дальнейшем окислении, Pb3O4 . Он описывается как оксид свинца(II,IV) или структурно 2PbO·PbO2 и является наиболее известным соединением свинца со смешанной валентностью. Диоксид свинца является сильным окислителем, способным окислять соляную кислоту до газообразного хлора. [77] Это связано с тем, что ожидаемый PbCl4 , который будет получен, нестабилен и спонтанно разлагается на PbCl2 и Cl2 . [ 78] Аналогично монооксиду свинца , диоксид свинца способен образовывать анионы плюмбата . Дисульфид свинца [79] и диселенид свинца [80] стабильны только при высоких давлениях. Тетрафторид свинца , желтый кристаллический порошок, стабилен, но менее стабилен, чем дифторид . Тетрахлорид свинца (желтое масло) разлагается при комнатной температуре, тетрабромид свинца еще менее стабилен, а существование тетраиодида свинца сомнительно. [81]

Некоторые соединения свинца существуют в формальных степенях окисления, отличных от +4 или +2. Свинец(III) может быть получен как промежуточное вещество между свинцом(II) и свинцом(IV) в более крупных свинцовоорганических комплексах; эта степень окисления нестабильна, поскольку и ион свинца(III), и более крупные комплексы, содержащие его, являются радикалами . [83] [84] [85] То же самое относится к свинцу(I), который может быть обнаружен в таких радикальных видах. [86]
Известны многочисленные смешанные оксиды свинца (II, IV). Когда PbO 2 нагревается на воздухе, он становится Pb 12 O 19 при 293 °C, Pb 12 O 17 при 351 °C, Pb 3 O 4 при 374 °C и, наконец, PbO при 605 °C. Еще один полуторный оксид , Pb 2 O 3 , может быть получен при высоком давлении вместе с несколькими нестехиометрическими фазами. Многие из них показывают дефектные структуры флюорита , в которых некоторые атомы кислорода замещены вакансиями: PbO можно рассматривать как имеющий такую структуру, в которой каждый дополнительный слой атомов кислорода отсутствует. [87]
Отрицательные состояния окисления могут возникать в виде фаз Цинтля , либо в виде свободных анионов свинца, как в Ba 2 Pb, где свинец формально является свинцом (−IV), [88] или в кислородочувствительных кольцевых или полиэдрических кластерных ионах, таких как тригональный бипирамидальный ион Pb 5 2− , где два атома свинца являются свинцом (−I), а три — свинцом (0). [89] В таких анионах каждый атом находится в полиэдрической вершине и вносит два электрона в каждую ковалентную связь вдоль края из своих гибридных орбиталей sp 3 , а два других являются внешней неподеленной парой . [65] Их можно получить в жидком аммиаке путем восстановления свинца натрием . [90]

Свинец может образовывать многосвязанные цепи , свойство, которое он разделяет со своими более легкими гомологами в группе углерода. Его способность делать это намного меньше, поскольку энергия связи Pb–Pb более чем в три с половиной раза ниже, чем у связи C–C . [59] Сам по себе свинец может образовывать связи металл–металл порядка до трех. [91] С углеродом свинец образует свинцовоорганические соединения, похожие на типичные органические соединения, но в целом менее стабильные, чем они [92] (из-за того, что связь Pb–C довольно слабая). [65] Это делает металлоорганическую химию свинца гораздо менее широко распространенной, чем у олова. [93] Свинец преимущественно образует свинцовоорганические соединения (IV), даже если начинать с неорганических реагентов свинца (II); известно очень мало свинцовоорганических соединений (II). Наиболее хорошо охарактеризованными исключениями являются Pb[CH(SiMe 3 ) 2 ] 2 и плюмбоцен . [93]
Аналогом свинца простейшего органического соединения , метана , является плюмбан . Плюмбан может быть получен в реакции между металлическим свинцом и атомарным водородом. [94] Два простых производных, тетраметилсвинец и тетраэтилсвинец , являются наиболее известными свинцовоорганическими соединениями. Эти соединения относительно стабильны: тетраэтилсвинец начинает разлагаться только при нагревании [95] или под воздействием солнечного света или ультрафиолетового света. [96] [j] С металлическим натрием свинец легко образует эквимолярный сплав, который реагирует с алкилгалогенидами с образованием металлоорганических соединений, таких как тетраэтилсвинец. [97] Окислительная природа многих свинцовоорганических соединений используется с пользой: тетраацетат свинца является важным лабораторным реагентом для окисления в органическом синтезе. [98] Тетраэтилсвинец, однажды добавленный в автомобильный бензин, производился в больших количествах, чем любое другое металлоорганическое соединение, [93] и до сих пор широко используется в топливе для небольших самолетов . [99] Другие органосвинцовые соединения химически менее стабильны. [92] Для многих органических соединений аналога свинца не существует. [94]
Содержание свинца в расчете на частицу в Солнечной системе составляет 0,121 ppb (частей на миллиард). [100] [k] Эта цифра в два с половиной раза выше, чем у платины , в восемь раз больше, чем у ртути , и в семнадцать раз больше, чем у золота . [100] Количество свинца во Вселенной медленно увеличивается [101], поскольку большинство более тяжелых атомов (все из которых нестабильны) постепенно распадаются на свинец. [102] Содержание свинца в Солнечной системе с момента ее образования 4,5 миллиарда лет назад увеличилось примерно на 0,75%. [103] Таблица содержания свинца в Солнечной системе показывает, что свинец, несмотря на его относительно высокий атомный номер, более распространен, чем большинство других элементов с атомными номерами больше 40. [100]
Первичный свинец, который включает изотопы свинец-204, свинец-206, свинец-207 и свинец-208, в основном был создан в результате повторяющихся процессов захвата нейтронов, происходящих в звездах. Двумя основными режимами захвата являются s- и r-процессы . [104]
В s-процессе (s означает «медленный») захваты разделяются годами или десятилетиями, позволяя менее стабильным ядрам претерпеть бета-распад . [105] Стабильное ядро таллия-203 может захватить нейтрон и стать таллием-204; он претерпевает бета-распад, давая стабильный свинец-204; при захвате другого нейтрона он становится свинцом-205, период полураспада которого составляет около 17 миллионов лет. Дальнейшие захваты приводят к свинцу-206, свинцу-207 и свинцу-208. При захвате другого нейтрона свинец-208 становится свинцом-209, который быстро распадается на висмут-209. При захвате другого нейтрона висмут-209 становится висмутом-210, и этот бета-распад превращается в полоний-210, который альфа-распадается до свинца-206. Таким образом, цикл заканчивается на свинце-206, свинце-207, свинце-208 и висмуте-209. [106]

В r-процессе (r означает «быстрый») захваты происходят быстрее, чем ядра могут распадаться. [107] Это происходит в средах с высокой плотностью нейтронов, таких как сверхновая или слияние двух нейтронных звезд . Поток нейтронов может быть порядка 10 22 нейтронов на квадратный сантиметр в секунду. [108] r-процесс не образует столько свинца, сколько s-процесс. [109] Он имеет тенденцию останавливаться, как только нейтронно-богатые ядра достигают 126 нейтронов. [110] В этот момент нейтроны располагаются в полных оболочках в атомном ядре, и становится сложнее энергетически разместить больше из них. [111] Когда поток нейтронов спадает, эти ядра бета-распадаются на стабильные изотопы осмия , иридия , платины . [112]
Свинец классифицируется как халькофил по классификации Гольдшмидта , что означает, что он обычно встречается в сочетании с серой. [113] Он редко встречается в своей естественной , металлической форме. [114] Многие минералы свинца относительно легкие и на протяжении всей истории Земли оставались в коре , а не погружались глубже в недра Земли. Это объясняет относительно высокую распространенность свинца в земной коре — 14 частей на миллион; это 36-й по распространенности элемент в коре. [115] [l]
Основным минералом, содержащим свинец, является галенит (PbS), который в основном встречается в цинковых рудах. [117] Большинство других минералов свинца так или иначе связаны с галенитом; буланжерит , Pb 5 Sb 4 S 11 , представляет собой смешанный сульфид, полученный из галенита; англезит , PbSO 4 , является продуктом окисления галенита; а церуссит или белая свинцовая руда, PbCO 3 , является продуктом разложения галенита. Мышьяк , олово , сурьма , серебро , золото , медь , висмут являются обычными примесями в минералах свинца. [117]

Мировые ресурсы свинца превышают два миллиарда тонн. Значительные месторождения находятся в Австралии, Китае, Ирландии, Мексике, Перу, Португалии, России, США. Мировые запасы — ресурсы, которые экономически целесообразно извлекать — составили 88 миллионов тонн в 2016 году, из которых в Австралии было 35 миллионов, в Китае — 17 миллионов, в России — 6,4 миллиона. [118]
Типичные фоновые концентрации свинца не превышают 0,1 мкг/м 3 в атмосфере; 100 мг/кг в почве; 4 мг/кг в растительности, 5 мкг/л в пресной и морской воде. [119]
Современное английское слово lead имеет германское происхождение; оно происходит от среднеанглийского leed и древнеанглийского lēad (с макроном над «e», означающим, что гласный звук этой буквы долгий). [120] Древнеанглийское слово происходит от гипотетического реконструированного протогерманского * lauda- ('lead'). [121] Согласно лингвистической теории, это слово имело потомков во многих германских языках с точно таким же значением. [121]
Нет единого мнения о происхождении протогерманского * lauda- . Одна из гипотез предполагает, что оно произошло от протоиндоевропейского * lAudh- ('свинец'; заглавная буква гласной эквивалентна макрону). [122] Другая гипотеза предполагает, что оно заимствовано из протокельтского * ɸloud-io- ('свинец'). Это слово связано с латинским plumbum , который дал элементу его химический символ Pb . Слово * ɸloud-io- , как полагают, является источником протогерманского * bliwa- (что также означает 'свинец'), от которого произошло немецкое Blei . [123]
Название химического элемента не связано с глаголом того же написания, который происходит от протогерманского * laidijan- ('вести'). [124]
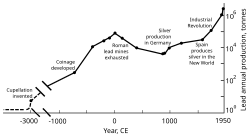
Металлические свинцовые бусины, датируемые 7000–6500 гг. до н. э., были найдены в Малой Азии и могут представлять собой первый пример выплавки металла . [126] В то время свинец имел мало (если вообще имел) применений из-за своей мягкости и тусклого вида. [126] Основной причиной распространения производства свинца была его связь с серебром, которое можно было получить путем сжигания галенита (распространенного минерала свинца). [127] Древние египтяне были первыми, кто использовал свинцовые минералы в косметике, применение, которое распространилось в Древней Греции и за ее пределами; [128] египтяне использовали свинец для грузил в рыболовных сетях , глазури , стекол , эмалей , украшений . [127] Различные цивилизации Плодородного полумесяца использовали свинец в качестве писчего материала , в качестве монет , [129] и в качестве строительного материала . [127] Свинец использовался древними китайцами как стимулятор , [127] как валюта , [130] как противозачаточное средство ; [131] цивилизация долины Инда и мезоамериканцы использовали его для изготовления амулетов ; [127] а восточные и южные африканцы использовали свинец для волочения проволоки . [132]
Поскольку серебро широко использовалось в качестве декоративного материала и средства обмена, месторождения свинца начали разрабатываться в Малой Азии с 3000 г. до н. э.; позднее месторождения свинца были разработаны в Эгейском море и Лаврионе . [133] Эти три региона совместно доминировали в производстве добываемого свинца примерно до 1200 г. до н. э . [134] Начиная с 2000 г. до н. э. финикийцы разрабатывали месторождения на Пиренейском полуострове ; к 1600 г. до н. э. добыча свинца существовала на Кипре , в Греции и на Сардинии . [135]

Территориальная экспансия Рима в Европе и по всему Средиземноморью, а также развитие горнодобывающей промышленности привели к тому, что Рим стал крупнейшим производителем свинца в классическую эпоху , с предполагаемым годовым объемом производства в 80 000 тонн. Как и их предшественники, римляне получали свинец в основном как побочный продукт плавки серебра. [125] [137] Добыча свинца велась в Центральной Европе , Британии , на Балканах , в Греции , Анатолии , Испании , причем на последнюю приходилось 40% мирового производства. [125]

Свинцовые таблички обычно использовались в качестве материала для писем. [138] Свинцовые гробы, отлитые в плоских песчаных формах и со сменными мотивами, подходящими для веры умершего, использовались в древней Иудее . [139] Свинец использовался для изготовления пуль для пращи с V века до н. э. Во времена Римской империи свинцовые пули для пращи широко использовались и были эффективны на расстоянии от 100 до 150 метров. Балеарские пращники , использовавшиеся в качестве наемников в карфагенских и римских армиях, славились своей дальностью стрельбы и точностью. [140]

Свинец использовался для изготовления водопроводных труб в Римской империи ; латинское слово для обозначения металла, plumbum , является источником английского слова « водопровод ». Его простота в обработке, его низкая температура плавления, позволяющая легко изготавливать полностью водонепроницаемые сварные соединения, и его устойчивость к коррозии [141] обеспечили его широкое использование в других областях, включая фармацевтику, кровельные работы, валюту, войну. [142] [143] [144] Писатели того времени, такие как Катон Старший , Колумелла и Плиний Старший , рекомендовали свинцовые (и покрытые свинцом) сосуды для приготовления подсластителей и консервантов, добавляемых в вино и пищу. Свинец придавал приятный вкус из-за образования «свинцового сахара» ( ацетата свинца (II) ), тогда как медные сосуды придавали горький привкус из-за образования яри-медянки . [145]
Этот металл был самым используемым материалом в классической античности, и его уместно отнести к (римскому) свинцовому веку. Свинец был для римлян тем же, чем для нас является пластик.
Хайнц Эшнауэр и Маркус Степплер
«Вино — банк энологических образцов», 1992 г. [146]
Римский автор Витрувий сообщал об опасности свинца для здоровья [147] [148], а современные авторы предположили, что отравление свинцом сыграло важную роль в упадке Римской империи . [149] [150] [n] Другие исследователи критиковали такие утверждения, указывая, например, на то, что не все боли в животе вызваны отравлением свинцом. [152] [153] Согласно археологическим исследованиям, римские свинцовые трубы повышали уровень свинца в водопроводной воде, но такой эффект «вряд ли был действительно вредным». [154] [155] Когда отравление свинцом действительно происходило, жертв называли «сатурнианскими», темными и циничными, в честь отвратительного отца богов, Сатурна . По ассоциации свинец считался отцом всех металлов. [156] Его статус в римском обществе был низким, поскольку он был легкодоступным [157] и дешевым. [158]
Начиная с бронзового века , металлурги и инженеры понимали разницу между редким и ценным оловом , необходимым для сплавления с медью для получения прочной и устойчивой к коррозии бронзы , и «дешевым и веселым» свинцом. Однако номенклатура в некоторых языках похожа. Римляне называли свинец plumbum nigrum («черный свинец»), а олово plumbum candidum («яркий свинец»). Связь свинца и олова можно увидеть и в других языках: слово olovo на чешском языке переводится как «свинец», но на русском его родственное слово олово ( olovo ) означает «олово». [159] Чтобы добавить путаницы, свинец имел тесную связь с сурьмой: оба элемента обычно встречаются в виде сульфидов (галенита и стибнита ), часто вместе. Плиний неправильно писал, что стибнит при нагревании даст свинец вместо сурьмы. [160] В таких странах, как Турция и Индия, изначально персидское название surma стало обозначать либо сульфид сурьмы, либо сульфид свинца, [161] а в некоторых языках, таких как русский, дало название сурьме ( сурьма ). [162]
_-_Portrait_of_Queen_Elizabeth_I_-_Google_Art_Project.jpg/440px-Nicholas_Hilliard_(called)_-_Portrait_of_Queen_Elizabeth_I_-_Google_Art_Project.jpg)
Добыча свинца в Западной Европе пошла на спад после падения Западной Римской империи , единственным регионом, где наблюдался значительный объем добычи, была Аравийская Иберия . [164] [165] Наибольшее производство свинца наблюдалось в Южной и Восточной Азии, особенно в Китае и Индии, где добыча свинца быстро росла. [165]
В Европе производство свинца начало расти в XI и XII веках, когда его снова стали использовать для кровли и труб. Начиная с XIII века, свинец использовался для создания витражей . [166] В европейских и арабских традициях алхимии свинец (символ ♄ в европейской традиции) [167] считался нечистым неблагородным металлом , который путем разделения, очистки и уравновешивания его составляющих эссенций можно было преобразовать в чистое и нетленное золото. [168] В этот период свинец все чаще использовался для фальсификации вина. Использование такого вина было запрещено для использования в христианских обрядах папской буллой в 1498 году, но его продолжали употреблять, что приводило к массовым отравлениям вплоть до конца XVIII века. [164] [169] Свинец был ключевым материалом в некоторых частях печатного станка , и свинцовая пыль обычно вдыхалась работниками печатного станка, вызывая отравление свинцом. [170] Свинец также стал основным материалом для изготовления пуль для огнестрельного оружия: он был дешев, наносил меньше повреждений железным стволам, имел более высокую плотность (что позволяло лучше сохранять скорость), а его более низкая температура плавления упрощала производство пуль, поскольку их можно было изготавливать с использованием дровяного огня. [171] Свинец в форме венецианских белил широко использовался в косметике западноевропейской аристократией, поскольку выбеленные лица считались признаком скромности. [172] [173] Эта практика позже распространилась на белые парики и подводки для глаз и сошла на нет только с Французской революцией в конце 18 века. Похожая мода появилась в Японии в 18 веке с появлением гейш , практика, которая продолжалась и в 20 веке. Белые лица женщин «стали представлять их женскую добродетель как японских женщин», [174] причем свинец обычно использовался в отбеливателе. [175]
В Новом Свете производство свинца было зафиксировано вскоре после прибытия европейских поселенцев. Самая ранняя запись датируется 1621 годом в английской колонии Вирджиния , через четырнадцать лет после ее основания. [176] В Австралии первой шахтой, открытой колонистами на континенте, была свинцовая шахта в 1841 году. [177] В Африке добыча и выплавка свинца были известны в желобе Бенуэ [178] и в нижнем бассейне реки Конго , где свинец использовался для торговли с европейцами и в качестве валюты к 17 веку, [179] задолго до борьбы за Африку .

Во второй половине XVIII века Великобритания, а затем континентальная Европа и США пережили Промышленную революцию . Это был первый раз, когда темпы производства свинца превысили темпы Рима. [180] Великобритания была ведущим производителем, потеряв этот статус к середине XIX века из-за истощения своих рудников и развития добычи свинца в Германии, Испании и США. [181] К 1900 году Соединенные Штаты были лидером по мировому производству свинца, а другие неевропейские страны — Канада, Мексика и Австралия — начали значительное производство; производство за пределами Европы превышало производство внутри. [182] Большая часть спроса на свинец приходилась на сантехнику и покраску — свинцовые краски использовались регулярно. [183] В это время все больше людей (рабочего класса) подвергались воздействию металла, и случаи отравления свинцом участились. Это привело к исследованию последствий потребления свинца. Было доказано, что свинец более опасен в форме паров, чем в виде твердого металла. Отравление свинцом и подагра были связаны; британский врач Альфред Баринг Гаррод отмечал, что треть его пациентов с подагрой были сантехниками и малярами. Последствия хронического приема свинца, включая психические расстройства, также изучались в 19 веке. Первые законы, направленные на снижение отравления свинцом на фабриках, были приняты в 1870-х и 1880-х годах в Соединенном Королевстве. [183]

Дальнейшие доказательства угрозы, которую свинец представляет для людей, были обнаружены в конце 19-го и начале 20-го веков. Механизмы вреда были лучше поняты, свинцовая слепота была задокументирована, и элемент был постепенно выведен из общественного использования в Соединенных Штатах и Европе. Соединенное Королевство ввело обязательные проверки фабрик в 1878 году и назначило первого медицинского инспектора фабрик в 1898 году; в результате было сообщено о 25-кратном снижении случаев отравления свинцом с 1900 по 1944 год. [184] Большинство европейских стран запретили свинцовую краску — обычно используемую из-за ее непрозрачности и водостойкости [185] — для внутренних работ к 1930 году. [186]
Последним серьезным воздействием свинца на человека было добавление тетраэтилсвинца в бензин в качестве антидетонационной присадки , практика, которая возникла в Соединенных Штатах в 1921 году. Она была прекращена в Соединенных Штатах и Европейском союзе к 2000 году. [183]
В 1970-х годах Соединенные Штаты и страны Западной Европы приняли законодательство по сокращению загрязнения воздуха свинцом. [187] [188] Влияние было значительным: в то время как исследование, проведенное Центрами по контролю и профилактике заболеваний в Соединенных Штатах в 1976–1980 годах, показало, что у 77,8% населения был повышен уровень свинца в крови , в 1991–1994 годах исследование того же института показало, что доля людей с таким высоким уровнем снизилась до 2,2%. [189] Основным продуктом, изготовленным из свинца к концу 20-го века, был свинцово-кислотный аккумулятор . [190]
С 1960 по 1990 год производство свинца в Западном блоке выросло примерно на 31%. [191] Доля мирового производства свинца Восточным блоком увеличилась с 10% до 30% с 1950 по 1990 год, причем Советский Союз был крупнейшим в мире производителем в середине 1970-х и 1980-х годов, а Китай начал крупное производство свинца в конце 20-го века. [192] В отличие от европейских коммунистических стран, Китай был в значительной степени неиндустриализирован к середине 20-го века; в 2004 году Китай превзошел Австралию как крупнейшего производителя свинца. [193] Как и во время европейской индустриализации, свинец оказал негативное влияние на здоровье в Китае. [194]
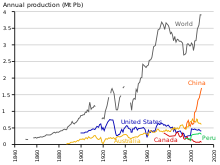
По состоянию на 2014 год производство свинца во всем мире увеличивается из-за его использования в свинцово-кислотных аккумуляторах. [195] Существует две основные категории производства: первичное из добытых руд и вторичное из лома. В 2014 году 4,58 миллиона метрических тонн было получено в результате первичного производства и 5,64 миллиона из вторичного производства. Тремя крупнейшими производителями добытого свинцового концентрата в том году были Китай, Австралия и Соединенные Штаты. [118] Тремя крупнейшими производителями очищенного свинца были Китай, Соединенные Штаты и Индия. [196] Согласно отчету Metal Stocks in Society за 2010 год, общее количество свинца, находящегося в использовании, складируемого, выбрасываемого или рассеиваемого в окружающей среде, в глобальном масштабе составляет 8 кг на душу населения. Большая часть этого приходится на более развитые страны (20–150 кг на душу населения), а не на менее развитые (1–4 кг на душу населения). [197]
Первичные и вторичные процессы производства свинца схожи. Некоторые заводы первичного производства теперь дополняют свои операции свинцовым ломом, и эта тенденция, вероятно, усилится в будущем. При наличии адекватных методов свинец, полученный с помощью вторичных процессов, неотличим от свинца, полученного с помощью первичных процессов. Свинцовый лом из строительной промышленности обычно довольно чистый и переплавляется без необходимости плавки, хотя иногда требуется очистка. Поэтому вторичное производство свинца дешевле с точки зрения энергетических потребностей, чем первичное производство, часто на 50% и более. [198]
Большинство свинцовых руд содержат низкий процент свинца (богатые руды имеют типичное содержание 3–8%), который необходимо концентрировать для извлечения. [199] Во время первичной обработки руды обычно подвергаются дроблению, разделению в тяжелой среде, измельчению , пенной флотации , сушке . Полученный концентрат, который имеет содержание свинца 30–80% по массе (обычно 50–60%), [199] затем превращается в (нечистый) металлический свинец.
Существует два основных способа сделать это: двухступенчатый процесс, включающий обжиг с последующим извлечением в доменной печи, осуществляемый в отдельных сосудах; или прямой процесс, при котором извлечение концентрата происходит в одном сосуде. Последний стал наиболее распространенным путем, хотя первый все еще имеет значение. [200]
Сначала сульфидный концентрат обжигают на воздухе для окисления сульфида свинца: [201]
Поскольку исходный концентрат не был чистым сульфидом свинца, обжиг дает не только желаемый оксид свинца(II), но и смесь оксидов, сульфатов и силикатов свинца и других металлов, содержащихся в руде. [202] Этот неочищенный оксид свинца восстанавливается в доменной печи, работающей на коксе , до (опять же неочищенного) металла: [203]
Примеси в основном представляют собой мышьяк, сурьму, висмут, цинк, медь, серебро и золото. Обычно их удаляют в серии пирометаллургических процессов . Расплав обрабатывается в отражательной печи воздухом, паром, серой, которая окисляет примеси, за исключением серебра, золота, висмута. Окисленные примеси всплывают на поверхность расплава и снимаются. [204] [205] Металлическое серебро и золото удаляются и извлекаются экономично с помощью процесса Паркса , в котором цинк добавляется к свинцу. Цинк, который не смешивается со свинцом, растворяет серебро и золото. Раствор цинка можно отделить от свинца, а серебро и золото извлечь. [205] [206] Десеребренный свинец освобождается от висмута с помощью процесса Беттертона-Кролла , обрабатывая его металлическим кальцием и магнием . Полученный висмутовый шлак можно снять. [205]
В качестве альтернативы пирометаллургическим процессам очень чистый свинец может быть получен путем электролитической обработки расплавленного свинца с использованием процесса Беттса . Аноды из неочищенного свинца и катоды из чистого свинца помещаются в электролит из фторсиликата свинца (PbSiF 6 ). После приложения электрического потенциала неочищенный свинец на аноде растворяется и осаждается на катоде, оставляя большую часть примесей в растворе. [205] [207] Это дорогостоящий процесс, поэтому его в основном используют для очистки слитков, содержащих высокий процент примесей. [208]
В этом процессе свинцовый слиток и шлак получаются непосредственно из свинцовых концентратов. Концентрат сульфида свинца плавится в печи и окисляется, образуя оксид свинца. Углерод (в виде кокса или угольного газа [o] ) добавляется в расплавленную шихту вместе с флюсующими веществами . Таким образом, оксид свинца восстанавливается до металлического свинца, посреди шлака, богатого оксидом свинца. [200]
Если исходный материал богат свинцом, то до 80% исходного свинца можно получить в виде слитка; оставшиеся 20% образуют шлак, богатый оксидом свинца. Для низкосортного сырья весь свинец можно окислить до шлака с высоким содержанием свинца. [200] Металлический свинец далее получают из шлаков с высоким содержанием свинца (25–40%) путем сжигания или впрыскивания топлива под слоем флюса, восстановления с помощью электропечи или комбинации того и другого. [200]
Исследования более чистого, менее энергоемкого процесса извлечения свинца продолжаются; основным недостатком является то, что либо слишком много свинца теряется в виде отходов, либо альтернативы приводят к высокому содержанию серы в полученном свинцовом металле. Гидрометаллургическое извлечение, при котором аноды из неочищенного свинца погружаются в электролит , а чистый свинец осаждается ( электронамоткой ) на катоды , является методом, который может иметь потенциал, но в настоящее время не является экономичным, за исключением случаев, когда электричество очень дешево. [209]
Плавка, которая является неотъемлемой частью первичного производства, часто пропускается во время вторичного производства. Она выполняется только тогда, когда металлический свинец подвергся значительному окислению. [198] Процесс аналогичен первичному производству в доменной или вращающейся печи , с существенным отличием в большей изменчивости выходов: доменные печи производят твердый свинец (10% сурьмы), тогда как отражательные и вращающиеся печи производят полумягкий свинец (3–4% сурьмы). [210]
Процесс ISASMELT является более новым методом плавки, который может выступать в качестве расширения первичного производства; аккумуляторная паста из отработанных свинцово-кислотных аккумуляторов (содержащих сульфат свинца и оксиды свинца) подвергается удалению сульфата путем обработки щелочью, а затем обрабатывается в угольной печи в присутствии кислорода, что дает неочищенный свинец, причем сурьма является наиболее распространенной примесью. [211] Очистка вторичного свинца аналогична очистке первичного свинца; некоторые процессы очистки могут быть пропущены в зависимости от перерабатываемого материала и его потенциального загрязнения. [211]
Из источников свинца для переработки наиболее важными являются свинцово-кислотные аккумуляторы; также существенны свинцовые трубы, листы и оболочки кабелей. [198]

Вопреки распространенному мнению, стержни деревянных карандашей никогда не изготавливались из свинца. Когда карандаш появился как обернутый графитовый пишущий инструмент, конкретный тип используемого графита назывался plumbago (буквально, макет свинца ). [213]
Металлический свинец обладает несколькими полезными механическими свойствами, включая высокую плотность, низкую температуру плавления, пластичность и относительную инертность. Многие металлы превосходят свинец в некоторых из этих аспектов, но, как правило, менее распространены и их труднее извлекать из исходных руд. Токсичность свинца привела к его постепенному отказу от некоторых видов использования. [214]
Свинец использовался для пуль с момента их изобретения в Средние века. Он недорогой; его низкая температура плавления означает, что боеприпасы для стрелкового оружия и дробовые пули можно отливать с минимальным техническим оборудованием; и он плотнее других распространенных металлов, что позволяет лучше сохранять скорость. Он остается основным материалом для пуль, легированным другими металлами в качестве отвердителей. [171] Высказывались опасения, что свинцовые пули, используемые для охоты, могут нанести вред окружающей среде. [p] Патроны для дробовиков, используемые для охоты на водоплавающую дичь, сегодня должны быть без свинца в Соединенных Штатах , [216] Канаде , [217] и в Европе . [218]
Высокая плотность свинца и его устойчивость к коррозии нашли применение в ряде смежных областей. Он используется в качестве балласта в килях парусных лодок; его плотность позволяет ему занимать небольшой объем и минимизировать сопротивление воды, тем самым уравновешивая кренящий эффект ветра на паруса. [219] Он используется в грузовых поясах для подводного плавания , чтобы противодействовать плавучести водолаза. [220] В 1993 году основание Пизанской башни было стабилизировано с помощью 600 тонн свинца. [221] Благодаря своей коррозионной стойкости свинец используется в качестве защитной оболочки для подводных кабелей. [222]
_07.jpg/440px-Parc_de_Versailles,_Bassin_de_Flore,_Jean-Baptiste_Tuby_(1672-79)_07.jpg)
Свинец имеет множество применений в строительной отрасли; свинцовые листы используются в качестве архитектурных металлов в кровельном материале , облицовке , фартуках , желобах и соединениях желобов, парапетах крыш. [223] [224] Свинец по-прежнему используется в статуях и скульптурах, [q] в том числе для арматуры . [226] В прошлом его часто использовали для балансировки колес автомобилей ; по экологическим причинам это использование постепенно прекращается в пользу других материалов. [118]
Свинец добавляют в медные сплавы, такие как латунь и бронза , для улучшения обрабатываемости и смазочных свойств. Будучи практически нерастворимым в меди, свинец образует твердые глобулы в дефектах по всему сплаву, таких как границы зерен . В низких концентрациях, а также действуя как смазка, глобулы препятствуют образованию стружки при обработке сплава, тем самым улучшая обрабатываемость. Медные сплавы с большей концентрацией свинца используются в подшипниках . Свинец обеспечивает смазку, а медь обеспечивает несущую опору. [227]
Высокая плотность свинца, атомный номер и формуемость формируют основу для использования свинца в качестве барьера, поглощающего звук, вибрацию и излучение. [228] Свинец не имеет собственных резонансных частот; [228] в результате листовой свинец используется в качестве звукоизолирующего слоя на стенах, полах и потолках звуковых студий. [229] Органные трубы часто изготавливаются из свинцового сплава, смешанного с различным количеством олова для управления тоном каждой трубы. [230] [231] Свинец является признанным защитным материалом от радиации в ядерной науке и в рентгеновских кабинетах [232] из-за своей плотности и высокого коэффициента затухания . [233] Расплавленный свинец использовался в качестве охладителя для быстрых реакторов со свинцовым охлаждением . [234]
Наибольшее применение свинец в начале 21 века получил в свинцово-кислотных аккумуляторах . Свинец в аккумуляторах не контактирует напрямую с людьми, поэтому существует меньше проблем с токсичностью. [r] Люди, работающие на заводах по производству свинцовых аккумуляторов или на заводах по переработке, могут подвергаться воздействию свинцовой пыли и вдыхать ее. [236] Реакции в аккумуляторе между свинцом, диоксидом свинца и серной кислотой обеспечивают надежный источник напряжения . [s] Суперконденсаторы , включающие свинцово-кислотные аккумуляторы, были установлены в приложениях киловаттного и мегаваттного масштаба в Австралии, Японии и Соединенных Штатах для регулирования частоты, сглаживания и смещения солнечной энергии, сглаживания ветра и других приложений. [238] Эти аккумуляторы имеют более низкую плотность энергии и эффективность заряда-разряда, чем литий-ионные аккумуляторы , но они значительно дешевле. [239]
Свинец используется в высоковольтных силовых кабелях в качестве материала оболочки для предотвращения диффузии воды в изоляцию; это использование уменьшается, поскольку свинец постепенно выводится из употребления. [240] Его использование в припое для электроники также постепенно выводится из употребления некоторыми странами, чтобы сократить количество экологически опасных отходов. [241] Свинец является одним из трех металлов, используемых в тесте Одди для музейных материалов, помогая обнаруживать органические кислоты, альдегиды, кислотные газы. [242] [243]


Помимо того, что свинцово-кислотные аккумуляторы являются основным применением свинцового металла, они также являются основным потребителем соединений свинца. Реакция накопления/выделения энергии, используемая в этих устройствах, включает сульфат свинца и диоксид свинца :
Другие применения соединений свинца очень специализированы и часто исчезают. Красители на основе свинца используются в керамической глазури и стекле, особенно для красных и желтых оттенков. [244] Хотя свинцовые краски постепенно выводятся из употребления в Европе и Северной Америке, они по-прежнему используются в менее развитых странах, таких как Китай, [245] Индия, [246] или Индонезия. [247] Тетраацетат свинца и диоксид свинца используются в качестве окислителей в органической химии. Свинец часто используется в поливинилхлоридном покрытии электрических шнуров. [248] [249] Его можно использовать для обработки фитилей свечей, чтобы обеспечить более длительное и равномерное горение. Из-за его токсичности европейские и североамериканские производители используют альтернативы, такие как цинк. [250] [251] Свинцовое стекло состоит из 12–28% оксида свинца , что изменяет его оптические характеристики и снижает передачу ионизирующего излучения, [252] свойство, используемое в старых телевизорах и компьютерных мониторах с электронно-лучевыми трубками . Полупроводники на основе свинца, такие как теллурид свинца и селенид свинца, используются в фотоэлектрических элементах и инфракрасных детекторах. [253]
Свинец не имеет подтвержденной биологической роли, и не существует подтвержденного безопасного уровня воздействия свинца. [255] Канадско-американское исследование 2009 года пришло к выводу, что даже на уровнях, которые считаются не представляющими большого или нулевого риска, свинец может вызывать «неблагоприятные последствия для психического здоровья». [256] Его распространенность в организме человека — в среднем для взрослого человека 120 мг [т] — тем не менее, уступает только цинку (2500 мг) и железу (4000 мг) среди тяжелых металлов. [258] Соли свинца очень эффективно усваиваются организмом. [259] Небольшое количество свинца (1%) хранится в костях; остальное выводится с мочой и калом в течение нескольких недель после воздействия. Только около трети свинца выводится ребенком. Постоянное воздействие может привести к биоаккумуляции свинца. [260]
Свинец является крайне ядовитым металлом (как при вдыхании, так и при проглатывании), поражая практически все органы и системы человеческого организма. [261] При концентрации в воздухе 100 мг/м3 он немедленно становится опасным для жизни и здоровья . [262] Большая часть проглоченного свинца всасывается в кровоток. [263] Основной причиной его токсичности является его склонность мешать правильному функционированию ферментов. Он делает это, связываясь с сульфгидрильными группами , обнаруженными во многих ферментах, [264] или имитируя и вытесняя другие металлы, которые действуют как кофакторы во многих ферментативных реакциях. [265] Основные металлы, с которыми взаимодействует свинец, включают кальций, железо и цинк. [266] Высокие уровни кальция и железа, как правило, обеспечивают некоторую защиту от отравления свинцом; низкие уровни вызывают повышенную восприимчивость. [259]
Свинец может вызвать серьезные повреждения мозга и почек и, в конечном итоге, смерть. Подражая кальцию, свинец может пересекать гематоэнцефалический барьер . Он разрушает миелиновые оболочки нейронов , уменьшает их количество, мешает путям нейротрансмиссии и уменьшает рост нейронов. [264] В организме человека свинец ингибирует порфобилиногенсинтазу и феррохелатазу , предотвращая как образование порфобилиногена , так и включение железа в протопорфирин IX , конечный этап синтеза гема . Это вызывает неэффективный синтез гема и микроцитарную анемию . [267]

Симптомы отравления свинцом включают нефропатию , коликообразные боли в животе и, возможно, слабость в пальцах, запястьях или лодыжках. Небольшое повышение артериального давления, особенно у людей среднего и пожилого возраста, может быть очевидным и может вызвать анемию . [ необходима ссылка ] Несколько исследований, в основном перекрестных, обнаружили связь между повышенным воздействием свинца и снижением вариабельности сердечного ритма. [268] У беременных женщин высокие уровни воздействия свинца могут вызвать выкидыш. Было показано, что хроническое воздействие высокого уровня снижает фертильность у мужчин. [269]
В развивающемся мозге ребенка свинец влияет на формирование синапсов в коре головного мозга , нейрохимическое развитие (включая развитие нейротрансмиттеров) и организацию ионных каналов . [270] Раннее воздействие свинца связано с повышенным риском нарушений сна и чрезмерной дневной сонливости в более позднем детстве. [271] Высокий уровень свинца в крови связан с задержкой полового созревания у девочек. [272] Рост и падение воздействия свинца в воздухе от сгорания тетраэтилсвинца в бензине в течение 20-го века были связаны с историческим ростом и снижением уровня преступности .
Воздействие свинца является глобальной проблемой, поскольку добыча и выплавка свинца, а также производство, утилизация и переработка аккумуляторов распространены во многих странах. Свинец попадает в организм через вдыхание, проглатывание или через кожу. Почти весь вдыхаемый свинец всасывается в организм; при проглатывании этот показатель составляет 20–70%, причем дети всасывают больше, чем взрослые. [273]
Отравление обычно происходит в результате употребления пищи или воды, загрязненной свинцом, и реже после случайного употребления загрязненной почвы, пыли или краски на основе свинца. [274] Продукты из морской воды могут содержать свинец, если они подверглись воздействию близлежащих промышленных вод. [275] Фрукты и овощи могут быть загрязнены высоким содержанием свинца в почве, в которой они были выращены. Почва может быть загрязнена из-за накопления частиц свинца в трубах, свинцовой краски , остаточных выбросов от этилированного бензина. [276]
Использование свинца для водопроводных труб является проблемой в районах с мягкой или кислой водой . [277] Жесткая вода образует нерастворимые защитные слои на внутренней поверхности труб, тогда как мягкая и кислая вода растворяет свинцовые трубы. [278] Растворенный углекислый газ в транспортируемой воде может привести к образованию растворимого бикарбоната свинца ; насыщенная кислородом вода может аналогичным образом растворять свинец в виде гидроксида свинца (II) . Употребление такой воды со временем может вызвать проблемы со здоровьем из-за токсичности растворенного свинца. Чем жестче вода, тем больше в ней бикарбоната кальция и сульфата , и тем больше внутренняя часть труб покрыта защитным слоем карбоната свинца или сульфата свинца. [279]

Проглатывание нанесенной свинцовой краски является основным источником воздействия для детей: прямым источником является жевание старых окрашенных подоконников. Кроме того, по мере того, как свинцовая краска на поверхности портится, она отслаивается и измельчается в пыль. Затем пыль попадает в организм через руки и рот или через зараженную пищу или питье. Проглатывание некоторых домашних средств может привести к воздействию свинца или его соединений. [280]
Вдыхание является вторым основным путем воздействия, влияющим на курильщиков и особенно на рабочих, чья профессия связана со свинцом. [263] Сигаретный дым содержит, среди прочих токсичных веществ, радиоактивный свинец-210 . [281] «В результате регулирующих усилий Агентства по охране окружающей среды, уровень свинца в воздухе [в Соединенных Штатах] снизился на 86 процентов в период с 2010 по 2020 год». [282] Концентрация свинца в воздухе в Соединенных Штатах упала ниже национального стандарта 0,15 мкг/м 3 [283] в 2014 году. [284]
Воздействие на кожу может быть значительным для людей, работающих с органическими соединениями свинца. Скорость поглощения кожей ниже для неорганического свинца. [285]
Свинец может быть обнаружен в пище, если она выращивается на почве с высоким содержанием свинца, свинец, переносимый по воздуху, загрязняет урожай, животные употребляют свинец в пищу или свинец попадает в пищу из того, в чем он хранился или готовился. [286] Проглатывание свинцовой краски и батареек также является путем воздействия на скот, что впоследствии может повлиять на людей. [287] Молоко, произведенное зараженным скотом, можно разбавить до более низкой концентрации свинца и продать для потребления. [288]
В Бангладеш в куркуму добавляют соединения свинца , чтобы сделать ее более желтой. [289] Считается, что это началось в 1980-х годах и продолжается по состоянию на 2019 год [обновлять]. [289] Считается, что это один из основных источников высокого уровня свинца в стране. [290] В Гонконге максимально допустимый уровень свинца в пище составляет 6 частей на миллион в твердых веществах и 1 часть на миллион в жидкостях. [291]
Пыль, содержащая свинец, может оседать на сушащихся какао-бобах, когда они находятся на улице вблизи загрязняющих промышленных предприятий. [292] В декабре 2022 года Consumer Reports протестировал 28 марок темного шоколада и обнаружил, что 23 из них содержали потенциально опасные уровни свинца, кадмия или и того, и другого. Они призвали производителей шоколада снизить уровень свинца, который может быть вреден, особенно для развивающегося плода. [293]
По данным Центра по контролю и профилактике заболеваний США , использование свинца в пластмассах не было запрещено по состоянию на 2024 год. Свинец смягчает пластик и делает его более гибким, чтобы он мог вернуться к своей первоначальной форме. Было обнаружено, что регулярное жевание цветной пластиковой изоляции от оголенных электрических проводов приводит к повышению уровня свинца у 46-летнего мужчины. [294] Свинец может использоваться в пластиковых игрушках для стабилизации молекул от тепла. Свинцовая пыль может образовываться, когда пластик подвергается воздействию солнечного света, воздуха и моющих средств, которые разрушают химическую связь между свинцом и пластмассой. [295]
Лечение отравления свинцом обычно включает в себя введение димеркапрола и сукцимера . [296] Острые случаи могут потребовать использования динатриевой соли кальция эдетата , хелата кальция и динатриевой соли этилендиаминтетрауксусной кислоты ( ЭДТА ). Он имеет большее сродство к свинцу, чем к кальцию, в результате чего хелат свинца образуется путем обмена и выводится с мочой, оставляя безвредный кальций. [297]

Добыча, производство, использование и утилизация свинца и его продуктов привели к значительному загрязнению почв и вод Земли. Выбросы свинца в атмосферу достигли пика во время промышленной революции и периода этилированного бензина во второй половине двадцатого века. [298]
Выбросы свинца происходят из природных источников (т. е. концентрации встречающегося в природе свинца), промышленного производства, сжигания и переработки, а также мобилизации ранее захороненного свинца. [298] В частности, поскольку свинец был постепенно выведен из других областей применения, на Глобальном Юге операции по переработке свинца, предназначенные для извлечения дешевого свинца, используемого для мирового производства, стали хорошо документированным источником воздействия. [299] Повышенные концентрации свинца сохраняются в почвах и отложениях в постиндустриальных и городских районах; промышленные выбросы, включая те, которые возникают при сжигании угля, [300] продолжаются во многих частях мира, особенно в развивающихся странах. [301]
Свинец может накапливаться в почвах, особенно с высоким содержанием органических веществ, где он остается в течение сотен или тысяч лет. Экологический свинец может конкурировать с другими металлами, обнаруженными в и на поверхности растений, потенциально подавляя фотосинтез и при достаточно высоких концентрациях отрицательно влияя на рост и выживание растений. Загрязнение почв и растений может позволить свинцу подняться по пищевой цепи, поражая микроорганизмы и животных. У животных свинец проявляет токсичность во многих органах, повреждая нервную, почечную , репродуктивную, кроветворную и сердечно-сосудистую системы после приема внутрь, вдыхания или всасывания через кожу. [302] Рыбы поглощают свинец как из воды, так и из отложений; [303] биоаккумуляция в пищевой цепи представляет опасность для рыб, птиц и морских млекопитающих. [304]
Антропогенный свинец включает свинец из дроби и грузил . Они являются одними из самых мощных источников свинцового загрязнения наряду с местами производства свинца. [305] Свинец был запрещен для дроби и грузил в Соединенных Штатах в 2017 году, [306] хотя этот запрет действовал только в течение месяца, [307] и аналогичный запрет рассматривается в Европейском союзе. [308]
Аналитические методы определения свинца в окружающей среде включают спектрофотометрию , рентгеновскую флуоресценцию , атомную спектроскопию и электрохимические методы . Разработан специальный ионселективный электрод на основе ионофора S , S'- метиленбис( N , N - диизобутилдитиокарбамат ). [309] Важным биомаркером отравления свинцом является анализ уровня δ-аминолевулиновой кислоты в плазме, сыворотке и моче. [310]

К середине 1980-х годов наблюдалось значительное снижение использования свинца в промышленности. [311] В Соединенных Штатах экологические нормы сократили или исключили использование свинца в небатарейных продуктах, включая бензин, краски, припои и системы водоснабжения. На угольных электростанциях были установлены устройства контроля твердых частиц для улавливания выбросов свинца. [300] В 1992 году Конгресс США потребовал от Агентства по охране окружающей среды снизить уровень свинца в крови детей страны. [312] Использование свинца было еще больше сокращено Директивой Европейского союза об ограничении опасных веществ 2003 года . [313] Значительное снижение отложений свинца произошло в Нидерландах после введения в 1993 году национального запрета на использование свинцовой дроби для охоты и спортивной стрельбы: с 230 тонн в 1990 году до 47,5 тонн в 1995 году. [314] Использование свинца в топливе Avgas 100LL для авиации общего назначения разрешено в ЕС с 2022 года. [315]
В Соединенных Штатах допустимый предел воздействия свинца на рабочем месте, включая металлический свинец, неорганические соединения свинца и свинцовые мыла, был установлен на уровне 50 мкг/м3 в течение 8-часового рабочего дня, а предельный уровень свинца в крови - 5 мкг на 100 г крови в 2012 году. [316] Свинец все еще может быть обнаружен во вредных количествах в керамической посуде, [317] виниле [318] (например, используемом для труб и изоляции электрических шнуров) и китайской латуни. [u] Старые дома все еще могут содержать свинцовую краску. [318] Белая свинцовая краска была изъята из продажи в промышленно развитых странах, но специализированное использование других пигментов, таких как желтый хромат свинца, сохраняется, [185] особенно в краске для разметки дорожного покрытия. [320] Удаление старой краски путем шлифования приводит к образованию пыли, которую можно вдыхать. [321] Программы по борьбе с выбросами свинца были предписаны некоторыми органами власти в домах, где проживают маленькие дети. [322] Использование свинца в топливе Avgas 100LL для авиации общего назначения, как правило, разрешено в Соединенных Штатах с 2023 года. [323]
Отходы свинца, в зависимости от юрисдикции и характера отходов, могут рассматриваться как бытовые отходы (для содействия мероприятиям по снижению выбросов свинца) [324] или как потенциально опасные отходы, требующие специальной обработки или хранения. [325] Свинец выбрасывается в окружающую среду в местах стрельбы, и для борьбы с загрязнением свинцом был разработан ряд методов управления свинцом. [326] Миграция свинца может усиливаться в кислых почвах; для борьбы с этим рекомендуется обрабатывать почвы известью для нейтрализации почв и предотвращения выщелачивания свинца. [327]
Были проведены исследования того, как удалить свинец из биосистем биологическими способами: кости рыб исследуются на предмет их способности биоремедиировать свинец в загрязненной почве. [328] [329] Грибок Aspergillus versicolor эффективен при поглощении ионов свинца из промышленных отходов перед их сбросом в водоемы. [330] Были исследованы несколько бактерий на предмет их способности удалять свинец из окружающей среды, включая сульфатредуцирующие бактерии Desulfovibrio и Desulfotomaculum , обе из которых высокоэффективны в водных растворах. [331] Просо Urochloa ramosa обладает способностью накапливать значительные количества металлов, таких как свинец и цинк, в своих побегах и корневых тканях, что делает его важным растением для рекультивации загрязненных почв. [332]
результате регулирующих усилий Агентства по охране окружающей среды уровень свинца в воздухе в стране снизился на 86 процентов в период с 2010 по 2020 год.
Национальные стандарты качества окружающего воздуха (40 CFR часть 50) для шести основных загрязняющих веществ
![]() Эта статья была отправлена в WikiJournal of Science для внешнего академического рецензирования в 2017 году (отчеты рецензентов). Обновленный контент был повторно интегрирован в страницу Википедии по лицензии CC-BY-SA-3.0 ( 2018 ). Версия записи, на которой она была проверена: Михаил Болдырев; и др. (3 июля 2018 г.). "Lead: properties, history, and applications" (PDF) . WikiJournal of Science . 1 (2): 7. doi : 10.15347/WJS/2018.007 . ISSN 2470-6345. Wikidata Q56050531.
Эта статья была отправлена в WikiJournal of Science для внешнего академического рецензирования в 2017 году (отчеты рецензентов). Обновленный контент был повторно интегрирован в страницу Википедии по лицензии CC-BY-SA-3.0 ( 2018 ). Версия записи, на которой она была проверена: Михаил Болдырев; и др. (3 июля 2018 г.). "Lead: properties, history, and applications" (PDF) . WikiJournal of Science . 1 (2): 7. doi : 10.15347/WJS/2018.007 . ISSN 2470-6345. Wikidata Q56050531.
спрос на свинец более чем удвоился с начала 1990-х годов, и почти 90% его использования теперь приходится на свинцово-кислотные аккумуляторы.