Селен — химический элемент ; он имеет символ Se и атомный номер 34. Это неметалл (реже считается металлоидом ) со свойствами, занимающими промежуточное положение между элементами выше и ниже в таблице Менделеева , серой и теллуром , а также имеет сходство с мышьяком . [8] Он редко встречается в элементарном состоянии или в виде чистых рудных соединений в земной коре . Селен (от древнегреческого σελήνη ( selḗnē ) «луна») был открыт в 1817 году Йёнсом Якобом Берцелиусом , который отметил сходство нового элемента с ранее открытым теллуром (названным в честь Земли).
Селен встречается в сульфидных рудах металлов , где он частично заменяет серу. В промышленных масштабах селен производится как побочный продукт при переработке этих руд, чаще всего во время производства. Минералы, представляющие собой чистые селенидные или селенатные соединения, известны, но редки. Сегодня основными коммерческими сферами применения селена являются производство стекла и производство пигментов . Селен является полупроводником и используется в фотоэлементах . Приложения в электронике , когда-то важные, в основном заменены кремниевыми полупроводниковыми устройствами. Селен до сих пор используется в нескольких типах устройств защиты от перенапряжения постоянного тока и в одном типе флуоресцентных квантовых точек .
Хотя следовые количества селена необходимы для клеточного функционирования у многих животных, включая человека, как элементарный селен, так и (особенно) соли селена токсичны даже в небольших дозах, вызывая селеноз. [9] Селен указан в качестве ингредиента во многих поливитаминах и других пищевых добавках, а также в детских смесях и является компонентом антиоксидантных ферментов глутатионпероксидазы и тиоредоксинредуктазы (которые косвенно восстанавливают некоторые окисленные молекулы в животных и некоторых растениях). а также в трех ферментах дейодиназах . Потребности растений в селене различаются в зависимости от вида: некоторым растениям требуется относительно большое количество селена, а другим, по-видимому, вообще не требуется. [10]

Селен образует несколько аллотропов , которые преобразуются при изменении температуры , в некоторой степени в зависимости от скорости изменения температуры. Селен, полученный химическими реакциями, обычно представляет собой аморфный порошок кирпично-красного цвета. При быстром плавлении он образует черную стекловидную форму, обычно продаваемую в виде шариков. [11] Структура черного селена нерегулярна и сложна и состоит из полимерных колец, содержащих до 1000 атомов в каждом кольце. Черный селен представляет собой хрупкое блестящее твердое вещество, слабо растворимое в CS 2 . При нагревании он размягчается при 50 °С и превращается в серый селен при 180 °С; температура превращения снижается за счет присутствия галогенов и аминов . [8]
Красные α-, β- и γ-формы получают из растворов черного селена путем изменения скорости испарения растворителя (обычно CS 2 ). Все они имеют относительно низкую моноклинную кристаллическую симметрию ( пространственная группа 14) и содержат почти идентичные сморщенные кольца циклооктаселена (Se 8 ) с разным геометрическим расположением, как и в сере . [12] Восемь атомов кольца не эквивалентны (т.е. они не отображаются друг на друга какой-либо операцией симметрии), и фактически в γ-моноклинной форме половина колец находится в одной конфигурации (и ее зеркальном отображении). и половина в другом. [13] [14] Наиболее плотна упаковка в α-форме. В кольцах Se 8 расстояние Se–Se варьируется в зависимости от того, где находится пара атомов в кольце, но в среднем составляет 233,5 пм, а угол Se–Se–Se составляет в среднем 105,7°. Другие аллотропы селена могут содержать кольца Se 6 или Se 7 . [8]
Наиболее стабильная и плотная форма селена — серая и имеет хиральную гексагональную кристаллическую решетку (пр. гр. 152 или 154 в зависимости от хиральности) [15] , состоящую из спиральных полимерных цепочек, где расстояние Se–Se составляет 237,3 пм, а Se–Se – Угол Se равен 103,1°. Минимальное расстояние между цепями — 343,6 м. Серый селен образуется при умеренном нагревании других аллотропов, медленном охлаждении расплавленного селена или конденсации паров селена чуть ниже точки плавления. В то время как другие формы селена являются изоляторами , серый селен является полупроводником , обладающим значительной фотопроводимостью . В отличие от других аллотропов, он нерастворим в CS 2 . [8] Он устойчив к окислению воздухом и не подвергается воздействию неокисляющих кислот . С сильными восстановителями образует полиселениды. Селен не демонстрирует таких изменений вязкости, как сера при постепенном нагревании. [11] [16]
Селен имеет семь встречающихся в природе изотопов . Пять из них, 74 Se, 76 Se, 77 Se, 78 Se, 80 Se, стабильны, при этом 80 Se является наиболее распространенным (49,6% естественного содержания). В природе также встречается долгоживущий первичный радионуклид 82 Se с периодом полураспада 8,76×10 19 лет. [7] Непервичный радиоизотоп 79 Se также встречается в незначительных количествах в урановых рудах как продукт ядерного деления . Селен также имеет множество нестабильных синтетических изотопов от 64 Se до 95 Se; наиболее стабильными являются 75 Se с периодом полураспада 119,78 суток и 72 Se с периодом полураспада 8,4 суток. [17] Изотопы, более легкие, чем стабильные изотопы, в первую очередь подвергаются бета-плюс-распаду до изотопов мышьяка , а изотопы, более тяжелые, чем стабильные изотопы, подвергаются бета-распаду до изотопов брома , с некоторыми незначительными ветвями нейтронного излучения в самых тяжелых известных изотопах.
Соединения селена обычно существуют в степенях окисления -2, +2, +4 и +6.

Селен образует два оксида : диоксид селена (SeO 2 ) и триоксид селена (SeO 3 ). Диоксид селена образуется при сгорании элементарного селена: [11]
Это полимерное твердое вещество, образующее мономерные молекулы SeO 2 в газовой фазе. Растворяется в воде с образованием селенистой кислоты H 2 SeO 3 . Селенистую кислоту также можно получить непосредственно путем окисления элементарного селена азотной кислотой : [20]
В отличие от серы, которая образует стабильный триоксид , триоксид селена термодинамически нестабилен и при температуре выше 185 °C разлагается на диоксид: [11] [20]
Триоксид селена получают в лаборатории реакцией безводного селената калия (K 2 SeO 4 ) и триоксида серы (SO 3 ). [21]
Соли селенистой кислоты называются селенитами. К ним относятся селенит серебра (Ag 2 SeO 3 ) и селенит натрия (Na 2 SeO 3 ).
Сероводород реагирует с водным раствором селенистой кислоты с образованием дисульфида селена :
Дисульфид селена состоит из 8-членных колец. Он имеет приблизительный состав SeS 2 , с отдельными кольцами разного состава, например Se 4 S 4 и Se 2 S 6 . Дисульфид селена использовался в шампунях в качестве средства против перхоти , ингибитора в химии полимеров, красителя для стекла и восстановителя в фейерверках . [20]
Триоксид селена может быть синтезирован путем дегидратации селеновой кислоты H 2 SeO 4 , которая сама получается окислением диоксида селена перекисью водорода : [22]
Горячая концентрированная селеновая кислота реагирует с золотом с образованием селената золота (III). [23]
Селен реагирует с фтором с образованием гексафторида селена :
По сравнению со своим серным аналогом ( гексафторидом серы ) гексафторид селена (SeF 6 ) более реактивен и является токсичным раздражителем легких . [24] Обладая различной стехиометрией, элементы вместо этого образуют тетрафторид селена , фторирующий агент лабораторного масштаба .
Единственными стабильными хлоридами являются тетрахлорид селена (SeCl 4 ) и монохлорид селена (Se 2 Cl 2 ), который может быть более известен как хлорид селена (I) и по структуре аналогичен дихлориду дисеры . Метастабильные растворы дихлорида селена могут быть приготовлены из сульфурилхлорида и селена (вместо этого в результате реакции элементов образуется тетрахлорид ) и представляют собой важный реагент при получении соединений селена (например, Se 7 ). Все соответствующие бромиды известны и имеют ту же стабильность и структуру, что и хлориды. [25]
Йодиды селена малоизвестны, и долгое время считалось, что они не существуют . [26] Имеются ограниченные спектроскопические доказательства того, что низшие иодиды могут образовываться в двухэлементных растворах с неполярными растворителями, такими как сероуглерод [27] и четыреххлористый углерод ; [26] но даже они, по-видимому, разлагаются под воздействием света . [28]
Некоторые оксигалогениды селена — селенинилфторид (SeOF 2 ) и оксихлорид селена (SeOCl 2 ) — использовались в качестве специальных растворителей. [11]
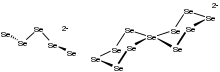
Аналогично поведению других халькогенов селен образует селеноводород H 2 Se. Это сильно пахучий, токсичный и бесцветный газ. Он более кислый, чем H 2 S. В растворе он ионизируется до HSe − . Селенид-дианион Se 2- образует множество соединений, в том числе минералы, из которых селен получают в промышленных масштабах. Иллюстративные селениды включают селенид ртути (HgSe), селенид свинца (PbSe), селенид цинка (ZnSe) и диселенид меди, индия-галлия (Cu(Ga,In)Se 2 ). Эти материалы являются полупроводниками . В случае металлов с высокими электроположительными свойствами, таких как алюминий , эти селениды склонны к гидролизу, который можно описать этим идеализированным уравнением: [11]
Селениды щелочных металлов реагируют с селеном с образованием полиселенидов Se .2−
н, которые существуют в виде цепочек и колец.
Тетраселен тетранитрид Se 4 N 4 представляет собой взрывчатое оранжевое соединение, аналогичное тетранитриду тетраселена (S 4 N 4 ). [11] [30] [31] Его можно синтезировать реакцией тетрахлорида селена (SeCl 4 ) с [((CH
3)
3Си)
2Н]
2Се . [32]
Селен реагирует с цианидами с образованием селеноцианатов : [11]
Селен, особенно во II степени окисления, образует множество органических производных. Структурно они аналогичны соответствующим сероорганическим соединениям . Особенно распространены селениды (R 2 Se, аналоги тиоэфиров ), диселениды (R 2 Se 2 , аналоги дисульфидов ) и селенолы (RSeH, аналоги тиолов ). Представители селенидов, диселенидов и селенолов включают соответственно селенометионин , дифенилдиселенид и бензолселенол . Сульфоксид в химии серы представлен в химии селена селеноксидами (формула RSe(O)R), которые являются промежуточными продуктами органического синтеза, о чем свидетельствует реакция удаления селеноксида . В соответствии с тенденциями, указанными правилом двойной связи , селенокетоны R(C=Se)R и селенальдегиды R(C=Se)H наблюдаются редко. [33]
Селен ( греческое σελήνη selene означает «Луна») был открыт в 1817 году Йенсом Якобом Берцелиусом и Йоханом Готлибом Ганом . [34] Оба химика владели химическим заводом недалеко от Грипсхольма , Швеция, производящим серную кислоту методом свинцовой камеры . Образцы пирита из шахты Фалунь дали красный твердый осадок в свинцовых камерах, который предположительно был соединением мышьяка, поэтому использование пирита для производства кислоты было прекращено. Берцелиус и Ган, которые хотели использовать пирит, заметили, что красный осадок при сжигании издает запах хрена . Этот запах не был свойственен мышьяку, но аналогичный запах был известен у соединений теллура . Следовательно, в первом письме Берцелиуса Александру Марсету говорилось, что это соединение теллура. Однако отсутствие соединений теллура в минералах шахты Фалун в конечном итоге заставило Берцелиуса повторно проанализировать красный осадок, и в 1818 году он написал Марсет второе письмо, описывая недавно обнаруженный элемент, похожий на серу и теллур. Из-за его сходства с теллуром, названным в честь Земли, Берцелиус назвал новый элемент в честь Луны . [35] [36]
В 1873 году Уиллоби Смит обнаружил, что свет влияет на электропроводность серого селена. [37] [38] Это привело к его использованию в качестве клетки для восприятия света. Первые коммерческие продукты с использованием селена были разработаны Вернером Сименсом в середине 1870-х годов. Селеновая ячейка использовалась в фотофоне , разработанном Александром Грэмом Беллом в 1879 году. Селен передает электрический ток, пропорциональный количеству света, падающего на его поверхность. Это явление было использовано при проектировании люксметров и подобных устройств. Полупроводниковые свойства селена нашли множество других применений в электронике. [39] [40] [41] Разработка селеновых выпрямителей началась в начале 1930-х годов, и они заменили выпрямители из оксида меди , поскольку они были более эффективными. [42] [43] [44] Они использовались в коммерческих целях до 1970-х годов, после чего были заменены менее дорогими и даже более эффективными кремниевыми выпрямителями .
Селен привлек внимание врачей позже из-за его токсичности для промышленных рабочих. Селен также был признан важным ветеринарным токсином, который наблюдается у животных, которые ели растения с высоким содержанием селена. В 1954 году биохимик Джейн Пинсент обнаружила первые намеки на специфические биологические функции селена в микроорганизмах . [45] [46] В 1957 году было обнаружено, что он необходим для жизни млекопитающих. [47] [48] В 1970-х годах было показано, что он присутствует в двух независимых наборах ферментов . За этим последовало открытие селеноцистеина в белках. В 1980-х годах было показано, что селеноцистеин кодируется кодоном UGA . Механизм перекодирования был отработан сначала у бактерий , а затем и у млекопитающих (см. элемент SECIS ). [49]

Самородный (т. е. элементарный) селен — редкий минерал, который обычно не образует хороших кристаллов, но если и образует, то представляет собой крутые ромбоэдры или крошечные игольчатые (волосообразные) кристаллы. [50] Выделение селена часто осложняется присутствием других соединений и элементов.
Селен встречается в природе в ряде неорганических форм, включая селенид , селенат и селенит , но эти минералы встречаются редко. Обычный минерал селенит не является минералом селена и не содержит ионов селенита , а представляет собой разновидность гипса (гидрат сульфата кальция), названного как селен в честь Луны задолго до открытия селена. Селен чаще всего встречается в виде примеси, заменяя небольшую часть серы в сульфидных рудах многих металлов. [51] [52]
В живых системах селен содержится в аминокислотах селенометионин , селеноцистеин и метилселеноцистеин . В этих соединениях селен играет роль, аналогичную роли серы. Другое встречающееся в природе селенорганическое соединение — диметилселенид . [53] [54]
Некоторые почвы богаты селеном, а некоторые растения могут биоконцентрировать селен. В почвах селен чаще всего встречается в растворимых формах, таких как селенат (аналог сульфата), которые очень легко вымываются в реки со стоками. [51] [52] Океанская вода содержит значительное количество селена. [55] [56]
Типичные фоновые концентрации селена в атмосфере не превышают 1 нг/м 3 ; 1 мг/кг в почве и растительности и 0,5 мкг/л в пресной и морской воде. [57]
Антропогенные источники селена включают сжигание угля, а также добычу и плавку сульфидных руд. [58]
Селен чаще всего производится из селенида во многих сульфидных рудах , таких как медь , никель или свинец . Электролитическое рафинирование металлов особенно продуктивно по селену как побочному продукту, получаемому из анодного шлама медеперерабатывающих заводов. Другим источником был шлам из свинцовых камер сернокислотных заводов - процесс, который больше не используется . Селен можно очистить из этих грязей несколькими методами. Однако большая часть элементарного селена является побочным продуктом переработки меди или производства серной кислоты . [59] [60] С момента своего изобретения экстракция растворителем и электролизное производство меди (SX/EW) производят все большую долю мировых поставок меди. [61] Это изменяет доступность селена, поскольку только сравнительно небольшая часть селена в руде выщелачивается с медью. [62]
Промышленное производство селена обычно предполагает извлечение диоксида селена из остатков, полученных при очистке меди. Затем обычное производство из остатка начинается с окисления карбонатом натрия с образованием диоксида селена, который смешивается с водой и подкисляется с образованием селенистой кислоты ( стадия окисления ). Селенистую кислоту барботируют диоксидом серы ( этап восстановления ) с получением элементарного селена. [63] [64]
В 2011 году во всем мире было произведено около 2000 тонн селена, в основном в Германии (650 т), Японии (630 т), Бельгии (200 т) и России (140 т), а общие запасы оцениваются в 93 000 т. Эти данные не включают двух крупных производителей: США и Китай. Предыдущий резкий рост наблюдался в 2004 году с 4–5 долларов до 27 долларов за фунт. Цена была относительно стабильной в течение 2004–2010 годов и составляла около 30 долларов США за фунт (партиями по 100 фунтов), но в 2011 году выросла до 65 долларов США за фунт. Потребление в 2010 году распределялось следующим образом: металлургия – 30%, производство стекла – 30%, сельское хозяйство – 10%, химикаты и пигменты – 10% и электроника – 10%. Китай является доминирующим потребителем селена (1500–2000 тонн в год). [65]
При электровыделении марганца добавление диоксида селена снижает мощность, необходимую для работы электролизеров . Китай является крупнейшим потребителем диоксида селена для этих целей. На каждую тонну марганца используется в среднем 2 кг оксида селена. [65] [66]
Наибольшее коммерческое использование селена, составляющее около 50% потребления, приходится на производство стекла. Соединения селена придают стеклу красный цвет. Этот цвет нейтрализует зеленые или желтые оттенки, возникающие из-за примесей железа, типичных для большинства стекол. Для этого добавляют различные соли селенита и селената. Для других применений может потребоваться красный цвет, получаемый смесями CdSe и CdS. [67]
Селен используется вместе с висмутом в латуни для замены более токсичного свинца . Регулирование содержания свинца в питьевой воде, например, в США, с помощью Закона о безопасной питьевой воде 1974 года, сделало необходимым сокращение содержания свинца в латуни. Новая латунь продается под названием EnviroBrass. [68] Подобно свинцу и сере, селен улучшает обрабатываемость стали в концентрациях около 0,15%. [69] [70] Селен обеспечивает такое же улучшение обрабатываемости медных сплавов. [71]
Литий-селеновая (Li-Se) батарея — одна из наиболее перспективных систем хранения энергии в семействе литиевых батарей. [72] Литий-Se аккумулятор является альтернативой литий-серному аккумулятору с преимуществом высокой электропроводности.
Селен использовался в качестве фотопоглощающего слоя в первом твердотельном солнечном элементе, который был продемонстрирован английским физиком Уильямом Гриллсом Адамсом и его учеником Ричардом Эвансом Дэем в 1876 году . [73] Всего за несколько лет Чарльз Фриттс изготовил первый тонкий слой -пленочный солнечный элемент, также использующий селен в качестве фотопоглотителя. Однако с появлением кремниевых солнечных элементов в 1950-х годах исследования тонкопленочных солнечных элементов из селена пошли на спад. В результате рекордная эффективность в 5,0%, продемонстрированная Токио Накада и Акио Куниока в 1985 году, оставалась неизменной более 30 лет. [74] В 2017 году исследователи из IBM достигли нового рекорда эффективности в 6,5% за счет изменения структуры устройства. [75] После этого достижения селен вновь приобрел интерес в качестве фотопоглотителя с широкой запрещенной зоной с потенциалом интеграции в тандеме с фотопоглотителями с более низкой запрещенной зоной. [76] Однако большой дефицит напряжения холостого хода в настоящее время является основным ограничивающим фактором для дальнейшего повышения эффективности, что требует дефектоскопии тонких пленок селена для увеличения срока службы носителей . [77] На сегодняшний день единственная стратегия устранения дефектов, которая была исследована для тонкопленочных солнечных элементов селена, включает кристаллизацию селена с использованием лазера . [78]
Тонкие пленки аморфного селена (α-Se) нашли применение в качестве фотопроводников в плоских детекторах рентгеновского излучения . В этих детекторах используется аморфный селен для захвата и преобразования падающих рентгеновских фотонов непосредственно в электрический заряд. Селен был выбран для этого применения среди других полупроводников благодаря сочетанию его благоприятных технологических и физических свойств: [79] [80]
Селеновые выпрямители были впервые использованы в 1933 году. В основном их заменили устройства на основе кремния. Одним заметным исключением является защита от скачков напряжения постоянного тока , где превосходные энергетические возможности селеновых подавителей делают их более желательными, чем металлооксидные варисторы . [ нужна цитата ]
Небольшие количества селенорганических соединений использовались для модификации катализаторов, используемых для вулканизации при производстве каучука. [62]
Спрос на селен со стороны электронной промышленности снижается. [65] Его фотоэлектрические и фотопроводящие свойства до сих пор используются в фотокопировании , [81] [82] [83] [84] фотоэлементах , люксметрах и солнечных элементах . Его использование в качестве фотопроводника в копировальных аппаратах для обычной бумаги когда-то было ведущим применением, но в 1980-х годах применение фотокондуктора сократилось (хотя оно все еще оставалось крупным конечным пользователем), поскольку все больше и больше копировальных аппаратов переходили на органические фотопроводники.
Селенид цинка был первым материалом для изготовления синих светодиодов , но на этом рынке доминирует нитрид галлия. [85] Селенид кадмия был важным компонентом квантовых точек . Листы аморфного селена преобразуют рентгеновские изображения в образцы заряда в ксерорадиографии и в твердотельных плоских рентгеновских камерах. [86] Ионизированный селен (Se+24, где 24 внешних D, S и P-орбиталей удалены из-за высоких входных энергий [ необходимы пояснения ] ) является одной из активных сред, используемых в рентгеновских лазерах. [87]
Селен катализирует некоторые химические реакции, но широко не используется из-за проблем с токсичностью. [88] В рентгеновской кристаллографии включение одного или нескольких атомов селена вместо серы помогает при многоволновой аномальной дисперсии и одноволновой аномальной фазировке дисперсии. [89]
Селен используется при тонировании фотоотпечатков и продается в качестве тонера многими производителями фототехники. Селен усиливает и расширяет тональный диапазон черно-белых фотографических изображений и улучшает стойкость отпечатков. [90] [91] [92]
75 Se используется в качестве источника гамма-излучения в промышленной радиографии. [93]
Селен используется в некоторых шампунях против перхоти в форме дисульфида селена , таких как марки Selsun и Vichy Dereos [94] .
Загрязнение селеном может повлиять на некоторые водные системы и быть вызвано антропогенными факторами, такими как сельскохозяйственные стоки и промышленные процессы. [95] Люди, которые едят больше рыбы, как правило, более здоровы, чем те, кто ест меньше, [96] что предполагает отсутствие серьезной проблемы для здоровья человека из-за загрязнения селеном, хотя селен потенциально оказывает воздействие на человека. [97]
Существенные физиологические изменения могут произойти у рыб с высоким содержанием селена в тканях. У рыб, подвергшихся воздействию селена, может наблюдаться отек жаберных пластинок , что препятствует диффузии кислорода через жабры и кровотоку внутри жабр. Дыхательная способность еще больше снижается из-за связывания селена с гемоглобином . Другие проблемы включают дегенерацию ткани печени, отек вокруг сердца, повреждение яйцеклеток в яичниках, катаракту и скопление жидкости в полости тела и голове. Селен часто вызывает уродство у плода рыбы, у которого могут возникнуть проблемы с питанием или дыханием; Также часто встречается деформация плавников или позвоночника. Взрослые рыбы могут выглядеть здоровыми, несмотря на их неспособность производить жизнеспособное потомство.
Селен биоаккумулируется в водной среде обитания, что приводит к более высоким концентрациям в организмах, чем в окружающей воде. Селенорганические соединения могут концентрироваться зоопланктоном более чем в 200 000 раз, когда концентрация в воде находится в диапазоне от 0,5 до 0,8 мкг Se/л. Неорганический селен легче биоаккумулируется в фитопланктоне , чем в зоопланктоне. Фитопланктон может концентрировать неорганический селен в 3000 раз. Дальнейшая концентрация за счет биоаккумуляции происходит вдоль пищевой цепи, поскольку хищники потребляют богатую селеном добычу. Рекомендуется считать концентрацию воды 2 мкг Se/л очень опасной для чувствительных рыб и водоплавающих птиц . Отравление селеном может передаваться от родителей потомству через яйцо, и отравление селеном может сохраняться на протяжении многих поколений. Размножение кряквы нарушается при концентрации в рационе 7 мкг Se/л. Многие донные беспозвоночные могут переносить концентрацию селена в своем рационе до 300 мкг/л. [98]
Биоаккумуляция селена в водной среде приводит к гибели рыбы в зависимости от вида в пораженной зоне. Однако есть несколько видов, которые пережили эти события и перенесли повышенное содержание селена. Также было высказано предположение, что сезон может повлиять на вредное воздействие селена на рыбу. [99]
Отравление водных систем селеном может произойти всякий раз, когда новые сельскохозяйственные стоки проходят через засушливые земли. В результате этого процесса в воду выщелачиваются природные растворимые соединения селена (такие как селенаты), которые затем могут концентрироваться на водно-болотных угодьях по мере испарения воды. Загрязнение водных путей селеном также происходит при выщелачивании селена из золы угольных дымов, при горнодобывающей промышленности и выплавке металлов , переработке сырой нефти и на свалках. [100] Было обнаружено, что высокие уровни селена в водных путях вызывают врожденные заболевания у яйцекладущих видов, включая водно-болотных птиц [101] и рыб. [102] Повышенные уровни метилртути в пище могут усилить вред токсичности селена у яйцекладущих видов. [103] [104]
В озере Бельюс, Северная Каролина, 19 видов рыб были уничтожены из озера из-за сточных вод с содержанием 150–200 мкг Se/л, сброшенных с 1974 по 1986 год с угольной электростанции Duke Energy . В Национальном заповеднике дикой природы Кестерсон в Калифорнии тысячи рыб и водоплавающих птиц были отравлены селеном, находящимся в дренажной системе сельскохозяйственного орошения.
Несмотря на то, что селен в больших дозах токсичен, он является важным микроэлементом для животных. В растениях он встречается в качестве минерала-свидетеля, [105] иногда в токсичных пропорциях в корме (некоторые растения могут накапливать селен в качестве защиты от поедания животными, [106] но другие растения, такие как лосось , требуют селена, и их рост указывает на наличие селена в почве). [107]
Селен является компонентом необычных аминокислот селеноцистеина и селенометионина . У людей селен является питательным микроэлементом , который действует как кофактор восстановления антиоксидантных ферментов, таких как глутатионпероксидазы [108] и некоторых форм тиоредоксинредуктазы, обнаруженных у животных и некоторых растений (этот фермент встречается во всех живых организмах, но не во всех его формы в растениях требуют селена).
Семейство ферментов глутатионпероксидазы (GSH-Px) катализирует определенные реакции, которые удаляют активные формы кислорода, такие как перекись водорода и органические гидропероксиды :
Щитовидная железа и каждая клетка, которая использует гормон щитовидной железы, используют селен, [109] который является кофактором трех из четырех известных типов дейодиназ гормонов щитовидной железы , которые активируют, а затем деактивируют различные гормоны щитовидной железы и их метаболиты; Йодтирониндейодиназы представляют собой подсемейство ферментов дейодиназ , которые используют селен в качестве редкой аминокислоты селеноцистеина. (Только дейодиназа йодтирозиндейодиназа , которая воздействует на последние продукты распада гормона щитовидной железы, не использует селен.) [110]
Селен может ингибировать болезнь Хашимото , при которой собственные клетки щитовидной железы подвергаются атаке как чужеродные. Сообщается о снижении антител к ТПО на 21% при употреблении с пищей 0,2 мг селена. [111]
Повышенное содержание селена в рационе снижает последствия токсичности ртути, [112] [113] [114] , хотя он эффективен только при низких и умеренных дозах ртути. [115] Имеющиеся данные свидетельствуют о том, что молекулярные механизмы токсичности ртути включают необратимое ингибирование селеноферментов, которые необходимы для предотвращения и устранения окислительных повреждений в мозге и эндокринных тканях. [116] [117] Селенсодержащее соединение селенонеин присутствует в крови голубого тунца. [118] [119]
Примерно три миллиарда лет назад прокариотические семейства селенопротеинов стимулировали эволюцию селеноцистеина, аминокислоты. Селен включен в несколько семейств прокариотических селенопротеинов у бактерий, архей и эукариот в виде селеноцистеина [120] , где селенопротеиновые пероксиредоксины защищают бактериальные и эукариотические клетки от окислительного повреждения. Семейства селенопротеинов GSH-Px и дейодиназ эукариотических клеток, по-видимому, имеют бактериальное филогенетическое происхождение. Селеноцистеин-содержащая форма встречается у таких разнообразных видов, как зеленые водоросли, диатомовые водоросли, морские ежи, рыбы и куры. Ферменты селена участвуют в небольших восстанавливающих молекулах глутатиона и тиоредоксина . Одно семейство селенсодержащих молекул (глутатионпероксидазы ) разрушает перекись и восстанавливает поврежденные перекисные клеточные мембраны с помощью глутатиона. Другой селенсодержащий фермент у некоторых растений и животных ( тиоредоксинредуктаза ) генерирует восстановленный тиоредоксин, дитиол, который служит источником электронов для пероксидаз, а также важный восстанавливающий фермент рибонуклеотидредуктазу , который делает предшественники ДНК из предшественников РНК. [121]
Микроэлементы, участвующие в активности ферментов GSH-Px и супероксиддисмутазы, например, селен, ванадий , магний , медь и цинк , возможно, отсутствовали в некоторых земных районах с дефицитом минералов. [120] Морские организмы сохранили, а иногда и расширили свои селенопротеомы, тогда как у некоторых наземных организмов селенопротеомы были редуцированы или полностью утрачены. Эти данные свидетельствуют о том, что, за исключением позвоночных , водная жизнь поддерживает использование селена, тогда как наземная среда обитания приводит к снижению использования этого микроэлемента. [122] Морские рыбы и щитовидная железа позвоночных имеют самую высокую концентрацию селена и йода. Примерно 500 миллионов лет назад пресноводные и наземные растения постепенно оптимизировали выработку «новых» эндогенных антиоксидантов, таких как аскорбиновая кислота (витамин С), полифенолы (включая флавоноиды), токоферолы и т. д. Некоторые из них появились в последние 50–50 лет. 200 миллионов лет, в плодах и цветах покрытосеменных растений. Фактически, покрытосеменные растения (доминирующий сегодня тип растений) и большая часть их антиоксидантных пигментов эволюционировали в конце юрского периода. [ нужна цитата ]
Изоферменты дейодиназы составляют другое семейство эукариотических селеноферментов. Дейодиназы участвуют в регуляции гормонов щитовидной железы, участвуя в защите тироцитов от повреждения H 2 O 2 , образующегося для биосинтеза гормонов щитовидной железы. [123] Около 200 миллионов лет назад были разработаны новые селенопротеины как ферменты GSH-Px млекопитающих. [124] [125] [126] [127]
Диетический селен поступает из мяса, орехов, круп и грибов. Бразильские орехи являются самым богатым пищевым источником (хотя это зависит от почвы, поскольку бразильскому ореху не требуется большое количество этого элемента для собственных нужд). [128] [129]
Рекомендуемая в США диетическая норма (RDA) селена для подростков и взрослых составляет 55 мкг /день. Селен в качестве пищевой добавки доступен во многих формах, включая мультивитаминные/минеральные добавки, которые обычно содержат 55 или 70 мкг на порцию. Добавки, содержащие селен, обычно содержат 100 или 200 мкг/порцию.
В июне 2015 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) опубликовало окончательное правило, устанавливающее требования к минимальному и максимальному уровню содержания селена в детской смеси . [130]
Считается, что содержание селена в организме человека находится в диапазоне 13–20 мг. [131]
Некоторые виды растений считаются индикаторами высокого содержания селена в почве, поскольку для их роста требуется высокий уровень селена. Основными растениями-индикаторами селена являются виды Astragalus (в том числе некоторые виды лосось ), плюмаж принца ( Stanleya sp.), астры древесные ( Xylorhiza sp.) и золотарник ложный ( Oonopsis sp.) [132].
Селен можно измерять в крови, плазме, сыворотке или моче для мониторинга чрезмерного воздействия окружающей среды или на рабочем месте, для подтверждения диагноза отравления у госпитализированных жертв или для расследования предполагаемого случая смертельной передозировки. Некоторые аналитические методы способны отличать органические формы элемента от неорганических. Как органические, так и неорганические формы селена в значительной степени превращаются в организме в конъюгаты моносахаридов (селеносахара) перед выведением с мочой. У онкологических больных, получающих ежедневные пероральные дозы селенотионина, могут достигаться очень высокие концентрации селена в плазме и моче. [133]

Хотя селен является важным микроэлементом , он токсичен, если принимать его в избытке. Превышение допустимого верхнего уровня потребления в 400 микрограммов в день может привести к селенозу. [135] Этот допустимый верхний уровень потребления в 400 мкг основан главным образом на исследовании 1986 года с участием пяти китайских пациентов, у которых наблюдались явные признаки селеноза, и на последующем исследовании с участием тех же пяти человек в 1992 году. [136] Исследование 1992 года выявило максимальный уровень потребления. безопасное потребление селена с пищей должно составлять примерно 800 микрограммов в день (15 микрограммов на килограмм массы тела), но рекомендуется 400 микрограммов в день, чтобы избежать дисбаланса питательных веществ в рационе и соответствовать данным других стран. [137] В Китае люди, которые употребляли кукурузу, выращенную в чрезвычайно богатом селеном каменном угле (углистом сланце ), страдали от токсичности селена. Было показано, что в этом угле содержание селена достигает 9,1%, что является самой высокой концентрацией в угле, когда-либо зарегистрированной. [138]
Признаки и симптомы селеноза включают запах чеснока изо рта, желудочно-кишечные расстройства, выпадение волос, шелушение ногтей, усталость, раздражительность и неврологические нарушения. Крайние случаи селеноза могут проявляться циррозом печени, отеком легких или смертью. [139] Элементарный селен и большинство селенидов металлов обладают относительно низкой токсичностью из-за низкой биодоступности . Напротив, селенаты и селениты обладают окислительным механизмом действия, аналогичным действию триоксида мышьяка , и очень токсичны. Хроническая токсическая доза селенита для человека составляет от 2400 до 3000 мкг селена в день. [140] Селеноводород — чрезвычайно токсичный и едкий газ. [141] Селен также встречается в органических соединениях, таких как диметилселенид, селенометионин , селеноцистеин и метилселеноцистеин , все из которых имеют высокую биодоступность и токсичны в больших дозах.
19 апреля 2009 года 21 пони для игры в поло умерла незадолго до матча Открытого чемпионата США по поло. Три дня спустя аптека опубликовала заявление, объясняющее, что лошади получили неправильную дозу одного из ингредиентов, используемых в витаминно-минеральной добавке, которая была неправильно приготовлена в аптеке . Анализ уровней неорганических соединений в добавке в крови показал, что концентрации селена в образцах крови были в 10–15 раз выше нормы , а в образцах печени – в 15–20 раз выше нормы. Позже было подтверждено, что селен является токсичным фактором. [142]

Рыбам и другим диким животным селен необходим для жизни, но в высоких дозах токсичен. Для лосося оптимальная концентрация селена составляет около 1 микрограмма селена на грамм массы всего тела. Гораздо ниже этого уровня молодь лосося умирает от дефицита; [144] гораздо выше, они умирают от избытка токсических веществ. [143]
Управление по охране труда (OSHA) установило законный предел ( допустимый предел воздействия ) для селена на рабочем месте на уровне 0,2 мг/м 3 в течение 8-часового рабочего дня. Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) 0,2 мг/м 3 в течение 8-часового рабочего дня. При уровне 1 мг/м 3 селен сразу опасен для жизни и здоровья . [146]
Дефицит селена может возникнуть у пациентов с тяжелыми нарушениями функции кишечника , у пациентов, находящихся на полном парентеральном питании , и [147] у лиц пожилого возраста (старше 90 лет). Кроме того, в зоне риска находятся люди, зависящие от продуктов питания, выращенных на почвах с дефицитом селена. Хотя почва Новой Зеландии имеет низкий уровень селена, у жителей не было обнаружено вредных последствий для здоровья. [148]
Дефицит селена, определяемый низкими (<60% от нормы) уровнями активности селеноферментов в мозге и эндокринных тканях, возникает только тогда, когда низкий уровень селена связан с дополнительным стрессом, таким как сильное воздействие ртути [ 149] или повышенным окислительным стрессом от дефицит витамина Е. [150]
Селен взаимодействует с другими питательными веществами, такими как йод и витамин Е. Влияние дефицита селена на здоровье остается неопределенным, особенно в отношении болезни Кашина-Бека . [151] Кроме того, селен взаимодействует с другими минералами, такими как цинк и медь . Высокие дозы добавок селена у беременных животных могут нарушить соотношение цинк:медь и привести к снижению содержания цинка; в таких случаях лечения следует контролировать уровень цинка. Для подтверждения этих взаимодействий необходимы дальнейшие исследования. [152]
В регионах (например, в различных регионах Северной Америки), где низкие уровни селена в почве приводят к низким концентрациям в растениях, некоторые виды животных могут испытывать дефицит, если селен не дополняется с помощью диеты или инъекций. [153] Жвачные животные особенно восприимчивы. В целом всасывание пищевого селена у жвачных ниже, чем у других животных, и ниже из кормов, чем из зерна. [154] Жвачные животные, выпасающие определенные корма, например, некоторые сорта белого клевера , содержащие цианогенные гликозиды , могут иметь более высокие потребности в селене, [154] предположительно потому, что цианид высвобождается из агликона под действием глюкозидазы в рубце [155] , а глутатионпероксидазы дезактивируются цианид, действующий на глутатионовый фрагмент . [156] Новорожденным жвачным животным, подверженным риску заболевания белых мышц , можно вводить как селен, так и витамин Е путем инъекций; некоторые из миопатий ОМП реагируют только на селен, некоторые только на витамин Е, а некоторые и на то и на другое. [157]
Влияние потребления селена на рак изучалось в нескольких клинических и эпидемиологических исследованиях на людях. Селен может играть химиопрофилактическую роль в предотвращении риска развития рака в качестве антиоксиданта и может вызывать иммунный ответ. В низких концентрациях он используется в организме для создания антиоксидантных селенопротеинов , в более высоких дозах, чем обычно, он вызывает гибель клеток. [134]
Селен (в тесной взаимосвязи с йодом ) играет роль в здоровье щитовидной железы. Селен является кофактором трех дейодиназ гормонов щитовидной железы , помогая активировать, а затем деактивировать различные гормоны щитовидной железы и их метаболиты. Изолированный дефицит селена в настоящее время исследуется на предмет его роли в индукции аутоиммунных реакций в щитовидной железе при болезни Хашимото . [158] Однако в случае комбинированного дефицита йода и селена было показано, что дефицит селена играет защитную роль для щитовидной железы. [159]
NUBASE2016была вызвана, но так и не определена (см. страницу справки ).В более высоких дозах селен может быть токсичным для ряда животных, включая человека.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )