Эстрадиол ( E2 ), также называемый эстрогеном , эстрадиолом , является эстрогеновым стероидным гормоном и основным женским половым гормоном . Он участвует в регуляции женских репродуктивных циклов, таких как эстральный и менструальный циклы . Эстрадиол отвечает за развитие женских вторичных половых признаков , таких как грудь , расширение бедер и женский тип распределения жира . Он также важен для развития и поддержания женских репродуктивных тканей, таких как молочные железы , матка и влагалище, в период полового созревания , взрослой жизни и беременности . [7] Он также оказывает важное влияние на многие другие ткани, включая кости , жир , кожу , печень и мозг .
Хотя уровень эстрадиола у мужчин намного ниже, чем у женщин, эстрадиол играет важную роль и у мужчин. Помимо людей и других млекопитающих , эстрадиол также обнаружен у большинства позвоночных и ракообразных , насекомых , рыб и других видов животных . [8] [9]
Эстрадиол вырабатывается в фолликулах яичников и в других тканях, включая яички , надпочечники , жир, печень , грудь и мозг. Эстрадиол вырабатывается в организме из холестерина через ряд реакций и промежуточных продуктов . [10] Основной путь включает образование андростендиона , который затем преобразуется ароматазой в эстрон и впоследствии преобразуется в эстрадиол. Альтернативно, андростендион может быть преобразован в тестостерон , который затем может быть преобразован в эстрадиол. После менопаузы у женщин выработка эстрогенов яичниками прекращается, и уровень эстрадиола снижается до очень низкого уровня.
Помимо своей роли естественного гормона, эстрадиол используется в качестве лекарственного средства , например, в менопаузальной гормональной терапии и феминизирующей гормональной терапии для трансгендерных женщин ; для получения информации об эстрадиоле как лекарственном средстве см. статью Эстрадиол (лекарство) .
Развитие вторичных половых признаков у женщин обусловлено эстрогенами, а именно эстрадиолом. [11] [12] Эти изменения инициируются во время полового созревания , большинство из них усиливаются в репродуктивном возрасте и становятся менее выраженными с уменьшением поддержки эстрадиола после менопаузы . Таким образом, эстрадиол вызывает развитие груди и отвечает за изменения формы тела , влияя на кости, суставы и отложение жира . [11] [12] У женщин эстрадиол вызывает развитие груди, расширение бедер , женское распределение жира (с отложением жира, в частности, в груди, бедрах, бедрах и ягодицах), а также созревание влагалища и вульвы , тогда как он опосредует пубертатный скачок роста (косвенно через повышенную секрецию гормона роста ) [13] и эпифизарное закрытие (тем самым ограничивая окончательный рост ) у обоих полов. [11] [12]
У женщин эстрадиол действует как гормон роста для тканей репродуктивных органов, поддерживая слизистую оболочку влагалища , цервикальные железы, эндометрий и слизистую оболочку маточных труб. Он усиливает рост миометрия . Эстрадиол, по-видимому, необходим для поддержания ооцитов в яичнике . Во время менструального цикла эстрадиол, вырабатываемый растущими фолликулами, запускает через систему положительной обратной связи гипоталамо-гипофизарные события, которые приводят к выбросу лютеинизирующего гормона , вызывая овуляцию. В лютеиновой фазе эстрадиол в сочетании с прогестероном подготавливает эндометрий к имплантации . Во время беременности эстрадиол увеличивается из-за продукции плаценты . Эффект эстрадиола вместе с эстроном и эстриолом во время беременности менее ясен. Они могут способствовать кровотоку в матке, росту миометрия, стимулировать рост груди и в срок, способствовать размягчению шейки матки и экспрессии миометриальных окситоциновых рецепторов. [ необходима цитата ] У бабуинов блокирование выработки эстрогена приводит к потере беременности, что предполагает, что эстрадиол играет роль в поддержании беременности. Исследования изучают роль эстрогенов в процессе инициации родов . Действия эстрадиола необходимы до воздействия прогестерона в лютеиновой фазе. [ необходима цитата ]
Влияние эстрадиола (и эстрогенов в целом) на мужскую репродуктивную функцию является сложным. Эстрадиол вырабатывается под действием ароматазы, в основном, в клетках Лейдига яичек млекопитающих , а также некоторыми зародышевыми клетками и клетками Сертоли неполовозрелых млекопитающих. [14] Он действует ( in vitro ), предотвращая апоптоз мужских сперматозоидов . [15] Хотя некоторые исследования в начале 1990-х годов утверждали о связи между глобальным снижением количества сперматозоидов и воздействием эстрогена в окружающей среде, [16] более поздние исследования не обнаружили такой связи или доказательств общего снижения количества сперматозоидов. [17] [18] Подавление выработки эстрадиола в субпопуляции субфертильных мужчин может улучшить анализ спермы . [19]
У мужчин с определенными генетическими заболеваниями половых хромосом , такими как синдром Клайнфельтера , будет более высокий уровень эстрадиола. [20]
Эстрадиол оказывает сильное воздействие на кости. Люди без него (или других эстрогенов) станут высокими и евнухоидными , поскольку закрытие эпифизов задерживается или может не произойти. [21] Плотность костей также страдает, что приводит к ранней остеопении и остеопорозу . [22] Низкий уровень эстрадиола также может предсказывать переломы, причем женщины в постменопаузе имеют самую высокую частоту переломов костей . [23] Женщины после менопаузы испытывают ускоренную потерю костной массы из-за относительного дефицита эстрогена. [24]
Рецептор эстрогена , а также рецептор прогестерона были обнаружены в коже , в том числе в кератиноцитах и фибробластах . [25] [26] В период менопаузы и после нее снижение уровня женских половых гормонов приводит к атрофии , истончению и увеличению морщинистости кожи, а также к снижению эластичности , упругости и прочности кожи. [25] [26] Эти изменения кожи представляют собой ускорение старения кожи и являются результатом снижения содержания коллагена , нарушений в морфологии эпидермальных клеток кожи , уменьшения основного вещества между волокнами кожи и уменьшения капилляров и кровотока . [25] [26] Кожа также становится более сухой во время менопаузы, что связано с уменьшением гидратации кожи и поверхностных липидов (выработки кожного сала). [25] Наряду с хронологическим старением и фотостарением, дефицит эстрогена в период менопаузы является одним из трех основных факторов, которые преимущественно влияют на старение кожи. [25]
Гормонозаместительная терапия, состоящая из системного лечения эстрогеном отдельно или в сочетании с прогестагеном, имеет хорошо документированные и значительные полезные эффекты на кожу женщин в постменопаузе. [25] [26] Эти преимущества включают увеличение содержания коллагена в коже, толщины и эластичности кожи, а также увлажнения кожи и поверхностных липидов. [25] [26] Было обнаружено, что местный эстроген оказывает аналогичное полезное воздействие на кожу. [25] Кроме того, исследование показало, что местный 2% прогестероновый крем значительно повышает эластичность и упругость кожи и заметно уменьшает морщины у женщин в пери- и постменопаузе. [26] С другой стороны, увлажнение кожи и поверхностные липиды существенно не изменились при местном применении прогестерона. [26] Эти результаты свидетельствуют о том, что прогестерон, как и эстроген, также оказывает полезное воздействие на кожу и может независимо защищать от старения кожи. [26]
Эстрогены могут вырабатываться в мозге из стероидных предшественников. Как антиоксиданты , они, как было обнаружено, обладают нейропротекторной функцией. [27]
Положительные и отрицательные обратные связи менструального цикла включают эстрадиол яичников как связующее звено с гипоталамо-гипофизарной системой для регуляции гонадотропинов . [28]
Эстроген, как полагают, играет важную роль в психическом здоровье женщин, и предполагается связь между уровнем гормонов, настроением и благополучием. Внезапные падения или колебания или длительные периоды устойчиво низких уровней эстрогена могут быть связаны со значительным снижением настроения. Было показано, что клиническое выздоровление от депрессии после родов, перименопаузы и постменопаузы эффективно после стабилизации и/или восстановления уровней эстрогена. [29] [30]
Было обнаружено, что объемы сексуально диморфных структур мозга у трансгендерных женщин изменяются и приближаются к типичным женским структурам мозга при воздействии эстрогена одновременно с лишением андрогенов в течение нескольких месяцев [31] , что позволяет предположить, что эстроген и/или андрогены играют важную роль в половой дифференциации мозга как в пренатальный период , так и на более поздних этапах жизни.
Также имеются данные, что программирование полового поведения взрослых самцов у многих позвоночных в значительной степени зависит от эстрадиола, вырабатываемого в пренатальном периоде и раннем младенчестве. [32] Пока неизвестно, играет ли этот процесс значительную роль в сексуальном поведении человека, хотя данные, полученные в ходе исследований других млекопитающих, указывают на наличие связи. [33]
Было обнаружено, что эстроген увеличивает секрецию окситоцина и увеличивает экспрессию его рецептора , рецептора окситоцина , в мозге . [34] Было обнаружено, что у женщин однократная доза эстрадиола достаточна для увеличения концентрации циркулирующего окситоцина. [35]
Эстрадиол был связан с развитием и прогрессированием таких видов рака, как рак груди, рак яичников и рак эндометрия. Эстрадиол влияет на целевые ткани в основном путем взаимодействия с двумя ядерными рецепторами, называемыми рецептором эстрогена α (ERα) и рецептором эстрогена β (ERβ). [36] [37] Одной из функций этих рецепторов эстрогена является модуляция экспрессии генов . После того, как эстрадиол связывается с ER, рецепторные комплексы затем связываются со специфическими последовательностями ДНК , что может привести к повреждению ДНК и увеличению деления клеток и репликации ДНК . Эукариотические клетки реагируют на поврежденную ДНК, стимулируя или нарушая фазы G1, S или G2 клеточного цикла, чтобы инициировать репарацию ДНК . В результате происходит клеточная трансформация и пролиферация раковых клеток. [38]
Эстроген влияет на определенные кровеносные сосуды . Улучшение артериального кровотока было продемонстрировано в коронарных артериях . [39] 17-бета-эстрадиол (E2) считается самым мощным эстрогеном, обнаруженным у людей. E2 влияет на сосудистую функцию, апоптоз и повреждение во время сердечной ишемии и реперфузии. E2 может защитить сердце и отдельные сердечные миоциты от повреждений, связанных с ишемией. После сердечного приступа или длительных периодов гипертонии E2 подавляет неблагоприятные эффекты патологического ремоделирования сердца. [40]
Во время беременности высокий уровень эстрогенов, а именно эстрадиола, увеличивает коагуляцию и риск венозной тромбоэмболии .
Эстрадиол оказывает комплексное воздействие на печень . Он влияет на выработку множества белков , включая липопротеины , связывающие белки и белки, отвечающие за свертываемость крови . [ необходима цитата ] В больших количествах эстрадиол может привести к холестазу , например, холестазу беременности .
Некоторые гинекологические состояния зависят от эстрогена, такие как эндометриоз , лейомиома матки и маточное кровотечение . [ необходима ссылка ]
Эстрадиол действует в первую очередь как агонист рецептора эстрогена ( ER), ядерного рецептора стероидных гормонов . Существует два подтипа ER, ERα и ERβ , и эстрадиол мощно связывается с обоими этими рецепторами и активирует их. Результатом активации ER является модуляция транскрипции и экспрессии генов в клетках , экспрессирующих ER , что является преобладающим механизмом, с помощью которого эстрадиол опосредует свои биологические эффекты в организме. Эстрадиол также действует как агонист мембранных рецепторов эстрогена (mER), таких как GPER (GPR30), недавно обнаруженный неядерный рецептор эстрадиола, через который он может опосредовать множество быстрых негеномных эффектов . [42] В отличие от случая ER, GPER, по-видимому, является селективным для эстрадиола и демонстрирует очень низкое сродство к другим эндогенным эстрогенам, таким как эстрон и эстриол . [43] Дополнительные mER помимо GPER включают ER-X , ERx и G q -mER . [44] [45]
ERα/ERβ находятся в неактивном состоянии, запертые в мультимолекулярных шаперонных комплексах, организованных вокруг белка теплового шока 90 (HSP90), содержащего белок p23 и иммунофилин, и расположенных в основном в цитоплазме и частично в ядре. В классическом пути E2 или классическом пути эстрогена эстрадиол попадает в цитоплазму , где взаимодействует с ER. После связывания с E2 ER диссоциируют от молекулярных шаперонных комплексов и становятся компетентными для димеризации, миграции в ядро и связывания со специфическими последовательностями ДНК ( элемент ответа эстрогена , ERE), что позволяет транскрипцию генов, которая может происходить в течение часов и дней.
Введенный мышам путем подкожной инъекции , эстрадиол примерно в 10 раз более эффективен, чем эстрон, и примерно в 100 раз более эффективен, чем эстриол. [46] [47] [48] Таким образом, эстрадиол является основным эстрогеном в организме, хотя роль эстрона и эстриола как эстрогенов, как говорят, не является незначительной. [48]

Эстрадиол, как и другие стероидные гормоны , образуется из холестерина . После расщепления боковой цепи и использования Δ 5 или Δ 4 - пути, андростендион является ключевым посредником. Часть андростендиона преобразуется в тестостерон, который, в свою очередь, подвергается преобразованию в эстрадиол ароматазой. В альтернативном пути андростендион ароматизируется в эстрон , который впоследствии преобразуется в эстрадиол через 17β-гидроксистероиддегидрогеназу (17β-HSD). [50]
В репродуктивном возрасте большая часть эстрадиола у женщин вырабатывается гранулезными клетками яичников путем ароматизации андростендиона (вырабатываемого в клетках теки фолликули) в эстрон, с последующим преобразованием эстрона в эстрадиол 17β-HSD. Меньшие количества эстрадиола также вырабатываются корой надпочечников , а у мужчин — яичками. [ медицинская цитата необходима ]
Эстрадиол вырабатывается не только в половых железах ; в частности, жировые клетки вырабатывают активные предшественники эстрадиола и будут продолжать делать это даже после менопаузы. [51] Эстрадиол также вырабатывается в мозге и в стенках артерий .
У мужчин приблизительно от 15 до 25% циркулирующего эстрадиола вырабатывается в яичках . [52] [53] Остальная часть синтезируется путем периферической ароматизации тестостерона в эстрадиол и андростендиона в эстрон (который затем трансформируется в эстрадиол через периферический 17β-HSD). [52] [53] Эта периферическая ароматизация происходит преимущественно в жировой ткани , но также происходит и в других тканях, таких как кости , печень и мозг . [52] Примерно от 40 до 50 мкг эстрадиола вырабатывается в день у мужчин. [52]
В плазме эстрадиол в основном связан с ГСПГ и альбумином . Только около 2,21% (± 0,04%) эстрадиола является свободным и биологически активным. Процент остается постоянным в течение менструального цикла . [54]
Инактивация эстрадиола включает преобразование в менее активные эстрогены, такие как эстрон и эстриол. Эстриол является основным мочевым метаболитом . [ требуется цитата ] Эстрадиол конъюгируется в печени с образованием конъюгатов эстрогена , таких как эстрадиолсульфат , эстрадиолглюкуронид , и, как таковые, выводятся через почки . Некоторые из водорастворимых конъюгатов выводятся через желчные протоки и частично реабсорбируются после гидролиза из кишечного тракта . Эта энтерогепатическая циркуляция способствует поддержанию уровня эстрадиола.
Эстрадиол также метаболизируется посредством гидроксилирования в катехолэстрогены . В печени он неспецифически метаболизируется CYP1A2 , CYP3A4 и CYP2C9 посредством 2-гидроксилирования в 2-гидроксиэстрадиол , а также CYP2C9 , CYP2C19 и CYP2C8 посредством 17β-гидроксидегидрогенизации в эстрон , [55] с участием различных других ферментов цитохрома P450 (CYP) и метаболических преобразований . [56]
Эстрадиол дополнительно конъюгируется со сложным эфиром в липоидные формы эстрадиола, такие как эстрадиолпальмитат и эстрадиолстеарат в определенной степени; эти сложные эфиры хранятся в жировой ткани и могут действовать как очень долгосрочный резервуар эстрадиола. [57] [58]
Эстрадиол выводится в виде глюкуронида и сульфатных эстрогеновых конъюгатов в мочу . После внутривенной инъекции меченого эстрадиола у женщин почти 90% выводится с мочой и калом в течение 4–5 дней. [59] [60] Энтерогепатическая рециркуляция вызывает задержку выведения эстрадиола. [59 ]

Уровни эстрадиола у женщин в пременопаузе сильно варьируются в течение менструального цикла, и референтные диапазоны значительно различаются от источника к источнику. [62] Уровни эстрадиола минимальны и, по данным большинства лабораторий, колеблются от 20 до 80 пг/мл в течение ранней и средней фолликулярной фазы (или первой недели менструального цикла, также известной как менструация). [63] [64] Уровни эстрадиола постепенно увеличиваются в течение этого времени и в течение средней и поздней фолликулярной фазы (или второй недели менструального цикла) до преовуляторной фазы. [62] [63] Во время преовуляции (период примерно от 24 до 48 часов) уровни эстрадиола кратковременно повышаются и достигают самых высоких концентраций в любое другое время в течение менструального цикла. [62] Уровень циркулирующего эстрадиола обычно составляет от 130 до 200 пг/мл в это время, но у некоторых женщин он может достигать 300–400 пг/мл, а верхний предел референтного диапазона некоторых лабораторий даже выше (например, 750 пг/мл). [62] [63] [65] [66] [67] После овуляции (или середины цикла) и во второй половине менструального цикла или лютеиновой фазы уровни эстрадиола выходят на плато и колеблются между примерно 100 и 150 пг/мл в течение ранней и средней лютеиновой фазы, а во время поздней лютеиновой фазы или за несколько дней до менструации достигают минимума около 40 пг/мл. [62] [64] Средние интегрированные уровни эстрадиола в течение полного менструального цикла по-разному сообщались разными источниками как 80, 120 и 150 пг/мл. [64] [68] [69] Хотя существуют противоречивые сообщения, одно исследование обнаружило средние интегрированные уровни эстрадиола 150 пг/мл у молодых женщин, тогда как средние интегрированные уровни варьировались от 50 до 120 пг/мл у женщин старшего возраста. [69]
В репродуктивном возрасте у женщин уровень эстрадиола несколько выше, чем у эстрона, за исключением ранней фолликулярной фазы менструального цикла; таким образом, эстрадиол можно считать преобладающим эстрогеном в репродуктивном возрасте у женщин с точки зрения абсолютных уровней в сыворотке и эстрогенной активности. [ необходима цитата ] Во время беременности эстриол становится преобладающим циркулирующим эстрогеном, и это единственное время, когда в организме появляется эстерол, в то время как во время менопаузы преобладает эстрон (оба на основе уровней в сыворотке). [ необходима цитата ] Эстрадиол, вырабатываемый мужчинами из тестостерона, присутствует на уровнях в сыворотке, примерно сопоставимых с уровнями у женщин в постменопаузе (14–55 против <35 пг/мл соответственно). [ необходима цитата ] Также сообщалось, что если сравнить концентрацию эстрадиола у 70-летнего мужчины с концентрацией у 70-летней женщины, то у мужчины она будет примерно в 2–4 раза выше. [70]
У женщин сывороточный эстрадиол измеряется в клинической лаборатории и отражает в первую очередь активность яичников. Анализ крови на эстрадиол измеряет количество эстрадиола в крови. [77] Он используется для проверки функции яичников, плаценты, надпочечников. [77] Это может определить базовый уровень эстрогена у женщин с аменореей или менструальной дисфункцией, а также выявить состояние гипоэстрогении и менопаузы. Кроме того, мониторинг эстрогена во время терапии бесплодия оценивает рост фолликулов и полезен для мониторинга лечения. Опухоли, продуцирующие эстроген, будут демонстрировать постоянно высокие уровни эстрадиола и других эстрогенов. При преждевременном половом созревании уровни эстрадиола ненадлежащим образом повышаются.
Результаты отдельных лабораторных исследований всегда следует интерпретировать с использованием диапазонов, предоставленных лабораторией, выполнившей тест.
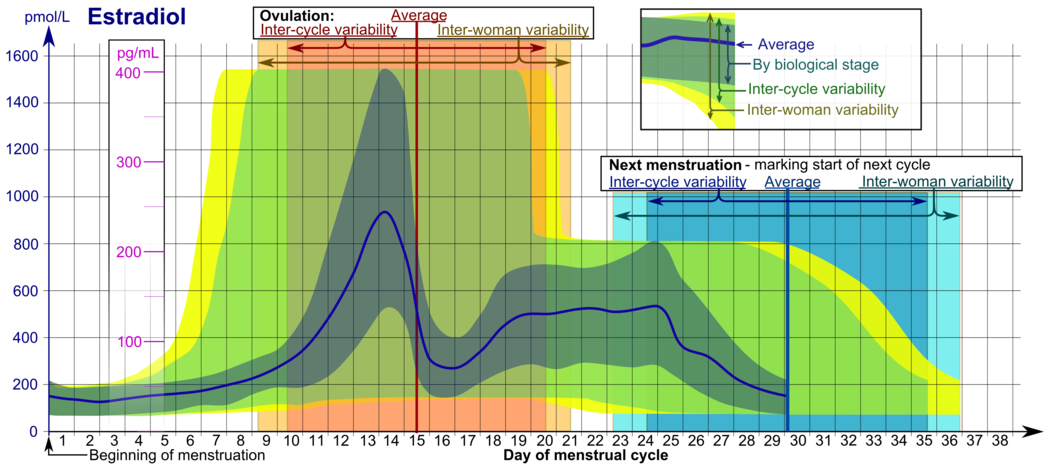
В нормальном менструальном цикле уровень эстрадиола обычно составляет <50 пг/мл во время менструации, повышается с развитием фолликулов (пик: 200 пг/мл), кратковременно падает во время овуляции и снова повышается во время лютеиновой фазы для второго пика. В конце лютеиновой фазы уровень эстрадиола падает до менструального уровня, если только не наступает беременность.
Во время беременности уровень эстрогенов, включая эстрадиол, неуклонно растет к сроку. Источником этих эстрогенов является плацента , которая ароматизирует прогормоны, вырабатываемые в надпочечниках плода.
Эстрадиол используется в качестве лекарственного средства, в основном в гормональной терапии симптомов менопаузы , а также в феминизирующей гормональной терапии для трансгендерных людей. [82]
Эстрадиол — это эстрановый стероид . [82] Он также известен как 17β-эстрадиол (чтобы отличить его от 17α-эстрадиола ) или как эстра-1,3,5(10)-триен-3,17β-диол. Он имеет две гидроксильные группы , одну в положении C3, а другую в положении 17β, а также три двойные связи в кольце A. Из-за двух гидроксильных групп эстрадиол часто сокращенно обозначается как E2. Структурно родственные эстрогены, эстрон (E1), эстриол (E3) и эстетрол (E4) имеют одну, три и четыре гидроксильные группы соответственно.
В рандомизированном, двойном слепом, плацебо-контролируемом исследовании было показано, что эстрадиол оказывает гендерно-специфическое воздействие на чувствительность к справедливости. В целом, когда раздел определенной суммы денег был оформлен как справедливый или несправедливый в модифицированной версии игры в ультиматум , эстрадиол увеличивал процент принятия справедливо сформулированных предложений среди мужчин и уменьшал его среди женщин. Однако в группе плацебо «простая вера в получение лечения эстрадиолом значительно увеличивала принятие несправедливо сформулированных предложений у обоих полов», что указывает на то, что так называемые «средовые» факторы играли роль в организации ответов на эти презентации игры в ультиматум . [83]
Открытие эстрогена обычно приписывают американским ученым Эдгару Аллену и Эдварду А. Дойзи . [84] [85] В 1923 году они наблюдали, что инъекция жидкости из фолликулов свиных яичников вызывала изменения пубертатного и эстрального типа (включая изменения влагалища , матки и молочных желез , а также половую восприимчивость ) у неполовозрелых , овариэктомированных мышей и крыс. [84] [85] [86] Эти результаты продемонстрировали существование гормона , который вырабатывается яичниками и участвует в половом созревании и воспроизводстве . [84] [85] [86] Во время его открытия Аллен и Дойзи не дали гормону названия, а просто назвали его «гормоном яичников» или «фолликулярным гормоном»; [85] другие называли его по-разному: феминин , фолликулин , менформон , теликинин и эмменин . [87] [88] В 1926 году Паркс и Беллерби ввели термин эстрин для описания гормона на основе того, что он вызывает эструс у животных. [89] [87] Эстрон был выделен и очищен независимо Алленом и Дойзи и немецким ученым Адольфом Бутенандтом в 1929 году, а эстриол был выделен и очищен Маррианом в 1930 году; они были первыми идентифицированными эстрогенами. [85] [90] [91]
Эстрадиол, самый мощный из трех основных эстрогенов, был идентифицирован последним из трех. [85] [89] Он был открыт Швенком и Хильдебрантом в 1933 году, которые синтезировали его путем восстановления эстрона. [85] Эстрадиол был впоследствии выделен и очищен из яичников свиноматки Дойзи в 1935 году, при этом его химическая структура была определена одновременно, [92] и назывался по-разному: дигидротелин , дигидрофолликулин , дигидрофолликулярный гормон и дигидроксиэстрин . [85] [93] [94] В 1935 году название эстрадиол и термин эстроген были официально установлены Комитетом по половым гормонам Организации здравоохранения Лиги Наций ; это последовало за названиями эстрон (который изначально назывался телин, прогинон, фолликулин и кетогидроксиэстрин) и эстриол (первоначально называвшийся телол и тригидроксиэстрин), которые были установлены в 1932 году на первом заседании Международной конференции по стандартизации половых гормонов в Лондоне . [89] [95] После его открытия частичный синтез эстрадиола из холестерина был разработан Инхоффеном и Хольвегом в 1940 году, а полный синтез был разработан Аннером и Мишером в 1948 году. [85]
Название эстрадиол происходит от estra- , греч. οἶστρος ( oistros , буквально означает «воодушевление или вдохновение»), [96] что относится к стероидной кольцевой системе эстрана , и -диол , химического термина и суффикса, указывающего на то, что соединение представляет собой тип спирта, содержащего две гидроксильные группы .
Уровни эстрадиола минимальны в течение самых ранних дней фолликулярной фазы, но по мере созревания фолликула в общий кровоток выделяется все большее количество эстрадиола. Самые высокие уровни достигаются примерно за 24–48 часов до пика ЛГ. Фактически, предовуляторный пик эстрадиола представляет собой его самую высокую концентрацию в течение всего менструального цикла. Концентрации сыворотки в это время обычно составляют около 130–200 пг/мл, но у некоторых женщин могут быть достигнуты концентрации до 300–400 пг/мл. После временного падения, связанного с овуляцией, секреция эстрадиола восстанавливается за счет продукции желтым телом во время лютеиновой фазы. Уровни плато около 100–150 пг/мл (Abraham, 1978; Thorneycroft et al., 1971) чаще всего наблюдаются в период от −10 до −5 дней до начала менструации. С регрессией желтого тела уровни эстрадиола падают, постепенно у некоторых женщин и стремительно у других, в течение последних нескольких дней лютеиновой фазы. Это знаменует начало менструации, отторжение эндометрия. Эстрадиол сыворотки во время менструации составляет приблизительно 30–50 пг/мл. (Источник.)
В большинстве лабораторий уровень эстрадиола в сыворотке варьируется от 20 до 80 пг/мл в течение ранней и средней фолликулярной фазы менструального цикла и достигает пика в 200–500 пг/мл во время преовуляторного всплеска. В середине лютеиновой фазы уровень эстрадиола в сыворотке варьируется от 60 до 200 пг/мл.
Уровень эстрадиола в плазме колеблется от 40 до 80 пг/мл в течение 1-й недели овариального цикла (ранняя фолликулярная фаза) и от 80 до 300 пг/мл в течение 2-й недели (средняя и поздняя фолликулярная фаза, включая периовуляторный пик). Затем в течение 3-й и 4-й недель эстрадиол колеблется от 100 до 150 пг/мл (ранняя и средняя лютеиновая фаза) до 40 пг/мл за несколько дней до менструации (поздняя лютеиновая фаза). Средний интегрированный уровень эстрадиола в течение полного 28-дневного нормального цикла составляет около 80 пг/мл.
В середине цикла: 150-750 пг/мл
Середина цикла: 110-330 пг/мл
Овуляторный: 200-400 пг/мл
[...] после менопаузы уровень циркулирующего эстрадиола снижается со среднего значения в пременопаузе 120 пг/мл до всего лишь 13 пг/мл.
[...] [пременопаузальная] средняя концентрация [эстрадиола] 150 пг/мл [...]