Бериллий — химический элемент ; имеет символ Be и атомный номер 4. Это стально-серый, прочный, легкий и хрупкий щелочноземельный металл . Это двухвалентный элемент, который встречается в природе только в сочетании с другими элементами с образованием минералов. Драгоценные камни с высоким содержанием бериллия включают берилл ( аквамарин , изумруд , красный берилл ) и хризоберилл . Это относительно редкий элемент во Вселенной , обычно образующийся в результате расщепления более крупных атомных ядер, столкнувшихся с космическими лучами . В ядрах звезд бериллий обедняется, поскольку он превращается в более тяжелые элементы. Бериллий составляет около 0,0004 процента массы земной коры. Ежегодный объем производства бериллия в мире, составляющий 220 тонн, обычно производится путем экстракции из минерала берилла . Это сложный процесс, поскольку бериллий прочно связывается с кислородом .
В конструкционных применениях сочетание высокой жесткости на изгиб , термической стабильности , теплопроводности и низкой плотности (в 1,85 раза выше, чем у воды) делает металлический бериллий желательным аэрокосмическим материалом для компонентов самолетов, ракет , космических кораблей и спутников . [8] Из-за своей низкой плотности и атомной массы бериллий относительно прозрачен для рентгеновских лучей и других форм ионизирующего излучения ; следовательно, это наиболее распространенный материал окон для рентгеновского оборудования и компонентов детекторов частиц . [8] При добавлении в качестве легирующего элемента к алюминию , меди (особенно сплаву бериллий-медь ), железу или никелю бериллий улучшает многие физические свойства. [8] Например, инструменты и компоненты из медно-бериллиевых сплавов прочны и тверды и не создают искр при ударе о стальную поверхность. На воздухе поверхность бериллия при комнатной температуре легко окисляется с образованием пассивационного слоя толщиной 1–10 нм, защищающего его от дальнейшего окисления и коррозии. [ нужна ссылка ] Металл окисляется в массе (за пределами пассивационного слоя) при нагревании выше 500 ° C (932 ° F) и блестяще горит при нагревании примерно до 2500 ° C (4530 ° F). [ нужна цитата ]
Коммерческое использование бериллия требует постоянного использования соответствующего оборудования для борьбы с пылью и промышленного контроля из-за токсичности вдыхаемой бериллийсодержащей пыли, которая может вызвать у некоторых людей хроническое опасное для жизни аллергическое заболевание, называемое бериллиозом . [9] Бериллиоз вызывает пневмонию и другие сопутствующие респираторные заболевания.
Бериллий представляет собой твердый металл стального цвета , хрупкий при комнатной температуре и имеющий плотноупакованную гексагональную кристаллическую структуру . [8] Он обладает исключительной жесткостью ( модуль Юнга 287 ГПа) и температурой плавления 1287 °C. Модуль упругости бериллия примерно на 35% больше, чем у стали. Сочетание этого модуля и относительно низкой плотности приводит к необычайно высокой скорости звукопроводимости в бериллии — около 12,9 км/с в условиях окружающей среды . Другими важными свойствами являются высокая удельная теплоемкость (1925 Дж·кг -1 ·К -1 ) и теплопроводность (216 Вт·м -1 ·К -1 ), что делает бериллий металлом с лучшими характеристиками теплоотдачи на единицу веса. В сочетании с относительно низким коэффициентом линейного теплового расширения (11,4×10 -6 К -1 ) эти характеристики обеспечивают уникальную стабильность в условиях термической нагрузки. [10]
Встречающийся в природе бериллий, за исключением небольшого загрязнения космогенными радиоизотопами , представляет собой изотопно чистый бериллий-9, имеющий ядерный спин3/2. Бериллий имеет большое сечение рассеяния нейтронов высоких энергий, около 6 барнов для энергий выше примерно 10 кэВ. Следовательно, он работает как отражатель нейтронов и замедлитель нейтронов , эффективно замедляя нейтроны до диапазона тепловой энергии ниже 0,03 эВ, где полное сечение как минимум на порядок ниже; точное значение сильно зависит от чистоты и размера кристаллитов материала.
Единственный первичный изотоп бериллия 9 Be также подвергается нейтронной реакции (n, 2n) с энергией нейтронов около 1,9 МэВ с образованием 8 Be , который почти сразу распадается на две альфа-частицы. Таким образом, для нейтронов высоких энергий бериллий является умножителем нейтронов, выделяя больше нейтронов, чем поглощая. Эта ядерная реакция: [11]
Нейтроны высвобождаются при столкновении ядер бериллия с энергичными альфа-частицами [10] , вызывающими ядерную реакцию.
где4
2Он
является альфа-частицей и12
6С
представляет собой ядро углерода-12 . [11]
Бериллий также выделяет нейтроны при бомбардировке гамма-лучами. Таким образом, природный бериллий, бомбардируемый альфа- или гамма-излучением подходящего радиоизотопа, является ключевым компонентом большинства источников нейтронов ядерных реакций с питанием от радиоизотопов для лабораторного производства свободных нейтронов.
Небольшие количества трития выделяются при9
4Быть
ядра поглощают нейтроны низкой энергии в трехступенчатой ядерной реакции
6
2Он
имеет период полураспада всего 0,8 секунды, β - это электрон, а6
3Ли
имеет высокое сечение поглощения нейтронов. Тритий является вызывающим озабоченность радиоизотопом в потоках отходов ядерных реакторов. [12]
Как металл, бериллий прозрачен или полупрозрачен для большинства длин волн рентгеновских лучей и гамма-лучей , что делает его полезным для выходных окон рентгеновских трубок и других подобных устройств. [13]
В звездах создаются как стабильные, так и нестабильные изотопы бериллия, но радиоизотопы сохраняются недолго. Считается, что большая часть стабильного бериллия во Вселенной изначально образовалась в межзвездной среде, когда космические лучи вызвали деление более тяжелых элементов, обнаруженных в межзвездном газе и пыли. [14] Первичный бериллий содержит только один стабильный изотоп, 9 Be, и поэтому бериллий является моноизотопным и мононуклидным элементом .

Радиоактивный космогенный 10 Be образуется в атмосфере Земли в результате расщепления кислорода космическими лучами . [15] 10 Be накапливается на поверхности почвы , где его относительно длительный период полураспада (1,36 миллиона лет) обеспечивает длительное время пребывания перед распадом до бора -10. Таким образом, 10 Be и его дочерние продукты используются для изучения естественной эрозии почвы , почвообразования и развития латеритных почв , а также в качестве показателя для измерения изменений солнечной активности и возраста ледяных кернов . [16] Производство 10 Be обратно пропорционально солнечной активности, поскольку усиление солнечного ветра в периоды высокой солнечной активности уменьшает поток галактических космических лучей , достигающих Земли. [15] Ядерные взрывы также образуют 10 Be в результате реакции быстрых нейтронов с 13 C в углекислом газе в воздухе. Это один из показателей прошлой активности на полигонах ядерного оружия . [17] Изотоп 7 Be (период полураспада 53 дня) также является космогенным, и его содержание в атмосфере связано с солнечными пятнами, как и 10 Be.
8 Be имеет очень короткий период полураспада, около 8 × 10.−17 с, что способствует его значительной космологической роли, поскольку элементы тяжелее бериллия не могли быть произведены в результате ядерного синтеза во время Большого взрыва . [18] Это связано с отсутствием достаточного времени во время фазы нуклеосинтеза Большого взрыва для производства углерода путем слияния ядер 4 He и очень низкими концентрациями доступного бериллия-8. Британский астроном сэр Фред Хойл впервые показал, что энергетические уровни 8 Be и 12 C позволяют производить углерод посредством так называемого процесса тройного альфа в звездах, питаемых гелием, где доступно больше времени нуклеосинтеза. Этот процесс позволяет производить углерод в звездах, но не в результате Большого взрыва. Созданный звездами углерод (основа углеродной жизни ), таким образом, является компонентом элементов газа и пыли, выбрасываемых звездами AGB и сверхновыми (см. Также нуклеосинтез Большого взрыва ), а также созданием всех других элементов с помощью атомных числа больше, чем у углерода. [19]
2s-электроны бериллия могут способствовать образованию химической связи. Следовательно, когда 7 Be распадается в результате захвата L-электрона , он делает это, забирая электроны со своих атомных орбиталей , которые могут участвовать в связывании. Это делает скорость его распада в измеримой степени зависимой от химического окружения – редкое явление при ядерном распаде. [20]
Самый короткоживущий известный изотоп бериллия — 16 Be, который распадается за счет нейтронного излучения с периодом полураспада6,5 × 10 −22 с . [21] Известно , что экзотические изотопы 11 Be и 14 Be обладают ядерным гало . [22] Это явление можно объяснить тем, что ядра 11 Be и 14 Be имеют, соответственно, 1 и 4 нейтрона, вращающихся по орбитам существенно за пределами классической фермиевской модели ядра «капля воды».


На Солнце концентрация бериллия составляет 0,1 части на миллиард (ppb). [23] Бериллий имеет концентрацию от 2 до 6 частей на миллион (ppm) в земной коре. [24] Наибольшая концентрация в почвах – 6 ppm. [25] Следовые количества 9 Be обнаружены в атмосфере Земли. [25] Концентрация бериллия в морской воде составляет 0,2–0,6 частей на триллион . [25] [26] Однако в речной воде бериллий более распространен с концентрацией 0,1 частей на миллиард. [27]
Бериллий встречается более чем в 100 минералах, [28] но большинство из них встречаются редко или редко. Наиболее распространенные бериллийсодержащие минералы включают: бертрандит (Be 4 Si 2 O 7 (OH) 2 ), берилл (Al 2 Be 3 Si 6 O 18 ), хризоберилл (Al 2 BeO 4 ) и фенакит (Be 2 SiO 4 ). Драгоценными формами берилла являются аквамарин , красный берилл и изумруд . [10] [29] [30] Зеленый цвет бериллов ювелирного качества обусловлен различным количеством хрома (около 2% для изумруда). [31]
Две основные руды бериллия, берилл и бертрандит, находятся в Аргентине, Бразилии, Индии, Мадагаскаре, России и США. [31] Общие мировые запасы бериллиевой руды превышают 400 000 тонн. [31]
Извлечение бериллия из его соединений — сложный процесс из-за его высокого сродства к кислороду при повышенных температурах и способности восстанавливать воду при удалении оксидной пленки. В настоящее время США, Китай и Казахстан являются единственными тремя странами, занимающимися добычей бериллия в промышленных масштабах. [32] Казахстан производит бериллий из концентрата, накопленного до распада Советского Союза примерно в 1991 году. К середине 2010-х годов этот ресурс был практически исчерпан. [33]
Производство бериллия в России было остановлено в 1997 году, его планируется возобновить в 2020-х годах. [34] [35]
Бериллий чаще всего добывается из минерала берилла , который либо спекается с использованием экстрагента, либо плавится в растворимую смесь. Процесс спекания включает смешивание берилла с фторосиликатом натрия и содой при температуре 770 ° C (1420 ° F) с образованием фторбериллата натрия , оксида алюминия и диоксида кремния . [8] Гидроксид бериллия осаждают из раствора фторбериллата натрия и гидроксида натрия в воде. Добыча бериллия методом расплава включает измельчение берилла в порошок и нагревание его до 1650 °C (3000 °F). [8] Расплав быстро охлаждают водой, а затем повторно нагревают до 250–300 °C (от 482 до 572 °F) в концентрированной серной кислоте , в результате чего в основном получаются сульфат бериллия и сульфат алюминия . [8] Затем используется водный аммиак для удаления алюминия и серы, в результате чего остается гидроксид бериллия.
Гидроксид бериллия, полученный методом агломерации или расплава, затем преобразуется во фторид бериллия или хлорид бериллия . Для образования фторида водный фторид аммония добавляют к гидроксиду бериллия с образованием осадка тетрафторбериллата аммония, который нагревают до 1000 ° C (1830 ° F) с образованием фторида бериллия. [8] Нагревание фторида до 900 °C (1650 °F) с магнием образует мелкодисперсный бериллий, а дополнительный нагрев до 1300 °C (2370 °F) создает компактный металл. [8] При нагревании гидроксида бериллия образуется оксид, который при соединении с углеродом и хлором становится хлоридом бериллия. Затем для получения металла используют электролиз расплавленного хлорида бериллия. [8]
Атом бериллия имеет электронную конфигурацию [He] 2s 2 . Преобладающая степень окисления бериллия +2; атом бериллия потерял оба своих валентных электрона. Комплексы низших степеней окисления бериллия чрезвычайно редки. Например, сообщалось о соединениях бис (карбена), которые, как предполагается, содержат бериллий в состояниях окисления 0 и +1, хотя эти утверждения оказались противоречивыми. [36] [37] Описан стабильный комплекс со связью Be-Be, формально характеризующий бериллий в степени окисления +1. [38] Химическое поведение бериллия во многом обусловлено его малыми атомными и ионными радиусами. Таким образом, он имеет очень высокие потенциалы ионизации и сильную поляризацию, когда он связан с другими атомами, поэтому все его соединения являются ковалентными . Его химический состав имеет сходство с химическим составом алюминия, что является примером диагонального взаимодействия .
При комнатной температуре на поверхности бериллия образуется оксидный пассивирующий слой толщиной 1–10 нм, который предотвращает дальнейшие реакции с воздухом, за исключением постепенного утолщения оксида примерно до 25 нм. При нагреве выше примерно 500 °C окисление в объеме металла происходит вдоль границ зерен. [39] Когда металл воспламеняется на воздухе при нагревании выше температуры плавления оксида около 2500 ° C, бериллий ярко горит, образуя смесь оксида бериллия и нитрида бериллия . Бериллий легко растворяется в неокисляющих кислотах , таких как HCl и разбавленная H 2 SO 4 , но не в азотной кислоте или воде, поскольку при этом образуется оксид. Это поведение похоже на поведение металлического алюминия. Бериллий растворяется также в растворах щелочей. [8] [40]
Бинарные соединения бериллия(II) полимерны в твердом состоянии. BeF 2 имеет структуру, подобную кремнезему , с тетраэдрами BeF 4 , разделенными по углам . BeCl 2 и BeBr 2 имеют цепочечную структуру с тетраэдрами, разделенными по краям. Оксид бериллия BeO представляет собой белое тугоплавкое твердое вещество, имеющее кристаллическую структуру вюрцита и теплопроводность, такую же высокую, как у некоторых металлов. BeO амфотерен . Известны сульфид бериллия , селенид и теллурид , имеющие структуру цинковой обманки . [41] Нитрид бериллия Be 3 N 2 представляет собой тугоплавкое соединение, которое легко гидролизуется. Известен азид бериллия BeN 6 , а фосфид бериллия Be 3 P 2 имеет структуру, аналогичную Be 3 N 2 . Известен ряд боридов бериллия, таких как Be 5 B, Be 4 B, Be 2 B, BeB 2 , BeB 6 и BeB 12 . Карбид бериллия Be 2 C — тугоплавкое соединение кирпично-красного цвета, которое вступает в реакцию с водой с образованием метана . [41] Силицид бериллия не обнаружен. [40]
Галогениды BeX 2 (X = F, Cl, Br, I) имеют линейное мономерное молекулярное строение в газовой фазе. [40] Комплексы галогенидов образуются с одним или несколькими лигандами, отдающими в общей сложности две пары электронов. Такие соединения подчиняются правилу октетов . Другие 4-координатные комплексы, такие как акваион [Be(H 2 O) 4 ] 2+, также подчиняются правилу октетов.
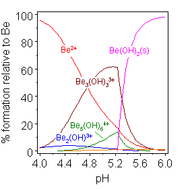
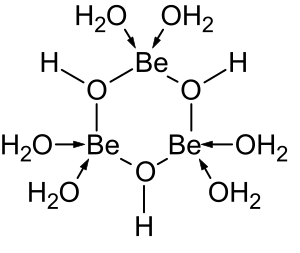
Растворы солей бериллия, таких как сульфат бериллия и нитрат бериллия , являются кислыми из-за гидролиза иона [Be(H 2 O) 4 ] 2+ . Концентрация первого продукта гидролиза [Be(H 2 O) 3 (OH)] + составляет менее 1% от концентрации бериллия. Наиболее стабильным продуктом гидролиза является тримерный ион [Be 3 (OH) 3 (H 2 O) 6 ] 3+ . Гидроксид бериллия Be(OH) 2 нерастворим в воде при pH 5 и более. Следовательно, соединения бериллия обычно нерастворимы при биологическом pH. Из-за этого вдыхание человеком пыли металлического бериллия приводит к развитию смертельного состояния бериллиоза . Be(OH) 2 растворяется в сильнощелочных растворах . [42]
Бериллий(II) образует мало комплексов с монодентатными лигандами, поскольку молекулы воды в аква-ионе [Be(H 2 O) 4 ] 2+ очень прочно связаны с ионом бериллия. Заметным исключением является ряд водорастворимых комплексов с фторид -ионом: [43]
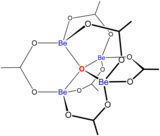
Бериллий(II) образует множество комплексов с бидентатными лигандами, содержащими атомы донора кислорода. [42] Вид [Be 3 O(H 2 PO 4 ) 6 ] 2- отличается наличием 3-координационного оксидного иона в центре. Основной ацетат бериллия Be 4 O(OAc) 6 имеет оксидный ион, окруженный тетраэдром атомов бериллия.
С органическими лигандами, такими как малонат- ион, кислота депротонирует при образовании комплекса. Донорными атомами являются два атома кислорода.
Алифатические гидроксикарбоновые кислоты, такие как гликолевая кислота, образуют в растворе довольно слабые монодентатные комплексы, в которых гидроксильная группа остается неповрежденной. В твердом состоянии гидроксильная группа может депротонироваться: давно выделен гексамер . [44] [45] Ароматические гидроксилиганды (т.е. фенолы ) образуют относительно прочные комплексы. Например, для комплексов с тироном были зарегистрированы значения log K 1 и log K 2 , равные 12,2 и 9,3 . [44] [46]
Бериллий обычно имеет довольно плохое сродство к амминным лигандам. [44] [47] Лиганды, такие как ЭДТА, ведут себя как дикарбоновые кислоты. [ нужна ссылка ] Есть много ранних сообщений о комплексах с аминокислотами, но, к сожалению, они ненадежны, поскольку сопутствующие реакции гидролиза не были понятны на момент публикации. Значения log β ок. Сообщается о 6-7 случаях. Степень образования невелика из-за конкуренции с реакциями гидролиза. [44] [47]
Бериллийорганическая химия ограничена академическими исследованиями из-за стоимости и токсичности бериллия, производных бериллия и реагентов, необходимых для введения бериллия, таких как хлорид бериллия . Известно, что металлоорганические соединения бериллия обладают высокой реакционной способностью [48]. Примерами известных бериллийорганических соединений являются динеопентилбериллий , [49] бериллоцен (Cp 2 Be), [50] [51] [52] [53] диаллилбериллий (по реакции обмена диэтилбериллия с триаллилбором), [54] бис(1,3-триметилсилилаллил)бериллий, [55] Be(mes) 2 , [48] и (комплекс бериллия(I)) дибериллоцен . [38] Лигандами также могут быть арилы [56] и алкинилы. [57]
Минерал берилл , содержащий бериллий, использовался, по крайней мере, со времен династии Птолемеев в Египте. [58] В первом веке нашей эры римский натуралист Плиний Старший упомянул в своей энциклопедии « Естественная история» , что берилл и изумруд («смарагдус») похожи. [59] Папирус Graecus Holmiensis , написанный в третьем или четвертом веке нашей эры, содержит заметки о том, как приготовить искусственный изумруд и берилл. [59]

Ранние анализы изумрудов и бериллов, проведенные Мартином Генрихом Клапротом , Торберном Улофом Бергманом , Францем Карлом Ахардом и Иоганном Якобом Биндхаймом, всегда давали схожие элементы, что приводило к ошибочному выводу, что оба вещества представляют собой алюмосиликаты . [60] Минералог Рене Жюст Аюи обнаружил, что оба кристалла геометрически идентичны, и попросил химика Луи-Николя Воклена провести химический анализ. [58]
В статье 1798 года, прочитанной в Институте Франции , Воклен сообщил, что он нашел новую «землю», растворив гидроксид алюминия из изумруда и берилла в дополнительной щелочи . [61] Редакторы журнала Annales de Chimie et de Physique назвали новую землю «глюцином» из-за сладкого вкуса некоторых ее соединений. [62] Клапрот предпочел название «бериллина» из-за того, что иттрий также образует сладкие соли. [63] [64] Название «бериллий» впервые было использовано Вёлером в 1828 году. [65]

Фридрих Вёлер [66] и Антуан Бюсси [67] независимо выделили бериллий в 1828 году химической реакцией металлического калия с хлоридом бериллия следующим образом:
Используя спиртовку, Вёлер нагрел чередующиеся слои хлорида бериллия и калия в платиновом тигле с проволочной заглушкой. Вышеуказанная реакция произошла немедленно и привела к тому, что тигель нагрелся добела. Охладив и промыв полученный серо-черный порошок, он увидел, что он состоит из мелких частиц с темным металлическим блеском. [68] Высокореактивный калий был получен электролизом его соединений, процессом, открытым 21 год назад. Химический метод с использованием калия давал лишь мелкие зерна бериллия, из которых невозможно было отлить или отковать слиток металла.
В результате прямого электролиза расплавленной смеси фторида бериллия и фторида натрия , проведенного Полем Лебо в 1898 году, были получены первые чистые (от 99,5 до 99,8%) образцы бериллия. [68] Однако промышленное производство началось только после Первой мировой войны. Первоначальное промышленное участие включало дочерние компании и ученых, связанных с Union Carbide and Carbon Corporation в Кливленде, штат Огайо, и Siemens & Halske AG в Берлине. В США процессом руководил Хью С. Купер, директор компании Kemet Laboratories. В Германии первый коммерчески успешный процесс производства бериллия был разработан в 1921 году Альфредом Штоком и Гансом Гольдшмидтом . [69]
Образец бериллия подвергся бомбардировке альфа-лучами распада радия в ходе эксперимента Джеймса Чедвика 1932 года , который открыл существование нейтрона . [31] Этот же метод используется в одном классе лабораторных источников нейтронов на основе радиоизотопов , которые производят 30 нейтронов на каждый миллион α-частиц. [24]
Производство бериллия резко возросло во время Второй мировой войны из-за растущего спроса на твердые сплавы бериллия и меди и люминофоры для люминесцентных ламп . В большинстве ранних люминесцентных ламп использовался ортосиликат цинка с различным содержанием бериллия, излучающий зеленоватый свет. Небольшие добавки вольфрамата магния улучшили синюю часть спектра и позволили получить приемлемый белый свет. Люминофоры на основе галофосфатов заменили люминофоры на основе бериллия после того, как бериллий оказался токсичным. [70]
Электролиз смеси фторида бериллия и фторида натрия использовался для выделения бериллия в 19 веке. Высокая температура плавления металла делает этот процесс более энергозатратным, чем соответствующие процессы, используемые для щелочных металлов . В начале 20 века производство бериллия путем термического разложения йодида бериллия было исследовано после успеха аналогичного процесса производства циркония , но этот процесс оказался неэкономичным для массового производства. [71]
Чистый металлический бериллий стал доступен только в 1957 году, хотя гораздо раньше он использовался в качестве легирующего металла для упрочнения меди. [31] Бериллий можно производить путем восстановления соединений бериллия, таких как хлорид бериллия , металлическим калием или натрием. В настоящее время большая часть бериллия производится восстановлением фторида бериллия магнием . [72] Цена на слитки бериллия , отлитые в вакууме, на американском рынке в 2001 году составляла около 338 долларов за фунт (745 долларов за килограмм). [73]
В период с 1998 по 2008 год мировое производство бериллия снизилось с 343 до примерно 200 тонн . Затем к 2018 году он увеличился до 230 тонн, из которых 170 тонн поступило из США. [74] [75]
Назван в честь берилла , полудрагоценного минерала, из которого он был впервые выделен. [76] [77] [78]


Из-за его низкого атомного номера и очень низкого поглощения рентгеновских лучей старейшим и до сих пор одним из наиболее важных применений бериллия является изготовление радиационных окон для рентгеновских трубок . [31] К чистоте и чистоте бериллия предъявляются экстремальные требования, чтобы избежать появления артефактов на рентгеновских изображениях. Тонкая бериллиевая фольга используется в качестве радиационных окон для детекторов рентгеновского излучения, а чрезвычайно низкое поглощение сводит к минимуму эффекты нагрева, вызванные рентгеновскими лучами высокой интенсивности и низкой энергии, типичными для синхротронного излучения. Вакуумонепроницаемые окна и пучковые трубки для радиационных экспериментов на синхротронах изготавливаются исключительно из бериллия. В научных установках для различных исследований рентгеновской эмиссии (например, энергодисперсионной рентгеновской спектроскопии ) держатель образца обычно изготавливается из бериллия, поскольку испускаемые им рентгеновские лучи имеют гораздо меньшую энергию (≈100 эВ), чем рентгеновские лучи от большинства изученные материалы. [10]
Низкий атомный номер также делает бериллий относительно прозрачным для энергичных частиц . Поэтому он используется для построения лучевой трубы вокруг области столкновения в установках физики элементарных частиц , таких как все четыре эксперимента с основными детекторами на Большом адронном коллайдере ( ALICE , ATLAS , CMS , LHCb ), [79] на Тэватроне и в SLAC . Низкая плотность бериллия позволяет продуктам столкновения достигать окружающих детекторов без значительного взаимодействия, его жесткость позволяет создавать мощный вакуум внутри трубы для минимизации взаимодействия с газами, его термическая стабильность позволяет ему правильно функционировать при температуре всего в несколько градусов. выше абсолютного нуля , и его диамагнитная природа не позволяет ему мешать сложным мультипольным магнитным системам, используемым для управления и фокусировки пучков частиц . [80]
Благодаря своей жесткости, легкому весу и стабильности размеров в широком диапазоне температур металлический бериллий используется для изготовления легких конструкционных компонентов в оборонной и аэрокосмической промышленности, в высокоскоростных самолетах , управляемых ракетах , космических кораблях и спутниках , включая космический телескоп Джеймса Уэбба. . В некоторых ракетах на жидком топливе использовались сопла из чистого бериллия. [81] [82] Порошок бериллия сам по себе изучался в качестве ракетного топлива , но его использование так и не было реализовано. [31] Небольшое количество велосипедных рам экстремального класса было изготовлено из бериллия. [83] С 1998 по 2000 год команда McLaren Формулы-1 использовала двигатели Mercedes-Benz с поршнями из бериллий-алюминиевого сплава . [84] Использование бериллиевых компонентов двигателя было запрещено после протеста Scuderia Ferrari . [85]
При смешивании около 2,0% бериллия с медью образуется сплав , называемый бериллиевой медью , который в шесть раз прочнее меди в отдельности. [86] Сплавы бериллия используются во многих областях применения благодаря сочетанию эластичности, высокой электропроводности и теплопроводности , высокой прочности и твердости , немагнитных свойств, а также хорошей коррозионной и усталостной стойкости . [31] [8] Эти области применения включают в себя неискрящие инструменты, которые используются рядом с горючими газами (бериллий-никель), в пружинах и мембранах (бериллий-никель и бериллий-железо), используемых в хирургических инструментах и высокотемпературных устройствах. [31] [8] Всего 50 частей на миллион бериллия, легированного жидким магнием , приводит к значительному увеличению стойкости к окислению и снижению воспламеняемости. [8]

Высокая упругая жесткость бериллия привела к его широкому использованию в точном приборостроении, например, в инерциальных системах наведения и в опорных механизмах оптических систем. [10] Сплавы бериллия и меди также применялись в качестве отвердителя в « пистолетах Джейсона », которые использовались для снятия краски с корпусов кораблей. [87]
Бериллий также использовался для изготовления кантилеверов в высокопроизводительных иглах картриджей для фонографов, где его чрезвычайная жесткость и низкая плотность позволили уменьшить отслеживающий вес до 1 грамма, но при этом отслеживать высокочастотные отрывки с минимальными искажениями. [88]
Ранее бериллий широко применялся в тормозах военных самолетов из-за его твердости, высокой температуры плавления и исключительной способности рассеивать тепло . Экологические соображения привели к замене другими материалами. [10]
Чтобы снизить затраты, бериллий можно легировать значительным количеством алюминия , в результате чего получается сплав AlBeMet (торговое название). Эта смесь дешевле чистого бериллия, но при этом сохраняет многие полезные свойства.
Особый интерес представляют бериллиевые зеркала . Зеркала большой площади, часто с сотовой опорной конструкцией , используются, например, в метеорологических спутниках , где малый вес и долговременная стабильность размеров имеют решающее значение. Бериллиевые зеркала меньшего размера используются в оптических системах наведения и системах управления огнем , например, в основных боевых танках немецкого производства Leopard 1 и Leopard 2 . В этих системах требуется очень быстрое перемещение зеркала, что опять-таки требует малой массы и высокой жесткости. Обычно бериллиевое зеркало покрыто твердым химическим никелированием , которое легче полировать до более высокого оптического качества, чем бериллий. Однако в некоторых случаях бериллиевую заготовку полируют без какого-либо покрытия. Это особенно применимо к криогенным операциям, где несоответствие теплового расширения может привести к короблению покрытия. [10]
Космический телескоп Джеймса Уэбба имеет 18 шестиугольных бериллиевых секций зеркал, каждое из которых покрыто тонким слоем золота. [89] Поскольку JWST будет работать при температуре 33 К, зеркало изготовлено из позолоченного бериллия, способного выдерживать экстремальные холода лучше, чем стекло. Бериллий сжимается и деформируется меньше, чем стекло, и остается более однородным при таких температурах. [90] По той же причине оптика космического телескопа «Спитцер» полностью изготовлена из металлического бериллия. [91]

Бериллий немагнитен. Поэтому инструменты, изготовленные из материалов на основе бериллия, используются военно-морскими или военными группами по обезвреживанию боеприпасов для работы на морских минах или вблизи них , поскольку эти мины обычно имеют магнитные взрыватели . [93] Они также встречаются в ремонтных и строительных материалах рядом с аппаратами магнитно-резонансной томографии (МРТ) из-за генерируемых сильных магнитных полей. [94] В области радиосвязи и мощных (обычно военных) радаров ручные инструменты из бериллия используются для настройки сильномагнитных клистронов , магнетронов , ламп бегущей волны и т. д., которые используются для генерации высоких уровней микроволновой энергии . в передатчиках . [ нужна цитата ]
Тонкие пластины или фольга из бериллия иногда используются в конструкциях ядерного оружия в качестве самого внешнего слоя плутониевых ям на начальных стадиях термоядерных бомб , расположенных вокруг делящегося материала. Эти слои бериллия являются хорошими «толкателями» для взрыва плутония -239 и хорошими отражателями нейтронов , как и в ядерных реакторах с бериллиевым замедлителем . [95]
Бериллий также широко используется в некоторых источниках нейтронов в лабораторных устройствах, в которых требуется относительно мало нейтронов (вместо использования ядерного реактора или генератора нейтронов с питанием от ускорителя частиц ). Для этой цели мишень из бериллия-9 бомбардируется энергичными альфа-частицами радиоизотопа, такого как полоний -210, радий -226, плутоний -238 или америций -241. В ходе происходящей ядерной реакции ядро бериллия преобразуется в углерод-12 и испускается один свободный нейтрон, движущийся примерно в том же направлении, в котором двигалась альфа-частица. Такие источники нейтронов из бериллия, управляемые альфа-распадом , называемые «ежовыми» нейтронными инициаторами, использовались в некоторых ранних атомных бомбах . [95] Источники нейтронов, в которых бериллий бомбардируется гамма-лучами радиоизотопа гамма-распада , также используются для производства лабораторных нейтронов. [96]
Бериллий также используется при производстве топлива для реакторов CANDU . Топливные элементы имеют небольшие придатки, которые припаиваются к оболочке твэла методом индукционной пайки с использованием бериллия в качестве припоя. Подушки подшипников припаяны для предотвращения контакта топливного пучка с содержащей его напорной трубкой, а также межэлементные проставки для предотвращения контакта элементов с элементами.
Бериллий также используется в Объединенной европейской научно-исследовательской лаборатории ядерного синтеза « Торус » и в более совершенном ИТЭР для подготовки компонентов, контактирующих с плазмой. [97] Бериллий также был предложен в качестве материала оболочки для ядерных топливных стержней из-за его хорошего сочетания механических, химических и ядерных свойств. [10] Фторид бериллия является одной из составляющих солей эвтектической смеси солей FLiBe , которая используется в качестве растворителя, замедлителя и теплоносителя во многих гипотетических конструкциях реакторов с расплавленными солями , включая реактор с жидким фторидом тория (LFTR). [98]
Малый вес и высокая жесткость бериллия делают его полезным в качестве материала для высокочастотных динамиков . Поскольку бериллий дорог (во много раз дороже титана ), его трудно поддавать формованию из-за его хрупкости и он токсичен при неправильном обращении, бериллиевые твитеры предназначены только для домашнего использования, [99] [100] [101] профессионального аудио и громкоговорителей. Приложения. [102] [103] Некоторые высококачественные продукты были обманным путем заявлены как изготовленные из этого материала. [104]
В некоторых высококачественных картриджах для фонографов использовались бериллиевые кантилеверы для улучшения отслеживания за счет уменьшения массы. [105]
Бериллий является легирующей примесью p-типа в полупроводниках соединений III-V . Он широко используется в таких материалах, как GaAs , AlGaAs , InGaAs и InAlAs , выращенных методом молекулярно-лучевой эпитаксии (МЛЭ). [106] Прокатанный поперек лист бериллия является превосходной структурной опорой для печатных плат в технологии поверхностного монтажа . В критически важных электронных приложениях бериллий является одновременно структурной опорой и теплоотводом . Для применения также требуется коэффициент теплового расширения , хорошо соответствующий подложкам из оксида алюминия и полиимидного стекла . Композитный оксид бериллия-бериллия « E-Materials » был специально разработан для этих электронных приложений и имеет дополнительное преимущество, заключающееся в том, что коэффициент теплового расширения может быть адаптирован для соответствия различным материалам подложки. [10]
Оксид бериллия полезен во многих случаях, когда требуется сочетание свойств электрического изолятора и превосходного проводника тепла, обладающего высокой прочностью и твердостью, а также очень высокой температурой плавления. Оксид бериллия часто используется в качестве изоляционной опорной пластины в мощных транзисторах радиочастотных передатчиков для телекоммуникаций. Оксид бериллия также изучается на предмет использования для увеличения теплопроводности таблеток ядерного топлива из диоксида урана . [107] Соединения бериллия использовались в лампах люминесцентного освещения , но это использование было прекращено из-за заболевания бериллиоза , развившегося у рабочих, производивших лампы. [108]
Бериллий входит в состав ряда стоматологических сплавов . [109] [110]
В среднем человеческом организме содержится около 35 микрограммов бериллия, и это количество не считается вредным. [112] Бериллий химически подобен магнию и поэтому может вытеснять его из ферментов , что приводит к их неисправности. [112] Поскольку Be 2+ представляет собой высокозаряженный и небольшой ион, он может легко проникать во многие ткани и клетки, где специфически поражает ядра клеток, ингибируя многие ферменты, в том числе те, которые используются для синтеза ДНК. Его токсичность усугубляется тем фактом, что у организма нет средств для контроля уровня бериллия, и, попав в организм, бериллий не может быть удален. [113]
Хроническая бериллиевая болезнь (ХББ), или бериллиоз , — легочное и системное гранулематозное заболевание, вызываемое вдыханием пыли или паров, загрязненных бериллием; К этому недугу могут привести либо большие количества в течение короткого времени, либо небольшие количества в течение длительного времени. Для развития симптомов заболевания может потребоваться до пяти лет; около трети пациентов с ним умирают, а выжившие остаются инвалидами. [112] Международное агентство по изучению рака (IARC) относит бериллий и его соединения к канцерогенам 1-й категории . [114]
В США Управление по охране труда (OSHA) установило допустимый предел воздействия (PEL) для бериллия и его соединений на уровне 0,2 мкг/м 3 как средневзвешенное по времени значение (TWA) за 8 часов и 2,0 мкг/м. 3 как предел кратковременного воздействия в течение периода выборки 15 минут. Национальный институт охраны труда (NIOSH) установил верхний предел рекомендуемого предела воздействия (REL) на уровне 0,5 мкг/м 3 . Значение IDLH (непосредственно опасное для жизни и здоровья) составляет 4 мг/м 3 . [115] Токсичность бериллия находится на одном уровне с другими токсичными металлоидами/металлами, такими как мышьяк и ртуть . [116] [117]
Воздействие бериллия на рабочем месте может привести к сенсибилизирующей иммунной реакции и со временем может привести к развитию хронической бериллиевой болезни . [118] Национальный институт охраны труда (NIOSH) в США исследует эти эффекты в сотрудничестве с крупным производителем бериллиевой продукции. NIOSH также проводит генетические исследования сенсибилизации и КБД, независимо от этого сотрудничества. [118]
Острая бериллиевая болезнь в форме химического пневмонита впервые была зарегистрирована в Европе в 1933 году и в США в 1943 году. Исследование показало, что около 5% рабочих заводов, производящих люминесцентные лампы в 1949 году в США, страдали бериллиевыми заболеваниями легких. . [119] Хронический бериллиоз во многих отношениях напоминает саркоидоз , и дифференциальный диагноз часто затруднен. Он убил некоторых первых исследователей ядерного оружия, таких как Герберт Л. Андерсон . [120]
Бериллий можно найти в угольных шлаках. Когда шлак используется в качестве абразивного агента для удаления краски и ржавчины с твердых поверхностей, бериллий может попасть в воздух и стать источником воздействия. [121]
Хотя использование соединений бериллия в люминесцентных осветительных лампах было прекращено в 1949 году, потенциал воздействия бериллия существует в атомной и аэрокосмической промышленности, а также при очистке металлического бериллия и плавке бериллийсодержащих сплавов, производстве электронных устройств и обращение с другими бериллийсодержащими материалами. [122]
Ранние исследователи предприняли весьма опасную практику определения бериллия и его различных соединений по сладкому вкусу. Идентификация теперь проводится с использованием безопасных современных методов диагностики. [8] Успешный тест на содержание бериллия в воздухе и на поверхностях был разработан и опубликован в качестве международного добровольного консенсусного стандарта ASTM D7202. В процедуре используется разбавленный бифторид аммония для обнаружения растворения и флуоресценции бериллия, связанного с сульфонированным гидроксибензохинолином, что обеспечивает до 100 раз более чувствительное обнаружение, чем рекомендуемый предел концентрации бериллия на рабочем месте. Флуоресценция увеличивается с увеличением концентрации бериллия. Новая процедура была успешно протестирована на различных поверхностях и эффективна для растворения и обнаружения тугоплавкого оксида бериллия и кремниевого бериллия в минимальных концентрациях (ASTM D7458). [123] [124] Руководство NIOSH по аналитическим методам содержит методы измерения профессионального воздействия бериллия. [125]
{{cite journal}}: CS1 maint: несколько имен: список редакторов ( ссылка )