Закись азота (оксид азота или монооксид динитрогена), широко известный как веселящий газ , азот , нитро или NO , [4] представляет собой химическое соединение , оксид азота с формулой N
2О. _ При комнатной температуре это бесцветный негорючий газ со слегка сладковатым запахом и вкусом. [5] При повышенных температурах закись азота является мощным окислителем, подобным молекулярному кислороду.
Закись азота имеет широкое медицинское применение , особенно в хирургии и стоматологии , из-за ее анестезирующего и обезболивающего действия. [6] Его разговорное название «веселящий газ», придуманное Хамфри Дэви , связано с эйфорическим эффектом при его вдыхании, свойством, которое привело к его рекреационному использованию в качестве диссоциативного анестетика. [6] Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [7] Он также используется в качестве окислителя в ракетном топливе и в автоспорте для увеличения выходной мощности двигателей .
Концентрация закиси азота в атмосфере достигла 333 частей на миллиард (частей на миллиард) в 2020 году, увеличиваясь примерно на 1 миллиардную долю в год. [8] [9] Это основной поглотитель стратосферного озона , воздействие которого сравнимо с воздействием ХФУ . [10] Глобальный учет N
2Источники и поглотители O за десятилетие, закончившееся 2016 годом, указывают на то, что около 40% из средних выбросов азота в размере 17 TgN/год ( тераграммов или миллионов метрических тонн азота в год) возникли в результате человеческой деятельности, и показывает, что рост выбросов в основном происходил за счет расширения сельское хозяйство . [11] [12] Будучи третьим по значимости парниковым газом , закись азота также вносит существенный вклад в глобальное потепление . [13] [14]
Закись азота используется в качестве топлива и имеет множество применений: от ракетной техники до приготовления взбитых сливок. Его используют в качестве рекреационного наркотика из-за его способности вызывать кратковременный «кайф». Большинство рекреационных потребителей не подозревают о его нейротоксических эффектах при злоупотреблении. При хроническом использовании закись азота может вызвать неврологические нарушения за счет инактивации витамина B12 .
Закись азота может использоваться в качестве окислителя в ракетном двигателе. Он имеет преимущества перед другими окислителями в том, что он гораздо менее токсичен, а благодаря его стабильности при комнатной температуре его легче хранить и относительно безопасно перевозить в полете. В качестве вторичного преимущества он может легко разлагаться с образованием воздуха для дыхания. Его высокая плотность и низкое давление хранения (при сохранении при низких температурах) позволяют ему быть весьма конкурентоспособным по сравнению с системами хранения газа высокого давления. [15]
В патенте 1914 года пионер американского ракетостроения Роберт Годдард предложил закись азота и бензин в качестве топлива для ракеты на жидком топливе. [16] Закись азота была предпочтительным окислителем в нескольких конструкциях гибридных ракет (с использованием твердого топлива с жидким или газообразным окислителем). Комбинация закиси азота с полибутадиеновым топливом с концевыми гидроксильными группами использовалась SpaceShipOne и другими. Он также широко используется в любительской и ракетной технике большой мощности с использованием различных пластмасс в качестве топлива.
Закись азота также может использоваться в монотопливной ракете . В присутствии нагретого катализатора N
2O будет экзотермически разлагаться на азот и кислород при температуре примерно 1070 ° F (577 ° C). [17] Из-за большого тепловыделения каталитическое действие быстро становится вторичным, поскольку термическое саморазложение становится доминирующим. В вакуумном двигателе это может обеспечить удельный импульс монотоплива ( I sp ) до 180 с. Хотя I sp заметно меньше, чем у гидразиновых двигателей (монотопливных или двухтопливных с тетроксидом азота ), пониженная токсичность делает закись азота достойным изучения вариантом.
Говорят, что закись азота сгорает при температуре примерно 600 ° C (1112 ° F) и давлении 309 фунтов на квадратный дюйм (21 атмосфера). [18] Например, при давлении 600 фунтов на квадратный дюйм необходимая энергия воспламенения составляет всего 6 джоулей, тогда как N
2O при 130 фунтах на квадратный дюйм энергии зажигания в 2500 джоулей недостаточно. [19] [20]
В автогонках закись азота (часто называемая « закись азота ») позволяет двигателю сжигать больше топлива, обеспечивая больше кислорода во время сгорания. Увеличение количества кислорода позволяет увеличить впрыск топлива, что позволяет двигателю развивать большую мощность . Газ не воспламеняется при низком давлении/температуре, но он доставляет больше кислорода, чем атмосферный воздух, разлагаясь при повышенных температурах, около 570 градусов F (~ 300 C). Поэтому его часто смешивают с другим топливом, которое легче дефлагрировать. Закись азота — сильный окислитель, примерно эквивалентный перекиси водорода, и намного более сильный, чем газообразный кислород.
Закись азота хранится в виде сжатой жидкости; Испарение и расширение жидкого закиси азота во впускном коллекторе вызывает значительное падение температуры впускного заряда, что приводит к более плотному заряду, что дополнительно позволяет большему количеству воздушно-топливной смеси попасть в цилиндр. Иногда закись азота впрыскивается во впускной коллектор (или перед ним), тогда как другие системы впрыскивают непосредственно перед цилиндром (прямой впрыск) для увеличения мощности.
Этот метод использовался во время Второй мировой войны самолетами Люфтваффе с системой GM-1 для повышения выходной мощности авиационных двигателей . Первоначально предназначенный для обеспечения стандартных самолетов Люфтваффе превосходными высотными характеристиками, технологические соображения ограничивали его использование на чрезвычайно больших высотах. Соответственно, он использовался только специализированными самолетами, такими как высотные самолеты-разведчики , скоростные бомбардировщики и высотные самолеты-перехватчики . Иногда его можно было встретить на самолетах Люфтваффе, также оснащенных другой системой наддува двигателя, MW 50 , формой впрыска воды для авиационных двигателей, в которых для наддува использовался метанол .
Одна из основных проблем использования закиси азота в поршневом двигателе заключается в том, что он может производить достаточно мощности, чтобы повредить или вывести из строя двигатель. Возможно очень большое увеличение мощности, и если механическая конструкция двигателя не усилена должным образом, двигатель может быть серьезно поврежден или разрушен во время работы такого типа. При добавлении закиси азота в бензиновые двигатели важно поддерживать надлежащие рабочие температуры и уровни топлива, чтобы предотвратить « раннее зажигание » [21] или «детонацию» (иногда называемую «детонацией»). Большинство проблем, связанных с закисью азота, возникают не из-за механических повреждений из-за увеличения мощности. Поскольку закись азота обеспечивает гораздо более плотный заряд в цилиндре, это резко увеличивает давление в цилиндре. Повышенное давление и температура могут вызвать такие проблемы, как расплавление поршней или клапанов. Это также может привести к растрескиванию или деформации поршня или головки блока цилиндров и вызвать преждевременное зажигание из-за неравномерного нагрева.
Жидкая закись азота автомобильного качества немного отличается от закиси азота медицинского назначения. Небольшое количество диоксида серы ( SO
2) добавляется для предотвращения злоупотребления психоактивными веществами. [22]

Газ одобрен для использования в качестве пищевой добавки ( номер E : E942), в частности, в качестве пропеллента для аэрозольных распылителей . Его наиболее распространенное применение в этом контексте - аэрозольные баллончики со взбитыми сливками и кулинарные спреи .
Газ чрезвычайно растворим в жирных соединениях. В аэрозольных взбитых сливках он растворяется в жирных сливках до тех пор, пока они не покинут баллон, затем становятся газообразными и образуют пену. При таком использовании получаются взбитые сливки, объем которых в четыре раза превышает объем жидкости, тогда как при взбивании сливок воздухом получается только вдвое больший объем. Если бы в качестве топлива использовался воздух, кислород ускорил бы прогоркание молочного жира, но закись азота препятствует такому разложению. Углекислый газ нельзя использовать для взбитых сливок, потому что он имеет кислую реакцию в воде, что может свернуть сливки и придать им ощущение «игристости», напоминающее сельтерскую воду.
Взбитые сливки, приготовленные с использованием закиси азота, нестабильны и вернутся в более жидкое состояние в течение получаса-одного часа. [23] Таким образом, этот метод не подходит для украшения блюд, которые не будут поданы немедленно.
В декабре 2016 года некоторые производители сообщили о нехватке аэрозольных взбитых сливок в США из-за взрыва на заводе по производству закиси азота Air Liquide во Флориде в конце августа. Поскольку крупный объект был отключен от сети, сбой вызвал дефицит, в результате чего компания перенаправила поставки закиси азота медицинским клиентам, а не на производство продуктов питания. Дефицит возник в период Рождества и праздников , когда потребление консервированных взбитых сливок обычно достигает максимума. [24]
Аналогичным образом, кулинарный спрей, который изготавливается из различных типов масел в сочетании с лецитином ( эмульгатором ), может использовать в качестве пропеллента закись азота . Другие пропелленты, используемые в кулинарных спреях, включают пищевой спирт и пропан .

Закись азота использовалась в стоматологии и хирургии в качестве анестетика и анальгетика с 1844 года. [25] Раньше газ вводился через простые ингаляторы, состоящие из дыхательного мешка из резиновой ткани. [26] Сегодня газ вводится в больницах с помощью автоматизированного аппарата для относительной аналгезии с испарителем анестетика и аппаратом искусственной вентиляции легких , который подает точно дозированный и активируемый дыханием поток закиси азота, смешанной с кислородом в соотношении 2:1. соотношение.
Закись азота является слабым общим анестетиком и поэтому обычно не используется отдельно при общей анестезии, а используется в качестве газа-носителя (смешанного с кислородом) для более мощных общих анестетиков, таких как севофлюран или десфлуран . Он имеет минимальную альвеолярную концентрацию 105% и коэффициент распределения кровь/газ 0,46. Использование закиси азота при анестезии может увеличить риск послеоперационной тошноты и рвоты. [27] [28] [29]
Стоматологи используют более простой аппарат, который обеспечивает только N
2О / О
2смесь, которую пациент может вдыхать, находясь в сознании, но при этом должен иметь специально разработанный относительный расходомер для анальгетиков с минимумом 30 % кислорода в любое время и максимальным верхним пределом 70 % закиси азота. Пациент остается в сознании на протяжении всей процедуры и сохраняет достаточные умственные способности, чтобы отвечать на вопросы и инструкции стоматолога. [30]
Вдыхание закиси азота часто используется для облегчения боли, связанной с родами , травмами , хирургическими вмешательствами в полости рта и острым коронарным синдромом (включая сердечные приступы). Было доказано, что его использование во время родов является безопасным и эффективным вспомогательным средством для рожающих женщин. [31] Его использование при остром коронарном синдроме имеет неизвестную пользу. [32]
В Великобритании и Канаде Энтонокс и Нитронокс обычно используются бригадами скорой помощи (включая незарегистрированных врачей) в качестве быстрого и высокоэффективного обезболивающего газа.
Пятьдесят процентов закиси азота можно рассматривать для использования обученными непрофессиональными специалистами по оказанию первой помощи на догоспитальном этапе, учитывая относительную простоту и безопасность введения 50% закиси азота в качестве анальгетика. Быстрая обратимость его эффекта также не позволит поставить диагноз. [33]



Рекреационное вдыхание закиси азота с целью вызвать эйфорию и/или легкие галлюцинации началось как явление среди британского высшего класса в 1799 году, известное как «вечеринки веселящего газа». [34]
Начиная с 19 века, повсеместная доступность газа для медицинских и кулинарных целей позволила значительно расширить его использование в рекреационных целях по всему миру. По оценкам, в Великобритании по состоянию на 2014 год закись азота использовали почти полмиллиона молодых людей в ночных клубах, на фестивалях и вечеринках. [35]
Широкое распространение наркотика в рекреационных целях по всей Великобритании было показано в документальном фильме Vice 2017 года «Внутри черного рынка веселящего газа» , в котором журналист Мэтт Ши встретился с торговцами наркотиком, укравшими его из больниц. [36]
Важным вопросом, упоминаемым в лондонской прессе, является эффект засорения канистр с закисью азота, который очень заметен и вызывает серьезные жалобы со стороны населения. [37]
До 8 ноября 2023 года закись азота подпадала под действие Закона о психоактивных веществах 2016 года в Великобритании. Уже было незаконно производить, поставлять, импортировать или экспортировать закись азота для рекреационного использования. Однако 8 ноября 2023 года правительство Великобритании обновило закон, включив в него хранение закиси азота, классифицировав его как наркотик класса C в соответствии с Законом о злоупотреблении наркотиками 1971 года. [38]
Хотя случайное употребление закиси азота большинством любителей для отдыха воспринимается как путь к «безопасному кайфу», многие не осознают, что чрезмерное потребление может вызвать неврологический вред, который, если его не лечить, может привести к необратимому неврологическому повреждению. [39] В Австралии использование для отдыха стало проблемой общественного здравоохранения после роста числа зарегистрированных случаев нейротоксичности и увеличения числа госпитализаций в отделения неотложной помощи , а в (штате) Южной Австралии в 2020 году было принято законодательство, ограничивающее продажу канистр. [40]
Закись азота представляет собой серьезную профессиональную опасность для хирургов, стоматологов и медсестер. Поскольку закись азота минимально метаболизируется у людей (со скоростью 0,004%), она сохраняет свою эффективность при выдыхании пациентом помещения и может представлять опасность отравляющего воздействия и длительного воздействия для персонала клиники, если помещение плохо проветривается. При введении закиси азота необходимо использовать систему непрерывной приточной вентиляции или N
2 Система удаления O используется для предотвращения накопления отходящих газов. [ нужна цитата ]
Национальный институт безопасности и гигиены труда рекомендует контролировать воздействие на работников закиси азота во время введения анестезирующего газа медицинскими, стоматологическими и ветеринарными операторами. [41] Он установил рекомендуемый предел воздействия (REL) 25 частей на миллион (46 мг/м 3 ) для вырвавшегося анестетика. [42]
Воздействие закиси азота вызывает кратковременное снижение умственной работоспособности, аудиовизуальных способностей и ловкости рук. [43] Эти эффекты в сочетании с вызванной пространственной и временной дезориентацией могут привести к физическому вреду пользователю из-за опасностей окружающей среды. [44]
Закись азота нейротоксична , и есть свидетельства того, что регулярное употребление значительных количеств в среднесрочной или долгосрочной перспективе может вызвать неврологический вред с потенциалом необратимого повреждения, если его не лечить. [40] [45]
Как и другие антагонисты рецепторов NMDA , было высказано предположение, что N
2O вызывает нейротоксичность в виде поражений Олни у грызунов при длительном (несколько часов) воздействии. [46] [47] [48] [49]
Утверждалось, что, поскольку N
2O быстро выводится из организма в нормальных условиях, он менее нейротоксичен, чем другие антагонисты NMDAR. [50] Действительно, у грызунов кратковременное воздействие приводит лишь к легкому повреждению, которое быстро обратимо, а гибель нейронов происходит только после постоянного и длительного воздействия. [46] Закись азота также может вызывать нейротоксичность после длительного воздействия из-за гипоксии . Это особенно верно в отношении немедицинских составов, таких как наполнители для взбитых сливок (также известные как «уиппеты» или «нанг») [51] , которые никогда не содержат кислород, поскольку кислород делает сливки прогорклыми. [52]
У тяжелых (400 г или 200 л газа N 2 O за один сеанс) или частых (регулярных, т. е. ежедневных или еженедельных) потребителей, обратившихся в токсикологические центры, были отмечены признаки периферической невропатии : наличие атаксии ( нарушения походки) или парестезии (ощущение ненормальных ощущений, например, покалывания, онемения, покалывания, преимущественно в конечностях). Они считаются ранним признаком неврологического повреждения и указывают на хроническую токсичность . [53]
Закись азота в концентрации 75% по объему снижает вызванную ишемией гибель нейронов, вызванную окклюзией средней мозговой артерии у грызунов, и уменьшает NMDA-индуцированный приток Ca 2+ в культурах нейрональных клеток, что является критическим событием, связанным с эксайтотоксичностью . [50]
Профессиональное воздействие закиси азота связано с повреждением ДНК из-за перебоев в синтезе ДНК. [54] Эта корреляция является дозозависимой [55] [56] и, по-видимому, не распространяется на случайное использование препарата в рекреационных целях; однако необходимы дальнейшие исследования для подтверждения продолжительности и количества воздействия, необходимого для причинения ущерба.
Если вдыхать чистый закись азота без кислорода, может возникнуть кислородное голодание, что приводит к низкому кровяному давлению, обморокам и даже сердечным приступам. Это может произойти, если пользователь непрерывно вдыхает большие количества газа, например, при использовании надеваемой маски, подключенной к баллону с газом. Это также может произойти, если пользователь чрезмерно задерживает дыхание или использует любую другую систему ингаляции, которая перекрывает подачу свежего воздуха. [57]
Длительное воздействие закиси азота может вызвать дефицит витамина B12 . Это может вызвать серьезную нейротоксичность, если у пользователя уже имеется дефицит витамина B12 . [58] Он инактивирует кобаламиновую форму витамина B 12 путем окисления. Симптомы дефицита витамина B12 , включая сенсорную нейропатию , миелопатию и энцефалопатию , могут возникнуть в течение нескольких дней или недель после воздействия анестезии закисью азота у людей с субклиническим дефицитом витамина B12 .
Симптомы лечат высокими дозами витамина B 12 , но выздоровление может быть медленным и неполным. [59]
У людей с нормальным уровнем витамина B12 есть запасы, которые делают воздействие закиси азота незначительным, если только воздействие не повторяется и не продлевается (злоупотребление закисью азота). Уровни витамина B12 следует проверять у людей с факторами риска дефицита витамина B12 перед использованием анестезии закисью азота. [60]
Несколько экспериментальных исследований на крысах показывают, что хроническое воздействие закиси азота на беременных самок может оказывать неблагоприятное воздействие на развивающийся плод. [61] [62] [63]
При комнатной температуре (20 °C [68 °F]) давление насыщенного пара составляет 50,525 бар и возрастает до 72,45 бар при 36,4 °C (97,5 °F) — критической температуре . Таким образом, кривая давления необычайно чувствительна к температуре. [64]
Как и в случае со многими сильными окислителями, загрязнение деталей топливом приводило к авариям ракетной техники, когда небольшие количества смесей азота и топлива взрывались из-за эффектов, подобных «гидравлическому удару » (иногда называемых «дизельным топливом» — нагреву из-за адиабатического сжатия газов). может достигать температуры разложения). [65] Некоторые распространенные строительные материалы, такие как нержавеющая сталь и алюминий, могут действовать как топливо с сильными окислителями, такими как закись азота, а также загрязняющими веществами, которые могут воспламениться из-за адиабатического сжатия. [66]
Также были случаи, когда разложение закиси азота в водопроводе приводило к взрывам больших резервуаров. [18]
Фармакологический механизм действия Н
2О в медицине до конца не известен. Однако было показано, что он напрямую модулирует широкий спектр лиганд-управляемых ионных каналов , и это, вероятно, играет важную роль во многих его эффектах. Он умеренно блокирует NMDAR и каналы nACh , содержащие β 2 -субъединицу , слабо ингибирует АМРА , каинатные , ГАМК С и 5-НТ 3 рецепторы и слегка потенцирует ГАМК А и глициновые рецепторы . [67] [68] Также было показано, что он активирует двухпоровый домен K.+
каналы . [69] В то время как Н
2O влияет на довольно много ионных каналов, его анестезирующие, галлюциногенные и эйфорические эффекты, вероятно, обусловлены преимущественно или полностью ингибированием токов, опосредованных рецептором NMDA. [67] [70] Помимо воздействия на ионные каналы, N
2O может имитировать оксид азота (NO) в центральной нервной системе, и это может быть связано с его анальгетическими и анксиолитическими свойствами. [70] Закись азота в 30–40 раз более растворима, чем азот.
Известно, что эффекты вдыхания субанестезирующих доз закиси азота различаются в зависимости от нескольких факторов, включая условия и индивидуальные различия; [71] [72] однако из своего обсуждения Джей (2008) [44] предполагает, что достоверно известно, что он вызывает следующие состояния и ощущения:
У меньшинства пользователей также наблюдаются неконтролируемые вокализации и мышечные спазмы. Эти эффекты обычно исчезают через несколько минут после удаления источника закиси азота. [44]
В поведенческих тестах на тревогу низкая доза N
2O является эффективным анксиолитиком, и этот противотревожный эффект связан с повышенной активностью рецепторов ГАМК А , поскольку он частично устраняется антагонистами бензодиазепиновых рецепторов . Отражая это, животные, у которых развилась толерантность к анксиолитическому действию бензодиазепинов, частично толерантны к N.
2О. _ [73] Действительно, у людей, получавших 30% N
2В клинических исследованиях на людях антагонисты бензодиазепиновых рецепторов снижали субъективные ощущения «приподнятого настроения», но не изменяли психомоторные характеристики. [74] [75]
Анальгетический эффект Н.
2О связаны с взаимодействием эндогенной опиоидной системы и нисходящей норадренергической системы. Когда животным хронически дают морфин, у них развивается толерантность к его обезболивающему эффекту, что также делает животных толерантными к обезболивающему эффекту N.
2О. _ [76] Введение антител , которые связывают и блокируют активность некоторых эндогенных опиоидов (не β-эндорфина ), также блокируют антиноцицептивные эффекты N.
2О. _ [77] Препараты, ингибирующие распад эндогенных опиоидов, также усиливают антиноцицептивные эффекты N.
2О. _ [77] Несколько экспериментов показали, что антагонисты опиоидных рецепторов, наносимые непосредственно на мозг, блокируют антиноцицептивные эффекты N.
2О , но эти препараты не оказывают никакого эффекта при введении в спинной мозг .
Помимо непрямого действия, закись азота, как и морфин [78], также напрямую взаимодействует с эндогенной опиоидной системой, связываясь с сайтами связывания опиоидных рецепторов. [79] [80]
И наоборот, антагонисты α 2 -адренорецепторов блокируют обезболивающее действие N.
2О , если вводить непосредственно в спинной мозг, но не вводить непосредственно в головной мозг. [81] Действительно, мыши с нокаутом α2B - адренорецепторов или животные с истощением норадреналина практически полностью резистентны к антиноцицептивным эффектам N
2О. _ [82] Видимо Н
2O -индуцированное высвобождение эндогенных опиоидов вызывает растормаживание норадренергических нейронов ствола мозга , которые выделяют норадреналин в спинной мозг и подавляют передачу болевых сигналов. [83] Именно так Н.
2Причины высвобождения эндогенных опиоидных пептидов остаются неясными.
Закись азота — бесцветный газ со слабым сладковатым запахом.
Закись азота поддерживает горение, высвобождая диполярный связанный кислородный радикал, и, таким образом, может повторно зажечь светящуюся лучину .
Н
2O инертен при комнатной температуре и мало реагирует. При повышенных температурах его реакционная способность увеличивается. Например, закись азота реагирует с NaNH.
2при 460 К (187 ° C), чтобы получить NaN3:
Вышеуказанная реакция представляет собой путь, принятый в коммерческой химической промышленности для производства солей азидов , которые используются в качестве детонаторов. [84]
Газ был впервые синтезирован в 1772 году английским натурфилософом и химиком Джозефом Пристли , который назвал его дефлогистизированным азотистым воздухом (см. теорию флогистона ) [85] или горючим азотистым воздухом . [86] Пристли опубликовал свое открытие в книге «Опыты и наблюдения над различными видами воздуха» (1775) , где он описал, как получить препарат «уменьшенного азотистого воздуха» путем нагревания железных опилок, смоченных азотной кислотой . [87]

Первое важное использование закиси азота стало возможным благодаря Томасу Беддоусу и Джеймсу Уотту , которые вместе работали над публикацией книги «Соображения о медицинском использовании и производстве искусственных эфиров» (1794) . Эта книга была важна по двум причинам. Во-первых, Джеймс Уатт изобрел новую машину для производства « искусственного воздуха » (включая закись азота) и новый «дыхательный аппарат» для вдыхания этого газа. Во-вторых, в книге также представлены новые медицинские теории Томаса Беддоса о том, что туберкулез и другие легочные заболевания можно лечить вдыханием «искусственного воздуха». [25]

Машина для производства «фальшивых эфиров» состояла из трех частей: печи для сжигания необходимого материала, сосуда с водой, через который по спиральной трубе проходил добываемый газ (для «смывания» примесей) и, наконец, газового баллона. с помощью газометра, с помощью которого образующийся газ, «воздух», можно было подавать в переносные воздушные мешки (сделанные из воздухонепроницаемого маслянистого шелка). Дыхательный аппарат представлял собой одну из переносных подушек безопасности, соединенную трубкой с загубником. Когда это новое оборудование было спроектировано и произведено к 1794 году, был проложен путь для клинических испытаний , [ необходимы разъяснения ] , которые начались в 1798 году, когда Томас Беддос основал « Пневматический институт для облегчения заболеваний медицинским воздухом» в Хотвеллсе ( Бристоль ). В подвале здания большая машина производила газы под наблюдением молодого Хамфри Дэви, которому было предложено экспериментировать с новыми газами, которые пациенты могли бы вдыхать. [25] Первой важной работой Дэви было исследование закиси азота и публикация его результатов в книге: Исследования, химические и философские (1800) . В этой публикации Дэви отмечает обезболивающий эффект закиси азота на странице 465 и ее потенциал для использования в хирургических операциях на странице 556. [88] Дэви придумал название «веселящий газ» для закиси азота. [89]
Несмотря на открытие Дэви, что вдыхание закиси азота может избавить находящегося в сознании человека от боли, прошло еще 44 года, прежде чем врачи попытались использовать ее для анестезии . Использование закиси азота в качестве развлекательного наркотика на «вечеринках с веселящим газом», организованных в первую очередь для представителей высшего класса Великобритании , стало немедленным успехом, начиная с 1799 года. люди также «хихикают» в состоянии эйфории и часто разражаются смехом. [90]
Одним из первых коммерческих производителей в США был Джордж По , двоюродный брат поэта Эдгара Аллана По , который также был первым, кто сжижал газ. [91]
Впервые закись азота была использована в качестве анестезирующего препарата при лечении пациента, когда дантист Хорас Уэллс при содействии Гарднера Куинси Колтона и Джона Мэнки Риггса продемонстрировал нечувствительность к боли при удалении зуба 11 декабря 1844 года. [92] В последующие недели Уэллс лечил первых 12–15 пациентов закисью азота в Хартфорде, штат Коннектикут , и, согласно его собственным данным, безуспешно только в двух случаях. [93] Несмотря на то, что Уэллс сообщил об этих убедительных результатах медицинскому обществу Бостона в декабре 1844 года, этот новый метод не был сразу принят другими стоматологами. Причиной этого, скорее всего, было то, что Уэллс в январе 1845 года на своей первой публичной демонстрации на медицинском факультете в Бостоне оказался частично неудачным, что заставило его коллег усомниться в ее эффективности и безопасности. [94] Этот метод не получил широкого распространения до 1863 года, когда Гарднер Куинси Колтон успешно начал использовать его во всех своих клиниках «Стоматологической ассоциации Колтона», которые он только что открыл в Нью-Хейвене и Нью-Йорке . [25] В течение следующих трех лет Колтон и его коллеги успешно вводили закись азота более чем 25 000 пациентам. [26] Сегодня закись азота используется в стоматологии как анксиолитик, как дополнение к местному анестетику .
Однако закись азота не оказалась достаточно сильным анестетиком для использования при крупных операциях в больницах. Вместо этого в октябре 1846 года был продемонстрирован и принят к использованию диэтиловый эфир , являющийся более сильным и мощным анестетиком, наряду с хлороформом в 1847 году . В больницах стало обычной практикой начинать все анестезирующие процедуры с легкой подачи закиси азота, а затем постепенно усиливать анестезию более сильным эфиром или хлороформом. Газо-эфирный ингалятор Клевера был предназначен для подачи пациенту закиси азота и эфира одновременно, при этом точная смесь контролируется оператором аппарата. Он использовался во многих больницах до 1930-х годов. [26] Хотя сегодня в больницах используется более совершенный наркозный аппарат , эти аппараты по-прежнему используют тот же принцип, что и газо-эфирный ингалятор Клевера, для инициирования анестезии закисью азота перед введением более мощного анестетика.
Популяризация закиси азота Колтоном привела к ее принятию рядом не слишком уважаемых шарлатанов , которые рекламировали ее как лекарство от чахотки , золотухи , катара и других заболеваний крови, горла и легких. Лечение закисью азота проводилось и лицензировалось как патентованное лекарство такими компаниями, как CL Blood и Джером Харрис из Бостона и Чарльзом Э. Барни из Чикаго. [95] [96]
Опубликован обзор различных способов получения закиси азота. [97]
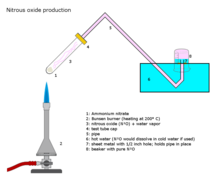
Закись азота получают в промышленных масштабах осторожным нагреванием нитрата аммония [97] при температуре около 250 °С, который разлагается на закись азота и водяной пар. [98]
Добавление различных фосфатных солей способствует образованию более чистого газа при несколько более низких температурах. Эту реакцию трудно контролировать, что приводит к детонации . [99]
Разложение нитрата аммония также является распространенным лабораторным методом подготовки газа. Эквивалентно его можно получить нагреванием смеси нитрата натрия и сульфата аммония : [100]
Другой метод предполагает реакцию мочевины, азотной и серной кислот: [101]
Сообщалось о прямом окислении аммиака катализатором диоксид марганца - оксид висмута : [102] ср. Оствальдовский процесс .
Хлорид гидроксиламмония реагирует с нитритом натрия с образованием закиси азота. Если к раствору гидроксиламина добавить нитрит, единственным оставшимся побочным продуктом будет соленая вода. Однако если к раствору нитрита добавить раствор гидроксиламина (нитрит в избытке), то образуются и токсичные высшие оксиды азота:
Лечение ГНО
3с SnCl
2и HCl также было продемонстрировано:
Азотистистая кислота разлагается на N 2 O и воду с периодом полураспада 16 дней при 25 °C и pH 1–3. [103]
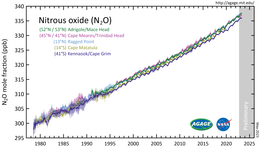



Закись азота является второстепенным компонентом земной атмосферы и активной частью планетарного цикла азота . Судя по анализу проб воздуха, собранных на объектах по всему миру, его концентрация превысила 330 частей на миллиард в 2017 году . [8] Темпы роста примерно на 1 часть на миллиард в год также ускорились в последние десятилетия. [9] Содержание закиси азота в атмосфере выросло более чем на 20% по сравнению с базовым уровнем около 270 частей на миллиард в 1750 году. [105]
Важные атмосферные свойства N
2O сведены в следующую таблицу:
В 2022 году МГЭИК сообщила, что: «Нарушение человеком естественного азотного цикла посредством использования синтетических удобрений и навоза, а также отложение азота в результате наземного сельского хозяйства и сжигания ископаемого топлива стали крупнейшим фактором увеличения атмосферных выбросов». N2O 31,0 ± 0,5 частей на миллиард (10%) в период с 1980 по 2019 год». [108]
17,0 (от 12,2 до 23,5) миллионов тонн общего среднегодового азота в N
2O выделялся в 2007–2016 гг. [108] Около 40% N
2Выбросы O происходят от человека, а остальная часть является частью естественного цикла азота . [109 ] Н
2O, выбрасываемый людьми каждый год, имеет парниковый эффект, эквивалентный примерно 3 миллиардам тонн углекислого газа: для сравнения, в 2019 году люди выбросили 37 миллиардов тонн фактического углекислого газа, а метан эквивалентен 9 миллиардам тонн углекислого газа. [110]
Большая часть Н
2O , выбрасываемый в атмосферу из природных и антропогенных источников, производится микроорганизмами , такими как денитрифицирующие бактерии и грибы в почвах и океанах. [111] Почвы под естественной растительностью являются важным источником закиси азота, на их долю приходится 60% всех выбросов, производимых естественным путем. Другие природные источники включают океаны (35%) и химические реакции в атмосфере (5%). [112] Водно-болотные угодья также могут быть источниками выбросов закиси азота . [113] [114] Выбросы от таяния вечной мерзлоты могут быть значительными, но по состоянию на 2022 год это не точно. [108]
Основными компонентами антропогенных выбросов являются удобренные сельскохозяйственные почвы и навоз скота (42 %), стоки и вымывание удобрений (25 %), сжигание биомассы (10 %), сжигание ископаемого топлива и промышленные процессы (10 %), биологическая деградация других азотсодержащие выбросы в атмосферу (9%) и сточные воды жизнедеятельности человека (5%). [115] [116] [117] [118] [119] Сельское хозяйство увеличивает производство закиси азота за счет обработки почвы, использования азотных удобрений и переработки отходов животноводства. [120] Эти действия стимулируют встречающиеся в природе бактерии производить больше закиси азота. Выбросы закиси азота из почвы сложно измерить, поскольку они заметно различаются во времени и пространстве, [121] и большая часть годовых выбросов может происходить, когда условия благоприятны в «жаркие моменты» [122] [123] и/или в благоприятные места, известные как «горячие точки». [124]
Среди промышленных выбросов крупнейшими источниками выбросов закиси азота являются производство азотной кислоты и адипиновой кислоты . Выбросы адипиновой кислоты возникают, в частности, в результате разложения промежуточного продукта нитроловой кислоты , полученного в результате нитрования циклогексанона. [115] [125] [126]
Естественные процессы, в результате которых образуется закись азота, можно классифицировать как нитрификацию и денитрификацию . В частности, они включают в себя:
На эти процессы влияют химические и физические свойства почвы, такие как наличие минерального азота и органических веществ , кислотность и тип почвы, а также факторы, связанные с климатом, такие как температура почвы и содержание воды.
Выброс газа в атмосферу в значительной степени ограничивается его потреблением внутри клеток процессом, катализируемым ферментом редуктазой закиси азота . [127]

Закись азота обладает значительным потенциалом глобального потепления как парниковый газ . В пересчете на молекулу, если рассматривать 100-летний период, закись азота имеет в 265 раз большую способность улавливать тепло в атмосфере, чем углекислый газ ( CO
2). [107] Однако из-за его низкой концентрации (менее 1/1000 от концентрации CO
2), его вклад в парниковый эффект составляет менее трети вклада углекислого газа, а также меньше, чем водяного пара и метана . [128] С другой стороны, поскольку около 40% N
2Попадание O в атмосферу является результатом деятельности человека, [115] контроль за закисью азота считается частью усилий по ограничению выбросов парниковых газов. [129]
Большая часть выбросов закиси азота в атмосферу происходит в результате деятельности сельского хозяйства, когда фермеры добавляют на поля азотные удобрения, а также в результате разложения навоза животных. Сокращение выбросов может стать горячей темой в политике по изменению климата . [130]
Закись азота также выделяется как побочный продукт сжигания ископаемого топлива, хотя его количество зависит от того, какое топливо использовалось. Он также выделяется при производстве азотной кислоты , которая используется при синтезе азотных удобрений. Производство адипиновой кислоты, предшественника нейлона и других синтетических волокон для одежды, также приводит к выбросу закиси азота. [131]
Повышение концентрации закиси азота в атмосфере считается возможным фактором чрезвычайно интенсивного глобального потепления во время пограничного события сеномана и турона . [132]
Закись азота также участвует в истончении озонового слоя . Исследование 2009 года показало, что N
2Выбросы O были наиболее важными выбросами, разрушающими озоновый слой, и ожидалось, что они останутся крупнейшими на протяжении всего 21 века. [10] [133]
В Соединенных Штатах хранение закиси азота разрешено федеральным законом и не подпадает под действие DEA . [134] Однако это регулируется Управлением по контролю за продуктами и лекарствами в соответствии с Законом о пищевых лекарствах и косметике; Судебное преследование возможно в соответствии с его статьями о «неправильной маркировке», запрещающими продажу или распространение закиси азота для целей потребления человеком . Во многих штатах действуют законы, регулирующие хранение, продажу и распространение закиси азота. Такие законы обычно запрещают распространение среди несовершеннолетних или ограничивают количество закиси азота, которое можно продавать без специальной лицензии. [ необходима цитата ] Например, в штате Калифорния хранение для рекреационного использования запрещено и квалифицируется как правонарушение. [135]
В августе 2015 года совет лондонского района Ламбет ( Великобритания ) запретил использование препарата в рекреационных целях, в результате чего нарушители будут подлежать штрафу на месте в размере до 1000 фунтов стерлингов. [136]
В Новой Зеландии Министерство здравоохранения предупредило, что закись азота является лекарством, отпускаемым по рецепту, и ее продажа или хранение без рецепта является преступлением в соответствии с Законом о лекарственных средствах. [137] Это заявление, по-видимому, запрещает любое немедицинское использование закиси азота, хотя подразумевается, что законом будет запрещено только рекреационное использование.
В Индии перекачка закиси азота из баллонов в меньшие по размеру и более транспортабельные резервуары типа Е емкостью 1590 литров [138] является законной, если газ предполагается использовать для медицинской анестезии.
В сентябре 2023 года правительство Великобритании объявило, что к концу года закись азота будет объявлена незаконной, а ее хранение может караться тюремным заключением на срок до двух лет или штрафом в неограниченном размере. [139]
{{cite journal}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка )... Самогерметизация (давление пара при 20 ° C составляет ~ 50,1 бар ... Нетоксично, низкая реакционная способность -> относительно безопасное обращение (Общая безопасность ???).. .Дополнительная энергия от разложения (в качестве монотоплива: ISP 170 с)...Удельный импульс не сильно меняется при использовании O/F...[страница 2] N
2
O является монотопливом (как H
2
O
2
или гидразин) ...)
Например, N2O, текущий под давлением 130 фунтов на квадратный дюйм в композитной трубе из эпоксидной смолы, не вступит в реакцию даже при подаче энергии воспламенения 2500 Дж. Однако при давлении 600 фунтов на квадратный дюйм необходимая энергия зажигания составляла всего 6 Дж.