Нитроглицерин ( НГ ), (альтернативное написание нитроглицерина), также известный как тринитроглицерин ( ТНГ ), нитро , тринитрат глицерина ( ГТН ) или 1,2,3-тринитроксипропан , представляет собой плотную, бесцветную, маслянистую, взрывчатую жидкость, чаще всего производимую нитрование глицерина белой дымящей азотной кислотой в условиях, подходящих для образования эфира азотной кислоты . Химически вещество представляет собой органическое нитратное соединение, а не нитросоединение , но традиционное название сохранено. Обнаруженный в 1847 году Асканио Собреро , нитроглицерин использовался в качестве активного ингредиента при производстве взрывчатых веществ , а именно динамита , и как таковой он применяется в строительстве , сносе зданий и горнодобывающей промышленности. В сочетании с нитроцеллюлозой он образует бездымный порох двойной основы , который с 1880-х годов используется в качестве пороха в артиллерийском и огнестрельном оружии.
Нитроглицерин уже более 130 лет используется в медицине в качестве мощного сосудорасширяющего средства (вызывающего расширение сосудистой системы) для лечения заболеваний сердца , таких как стенокардия и хроническая сердечная недостаточность . Хотя ранее было известно, что эти положительные эффекты обусловлены превращением нитроглицерина в оксид азота , мощный венодилататор, только в 2002 году было обнаружено, что ферментом этого преобразования является митохондриальная альдегиддегидрогеназа ( ALDH2 ). [4] Нитроглицерин доступен для сублингвального введения . таблетки , спреи, мази и пластыри. [5]
Нитроглицерин был первым практически изготовленным взрывчатым веществом, которое было сильнее черного пороха . Он был синтезирован итальянским химиком Асканио Собреро в 1847 году, работавшим под руководством Теофиля-Жюля Пелуза в Туринском университете . [6] Собреро первоначально назвал свое открытие пироглицерином и решительно предостерег от его использования в качестве взрывчатого вещества. [7]
Нитроглицерин был принят в качестве коммерчески полезного взрывчатого вещества Альфредом Нобелем , который экспериментировал с более безопасными способами обращения с опасным соединением после того, как его младший брат Эмиль Оскар Нобель и несколько рабочих погибли в результате взрыва на оружейном заводе Нобелей в 1864 году в Хеленеборге . , Швеция. [8]

Год спустя Нобель основал Alfred Nobel and Company в Германии и построил изолированную фабрику на холмах Круммель в Гестахте недалеко от Гамбурга . Этот бизнес экспортировал жидкую смесь нитроглицерина и пороха под названием «Взрывное масло», но она была крайне нестабильной и с ней было трудно обращаться, о чем свидетельствуют многочисленные катастрофы. Здания завода Круммель были разрушены дважды. [9]
В апреле 1866 года несколько ящиков нитроглицерина были отправлены в Калифорнию , три из которых предназначались для Центрально-Тихоокеанской железной дороги , которая планировала экспериментировать с ним в качестве взрывчатого вещества, чтобы ускорить строительство вершины Саммита длиной 1659 футов (506 м). Туннель через горы Сьерра-Невада . Один из оставшихся ящиков взорвался, разрушив офис компании Wells Fargo в Сан-Франциско и убив 15 человек. Это привело к полному запрету перевозки жидкого нитроглицерина в Калифорнии. Таким образом, производство нитроглицерина на месте потребовалось для оставшихся буровых и взрывных работ в твердых породах , необходимых для завершения строительства Первой трансконтинентальной железной дороги в Северной Америке. [10]
В день Рождества 1867 года попытка избавиться от девяти канистр с взрывчатым маслом, незаконно хранившихся в гостинице «Белый лебедь» в центре Ньюкасл-апон-Тайн, привела к взрыву на Таун-Мур, в результате которого погибли восемь человек. В июне 1869 года два однотонных фургона, груженные нитроглицерином, тогда известным как «Паудер-ойл», взорвались на дороге в деревне Кум-и-гло в Северном Уэльсе . Взрыв привел к гибели шести человек, многочисленным ранениям и серьезному ущербу села. Маленький след был найден из двух лошадей. Правительство Великобритании было настолько встревожено нанесенным ущербом и тем, что могло произойти в районе города (эти две тонны были частью более крупного груза, идущего из Германии через Ливерпуль), что вскоре приняло Закон о нитро-глицерине 1869 года. [11] Жидкий нитроглицерин был широко запрещен и в других местах, и эти правовые ограничения привели к тому, что Альфред Нобель и его компания в 1867 году разработали динамит . Он был изготовлен путем смешивания нитроглицерина с диатомовой землей (« Кизельгур » по-немецки), найденной на холмах Круммель. Подобные смеси, такие как «дуалин» (1867 г.), «литофрактер» (1869 г.) и « гелигнит » (1875 г.), были получены путем смешивания нитроглицерина с другими инертными абсорбентами, и многие комбинации были опробованы другими компаниями в попытках обойти Нобелевские плотно удержанные патенты на динамит.
Динамитовые смеси, содержащие нитроцеллюлозу , повышающую вязкость смеси, широко известны как «желатины».
После открытия того, что амилнитрит помогает облегчить боль в груди, врач Уильям Мюррелл экспериментировал с использованием нитроглицерина для облегчения стенокардии и снижения артериального давления . Он начал лечить своих пациентов небольшими разбавленными дозами нитроглицерина в 1878 году, и это лечение вскоре получило широкое распространение после того, как Мюррелл опубликовал свои результаты в журнале The Lancet в 1879 году . [12] [13] За несколько месяцев до своей смерти в 1896 году. Альфреду Нобелю при этом заболевании сердца прописали нитроглицерин, и он написал другу: «Разве это не ирония судьбы, что мне прописали нитроглицерин для приема внутрь! Они называют его тринитрином, чтобы не пугать химик и общественность». [14] По той же причине медицинские учреждения также использовали название «тринитрат глицерина».
Во время Первой и Второй мировых войн производилось большое количество нитроглицерина для использования в качестве военного топлива и в военно-инженерных работах. Во время Первой мировой войны завод HM в Гретне , крупнейший завод по производству топлива в Соединенном Королевстве , производил около 800 тонн кордита RDB в неделю. На этот объем требовалось не менее 336 тонн нитроглицерина в неделю (при условии отсутствия потерь в производстве). Королевский флот имел собственную фабрику на заводе кордитов Королевского флота в Холтон-Хит в Дорсете , Англия. Большой завод по производству кордита был также построен в Канаде во время Первой мировой войны. Завод по производству кордита Canadian Explosives Limited в Нобеле, Онтарио , был спроектирован для производства 1 500 000 фунтов (680 тонн) кордита в месяц, что требовало около 286 тонн нитроглицерина в месяц.
В неразбавленном виде нитроглицерин является контактным взрывчатым веществом , при физическом ударе он взрывается. Если он не был должным образом очищен во время производства, он может со временем разложиться до еще более нестабильных форм. Это делает нитроглицерин очень опасным при транспортировке или использовании. В неразбавленном виде это одно из самых мощных взрывчатых веществ в мире, сравнимое с недавно разработанными гексогеном и тэном .
В начале своей истории было обнаружено, что жидкий нитроглицерин « снижается чувствительность » путем замораживания его при температуре ниже 45–55 °F (7–13 °C) в зависимости от его чистоты. [15] Его чувствительность к ударам в замороженном состоянии несколько непредсказуема: «В таком состоянии он более нечувствителен к ударам от молниеносного капсюля или винтовочной пули, но, с другой стороны, он более склонен взорваться при разбивании или раздавливании». , трамбовка и т. д." [16] Замороженный нитроглицерин гораздо менее энергичен, чем жидкий, поэтому перед использованием его необходимо разморозить. [17] Оттаивание может быть чрезвычайно чувствительным, особенно если присутствуют примеси или потепление слишком быстрое. [18] Динитрат этиленгликоля или другой полинитрат могут быть добавлены для снижения температуры плавления и, таким образом, устранения необходимости оттаивания замороженного взрывчатого вещества. [19]
Химически «десенсибилизировать» нитроглицерин можно до такой степени, что его можно будет считать примерно таким же «безопасным», как современные бризантные взрывчатые вещества , например, путем добавления этанола , ацетона или динитротолуола . [20] Нитроглицерин, возможно, придется экстрагировать из химического десенсибилизатора, чтобы восстановить его эффективность перед использованием, например, путем добавления воды для удаления этанола, используемого в качестве десенсибилизатора. [20]
При взрыве нитроглицерина продукты после охлаждения имеют вид:
Выделяемое тепло можно рассчитать по теплоте образования. Использование -371 кДж/ моль на теплоту образования конденсированной фазы нитроглицерина [21] дает 1414 кДж/моль, выделяющуюся при образовании водяного пара, и 1524 при образовании жидкой воды.
Скорость детонации нитроглицерина составляет 7820 метров в секунду, что примерно на 113% превышает скорость тротила . Соответственно, нитроглицерин считается взрывчатым веществом высокой бризантности , то есть обладает превосходной разрушающей способностью. Тепло, выделяющееся при детонации, повышает температуру газообразных побочных продуктов примерно до 5000 ° C (9000 ° F). [19] При стандартной энтальпии взрывного разложения -1414 кДж/ моль и молекулярной массе 227,0865 г/моль нитроглицерин имеет удельную плотность энергии взрыва 1,488 килокалорий на грамм, или 6,23 кДж/г, что делает нитроглицерин на 49% больше. энергичен по массе, чем стандартное значение, присвоенное тротилу (точно 1 ккал/г).
Нитроглицерин можно получить кислотно-катализируемым нитрованием глицерина (глицерина).
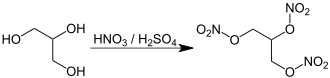
В процессе промышленного производства глицерин часто реагирует со смесью концентрированной серной и концентрированной азотной кислот в соотношении почти 1:1 . Его можно получить, смешивая белую дымящую азотную кислоту — довольно дорогую чистую азотную кислоту , в которой удалены оксиды азота, в отличие от красной дымящей азотной кислоты , которая содержит оксиды азота , — и концентрированной серной кислоты . Чаще всего эту смесь получают более дешевым методом смешивания дымящей серной кислоты , также известной как олеум , — серной кислоты , содержащей избыток триоксида серы , — и азеотропной азотной кислоты (состоящей примерно на 70% из азотной кислоты , а остальное — вода).
Серная кислота производит протонированные формы азотной кислоты , которые подвергаются атаке нуклеофильных атомов кислорода глицерина . Таким образом , нитрогруппа добавляется в виде сложного эфира C-O-NO 2 и образуется вода. Это отличается от реакции электрофильного ароматического замещения, в которой ионы нитрония являются электрофилами .
Добавление глицерина приводит к экзотермической реакции (т.е. выделяется тепло), как это обычно бывает при нитровании смешанными кислотами. Если смесь становится слишком горячей, это приводит к неконтролируемой реакции, состоянию ускоренного нитрования, сопровождающемуся разрушительным окислением органических материалов горячей азотной кислотой и выделением ядовитого газообразного диоксида азота с высоким риском взрыва. Таким образом, смесь глицерина медленно добавляют в реакционный сосуд, содержащий смешанную кислоту (а не кислоту к глицерину). Нитратор охлаждается холодной водой или какой-либо другой охлаждающей смесью и во время добавления глицерина поддерживается при температуре около 22 ° C (72 ° F), достаточно горячей для того, чтобы этерификация происходила с высокой скоростью, но достаточно холодной, чтобы избежать неконтролируемой реакции. Сосуд нитрататора, часто изготавливаемый из железа или свинца и обычно перемешиваемый сжатым воздухом , имеет в основании аварийный люк, который нависает над большим бассейном с очень холодной водой и в который может быть помещена вся реакционная смесь (называемая загрузкой). сбрасывают, чтобы предотвратить взрыв - процесс, называемый утоплением. Если температура заряда превышает примерно 30 ° C (86 ° F) (фактическое значение зависит от страны) или в вентиляционном отверстии нитрататора появляются коричневые пары, его немедленно топят.
Основное применение нитроглицерина по тоннажу приходится на производство взрывчатых веществ, таких как динамит, и ракетного топлива.
Нитроглицерин — маслянистая жидкость, которая может взорваться при воздействии тепла, удара или пламени.
Альфред Нобель разработал применение нитроглицерина в качестве бризантного взрывчатого вещества путем смешивания нитроглицерина с инертными поглотителями , в частности с « Кизельгуром », или диатомитовой землей . Он назвал это взрывчатое вещество динамитом и запатентовал его в 1867 году. [25] Он поставлялся готовым к использованию в виде палочек, индивидуально завернутых в промасленную водонепроницаемую бумагу. Динамит и подобные взрывчатые вещества широко применялись для задач гражданского строительства , например, при бурении автомобильных и железнодорожных туннелей , в горнодобывающей промышленности , для расчистки сельскохозяйственных угодий от пней, в карьерах и при работах по сносу зданий . Точно так же военные инженеры использовали динамит для строительных и сносных работ.
Нитроглицерин также использовался в качестве ингредиента военного топлива для огнестрельного оружия .
Нитроглицерин использовался в сочетании с гидроразрывом пласта — процессом, используемым для добычи нефти и газа из сланцевых пластов. Этот метод включает вытеснение и детонацию нитроглицерина в системах естественных или гидравлических трещин или вытеснение и детонацию нитроглицерина в гидравлических трещинах с последующими выстрелами в ствол скважины с использованием гранулированного тротила . [26]
Нитроглицерин имеет преимущество перед некоторыми другими бризантными взрывчатыми веществами в том, что при детонации он практически не выделяет видимого дыма. Поэтому он полезен в качестве ингредиента в составе различных видов бездымного пороха . [27]
Его чувствительность ограничила полезность нитроглицерина в качестве военного взрывчатого вещества, а менее чувствительные взрывчатые вещества, такие как тротил , гексоген и октоген , в значительной степени заменили его в боеприпасах. Он по-прежнему важен в военной технике, и саперы до сих пор используют динамит.
Альфред Нобель затем разработал баллистит , соединив нитроглицерин и пороховую вату . Он запатентовал его в 1887 году. Баллистит был принят на вооружение рядом европейских правительств в качестве военного топлива. Италия была первой, кто принял его. Вместо этого британское правительство и правительства Содружества приняли на вооружение кордит , который был разработан сэром Фредериком Абелем и сэром Джеймсом Дьюаром из Соединенного Королевства в 1889 году. Первоначальный кордит Mk I состоял из 58% нитроглицерина, 37% порохового хлопка и 5,0% вазелина. . Баллистит и кордит изготавливались в виде «шнуров».
Первоначально бездымные пороха были разработаны с использованием нитроцеллюлозы в качестве единственного взрывчатого ингредиента. Поэтому они были известны как одноосновное топливо. Также был разработан ряд бездымных порохов, содержащих как нитроцеллюлозу, так и нитроглицерин, известных как двухосновные пороха. Бездымные пороха изначально поставлялись только для военного использования, но вскоре были разработаны и для гражданского использования и быстро были приняты на вооружение в спорте. Некоторые из них известны как спортивные порошки. Трехосновное порох содержит нитроцеллюлозу, нитроглицерин и нитрогуанидин , но предназначено в основном для боеприпасов чрезвычайно высокого калибра, таких как те, которые используются в танковых пушках и морской артиллерии . Взрывчатый желатин, также известный как гелигнит , был изобретен Нобелем в 1875 году с использованием нитроглицерина, древесной массы и нитрата натрия или калия . Это было первое недорогое гибкое взрывчатое вещество.
Нитроглицерин принадлежит к группе препаратов, называемых нитратами, в которую входят многие другие нитраты, такие как динитрат изосорбида (Изордил) и мононитрат изосорбида (Имдур, Исмо, Монокет). [28] Все эти агенты оказывают свое действие, превращаясь в оксид азота в организме под действием митохондриальной альдегиддегидрогеназы ( ALDH2 ), [4] а оксид азота является мощным природным сосудорасширяющим средством.

В медицине нитроглицерин, вероятно, чаще всего назначают при стенокардии — болезненном симптоме ишемической болезни сердца , вызванном недостаточным притоком крови и кислорода к сердцу, а также в качестве мощного антигипертензивного средства. Нитроглицерин исправляет дисбаланс между потоком кислорода и крови к сердцу и потребностями сердца в энергии. [28] На рынке представлено множество препаратов в разных дозах. В низких дозах нитроглицерин расширяет вены больше, чем артерии, тем самым уменьшая преднагрузку (объем крови в сердце после наполнения); Считается, что это его основной механизм действия. Уменьшая преднагрузку, сердцу приходится перекачивать меньше крови, что снижает потребность в кислороде, поскольку сердцу не приходится работать так усердно. Кроме того, меньшая преднагрузка снижает трансмуральное давление желудочков (давление, оказываемое на стенки сердца), что уменьшает компрессию сердечных артерий, позволяя большему количеству крови течь через сердце. В более высоких дозах он также расширяет артерии, тем самым уменьшая постнагрузку (уменьшая давление, против которого сердце должно качать кровь). [28] Улучшение соотношения потребности миокарда в кислороде и его снабжении приводит к следующим терапевтическим эффектам во время эпизодов стенокардии: стиханию боли в груди, снижению артериального давления , увеличению частоты сердечных сокращений и ортостатической гипотензии . Пациенты, испытывающие стенокардию при выполнении определенных физических нагрузок, часто могут предотвратить симптомы, принимая нитроглицерин за 5–10 минут до занятия. Передозировки могут генерировать метгемоглобинемию . [29] [30]
Нитроглицерин выпускается в виде таблеток, мази, раствора для внутривенного применения, трансдермальных пластырей или спреев, вводимых сублингвально . Некоторые формы нитроглицерина сохраняются в организме гораздо дольше, чем другие. Нитроглицерин, а также начало и продолжительность действия каждой формы различны. Сублингвальный или таблетированный спрей нитроглицерина имеет начало действия через две минуты и продолжительность действия двадцать пять минут. При пероральном приеме нитроглицерина начало действия начинается через тридцать пять минут, а продолжительность действия составляет 4–8 часов. Действие трансдермального пластыря начинается через тридцать минут, а продолжительность действия составляет от десяти до двенадцати часов. Было показано, что постоянное воздействие нитратов приводит к тому, что организм перестает нормально реагировать на это лекарство. Специалисты рекомендуют снимать пластыри на ночь, давая организму несколько часов для восстановления реакции на нитраты. Препараты нитроглицерина более короткого действия можно применять несколько раз в день с меньшим риском развития толерантности. [31] Нитроглицерин впервые был использован Уильямом Мюрреллом для лечения приступов стенокардии в 1878 году, а открытие было опубликовано в том же году. [13] [32]
Редкое воздействие высоких доз нитроглицерина может вызвать сильные головные боли , известные как «голова НГ» или «голова с ударом». Эти головные боли могут быть достаточно сильными, чтобы вывести некоторых людей из строя; однако после длительного воздействия у людей развивается толерантность и зависимость от нитроглицерина. Хотя и редко, абстиненция может быть фатальной. [33] Симптомы абстиненции включают боль в груди и другие проблемы с сердцем. Эти симптомы можно облегчить при повторном воздействии нитроглицерина или других подходящих органических нитратов. [34]
Для работников предприятий по производству нитроглицерина (НТГ) последствия абстиненции иногда включают «воскресные сердечные приступы» у тех, кто регулярно подвергается воздействию нитроглицерина на рабочем месте, что приводит к развитию толерантности к венодилатирующим эффектам. За выходные рабочие теряют толерантность, а когда их повторно подвергают воздействию в понедельник, резкое расширение сосудов вызывает учащенное сердцебиение , головокружение и головную боль. Это называется «болезнь понедельника». [35] [36]
Люди могут подвергнуться воздействию нитроглицерина на рабочем месте при вдыхании, попадании через кожу, проглатывании или попадании в глаза. Управление по охране труда установило законный предел ( допустимый предел воздействия ) для воздействия нитроглицерина на рабочем месте как воздействие на кожу 0,2 ppm (2 мг/м 3 ) в течение 8-часового рабочего дня. Национальный институт охраны труда и здоровья установил рекомендуемый предел воздействия на кожу в размере 0,1 мг/м 3 в течение 8-часового рабочего дня. При уровне 75 мг/м 3 нитроглицерин сразу опасен для жизни и здоровья . [37]
{{cite web}}: Внешняя ссылка |series={{cite web}}: Внешняя ссылка |series={{cite web}}: Внешняя ссылка |series=