Протактиний — химический элемент ; имеет символ Pa и атомный номер 91. Это плотный, радиоактивный , серебристо-серый актиноидный металл, который легко реагирует с кислородом , водяным паром и неорганическими кислотами . Он образует различные химические соединения , в которых протактиний обычно присутствует в степени окисления +5, но может также принимать состояния +4 и даже +3 или +2. Концентрации протактиния в земной коре обычно составляют несколько частей на триллион, но могут достигать нескольких частей на миллион в некоторых месторождениях уранинитовой руды. Из-за его редкости, высокой радиоактивности и высокой токсичности в настоящее время нет никаких применений для протактиния за пределами научных исследований, и для этой цели протактиний в основном извлекается из отработанного ядерного топлива .
Элемент был впервые идентифицирован в 1913 году Казимежом Фаянсом и Освальдом Хельмутом Герингом и назван «бревиум» из-за короткого периода полураспада конкретного изученного изотопа , протактиния-234 m . Более стабильный изотоп протактиния, 231 Pa, был открыт в 1917/18 годах Лизой Мейтнер в сотрудничестве с Отто Ганом , и они назвали элемент протактинием. [8] В 1949 году ИЮПАК выбрал название «протактиний» и подтвердил, что Ган и Мейтнер являются его первооткрывателями. Новое название означало «(ядерный) предшественник актиния », [9] предполагая, что актиний является продуктом радиоактивного распада протактиния. Джон Арнольд Крэнстон (работая с Фредериком Содди и Адой Хитчинс ) также считается первооткрывателем самого стабильного изотопа в 1915 году, но он отложил свое заявление из-за призыва на службу во время Первой мировой войны . [10]
Самый долгоживущий и самый распространенный (почти 100%) встречающийся в природе изотоп протактиния, протактиний-231, имеет период полураспада 32 760 лет и является продуктом распада урана-235 . Гораздо меньшие следовые количества короткоживущего протактиния-234 и его ядерного изомера протактиния-234m встречаются в цепочке распада урана-238 . Протактиний-233 возникает в результате распада тория -233 как часть цепочки событий, необходимых для получения урана-233 путем нейтронного облучения тория-232. Он является нежелательным промежуточным продуктом в ядерных реакторах на основе тория и поэтому удаляется из активной зоны реактора в процессе воспроизводства. Наука об океане использует этот элемент для понимания географии древнего океана. Анализ относительных концентраций различных изотопов урана, тория и протактиния в воде и минералах используется при радиометрическом датировании отложений возрастом до 175 000 лет и при моделировании различных геологических процессов. [11]

В 1871 году Дмитрий Менделеев предсказал существование элемента между торием и ураном . [12] В то время ряд актиноидов был неизвестен, поэтому Менделеев поместил уран под вольфрамом в группе VI, а торий под цирконием в группе IV, оставив пространство под танталом в группе V пустым. До всеобщего принятия концепции актиноидов в конце 1940-х годов периодические таблицы публиковались с этой структурой. [13] Долгое время химики искали эка -тантал [примечание 1] как элемент с химическими свойствами, схожими с танталом, что сделало открытие протактиния практически невозможным. Позднее было обнаружено, что более тяжелым аналогом тантала является трансурановый элемент дубний , хотя дубний химически более похож на протактиний, а не на тантал. [14]
В 1900 году Уильям Крукс выделил протактиний как чрезвычайно радиоактивный материал из урана; однако он не смог охарактеризовать его как новый химический элемент и поэтому назвал его ураном X (UX). [12] [15] [16] Крукс растворил нитрат урана в эфире , и остаточная водная фаза содержала большую часть234
90Чт
и234
91Па
. Его метод использовался в 1950-х годах для выделения234
90Чт
и234
91Па
из соединений урана. [17] Протактиний был впервые обнаружен в 1913 году, когда Казимир Фаянс и Освальд Хельмут Геринг столкнулись с изотопом 234m Pa во время своих исследований цепочек распада урана-238 :238
92У
→234
90Чт
→234м
91Па
→234
92У
Они назвали новый элемент « бревиум » (от латинского слова brevis , что означает краткий или короткий) из-за короткого периода полураспада, составляющего 1,16 минуты для234м
91Па
(уран X2). [18] [19] [20] [21] [22] [23] В 1917–18 годах две группы ученых, Лиза Мейтнер в сотрудничестве с Отто Ганом из Германии и Фредериком Содди и Джоном Крэнстоном из Великобритании , независимо друг от друга открыли другой изотоп, 231 Pa, имеющий гораздо более длительный период полураспада — 32 760 лет. [8] [22] [24] Мейтнер изменила название «бревиум» на протактиний, поскольку новый элемент был частью цепочки распада урана-235 как родителя актиния (от греч . πρῶτος prôtos , что означает «первый, прежде»). [25] ИЮПАК подтвердил это наименование в 1949 году. [26] [27] Открытие протактиния заполнило один из последних пробелов в ранних версиях периодической таблицы и принесло известность ученым, принимавшим в нем участие. [ 28]
Аристид фон Гроссе получил 2 миллиграмма Pa 2 O 5 в 1927 году [29], а в 1934 году впервые выделил элементарный протактиний из 0,1 миллиграмма Pa 2 O 5 . [30] Он использовал две разные процедуры: в первой оксид протактиния облучался электронами с энергией 35 кэВ в вакууме. В другой, называемой процессом Ван Аркеля–де Бура , оксид химически превращался в галогенид ( хлорид , бромид или иодид ) , а затем восстанавливался в вакууме с помощью электрически нагретой металлической нити: [26] [31]
В 1961 году Управление по атомной энергии Соединенного Королевства (UKAEA) произвело 127 граммов 99,9% чистого протактиния-231 путем переработки 60 тонн отходов в 12-этапном процессе стоимостью около 500 000 долларов США. [26] [32] В течение многих лет это была единственная в мире значительная поставка протактиния, которая предоставлялась различным лабораториям для научных исследований. [12] Национальная лаборатория Ок-Ридж в США поставляла протактиний по цене около 280 долларов США/грамм. [33]
Было обнаружено двадцать девять радиоизотопов протактиния. Наиболее стабильными являются 231 Pa с периодом полураспада 32 760 лет [34], 233 Pa с периодом полураспада 27 дней и 230 Pa с периодом полураспада 17,4 дня. Все остальные изотопы имеют период полураспада короче 1,6 дня, и большинство из них имеют период полураспада менее 1,8 секунды. Протактиний также имеет два ядерных изомера , 217m Pa (период полураспада 1,2 миллисекунды) и 234m Pa (период полураспада 1,16 минуты). [35]
Основной режим распада для самого стабильного изотопа 231 Pa и более легких ( 211 Pa до 231 Pa) — это альфа-распад , производящий изотопы актиния . Основной режим для более тяжелых изотопов ( 232 Pa до 239 Pa) — это бета-распад , производящий изотопы урана . [35]
Самый долгоживущий и самый распространенный изотоп, 231 Pa, может делиться от быстрых нейтронов, превышающих ~1 МэВ. [36] 233 Pa, другой изотоп протактиния, производимый в ядерных реакторах, также имеет порог деления 1 МэВ. [37]
Протактиний — один из самых редких и дорогих элементов природного происхождения. Он встречается в виде двух изотопов — 231 Pa и 234 Pa, причем изотоп 234 Pa находится в двух различных энергетических состояниях. Почти весь природный протактиний — это протактиний-231. Он является альфа-излучателем и образуется при распаде урана-235, тогда как бета-излучающий протактиний-234 образуется в результате распада урана-238 . Почти весь уран-238 (99,8%) сначала распадается на более короткоживущий изомер 234m Pa. [38]
Протактиний встречается в уранините (урановой смолке) в концентрациях около 0,3-3 частей 231 Pa на миллион частей (ppm) руды. [12] В то время как обычное содержание ближе к 0,3 ppm [39] (например, в Яхимове , Чешская Республика [40] ), некоторые руды из Демократической Республики Конго содержат около 3 ppm. [26] Протактиний однородно распределен в большинстве природных материалов и в воде, но в гораздо более низких концентрациях, порядка одной части на триллион, что соответствует радиоактивности 0,1 пикокюри (пКи)/г. В песчаных частицах почвы содержится примерно в 500 раз больше протактиния, чем в воде, даже по сравнению с водой, присутствующей в том же образце почвы. Гораздо более высокие соотношения 2000 и выше измерены в суглинистых почвах и глинах, таких как бентонит . [38] [41]
Два основных изотопа протактиния, 231 Pa и 233 Pa, производятся из тория в ядерных реакторах ; оба нежелательны и обычно удаляются, тем самым усложняя конструкцию и эксплуатацию реактора. В частности, 232 Th посредством реакций ( n , 2 n ) производит 231 Th, который быстро распадается до 231 Pa (период полураспада 25,5 часов). Последний изотоп, хотя и не является трансурановыми отходами, имеет длительный период полураспада 32 760 лет и вносит основной вклад в долгосрочную радиотоксичность отработанного ядерного топлива. [42]
Протактиний-233 образуется при захвате нейтрона 232Th . Он либо далее распадается до урана-233, либо захватывает другой нейтрон и превращается в неделящийся уран-234. [43] 233Pa имеет относительно длительный период полураспада 27 дней и высокое сечение захвата нейтронов (так называемый « нейтронный яд »). Таким образом, вместо быстрого распада до полезного 233U , значительная часть 233Pa преобразуется в неделящиеся изотопы и потребляет нейтроны, снижая эффективность реактора . Чтобы ограничить потерю нейтронов, 233Pa извлекается из активной зоны реакторов на расплавленных солях тория во время их работы, так что он может распадаться только до 233U . Извлечение 233Pa достигается с помощью колонн расплавленного висмута с растворенным в нем литием. Короче говоря, литий селективно восстанавливает соли протактиния до металлического протактиния, который затем извлекается из цикла расплавленной соли, в то время как расплавленный висмут является всего лишь носителем, выбранным из-за его низкой температуры плавления 271 °C, низкого давления паров, хорошей растворимости для лития и актинидов и несмешиваемости с расплавленными галогенидами . [42]

До появления ядерных реакторов протактиний выделялся для научных экспериментов из урановых руд. С тех пор как реакторы стали более распространенными, он в основном производится как промежуточный продукт ядерного деления в реакторах ториевого топливного цикла как промежуточный продукт в производстве делящегося урана-233:
Изотоп 231 Pa можно получить, облучая торий-230 медленными нейтронами , превращая его в бета-распадающийся торий-231; или облучая торий-232 быстрыми нейтронами, получая торий-231 и 2 нейтрона.
Металлический протактиний может быть получен восстановлением его фторида кальцием , [44] литием или барием при температуре 1300–1400 °C. [45] [ 46]
Протактиний — актиноид , расположенный в периодической таблице слева от урана и справа от тория , и многие его физические свойства являются промежуточными между соседними актиноидами. Протактиний плотнее и жёстче, чем торий, но легче урана; его температура плавления ниже, чем у тория, но выше, чем у урана. Тепловое расширение, электро- и теплопроводность этих трёх элементов сопоставимы и типичны для постпереходных металлов . Оценочный модуль сдвига протактиния аналогичен модулю сдвига титана . [47] Протактиний — металл с серебристо-серым блеском, который сохраняется некоторое время на воздухе. [26] [32] Протактиний легко реагирует с кислородом, водяным паром и кислотами, но не со щелочами. [12]
При комнатной температуре протактиний кристаллизуется в объемно-центрированной тетрагональной структуре, которую можно рассматривать как искаженную объемно-центрированную кубическую решетку; эта структура не изменяется при сжатии до 53 ГПа. Структура изменяется на гранецентрированную кубическую ( ГЦК ) при охлаждении от высокой температуры, около 1200 °C. [44] [48] Коэффициент теплового расширения тетрагональной фазы между комнатной температурой и 700 °C составляет 9,9 × 10−6 /°С. [44]
Протактиний парамагнитен , и для него не известны магнитные переходы ни при какой температуре. [49] Он становится сверхпроводящим при температурах ниже 1,4 К. [12] [45] Тетрахлорид протактиния парамагнитен при комнатной температуре, но становится ферромагнитным при охлаждении до 182 К. [50]
Протактиний существует в двух основных степенях окисления : +4 и +5, как в твердых телах, так и в растворах; и состояния +3 и +2, которые наблюдались в некоторых твердых телах. Поскольку электронная конфигурация нейтрального атома - [Rn]5f 2 6d 1 7s 2 , степень окисления +5 соответствует низкоэнергетической (и, следовательно, предпочтительной) конфигурации 5f 0 . Оба состояния +4 и +5 легко образуют гидроксиды в воде, причем преобладающими ионами являются Pa(OH) 3+ , Pa(OH)2+2, Па(ОН)+3, и Pa(OH) 4 , все из которых бесцветны. [51] Другие известные ионы протактиния включают PaCl2+2, ПаСО2+4, ПаФ 3+ , ПаФ2+2, ПаФ−6, ПаФ2−7, и ПаФ3−8. [52] [53]
Здесь a , b и c — постоянные решетки в пикометрах, No — номер пространственной группы, а Z — число формульных единиц на элементарную ячейку ; fcc обозначает гранецентрированную кубическую симметрию. Плотность не измерялась напрямую, а рассчитывалась из параметров решетки.
Оксиды протактиния известны по степеням окисления металлов +2, +4 и +5. Наиболее стабильным является белый пентоксид Pa2O5 , который может быть получен путем прокаливания гидроксида протактиния(V) на воздухе при температуре 500 °C. [ 61] Его кристаллическая структура кубическая, а химический состав часто нестехиометрический, описываемый как PaO2.25 . Также сообщалось о другой фазе этого оксида с орторомбической симметрией. [46] [62] Черный диоксид PaO2 получают из пентоксида путем восстановления его при 1550 °C водородом. Он плохо растворяется ни в разбавленной, ни в концентрированной азотной , соляной или серной кислоте , но легко растворяется в плавиковой кислоте . [46] Диоксид можно преобразовать обратно в пентоксид путем нагревания в кислородсодержащей атмосфере до 1100 °C. [62] Монооксид PaO наблюдался только в виде тонкого покрытия на металлическом протактинии, но не в изолированной объемной форме. [46]
Протактиний образует смешанные бинарные оксиды с различными металлами. Со щелочными металлами A кристаллы имеют химическую формулу APaO 3 и структуру перовскита ; A 3 PaO 4 и искаженную структуру каменной соли; или A 7 PaO 6 , где атомы кислорода образуют гексагональную плотноупакованную решетку. Во всех этих материалах ионы протактиния октаэдрически координированы. [63] [64] Пентоксид Pa 2 O 5 соединяется с оксидами редкоземельных металлов R 2 O 3 , образуя различные нестехиометрические смешанные оксиды, также имеющие структуру перовскита. [65]
Оксиды протактиния являются основными ; они легко превращаются в гидроксиды и могут образовывать различные соли, такие как сульфаты , фосфаты , нитраты и т. д. Нитрат обычно белый, но может быть коричневым из-за радиолитического разложения. Нагревание нитрата на воздухе при 400 °C преобразует его в белый пентаоксид протактиния. [66] Политриоксофосфат Pa(PO3 ) 4 может быть получен путем реакции дифторидсульфата PaF2SO4 с фосфорной кислотой ( H3PO4 ) в инертной атмосфере. Нагревание продукта примерно до 900 ° C устраняет побочные продукты реакции, которые включают плавиковую кислоту , триоксид серы и фосфорный ангидрид . Нагревание его до более высоких температур в инертной атмосфере разлагает Pa(PO3 ) 4 в дифосфат PaP2O7 , который аналогичен дифосфатам других актинидов. В дифосфате группы PO 3 образуют пирамиды симметрии C 2v . Нагревание PaP 2 O 7 на воздухе до 1400 °C разлагает его на пентаоксиды фосфора и протактиния. [59]
Фторид протактиния(V) образует белые кристаллы, в которых ионы протактиния расположены в пентагональных бипирамидах и координируются 7 другими ионами. Координация та же самая в хлориде протактиния(V), но цвет желтый. Координация меняется на октаэдрическую в коричневом бромиде протактиния(V), но неизвестна для иодида протактиния(V). Координация протактиния во всех его тетрагалогенидах равна 8, но расположение является квадратным антипризматическим во фториде протактиния(IV) и додекаэдрическим в хлориде и бромиде. Сообщалось о коричневом иодиде протактиния(III), в котором ионы протактиния координируются 8 в двушапочной тригональной призматической компоновке. [67]

Фторид протактиния(V) и хлорид протактиния(V) имеют полимерную структуру моноклинной симметрии. Там, в пределах одной полимерной цепи, все атомы галогенидов лежат в одной графитоподобной плоскости и образуют плоские пентагоны вокруг ионов протактиния. 7-координация протактиния происходит от пяти атомов галогенидов и двух связей с атомами протактиния, принадлежащих соседним цепям. Эти соединения легко гидролизуются в воде. [68] Пентахлорид плавится при 300 °C и сублимируется при еще более низких температурах.
Фторид протактиния(V) может быть получен путем реакции оксида протактиния с пентафторидом брома или трифторидом брома при температуре около 600 °C, а фторид протактиния(IV) получается из оксида и смеси водорода и фторида водорода при температуре 600 °C; для удаления утечек атмосферного кислорода в реакцию требуется большой избыток водорода. [46]
Хлорид протактиния(V) получают путем реакции оксида протактиния с четыреххлористым углеродом при температурах 200–300 °C. [46] Побочные продукты (такие как PaOCl 3 ) удаляют фракционной сублимацией. [57] Восстановление хлорида протактиния(V) водородом при температуре около 800 °C дает хлорид протактиния(IV) — желто-зеленое твердое вещество, которое сублимируется в вакууме при 400 °C. Его также можно получить непосредственно из диоксида протактиния путем обработки его четыреххлористым углеродом при 400 °C. [46]
Бромиды протактиния получаются при воздействии бромида алюминия , бромистого водорода , тетрабромида углерода или смеси бромистого водорода и тионилбромида на оксид протактиния. Альтернативно их можно получить путем реакции пентахлорида протактиния с бромистым водородом или тионилбромидом. [46] Бромид протактиния(V) имеет две похожие моноклинные формы: одну получают путем сублимации при 400–410 °C, а другую — путем сублимации при несколько более низкой температуре 390–400 °C. [56] [58]
Иодиды протактиния могут быть получены путем реакции металлического протактиния с элементарным иодом при 600 °C и путем реакции Pa 2 O 5 с AlO 3 при 600 °C. [46] Иодид протактиния(III) может быть получен путем нагревания иодида протактиния(V) в вакууме. [68] Как и в случае с оксидами, протактиний образует смешанные галогениды со щелочными металлами. Наиболее примечательным среди них является Na 3 PaF 8 , где ион протактиния симметрично окружен 8 ионами F − , образуя почти идеальный куб. [52]
Известны также более сложные фториды протактиния, такие как Pa2F9 [ 68 ] и тройные фториды типов MPaF6 ( M = Li, Na, K, Rb, Cs или NH4 ), M2PaF7 (M = K, Rb, Cs или NH4) и M3PaF8 ( M = Li , Na , Rb, Cs), все из которых представляют собой белые кристаллические твердые вещества. Формула MPaF6 может быть представлена как комбинация MF и PaF5 . Эти соединения могут быть получены путем испарения раствора плавиковой кислоты, содержащего оба комплекса. Для небольших щелочных катионов, таких как Na, кристаллическая структура является тетрагональной, тогда как для более крупных катионов K + , Rb + , Cs + или NH4 + она становится орторомбической . Аналогичное изменение наблюдалось для фторидов M 2 PaF 7 : а именно, симметрия кристалла зависела от катиона и различалась для Cs 2 PaF 7 и M 2 PaF 7 (M = K, Rb или NH 4 ). [53]
Известны оксигалогениды и оксисульфиды протактиния. PaOBr 3 имеет моноклинную структуру, состоящую из двухцепочечных единиц, где протактиний имеет координацию 7 и организован в пентагональные бипирамиды. Цепи связаны между собой через атомы кислорода и брома, и каждый атом кислорода связан с тремя атомами протактиния. [56] PaOS — это светло-желтое нелетучее твердое вещество с кубической кристаллической решеткой, изоструктурной решетке других оксисульфидов актинидов. Он получается путем реакции хлорида протактиния(V) со смесью сероводорода и сероуглерода при 900 °C. [46]
В гидридах и нитридах протактиний имеет низкую степень окисления около +3. Гидрид получается прямым действием водорода на металл при 250 °C, а нитрид является продуктом аммиака и тетрахлорида или пентахлорида протактиния. Это ярко-желтое твердое вещество термически стабильно до 800 °C в вакууме. Карбид протактиния (PaC) образуется путем восстановления тетрафторида протактиния барием в углеродном тигле при температуре около 1400 °C. [46] Протактиний образует борогидриды , в состав которых входит Pa(BH 4 ) 4 . Он имеет необычную полимерную структуру со спиральными цепями, где атом протактиния имеет координационное число 12 и окружен шестью ионами BH 4 − . [69]
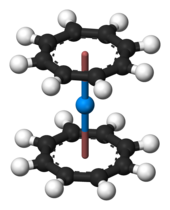
Протактиний(IV) образует тетраэдрический комплекс тетракис(циклопентадиенил)протактиний(IV) (или Pa(C 5 H 5 ) 4 ) с четырьмя циклопентадиенильными кольцами, которые можно синтезировать путем реакции хлорида протактиния(IV) с расплавленным Be(C 5 H 5 ) 2 . Одно кольцо может быть замещено атомом галогенида. [70] Другим металлоорганическим комплексом является золотисто-желтый бис(π-циклооктатетраен)протактиний, или протактиноцен (Pa(C 8 H 8 ) 2 ), который по структуре аналогичен ураноцену . Там атом металла зажат между двумя циклооктатетраеновыми лигандами. Подобно ураноцену, его можно получить путем реакции тетрахлорида протактиния с дикалийциклооктатетраенидом ( K 2 C 8 H 8 ) в тетрагидрофуране . [60]
Хотя протактиний расположен в периодической таблице между ураном и торием, оба из которых имеют многочисленные применения, в настоящее время протактиний не находит применения за пределами научных исследований из-за его редкости, высокой радиоактивности и высокой токсичности. [38]
Протактиний-231 возникает естественным образом при распаде природного урана-235, а также искусственно в ядерных реакторах в результате реакции 232 Th + n → 231 Th + 2n и последующего бета-распада 231 Th . Когда-то считалось, что он способен поддерживать ядерную цепную реакцию, которая в принципе может быть использована для создания ядерного оружия ; физик Вальтер Зейфриц однажды оценил связанную с этим критическую массу как750 ± 180 кг . [71] Однако возможность критичности 231 Па с тех пор была исключена. [36] [72]
С появлением высокочувствительных масс-спектрометров стало возможным применение 231 Pa в качестве трассера в геологии и палеоокеанографии . В этом применении отношение протактиния-231 к торию-230 используется для радиометрического датирования осадков возрастом до 175 000 лет и для моделирования образования минералов. [39] В частности, его оценка в океанических отложениях помогла реконструировать движения водоемов Северной Атлантики во время последнего таяния ледников ледникового периода . [73] Некоторые из вариаций датирования, связанных с протактинием, основаны на анализе относительных концентраций нескольких долгоживущих членов цепи распада урана — например, урана, протактиния и тория. Эти элементы имеют 6, 5 и 4 валентных электрона, что благоприятствует состояниям окисления +6, +5 и +4 соответственно, и демонстрируют различные физические и химические свойства. Торий и протактиний, но не соединения урана, плохо растворимы в водных растворах и выпадают в осадок; скорость осаждения для тория выше, чем для протактиния. Анализ концентрации как для протактиния-231 (период полураспада 32 760 лет), так и для тория-230 (период полураспада 75 380 лет) повышает точность измерений по сравнению с измерением только одного изотопа; этот метод двойных изотопов также слабо чувствителен к неоднородностям в пространственном распределении изотопов и к изменениям в скорости их осаждения. [39] [74]
Протактиний является одновременно токсичным и высокорадиоактивным; поэтому с ним работают исключительно в герметичном перчаточном боксе . Его основной изотоп 231 Pa имеет удельную активность 0,048 кюри (1,8 ГБк ) на грамм и в основном испускает альфа-частицы с энергией 5 МэВ, которые могут быть остановлены тонким слоем любого материала. Однако он медленно распадается, с периодом полураспада 32 760 лет, в 227 Ac, который имеет удельную активность 74 кюри (2700 ГБк) на грамм, испускает как альфа-, так и бета-излучение и имеет гораздо более короткий период полураспада 22 года. 227 Ac, в свою очередь, распадается на более легкие изотопы с еще более короткими периодами полураспада и гораздо большей удельной активностью (SA). [38]
Поскольку протактиний присутствует в небольших количествах в большинстве натуральных продуктов и материалов, он попадает в организм с пищей или водой и вдыхается с воздухом. Только около 0,05% потребленного протактиния всасывается в кровь, а остальное выводится. Из крови около 40% протактиния откладывается в костях, около 15% поступает в печень, 2% в почки, а остальное выводится из организма. Биологический период полураспада протактиния составляет около 50 лет в костях, тогда как его биологический период полураспада в других органах имеет быструю и медленную составляющую. Например, 70% протактиния в печени имеют биологический период полураспада 10 дней, а остальные 30% — 60 дней. Соответствующие значения для почек составляют 20% (10 дней) и 80% (60 дней). В каждом пораженном органе протактиний способствует развитию рака посредством своей радиоактивности. [38] [66] Максимальная безопасная доза Pa в организме человека составляет 0,03 мкКи (1,1 кБк), что соответствует 0,5 микрограммам 231 Pa. [75] Максимально допустимая концентрация 231 Pa в воздухе в Германии составляет3 × 10−4 Бк / м 3 . [66]
происходит от греческого слова protos (что означает «первый») и элемента актиний, поскольку протактиний является предшественником актиния.
В этот момент Фаянс отозвал название brevium, поскольку принято было называть элемент по самому долгоживущему изотопу. Затем Мейтнер выбрала название protactinium.