Гепатотоксичность (от hepatic toxicity ) подразумевает химическое повреждение печени . Лекарственное поражение печени (ЛПП) является причиной острого и хронического заболевания печени, вызванного, в частности, лекарствами, и наиболее распространенной причиной отзыва препарата с рынка после одобрения.
Печень играет центральную роль в преобразовании и очистке химических веществ и восприимчива к токсичности этих агентов. Некоторые лекарственные средства при приеме в передозировках (например, ацетаминофен, парацетамол ), а иногда даже при введении в терапевтических пределах (например, галотан ), могут повредить орган. Другие химические вещества, такие как те, что используются в лабораториях и промышленности, природные химикаты (например, альфа-аманитин ) и растительные лекарственные средства (два ярких примера — кава , хотя причинный механизм неизвестен, и окопник , из-за содержания пирролизидиновых алкалоидов) также могут вызывать гепатотоксичность. Химические вещества, вызывающие повреждение печени, называются гепатотоксинами .
Более 900 препаратов были замешаны в поражении печени [1] (см. LiverTox, внешняя ссылка, ниже), и это самая распространенная причина отзыва препарата с рынка. Гепатотоксичность и вызванное лекарствами поражение печени также являются причиной значительного числа неудачных соединений, что подчеркивает необходимость моделей прогнозирования токсичности (например, DTI), [2] и анализов скрининга лекарств, таких как гепатоцитоподобные клетки, полученные из стволовых клеток , которые способны обнаруживать токсичность на ранних стадиях процесса разработки препарата . [3] Химические вещества часто вызывают субклиническое повреждение печени, которое проявляется только в виде аномальных результатов тестов на печеночные ферменты .
Повреждения печени, вызванные лекарственными средствами, являются причиной 5% всех госпитализаций и 50% всех случаев острой печеночной недостаточности . [4] [5]
Неблагоприятные реакции на лекарства классифицируются как тип А (внутренние или фармакологические) или тип В (идиосинкразические). [6] На долю реакций на лекарства типа А приходится 80% всех токсичностей. [7]
Лекарства или токсины, которые имеют фармакологическую (тип А) гепатотоксичность, — это те, которые имеют предсказуемые кривые доза-реакция (более высокие концентрации вызывают большее повреждение печени) и хорошо описанные механизмы токсичности, такие как прямое повреждение ткани печени или блокирование метаболического процесса. Как и в случае передозировки парацетамола , этот тип повреждения возникает вскоре после достижения некоторого порога токсичности. Четыреххлористый углерод обычно используется для того, чтобы вызвать острое повреждение печени типа А в моделях животных.
Идиосинкразическое (тип B) поражение происходит без предупреждения, когда агенты вызывают непредсказуемую гепатотоксичность у восприимчивых лиц, которая не связана с дозой и имеет переменный латентный период. [8] Этот тип поражения не имеет четкой зависимости доза-реакция или временной связи, и чаще всего не имеет прогностических моделей. Идиосинкразическое поражение печени привело к отзыву нескольких препаратов с рынка даже после строгих клинических испытаний в рамках процесса одобрения FDA; Троглитазон (Резулин) [2] [9] и тровафлоксацин (Трован) являются двумя яркими примерами идиосинкразических гепатотоксинов, снятых с рынка.
Трава кава стала причиной ряда случаев идиосинкразического поражения печени, варьирующихся от бессимптомных до смертельных.
Пероральное применение противогрибкового препарата кетоконазол было связано с гепатотоксичностью, включая несколько случаев со смертельным исходом; [10] однако такие эффекты, по-видимому, ограничиваются дозами, принимаемыми в течение периода более 7 дней. [11]
Парацетамол, также известный как ацетаминофен, и под торговыми марками Tylenol и Panadol, обычно хорошо переносится в назначенной дозе, но передозировка является наиболее распространенной причиной лекарственно-индуцированных заболеваний печени и острой печеночной недостаточности во всем мире. [12] Повреждение печени вызвано не самим препаратом, а токсичным метаболитом ( N -ацетил- p -бензохинонимин (NAPQI)), вырабатываемым ферментами цитохрома P-450 в печени. [13] В нормальных условиях этот метаболит детоксицируется путем конъюгации с глутатионом в реакции фазы 2. При передозировке образуется большое количество NAPQI, что подавляет процесс детоксикации и приводит к повреждению клеток печени. Оксид азота также играет роль в индуцировании токсичности. [14] Риск повреждения печени зависит от нескольких факторов, включая принятую дозу, сопутствующий прием алкоголя или других наркотиков, интервал между приемом и антидотом и т. д. Доза, токсичная для печени, довольно сильно варьируется от человека к человеку и часто считается более низкой у хронических алкоголиков. [15] [16] Измерение уровня в крови важно для оценки прогноза, более высокие уровни предсказывают худший прогноз. Введение ацетилцистеина , предшественника глутатиона, может ограничить тяжесть повреждения печени, захватывая токсичный NAPQI. Те, у кого развивается острая печеночная недостаточность , все еще могут выздороветь спонтанно, но могут потребовать трансплантации, если присутствуют плохие прогностические признаки, такие как энцефалопатия или коагулопатия (см. Критерии Королевского колледжа ). [17]
Хотя отдельные анальгетики редко вызывают повреждение печени из-за их широкого применения, НПВП стали основной группой препаратов, проявляющих гепатотоксичность. Были зарегистрированы как дозозависимые, так и идиосинкразические реакции. [18] Аспирин и фенилбутазон связаны с внутренней гепатотоксичностью; идиосинкразическая реакция была связана с ибупрофеном, сулиндаком, фенилбутазоном, пироксикамом, диклофенаком и индометацином.
Глюкокортикоиды так названы из-за их влияния на углеводный механизм. Они способствуют накоплению гликогена в печени. Увеличение печени является редким побочным эффектом длительного использования стероидов у детей. [19] Классический эффект длительного использования как у взрослых, так и у детей — стеатоз . [20]
Изониазид (INH) является одним из наиболее часто используемых препаратов для лечения туберкулеза ; он связан с небольшим повышением уровня печеночных ферментов у 20% пациентов и тяжелой гепатотоксичностью у 1-2% пациентов. [21]
Также известны случаи, когда другие производные гидразина , такие как антидепрессант ИМАО ипрониазид , связаны с повреждением печени. [22] [23] Фенелзин был связан с аномальными результатами печеночных тестов. [24] Токсические эффекты могут развиться из-за антибиотиков. [25]

Примерами служат грибы, содержащие альфа-аманитин , кава и плесень, производящая афлатоксин. Пирролизидиновые алкалоиды , которые встречаются в некоторых растениях, могут быть токсичными. [26] [27] Экстракт зеленого чая становится все более частой причиной печеночной недостаточности из-за его включения во все большее количество продуктов. [28] [29] [30]
Примеры включают: плоды аки , бацзяолян , камфара , копалтра, цикасин , гарциния , [31] листья кавы , пирролизидиновые алкалоиды , листья конского каштана , валериана , окопник . [32] [33] Китайские травяные средства: Цзинь Бу Хуань, эфедра , Шоу Ву Пянь , Бай Сянь Пи . [34] [35]
Примерами являются мышьяк , четыреххлористый углерод и винилхлорид . [36]
Лекарства продолжают снимать с рынка из-за позднего обнаружения гепатотоксичности. Из-за своего уникального метаболизма и тесной связи с желудочно-кишечным трактом печень подвержена повреждениям от лекарств и других веществ. 75% крови, поступающей в печень, поступает непосредственно из желудочно-кишечных органов и селезенки через воротные вены , которые доставляют лекарства и ксенобиотики в почти неразбавленной форме. Несколько механизмов ответственны либо за повреждение печени, либо за ухудшение процесса повреждения.
Многие химические вещества повреждают митохондрии , внутриклеточные органеллы, которые вырабатывают энергию. Их дисфункция высвобождает избыточное количество окислителей, которые, в свою очередь, повреждают клетки печени. Активация некоторых ферментов в системе цитохрома P-450, таких как CYP2E1, также приводит к окислительному стрессу. [37] Повреждение гепатоцитов и клеток желчных протоков приводит к накоплению желчной кислоты внутри печени . Это способствует дальнейшему повреждению печени. [38] Непаренхиматозные клетки, такие как клетки Купфера , коллаген-продуцирующие звездчатые клетки и лейкоциты (т. е. нейтрофилы и моноциты ) также играют роль в этом механизме.
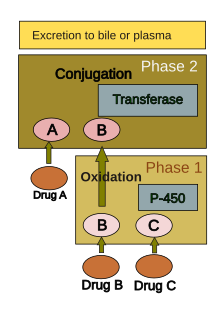
Человеческое тело подвергает большинство, но не все, соединений различным химическим процессам (то есть метаболизму ), чтобы сделать их пригодными для выведения. Это включает в себя химические преобразования для (a) снижения растворимости жира и (b) изменения биологической активности. Хотя почти все ткани в организме обладают некоторой способностью метаболизировать химические вещества, гладкий эндоплазматический ретикулум в печени является основным «метаболическим клиринговым центром» как для эндогенных химических веществ (например, холестерина , стероидных гормонов, жирных кислот , белков ), так и для экзогенных веществ (например, наркотиков, алкоголя). [39] Центральная роль, которую печень играет в очистке и преобразовании химических веществ, делает ее восприимчивой к лекарственным повреждениям.
Метаболизм лекарств обычно делится на две фазы: фазу 1 и фазу 2. Реакция фазы 1, как правило, предназначена для подготовки лекарства к фазе 2. Однако многие соединения могут метаболизироваться фазой 2 напрямую или выводиться без каких-либо реакций фазы 2. Реакция фазы 1 включает окисление , восстановление , гидролиз , гидратацию и многие другие редкие химические реакции. Эти процессы, как правило, увеличивают растворимость лекарства в воде и могут генерировать метаболиты, которые являются более химически активными и/или потенциально токсичными. Большинство реакций фазы 2 происходят в цитозоле и включают конъюгацию с эндогенными соединениями через ферменты трансферазы . Фаза 1, как правило, более подходит для элиминации.
Группа ферментов, расположенных в эндоплазматическом ретикулуме, известная как цитохром P-450 , является наиболее важным семейством метаболизирующих ферментов в печени. Цитохром P-450 не является одним ферментом, а скорее состоит из тесно связанного семейства из 50 изоформ ; шесть из них метаболизируют 90% лекарств. [40] [41] Существует огромное разнообразие индивидуальных продуктов гена P-450, и эта гетерогенность позволяет печени выполнять окисление огромного количества химических веществ (включая большинство лекарств) в фазе 1. Три важные характеристики системы P-450 играют роль в токсичности, вызванной лекарствами:
Каждый из белков P-450 уникален и отвечает (в некоторой степени) за различия в метаболизме лекарств между людьми. Генетические вариации ( полиморфизм ) в метаболизме P-450 следует учитывать, когда пациенты проявляют необычную чувствительность или устойчивость к эффектам лекарств в обычных дозах. Такой полиморфизм также отвечает за различную реакцию на лекарства среди пациентов разного этнического происхождения.
Многие вещества могут влиять на механизм фермента P-450. Лекарственные препараты взаимодействуют с семейством ферментов несколькими способами. [44] Лекарственные препараты, которые модифицируют фермент цитохрома P-450, называются либо ингибиторами, либо индукторами. Ингибиторы ферментов блокируют метаболическую активность одного или нескольких ферментов P-450. Этот эффект обычно проявляется немедленно. С другой стороны, индукторы повышают активность P-450, увеличивая выработку фермента или, в случае CYP2E1, предотвращая деградацию в протеасоме . Обычно существует задержка перед увеличением активности фермента. [41]
Некоторые препараты могут иметь одинаковую специфичность P-450 и, таким образом, конкурентно блокировать их биотрансформацию. Это может привести к накоплению препаратов, метаболизируемых ферментом. Этот тип взаимодействия препаратов может также снизить скорость образования токсичных метаболитов.
Химические вещества вызывают широкий спектр клинических и патологических повреждений печени. Биохимические маркеры (например, аланинтрансфераза , щелочная фосфатаза и билирубин ) часто используются для определения повреждения печени. Повреждение печени определяется как повышение либо (a) уровня АЛТ более чем в три раза от верхней границы нормы (ВГН), (b) уровня ЩФ более чем в два раза от ВГН, или (c) уровня общего билирубина более чем в два раза от ВГН, когда оно связано с повышением АЛТ или ЩФ. [45] [46] Повреждение печени далее характеризуется как гепатоцеллюлярный (преимущественно начальное повышение аланинтрансферазы ) и холестатический (начальное повышение щелочной фосфатазы) типы. Однако они не являются взаимоисключающими, и часто встречаются смешанные типы повреждений.
Ниже обсуждаются конкретные гистопатологические закономерности поражения печени, вызванного лекарственными средствами.
Это наиболее распространенный тип некроза клеток печени, вызванного лекарственными средствами , при котором повреждение в значительной степени ограничивается определенной зоной печеночной дольки . Он может проявляться в виде очень высокого уровня АЛТ и тяжелого нарушения функции печени, приводящего к острой печеночной недостаточности .
В этой модели гепатоцеллюлярный некроз связан с инфильтрацией воспалительных клеток. Может быть три типа лекарственного гепатита. (A) вирусный гепатит является наиболее распространенным, при котором гистологические признаки схожи с острым вирусным гепатитом. (B) при очаговом или неспецифическом гепатите рассеянные очаги клеточного некроза могут сопровождать лимфоцитарную инфильтрацию. (C) хронический гепатит очень похож на аутоиммунный гепатит клинически, серологически и гистологически.
Повреждение печени приводит к нарушению оттока желчи, и в большинстве случаев наблюдаются зуд и желтуха. Гистология может показать воспаление (холестатический гепатит) или оно может быть невыраженным (без паренхиматозного воспаления). В редких случаях могут наблюдаться признаки, похожие на первичный билиарный цирроз из-за прогрессирующего разрушения мелких желчных протоков ( синдром исчезающего протока ).
Гепатотоксичность может проявляться накоплением триглицеридов, что приводит к мелкокапельной (микровезикулярной) или крупнокапельной (макровезикулярной) жировой печени. Существует отдельный тип стеатоза, при котором накопление фосфолипидов приводит к картине, схожей с заболеваниями с наследственными дефектами метаболизма фосфолипидов (например, болезнь Тея-Сакса ).
Лекарственные гранулемы печени обычно связаны с гранулемами в других тканях, и у пациентов обычно наблюдаются признаки системного васкулита и гиперчувствительности. Было выявлено более 50 лекарственных препаратов.
Они возникают в результате повреждения эндотелия сосудов.
Были описаны новообразования при длительном воздействии некоторых лекарств или токсинов. Обычно сообщалось о гепатоцеллюлярной карциноме, ангиосаркоме и аденомах печени.

Это остается проблемой в клинической практике из-за отсутствия надежных маркеров. [47] Многие другие состояния приводят к схожим клиническим и патологическим картинам. Для диагностики гепатотоксичности необходимо установить причинно-следственную связь между использованием токсина или препарата и последующим повреждением печени, но это может быть сложно, особенно если подозревается идиосинкразическая реакция. [48] Одновременное использование нескольких препаратов может усложнить ситуацию. Как и в случае с токсичностью ацетаминофена, хорошо установленную, дозозависимую, фармакологическую гепатотоксичность легче обнаружить. Было предложено несколько клинических шкал, таких как шкала CIOMS /RUCAM и критерии Maria и Victorino, для установления причинно-следственной связи между препаратом, вызывающим заболевание, и повреждением печени. Шкала CIOMS/RUCAM включает в себя систему оценок, которая классифицирует подозрение как «определенное или высоко вероятное» (балл > 8), «вероятное» (балл 6–8), «возможное» (балл 3–5), «маловероятное» (балл 1–2) и «исключенное» (балл ≤ 0). В клинической практике врачи уделяют больше внимания наличию или отсутствию сходства между биохимическим профилем пациента и известным биохимическим профилем предполагаемой токсичности (например, холестатическое повреждение при амоксициллин-клавоновой кислоте ). [47]
В большинстве случаев функция печени возвращается к норме, если прием препарата, вызывающего заболевание, прекращается на ранней стадии. Кроме того, пациенту может потребоваться поддерживающее лечение. Однако при отравлении ацетаминофеном начальный инсульт может оказаться фатальным. Молниеносная печеночная недостаточность из-за гепатотоксичности, вызванной лекарственными средствами, может потребовать трансплантации печени. В прошлом применялись глюкокортикоиды при аллергических проявлениях и урсодезоксихолевая кислота при холестатических случаях, но нет убедительных доказательств, подтверждающих их эффективность. [ необходима цитата ]
Повышение уровня билирубина в сыворотке более чем в 2 раза от верхней границы нормы с сопутствующим повышением трансаминазы является зловещим признаком. Это указывает на тяжелую гепатотоксичность и, вероятно, приведет к смерти у 10% - 15% пациентов, особенно если не прекратить прием вызывающего заболевание препарата ( закон Хай ). [49] [50] Это связано с тем, что для нарушения выведения билирубина требуется значительное повреждение печени, поэтому незначительное нарушение (при отсутствии обструкции желчных протоков или синдрома Жильбера ) не приведет к желтухе. Другими плохими предикторами исхода являются пожилой возраст, женский пол, высокий уровень АСТ . [51] [52]
Следующие терапевтические препараты были отозваны с рынка в первую очередь из-за гепатотоксичности: троглитазон , бромфенак , тровафлоксацин , эбротидин , нимесулид , нефазодон , ксимелагатран и пемолин . [47] [53] [54]