Лептоспироз — инфекция крови , вызываемая бактериями Leptospira [8] , которая может инфицировать человека, собак, грызунов и многих других диких и домашних животных. [8] Признаки и симптомы могут варьироваться от отсутствия до легких ( головные боли , мышечные боли и лихорадка ) до тяжелых ( легочное кровотечение или менингит ). [5] Болезнь Вейля ( / ˈ v aɪ l z / VILES ), [12] острая, тяжелая форма лептоспироза, вызывает у инфицированного человека желтуху ( кожа и глаза становятся желтыми), развивается почечная недостаточность и кровотечение. [6] Легочное кровотечение, связанное с лептоспирозом, известно как синдром тяжелого легочного кровотечения . [5]
Более десяти генетических типов лептоспир вызывают заболевания у человека. [13] Распространителями болезни могут быть как дикие, так и домашние животные, чаще всего грызуны. [8] Бактерии передаются человеку через мочу или фекалии животных , а также воду или почву, загрязненную мочой и фекалиями животных, при попадании в глаза, рот, нос или через повреждения кожи. [8] В развивающихся странах заболевание чаще всего встречается у фермеров, занимающихся борьбой с вредителями, и у людей с низкими доходами, которые живут в районах с плохими санитарными условиями. [5] В развитых странах это происходит во время сильных ливней и представляет опасность для специалистов по борьбе с вредителями, работников канализации [14] и тех, кто занимается активным отдыхом в теплых и влажных районах. [5] Диагноз обычно ставится путем тестирования на антитела против бактерий или обнаружения бактериальной ДНК в крови. [5]
Усилия по предотвращению заболевания включают защитное оборудование для блокировки контакта при работе с потенциально зараженными животными, мытье после контакта и сокращение количества грызунов в районах, где живут и работают люди. [7] Антибиотик доксициклин эффективен для предотвращения заражения лептоспирозом. [7] Человеческие вакцины имеют ограниченную полезность; [15] вакцины для других животных более доступны. [16] Лечение при инфицировании проводится антибиотиками, такими как доксициклин, пенициллин или цефтриаксон . [8] Общий риск смерти составляет 5–10%. [10] Однако при поражении легких риск смерти увеличивается до 50–70%. [8]
По оценкам, каждый год у людей возникает один миллион тяжелых случаев лептоспироза, вызывающих около 58 900 смертей. [11] Заболевание наиболее распространено в тропических регионах мира, но может возникнуть где угодно. [7] Вспышки могут возникнуть после сильных дождей. [7] Заболевание впервые описал врач Адольф Вейль в 1886 году в Германии. [17] [18] Зараженные животные могут не иметь легких или тяжелых симптомов. [19] Они могут различаться в зависимости от типа животного. [16] [19] У некоторых животных лептоспиры живут в репродуктивных путях, что приводит к передаче инфекции во время спаривания. [16]


Симптомы лептоспироза обычно появляются через одну-две недели после заражения [7] , но инкубационный период может достигать месяца. [21] В большинстве симптоматических случаев заболевание носит двухфазный характер . Симптомы первой фазы (острой или лептоспиремической фазы) длятся пять-семь дней. На второй фазе (иммунная фаза) симптомы исчезают по мере выработки антител против бактерий. [8] На втором этапе развиваются дополнительные симптомы. [22] Фазы заболевания могут быть нечеткими, особенно у пациентов с тяжелым заболеванием. [23] У 90% инфицированных наблюдаются легкие симптомы, а у 10% - тяжелая форма лептоспироза. [24]
Лептоспиральная инфекция у людей вызывает ряд симптомов , хотя у некоторых инфицированных людей их может не быть. Заболевание начинается внезапно с лихорадки, сопровождающейся ознобом, сильной головной болью, сильными мышечными болями и болями в животе. [5] [21] Головная боль, вызванная лептоспирозом, вызывает пульсирующую боль и обычно локализуется в двусторонних височных или лобных областях головы . У человека также может быть боль за глазами и повышенная чувствительность к свету . Мышечная боль обычно затрагивает икроножную мышцу и поясницу. Наиболее характерным признаком лептоспироза является выпот конъюнктивы ( конъюнктивит без экссудата ), который редко встречается при других лихорадочных заболеваниях. Другие характерные изменения на глазах включают субконъюнктивальное кровотечение и желтуху . Сыпь при лептоспирозе встречается редко. При обнаружении такого заболевания следует рассмотреть альтернативные диагнозы, такие как лихорадка денге и лихорадка чикунгунья . Сухой кашель наблюдается у 20–57% больных лептоспирозом. Таким образом, эта клиническая особенность может ввести врача в заблуждение и диагностировать заболевание как респираторное заболевание. Кроме того, часто возникают желудочно-кишечные симптомы, такие как тошнота , рвота, боль в животе и диарея. Рвота и диарея могут способствовать обезвоживанию . Боль в животе может быть следствием бескалькулезного холецистита или воспаления поджелудочной железы . [21] Редко лимфатические узлы , печень и селезенка могут быть увеличены и пальпироваться. [8]
Симптомы исчезнут в течение одного-трех дней. [7] После этого начинается иммунная фаза, которая может длиться от четырех до 30 дней и может быть любой: от осложнений со стороны мозга до почек. [25] Отличительной чертой второй фазы является воспаление оболочек, покрывающих мозг . [7] Признаки и симптомы менингита включают сильную головную боль и ригидность шеи. [7] Поражение почек связано со снижением или отсутствием диуреза. [7]
Классическая форма тяжелого лептоспироза, известная как болезнь Вейля, характеризуется поражением печени (вызывающим желтуху), почечной недостаточностью и кровотечением, которое случается у 5–10% инфицированных. [7] Также может произойти повреждение легких и головного мозга. У тех, у кого есть признаки воспаления оболочек, покрывающих мозг и сам мозг , может произойти изменение уровня сознания . Осложнениями являются различные неврологические проблемы, такие как паралич половины тела , полное воспаление всего горизонтального отдела спинного мозга и синдром Гийена-Барре . Также могут быть обнаружены такие признаки кровотечения, как петехии , экхимозы , носовые кровотечения , черноватый стул из-за желудочного кровотечения , рвота с кровью и кровотечение из легких . Удлинение протромбинового времени при коагуляционном тесте связано с проявлением выраженного кровотечения. Однако низкое количество тромбоцитов не связано с тяжелым кровотечением. [21] Легочное кровотечение – это альвеолярное кровотечение (кровотечение в альвеолы легких), приводящее к массивному кашлю с кровью и вызывающее острый респираторный дистресс-синдром , при котором риск смерти составляет более 50%. [21] Редко могут возникать воспаление сердечных мышц , воспаление оболочек, покрывающих сердце , нарушения естественного водителя ритма сердца и аномальные сердечные ритмы . [8]
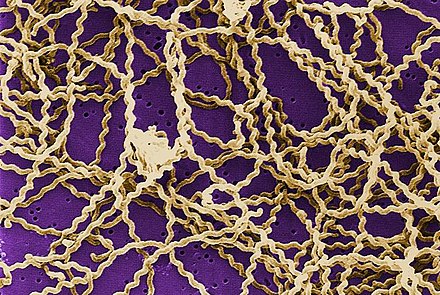
Лептоспироз вызывают бактерии -спирохеты , принадлежащие к роду Leptospira , которые являются аэробными , [8] правоспиральными , [13] и длиной 6–20 микрометров . [7] Как и грамотрицательные бактерии, лептоспиры имеют внешнюю мембрану , покрытую липополисахаридом (ЛПС) на поверхности, внутреннюю мембрану и слой пептидогликановой клеточной стенки. Однако в отличие от грамотрицательных бактерий слой пептидогликана у лептоспир лежит ближе к внутренней, чем к внешней мембране. В результате образуется жидкая внешняя мембрана, слабо связанная с клеточной стенкой. [26] Кроме того, у Leptospira есть жгутик, расположенный в периплазме , связанный с движением в виде штопора. [7] Хеморецепторы на полюсах бактерий воспринимают различные субстраты и меняют направление их движения. [13] Бактерии традиционно визуализируются с помощью темнопольной микроскопии без окрашивания. [7]
Всего идентифицировано 66 видов лептоспир . В зависимости от их геномной последовательности они делятся на две клады и четыре субклада: P1, P2, S1 и S2. [27] 19 членов субклада P1 включают 8 видов, которые могут вызывать тяжелые заболевания у человека: L. alexanderi , L. borgpetersenii , L. interrogans , L. kirschneri , L. mayottensis , L. noguchii , L. santarosai , и L. weilii . [13] [27] Клада P2 включает 21 вид, которые могут вызывать легкие заболевания у людей. Остальные 26 видов составляют субклады S1 и S2, в которые входят «сапрофиты», которые, как известно, потребляют разлагающиеся вещества ( сапротрофное питание ). [27] Патогенные лептоспиры не размножаются в окружающей среде. Лептоспирам для выживания требуется высокая влажность, но они могут оставаться живыми в такой среде, как стоячая вода или загрязненная почва. Бактерию можно убить при температуре 50 °C (122 °F) и инактивировать 70% этанолом , 1% гипохлоритом натрия , формальдегидом , моющими средствами и кислотами. [28]
Лептоспиры также классифицируются на основе их серовара . Разнообразный сахарный состав липополисахарида на поверхности бактерий ответственен за антигенное различие между сероварами. [13] Выявлено около 300 патогенных сероваров лептоспир . Антигенно родственные серовары (принадлежащие к одной и той же серогруппе) могут принадлежать разным видам из-за горизонтального переноса генов биосинтеза ЛПС между разными видами. В настоящее время для классификации видов Leptospira используются тест перекрестной агглютинации и гибридизация ДНК-ДНК , но они отнимают много времени. Таким образом, полное геномное секвенирование потенциально может заменить эти два метода в качестве нового золотого стандарта классификации видов Leptospira . [13]

Бактерии можно найти в прудах, реках, лужах, канализации, сельскохозяйственных полях и влажной почве. [7] Патогенные лептоспиры были обнаружены в форме водных биопленок , которые могут способствовать выживанию в окружающей среде. [29]
Число случаев лептоспироза напрямую связано с количеством осадков, что делает заболевание сезонным в умеренном климате и круглогодичным в тропическом климате. [7] Риск заражения лептоспирозом зависит от риска носительства заболевания в обществе и частоты заражения. [21] В сельской местности основными факторами риска заражения лептоспирозом являются сельское хозяйство и животноводство. [5] Плохое жилье и неадекватные санитарные условия также повышают риск заражения. [21] В тропических и субтропических регионах болезнь часто распространяется после проливных дождей или после наводнений. [7]
Лептоспиры встречаются преимущественно у млекопитающих. [5] Однако было доказано, что рептилии и хладнокровные животные, такие как лягушки, змеи, черепахи и жабы, могут заразиться этой инфекцией. [16] Существуют ли резервуары заражения человека, неизвестно. [21] [16] Крысы, мыши и кроты являются важными первичными хозяевами , но другие млекопитающие, включая собак, оленей, кроликов, ежей, коров, овец, свиней, енотов, опоссумов и скунсов, также могут переносить болезнь. [16] В Африке переносчиками инфекции были идентифицированы несколько диких животных, включая полосатого мангуста , египетскую лисицу , русанского оленя и землероек . [30] Существуют различные механизмы, с помощью которых животные могут заражать друг друга. Собаки могут слизывать мочу зараженного животного с травы или почвы или пить из зараженной лужи. Домашние собаки, находящиеся в доме, заразились лептоспирозом, по-видимому, из-за того, что слизывали мочу инфицированных мышей в доме. [31] Лептоспироз также может передаваться через сперму инфицированных животных. [16] Бактерии, постоянно присутствующие в моче животных, могут сохраняться годами. [16]
Человек является случайным хозяином лептоспиры . [5] Люди заражаются при контакте с водой или влажной почвой, содержащей мочу и фекалии инфицированных животных. [7] Бактерии проникают через порезы, ссадины, [7] проглатывание зараженной пищи или контакт со слизистыми оболочками тела (например, рта, носа и глаз). [32] К профессиям, подверженным риску заражения лептоспирозом, относятся фермеры, рыбаки, сборщики мусора и работники канализации. [5] Заболевание также связано с приключенческим туризмом и развлекательной деятельностью. [5] Это распространено среди любителей водных видов спорта в определенных областях, включая триатлон , рафтинг , греблю на каноэ и плавание, поскольку длительное погружение в воду способствует проникновению бактерий. [5] Однако Leptospira вряд ли проникнут через неповрежденную кожу. [8] Не известно, как заболевание распространяется между людьми, а распространение бактерий в период выздоровления у людей встречается крайне редко. [8] После заражения человека выделение бактерий из почек обычно сохраняется до 60 дней. [28]
В редких случаях лептоспироз может передаваться при трансплантации органов. [33] Также возможно заражение через плаценту во время беременности. [34] [35] [36] Это может вызвать выкидыш и инфекцию у младенцев . [37] Также сообщалось о передаче лептоспироза при употреблении в пищу сырого мяса диких животных (например, у психиатрических пациентов с аллотриофагией). [38]

Когда животные проглатывают бактерии, они циркулируют в кровотоке, а затем попадают в почки через клубочковые или перитубулярные капилляры . Затем бактерии проникают в просвет почечных канальцев и колонизируют щеточную кайму и проксимальные извитые канальцы . Это приводит к непрерывному выделению бактерий с мочой, при этом животное не испытывает серьезных побочных эффектов. Эти отношения между животным и бактериями известны как комменсальные отношения , а животное известно как резервуар-хозяин . [21]
Человек является случайным хозяином лептоспиры . [5] Патогенез лептоспироза остается плохо изученным, несмотря на усилия исследователей. [7] [32] Бактерии попадают в организм человека через повреждения кожи или слизистой оболочки, а затем в кровоток. Позже бактерии прикрепляются к эндотелиальным клеткам кровеносных сосудов и внеклеточному матриксу (сложная сеть белков и углеводов, присутствующая между клетками). Бактерии используют свои жгутики для перемещения между слоями клеток. Они связываются с такими клетками, как фибробласты , макрофаги , эндотелиальные клетки и эпителиальные клетки почек. Они также связываются с некоторыми белками человека, такими как белки комплемента, тромбин , фибриноген и плазминоген, используя поверхностные лептоспиральные иммуноглобулиноподобные (Lig) белки, такие как LigB и LipL32, гены которых обнаружены у всех патогенных видов. [13] [32]
Благодаря врожденной иммунной системе эндотелиальные клетки капилляров в организме человека активируются присутствием этих бактерий. Эндотелиальные клетки вырабатывают цитокины и антимикробные пептиды против бактерий. Эти продукты регулируют каскад свертывания крови и движение лейкоцитов. [13] Макрофаги, присутствующие у человека, способны поглощать Leptospira . Однако лептоспиры способны жить и размножаться в цитоплазматическом матриксе после попадания в организм макрофагов. [13] У людей с тяжелым лептоспирозом может наблюдаться высокий уровень цитокинов, таких как интерлейкин 6 , фактор некроза опухоли альфа (TNF-α) и интерлейкин 10 . Высокий уровень цитокинов вызывает симптомы, подобные сепсису , которые опасны для жизни, вместо того, чтобы помочь бороться с инфекцией. [24] У тех, кто имеет высокий риск сепсиса во время инфекции лептоспироза, обнаруживается генотип HLA-DQ6 , возможно, из-за активации суперантигена , который повреждает органы тела. [21]
ЛПС Leptospira активирует только толл-подобный рецептор 2 (TLR2) в моноцитах человека. Молекула липида А бактерий не распознается рецепторами TLR4 человека . Таким образом, отсутствие распознавания Leptospira рецепторами TLR4, вероятно, способствует процессу заболевания лептоспирозом у человека. [13]
Хотя в человеческом организме существуют различные механизмы борьбы с бактериями, лептоспира хорошо адаптирована к такому воспалительному состоянию, которое она вызывает. В кровотоке он может активировать плазминоген хозяина, превращая его в плазмин , который разрушает внеклеточный матрикс, разрушает сгустки фибрина и комплементарные белки ( C3b и C5 ), чтобы избежать опсонизации . Он также может рекрутировать регуляторы комплемента, такие как фактор H , C4b -связывающий белок, фактор H-подобный связывающий белок и витронектин , чтобы предотвратить активацию мембраноатакующего комплекса на его поверхности. Он также секретирует протеазы для разрушения белков комплемента, таких как C3 . Он может связываться с тромбином, который уменьшает образование фибрина. Снижение образования фибрина увеличивает риск кровотечений. [13] Leptospira также секретирует сфингомиелиназу и гемолизин , которые воздействуют на эритроциты. [7]
Лептоспира быстро распространяется во все органы через кровоток. [13] В основном они поражают печень. Они проникают в пространство между гепатоцитами , вызывая апоптоз. Поврежденные гепатоциты и межклеточные соединения гепатоцитов вызывают утечку желчи в кровоток, вызывая повышение уровня билирубина , что приводит к желтухе. Сообщалось о перегруженности синусоидов печени и перисинусоидальных пространств . В то же время в легких в области альвеолярной перегородки и промежутков между альвеолами можно обнаружить петехии или явные кровотечения . [21] Leptospira выделяет токсины, которые вызывают легкую или тяжелую почечную недостаточность или интерстициальный нефрит . [32] Почечная недостаточность может полностью восстановиться или привести к атрофии и фиброзу . [21] Редко выявляют воспаление сердечных мышц, коронарных артерий и аорты . [25]


У инфицированных общий анализ крови может показать высокое количество лейкоцитов и низкое количество тромбоцитов. Когда низкий уровень гемоглобина сочетается с низким количеством лейкоцитов и тромбоцитопенией , следует рассмотреть возможность подавления костного мозга . [21] Скорость оседания эритроцитов и уровень С-реактивного белка также могут быть повышены. [8]
При лептоспирозе обычно поражаются почки. Уровни мочевины и креатинина в крови будут повышены. Лептоспироз увеличивает экскрецию калия с мочой, что приводит к низкому уровню калия [21] и низкому уровню натрия в крови. [8] [21] Анализ мочи может выявить наличие белка , лейкоцитов и микроскопическую гематурию . [8] Поскольку бактерии оседают в почках, посев мочи будет положительным на лептоспироз, начиная со второй недели болезни и до 30 дней после заражения. [8]
У пациентов с поражением печени в тестах функции печени повышены трансаминазы и прямой билирубин . Серогруппа Icterohaemorragiae связана с желтухой и повышенным уровнем билирубина. Гемолитическая анемия способствует развитию желтухи. Особенностью лептоспироза является острая гемолитическая анемия и конъюгированная гипербилирубинемия, особенно у больных с дефицитом глюкозо-6-фосфатдегидрогеназы . [21] Аномальные уровни сывороточной амилазы и липазы (связанные с панкреатитом) обнаруживаются у тех, кто поступает в больницу из-за лептоспироза. Нарушение функции почек с клиренсом креатинина менее 50 мл/мин связано с повышенным уровнем ферментов поджелудочной железы. [21]
Тем, у кого сильная головная боль и имеются признаки менингита, можно сделать люмбальную пункцию . В случае заражения исследование спинномозговой жидкости (СМЖ) показывает преобладание лимфоцитов с количеством клеток около 500/мм 3 , содержанием белка от 50 до 100 мг/мл и нормальным уровнем глюкозы. Эти данные согласуются с асептическим менингитом . [21]
Быстрое обнаружение лептоспир можно провести путем количественного определения антител IgM с помощью иммуноферментного анализа (ИФА) . Обычно для обнаружения антител IgM используется антиген L. biflexa . Этот тест позволяет быстро определить диагноз и помочь в раннем лечении. Однако специфичность теста зависит от типа используемого антигена и наличия антител от предыдущих инфекций. Наличие других заболеваний, таких как вирусная инфекция Эпштейна-Барра , вирусный гепатит и цитомегаловирусная инфекция, может привести к ложноположительным результатам. [21] Были разработаны и другие быстрые скрининговые тесты, такие как тесты с тест-полосками, латексные тесты и тесты агглютинации на предметных стеклах. [8]
Микроскопическая реакция агглютинации (МАТ) является эталонным тестом для диагностики лептоспироза. [21] MAT – это тест, в котором серийные разведения сыворотки пациентов смешиваются с различными сероварами Leptospira . Затем смесь исследуют под темнопольным микроскопом на предмет агглютинации . Результатом является наибольшее разведение, при котором происходит 50% агглютинация. [21] Титры MAT от 1:100 до 1:800 являются диагностическими показателями лептоспироза. [8] Четырехкратное или более увеличение титра двух сывороток, взятых при появлении симптомов и через 3-10 дней от начала заболевания, подтверждает диагноз. Во время острой фазы заболевания МАТ неспецифичен для выявления серотипа лептоспир из-за перекрестной реактивности между сероварами. [21] В фазе выздоровления МАТ более специфичен для выявления типов сероваров. [21] MAT требует панели живых антигенов и требует кропотливой работы. [25]
Лептоспиральную ДНК можно амплифицировать с помощью полимеразной цепной реакции (ПЦР) из сыворотки, мочи, водянистой жидкости , спинномозговой жидкости и аутопсийных образцов. [21] Он обнаруживает присутствие бактерий быстрее, чем MAT, в течение первых нескольких дней заражения, не дожидаясь появления антител. [25] Поскольку ПЦР обнаруживает наличие лептоспиральной ДНК в крови, она полезна даже тогда, когда бактерии уничтожаются антибиотиками. [39]
У пациентов с поражением легких рентгенография грудной клетки может выявить диффузные альвеолярные помутнения. [21]
В 1982 году Всемирная организация здравоохранения (ВОЗ) предложила критерии Фейна для диагностики лептоспироза. Он состоит из трех частей: А (клинические данные), Б (эпидемиологические факторы) и С (лабораторные и бактериологические данные). Поскольку первоначальные критерии Фейна включали только культуру и МАТ в части C, что сложно и сложно выполнить, в 2004 году были предложены модифицированные критерии Фейна, включающие ИФА и тесты агглютинации на предметных стеклах, которые легче выполнить. В 2012 году были предложены модифицированные критерии Фейна (с поправками), включающие в диагноз одышку и кашель с кровью. В 2013 году Индия рекомендовала модифицированные критерии Фейна для диагностики лептоспироза. [40]


Уровень заболеваемости лептоспирозом можно снизить за счет улучшения жилищных, инфраструктурных и санитарных стандартов. Усилия по борьбе с грызунами и проекты по смягчению последствий наводнений также могут помочь предотвратить это. [21] Правильное использование средств индивидуальной защиты (СИЗ) людьми с высоким риском профессионального заражения может в большинстве случаев предотвратить заражение лептоспирозом. [21]
Не существует вакцины для человека, подходящей для использования во всем мире. [15] Лишь несколько стран, таких как Куба, Япония, Франция и Китай, одобрили использование инактивированных вакцин с ограниченным защитным эффектом. [15] [41] После введения вакцины сообщалось о таких побочных эффектах, как тошнота, покраснение и отек в месте инъекции . Поскольку иммунитет, индуцируемый одним сероваром Leptospira , защищает только от этого конкретного серовара, были разработаны трехвалентные вакцины. [21] Однако они не дают длительного иммунитета людям или животным. [13] Вакцины для других животных более доступны. [16]
Доксициклин назначается один раз в неделю в качестве профилактики и эффективен для снижения уровня заражения лептоспирозом среди лиц из группы высокого риска в районах, подверженных наводнениям. [42] Согласно данным одного исследования, он снизил количество случаев заболевания лептоспирозом у военнослужащих, проходящих учения в джунглях. В другом исследовании это уменьшило количество симптоматических случаев после заражения лептоспирозом во время сильных дождей в эндемичных районах. [21]
Профилактика лептоспироза из источников окружающей среды, таких как загрязненные водные пути, почва, канализация и сельскохозяйственные поля, представляет собой дезинфекцию, используемую эффективными микроорганизмами , которые смешиваются с комками грязи бокаши для зараженных водных путей и канализации.
Большинство случаев лептоспиралей разрешаются спонтанно. Раннее начало приема антибиотиков может предотвратить прогрессирование заболевания в тяжелую форму. Таким образом, в условиях ограниченных ресурсов прием антибиотиков можно начинать при подозрении на лептоспироз после сбора анамнеза и обследования. [21]
При легком лептоспирозе рекомендации по назначению антибиотиков, таких как доксициклин, азитромицин , ампициллин и амоксициллин , основывались исключительно на результатах испытаний in vitro . [8] В 2001 году ВОЗ рекомендовала пероральный доксициклин (от 2 до 100 мг каждые 12 часов) в течение пяти-семи дней людям с легкой формой лептоспироза. В таких случаях также можно использовать тетрациклин , ампициллин и амоксициллин. [43] Однако в районах, где риккетсии и лептоспироз являются эндемичными, препаратами выбора являются азитромицин и доксициклин. [8] Доксициклин не используется в случаях, когда пациент страдает повреждением печени, поскольку оно связано с гепатотоксичностью. [44]
На основании исследования 1988 года для лечения тяжелого лептоспироза рекомендуется внутривенное введение бензилпенициллина ( также известного как пенициллин G). [8] Бензилпенициллин внутривенно (30 мг/кг до 1,2 г каждые шесть часов) применяют в течение пяти-семи дней. В тяжелых случаях также можно использовать амоксициллин, ампициллин и эритромицин. [43] Цефтриаксон (1 г внутривенно каждые 24 часа в течение семи дней) также эффективен при тяжелом лептоспирозе. [21] [8] [45] Цефотаксим (1 г внутривенно каждые шесть часов в течение семи дней) и доксициклин (первоначально 200 мг, затем по 100 мг внутривенно каждые 12 часов в течение семи дней) столь же эффективны, как и бензилпенициллин (1,5 миллиона единиц внутривенно каждые сутки). шесть часов в течение семи дней). [8] [46] Таким образом, нет данных о различиях в снижении смертности при сравнении бензилпенициллина с цефтриаксоном или цефотаксимом. [8] Другое исследование, проведенное в 2007 году, также не выявило различий в эффективности между доксициклином (первоначально 200 мг, затем по 100 мг перорально каждые 12 часов в течение семи дней) и азитромицином (2 г в первый день, затем по 1 г ежедневно в течение еще двух дней). при подозрении на лептоспироз. Разницы в уменьшении лихорадки не было, а азитромицин переносится лучше, чем доксициклин. [47] [48] [49]
Амбулаторным пациентам назначают доксициклин или азитромицин. Доксициклин может сократить продолжительность лептоспироза на два дня, улучшить симптомы и предотвратить выделение микроорганизмов с мочой. Азитромицин и амоксициллин назначают беременным женщинам и детям. [21] В редких случаях реакция Яриша-Герксхаймера может развиться в первые несколько часов после введения антибиотика. [8] Однако, согласно метаанализу, проведенному в 2012 году, польза антибиотиков при лечении лептоспироза была неясной, хотя использование антибиотиков может сократить продолжительность болезни на два-четыре дня. [8] [48] Другой метаанализ, проведенный в 2013 году, пришел к аналогичному выводу. [8] [49]
У пациентов с тяжелым лептоспирозом, в том числе с потерей калия и нарушением функции почек, внутривенная гидратация и добавки калия могут предотвратить обезвоживание и гипокалиемию . При возникновении острой почечной недостаточности раннее начало гемодиализа или перитонеального диализа может помочь улучшить выживаемость. У пациентов с дыхательной недостаточностью интубация трахеи с низким дыхательным объемом улучшает показатели выживаемости. [21]
Кортикостероиды были предложены для подавления воспаления при лептоспирозе, поскольку инфекция Leptospira может вызывать высвобождение химических сигналов , которые способствуют воспалению кровеносных сосудов в легких. Однако недостаточно доказательств, чтобы определить, полезно ли использование кортикостероидов. [8] [50]
Общий риск смерти от лептоспироза составляет 5–10%. [10] Для людей с желтухой летальность может увеличиться до 15%. [28] Для инфицированных, у которых наблюдается спутанность сознания и неврологические симптомы, существует высокий риск смерти. [21] Другие факторы, повышающие риск смерти, включают снижение диуреза, возраст старше 36 лет и дыхательную недостаточность. [21] При правильном уходе большинство инфицированных полностью выздоравливают. У людей с острой почечной недостаточностью после выздоровления может развиться стойкая легкая почечная недостаточность. [21] У пациентов с тяжелым поражением легких риск смерти составляет 50–70%. [8] Тридцать процентов людей с острым лептоспирозом жаловались на длительные симптомы, характеризующиеся слабостью, мышечными болями и головными болями. [21]
Проблемы с глазами могут возникнуть у 10% выздоровевших от лептоспироза [28] в период от двух недель до нескольких лет после заражения. Чаще всего осложнения со стороны глаз могут возникнуть через шесть месяцев после заражения. Это связано с иммунными привилегиями глаза, которые защищают его от иммунологического повреждения на начальной стадии лептоспиральной инфекции. [51] Эти осложнения могут варьироваться от легкого переднего увеита до тяжелого панувеита (поражающего все три слоя сосудов глаза). [28] Увеит чаще встречается у мужчин молодого и среднего возраста, а также у тех, кто работает в сельском хозяйстве. [51] До 80% инфицированных ДНК Leptospira можно обнаружить в водянистой влаге глаза. [21] Проблемы с глазами обычно имеют хороший прогноз после лечения или проходят самостоятельно. [28] При переднем увеите необходимы только топические стероиды и мидриатики (средства, вызывающие расширение зрачка), тогда как при панувеите требуются периокулярные кортикостероиды. [51] Лептоспиральный увеит характеризуется гипопионом , быстро созревающей катарактой , свободно плавающими оболочками стекловидного тела, гиперемией диска и васкулитом сетчатки . [51] [52] [53]

По оценкам, ежегодно происходит один миллион тяжелых случаев лептоспироза, при этом 58 900 человек погибают. Тяжелые случаи составляют 5–15% всех случаев лептоспироза. [11] Лептоспироз встречается как в городских, так и в сельских районах тропических , субтропических и умеренных регионов. [10] Глобальное бремя лептоспироза для здоровья можно измерить с помощью года жизни с поправкой на инвалидность (DALY). Этот показатель составляет 42 на 100 000 человек в год, что больше, чем при других заболеваниях, таких как бешенство и филяриатоз . [7]
Заболевание постоянно наблюдается в некоторых частях Азии, Океании, Карибского бассейна, Латинской Америки и Африки. [28] Антарктида — единственное место, не пораженное лептоспирозом. [28] В Соединенных Штатах ежегодно регистрировалось от 100 до 150 случаев лептоспироза. [54] В 1994 году лептоспироз перестал быть болезнью, подлежащей регистрации в Соединенных Штатах, за исключением 36 штатов/территорий, где он распространен, таких как Гавайи, Техас, Калифорния и Пуэрто-Рико. [55] Около 50% зарегистрированных случаев произошли в Пуэрто-Рико. В январе 2013 года лептоспироз был восстановлен в качестве заболевания, подлежащего уведомлению на национальном уровне в США. [54] Исследования по эпидемиологии лептоспироза в группах высокого риска и факторах риска в Индии ограничены. [56]
Глобальные показатели заболеваемости лептоспирозом недооценены, поскольку в большинстве затронутых стран уведомление отсутствует или уведомление не является обязательным. [21] Другими проблемами являются отличие клинических признаков лептоспироза от других заболеваний и отсутствие лабораторной диагностики. [57] Социально-экономический статус значительной части населения мира тесно связан с недоеданием; последующий недостаток микроэлементов может привести к повышенному риску заражения и смерти из-за заражения лептоспирозом. [58] Микронутриенты, такие как железо , кальций и магний, представляют собой важные области для будущих исследований. [58]
Заболевание было впервые описано Адольфом Вейлем в 1886 году, когда он сообщил об «остром инфекционном заболевании с увеличением селезенки, желтухой и нефритом ». [18] До описания Вейля болезнь была известна как « желтуха рисового поля » в древнем китайском тексте, «осенняя лихорадка», «семидневная лихорадка» [59] и « лихорадка нанукаями » [60] в Японии; в Европе и Австралии болезнь ассоциировалась с определенными профессиями и получила такие названия, как «болезнь тростника», «болезнь свинопаса» и « Шламмфибер » (грязевая лихорадка). [59] Исторически она была известна как «черная желтуха» [61] или «лихорадка молочных ферм» в Новой Зеландии. [62] Лептоспироз был постулирован как причина эпидемии среди коренных американцев на побережье нынешней Новой Англии в 1616–1619 годах. Заболевание, скорее всего, было занесено в Новый Свет европейцами. [63]
Leptospira впервые была обнаружена в 1907 году в посмертном срезе ткани почки Артуром Стимсоном с использованием техники окрашивания отложениями серебра . Он назвал этот организм Spirocheta interrogans, потому что бактерии напоминали вопросительный знак. [59] [64] В 1908 году японская исследовательская группа под руководством Рюкичи Инада и Ютаки Ито впервые идентифицировала эту бактерию как возбудителя лептоспироза [65] и отметила ее присутствие у крыс в 1916 году. [66] Японские рабочие угольных шахт часто заразился лептоспирозом. В Японии организм получил название Spirocheta icterohaemorragiae . Японская группа также экспериментировала с первыми исследованиями лептоспиральной иммунизации на морских свинках. Они продемонстрировали, что путем инъекции инфицированным морским свинкам сыворотки выздоравливающих людей или коз можно обеспечить пассивный иммунитет морским свинкам. В 1917 году японская группа обнаружила крыс как переносчиков лептоспироза. [59] Не зная о работе японской группы, две немецкие группы независимо и почти одновременно опубликовали свою первую демонстрацию передачи лептоспиральной инфекции на морских свинках в октябре 1915 года. Они назвали организм Spirochaeta nodosa и Spirochaeta Icterogenes соответственно. [59]
Впоследствии лептоспироз был признан заболеванием всех видов млекопитающих. В 1933 году голландские рабочие сообщили об выделении Leptospira canicola , которая поражает исключительно собак. В 1940 г. в России впервые был зарегистрирован штамм, специфически поражающий крупный рогатый скот. [59] В 1942 году у солдат в Форт-Брэгге , Северная Каролина , было зафиксировано инфекционное заболевание, вызвавшее сыпь на голенях . Позже стало известно, что это заболевание вызвано лептоспирозом. [21] К 1950-м годам число сероваров, инфицирующих различных млекопитающих, значительно увеличилось. В 1980-х годах лептоспироз был признан ветеринарным заболеванием, имеющим большое экономическое значение. [59]
В 1982 г. для классификации было доступно около 200 сероваров лептоспир . Подкомитет Международного комитета систематической бактериологии по таксономии лептоспир предложил разделить эти серовары на две большие группы: L. interrogans , содержащие патогенные серовары, и L. biflexa , содержащие сапрофитные серовары. [59] В 1979 году было предложено лептоспиральное семейство Leptospiraceae . В том же году Leptospira illini была реклассифицирована в новый род Leptonema . [59] В 2002 году был придуман «синдром Лептангамуши» для описания ряда перекрывающихся симптомов лептоспироза, хантавирусной геморрагической лихорадки с почечным синдромом и сыпного тифа , вызываемого Orientia tsutsugamushi . [67] [68] В 2005 году Leptospira parva была классифицирована как Turneriella . [59] С помощью технологии гибридизации ДНК-ДНК L. interrogans была разделена на семь видов. С тех пор было обнаружено больше видов Leptospira . [59] ВОЗ создала Справочную группу по эпидемиологии бремени лептоспироза (LERG) для анализа последних эпидемиологических данных о лептоспирозе, формулирования модели передачи заболевания и выявления пробелов в знаниях и исследованиях. Первое совещание было созвано в 2009 году. По оценкам LERG, в 2011 году ежегодная заболеваемость лептоспирозом в мире составляет от пяти до 14 случаев на 100 000 населения. [21]


У инфицированных животных симптомы могут отсутствовать, иметь легкие или тяжелые симптомы; [19] симптомы могут варьироваться в зависимости от типа животного. [16] [19] У некоторых животных бактерии живут в репродуктивных путях, что приводит к передаче инфекции во время спаривания. [16]
Животные также имеют схожие клинические особенности по сравнению с людьми. Клинические признаки у собак могут появиться через 5–15 дней. Инкубационный период у кошек может затягиваться. Лептоспироз может вызывать аборты через 2–12 недель у крупного рогатого скота и через 1–4 недели после заражения у свиней. У резервуарных хозяев заболевание протекает мягче. Чаще всего поражаются почки, печень и репродуктивная система, но могут поражаться и другие органы. [28] У собак острые клинические признаки включают лихорадку, потерю аппетита , озноб, мышечные боли, слабость и симптомы мочеиспускания. Также могут наблюдаться рвота, диарея и боль в животе. На слизистых оболочках могут наблюдаться петехии и экхимозы. Кровотечение из легких также может наблюдаться у собак. При хронических проявлениях у пораженной собаки симптомы могут отсутствовать. У животных, погибших от лептоспироза, почки могут быть опухшими с серыми и белыми пятнами, крапчатостью или рубцеванием. Их печень может быть увеличена с участками гибели клеток . Петехии и экхимозы могут обнаруживаться в различных органах. [28] [69] Также возможны воспаление кровеносных сосудов , воспаление сердца, менингеальных оболочек, покрывающих головной и спинной мозг, и увеит . [16] Рецидивирующий увеит лошадей (ЭРУ) является наиболее распространенным заболеванием, связанным с инфекцией Leptospira у лошадей в Северной Америке, и может привести к слепоте. [70] [71] ERU представляет собой аутоиммунное заболевание, включающее антитела против белков LruA и LruB лептоспир , перекрестно реагирующих с белками глаза. [70] Живые лептоспиры могут быть выделены из водной жидкости или жидкости стекловидного тела многих лошадей с лептоспирами -ассоциированными ЕСВ. [71] Риск смерти или инвалидности у инфицированных животных варьируется в зависимости от вида и возраста животных. У взрослых свиней и крупного рогатого скота репродуктивные признаки являются наиболее распространенными признаками лептоспироза. До 40% коров могут иметь самопроизвольный аборт. У молодых животных заболевание обычно протекает более тяжело. Около 80% собак могут выжить при лечении, но выживаемость снижается, если поражаются легкие. [28]
Для диагностики лептоспироза у животных чаще всего используются ИФА и микроскопические реакции агглютинации. Бактерии можно обнаружить в крови, моче и молоке, а также в образцах печени, почек или других тканей с помощью методов иммунофлуоресценции , иммуногистохимии или полимеразной цепной реакции. Окрашивание серебром или иммунозолото-серебряное окрашивание используется для обнаружения Leptospira в срезах тканей. Организмы плохо окрашиваются красителем по Граму . Темнопольную микроскопию можно использовать для обнаружения Leptospira в жидкостях организма, но она не является ни чувствительной, ни специфичной для обнаружения микроорганизма. Положительный результат посева на лептоспироз является окончательным, но его доступность ограничена, а для получения результата посева может потребоваться 13–26 недель, что ограничивает его полезность. Для серологической диагностики лептоспироза у животных предпочтительны парные образцы в остром периоде и в период выздоровления. Положительный серологический образец абортированного плода также является диагностическим признаком лептоспироза. [28]
Для лечения лептоспироза у животных использовались различные антибиотики, такие как доксициклин, пенициллины, дигидрострептомицин и стрептомицин . При тяжелом течении заболевания может потребоваться инфузионная терапия, переливание крови и респираторная поддержка. Для лошадей с ЕСВ основное лечение проводится противовоспалительными препаратами. [28] [16]
Вакцины против лептоспироза доступны для таких животных, как свиньи, собаки, крупный рогатый скот, овцы и козы. Вакцины для крупного рогатого скота обычно содержат серовар Leptospira Hardjo и Pomona, для собак вакцины обычно содержат серовар Icterohaemorragiae и Canicola. Вакцины, содержащие несколько сероваров, не эффективны для крупного рогатого скота так же, как вакцины, содержащие один серовар, однако поливалентные вакцины продолжают продаваться. [16] Изоляция инфицированных животных и профилактическое назначение антибиотиков также эффективны для предотвращения передачи лептоспироза между животными. Экологический контроль и санитария также снижают скорость передачи инфекции. [28] [16]
![]() Эта статья была отправлена в WikiJournal of Medicine на внешнюю академическую рецензию в 2019 году (отчеты рецензентов). Обновленный контент был реинтегрирован на страницу Википедии по лицензии CC-BY-SA-3.0 ( 2022 г. ). Проверенная версия протокола: Сян Чинг Раймонд Чиенг; и другие. (21 июня 2022 г.). "Лептоспироз". Викижурнал медицины . 9 (1): 2. doi : 10.15347/WJM/2022.002 . ISSN 2002-4436. Викиданные Q100400590.
Эта статья была отправлена в WikiJournal of Medicine на внешнюю академическую рецензию в 2019 году (отчеты рецензентов). Обновленный контент был реинтегрирован на страницу Википедии по лицензии CC-BY-SA-3.0 ( 2022 г. ). Проверенная версия протокола: Сян Чинг Раймонд Чиенг; и другие. (21 июня 2022 г.). "Лептоспироз". Викижурнал медицины . 9 (1): 2. doi : 10.15347/WJM/2022.002 . ISSN 2002-4436. Викиданные Q100400590.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )