
Ингибитор фермента – это молекула , которая связывается с ферментом и блокирует его активность . Ферменты — белки , ускоряющие необходимые для жизни химические реакции , в которых молекулы субстрата превращаются в продукты . [1] Фермент облегчает конкретную химическую реакцию, связывая субстрат с его активным центром , специализированной областью фермента, которая ускоряет наиболее трудную стадию реакции .
Ингибитор фермента останавливает («ингибирует») этот процесс либо путем связывания с активным центром фермента (таким образом предотвращая связывание самого субстрата), либо путем связывания с другим участком фермента, так что катализ реакции ферментом блокируется . Ингибиторы ферментов могут связываться обратимо или необратимо. Необратимые ингибиторы образуют химическую связь с ферментом, так что фермент ингибируется до тех пор, пока химическая связь не будет разорвана. Напротив, обратимые ингибиторы связываются нековалентно и могут спонтанно покинуть фермент, позволяя ферменту возобновить свою функцию. Обратимые ингибиторы вызывают различные типы ингибирования в зависимости от того, связываются ли они с ферментом, комплексом фермент-субстрат или с обоими.
Ингибиторы ферментов играют важную роль во всех клетках, поскольку они обычно специфичны для каждого фермента и служат для контроля активности этого фермента. Например, ферменты метаболического пути могут ингибироваться молекулами, образующимися на более поздних стадиях этого пути, тем самым ограничивая выработку молекул, которые больше не нужны. Этот тип отрицательной обратной связи является важным способом поддержания баланса в клетке . [2] Ингибиторы ферментов также контролируют основные ферменты, такие как протеазы или нуклеазы , которые, если их не контролировать, могут повредить клетку. Многие яды, вырабатываемые животными и растениями, являются ингибиторами ферментов, которые блокируют активность важнейших ферментов у добычи или хищников .
Многие молекулы лекарств являются ингибиторами ферментов, которые ингибируют аберрантный человеческий фермент или фермент, критически важный для выживания патогена, такого как вирус , бактерия или паразит . Примеры включают метотрексат (используемый в химиотерапии и при лечении ревматического артрита ) и ингибиторы протеазы, используемые для лечения ВИЧ/СПИДа . Поскольку ингибиторы антипатогенов обычно нацелены только на один фермент, такие препараты высокоспецифичны и обычно вызывают мало побочных эффектов у людей, при условии, что у людей не обнаружено аналогичного фермента. (Это часто так, поскольку такие патогены и люди генетически далеки .) Лекарственные ингибиторы ферментов часто имеют низкие константы диссоциации , а это означает, что для ингибирования фермента требуется лишь незначительное количество ингибитора. Низкая концентрация ингибитора фермента снижает риск поражения печени и почек и других побочных реакций на лекарственные препараты у человека. Следовательно, открытие и усовершенствование ингибиторов ферментов является активной областью исследований в области биохимии и фармакологии .
Ингибиторы ферментов представляют собой химически разнообразный набор веществ, размеры которых варьируются от органических небольших молекул до макромолекулярных белков .
Маломолекулярные ингибиторы включают основные первичные метаболиты , которые ингибируют вышестоящие ферменты, продуцирующие эти метаболиты. Это обеспечивает петлю отрицательной обратной связи, которая предотвращает чрезмерное производство метаболитов и, таким образом, поддерживает клеточный гомеостаз (постоянные внутренние условия). [3] [2] Маломолекулярные ингибиторы ферментов также включают вторичные метаболиты , которые не являются существенными для организма, который их производит, но дают организму эволюционное преимущество, поскольку их можно использовать для отпугивания хищников или конкурирующих организмов или для обездвиживания добычи. . [4] Кроме того, многие лекарства представляют собой низкомолекулярные ингибиторы ферментов, которые нацелены либо на ферменты, модифицирующие заболевание у пациента [1] :5 , либо на ферменты патогенов, которые необходимы для роста и размножения патогена. [5]
Помимо небольших молекул, некоторые белки действуют как ингибиторы ферментов. Наиболее ярким примером являются серпины ( сериновая протеаза в ингибиторах), которые вырабатываются животными для защиты от нежелательной активации ферментов, а также растениями для предотвращения нападения хищников . [6] Другой класс белков-ингибиторов — это ингибиторы рибонуклеаз , которые связываются с рибонуклеазами в одном из самых тесных известных межбелковых взаимодействий . [7] Особым случаем белковых ингибиторов ферментов являются зимогены , которые содержат аутоингибирующий N-концевой пептид, который связывается с активным центром фермента, который внутримолекулярно блокирует его активность в качестве защитного механизма против неконтролируемого катализа. N-концевой пептид отщепляется (отщепляется) от предшественника фермента зимогена другим ферментом с высвобождением активного фермента. [8]
Сайт связывания ингибиторов с ферментами чаще всего является тем же сайтом, который связывает субстрат фермента . Эти ингибиторы активного центра известны как ингибиторы ортостерической («регулярной» ориентации). [9] Механизм ортостерического ингибирования заключается в предотвращении связывания субстрата с ферментом посредством прямой конкуренции, что, в свою очередь, не позволяет ферменту катализировать превращение субстратов в продукты. Альтернативно, ингибитор может связываться с сайтом, удаленным от активного центра фермента. Они известны как аллостерические («альтернативной» ориентации) ингибиторы. [9] Механизмы аллостерического ингибирования разнообразны и включают изменение конформации (формы) фермента таким образом, что он больше не может связывать субстрат ( кинетически неотличимый от конкурентного ортостерического ингибирования) [10] или, альтернативно, стабилизировать связывание субстрата с ферментом, но зафиксировать фермент в конформации, которая больше не является каталитически активной. [11]
Обратимые ингибиторы прикрепляются к ферментам с помощью нековалентных взаимодействий, таких как водородные связи , гидрофобные взаимодействия и ионные связи . [12] Множественные слабые связи между ингибитором и активным центром фермента в совокупности образуют прочное и специфическое связывание.
В отличие от необратимых ингибиторов, обратимые ингибиторы обычно не вступают в химические реакции при связывании с ферментом и могут быть легко удалены путем разведения или диализа . Особым случаем являются ковалентные обратимые ингибиторы , которые образуют химическую связь с ферментом, но эту связь можно расщепить, поэтому ингибирование становится полностью обратимым. [13]
Обратимые ингибиторы обычно подразделяются на четыре типа, как это было предложено Клеландом в 1963 году. [14] Они классифицируются в соответствии с влиянием ингибитора на V max (максимальную скорость реакции, катализируемую ферментом) и K m (концентрацию субстрата). что приводит к половине максимальной активности фермента) при изменении концентрации субстрата фермента. [15] [16]
При конкурентном ингибировании субстрат и ингибитор не могут связываться с ферментом одновременно. [17] : 134 Обычно это происходит из-за того, что ингибитор имеет сродство к активному центру фермента, с которым также связывается субстрат; субстрат и ингибитор конкурируют за доступ к активному центру фермента. Этот тип ингибирования можно преодолеть за счет достаточно высоких концентраций субстрата ( V max остается постоянным), т. е. вытесняя ингибитор. [17] : 134–135 Однако кажущаяся K m будет увеличиваться, поскольку для достижения точки K m требуется более высокая концентрация субстрата , или половина V max . Конкурентные ингибиторы часто аналогичны по структуре реальному субстрату (см., например, рисунок «Метотрексат против фолата» в разделе «Лекарственные препараты»). [17] : 134
При неконкурентном ингибировании ингибитор связывается только с фермент-субстратным комплексом. [17] : 139 Этот тип ингибирования приводит к уменьшению V max (максимальная скорость снижается в результате удаления активированного комплекса) и уменьшению K m (за счет лучшей эффективности связывания в результате принципа Ле Шателье и эффективного устранения Комплекс ES, таким образом, уменьшает K m , что указывает на более высокую аффинность связывания). [18] Неконкурентное ингибирование встречается редко. [17] : 139 [19]
При неконкурентном ингибировании связывание ингибитора с ферментом снижает его активность , но не влияет на связывание субстрата. [16] Этот тип ингибитора связывается с равным сродством как со свободным ферментом, так и с фермент-субстратным комплексом. Его можно рассматривать как обладающий способностью к конкурентным и неконкурентным ингибиторам, но без предпочтения какому-либо типу. В результате степень ингибирования зависит только от концентрации ингибитора. V max уменьшится из-за неспособности реакции протекать столь же эффективно, но K m останется прежним, поскольку фактическое связывание субстрата, по определению, все равно будет функционировать должным образом. [20]
При смешанном ингибировании ингибитор может связываться с ферментом независимо от того, уже связался ли субстрат. Следовательно, смешанное ингибирование представляет собой комбинацию конкурентного и неконкурентного ингибирования. [16] Кроме того, сродство ингибитора к свободному ферменту и комплексу фермент-субстрат может различаться. [17] : 136–139 При увеличении концентрации субстрата [S] этот тип ингибирования можно уменьшить (за счет конкурентного вклада), но не преодолеть полностью (из-за неконкурентного компонента). [21] : 381–382 Хотя ингибиторы смешанного типа могут связываться в активном центре, этот тип ингибирования обычно является результатом аллостерического эффекта, когда ингибитор связывается с другим сайтом фермента. Связывание ингибитора с этим аллостерическим сайтом изменяет конформацию (то есть третичную структуру или трехмерную форму) фермента, так что сродство субстрата к активному центру снижается. [22]
Эти четыре типа ингибирования можно также отличить по влиянию увеличения концентрации субстрата [S] на степень ингибирования, вызываемого данным количеством ингибитора. При конкурентном ингибировании степень ингибирования снижается с увеличением [S], при неконкурентном ингибировании степень ингибирования не изменяется, а при неконкурентном (также называемом антиконкурентным) ингибировании степень ингибирования увеличивается с увеличением [S]. [23]
Обратимое ингибирование можно описать количественно с точки зрения связывания ингибитора с ферментом и комплексом фермент-субстрат, а также его влияния на кинетические константы фермента. [24] : 6 В классической схеме Михаэлиса-Ментена (показанной на «схеме механизма ингибирования») фермент (E) связывается со своим субстратом (S) с образованием фермент-субстратного комплекса ES. При катализе этот комплекс распадается с высвобождением продукта P и свободного фермента. [24] : 55 Ингибитор (I) может связываться либо с E, либо с ES с константами диссоциации K i или K i ' соответственно. [24] : 87
Когда фермент имеет несколько субстратов, ингибиторы могут проявлять разные типы ингибирования в зависимости от того, какой субстрат рассматривается. Это происходит из-за того, что активный сайт содержит два разных сайта связывания внутри активного сайта, по одному для каждого субстрата. Например, ингибитор может конкурировать с субстратом А за первый сайт связывания, но быть неконкурентным ингибитором по отношению к субстрату В во втором сайте связывания. [26]
Традиционно обратимые ингибиторы ферментов классифицируются как конкурентные, неконкурентные и неконкурентные в зависимости от их влияния на K m и V max . [14] Эти три типа ингибирования возникают соответственно в результате связывания ингибитора только с ферментом E в отсутствие субстрата S, с фермент-субстратным комплексом ES или с обоими. Разделение этих классов возникает из-за проблемы их вывода и приводит к необходимости использовать две разные константы привязки для одного события привязки. [27] Далее предполагается, что связывание ингибитора с ферментом приводит к 100% ингибированию, и не учитывается возможность частичного ингибирования. [27] Общая форма ингибирующего термина также скрывает взаимосвязь между связыванием ингибитора с ферментом и его связью с любым другим связывающим термином, будь то уравнение Михаэлиса-Ментен или кривая доза-эффект, связанная со связыванием лиганда с рецептором. Чтобы продемонстрировать взаимосвязь, можно сделать следующую перестановку: [28]
Эта перегруппировка демонстрирует, что, как и в уравнении Михаэлиса-Ментен, максимальная скорость реакции зависит от доли популяции фермента, взаимодействующей с его субстратом.
доля популяции ферментов, связанная с субстратом
доля популяции ферментов, связанная ингибитором
Эффект ингибитора зависит от процента популяции ферментов, взаимодействующих с ингибитором. Единственная проблема с этим уравнением в его нынешней форме заключается в том, что оно предполагает абсолютное ингибирование фермента при связывании ингибитора, хотя на самом деле может быть широкий диапазон эффектов от 100% ингибирования обмена субстрата до отсутствия ингибирования. Чтобы учесть это, уравнение можно легко изменить, чтобы учесть различные степени ингибирования, включив в него член дельта V max . [29] : 361
или
Этот термин затем может определять остаточную ферментативную активность, присутствующую, когда ингибитор взаимодействует с отдельными ферментами в популяции. Однако включение этого термина имеет дополнительную ценность, поскольку допускает возможность активации, если вторичный член V max окажется выше начального. Чтобы учесть возможность активации, обозначения можно затем переписать, заменив ингибитор «I» термином-модификатором (стимулятор или ингибитор), обозначенным здесь как «X». [28] : уравнение 13
Хотя эта терминология приводит к упрощенному способу рассмотрения кинетических эффектов, связанных с максимальной скоростью уравнения Михаэлиса-Ментен, она выдвигает на первый план потенциальные проблемы с термином, используемым для описания эффектов, связанных с K m . K m , относящийся к сродству фермента к субстрату, в большинстве случаев должен относиться к потенциальным изменениям в сайте связывания фермента, которые могут быть непосредственно результатом взаимодействия ингибитора фермента . Таким образом , в большинстве ситуаций должен подойти термин, аналогичный термину delta V max , предложенному выше для модуляции V max : [28] : уравнение 14.
![Двумерные графики концентрации 1/[S] (ось x) и 1/V (ось y), демонстрирующие, что при изменении концентрации ингибитора линии конкурентных ингибиторов пересекаются в одной точке на оси y, а неконкурентные ингибиторы пересекаются. по оси X, а смешанные ингибиторы пересекают точку, которая не находится ни на одной из осей.](http://upload.wikimedia.org/wikipedia/commons/thumb/b/ba/Inhibition_diagrams-1-.png/220px-Inhibition_diagrams-1-.png)
Ингибитор фермента характеризуется константой диссоциации K i , концентрацией, при которой ингибитор наполовину занимает фермент. При неконкурентном ингибировании ингибитор также может связываться с комплексом фермент-субстрат, и присутствие связанного субстрата может изменить сродство ингибитора к ферменту, что приводит к появлению второй константы диссоциации K i '. Следовательно, K i и Ki ' — константы диссоциации ингибитора фермента и фермент-субстратного комплекса соответственно. [30] : Глоссарий. Константу фермента-ингибитора K i можно измерить непосредственно различными методами; Одним из особенно точных методов является изотермическая титровальная калориметрия , при которой ингибитор титруется раствором фермента и измеряется выделяемое или поглощаемое тепло. [31] Однако другую константу диссоциации K i 'трудно измерить напрямую, поскольку комплекс фермент-субстрат недолговечен и подвергается химической реакции с образованием продукта. Следовательно, K i ' обычно измеряется косвенно, наблюдая за активностью фермента при различных концентрациях субстрата и ингибитора и подгоняя данные с помощью нелинейной регрессии [32] к модифицированному уравнению Михаэлиса-Ментен . [21]
где модифицирующие факторы α и α’ определяются концентрацией ингибитора и двумя его константами диссоциации.
Таким образом, в присутствии ингибитора эффективные K m и V max фермента становятся (α/α') K m и (1/α') V max соответственно. Однако модифицированное уравнение Михаэлиса-Ментен предполагает, что связывание ингибитора с ферментом достигло равновесия, что может быть очень медленным процессом для ингибиторов с субнаномолярными константами диссоциации. В этих случаях ингибирование становится фактически необратимым, поэтому более практично рассматривать такие ингибиторы с сильным связыванием как необратимые (см. Ниже).
Влияние различных типов обратимых ингибиторов ферментов на ферментативную активность можно визуализировать с помощью графических представлений уравнения Михаэлиса-Ментен, таких как графики Лайнуивера-Берка , Иди-Хофсти или Хейнса-Вульфа . [17] : 140–144 Иллюстрацией служат три графика Лайнуивера–Бёрка, изображенные на рисунке диаграмм Лайнуивера–Бёрка . На верхней диаграмме линии конкурентного ингибирования пересекаются по оси y , показывая, что такие ингибиторы не влияют на V max . На нижней диаграмме линии неконкурентного ингибирования пересекаются по оси x , показывая, что эти ингибиторы не влияют на K m . Однако, поскольку по таким графикам может быть трудно точно оценить K i и Ki ' , [33] рекомендуется оценивать эти константы с использованием более надежных методов нелинейной регрессии. [33]
Механизм частично конкурентного ингибирования аналогичен механизму неконкурентного, за исключением того, что комплекс ЭИС обладает каталитической активностью, которая может быть ниже или даже выше (частично конкурентная активация), чем у фермент-субстратного (ЭС) комплекса. Это ингибирование обычно демонстрирует более низкое значение V max , но неизменяемое значение K m . [18]
Ингибирование субстрата или продукта – это когда субстрат или продукт фермента также действуют как ингибитор. Это ингибирование может иметь конкурентный, неконкурентный или смешанный характер. При ингибировании субстрата происходит прогрессивное снижение активности при высоких концентрациях субстрата, возможно, из-за фермента, имеющего два конкурирующих сайта связывания субстрата. При низком уровне субстрата сайт с высоким сродством занят и наблюдается нормальная кинетика . Однако при более высоких концентрациях второй ингибирующий сайт оказывается занятым, ингибируя фермент. [34] Ингибирование продукта (либо собственного продукта фермента, либо продукта фермента, находящегося ниже по ходу его метаболического пути) часто является регуляторной особенностью метаболизма и может быть формой отрицательной обратной связи . [2]
Медленно-сильное ингибирование происходит, когда исходный комплекс фермент-ингибитор EI подвергается конформационной изомерии (изменению формы) со вторым, более прочно удерживаемым комплексом, EI*, но общий процесс ингибирования обратим. Это проявляется в медленно нарастающем ингибировании ферментов. В этих условиях традиционная кинетика Михаэлиса-Ментен дает ложное значение K i , которое зависит от времени. Истинное значение K i можно получить путем более сложного анализа констант скорости включения ( k on ) и выключения ( k off ) для ассоциации ингибитора с кинетикой, аналогичной необратимому ингибированию . [17] : 168
Мультисубстратные аналоговые ингибиторы представляют собой селективные ингибиторы с высоким сродством, которые можно получить для ферментов, которые катализируют реакции с более чем одним субстратом, улавливая энергию связи каждого из этих субстратов в одну молекулу. [35] [36] Например, в реакциях переноса формила при биосинтезе пуринов мощный мультисубстратный аддукт-ингибитор (MAI) к глицинамид-рибонуклеотиду (GAR) ТФазе был получен синтетически путем связывания аналогов субстрата GAR и N-10. Кофактор -формилтетрагидрофолата вместе для получения тиоглицинамидрибонуклеотиддидеазафолата (TGDDF) [37] или ферментативно из природного субстрата GAR для получения GDDF. [38] Здесь субнаномолярная константа диссоциации (KD) TGDDF была больше, чем прогнозировалось, предположительно из-за полученных энтропийных преимуществ и/или положительных взаимодействий, приобретенных через атомы, связывающие компоненты. Также наблюдалось, что MAI продуцируются в клетках в результате реакций пролекарств, таких как изониазид [39] или лигандов-ингибиторов ферментов (например, PTC124 ) [40] с клеточными кофакторами, такими как никотинамидадениндинуклеотид (НАДН) и аденозинтрифосфат (НАДН) . АТФ) соответственно. [41]
Поскольку ферменты научились прочно связывать свои субстраты, а большинство обратимых ингибиторов связываются в активном центре ферментов, неудивительно, что некоторые из этих ингибиторов поразительно похожи по структуре на субстраты своих мишеней. Яркими примерами являются ингибиторы дигидрофолатредуктазы (DHFR). [42] Другими примерами подобных субстратов являются ингибиторы протеазы , терапевтически эффективный класс антиретровирусных препаратов , используемых для лечения ВИЧ/СПИДа . [43] [44] Структура ритонавира , пептидомиметического (пептидомимического) ингибитора протеазы, содержащего три пептидные связи , как показано на рисунке «конкурентного ингибирования» выше. Поскольку этот препарат напоминает пептид, который является субстратом протеазы ВИЧ, он конкурирует с субстратом в активном центре фермента. [45]
Ингибиторы ферментов часто разрабатываются для имитации переходного состояния или промежуточного продукта реакции, катализируемой ферментом. [46] Это гарантирует, что ингибитор использует эффект стабилизации переходного состояния фермента, что приводит к лучшему сродству связывания (более низкому K i ), чем конструкции на основе субстрата. Примером такого ингибитора переходного состояния является противовирусный препарат осельтамивир ; этот препарат имитирует планарную природу кольцевого иона оксония в реакции вирусного фермента нейраминидазы . [47]
Однако не все ингибиторы основаны на структурах субстратов. Например, структура другого ингибитора протеазы ВИЧ, типранавира , не основана на пептиде и не имеет явного структурного сходства с белковым субстратом. Эти непептидные ингибиторы могут быть более стабильными, чем ингибиторы, содержащие пептидные связи, поскольку они не являются субстратами для пептидаз и с меньшей вероятностью подвергаются деградации. [48]
При разработке лекарств важно учитывать концентрации субстратов, воздействию которых подвергаются целевые ферменты. Например, некоторые ингибиторы протеинкиназ имеют химическую структуру, подобную АТФ, одному из субстратов этих ферментов. [49] Однако лекарствам, которые являются простыми конкурентными ингибиторами, придется конкурировать с высокими концентрациями АТФ в клетке. Протеинкиназы также могут ингибироваться за счет конкуренции в местах связывания, где киназы взаимодействуют с белками-субстратами, и большинство белков присутствуют внутри клеток в концентрациях, намного меньших, чем концентрация АТФ. Как следствие, если два ингибитора протеинкиназы связываются в активном центре с одинаковым сродством, но только один должен конкурировать с АТФ, то конкурентный ингибитор в сайте связывания белка будет более эффективно ингибировать фермент. [50]
Необратимые ингибиторы ковалентно связываются с ферментом, и поэтому этот тип ингибирования не может быть легко обращен вспять. [51] Необратимые ингибиторы часто содержат реактивные функциональные группы, такие как азотистые иприты , альдегиды , галогеналканы , алкены , акцепторы Михаэля , фенилсульфонаты или фторфосфонаты . [52] Эти электрофильные группы реагируют с боковыми цепями аминокислот с образованием ковалентных аддуктов . [51] Модифицированными остатками являются остатки, боковые цепи которых содержат нуклеофилы, такие как гидроксильные или сульфгидрильные группы; к ним относятся аминокислоты серин (который реагирует с ДФП , см. схему «Реакция ДФП»), а также цистеин , треонин или тирозин . [53]
Необратимое ингибирование отличается от необратимой инактивации ферментов. [54] Необратимые ингибиторы обычно специфичны для одного класса ферментов и не инактивируют все белки; они действуют не путем разрушения структуры белка , а путем специфического изменения активного центра своей мишени. Например, экстремальные значения pH или температуры обычно вызывают денатурацию всей структуры белка, но это неспецифический эффект. Точно так же некоторые неспецифические химические обработки разрушают структуру белка: например, нагревание в концентрированной соляной кислоте гидролизует пептидные связи, удерживающие белки вместе, высвобождая свободные аминокислоты. [55]
Необратимые ингибиторы обладают ингибированием, зависящим от времени, и поэтому их эффективность не может быть охарактеризована значением IC 50 . Это связано с тем, что количество активного фермента при данной концентрации необратимого ингибитора будет различным в зависимости от того, как долго ингибитор предварительно инкубируется с ферментом. Вместо этого используются значения kobs /[ I ] [56] , где kobs — наблюдаемая скорость инактивации псевдопервого порядка (полученная путем построения логарифма % активности в зависимости от времени), а [ I ] — концентрация ингибитора. Параметр k obs /[ I ] действителен до тех пор, пока ингибитор не насыщает связывание с ферментом (в этом случае k obs = k inact ), где k inact — скорость инактивации.
Необратимые ингибиторы сначала образуют обратимый нековалентный комплекс с ферментом (EI или ESI). Впоследствии между ферментом и ингибитором происходит химическая реакция с образованием ковалентно модифицированного «тупикового комплекса» EI* (необратимого ковалентного комплекса). Скорость образования ЭИ* называется скоростью инактивации или k инакт . [13] Поскольку образование EI может конкурировать с ES, связывание необратимых ингибиторов можно предотвратить путем конкуренции либо с субстратом, либо со вторым обратимым ингибитором. Этот защитный эффект является убедительным свидетельством специфической реакции необратимого ингибитора с активным центром.
Стадии связывания и инактивации этой реакции исследуются путем инкубации фермента с ингибитором и анализа степени активности, остающейся с течением времени. Активность будет снижаться в зависимости от времени, обычно после экспоненциального затухания . Сопоставление этих данных с уравнением скорости дает скорость инактивации при этой концентрации ингибитора. Это делается при нескольких различных концентрациях ингибитора. Если задействован обратимый комплекс EI, скорость инактивации будет насыщаемой, и подгонка этой кривой даст k inact и Ki . [57]
Другой метод, широко используемый в этих анализах, — масс-спектрометрия . Здесь точное измерение массы немодифицированного нативного фермента и инактивированного фермента дает увеличение массы, вызванное реакцией с ингибитором, и показывает стехиометрию реакции. [58] Обычно это делается с использованием масс-спектрометра MALDI-TOF . [59] В дополнительной методике массовый дактилоскопический анализ пептидов включает переваривание нативного и модифицированного белка протеазой, такой как трипсин . В результате будет получен набор пептидов , которые можно будет проанализировать с помощью масс-спектрометра. Пептид, масса которого изменится после реакции с ингибитором, будет тем пептидом, который содержит сайт модификации. [60]
Не все необратимые ингибиторы образуют ковалентные аддукты со своими ферментами-мишенями. Некоторые обратимые ингибиторы настолько прочно связываются с ферментом-мишенью, что практически необратимы. Эти ингибиторы с сильным связыванием могут демонстрировать кинетику, аналогичную кинетике ковалентных необратимых ингибиторов. В этих случаях некоторые из этих ингибиторов быстро связываются с ферментом в виде комплекса EI с низким сродством, который затем подвергается более медленной перегруппировке в очень прочно связанный комплекс EI* (см. диаграмму «механизма необратимого ингибирования»). Такое кинетическое поведение называется медленным связыванием. [62] Эта медленная перегруппировка после связывания часто включает в себя конформационные изменения , поскольку фермент «зажимается» вокруг молекулы ингибитора. Примеры ингибиторов медленного связывания включают некоторые важные лекарства, такие как метотрексат , [63], аллопуринол , [64] и активированная форма ацикловира . [65]

Диизопропилфторфосфат (ДФП) является примером необратимого ингибитора протеаз (см. схему «Реакция ДФП»). Фермент гидролизует связь фосфор-фтор, но фосфатный остаток остается связанным с серином в активном центре , дезактивируя его. [67] Аналогичным образом, DFP также реагирует с активным центром ацетилхолинэстеразы в синапсах нейронов и, следовательно, является мощным нейротоксином со смертельной дозой менее 100 мг. [68]
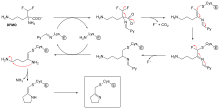
Суицидное ингибирование — это необычный тип необратимого ингибирования, при котором фермент превращает ингибитор в активную форму в его активном центре. [69] Примером может служить ингибитор биосинтеза полиаминов α-дифторметилорнитин (ДФМО), который является аналогом аминокислоты орнитина и используется для лечения африканского трипаносомоза (сонной болезни). Орнитиндекарбоксилаза может катализировать декарбоксилирование ДФМО вместо орнитина (см. Диаграмму «Механизм ингибитора ДФМО»). Однако за этой реакцией декарбоксилирования следует отщепление атома фтора, что превращает этот каталитический промежуточный продукт в конъюгированный имин , высокоэлектрофильную разновидность. Эта реактивная форма DFMO затем реагирует либо с остатком цистеина, либо с лизином в активном центре, необратимо инактивируя фермент. [61]
Поскольку необратимое ингибирование часто включает первоначальное образование комплекса нековалентного ингибитора фермента (EI), [13] иногда возможно, что ингибитор связывается с ферментом более чем одним способом. Например, на рисунке, показывающем трипанотионредуктазу простейшего человеческого паразита Trypanosoma cruzi , в ее активном центре связаны две молекулы ингибитора, называемого хинакриновым ипритом . Верхняя молекула связана обратимо, а нижняя – ковалентно, поскольку она прореагировала с аминокислотным остатком через свою азотистую ипритную группу. [70]
Ингибиторы ферментов встречаются в природе [71] , а также производятся искусственно в лаборатории. [72] Природные ингибиторы ферментов регулируют многие метаболические процессы и необходимы для жизни. [3] [1] Кроме того, яды естественного происхождения часто представляют собой ингибиторы ферментов, которые были разработаны для использования в качестве токсичных агентов против хищников, добычи и конкурирующих организмов. [4] Эти природные токсины включают в себя некоторые из наиболее ядовитых известных веществ. [73] Искусственные ингибиторы часто используются в качестве лекарств, но также могут представлять собой инсектициды, такие как малатион , гербициды, такие как глифосат , [74] или дезинфицирующие средства , такие как триклозан . Другие искусственные ингибиторы ферментов блокируют ацетилхолинэстеразу , фермент, расщепляющий ацетилхолин , и используются в качестве нервно-паралитических агентов в химической войне . [75]
Ингибирование ферментов является общей особенностью контроля метаболических путей в клетках. [3] Метаболический поток через путь часто регулируется метаболитами этого пути, действующими как ингибиторы и усилители ферментов этого же пути. Гликолитический путь является классическим примером. [76] Этот катаболический путь потребляет глюкозу и производит АТФ , НАДН и пируват . Ключевым этапом регуляции гликолиза является ранняя реакция пути, катализируемая фосфофруктокиназой-1 (PFK1). Когда уровень АТФ повышается, АТФ связывается с аллостерическим сайтом в PFK1, снижая скорость ферментативной реакции; гликолиз ингибируется и выработка АТФ падает. Этот контроль отрицательной обратной связи помогает поддерживать постоянную концентрацию АТФ в клетке. Однако метаболические пути регулируются не только посредством ингибирования, поскольку активация ферментов не менее важна. Что касается PFK1, фруктозо-2,6-бисфосфат и АДФ являются примерами метаболитов, которые являются аллостерическими активаторами. [77]
Физиологическое ингибирование ферментов также может быть вызвано специфическими белковыми ингибиторами. Этот механизм происходит в поджелудочной железе , которая синтезирует множество пищеварительных ферментов-предшественников, известных как зимогены . Многие из них активируются протеазой трипсина , поэтому важно ингибировать активность трипсина в поджелудочной железе, чтобы предотвратить самопереваривание органа. Одним из способов контроля активности трипсина является выработка специфического и мощного белка -ингибитора трипсина в поджелудочной железе. Этот ингибитор прочно связывается с трипсином, предотвращая активность трипсина, которая в противном случае была бы вредна для органа. [78] Хотя ингибитор трипсина представляет собой белок, он избегает гидролиза протеазой в качестве субстрата за счет исключения воды из активного центра трипсина и дестабилизации переходного состояния. [79] Другие примеры физиологических белков-ингибиторов ферментов включают барстарный ингибитор бактериальной рибонуклеазы барназы . [80]

Животные и растения научились синтезировать широкий спектр ядовитых продуктов, включая вторичные метаболиты , [81] пептиды и белки [82] , которые могут действовать как ингибиторы. Природные токсины обычно представляют собой небольшие органические молекулы и настолько разнообразны, что, вероятно, существуют естественные ингибиторы большинства метаболических процессов. [83] Метаболические процессы, на которые воздействуют природные яды, охватывают не только ферменты метаболических путей, но могут также включать ингибирование функций рецепторов, каналов и структурных белков в клетке. Например, паклитаксел (таксол), органическая молекула, обнаруженная в тихоокеанском тисе , прочно связывается с димерами тубулина и ингибирует их сборку в микротрубочки в цитоскелете . [84]
Многие природные яды действуют как нейротоксины , которые могут вызывать паралич , приводящий к смерти, и действуют для защиты от хищников или при охоте и поимке добычи. Некоторые из этих природных ингибиторов [85] , несмотря на их токсичные свойства, ценны для терапевтического применения в более низких дозах. [86] Примером нейротоксина являются гликоалкалоиды растений семейства пасленовых (включая картофель , томаты и баклажаны ), которые являются ингибиторами ацетилхолинэстеразы . Ингибирование этого фермента вызывает неконтролируемое увеличение уровня нейротрансмиттера ацетилхолина, мышечный паралич и затем смерть. Нейротоксичность также может быть результатом ингибирования рецепторов; например, атропин из паслена смертоносного ( Atropa belladonna ), который действует как конкурентный антагонист мускариновых рецепторов ацетилхолина . [87]
Хотя многие природные токсины являются вторичными метаболитами, к этим ядам также относятся пептиды и белки. Примером токсичного пептида является альфа-аманитин , который встречается у родственников смертного гриба . Это мощный ингибитор ферментов, в данном случае предотвращающий транскрипцию ДНК ферментом РНК-полимеразы II . [88] Водорослевой токсин микроцистин также является пептидом и ингибитором протеинфосфатаз . [89] Этот токсин может загрязнять источники воды после цветения водорослей и является известным канцерогеном, который также может вызвать острое кровотечение в печени и смерть при более высоких дозах. [90]
Белки также могут быть природными ядами или антинутриентами , такими как ингибиторы трипсина (обсуждаемые выше в разделе «метаболическая регуляция»), которые содержатся в некоторых бобовых . [91] Менее распространенным классом токсинов являются токсичные ферменты: они действуют как необратимые ингибиторы ферментов-мишеней и действуют путем химической модификации ферментов-субстратов. Примером является рицин , чрезвычайно мощный белковый токсин, обнаруженный в бобах касторового масла . [92] Этот фермент представляет собой гликозидазу , инактивирующую рибосомы. [93] Поскольку рицин является каталитическим необратимым ингибитором, это позволяет всего лишь одной молекуле рицина убить клетку. [94]

Ингибиторы ферментов чаще всего используются в качестве лекарств для лечения заболеваний. Многие из этих ингибиторов нацелены на человеческий фермент и направлены на коррекцию патологического состояния. Например, аспирин — широко используемый препарат, который действует как ингибитор фермента циклооксигеназы . [95] Это ингибирование, в свою очередь, подавляет выработку провоспалительных простагландинов , и, таким образом, аспирин можно использовать для уменьшения боли, лихорадки и воспаления. [95]
По оценкам , по состоянию на 2017 год [update]около 29% одобренных лекарств представляют собой ингибиторы ферментов [96] , из которых примерно одна пятая — ингибиторы киназ . [96] Примечательным классом киназных лекарственных средств являются рецепторные тирозинкиназы , которые являются важными ферментами, регулирующими рост клеток ; их чрезмерная активация может привести к раку. Следовательно, ингибиторы киназы , такие как иматиниб , часто используются для лечения злокачественных новообразований. [97] Янус-киназы являются еще одним ярким примером мишени для лекарственных ферментов. Ингибиторы Янус-киназы блокируют выработку воспалительных цитокинов и, следовательно, эти ингибиторы используются для лечения различных воспалительных заболеваний , включая артрит , астму и болезнь Крона . [98]
Пример структурного сходства некоторых ингибиторов с субстратами ферментов, на которые они нацелены, можно увидеть на рисунке, сравнивающем препарат метотрексат с фолиевой кислотой . Фолиевая кислота представляет собой окисленную форму субстрата дигидрофолатредуктазы , фермента, который сильно ингибируется метотрексатом. Метотрексат блокирует действие дигидрофолатредуктазы и тем самым останавливает биосинтез тимидина . [42] Этот блок биосинтеза нуклеотидов избирательно токсичен для быстро растущих клеток, поэтому метотрексат часто используется при химиотерапии рака. [99]
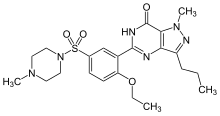
Распространенным средством лечения эректильной дисфункции является силденафил (Виагра). [100] Это соединение является мощным ингибитором цГМФ-специфической фосфодиэстеразы типа 5 , фермента, который разрушает сигнальную молекулу циклического гуанозинмонофосфата . [101] Эта сигнальная молекула вызывает расслабление гладких мышц и обеспечивает приток крови в пещеристые тела , что вызывает эрекцию. Поскольку препарат снижает активность фермента, останавливающего сигнал, этот сигнал сохраняется в течение более длительного периода времени.

Лекарства также используются для ингибирования ферментов, необходимых для выживания патогенов. Например, бактерии окружены толстой клеточной стенкой , состоящей из сетчатого полимера, называемого пептидогликаном . Многие антибиотики, такие как пенициллин и ванкомицин, ингибируют ферменты, которые производят, а затем сшивают цепи этого полимера вместе. [102] [103] Это приводит к тому, что клеточная стенка теряет прочность и бактерии лопаются. На рисунке молекула пенициллина (показана в форме шарика и палочки) связана со своей мишенью — транспептидазой бактерий Streptomyces R61 (белок показан в виде ленточной диаграммы ).
Разработка антибиотиков облегчается, когда фермент, необходимый для выживания патогена, отсутствует или сильно отличается у людей. [104] Люди не производят пептидогликан, поэтому антибиотики, ингибирующие этот процесс, избирательно токсичны для бактерий. [105] Избирательная токсичность антибиотиков также достигается за счет различий в структуре рибосом бактерий [ 106] или в том, как они производят жирные кислоты . [107]
Препараты, ингибирующие ферменты, необходимые для репликации вирусов, эффективны при лечении вирусных инфекций. [108] Противовирусные препараты включают ингибиторы протеазы, используемые для лечения ВИЧ/СПИДа, [109] и гепатита С , [110] ингибиторы обратной транскриптазы, нацеленные на ВИЧ/СПИД, [111] ингибиторы нейраминидазы , нацеленные на грипп , [112] и ингибиторы терминазы, нацеленные на цитомегаловирус человека. . [113]
Многие пестициды являются ингибиторами ферментов. [114] Ацетилхолинэстераза (АХЭ) — это фермент, обнаруженный у животных, от насекомых до человека. Он необходим для функционирования нервных клеток благодаря механизму расщепления нейромедиатора ацетилхолина на его составляющие — ацетат и холин . [115] Это несколько необычно среди нейротрансмиттеров, поскольку большинство из них, включая серотонин , дофамин и норадреналин , поглощаются из синаптической щели , а не расщепляются. Большое количество ингибиторов АХЭ используется как в медицине, так и в сельском хозяйстве. [116] Обратимые конкурентные ингибиторы, такие как эдрофоний , физостигмин и неостигмин , используются при лечении миастении [117] и в анестезии для снятия мышечной блокады. [118] Карбаматные пестициды также являются примерами обратимых ингибиторов АХЭ. Фосфорорганические пестициды, такие как малатион , паратион и хлорпирифос, необратимо ингибируют ацетилхолинэстеразу. [119]
Гербицид глифосат является ингибитором 3-фосфошикимат-1-карбоксивинилтрансферазы , [120] другие гербициды, такие как сульфонилмочевины, ингибируют фермент ацетолактатсинтазу . [121] Оба фермента необходимы растениям для производства аминокислот с разветвленной цепью . Гербициды ингибируют многие другие ферменты, в том числе ферменты, необходимые для биосинтеза липидов и каротиноидов , а также процессов фотосинтеза и окислительного фосфорилирования . [122]

Новые лекарства являются продуктом длительного процесса разработки лекарств , первым шагом которого часто является открытие нового ингибитора фермента. [123] Существует два принципиальных подхода к обнаружению этих ингибиторов. [124]
Первый общий метод — это рациональный дизайн лекарств , основанный на имитации переходного состояния химической реакции, катализируемой ферментом. [125] Разработанный ингибитор часто очень похож на субстрат, за исключением того, что часть субстрата, которая подвергается химической реакции, заменена химически стабильной функциональной группой , которая напоминает переходное состояние. Поскольку фермент эволюционировал для стабилизации переходного состояния, аналоги переходного состояния обычно обладают более высоким сродством к ферменту по сравнению с субстратом и, следовательно, являются эффективными ингибиторами. [46]
Второй способ обнаружения новых ингибиторов ферментов — это высокопроизводительный скрининг больших библиотек структурно разнообразных соединений для выявления молекул, которые связываются с ферментом. Этот метод был расширен и теперь включает виртуальный скрининг баз данных различных молекул с использованием компьютеров [126] [127] , за которым затем следует экспериментальное подтверждение связывания результатов виртуального скрининга. [128] Дополнительные подходы, которые могут обеспечить новые отправные точки для ингибиторов, включают открытие свинцов на основе фрагментов [129] и химические библиотеки, закодированные в ДНК (DEL). [130]
Результаты любого из вышеперечисленных подходов могут быть оптимизированы для связывания с высоким сродством, которое эффективно ингибирует фермент. [131] Компьютерные методы прогнозирования ориентации связывания и сродства ингибитора к ферменту, такие как молекулярный докинг [132] и молекулярная механика, могут использоваться для оказания помощи в процессе оптимизации. [133] Новые ингибиторы используются для получения кристаллографических структур фермента в комплексе ингибитор/фермент, чтобы показать, как молекула связывается с активным центром, что позволяет вносить изменения в ингибитор для оптимизации связывания в процессе, известном как структурирование. на основе дизайна лекарств . [1] : 66 Этот цикл испытаний и усовершенствований повторяется до тех пор, пока не будет получен достаточно мощный ингибитор.
В некоторых случаях ингибитор может связываться с отдельным участком фермента, который находится в аллостерической связи с карманом связывания субстрата. Во многих случаях аллостерические соединения, конкурирующие с субстратом, приводят к конформационным изменениям фермента, которые изменяют способность фермента связывать субстрат.
Инактивацию фермента обычно объясняют как химический процесс, включающий несколько явлений, таких как агрегация, диссоциация на субъединицы или денатурация (конформационные изменения), которые происходят одновременно во время инактивации определенного фермента.
Рисунок 1C: Клинический успех привилегированных классов семейства белков (% одобренных препаратов, нацеленных на каждый целевой класс): редуктаза 7,62, киназа 5,94, протеаза 3,35, гидролаза 2,76, НПТаза 2,09, трансфераза 1,92, лиаза 1,59, изомераза 1,51, фосфодиэстераза 1,50, Цитохром p450 0,84, Эпигенетический ластик 0,33, Общее количество ферментов-мишеней одобренных препаратов = 29,45%
{{cite book}}: CS1 maint: location missing publisher (link)Глава 10.2.1: Ингибиторы сульфонилмочевины ацетолактатсинтазы