Кадмий — химический элемент ; он имеет символ Cd и атомный номер 48. Этот мягкий серебристо-белый металл химически подобен двум другим стабильным металлам группы 12 , цинку и ртути . Как и цинк, он демонстрирует степень окисления +2 в большинстве своих соединений и, как и ртуть, имеет более низкую температуру плавления, чем переходные металлы в группах с 3 по 11 . Кадмий и его родственники в группе 12 часто не считаются переходными металлами, поскольку они не имеют частично заполненных электронных оболочек d или f в элементарных или обычных состояниях окисления. Средняя концентрация кадмия в земной коре составляет от 0,1 до 0,5 частей на миллион (ppm). Он был открыт в 1817 году одновременно Штромейером и Германом , оба в Германии, как примесь в карбонате цинка .
Кадмий встречается в качестве второстепенного компонента в большинстве цинковых руд и является побочным продуктом производства цинка. Кадмий использовался долгое время [ когда? ] в качестве антикоррозионного покрытия стали , а соединения кадмия используются в качестве красных, оранжевых и желтых пигментов , для окраски стекла и для стабилизации пластика . Использование кадмия в целом снижается, поскольку он токсичен (он специально указан в Европейской директиве об ограничении использования опасных веществ [6] ), а никель-кадмиевые батареи были заменены никель-металлогидридными и литий-ионными батареями. Одно из немногих новых применений — солнечные панели из теллурида кадмия .
Хотя кадмий не имеет известной биологической функции в высших организмах, у морских диатомей была обнаружена кадмий-зависимая карбоангидраза .
Кадмий — мягкий, ковкий , пластичный , серебристо-белый двухвалентный металл. Он во многом похож на цинк, но образует комплексные соединения. [7] В отличие от большинства других металлов, кадмий устойчив к коррозии и используется в качестве защитной пластины на других металлах. Кадмий как объемный металл нерастворим в воде [8] и не горюч ; однако в порошкообразной форме он может гореть и выделять токсичные пары . [9]
Хотя кадмий обычно имеет степень окисления +2, он также существует в состоянии +1. Кадмий и его родственные соединения не всегда считаются переходными металлами, поскольку они не имеют частично заполненных электронных оболочек d или f в элементарных или обычных состояниях окисления. [10] Кадмий сгорает на воздухе с образованием коричневого аморфного оксида кадмия (CdO); Кристаллическая форма этого соединения имеет темно -красный цвет, который меняет цвет при нагревании, подобно оксиду цинка . Соляная , серная и азотная кислоты растворяют кадмий с образованием хлорида кадмия (CdCl 2 ), сульфата кадмия (CdSO 4 ) или нитрата кадмия (Cd(NO 3 ) 2 ). Степень окисления +1 можно получить, растворяя кадмий в смеси хлоридов кадмия и хлоридов алюминия , образуя катион Cd 2 2+ , аналогичный катиону Hg 2 2+ в хлориде ртути(I) . [7]
Установлена структура многих комплексов кадмия с азотистыми основаниями , аминокислотами и витаминами . [11]
Встречающийся в природе кадмий состоит из восьми изотопов . Два из них радиоактивны , а три, как ожидается, распадутся , но в лабораторных условиях этого не произошло. Два естественных радиоактивных изотопа — 113 Cd ( бета-распад , период полураспада —7,7 × 10 15 лет ) и 116 Cd (двухнейтринный двойной бета-распад , период полураспада2,9 × 10 19 лет ). Остальные три — это 106 Cd, 108 Cd (оба с двойным захватом электронов ) и 114 Cd (двойной бета-распад); были определены только нижние пределы этих периодов полураспада. По крайней мере три изотопа – 110 Cd, 111 Cd и 112 Cd – стабильны. Среди изотопов, не встречающихся в природе, наиболее долгоживущими являются 109 Cd с периодом полураспада 462,6 суток и 115 Cd с периодом полураспада 53,46 часа. Все остальные радиоактивные изотопы имеют период полураспада менее 2,5 часов, а у большинства период полураспада менее 5 минут. Кадмий имеет 8 известных метасостояний , наиболее стабильными из которых являются 113m Cd ( t 1/2 = 14,1 года), 115m Cd ( t 1/2 = 44,6 дня) и 117m Cd ( t 1/2 = 3,36 часа). [12]
Атомные массы известных изотопов кадмия варьируются от 94,950 ед. ( 95 Cd) до 131,946 ед. ( 132 Cd). Для изотопов легче 112 u основным способом распада является захват электрона , а доминирующим продуктом распада является элемент 47 ( серебро ). Более тяжелые изотопы распадаются в основном за счет бета-излучения , образуя элемент 49 ( индий ). [12]
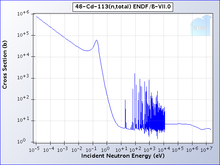
Один изотоп кадмия, 113 Cd, поглощает нейтроны с высокой селективностью: с очень высокой вероятностью будут поглощены нейтроны с энергией ниже порога отсечки кадмия ; те, которые выше порогового значения, будут переданы . Пороговое значение кадмия составляет около 0,5 эВ, и нейтроны ниже этого уровня считаются медленными нейтронами , в отличие от промежуточных и быстрых нейтронов . [13]
Кадмий создается в результате s-процесса в звездах малой и средней массы с массами от 0,6 до 10 солнечных масс в течение тысяч лет. В этом процессе атом серебра захватывает нейтрон , а затем подвергается бета-распаду . [14]

Кадмий ( лат. cadmia , греческое καδμεία означает « каламин », кадмийсодержащая смесь минералов, названная в честь греческого мифологического персонажа Κάδμος, Кадма , основателя Фив ) был обнаружен в загрязненных соединениях цинка, продаваемых в аптеках Германии [15] в 1817 году Фридрихом Штромейером . [16] Карл Самуэль Леберехт Герман одновременно исследовал изменение цвета оксида цинка и обнаружил примесь, первоначально предположительно мышьяк , из-за желтого осадка сероводорода . Кроме того, Стромейер обнаружил, что один поставщик продавал карбонат цинка вместо оксида цинка. [6] Стромейер обнаружил новый элемент в виде примеси в карбонате цинка (каламине), и в течение 100 лет Германия оставалась единственным крупным производителем металла. Металл был назван в честь латинского слова «каламин», поскольку он был обнаружен в цинковой руде. Стромейер отметил, что некоторые нечистые образцы каламина меняли цвет при нагревании, а чистый каламин - нет. Он настойчиво изучал эти результаты и в конечном итоге выделил металлический кадмий путем обжига и восстановления сульфида . Потенциал желтого кадмия в качестве пигмента был признан в 1840-х годах, но отсутствие кадмия ограничивало его применение. [17] [18] [19]
Несмотря на то, что кадмий и его соединения в определенных формах и концентрациях токсичны, в Британском фармацевтическом кодексе 1907 года говорится, что йодид кадмия использовался в качестве лекарства для лечения «увеличенных суставов, золотушных желез и обморожений». [20]
В 1907 году Международный астрономический союз определил международный ангстрем как красную спектральную линию кадмия (1 длина волны = 6438,46963 Å). [21] [22] Это было принято 7-й Генеральной конференцией по мерам и весам в 1927 году. В 1960 году определения метра и ангстрема были изменены на использование криптона . [23]
После того, как в 1930-х и 1940-х годах началось промышленное производство кадмия, основным применением кадмия стало покрытие железа и стали для предотвращения коррозии; в 1944 году 62%, а в 1956 году 59% кадмия в США использовалось для гальваники . [6] [24] В 1956 году 24% кадмия в Соединенных Штатах было использовано для вторичного применения в красных, оранжевых и желтых пигментах из сульфидов и селенидов кадмия. [24]
Стабилизирующее действие химических веществ кадмия, таких как карбоксилаты лаурат кадмия и стеарат кадмия, на ПВХ , привело к более широкому использованию этих соединений в 1970-х и 1980-х годах. Спрос на кадмий в пигментах, покрытиях, стабилизаторах и сплавах снизился в результате принятия экологических и санитарных норм в 1980-х и 1990-х годах; в 2006 году только 7% общего потребления кадмия было использовано для гальванических покрытий и только 10% - для пигментов. [6] В то же время данное снижение потребления было компенсировано растущим спросом на кадмий для никель-кадмиевых аккумуляторов, на долю которого приходилось 81% потребления кадмия в США в 2006 г. [25]

Кадмий составляет около 0,1 ppm земной коры . Он встречается гораздо реже, чем цинк, содержание которого составляет около 65 ppm. [26] Значительных месторождений кадмийсодержащих руд не известно. Единственный важный минерал кадмия, гринокит (CdS ) , почти всегда связан со сфалеритом (ZnS). Эта ассоциация вызвана геохимическим сходством цинка и кадмия, при этом геологический процесс, вероятно, не разделил их. Так, кадмий производится главным образом как побочный продукт добычи, плавки и переработки сульфидных руд цинка и, в меньшей степени, свинца и меди . Небольшие количества кадмия, около 10% потребления, производятся из вторичных источников, в основном из пыли, образующейся при переработке лома железа и стали. Производство в США началось в 1907 году, [19] , но широкое использование началось после Первой мировой войны. [27] [28]
Металлический кадмий встречается в бассейне реки Вилюй в Сибири . [29]
Породы, добываемые для фосфорных удобрений, содержат различное количество кадмия, в результате чего концентрация кадмия в удобрениях достигает 300 мг/кг, а в сельскохозяйственных почвах - высокое содержание кадмия. [30] [31] Уголь может содержать значительное количество кадмия, который в основном попадает в летучую золу . [32]
Кадмий из почвы может поглощаться такими культурами, как рис и какао. В 2002 году министерство сельского хозяйства Китая установило, что 28% отобранного им риса имели избыток свинца, а 10% имели избыток кадмия выше пределов, установленных законом. Consumer Reports протестировал 28 марок темного шоколада, продававшихся в США в 2022 году, и обнаружил во всех из них кадмий, причем 13 из них превысили предельно допустимую дозу в Калифорнии. [33]
Было обнаружено , что некоторые растения, такие как ивы и тополя, очищают почву от свинца и кадмия. [34]
Типичные фоновые концентрации кадмия в атмосфере не превышают 5 нг/м 3 ; 2 мг/кг в почве; 1 мкг/л в пресной воде и 50 нг/л в морской воде. [35] Концентрации кадмия выше 10 мкг/л могут быть стабильными в воде с низкими общими концентрациями растворенных веществ и pH , и их может быть трудно удалить обычными процессами очистки воды. [36]
Кадмий является распространенной примесью в цинковых рудах, и его чаще всего выделяют при производстве цинка . Некоторые концентраты цинковых руд из сульфатно- цинковых руд содержат до 1,4% кадмия. [37] В 1970-х годах производство кадмия составляло 6,5 фунтов (2,9 кг) на тонну цинка. [37] Сульфидные цинковые руды обжигаются в присутствии кислорода , превращая сульфид цинка в оксид . Металлический цинк получают либо плавлением оксида с углеродом , либо электролизом в серной кислоте . Кадмий выделяют из металлического цинка вакуумной перегонкой , если цинк плавят, или осаждают сульфат кадмия из электролизного раствора. [28] [38]
Британская геологическая служба сообщает, что в 2001 году Китай был ведущим производителем кадмия с почти одной шестой мирового производства, за ним с небольшим отрывом следовали Южная Корея и Япония. [39]
Кадмий является распространенным компонентом электрических батарей, пигментов , [40] покрытий, [41] и гальванических покрытий. [42]

В 2009 году 86% кадмия использовалось в батареях , преимущественно в перезаряжаемых никель-кадмиевых аккумуляторах . Никель-кадмиевые элементы имеют номинальный потенциал ячейки 1,2 В. Ячейка состоит из положительного электрода из гидроксида никеля и отрицательной пластины из кадмия, разделенных щелочным электролитом ( гидроксидом калия ). [43] Европейский Союз установил ограничение на содержание кадмия в электронике в 2004 году на уровне 0,01%, [44] за некоторыми исключениями, а в 2006 году снизил ограничение на содержание кадмия до 0,002%. [45] Другим типом аккумуляторов на основе кадмия являются серебряно-кадмиевые аккумуляторы .

Гальваника кадмием , занимающая 6% мирового производства, используется в авиационной промышленности для уменьшения коррозии стальных компонентов. [42] Это покрытие пассивируется солями хромата . [41] Ограничением кадмирования является водородное охрупчивание высокопрочных сталей в процессе гальванического покрытия. Поэтому на стальные детали, подвергнутые термообработке до предела прочности на растяжение выше 1300 МПа (200 фунтов на квадратный дюйм), следует наносить покрытие альтернативным методом (например, специальными процессами гальванопокрытия кадмием с низкой хрупкостью или физическим осаждением из паровой фазы).
Охрупчивание титана из-за остатков инструментов, покрытых кадмием, привело к исключению этих инструментов (и проведению регулярных испытаний инструментов для обнаружения загрязнения кадмием) в A-12 / SR-71, U-2 и последующих программах самолетов, в которых используется титан. [46]
Кадмий используется в управляющих стержнях ядерных реакторов, действуя как очень эффективный нейтронный поглотитель для контроля нейтронного потока при ядерном делении . [42] Когда кадмиевые стержни вставляются в активную зону ядерного реактора, кадмий поглощает нейтроны, не позволяя им создавать дополнительные события деления, тем самым контролируя количество реактивности. В реакторе с водой под давлением , разработанном Westinghouse Electric Company, используется сплав, состоящий из 80% серебра, 15% индия и 5% кадмия. [42]
В конструкции QLED-телевизоров начали использовать кадмий. Некоторые компании стремятся снизить воздействие на окружающую среду, связанное с воздействием на человека и загрязнением материалов телевизоров во время производства. [47]
Комплексы на основе тяжелых металлов имеют большой потенциал для лечения широкого спектра онкологических заболеваний, однако их применение часто ограничено из-за токсических побочных эффектов. Однако ученые продвигаются вперед в этой области и обнаруживают новые перспективные комплексные соединения кадмия с пониженной токсичностью. [48]

Оксид кадмия использовался в черно-белых телевизионных люминофорах, а также в синих и зеленых люминофорах цветных телевизионных электронно-лучевых трубок. [49] Сульфид кадмия (CdS) используется в качестве фотопроводящего поверхностного покрытия для фотокопировальных барабанов. [50]

В пигментах красок используются различные соли кадмия, наиболее распространенным из которых является CdS в качестве желтого пигмента . Селенид кадмия представляет собой красный пигмент, обычно называемый кадмиевым красным . Художникам, работающим с пигментом, кадмий дает самые яркие и стойкие желтые, оранжевые и красные цвета — настолько, что во время производства эти цвета значительно смягчаются, прежде чем их растирают маслом и связующими или смешивают с акварелью , гуашью и т . д. акриловые краски и другие составы красок и пигментов. Поскольку эти пигменты потенциально токсичны, пользователям следует наносить на руки защитный крем , чтобы предотвратить впитывание через кожу [40], даже несмотря на то, что количество кадмия, всасываемого в организм через кожу, составляет менее 1%. [9]
В ПВХ кадмий использовался в качестве стабилизатора тепла, света и атмосферных воздействий. [42] [51] В настоящее время кадмиевые стабилизаторы полностью заменены бариево-цинковыми, кальциево-цинковыми и оловоорганическими стабилизаторами. Кадмий используется во многих видах припоев и подшипниковых сплавов, поскольку он имеет низкий коэффициент трения и усталостную прочность. [42] Он также содержится в некоторых сплавах с самой низкой температурой плавления , таких как металл Вуда . [52]
Кадмий является элементом некоторых полупроводниковых материалов. Сульфид кадмия, селенид кадмия и теллурид кадмия используются в некоторых фотодетекторах и солнечных элементах . Детекторы HgCdTe чувствительны к среднему инфракрасному свету [42] и используются в некоторых детекторах движения.

Гелий-кадмиевые лазеры являются распространенным источником синего или ультрафиолетового лазерного света. С использованием этой усиливающей среды изготавливаются лазеры на длинах волн 325, 354 и 442 нм ; некоторые модели могут переключаться между этими длинами волн. В частности, они используются во флуоресцентной микроскопии , а также в различных лабораторных целях, требующих лазерного света на этих длинах волн. [53] [54]
Квантовые точки селенида кадмия излучают яркую люминесценцию при УФ-возбуждении (например, He-Cd-лазер). Цвет этого свечения может быть зеленым, желтым или красным в зависимости от размера частиц. Коллоидные растворы этих частиц используются для визуализации биологических тканей и растворов с помощью флуоресцентного микроскопа . [55]
В молекулярной биологии кадмий используется для блокирования потенциал-зависимых кальциевых каналов от потока ионов кальция, а также в исследованиях гипоксии для стимуляции протеасомно -зависимой деградации Hif-1α . [56]
Кадмий-селективные сенсоры на основе флуорофора BODIPY были разработаны для визуализации и обнаружения кадмия в клетках. [57] Один мощный метод мониторинга кадмия в водной среде включает электрохимию . Используя самоорганизующийся монослой, можно получить кадмиевый селективный электрод с чувствительностью на уровне ppt . [58]
Кадмий не имеет известной функции в высших организмах и считается токсичным. [59] Кадмий считается загрязнителем окружающей среды, который представляет опасность для здоровья живых организмов. [60] Введение кадмия в клетки вызывает окислительный стресс и повышает уровень антиоксидантов, вырабатываемых клетками для защиты от макромолекулярных повреждений. [61]
Однако у некоторых морских диатомей обнаружена кадмий-зависимая карбоангидраза . [62] Диатомовые водоросли живут в средах с очень низкими концентрациями цинка, а кадмий выполняет функцию, обычно выполняемую цинком в других ангидразах. Это было обнаружено с помощью спектроскопии рентгеновской абсорбционной ближнекраевой структуры (XANES). [62] [63]
Кадмий преимущественно всасывается в почках человека. В детстве и подростковом возрасте человек обычно вдыхает около 30 мг кадмия. [64] Кадмий исследуется на предмет его токсичности для человека, потенциально повышающей риск развития рака , сердечно-сосудистых заболеваний и остеопороза . [65] [66] [67] [68]
Биогеохимия кадмия и его выброс в окружающую среду были предметом обзора, а также видообразование кадмия в окружающей среде. [69] [70]
Отдельные лица и организации исследуют бионеорганические аспекты кадмия на предмет его токсичности. [72] Наиболее опасной формой профессионального воздействия кадмия является вдыхание мелкодисперсной пыли и паров или проглатывание хорошо растворимых соединений кадмия. [6] Вдыхание паров кадмия может первоначально привести к лихорадке от паров металлов , но может привести к химическому пневмониту , отеку легких и смерти. [73]
Кадмий также представляет опасность для окружающей среды. Воздействие на человека в основном происходит в результате сжигания ископаемого топлива, фосфатных удобрений, природных источников, производства железа и стали, производства цемента и связанной с ним деятельности, производства цветных металлов и сжигания твердых бытовых отходов. [6] Другие источники кадмия включают хлеб, корнеплоды и овощи. [74]

Было несколько случаев отравления населения в результате длительного воздействия кадмия в загрязненных продуктах питания и воде. По состоянию на 2012 год исследования мимикрии эстрогена, которая может вызывать рак молочной железы, продолжаются [обновлять]. [74] За десятилетия, предшествовавшие Второй мировой войне , горнодобывающие работы загрязнили реку Дзинзу в Японии кадмием и следами других токсичных металлов. В результате кадмий накапливался в посевах риса вдоль берегов рек ниже шахт. Некоторые члены местных сельскохозяйственных сообществ потребляли зараженный рис, и у них развилась болезнь итаи-итай и почечные нарушения, включая протеинурию и глюкозурию . [75] Жертвами этого отравления были почти исключительно женщины в постменопаузе с низким содержанием железа и других минералов в организме. Аналогичное воздействие кадмия на население в других частях мира не привело к таким же проблемам со здоровьем, поскольку население поддерживало достаточный уровень железа и других минералов. Таким образом, хотя кадмий является основным фактором болезни итай-итай в Японии, большинство исследователей пришли к выводу, что он был одним из нескольких факторов. [6]
Кадмий является одним из шести веществ, запрещенных директивой Европейского Союза об ограничении использования опасных веществ (RoHS), которая регулирует использование опасных веществ в электрическом и электронном оборудовании, но допускает определенные исключения из сферы действия закона. [76]
Международное агентство по изучению рака классифицировало кадмий и его соединения как канцерогенные для человека. [77] Хотя профессиональное воздействие кадмия связано с раком легких и простаты, все еще существует неопределенность относительно канцерогенности кадмия при низком воздействии на окружающую среду. Недавние данные эпидемиологических исследований показывают, что потребление кадмия с пищей связано с более высоким риском рака эндометрия, молочной железы и простаты, а также остеопороза у людей. [78] [79] [80] [81] Недавнее исследование показало, что ткань эндометрия характеризуется более высоким уровнем кадмия у нынешних и бывших курящих женщин. [82]
Воздействие кадмия связано с большим количеством заболеваний, включая заболевания почек, [83] ранний атеросклероз, гипертонию и сердечно-сосудистые заболевания. [84] Хотя исследования показывают значительную корреляцию между воздействием кадмия и возникновением заболеваний в человеческой популяции, молекулярный механизм еще не идентифицирован. Одна из гипотез утверждает, что кадмий является разрушителем эндокринной системы , а некоторые экспериментальные исследования показали, что он может взаимодействовать с различными гормональными сигнальными путями. Например, кадмий может связываться с альфа -рецептором эстрогена [85] [86] и влиять на передачу сигнала по сигнальным путям эстрогена и МАРК в низких дозах. [87] [88] [89]
Табачное растение поглощает и накапливает в своих листьях тяжелые металлы , такие как кадмий, из окружающей почвы. После вдыхания табачного дыма они легко всасываются в организм потребителя. [90] Курение табака является наиболее важным источником воздействия кадмия на население в целом. По оценкам, 10% содержания кадмия в сигарете вдыхается при курении. Абсорбция кадмия через легкие более эффективна, чем через кишечник. До 50% кадмия, вдыхаемого с сигаретным дымом, может быть поглощено. [91] В среднем концентрация кадмия в крови курильщиков в 4–5 раз выше, чем у некурящих, а в почках — в 2–3 раза выше, чем у некурящих. Несмотря на высокое содержание кадмия в сигаретном дыме, воздействие кадмия при пассивном курении , по-видимому, незначительно . [92]
Для некурящего населения пища является основным источником заражения. Большое количество кадмия содержится в ракообразных , моллюсках , субпродуктах , лягушачьих лапках , какао , горьком и полугорьком шоколаде , морских водорослях , грибах и продуктах из водорослей . Однако зерновые, овощи, а также крахмалистые корнеплоды и клубнеплоды потребляются в США в гораздо больших количествах и являются там источником наибольшего пищевого воздействия. [93] Большинство растений биоаккумулируют токсины металлов, такие как кадмий, и при компостировании с образованием органических удобрений дают продукт, который часто может содержать большое количество (например, более 0,5 мг) токсинов металлов на каждый килограмм удобрений. Удобрения, изготовленные из навоза животных (например, коровьего навоза) или городских отходов, могут содержать аналогичное количество кадмия. Кадмий, добавленный в почву из удобрений (фосфатов или органических удобрений), становится биодоступным и токсичным только в том случае, если pH почвы низкий (т. е. кислые почвы).
Ионы цинка, меди, кальция и железа, а также селена с витамином С используются для лечения интоксикации кадмием, хотя ее нелегко устранить. [83]
Из-за неблагоприятного воздействия кадмия на окружающую среду и здоровье человека поставка и использование кадмия в Европе ограничены в соответствии с Регламентом REACH . [94]
Группа экспертов EFSA по загрязнителям в пищевой цепи указывает, что 2,5 мкг/кг массы тела являются допустимой еженедельной нормой для человека. [93] Объединенный комитет экспертов ФАО/ВОЗ по пищевым добавкам объявил 7 мкг/кг массы тела предварительным переносимым уровнем еженедельного потребления. [95] В штате Калифорния требуется, чтобы на этикетках пищевых продуктов содержалось предупреждение о потенциальном воздействии кадмия на такие продукты, как какао-порошок. [96]
Управление по охране труда США (OSHA) установило допустимый предел воздействия (PEL) для кадмия на уровне средневзвешенного по времени значения (TWA) 0,005 частей на миллион. Национальный институт безопасности и гигиены труда (NIOSH) не установил рекомендуемый предел воздействия (REL) и назвал кадмий известным канцерогеном для человека. Уровень НДЛГ (непосредственно опасный для жизни и здоровья ) для кадмия составляет 9 мг/м 3 . [97]
Помимо ртути, присутствие в некоторых батареях кадмия привело к необходимости надлежащей утилизации (или переработки) батарей.
В мае 2006 года продажа сидений на старом стадионе футбольного клуба «Арсенал» Хайбери в Лондоне, Англия, была отменена, когда было обнаружено, что сиденья содержат следовые количества кадмия. [99] Сообщения о высоком уровне использования кадмия в детских украшениях в 2010 году привели к расследованию Комиссии по безопасности потребительских товаров США . [100] CPSC США выпустила специальные уведомления об отзыве ювелирных изделий, содержащих кадмий, которые продаются в магазинах Claire's [101] и Wal-Mart [102] .
В июне 2010 года McDonald's добровольно отозвал более 12 миллионов рекламных коллекционных стаканов для питья «Шрек навсегда 3D» из-за содержания кадмия в красочных пигментах на стеклянной посуде. [103] Очки были произведены компанией Arc International , Милвилл, Нью-Джерси , США. [104]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) CS1 maint: числовые имена: список авторов ( ссылка )