
В органической химии карбен — молекула , содержащая нейтральный атом углерода с двумя валентными и двумя неподеленными валентными электронами . Общая формула: R-:C-R' или R=C: где R представляет собой заместители или атомы водорода.
Термин «карбен» может также относиться к конкретному соединению :CH 2 , также называемому метиленом , исходному гидриду , из которого формально происходят все другие соединения карбена. [1] [2]
Существует два типа карбенов: синглеты и триплеты , в зависимости от их электронной структуры. [3] Различные классы подвергаются разным реакциям.
Большинство карбенов чрезвычайно реакционноспособны и недолговечны. Небольшое количество (дигалогенкарбены , окись углерода [4] и моносульфид углерода ) можно выделить и стабилизировать в виде металлических лигандов , но иначе их нельзя хранить в больших количествах . Редким исключением являются стойкие карбены , [5] имеющие широкое применение в современной металлоорганической химии .
Существует два распространенных метода получения карбена.
При α-элиминировании два заместителя удаляются от одного и того же атома углерода. Это происходит, когда реагенты, у которых нет хороших уходящих групп, вицинальных по отношению к кислому протону, подвергаются воздействию сильного основания; например, фениллитий отделяет HX от галоформы (CHX 3 ). [6] Такие реакции обычно требуют условий фазового переноса . [ нужна цитата ]
Молекулы, не содержащие кислых протонов, также могут образовывать карбены. Геминальный дигалогенид, подвергшийся воздействию литийорганических соединений , подвергается обмену металл-галоген , а затем отщепляет литиевую соль с образованием карбена, а металлический цинк отделяет галогены аналогичным образом в реакции Симмонса-Смита . [7]
Остается неясным, образуются ли в этих условиях действительно свободные карбены или комплекс металл-карбен. Тем не менее образующиеся таким образом металлокарбены дают ожидаемые органические продукты. [7] В специализированном, но поучительном случае α-галогенсодержащие соединения ртути можно выделить и отдельно термолизовать. «Реактив Зейферта» при нагревании выделяет CCl 2 :
Отдельно карбены могут быть получены реакцией экструзии с большим изменением свободной энергии. Диазирины и эпоксиды фотолизируются с огромным выделением карбенов при деформации кольца . Первые выдавливают инертный газообразный азот , но эпоксиды обычно дают реакционноспособные карбонильные отходы, а асимметричные эпоксиды потенциально могут образовывать два разных карбена. Обычно связь CO с меньшим дробным порядком связи (меньшее количество резонансных структур с двойной связью) разрывается. Например, когда один заместитель представляет собой алкил , а другой - арил , арилзамещенный углерод обычно высвобождается в виде карбенового фрагмента.
Кольцевая деформация не является необходимой для возникновения сильной термодинамической движущей силы. Фотолиз , тепло или катализаторы на основе переходных металлов (обычно родий и медь ) разлагают диазоалканы на карбен и газообразный азот ; это происходит в реакции Бэмфорда-Стивенса и перегруппировке Вольфа . Как и в случае с металлокарбенами, некоторые реакции диазоалканов, которые формально протекают через карбены, вместо этого могут образовывать промежуточный циклоаддукт [3+2] , который вытесняет азот.
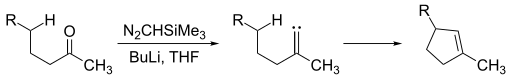
Для образования алкилиденкарбена кетон можно подвергнуть воздействию триметилсилилдиазометана , а затем сильного основания.

Двумя классами карбенов являются синглетные и триплетные карбены. Триплетные карбены представляют собой дирадикалы с двумя неспаренными электронами, обычно образуются в результате реакций, разрывающих две σ-связи (альфа-элиминирование и некоторые реакции экструзии), и не вызывают повторной гибридизации атома карбена. Синглетные карбены имеют одну неподеленную пару , обычно образуются в результате диазораспада и принимают орбитальную структуру sp2 . [8] Валентные углы (определенные методом ЭПР ) составляют 125–140° для триплетного метилена и 102° для синглетного метилена.
Большинство карбенов имеют нелинейное триплетное основное состояние. Для простых углеводородов триплетные карбены обычно всего лишь на 8 ккал / моль (33 кДж /моль) более стабильны, чем синглетные карбены, что сравнимо с инверсией азота . Стабилизация частично объясняется правилом максимальной множественности Хунда . Однако стратегии стабилизации триплетных карбенов при комнатной температуре неуловимы. Было показано, что 9-фторенилиден представляет собой быстро уравновешивающую смесь синглетных и триплетных состояний с разницей в энергии примерно 1,1 ккал/моль (4,6 кДж/моль), хотя обширная делокализация электронов в кольца усложняет любые выводы, сделанные на основе диарилкарбенов . [9] Моделирование показывает, что электроположительные гетероатомы могут термодинамически стабилизировать триплетные карбены, такие как силил- и силилокси- карбены, особенно трифторсилилкарбены. [10]
Льюис-основные азот, кислород, сера или галогенидные заместители , связанные с двухвалентным углеродом, могут делокализовать электронную пару на пустую p- орбиталь , чтобы стабилизировать синглетное состояние. Это явление лежит в основе замечательной стабильности стойких карбенов .
Карбены ведут себя как очень агрессивные кислоты Льюиса . Они могут атаковать неподеленные пары , но их основная синтетическая полезность связана с атаками на π-связи , которые дают циклопропаны; и на σ-связях , которые вызывают внедрение карбена . Другие реакции включают перегруппировки и димеризации. Реакционная способность конкретного карбена зависит от заместителей , включая любые присутствующие металлы .

Синглетные и триплетные карбены проявляют разную реакционную способность. [11] [ нужна страница ] [12]
Триплетные карбены являются дирадикалами и участвуют в ступенчатом радикальном присоединении . При присоединении триплетного карбена обязательно участвует (хотя бы один) интермедиат с двумя неспаренными электронами.
Синглетные карбены могут (и реагируют) как электрофилы , нуклеофилы или амбифилы. [4] Их реакции обычно согласованы и часто хелетропны . [ нужна цитация ] Синглетные карбены обычно электрофильны, [4] , если только у них нет заполненной p- орбитали, и в этом случае они могут реагировать как основания Льюиса. Реакция Бэмфорда-Стивенса дает карбены в апротонных растворителях и ионы карбения в протонных .
Различные механизмы подразумевают, что присоединения синглетных карбенов стереоспецифичны , а присоединения триплетных карбенов стереоселективны . Метилен в результате фотолиза диазометана реагирует либо с цис- , либо с транс - 2-бутеном , образуя единственный диастереомер 1,2- диметилциклопропана : цис из цис и транс из транс . Таким образом, метилен представляет собой синглетный карбен; если бы это был триплет, продукт не зависел бы от геометрии исходного алкена. [13]
Карбены присоединяются к двойным связям с образованием циклопропанов [ 14] и, в присутствии медного катализатора , к алкинам с образованием циклопропенов . Реакции присоединения обычно протекают очень быстро и экзотермично , а образование карбена ограничивает скорость реакции.
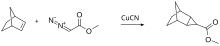
При циклопропанировании Симмонса-Смита йодид йодметилцинка обычно образует комплекс с любыми аллильными гидроксильными группами, так что присоединение происходит к гидроксильной группе .

Вставки — еще один распространенный тип реакции карбена, [15] форма окислительного присоединения . Вставки могут происходить, а могут и не происходить в один этап (см. выше). Конечным результатом является то, что карбен вставляется в существующую связь, предпочтительно X–H (X не углерод), в противном случае C–H или (в противном случае) связь C–C. Алкилкарбены встраиваются гораздо более избирательно, чем метилен, который не различает первичные, вторичные и третичные связи CH.

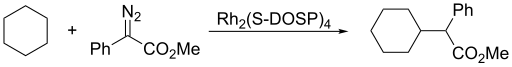
1,2-перегруппировка , возникающая в результате внутримолекулярного внедрения в связь, прилегающую к карбеновому центру, является помехой в некоторых реакционных схемах, поскольку она потребляет карбен, чтобы дать тот же эффект, что и традиционная реакция отщепления . [16] Как правило, жесткие структуры благоприятствуют внутримолекулярным внедрениям. В гибких структурах образование пятичленного кольца предпочтительнее образования шестичленного кольца. Когда такие вставки возможны, межмолекулярные вставки не наблюдаются. Как меж-, так и внутримолекулярные внедрения допускают асимметричную индукцию от хирального металлического катализатора.
Карбены могут образовывать аддукты с нуклеофилами и являются обычным предшественником различных 1,3-диполей . [16]

Карбены и предшественники карбеноидов могут димеризоваться до алкенов . Часто, но не всегда, это нежелательная побочная реакция; Димеризация карбенов металлов использовалась при синтезе полиалкинилэтенов и является основным промышленным путем получения тефлона (см. «Карбен § Промышленное применение»). Стойкие карбены приходят в равновесие со своими соответствующими димерами – равновесие Ванцлика .
В металлоорганических соединениях комплексы металлов с формулами L n MCRR' часто описываются как карбеновые комплексы. [17] Однако такие виды не реагируют как свободные карбены и редко образуются из предшественников карбенов, за исключением стойких карбенов. [ нужна цитация ] [18] Карбеновые комплексы переходных металлов можно классифицировать в зависимости от их реакционной способности, при этом первые два класса определены наиболее четко:

Масштабное применение карбенов — промышленное производство тетрафторэтилена , предшественника тефлона . Тетрафторэтилен образуется при посредничестве дифторкарбена : [22]
Введение карбенов в связи C–H широко используется, например, при функционализации полимерных материалов [23] и электроотверждении клеев . [24] Многие приложения основаны на синтетических 3-арил-3-трифторметилдиазиринах [ 25] [26] (предшественнике карбена, который может быть активирован теплом, [27] светом, [26] [27] или напряжением ) [28] [24] но существует целое семейство карбеновых красителей .
Карбены были впервые постулированы Эдуардом Бюхнером в 1903 году при исследованиях циклопропанирования этилдиазоацетата толуолом. [29] В 1912 году Герман Штаудингер [30] также превратил алкены в циклопропаны с диазометаном и CH 2 в качестве промежуточного продукта. Деринг в 1954 году продемонстрировал их синтетическую полезность с помощью дихлоркарбена . [31]