Литий (от древнегреческого λίθος ( líthos ) «камень») — химический элемент ; у него есть символ Li и атомный номер 3. Это мягкий серебристо-белый щелочной металл . В стандартных условиях это наименее плотный металл и наименее плотный твердый элемент. Как и все щелочные металлы, литий обладает высокой реакционной способностью и легковоспламеняемостью, поэтому его необходимо хранить в вакууме, инертной атмосфере или инертной жидкости, такой как очищенный керосин или минеральное масло. Он демонстрирует металлический блеск . На воздухе он быстро корродирует до тусклого серебристо-серого цвета, а затем чернеет. В природе он не встречается свободно, а встречается главным образом в виде пегматитовых минералов, которые когда-то были основным источником лития. Благодаря своей растворимости в виде иона он присутствует в океанской воде и обычно получается из рассолов . Металлический литий выделяют электролитически из смеси хлоридов лития и хлоридов калия .
Ядро атома лития граничит с нестабильностью, поскольку два стабильных изотопа лития , обнаруженные в природе, имеют одну из самых низких энергий связи на нуклон среди всех стабильных нуклидов . Из-за своей относительной ядерной нестабильности литий менее распространен в Солнечной системе, чем 25 из первых 32 химических элементов, хотя его ядра очень легкие: это исключение из тенденции, согласно которой более тяжелые ядра встречаются реже. [6] По этим же причинам литий имеет важное применение в ядерной физике . Трансмутация атомов лития в гелий в 1932 году была первой полностью рукотворной ядерной реакцией , а дейтерид лития служит термоядерным топливом в термоядерном оружии . [7]
Литий и его соединения имеют несколько промышленных применений, включая термостойкое стекло и керамику , литиевые смазочные материалы, флюсовые добавки для производства железа, стали и алюминия, литий-металлические батареи и литий-ионные батареи . Эти виды использования потребляют более трех четвертей производства лития. [ нужна ссылка ] [ когда? ]
Литий присутствует в биологических системах в следовых количествах. Он не имеет установленной метаболической функции. Препараты на основе лития полезны в качестве стабилизатора настроения и антидепрессанта при лечении психических заболеваний, таких как биполярное расстройство .

Щелочные металлы также называют семейством лития по имени его ведущего элемента. Как и другие щелочные металлы ( натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr)), литий имеет единственный валентный электрон , который в присутствии растворителей легко выделяется с образованием Li + . [8] По этой причине литий является хорошим проводником тепла и электричества, а также высокореактивным элементом, хотя он и наименее реактивный из щелочных металлов. Меньшая реакционная способность лития обусловлена близостью его валентного электрона к ядру (остальные два электрона находятся на 1s-орбитали , значительно ниже по энергии и не участвуют в химических связях). [8] Расплавленный литий значительно более реакционноспособен, чем его твердая форма. [9] [10]
Металлический литий достаточно мягок, чтобы его можно было резать ножом. Он серебристо-белый. На воздухе окисляется до оксида лития . [8] Его температура плавления 180,50 ° C (453,65 K; 356,90 ° F) [11] и температура кипения 1342 ° C (1615 K; 2448 ° F) [11] являются самыми высокими из всех щелочных металлов, в то время как его плотность 0,534 г/см 3 самая низкая.
Литий имеет очень низкую плотность (0,534 г/см 3 ), сравнимую с древесиной сосны . [12] Это наименее плотный из всех элементов, находящихся в твердом состоянии при комнатной температуре; следующий по легкости твердый элемент (калий, 0,862 г/см 3 ) плотнее более чем на 60%. За исключением гелия и водорода , в твердом состоянии он менее плотен, чем любой другой элемент в жидком состоянии, и составляет всего две трети плотности жидкого азота (0,808 г/см 3 ). [13] Литий может плавать на самых легких углеводородных маслах и является одним из трех металлов, которые могут плавать на воде, два других — натрий и калий .

Коэффициент теплового расширения лития в два раза выше, чем у алюминия , и почти в четыре раза больше, чем у железа . [14] Литий является сверхпроводящим ниже 400 мкК при стандартном давлении [15] и при более высоких температурах (более 9 К) при очень высоких давлениях (>20 ГПа). [16] При температуре ниже 70 К литий, как и натрий, претерпевает бездиффузионные фазовые превращения . При 4,2 К имеет ромбоэдрическую кристаллическую систему (с девятислойным интервалом повторов); при более высоких температурах он превращается в гранецентрированную кубическую , а затем в объемноцентрированную кубическую форму . При гелиевых температурах (4 К) преобладает ромбоэдрическая структура. [17] Множественные аллотропные формы были идентифицированы для лития при высоких давлениях. [18]
Литий имеет массовую удельную теплоемкость 3,58 килоджоуля на килограмм-кельвин, самую высокую из всех твердых тел. [19] [20] По этой причине металлический литий часто используется в охлаждающих жидкостях для теплопередачи . [19]
Встречающийся в природе литий состоит из двух стабильных изотопов : 6 Li и 7 Li, причем последний является более распространенным (95,15% естественного содержания ). [21] [22] Оба природных изотопа имеют аномально низкую энергию связи ядра на нуклон (по сравнению с соседними элементами таблицы Менделеева , гелием и бериллием ); Литий — единственный элемент с небольшим номером, который может производить чистую энергию посредством ядерного деления . Два ядра лития имеют более низкую энергию связи на нуклон, чем любые другие стабильные нуклиды, кроме водорода-1 , дейтерия и гелия-3 . [23] В результате этого, хотя литий очень легкий по атомному весу, он менее распространен в Солнечной системе, чем 25 из первых 32 химических элементов. [6] Охарактеризовано семь радиоизотопов , наиболее стабильными из которых являются 8 Li с периодом полураспада 838 мс и 9 Li с периодом полураспада 178 мс. Все остальные радиоактивные изотопы имеют период полураспада менее 8,6 мс. Самый короткоживущий изотоп лития — 4 Li, который распадается за счет испускания протонов и имеет период полураспада 7,6 × 10–23 с . [24] Изотоп Li -6 является одним из пяти стабильных нуклидов , которые имеют как нечетное число протонов, так и нечетное количество нейтронов. Остальные четыре стабильных нечетно -нечетных нуклида — водород-2 , бор-10 , азот-14 , и тантал-180м . [25]
7 Li — один из первичных элементов (или, точнее, первичных нуклидов ), образовавшихся в результате нуклеосинтеза Большого взрыва . Небольшое количество как 6 Li, так и 7 Li производится в звездах во время звездного нуклеосинтеза , но в дальнейшем оно « сгорает » так же быстро, как и производится. [26] 7 Li также может генерироваться в углеродных звездах . [27] Дополнительные небольшие количества как 6 Li, так и 7 Li могут образовываться в результате солнечного ветра, космических лучей, поражающих более тяжелые атомы, а также в результате радиоактивного распада 7 Be в ранней Солнечной системе . [28]
Изотопы лития существенно фракционируются в ходе самых разных природных процессов, [29] включая образование минералов (химическое осаждение), метаболизм и ионный обмен . Ионы лития замещают магний и железо в октаэдрических позициях глинистых минералов, где 6 Li предпочтительнее 7 Li, что приводит к обогащению легкого изотопа в процессах гиперфильтрации и изменения горных пород. Известно, что экзотический 11 Li имеет нейтронное гало с двумя нейтронами, вращающимися вокруг его ядра, состоящего из 3 протонов и 6 нейтронов. Процесс, известный как лазерное разделение изотопов, можно использовать для разделения изотопов лития, в частности 7 Li от 6 Li. [30]
Производство ядерного оружия и другие применения ядерной физики являются основным источником искусственного фракционирования лития, при этом легкий изотоп 6 Li сохраняется в промышленности и военных запасах до такой степени, что это вызывает небольшое, но измеримое изменение в соотношении 6 Li и 7 Li . в природных источниках, таких как реки. Это привело к необычной неопределенности в стандартизированном атомном весе лития, поскольку это количество зависит от природных соотношений содержания этих встречающихся в природе стабильных изотопов лития, поскольку они доступны в коммерческих минеральных источниках лития. [31]
Оба стабильных изотопа лития можно охлаждать лазером , и они были использованы для создания первой квантово-вырожденной бозе - фермиевской смеси. [32]

Хотя литий (вместе с бериллием и бором) был синтезирован во время Большого взрыва , во Вселенной его гораздо меньше, чем других элементов. Это результат сравнительно низких звездных температур, необходимых для разрушения лития, а также отсутствия общих процессов для его производства. [33]
Согласно современной космологической теории, литий — в обоих стабильных изотопах (литий-6 и литий-7) — был одним из трёх элементов, синтезированных в результате Большого взрыва. [34] Хотя количество лития, образующегося в ходе нуклеосинтеза Большого взрыва , зависит от числа фотонов на барион , для принятых значений можно рассчитать содержание лития, и во Вселенной существует « космологическое несоответствие лития »: более старые звезды, похоже, содержат меньше лития, чем следовало бы, а у некоторых более молодых звезд его гораздо больше. [35] Недостаток лития в старых звездах, по-видимому, вызван «подмешиванием» лития в недра звезд, где он разрушается, [36] тогда как в более молодых звездах литий образуется. Хотя он превращается в два атома гелия из-за столкновения с протоном при температуре выше 2,4 миллиона градусов по Цельсию (большинство звезд легко достигают этой температуры в своих недрах), лития в звездах более позднего поколения больше, чем предсказывают расчеты. [37]

Литий также содержится в субзвездных объектах коричневых карликов и некоторых аномальных оранжевых звездах. Поскольку литий присутствует в более холодных и менее массивных коричневых карликах, но разрушается в более горячих звездах красных карликов , его присутствие в спектрах звезд можно использовать в «литиевом тесте», чтобы различить их, поскольку оба они меньше Солнца. . [37] [39] [40] Некоторые оранжевые звезды также могут содержать высокую концентрацию лития. Эти оранжевые звезды, у которых обнаружено более высокое, чем обычно, содержание лития (например, Центавр X-4), вращаются вокруг массивных объектов — нейтронных звезд или черных дыр — чья гравитация, очевидно, притягивает более тяжелый литий к поверхности водородно-гелиевой звезды, вызывая увеличение количества лития. чтобы наблюдать. [37]
27 мая 2020 года астрономы сообщили, что взрывы классических новых являются галактическими производителями лития-7. [41] [42]
Хотя литий широко распространен на Земле, в природе он не встречается в элементарной форме из-за своей высокой реакционной способности. [8] Общее содержание лития в морской воде очень велико и оценивается в 230 миллиардов тонн, при этом элемент существует в относительно постоянной концентрации от 0,14 до 0,25 частей на миллион (ppm), [43] [44] или 25 микромолярных ; [45] более высокие концентрации, приближающиеся к 7 ppm, обнаруживаются вблизи гидротермальных источников . [44]
Оценки содержания земной коры варьируются от 20 до 70 частей на миллион по весу. [46] Литий составляет около 0,002 процента земной коры. [47] В соответствии со своим названием, литий образует незначительную часть магматических пород , с наибольшими концентрациями в гранитах . Гранитные пегматиты также обеспечивают наибольшее количество литийсодержащих минералов, причем наиболее коммерчески выгодными источниками являются сподумен и петалит . [46] Другим важным минералом лития является лепидолит , который в настоящее время является устаревшим названием для серии, образованной полилитионитом и трилитионитом. [48] [49] Другим источником лития является гекторитовая глина, единственная активная разработка которой осуществляется через Western Lithium Corporation в Соединенных Штатах. [50] При содержании лития 20 мг на кг земной коры [51] литий является 25-м по распространенности элементом.
Согласно Справочнику по литию и природному кальцию , «Литий — сравнительно редкий элемент, хотя он и встречается во многих горных породах и некоторых рассолах, но всегда в очень низких концентрациях. Существует довольно большое количество месторождений как литиевых минералов, так и рассолов, но лишь сравнительно немногие из них имеют фактическую или потенциальную коммерческую ценность. Многие из них очень малы, другие слишком низкого качества». [52]
По оценкам (2020 г.), Чили имеет самые большие запасы (9,2 миллиона тонн), [53] и Австралия - самый высокий годовой объем добычи (40 000 тонн). [53] Одна из крупнейших баз запасов [примечание 1] лития находится в районе Салар-де-Уюни в Боливии, где имеется 5,4 миллиона тонн. Другими крупными поставщиками являются Австралия, Аргентина и Китай. [54] [55] По состоянию на 2015 год Чешская геологическая служба считала все Рудные горы в Чехии литиевой провинцией. Зарегистрировано пять месторождений, одно возле Чиновца считается потенциально экономичным месторождением и содержит 160 000 тонн лития. [56] В декабре 2019 года финская горнодобывающая компания Keliber Oy сообщила, что ее литиевое месторождение Рапасаари оценивает доказанные и вероятные запасы руды в 5,280 млн тонн. [57]
В июне 2010 года газета The New York Times сообщила, что американские геологи проводят наземные исследования сухих соленых озер на западе Афганистана , полагая, что там расположены крупные месторождения лития. [58] Эти оценки «основаны главным образом на старых данных, которые были собраны в основном Советским Союзом во время оккупации Афганистана в 1979–1989 годах». [59] Министерство обороны оценило запасы лития в Афганистане на уровне запасов в Боливии и назвало его потенциальной «литиевой Саудовской Аравией». [60] В Корнуолле , Англия, о наличии рассола, богатого литием, было хорошо известно благодаря исторической горнодобывающей промышленности региона , и частные инвесторы провели испытания для изучения потенциальной добычи лития в этой области. [61] [62]
Литий содержится в следовых количествах во многих растениях, планктоне и беспозвоночных, в концентрациях от 69 до 5760 частей на миллиард (ppb). У позвоночных концентрация немного ниже, и почти все ткани и жидкости организма позвоночных содержат литий в диапазоне от 21 до 763 частей на миллиард. [44] Морские организмы склонны биоаккумулировать литий больше, чем наземные организмы. [63] Неизвестно, играет ли литий физиологическую роль в каком-либо из этих организмов. [44] Концентрация лития в тканях человека составляет в среднем около 24 частей на миллиард (4 частей на миллиард в крови и 1,3 частей на миллион в костях ). [64]
Литий легко усваивается растениями [64] , а концентрация лития в тканях растений обычно составляет около 1 ppm . [65] Некоторые семейства растений биоаккумулируют больше лития, чем другие. [65] Концентрация лития в сухом весе для представителей семейства пасленовых ( в которое входят картофель и томаты ), например, может достигать 30 частей на миллион, тогда как для кукурузных зерен она может достигать 0,05 частей на миллиард . [64] Исследования концентрации лития в богатой минералами почве дают диапазон от 0,1 до 50–100 частей на миллион , при этом некоторые концентрации достигают 100–400 частей на миллион, хотя маловероятно, что весь он доступен для поглощения растениями . [65] Накопление лития, по-видимому, не влияет на состав основных питательных веществ растений. [65] Толерантность к литию варьируется в зависимости от вида растений и обычно соответствует толерантности к натрию ; Например, кукуруза и трава Родоса очень устойчивы к повреждению литием, тогда как авокадо и соевые бобы очень чувствительны. [65] Аналогичным образом, литий в концентрации 5 ppm снижает всхожесть семян у некоторых видов (например, азиатского риса и нута ), но не у других (например, ячменя и пшеницы ). [65]
Многие из основных биологических эффектов лития можно объяснить его конкуренцией с другими ионами. [66 ]
Одновалентный ион лития Li+
конкурирует с другими ионами, такими как натрий (сразу ниже лития в таблице Менделеева ), который, как и литий, также является одновалентным щелочным металлом . Литий также конкурирует с ионами двухвалентного магния , ионный радиус которого (86 пм ) примерно равен иону лития [66] (90 пм). Механизмы, которые транспортируют натрий через клеточные мембраны, также транспортируют литий. Например, натриевые каналы (как потенциалзависимые, так и эпителиальные ) являются особенно важными путями поступления лития. [66]
Ионы лития также могут проникать через лиганд-управляемые ионные каналы , а также пересекать как ядерные , так и митохондриальные мембраны . [66]
Как и натрий, литий может проникать и частично блокировать (но не проникать ) калиевые и кальциевые каналы . [66]
Биологические эффекты лития многочисленны и разнообразны, но механизмы его действия изучены лишь частично. [67]
Например, исследования пациентов с биполярным расстройством , получавших литий, показывают, что, среди многих других эффектов, литий частично обращает вспять укорочение теломер у этих пациентов, а также увеличивает функцию митохондрий, хотя то, как литий оказывает эти фармакологические эффекты , не понятно. [67] [68]
Даже точные механизмы, участвующие в токсичности лития , до конца не изучены.

Петалит (LiAlSi 4 O 10 ) был открыт в 1800 году бразильским химиком и государственным деятелем Хосе Бонифасио де Андрада-э-Сильва в шахте на острове Уто , Швеция. [69] [70] [71] [72] Однако только в 1817 году Йохан Август Арфведсон , работавший тогда в лаборатории химика Йенса Якоба Берцелиуса , обнаружил присутствие нового элемента при анализе петалитовой руды. [73] [74] [75] [76] Этот элемент образовывал соединения, подобные соединениям натрия и калия , хотя его карбонат и гидроксид были менее растворимы в воде и менее щелочными . [77] Берцелиус дал щелочному материалу название « литион / литина », от греческого слова λιθoς (транслитерируемого как литос , что означает «камень»), чтобы отразить его открытие в твердом минерале, в отличие от калия, который был обнаружен в растительной золе и натрий, который был известен отчасти своим высоким содержанием в крови животных. Он назвал металл внутри материала «литием». [8] [71] [76]
Позднее Арфведсон показал, что этот же элемент присутствовал в минералах сподумене и лепидолите . [78] [71] В 1818 году Кристиан Гмелин первым заметил, что соли лития придают пламени ярко-красный цвет. [71] [79] Однако и Арфведсон, и Гмелин пытались, но не смогли изолировать чистый элемент от его солей. [71] [76] [80] Он не был выделен до 1821 года, когда Уильям Томас Бранде получил его путем электролиза оксида лития , процесса, который ранее использовался химиком сэром Хамфри Дэви для выделения щелочных металлов калия и натрия. [37] [80] [81] [82] [83] Бранде также описал некоторые чистые соли лития, такие как хлорид, и, подсчитав, что литий ( оксид лития ) содержит около 55% металла, оценил атомный вес лития. составлять около 9,8 г/моль (современное значение ~6,94 г/моль). [84] В 1855 году Роберт Бунзен и Август Маттиссен произвели большее количество лития посредством электролиза хлорида лития . [71] [85] Открытие этой процедуры привело к коммерческому производству лития в 1923 году немецкой компанией Metallgesellschaft AG , которая проводила электролиз жидкой смеси хлорида лития и хлорида калия . [71] [86] [87]
Австралийскому психиатру Джону Кейду приписывают повторное введение и популяризацию использования лития для лечения мании в 1949 году. [88] Вскоре после этого, в середине 20-го века, применение лития для стабилизации настроения при мании и депрессии стало широко применяться в Европе и Соединенных Штатах.
Производство и использование лития претерпело в истории несколько радикальных изменений. Первое крупное применение лития было в производстве высокотемпературных литиевых смазок для авиационных двигателей и аналогичных применений во время Второй мировой войны и вскоре после нее. Такое использование было подтверждено тем фактом, что мыло на основе лития имеет более высокую температуру плавления, чем другие щелочные мыла, и менее агрессивны, чем мыло на основе кальция. Небольшой спрос на литиевое мыло и смазочные материалы поддерживался несколькими небольшими горнодобывающими предприятиями, в основном в США.
Спрос на литий резко возрос во время Холодной войны с производством термоядерного оружия . И литий-6, и литий-7 производят тритий при облучении нейтронами и, таким образом, полезны для производства трития как такового, а также в качестве формы твердого термоядерного топлива, используемого внутри водородных бомб в форме дейтерида лития . США стали основным производителем лития в период с конца 1950-х по середину 1980-х годов. В итоге запасы лития составили примерно 42 000 тонн гидроксида лития. Запасы лития были обеднены литием-6 на 75%, что было достаточно, чтобы повлиять на измеренный атомный вес лития во многих стандартизированных химических веществах и даже на атомный вес лития в некоторых «природных источниках» ионов лития, которые были «загрязнены». "солями лития, выброшенными из установок разделения изотопов, которые попали в грунтовые воды. [31] [89]
Литий используется для снижения температуры плавления стекла и улучшения свойств плавления оксида алюминия в процессе Холла-Эру . [90] [91] Эти два применения доминировали на рынке до середины 1990-х годов. После окончания гонки ядерных вооружений спрос на литий снизился, а продажа энергетических запасов Министерства энергетики на открытом рынке еще больше снизила цены. [89] В середине 1990-х годов несколько компаний начали выделять литий из рассола , что оказалось менее дорогим вариантом, чем подземная или открытая добыча. Большинство рудников закрылись или переключили свое внимание на другие материалы, поскольку по конкурентоспособной цене можно было добывать только руду из зональных пегматитов. Например, шахты США возле Кингс-Маунтин , штат Северная Каролина, закрылись еще до начала XXI века.
Разработка литий-ионных батарей увеличила спрос на литий и стала доминирующим его применением в 2007 году. [92] С ростом спроса на литий в батареях в 2000-х годах новые компании расширили усилия по изоляции рассола, чтобы удовлетворить растущий спрос. [93] [94]
Утверждалось, что литий станет одним из главных объектов геополитической конкуренции в мире, работающем на возобновляемых источниках энергии и зависящем от батарей, но эта точка зрения также подвергалась критике за недооценку силы экономических стимулов для расширения производства. [95]
Литий реагирует с водой легко, но заметно с меньшей энергией, чем другие щелочные металлы. В результате реакции образуется газообразный водород и гидроксид лития . [8] При помещении в пламя соединения лития приобретают яркий малиновый цвет, но когда металл сильно горит, пламя становится блестящим серебром. Литий воспламеняется и горит в кислороде при контакте с водой или водяным паром. Во влажном воздухе литий быстро тускнеет с образованием черного налета из гидроксида лития (LiOH и LiOH·H 2 O), нитрида лития (Li 3 N) и карбоната лития (Li 2 CO 3 , в результате вторичной реакции между LiOH и СО 2 ). [46] Литий — один из немногих металлов, которые реагируют с газообразным азотом . [96] [97]
Из-за своей реакционной способности с водой и особенно с азотом металлический литий обычно хранят в углеводородном герметике, часто вазелине . Хотя более тяжелые щелочные металлы можно хранить под минеральным маслом , литий недостаточно плотный, чтобы полностью погрузиться в эти жидкости. [37]
Литий имеет диагональное отношение с магнием , элементом аналогичного атомного и ионного радиуса . Химическое сходство между двумя металлами включает образование нитрида при реакции с N 2 , образование оксида ( Li
2O ) и перекись ( Li
2О
2) при горении в O 2 , солях с одинаковой растворимостью и термической нестабильности карбонатов и нитридов. [46] [98] Металл реагирует с газообразным водородом при высоких температурах с образованием гидрида лития (LiH). [99]
Литий образует множество бинарных и тройных материалов в результате прямой реакции с элементами основной группы. Эти фазы Цинтла , хотя и обладают высокой ковалентностью, можно рассматривать как соли многоатомных анионов, таких как Si 4 4- , P 7 3- и Te 5 2- . С графитом литий образует множество интеркаляционных соединений . [98]
Он растворяется в аммиаке (и аминах) с образованием [Li(NH 3 ) 4 ] + и сольватированного электрона . [98]
Литий образует солеподобные производные со всеми галогенидами и псевдогалогенидами. Некоторые примеры включают галогениды LiF , LiCl , LiBr , LiI , а также псевдогалогениды и родственные анионы. Карбонат лития был описан как наиболее важное соединение лития. [98] Это белое твердое вещество является основным продуктом обогащения литиевых руд. Это предшественник других солей, включая керамику и материалы для литиевых батарей.
Соединения LiBH
4и ЛиАлХ
4являются полезными реагентами . Эти соли и многие другие соли лития обладают особенно высокой растворимостью в эфирах, в отличие от солей более тяжелых щелочных металлов.
В водном растворе для многих солей лития преобладает координационный комплекс [Li(H 2 O) 4 ] + . Известны родственные комплексы с аминами и простыми эфирами.
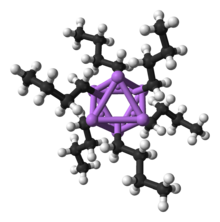
Литийорганические соединения многочисленны и полезны. Они определяются наличием связи между углеродом и литием. Они служат металлостабилизированными карбанионами , хотя их растворы и твердотельные структуры более сложны, чем это упрощенное представление. [100] Таким образом, это чрезвычайно мощные основания и нуклеофилы . Они также нашли применение в асимметричном синтезе в фармацевтической промышленности. Для лабораторного органического синтеза многие литийорганические реагенты коммерчески доступны в виде растворов. Эти реагенты высокореактивны, а иногда и пирофорны .
Как и его неорганические соединения, почти все органические соединения лития формально подчиняются правилу дуэта (например, BuLi , MeLi ). Однако важно отметить, что в отсутствие координирующих растворителей или лигандов литийорганические соединения образуют димерные, тетрамерные и гексамерные кластеры (например, BuLi фактически представляет собой [BuLi] 6 , а MeLi фактически представляет собой [MeLi] 4 ), которые характеризуются мульти- центральное соединение и увеличение координационного числа вокруг лития. Эти кластеры разбиваются на более мелкие или мономерные единицы в присутствии растворителей, таких как диметоксиэтан (ДМЭ), или лигандов, таких как тетраметилэтилендиамин (ТМЕДА). [101] В качестве исключения из правила дуэта кристаллографически охарактеризован двухкоординационный литатный комплекс с четырьмя электронами вокруг лития [Li(thf) 4 ] + [((Me 3 Si) 3 C) 2 Li] – . . [102]
Производство лития значительно возросло после окончания Второй мировой войны . Основными источниками лития являются рассолы и руды .
Металлический литий получают путем электролиза смеси 55% хлорида лития и 45% хлорида калия при температуре около 450 °C. [105]

Небольшой размер ионов затрудняет включение лития на ранние стадии кристаллизации минералов. В результате литий остается в расплавленной фазе, где он обогащается, пока не затвердеет на заключительных стадиях. Такое обогащение литием ответственно за все коммерчески перспективные месторождения литиевых руд . Рассолы (и сухая соль) являются еще одним важным источником Li + . Хотя число известных литийсодержащих месторождений и рассолов велико, большинство из них либо малы, либо имеют слишком низкие концентрации Li + . Таким образом, лишь немногие из них представляют коммерческую ценность. [106]
По оценкам Геологической службы США ( USGS), выявленные во всем мире запасы лития в 2020 и 2021 годах составят 17 миллионов и 21 миллион тонн соответственно. [54] [53] Точная оценка мировых запасов лития затруднена. [107] [108] Одной из причин этого является то, что большинство схем классификации лития разработаны для месторождений твердых руд, тогда как рассол представляет собой жидкость , которую проблематично обрабатывать по одной и той же схеме классификации из-за различных концентраций и эффектов перекачки. [109]
В 2019 году мировое производство лития из сподумена составило около 80 000 тонн в год, в основном из пегматита Гринбуш и из некоторых китайских и чилийских источников. Сообщается, что рудник Талисон в Гринбушесе является крупнейшим и имеет самое высокое содержание руды - 2,4% Li 2 O (данные за 2012 год). [110]
По данным Геологической службы США, в 2019 году в четверку крупнейших стран-производителей лития в мире вошли Австралия , Чили , Китай и Аргентина . [54]
Три страны – Чили , Боливия и Аргентина – содержат регион, известный как «литиевый треугольник» . Литиевый треугольник известен своими высококачественными солончаками, в число которых входят Салар-де-Уюни в Боливии , Салар-де-Атакама в Чили и Салар-де-Аризаро в Аргентине . Считается, что Литиевый треугольник содержит более 75% существующих известных запасов лития. [111] Месторождения также встречаются в Южной Америке по всей горной цепи Анд . Чили является ведущим производителем, за ним следует Аргентина. Обе страны извлекают литий из рассолов. По данным Геологической службы США, в пустыне Уюни в Боливии имеется 5,4 миллиона тонн лития. [112] [113] Половина известных в мире запасов расположена в Боливии вдоль центрально-восточного склона Анд. Правительство Боливии инвестировало 900 миллионов долларов США в производство лития и в 2021 году успешно произвело 540 тонн. [114] [112] Рассолы в соляных ваннах Литиевого треугольника сильно различаются по содержанию лития. [115] Концентрации также могут меняться во времени, поскольку рассолы представляют собой изменчивые и подвижные жидкости. [115]
В США литий добывают из рассолов в Неваде . [19]
С 2018 года известно, что Демократическая Республика Конго обладает крупнейшим в мире месторождением твердых пород литиевого сподумена . [116] Месторождение, расположенное в Маноно , ДРК , может содержать до 1,5 миллиардов тонн литиевого сподумена в твердых породах. Два крупнейших пегматита (известные как пегматит Carriere de l'Este и пегматит Roche Dure) имеют одинаковый размер или больше, чем знаменитый пегматит Greenbushes в Западной Австралии . Таким образом, ожидается, что Демократическая Республика Конго станет важным поставщиком лития в мир с его высоким качеством и низким содержанием примесей.
16 июля 2018 года на месторождении твердых пород Фальчани в регионе Пуно, Перу, было обнаружено 2,5 миллиона тонн высококачественного лития и 124 миллиона фунтов урана. [117] В 2020 году Австралия предоставила статус крупного проекта (MPS) литийовому проекту Finniss для стратегически важного месторождения лития: примерно 3,45 миллиона тонн (Мт) минеральных ресурсов с содержанием оксида лития 1,4 процента . [118] [119] Оперативная добыча началась в 2022 году. [120]
Месторождение, обнаруженное в 2013 году на поднятии Рок-Спрингс в Вайоминге , оценивается в 228 000 тонн. [ необходимы разъяснения ] Дополнительные залежи в том же пласте оцениваются в 18 миллионов тонн. [121] Аналогичным образом, в Неваде, в кальдере Макдермитта находятся литийсодержащие вулканические грязи, которые состоят из крупнейших известных месторождений лития в Соединенных Штатах. [122]
Известно, что в провинции Пампейских пегматитов в Аргентине в общей сложности имеется по меньшей мере 200 000 тонн сподумена с содержанием оксида лития (Li 2 O) в диапазоне от 5 до 8 мас.%. [123]
В России крупнейшее литиевое месторождение Колмозерское расположено в Мурманской области. В 2023 году право на разработку месторождения получила совместное предприятие «Норникеля» и «Росатома» «Полярный литий». Проект направлен на производство 45 000 тонн карбоната и гидроксида лития в год и планирует выйти на полную проектную мощность к 2030 году. [124]
Еще одним потенциальным источником лития по состоянию на 2012 год [обновлять]были идентифицированы фильтраты геотермальных скважин , которые выносятся на поверхность. [125] Восстановление этого типа лития было продемонстрировано в полевых условиях; литий отделяют простой фильтрацией. [126] [ необходимы разъяснения ] Запасы более ограничены, чем запасы рассолов и твердых пород. [ нужна цитата ]

В 1998 году цена металлического лития составляла около 95 долларов США/кг (или 43 доллара США/ фунт ). [127] После финансового кризиса 2007 года крупные поставщики, такие как Sociedad Química y Minera (SQM), снизили цены на карбонат лития на 20%. [128] Цены выросли в 2012 году. В статье Business Week 2012 года описывалась олигополия в сфере лития: «SQM, контролируемая миллиардером Хулио Понсе , является второй по величине, за ней следует Rockwood , поддерживаемая KKR & Co Генри Крависа. и FMC из Филадельфии», причем Талисон упоминается как крупнейший производитель. [129] Мировое потребление может подскочить до 300 000 метрических тонн в год к 2020 году [ не удалось проверить ] с примерно 150 000 тонн в 2012 году, чтобы соответствовать спросу на литиевые батареи, который растет примерно на 25% в год, опережая темпы роста с 4% до 5. % общего прироста производства лития. [129] [ нужно обновить ]
Служба информации о ценах ISE - Институт редкоземельных элементов и стратегических металлов - предоставляет на различные литиевые вещества в среднем с марта по август 2022 года следующие стабильные в курсе цены за килограмм: Карбонат лития, чистота 99,5% мин., от различных производителей от 63 и 72 евро/кг. Моногидрат гидроксида лития LiOH 56,5% мин., Китай, от 66 до 72 евро/кг; доставка Южная Корея - 73 евро/кг. Литий металлический не менее 99,9%, доставка Китай - 42 евро/кг. [130]

Литий и его соединения исторически были изолированы и извлечены из твердых пород, но к 1990-м годам доминирующим источником стали минеральные источники , рассолы и отложения рассола. [ нужна цитата ] Большинство из них находились в Чили, Аргентине и Боливии. [53] Крупные литий-глинистые месторождения, разрабатываемые в кальдере Макдермитт (Невада, США), требуют концентрированной серной кислоты для выщелачивания лития из глинистой руды. [131]
К началу 2021 года большая часть лития, добываемого во всем мире, будет происходить либо из « сподумена , минерала, содержащегося в твердых породах, обнаруженных в таких местах, как Австралия и Северная Каролина» [132] , либо из соленого рассола, выкачиваемого непосредственно из-под земли, как это в местах в Чили. [132] [115] В чилийском Салар-де-Атакама концентрация лития в рассоле повышается за счет солнечного испарения в системе прудов. [115] Процесс обогащения путем выпаривания может занять до полутора лет, когда содержание лития в рассоле достигнет 6%. [115] Окончательная обработка в этом примере производится недалеко от города Антофагаста на побережье, где из рассола производят чистый карбонат лития , гидроксид лития и хлорид лития . [115]
Ожидается, что катоды с низким содержанием кобальта для литиевых батарей потребуют в качестве сырья гидроксида лития , а не карбоната лития, и эта тенденция отдает предпочтение камню в качестве источника. [133] [134] [135]
Одним из методов извлечения лития, а также других ценных минералов , является обработка геотермальной морской воды через электролитическую ячейку, расположенную внутри мембраны. [136]
Было предложено использовать электродиализ и электрохимическую интеркаляцию для извлечения соединений лития из морской воды (которая содержит литий в количестве 0,2 части на миллион ). [137] [138] [139] [140] Ионоселективные клетки внутри мембраны в принципе могут собирать литий либо с помощью электрического поля , либо за счет разницы концентраций. [140]
Процессы производства лития, включая растворители и отходы горнодобывающей промышленности , представляют значительную опасность для окружающей среды и здоровья. [141] [142] [143] Извлечение лития может оказаться фатальным для водных организмов из-за загрязнения воды . [144] Известно, что он вызывает загрязнение поверхностных и питьевых вод, проблемы с дыханием, деградацию экосистем и ущерб ландшафту. [141] Это также приводит к нерациональному потреблению воды в засушливых регионах (1,9 млн литров на тонну лития). [141] Массовое образование побочных продуктов при экстракции лития также представляет собой нерешенные проблемы, такие как большое количество отходов магния и извести . [145]
В Соединенных Штатах добыча полезных ископаемых открытым способом и добыча на вершинах гор конкурирует с добычей соляных растворов . [146] Экологические проблемы включают деградацию среды обитания диких животных, загрязнение питьевой воды, включая загрязнение мышьяком и сурьмой , неустойчивое снижение уровня грунтовых вод и огромные отходы горнодобывающей промышленности , включая побочный радиоактивный уран и выбросы серной кислоты .
Исследование отношений между компаниями по добыче лития и коренными народами в Аргентине показало, что государство, возможно, не защищало право коренных народов на свободное предварительное и осознанное согласие , и что добывающие компании обычно контролировали доступ сообщества к информации и устанавливали условия для обсуждения проекты и распределение выгод. [147]
Разработка литиевого рудника Такер-Пасс в Неваде, США, вызвала протесты и судебные иски со стороны нескольких коренных племен, которые заявили, что им не было предоставлено свободное предварительное и осознанное согласие и что проект угрожает культурным и священным местам. [148] Они также выразили обеспокоенность тем, что реализация проекта создаст риски для женщин из числа коренного населения, поскольку добыча ресурсов связана с пропавшими без вести и убийствами женщин из числа коренного населения . [149] Протестующие оккупируют место предполагаемой шахты с января 2021 года. [150] [146]

В 2021 году большая часть лития будет использоваться для производства литий-ионных аккумуляторов для электромобилей и мобильных устройств .
Оксид лития широко используется в качестве флюса для обработки кремнезема , снижая температуру плавления и вязкость материала и приводя к получению глазурей с улучшенными физическими свойствами, включая низкие коэффициенты теплового расширения. Во всем мире это одно из крупнейших применений соединений лития. [152] [153] Для изготовления посуды используются глазури, содержащие оксиды лития. В этом применении обычно используется карбонат лития (Li 2 CO 3 ), поскольку он превращается в оксид при нагревании. [154]
В конце 20 века литий стал важным компонентом аккумуляторных электролитов и электродов из-за его высокого электродного потенциала . Из-за своей низкой атомной массы он имеет высокое соотношение заряда и мощности к весу . Типичная литий-ионная батарея может генерировать примерно 3 Вольта на ячейку по сравнению с 2,1 Вольт свинцово-кислотной и 1,5 Вольт угольно-цинковой батареи . Литий-ионные аккумуляторы, которые являются перезаряжаемыми и имеют высокую плотность энергии , отличаются от литий-металлических аккумуляторов , которые представляют собой одноразовые ( первичные ) аккумуляторы с литием или его соединениями в качестве анода . [155] [156] Другие перезаряжаемые батареи, в которых используется литий, включают литий-ионные полимерные батареи , литий-железо-фосфатные батареи и батареи нанопроволоки .
На протяжении многих лет мнения относительно потенциального роста расходились. Исследование 2008 года пришло к выводу, что «реально достижимого производства карбоната лития будет достаточно для удовлетворения лишь небольшой части будущих потребностей мирового рынка PHEV и EV », что «спрос со стороны сектора портативной электроники поглотит большую часть запланированного увеличения производства в следующее десятилетие». и что «массовое производство карбоната лития не является экологически безопасным, оно нанесет непоправимый экологический ущерб экосистемам, которые необходимо защищать, и что литий-ионные двигатели несовместимы с идеей «зеленого автомобиля»». [55]
Третье по распространенности использование лития — в смазках. Гидроксид лития является сильным основанием и при нагревании с жиром образует мыло, такое как стеарат лития из стеариновой кислоты . Литиевое мыло обладает способностью загущать масла и используется для производства универсальных высокотемпературных смазок . [19] [157] [158]
Литий (например, в виде карбоната лития) используется в качестве добавки к флюсовым шлакам форм непрерывной разливки , где он повышает текучесть, [159] [160] использование, на долю которого приходится 5% мирового использования лития (2011 г.). [54] Соединения лития также используются в качестве добавок (флюсов) к литейному песку для чугунного литья для уменьшения прожилок. [161]
Литий (как фторид лития ) используется в качестве добавки в алюминиевых заводах ( процесс Холла-Эру ), снижая температуру плавления и увеличивая электрическое сопротивление, [162] использование, на которое приходится 3% производства (2011 г.). [54]
При использовании в качестве флюса для сварки или пайки металлический литий способствует плавлению металлов в процессе [163] и исключает образование оксидов за счет поглощения примесей. [164] Сплавы металла с алюминием, кадмием , медью и марганцем используются для изготовления высокопроизводительных деталей самолетов низкой плотности (см. также Литий-алюминиевые сплавы ). [165]
Было обнаружено, что литий эффективен в совершенствовании кремниевых наносварных швов в электронных компонентах электрических батарей и других устройств. [166]

Соединения лития используются в качестве пиротехнических красителей и окислителей в красных фейерверках и ракетах . [19] [168]
Хлорид лития и бромид лития гигроскопичны и используются в качестве осушителей газовых потоков. [19] Гидроксид лития и пероксид лития — это соли, наиболее часто используемые в закрытых помещениях, например, на борту космических кораблей и подводных лодок , для удаления углекислого газа и очистки воздуха. Гидроксид лития поглощает углекислый газ из воздуха, образуя карбонат лития, и предпочтителен по сравнению с другими щелочными гидроксидами из-за его небольшого веса.
Пероксид лития (Li 2 O 2 ) в присутствии влаги не только реагирует с углекислым газом с образованием карбоната лития, но и выделяет кислород. [169] [170] Реакция следующая:
Некоторые из вышеупомянутых соединений, а также перхлорат лития используются в кислородных свечах , снабжающих подводные лодки кислородом . Они также могут включать небольшое количество бора , магния , алюминия , кремния , титана , марганца и железа . [171]
Фторид лития , искусственно выращенный в виде кристалла , является прозрачным и часто используется в специальной оптике для ИК- , УФ- и ВУФ-приложений ( вакуумного УФ-излучения ). Он имеет один из самых низких показателей преломления и самый дальний диапазон пропускания в глубоком УФ-диапазоне среди большинства распространенных материалов. [172] Мелкодисперсный порошок фторида лития использовался для дозиметрии термолюминесцентного излучения (ТЛД): когда его образец подвергается воздействию радиации, в нем накапливаются кристаллические дефекты , которые при нагревании разрешаются через выделение голубоватого света, интенсивность которого пропорциональна поглощенная доза , что позволяет определить ее количественно. [173] Фторид лития иногда используется в фокусных линзах телескопов . [19] [174]
Высокая нелинейность ниобата лития также делает его полезным в приложениях нелинейной оптики . Он широко используется в телекоммуникационной продукции, такой как мобильные телефоны и оптические модуляторы , а также в таких компонентах, как резонансные кристаллы . Литиевые приложения используются более чем в 60% мобильных телефонов. [175]
Литийорганические соединения широко используются в производстве полимеров и продуктов тонкой химии. В полимерной промышленности, которая является доминирующим потребителем этих реагентов, соединения алкиллития являются катализаторами / инициаторами [176] анионной полимеризации нефункционализированных олефинов . [177] [178] [179] Для производства тонких химикатов литийорганические соединения действуют как сильные основания и как реагенты для образования углерод-углеродных связей . Литийорганические соединения получают из металлического лития и алкилгалогенидов . [180]
Многие другие соединения лития используются в качестве реагентов для получения органических соединений. Некоторые популярные соединения включают литий-алюминийгидрид (LiAlH 4 ), триэтилборгидрид лития , н -бутиллитий и трет -бутиллитий .
_MK-50_Torpedo_is_launched_from_guided_missile_destroyer_USS_Bulkeley_(DDG_84).jpg/440px-US_Navy_040626-N-5319A-006_An_Anti-Submarine_Warfare_(ASW)_MK-50_Torpedo_is_launched_from_guided_missile_destroyer_USS_Bulkeley_(DDG_84).jpg)
Металлический литий и его сложные гидриды , например литийалюминийгидрид (LiAlH4 ) , используются в качестве высокоэнергетических добавок к ракетному топливу . [37] LiAlH 4 также может использоваться сам по себе в качестве твердого топлива . [181]
В двигательной установке торпеды Mark 50 с запасом химической энергии (SCEPS) используется небольшой резервуар с гексафторидом серы , который распыляется на блок твердого лития. В результате реакции выделяется тепло, создавая пар , приводящий в движение торпеду по замкнутому циклу Ренкина . [182]
Гидрид лития , содержащий литий-6, используется в термоядерном оружии , где служит топливом для термоядерной ступени бомбы. [183]
Литий-6 ценится как исходный материал для производства трития и как поглотитель нейтронов при ядерном синтезе . Природный литий содержит около 7,5% лития-6, из которого путем разделения изотопов было получено большое количество лития-6 для использования в ядерном оружии . [184] Литий-7 привлек интерес к использованию в теплоносителях ядерных реакторов . [185]

Дейтерид лития был выбран в качестве термоядерного топлива в ранних версиях водородной бомбы . При бомбардировке нейтронами и 6 Li , и 7 Li производят тритий — эта реакция, которая не была полностью понята при первых испытаниях водородных бомб , была ответственна за неконтролируемую мощность ядерного испытания в Касл-Браво . Тритий сплавляется с дейтерием в реакции термоядерного синтеза , которую относительно легко осуществить. Хотя подробности остаются секретными, дейтерид лития-6, очевидно, все еще играет роль в современном ядерном оружии в качестве термоядерного материала. [186]
Фторид лития , когда он сильно обогащен изотопом лития-7, образует основной компонент смеси фторидных солей LiF- BeF 2 , используемой в жидкофторидных ядерных реакторах . Фторид лития исключительно химически стабилен, а смеси LiF-BeF 2 имеют низкие температуры плавления. Кроме того, 7 Li, Be и F относятся к числу немногих нуклидов с достаточно низкими сечениями захвата тепловых нейтронов, чтобы не отравлять реакции деления внутри ядерного реактора деления. [примечание 3] [187]
В концептуальных (гипотетических) термоядерных электростанциях литий будет использоваться для производства трития в реакторах с магнитным удержанием , использующих дейтерий и тритий в качестве топлива. Встречающийся в природе тритий чрезвычайно редок, и его необходимо производить синтетически, окружая реагирующую плазму «одеялом», содержащим литий, где нейтроны из реакции дейтерия-трития в плазме будут расщеплять литий с образованием большего количества трития:
Литий также используется в качестве источника альфа-частиц или ядер гелия . При бомбардировке 7 Li ускоренными протонами образуется 8 Be , который практически сразу подвергается делению с образованием двух альфа-частиц. Этот подвиг, получивший в то время название «расщепление атома», был первой ядерной реакцией , полностью созданной человеком . Он был произведен Кокрофтом и Уолтоном в 1932 году. [188] [189] Инжекция литиевых порошков используется в термоядерных реакторах для управления взаимодействиями плазмы и материала и рассеивания энергии на границе горячей плазмы термоядерного синтеза. [190] [191]
В 2013 году Счетная палата правительства США заявила, что нехватка лития-7, критическая для работы 65 из 100 американских ядерных реакторов, «ставит под некоторый риск их способность продолжать производить электроэнергию». Касл Браво впервые использовал литий-7 в своем первом устройстве «Креветка» , которое весило всего 10 тонн, и вызвало массовое ядерное загрязнение атмосферы атолла Бикини . Возможно, именно этим и объясняется упадок ядерной инфраструктуры США. [192] Оборудование, необходимое для отделения лития-6 от лития-7, по большей части осталось от времен холодной войны. США остановили большую часть этого оборудования в 1963 году, когда у них был огромный избыток выделенного лития, который в основном потреблялся в двадцатом веке. В отчете говорится, что потребуется пять лет и от 10 до 12 миллионов долларов, чтобы восстановить способность отделять литий-6 от лития-7. [193]
Реакторы, в которых используется литий-7, нагревают воду под высоким давлением и передают тепло через теплообменники, склонные к коррозии. В реакторах используется литий для противодействия коррозионному воздействию борной кислоты , которую добавляют в воду для поглощения лишних нейтронов. [193]
Литий полезен при лечении биполярного расстройства . [194] Соли лития также могут быть полезны при сопутствующих диагнозах, таких как шизоаффективное расстройство и циклическая большая депрессия . Активной частью этих солей является ион лития Li + . [194] Литий может увеличить риск развития сердечной аномалии Эбштейна у младенцев, рожденных от женщин, принимавших литий в первом триместре беременности. [195]
Металлический литий вызывает коррозию и требует особого обращения во избежание контакта с кожей. Вдыхание литиевой пыли или соединений лития (которые часто являются щелочными) первоначально вызывает раздражение носа и горла , тогда как более сильное воздействие может вызвать накопление жидкости в легких , что приводит к отеку легких . Сам металл представляет опасность при обращении с ним, поскольку при контакте с влагой образуется едкий гидроксид лития . Литий безопасно хранится в нереактивных соединениях, таких как нафта . [198]
Загадочная космическая фабрика производит литий.
Ученые теперь приближаются к выяснению происхождения этого вещества.
{{cite web}}: CS1 maint: bot: original URL status unknown (link), Афхандлингар и Фисик, Кеми и Минералоги , 6 : 145–172. (на шведском языке)с.
238 Es löste sich in diesem ein Salz auf, das an der Luft zerfloss, und nach Art der Strontiansalze den Alkohol mit einer purpurrothen Flamme brennen machte.
(В этом [растворителе, а именно абсолютном спирте] растворялась соль, которая растворялась на воздухе и, подобно солям стронция, заставляла спирт гореть пурпурно-красным пламенем.)
{{cite web}}: CS1 maint: bot: original URL status unknown (link)определения: Слайды 8–10 (глава 14).
{{cite book}}: CS1 maint: multiple names: authors list (link){{cite journal}}: CS1 maint: DOI inactive as of January 2024 (link){{cite web}}: CS1 maint: multiple names: authors list (link){{cite journal}}: CS1 maint: multiple names: authors list (link){{cite book}}: CS1 maint: bot: original URL status unknown (link), Академическая пресса. ISBN 0-12-352651-5 , с. 1089 {{cite book}}: |journal=игнорируется ( помощь )