В химии переходный металл (или переходный элемент ) — химический элемент в d-блоке таблицы Менделеева (группы с 3 по 12), хотя элементы 12 группы (и реже группы 3 ) иногда исключаются. Элементы лантаноидов и актинидов ( f-блок ) называются внутренними переходными металлами и иногда также считаются переходными металлами.
Поскольку это металлы, они блестящие и обладают хорошей электро- и теплопроводностью. Большинство из них (за исключением групп 11 и 12) тверды и прочны, имеют высокие температуры плавления и кипения. Они образуют соединения в любой из двух или более различных степеней окисления и связываются с различными лигандами , образуя координационные комплексы , которые часто окрашены. Они образуют множество полезных сплавов и часто используются в качестве катализаторов в элементарной форме или в таких соединениях, как координационные комплексы и оксиды . Большинство из них , как и многие их соединения, являются сильно парамагнитными из-за неспаренных d-электронов . Все элементы, которые являются ферромагнитными при комнатной температуре, являются переходными металлами ( железо , кобальт и никель ) или внутренними переходными металлами ( гадолиний ).
Английский химик Чарльз Ругли Бери (1890–1968) впервые использовал слово « переход» в этом контексте в 1921 году, когда имел в виду переходный ряд элементов при изменении внутреннего слоя электронов (например, n = 3 в 4-м ряду периодической таблицы) из стабильной группы из 8 в одну из 18 или из 18 в 32. [1] [2] [3] Эти элементы теперь известны как d-блок.

В Принципах химической номенклатуры ИЮПАК 2011 года «переходный металл» описывается как любой элемент в группах с 3 по 12 таблицы Менделеева . [4] Это в точности соответствует элементам d-блока , и многие учёные используют это определение. [5] [6] На практике ряды лантаноидов и актинидов f-блока называются «внутренними переходными металлами». Красная книга 2005 года допускает исключение элементов группы 12, но не Принципы 2011 года . [7]
Золотая книга ИЮПАК [8] определяет переходный металл как « элемент , атом которого имеет частично заполненную подоболочку d или который может давать начало катионам с неполной подоболочкой d», но это определение взято из старого издание Красной книги и в нынешнем издании более не присутствует. [7]
В d-блоке атомы элементов имеют от нуля до десяти d-электронов.
Опубликованные тексты и таблицы Менделеева показывают различия в отношении более тяжелых членов группы 3 . [9] Обычное расположение лантана и актиния в этих положениях не подтверждается физическими, химическими и электронными доказательствами , [10] [11] [12] которые в подавляющем большинстве поддерживают размещение лютеция и лоуренция в этих местах. [13] [14] Некоторые авторы предпочитают оставлять пробелы под иттрием в качестве третьего варианта, но существует путаница относительно того, подразумевает ли этот формат, что группа 3 содержит только скандий и иттрий, или она также содержит все лантаноиды и актиниды; [15] [16] [17] [18] [19] кроме того, он создает f-блок шириной 15 элементов, тогда как квантовая механика требует, чтобы f-блок имел ширину только 14 элементов. [15] Форма с лютецием и лоуренсием в группе 3 поддерживается отчетом IUPAC 1988 года по физическим, химическим и электронным основаниям, [20] и снова предварительным отчетом IUPAC 2021 года, поскольку это единственная форма, которая допускает одновременное (1 ) сохранение последовательности возрастания атомных номеров, (2) f-блок шириной в 14 элементов и (3) предотвращение разделения d-блока. [15] В современной литературе все еще можно найти аргументацию, защищающую форму с лантаном и актинием в группе 3, но многие авторы считают ее логически непоследовательной (особым предметом разногласий является различное обращение с актинием и торием , которое оба могут использовать 5f в качестве валентной орбитали , но не занимают 5f в качестве отдельных атомов); [14] [21] [22] большинство исследователей, рассматривающих проблему, согласны с обновленной формой с лютецием и лоуренцием. [14]
Элементы 12-й группы цинк , кадмий и ртуть иногда исключаются из числа переходных металлов. [1] Это потому, что они имеют электронную конфигурацию [ ]d 10 s 2 , где d-оболочка является полной, [23] и они все еще имеют полную d-оболочку во всех известных им степенях окисления . Поэтому элементы группы 12 Zn, Cd и Hg при определенных критериях могут быть классифицированы в этом случае как постпереходные металлы . Однако часто бывает удобно включить эти элементы в обсуждение переходных элементов. Например, при обсуждении энергии стабилизации кристаллического поля переходных элементов первого ряда удобно также включать элементы кальций и цинк, поскольку оба Ca2+
и цинк2+
имеют нулевое значение, с которым можно сравнивать значение для других ионов переходных металлов. Другой пример имеет место в ряду констант устойчивости комплексов Ирвинга – Вильямса . Более того, Zn, Cd и Hg могут использовать свои d-орбитали для связывания , даже если они не известны в состояниях окисления, которые формально потребовали бы разрыва d-подоболочки, что отличает их от элементов p-блока. [24] [25] [26]
Недавний (хотя и оспариваемый и до сих пор не воспроизведенный независимо) синтез фторида ртути(IV) ( HgF
4) было принято некоторыми, чтобы укрепить мнение о том, что элементы группы 12 следует считать переходными металлами, [27] , но некоторые авторы все еще считают это соединение исключительным. [28] Ожидается, что коперниций сможет использовать свои d-электроны в химии, поскольку его 6d- оболочка дестабилизирована сильными релятивистскими эффектами из-за его очень высокого атомного номера, и поэтому ожидается, что он будет вести себя подобно переходному металлу и демонстрировать более высокие степени окисления, чем +2 (которые точно не известны для более легких элементов 12 группы). Прогнозируется , что даже в чистых вариантах Cn 2+ будет равен 6d 8 7s 2 , в отличие от Hg 2+ , который равен 5d 10 6s 0 .
Хотя мейтнерий , дармштадтий и рентгений находятся внутри d-блока и, как ожидается, будут вести себя как переходные металлы, аналогичные их более легким родственникам иридию , платине и золоту , это еще не подтверждено экспериментально. Неясно , ведет ли коперниций больше сходство с ртутью или имеет свойства, более схожие со свойствами благородного газа радона . Относительная инертность Cn может быть обусловлена релятивистски расширенной энергетической щелью 7s–7p 1/2 , которая уже намечена в щели 6s–6p 1/2 для Hg, ослабляя металлические связи и вызывая ее хорошо известные низкие температуры плавления и кипения.
Ранние переходные металлы находятся в левой части таблицы Менделеева от группы 3 до группы 7. Поздние переходные металлы находятся в правой части d-блока, от группы 8 до 11 (и 12, если ее считать переходными металлами).
Тяжелые элементы 2-й группы кальций , стронций и барий не имеют заполненных d-орбиталей в виде отдельных атомов, но, как известно, в некоторых соединениях участвуют d-орбитальные связи , и по этой причине их называют «почетными» переходными металлами. [29] Вероятно, то же самое можно сказать и о радие . [30]
Элементы f-блока La–Yb и Ac–No обладают химической активностью (n-1)d-оболочки, но, что важно, также обладают химической активностью (n-2)f-оболочки, отсутствующей у элементов d-блока. Следовательно, их часто рассматривают отдельно как внутренние переходные элементы.
Общая электронная конфигурация атомов d-блока: [благородный газ]( n - 1)d 0–10 ns 0–2 n p 0–1 . Здесь «[благородный газ]» — это электронная конфигурация последнего благородного газа, предшествующего рассматриваемому атому, а n — высшее главное квантовое число занятой орбитали в этом атоме. Например, Ti ( Z = 22) находится в периоде 4, так что n = 4, первые 18 электронов имеют ту же конфигурацию, что и Ar в конце периода 3, а общая конфигурация равна [Ar]3d 2 4s 2 . Переходные металлы периодов 6 и 7 также добавляют 14 электронов ядра ( n - 2)f , которые не включены в таблицы ниже. P-орбитали почти никогда не заполнены свободными атомами (единственным исключением является лоуренсий из-за релятивистских эффектов, которые становятся важными при таких высоких Z ), но они могут способствовать образованию химических связей в соединениях переходных металлов.
Правило Маделунга предсказывает, что внутренняя d-орбиталь заполняется после орбитали валентной оболочки . Типичная электронная структура атомов переходных металлов тогда записывается как [благородный газ] n s 2 ( n - 1)d m . Это правило приблизительное, но справедливо для большинства переходных металлов. Даже если это не соответствует нейтральному основному состоянию, оно точно описывает низколежащее возбужденное состояние.
Подоболочка d является предпоследней подоболочкой и обозначается как ( n − 1)d подоболочка. Число s-электронов в самой внешней s-подоболочке обычно составляет один или два, за исключением палладия (Pd), где в этой s-подоболочке нет электронов в основном состоянии. Подоболочка s в валентной оболочке представлена как подоболочка n s, например 4s. В периодической таблице переходные металлы представлены в десяти группах (от 3 до 12).
Элементы группы 3 имеют конфигурацию n s 2 ( n − 1)d 1 , за исключением лоуренсия (Lr): его конфигурация 7s 2 7p 1 в исключительных случаях вообще не заполняет 6d-орбитали. Первая переходная серия присутствует в 4-м периоде и начинается после Са ( Z = 20) группы 2 с конфигурацией [Ar]4s 2 , или скандия (Sc), первого элемента группы 3 с атомным номером Z = 21. и конфигурация [Ar]4s 2 3d 1 в зависимости от используемого определения. По мере движения слева направо электроны добавляются в одну и ту же подоболочку d, пока она не завершится. Поскольку добавленные электроны заполняют ( n − 1)d-орбитали, свойства элементов d-блока сильно отличаются от свойств элементов s- и p-блока, у которых заполнение происходит либо по s, либо по p-орбиталям валентной оболочки. Электронная конфигурация отдельных элементов, присутствующих во всех сериях d-блоков, приведена ниже: [31]
Внимательный взгляд на электронную конфигурацию элементов показывает, что из правила Маделунга существуют определенные исключения . Для Cr, например, правило предсказывает конфигурацию 3d 4 4s 2 , но наблюдаемые атомные спектры показывают, что реальное основное состояние — это 3d 5 4s 1 . Чтобы объяснить такие исключения, необходимо учитывать влияние увеличения заряда ядра на орбитальные энергии, а также электрон-электронные взаимодействия, включая как кулоновское отталкивание , так и обменную энергию . [31] Исключения в любом случае не очень важны для химии, поскольку разница в энергии между ними и ожидаемой конфигурацией всегда довольно мала. [32]
( n - 1)d-орбитали, участвующие в переходных металлах, очень важны, поскольку они влияют на такие свойства, как магнитный характер, переменные степени окисления, образование окрашенных соединений и т. д. Валентные s- и p-орбитали ( ns и n p) имеют очень небольшой вклад в этом отношении, поскольку они почти не меняются при движении слева направо в переходном ряду. В переходных металлах наблюдается большее горизонтальное сходство свойств элементов в периоде по сравнению с периодами, в которых d-орбитали не участвуют. Это связано с тем, что в переходной серии электронная конфигурация валентной оболочки элементов не меняется. Однако есть и некоторые сходства между группами.
Переходные элементы обладают рядом свойств, которых нет у других элементов, что является результатом частично заполненной оболочки d. К ним относятся
Большинство переходных металлов могут быть связаны с различными лигандами , что позволяет образовывать самые разнообразные комплексы переходных металлов. [34]

Цвет соединений металлов переходного ряда обычно обусловлен электронными переходами двух основных типов.
Переход с переносом заряда металл-лиганд (MLCT) будет наиболее вероятен, когда металл находится в низкой степени окисления и лиганд легко восстанавливается.
Обычно переходы с переносом заряда приводят к более интенсивным цветам, чем переходы d – d.
В центросимметричных комплексах, таких как октаэдрические, переходы d–d запрещены правилом Лапорта и происходят только из-за вибронной связи , при которой молекулярное колебание происходит вместе с переходом ad–d. Тетраэдрические комплексы имеют несколько более интенсивный цвет, поскольку смешивание d- и p-орбиталей возможно при отсутствии центра симметрии, поэтому переходы не являются чистыми d-d-переходами. Молярная поглощательная способность (ε) полос, обусловленных d–d-переходами, относительно невелика, примерно в диапазоне 5–500 М–1 см – 1 (где M = моль дм –3 ). [35] Некоторые d–d-переходы запрещены по спину . Пример встречается в октаэдрических высокоспиновых комплексах марганца (II), который имеет конфигурацию ad 5 , в которой все пять электронов имеют параллельные спины; окраска таких комплексов значительно слабее, чем у комплексов со спин-разрешенными переходами. Многие соединения марганца(II) кажутся почти бесцветными. Спектр [ Mn(H
2О)
6]2+
показывает максимальную молярную поглощающую способность около 0,04 М -1 см -1 в видимом спектре .
Характерной чертой переходных металлов является то, что они проявляют две или более степени окисления , обычно отличающиеся на одну. Например, соединения ванадия известны во всех степенях окисления от -1, например [V (CO)
6]−
и +5, например VO3−
4.
Элементы основной группы в группах с 13 по 18 также проявляют несколько степеней окисления. «Общие» степени окисления этих элементов обычно различаются на две, а не на одну. Например, существуют соединения галлия в степенях окисления +1 и +3, в которых имеется один атом галлия. Соединения Ga(II) имеют неспаренный электрон, ведут себя как свободные радикалы и обычно быстро разрушаются, но известны некоторые стабильные радикалы Ga(II). [36] Галлий также имеет формальную степень окисления +2 в димерных соединениях, таких как [Ga
2кл
6]2-
, которые содержат связь Ga-Ga, образованную неспаренным электроном на каждом атоме Ga. [37] Таким образом, основное различие в степенях окисления между переходными элементами и другими элементами заключается в том, что известны состояния окисления, в которых имеется один атом элемента и один или несколько неспаренных электронов.
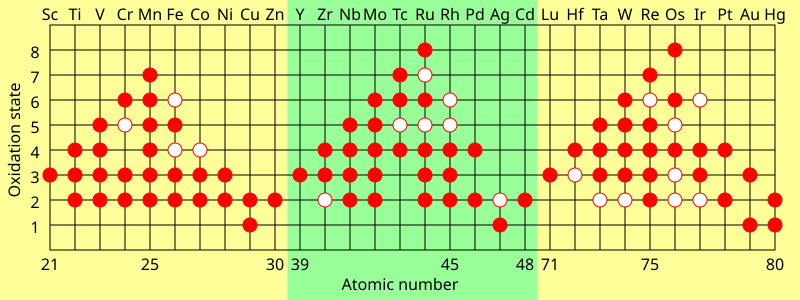
Максимальная степень окисления у переходных металлов первого ряда равна числу валентных электронов от титана (+4) до марганца (+7), но уменьшается у более поздних элементов. Во втором ряду максимум приходится на рутений (+8), а в третьем ряду максимум приходится на иридий (+9). В таких соединениях, как [MnO
4]−
и ОсО
4, элементы достигают стабильной конфигурации за счет ковалентной связи .
Наименьшие степени окисления проявляются у карбонильных комплексов металлов, таких как Cr (CO)
6(степень окисления ноль) и [Fe(CO)
4]2-
(степень окисления -2), при которой соблюдается правило 18 электронов . Эти комплексы также ковалентны.
Ионные соединения в основном образуются со степенями окисления +2 и +3. В водном растворе ионы гидратируются (обычно) шестью молекулами воды, расположенными октаэдрически.
Соединения переходных металлов являются парамагнитными, если у них есть один или несколько неспаренных d-электронов. [38] В октаэдрических комплексах с четырьмя и семью d-электронами возможны как высокоспиновые , так и низкоспиновые состояния. Тетраэдрические комплексы переходных металлов, такие как [FeCl
4]2-
имеют высокий спин, потому что расщепление кристаллического поля мало, так что энергия, которую можно получить за счет нахождения электронов на орбиталях с более низкой энергией, всегда меньше, чем энергия, необходимая для объединения спинов в пары. Некоторые соединения диамагнитны . К ним относятся октаэдрические, низкоспиновые, d6 и плоскоквадратные d8 комплексы . В этих случаях расщепление кристаллического поля таково, что все электроны спарены.
Ферромагнетизм возникает, когда отдельные атомы являются парамагнитными, а векторы спина ориентированы параллельно друг другу в кристаллическом материале. Металлическое железо и сплав алнико являются примерами ферромагнитных материалов, содержащих переходные металлы. Антиферромагнетизм — еще один пример магнитного свойства, возникающего в результате особого расположения отдельных спинов в твердом состоянии.
Переходные металлы и их соединения известны своей гомогенной и гетерогенной каталитической активностью. Эта активность объясняется их способностью принимать несколько степеней окисления и образовывать комплексы. Оксид ванадия (V) (в контактном процессе ), мелкодисперсное железо (в процессе Габера ) и никель (в каталитическом гидрировании ) являются лишь некоторыми примерами. Катализаторы на твердой поверхности ( катализаторы на основе наноматериалов ) предусматривают образование связей между молекулами реагентов и атомами поверхности катализатора (переходные металлы первого ряда используют для связи 3d и 4s электроны). Это приводит к увеличению концентрации реагентов на поверхности катализатора, а также к ослаблению связей в реагирующих молекулах (снижается энергия активации). Кроме того, поскольку ионы переходных металлов могут менять свою степень окисления, они становятся более эффективными катализаторами .
Интересный тип катализа возникает, когда продукты реакции катализируют реакцию, производя больше катализатора ( автокатализ ). Одним из примеров является реакция щавелевой кислоты с подкисленным перманганатом калия (или манганатом (VII)). [39] После образования небольшого количества Mn 2+ он может реагировать с MnO 4 − с образованием Mn 3+ . Затем он реагирует с ионами C 2 O 4 −, снова образуя Mn 2+ .
Как следует из названия, все переходные металлы являются металлами и, следовательно, являются проводниками электричества.
В целом переходные металлы обладают высокой плотностью и высокими температурами плавления и кипения . Эти свойства обусловлены металлической связью делокализованными d-электронами, что приводит к сплочению , которое увеличивается с увеличением количества общих электронов. Однако металлы группы 12 имеют гораздо более низкие температуры плавления и кипения, поскольку их полные подоболочки d предотвращают образование d – d-связей, что снова имеет тенденцию отличать их от общепринятых переходных металлов. Ртуть имеет температуру плавления -38,83 ° C (-37,89 ° F) и при комнатной температуре является жидкостью.
{{cite book}}: CS1 maint: location missing publisher (link)