Микробиом человека представляет собой совокупность всей микробиоты , которая находится на или внутри тканей и биологических жидкостей человека , а также соответствующих анатомических участков, в которых они находятся, [1] включая кожу, молочные железы, семенную жидкость, матку, фолликулы яичников, легкие, слюну. , слизистая оболочка полости рта , конъюнктива , желчевыводящие пути и желудочно-кишечный тракт . Типы микробиоты человека включают бактерии , археи , грибы , протисты и вирусы . Хотя микроживотные также могут жить на теле человека, они обычно исключаются из этого определения. В контексте геномики термин « микробиом человека» иногда используется для обозначения коллективных геномов резидентных микроорганизмов; [2] однако термин «метагеном человека» имеет то же значение. [1]
В организме человека обитает множество микроорганизмов, число нечеловеческих клеток примерно того же порядка, что и человеческие клетки. [3] Некоторые микроорганизмы, которые переносят люди, являются комменсалами , то есть они сосуществуют, не причиняя вреда человеку; у других есть мутуалистические отношения со своими человеческими хозяевами. [2] : 700 [4] И наоборот, некоторые непатогенные микроорганизмы могут нанести вред человеку через метаболиты, которые они производят, например, триметиламин , который организм человека преобразует в N-оксид триметиламина посредством FMO3 -опосредованного окисления. [5] [6] Определенные микроорганизмы выполняют задачи, которые, как известно, полезны для человека-хозяина, но роль большинства из них недостаточно изучена. Те, которые, как ожидается, присутствуют и которые при нормальных обстоятельствах не вызывают заболевания, иногда считаются нормальной флорой или нормальной микробиотой . [2]
В раннем возрасте формирование разнообразной и сбалансированной микробиоты человека играет решающую роль в формировании долгосрочного здоровья человека. [7] Исследования показали, что на состав микробиоты кишечника в младенчестве влияют различные факторы, включая способ родоразрешения, грудное вскармливание и воздействие факторов окружающей среды. [8] В грудном молоке присутствует несколько полезных видов бактерий и потенциальных пробиотиков . [9] Исследования выявили благотворное влияние здоровой микробиоты в раннем возрасте, такое как содействие развитию иммунной системы, регуляция обмена веществ и защита от патогенных микроорганизмов. [10] Понимание сложного взаимодействия между микробиотой человека и здоровьем в раннем возрасте имеет решающее значение для разработки мер и стратегий, направленных на поддержку оптимального развития микробиоты и улучшение общих показателей здоровья людей. [11]
Проект «Микробиом человека» (HMP) взялся за проект секвенирования генома микробиоты человека, уделяя особое внимание микробиоте, которая обычно населяет кожу, рот, нос, пищеварительный тракт и влагалище. [2] Важным событием стало 2012 год, когда были опубликованы первые результаты. [12]
Хотя слово «корневая флора» широко известно как «флора» или «микрофлора» , это неправильное название с технической точки зрения, поскольку слово «корневая флора» относится к растениям, а « биота» относится к общей совокупности организмов в конкретной экосистеме. В последнее время применяется более подходящий термин «микробиота» , хотя его использование не затмило укоренившееся использование и признание флоры в отношении бактерий и других микроорганизмов. Оба термина используются в различной литературе. [4]
По оценкам, количество бактериальных клеток в среднем 70-килограммовом человеке мужского пола составляет около 38 триллионов, а количество человеческих клеток оценивается примерно в 30 триллионов. [13] Число бактериальных генов (при условии, что в кишечнике обитает 1000 видов бактерий и по 2000 генов на вид) оценивается в 2 000 000 генов, что в 100 раз превышает количество примерно 20 000 человеческих генов. [14] [15] [3] [16] [17]

Проблема выяснения микробиома человека заключается, по сути, в идентификации членов микробного сообщества, в которое входят бактерии, эукариоты и вирусы. [18] Это делается в основном с использованием исследований на основе дезоксирибонуклеиновой кислоты (ДНК), хотя также проводятся исследования на основе рибонуклеиновой кислоты (РНК), белков и метаболитов. [18] [19] Исследования микробиома на основе ДНК обычно можно отнести либо к целевым исследованиям ампликонов , либо, в последнее время, к метагеномным исследованиям с применением дробовика . Первый фокусируется на конкретных известных генах-маркерах и в первую очередь информативен с таксономической точки зрения, а второй представляет собой целостный метагеномный подход, который также может быть использован для изучения функционального потенциала сообщества. [18] Одна из проблем, которая присутствует в исследованиях микробиома человека, но не в других метагеномных исследованиях, заключается в том, чтобы избежать включения ДНК хозяина в исследование. [20]
Помимо простого выяснения состава микробиома человека, один из основных вопросов, касающихся человеческого микробиома, заключается в том, существует ли «ядро», то есть существует ли подмножество сообщества, которое является общим для большинства людей. [21] [22] Если есть ядро, то можно было бы связать определенные составы сообщества с болезненными состояниями, что является одной из целей HMP. Известно, что микробиом человека (например, микробиота кишечника) сильно варьирует как у одного человека, так и у разных людей, и это явление также наблюдается у мышей. [4]
13 июня 2012 года директор Национального института здравоохранения (NIH) Фрэнсис Коллинз объявил о важной вехе HMP . [12] Это объявление сопровождалось серией согласованных статей, опубликованных в журнале Nature [23] [24] и нескольких журналах Публичной научной библиотеки (PLoS) в тот же день. Сопоставляя нормальный микробный состав здоровых людей с помощью методов секвенирования генома, исследователи HMP создали справочную базу данных и границы нормальных микробных вариаций у людей. У 242 здоровых добровольцев из США было собрано более 5000 образцов тканей от 15 (мужчины) до 18 (женщины) участков тела, таких как рот, нос, кожа, нижний отдел кишечника (кал) и влагалище. Вся ДНК, человеческая и микробная, была проанализирована с помощью секвенаторов ДНК. Данные микробного генома были извлечены путем идентификации бактериальной специфичной рибосомальной РНК, 16S рРНК . Исследователи подсчитали, что экосистему человека населяют более 10 000 видов микробов, и они определили 81–99% родов . [25]
Статистический анализ необходим для проверки полученных результатов ( дисперсионный анализ можно использовать для определения размеров различий между группами); если он сочетается с графическими инструментами, результат легко визуализируется и понятен. [26]
Как только метагеном собран, можно сделать вывод о функциональном потенциале микробиома. Вычислительные проблемы для этого типа анализа больше, чем для отдельных геномов, поскольку обычно сборщики метагеномов имеют более низкое качество, а многие восстановленные гены являются неполными или фрагментированными. После этапа идентификации гена данные можно использовать для проведения функциональной аннотации посредством множественного выравнивания целевых генов по базам данных ортологов . [27]
Это метод, который использует праймеры для нацеливания на конкретную генетическую область и позволяет определить микробную филогению . Генетическая область характеризуется высокой изменчивостью, что позволяет обеспечить детальную идентификацию; он ограничен консервативными областями, которые функционируют как сайты связывания для праймеров, используемых в ПЦР . Основным геном, используемым для характеристики бактерий и архей , является ген 16S рРНК , а идентификация грибов основана на внутреннем транскрибируемом спейсере (ITS). Этот метод является быстрым и не таким дорогим и позволяет получить классификацию микробного образца с низким разрешением; он оптимален для образцов, которые могут быть загрязнены ДНК хозяина. Сродство праймеров варьируется среди всех последовательностей ДНК, что может привести к систематическим ошибкам во время реакции амплификации; действительно, образцы с низкой численностью подвержены ошибкам чрезмерной амплификации, поскольку в случае увеличения количества циклов ПЦР другие загрязняющие микроорганизмы оказываются чрезмерно представленными. Таким образом, оптимизация выбора праймеров может помочь уменьшить такие ошибки, хотя для этого требуется полное знание микроорганизмов, присутствующих в образце, и их относительной численности. [28]
На анализ маркерного гена может влиять выбор праймера; в этом виде анализа желательно использовать хорошо проверенный протокол (например, тот, который используется в проекте «Микробиом Земли» ). Первое, что нужно сделать при анализе ампликона маркерного гена, — это удалить ошибки секвенирования; Многие платформы секвенирования очень надежны, но большая часть кажущегося разнообразия последовательностей по-прежнему обусловлена ошибками в процессе секвенирования. Чтобы уменьшить это явление, первый подход заключается в кластеризации последовательностей в операционную таксономическую единицу (OTU): этот процесс объединяет сходные последовательности (обычно принимается порог сходства 97%) в единый признак, который можно использовать на дальнейших этапах анализа; однако этот метод отбрасывает SNP , поскольку они группируются в один OTU. Другим подходом является олиготипирование , которое включает в себя информацию о положении, полученную в результате секвенирования 16s рРНК для обнаружения небольших вариаций нуклеотидов и различия между близкородственными отдельными таксонами. Эти методы дают на выходе таблицу последовательностей ДНК и количество различных последовательностей на образец, а не OTU. [28]
Еще одним важным шагом в анализе является присвоение таксономического названия микробным последовательностям в данных. Это можно сделать с помощью подходов машинного обучения , которые могут достичь точности на уровне рода около 80%. Другие популярные пакеты анализа обеспечивают поддержку таксономической классификации с использованием точных совпадений со справочными базами данных и должны обеспечивать большую специфичность, но низкую чувствительность. Неклассифицированные микроорганизмы следует дополнительно проверить на наличие последовательностей органелл. [28]
Многие методы, использующие филогенетический вывод, используют ген 16SRNA для архей и бактерий и ген 18SRNA для эукариот. Филогенетические сравнительные методы (PCS) основаны на сравнении множества признаков микроорганизмов; принцип таков: чем тесно они связаны, тем больше у них общих черт. Обычно PCS сочетается с филогенетическим обобщенным методом наименьших квадратов (PGLS) или другим статистическим анализом для получения более значимых результатов. Реконструкция наследственного состояния используется в исследованиях микробиома для определения значений признаков для таксонов, признаки которых неизвестны. Обычно это выполняется с помощью PICRSt , который опирается на доступные базы данных. Филогенетические переменные выбираются исследователями в соответствии с типом исследования: за счет выбора некоторых переменных, несущих значительную биологическую информацию, можно уменьшить размерность данных для анализа. [29]
Филогенетическое расстояние обычно определяется с помощью UniFrac или аналогичных инструментов, таких как индекс Соресена или D Рао, для количественной оценки различий между различными сообществами. На все эти методы негативно влияет горизонтальная передача генов (HGT), поскольку она может генерировать ошибки и приводить к корреляции отдаленных видов. Существуют разные способы уменьшить негативное влияние ГПГ: использование нескольких генов или вычислительных инструментов для оценки вероятности предполагаемых событий ГПГ. [29]
Микробные сообщества развиваются в очень сложной динамике, которую можно рассматривать и анализировать как экосистему. Экологические взаимодействия между микробами определяют его изменение, равновесие и стабильность и могут быть представлены динамической моделью популяции. [30] Продолжающиеся исследования экологических особенностей микробиома быстро растут и позволяют понять фундаментальные свойства микробиома. Понимание основных правил микробного сообщества может помочь в лечении заболеваний, связанных с нестабильными микробными сообществами. Очень простой вопрос заключается в том, имеют ли разные люди, имеющие разные микробные сообщества, одинаковую основную микробную динамику. [31] Все больше фактов и указаний показывают, что эта динамика действительно универсальна. [32] Этот вопрос является основным шагом, который позволит ученым разработать стратегии лечения, основанные на сложной динамике микробных сообществ человека. Есть более важные свойства, которые следует учитывать при разработке стратегий вмешательства для контроля динамики микробов человека. [33] Контроль над микробными сообществами может привести к решению очень тяжелых и вредных заболеваний.

Популяции микробов (таких как бактерии и дрожжи ) населяют кожу и слизистые оболочки в различных частях тела. Их роль является частью нормальной, здоровой физиологии человека, однако, если количество микробов выходит за пределы их типичных диапазонов (часто из-за ослабления иммунной системы) или если микробы заселяют (например, из-за плохой гигиены или травмы), участки тела, которые обычно не колонизированы или стерильны (например, кровь, нижние дыхательные пути или брюшная полость), что может привести к заболеванию (вызывающему соответственно бактериемию/сепсис, пневмонию и перитонит). [34]
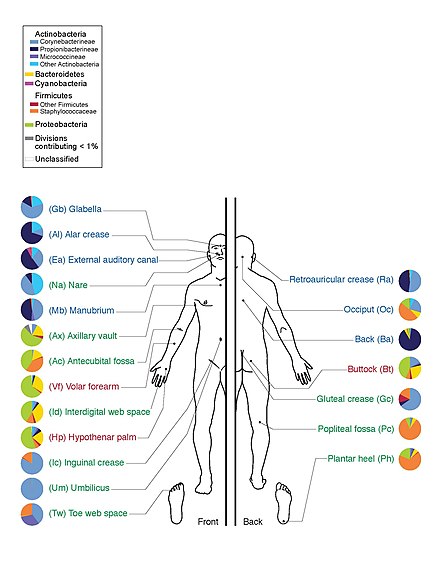
Проект «Микробиом человека» обнаружил, что люди являются носителями тысяч типов бактерий, причем в разных участках тела есть свои собственные особые сообщества. На участках кожи и влагалища было меньше разнообразия, чем во рту и кишечнике, причем они демонстрировали наибольшее богатство. Бактериальный состав определенного участка тела варьируется от человека к человеку не только по типу, но и по численности. Бактерии одного и того же вида, обнаруженные во рту, имеют несколько подтипов, предпочитая обитать в совершенно разных местах во рту. Даже энтеротипы кишечника человека, которые ранее считались хорошо изученными, происходят из широкого спектра сообществ с размытыми таксонными границами. [35] [36]
По оценкам, в кишечнике человека обитает от 500 до 1000 видов бактерий, но они принадлежат лишь к нескольким типам: преобладают Bacillota и Bacteroidota , но есть также Pseudomonadota , Verrucomicrobiota , Actinobacteriota , Fusobacteriota и « Cyanobacteria ». [37]
Ряд типов бактерий, таких как Actinomyces viscosus и A. naeslundii , живут во рту, где они являются частью липкого вещества, называемого зубным налетом . Если его не удалить щеткой, он затвердеет и превратится в камень (также называемый зубным камнем). Те же самые бактерии выделяют кислоты, которые растворяют зубную эмаль , вызывая кариес . [ нужна цитата ]
Микрофлора влагалища состоит преимущественно из различных видов лактобактерий . Долгое время считалось, что наиболее распространенным из этих видов является Lactobacillus acidophilus , но позже было показано, что на самом деле наиболее распространенным является L. iners , за которым следует L. Crispatus . Другими лактобактериями, обнаруженными во влагалище, являются L. jensenii, L. delbruekii и L. gasseri . Нарушение вагинальной флоры может привести к таким инфекциям, как бактериальный вагиноз и кандидоз. [38]
Археи присутствуют в кишечнике человека, но, в отличие от огромного разнообразия бактерий в этом органе, численность видов архей гораздо более ограничена. [39] Доминирующей группой являются метаногены , в частности Methanobrevibacter smithii и Methanosphaera stadtmanae . [40] Однако колонизация метаногенами варьируется, и только около 50% людей имеют легко обнаруживаемые популяции этих организмов. [41]
По состоянию на 2007 год не было известно никаких явных примеров архейных патогенов , [42] [43] , хотя была предложена связь между присутствием некоторых метаногенов и заболеваниями пародонта у человека . [44]
Грибки, в частности дрожжи , присутствуют в кишечнике человека. [45] [46] [47] [48] Наиболее изученными из них являются виды Candida из-за их способности становиться патогенными у людей с ослабленным иммунитетом и даже у здоровых хозяев. [46] [47] [48] Дрожжи также присутствуют на коже, [45] например , виды Malassezia , где они потребляют масла, выделяемые сальными железами . [49] [50]
Вирусы, особенно бактериальные вирусы ( бактериофаги ), колонизируют различные участки тела. Эти колонизированные участки включают кожу, [51] кишечник, [52] легкие, [53] и полость рта. [54] Вирусные сообщества связаны с некоторыми заболеваниями и не просто отражают бактериальные сообщества. [55] [56] [57]
В январе 2024 года биологи сообщили об открытии в микробиоме человека « обелисков », нового класса виродоподобных элементов , и «облинов», родственной им группы белков. [58] [59]
Исследование 20 участков кожи каждого из десяти здоровых людей выявило 205 идентифицированных родов в 19 типах бактерий, при этом большинство последовательностей было отнесено к четырем типам: Actinomycetota (51,8%), Bacillota (24,4%), Pseudomonadota (16,5%) и Bacteroidota . 6,3%). [60] На коже здорового человека присутствует большое количество родов грибов, с некоторой вариабельностью в зависимости от участка тела; однако при патологических состояниях в пораженном регионе имеют тенденцию доминировать определенные роды. [45] Например, Malassezia доминирует при атопическом дерматите , а Acremonium доминирует на коже головы, пораженной перхотью. [45]
Кожа действует как барьер, препятствующий проникновению болезнетворных микробов. Кожа человека содержит микробы, которые обитают либо внутри кожи, либо на ней и могут быть резидентными или временными. Типы резидентных микроорганизмов различаются в зависимости от типа кожи на теле человека. Большинство микробов обитают на поверхностных клетках кожи или предпочитают ассоциироваться с железами. Эти железы, такие как сальные или потовые железы, снабжают микробов водой, аминокислотами и жирными кислотами. Кроме того, резидентные бактерии, связанные с сальными железами, часто являются грамположительными и могут быть патогенными. [2]
В конъюнктиве обычно присутствует небольшое количество бактерий и грибков . [45] [61] Классы бактерий включают грамположительные кокки (например, стафилококки и стрептококки ) и грамотрицательные палочки и кокки (например, Haemophilus и Neisseria ). [61] Роды грибов включают Candida , Aspergillus и Penicillium . [45] Слезные железы непрерывно выделяют секрет, поддерживая влажность конъюнктивы, а периодическое моргание смазывает конъюнктиву и смывает инородный материал. Слезы содержат бактерициды, такие как лизоцим , поэтому микроорганизмам трудно выжить в условиях лизоцима и оседать на эпителиальных поверхностях.
У человека состав желудочно-кишечного микробиома формируется во время рождения. [66] Рождение путем кесарева сечения или вагинальных родов также влияет на микробный состав кишечника. Дети, рожденные через вагинальный канал, имеют непатогенную полезную микробиоту кишечника, аналогичную той, которая обнаружена у матери. [67] Однако микробиота кишечника детей, родившихся с помощью кесарева сечения, содержит больше патогенных бактерий, таких как Escherichia coli и стафилококк , и для развития непатогенной полезной микробиоты кишечника требуется больше времени. [68]
Отношения между некоторой кишечной микробиотой и людьми являются не просто комменсальными (безвредное сосуществование), а скорее мутуалистическими отношениями. [2] Некоторые кишечные микроорганизмы человека приносят пользу хозяину, ферментируя пищевые волокна в короткоцепочечные жирные кислоты (КЦЖК), такие как уксусная кислота и масляная кислота , которые затем поглощаются хозяином. [4] [69] Кишечные бактерии также играют роль в синтезе витамина B и витамина K , а также в метаболизме желчных кислот , стеринов и ксенобиотиков . [2] [69] Системное значение SCFAs и других соединений, которые они производят, аналогично гормонам , а сама кишечная флора, по-видимому, функционирует как эндокринный орган , [69] а нарушение регуляции кишечной флоры коррелирует с множеством воспалительных процессов. и аутоиммунные состояния. [4] [70]
Состав микробиоты кишечника человека меняется со временем, когда меняется диета и общее состояние здоровья. [4] [70] Систематический обзор 15 рандомизированных контролируемых исследований на людях , проведенных в июле 2016 года, показал, что некоторые коммерчески доступные штаммы пробиотических бактерий из родов Bifidobacterium и Lactobacillus ( B. longum , B. breve , B. infantis , L. helveticus , L. rhamnosus , L. plantarum и L. casei ) при приеме внутрь в суточных дозах 10 9 –10 10 колониеобразующих единиц (КОЕ) в течение 1–2 месяцев обладают лечебной эффективностью (т. е. улучшают поведенческие результаты) у некоторые расстройства центральной нервной системы , включая тревогу , депрессию , расстройства аутистического спектра и обсессивно-компульсивное расстройство , а также улучшает определенные аспекты памяти . [71]
В мочеполовой системе, по-видимому, имеется микробиота, [72] [73] что является неожиданным открытием в свете длительного использования стандартных клинических микробиологических методов культивирования для обнаружения бактерий в моче, когда у людей проявляются признаки инфекции мочевыводящих путей ; Эти тесты обычно не показывают присутствия бактерий. [74] Похоже, что обычные методы культивирования не обнаруживают многие виды бактерий и других микроорганизмов , которые обычно присутствуют. [74] По состоянию на 2017 год для идентификации этих микроорганизмов использовались методы секвенирования , чтобы определить, существуют ли различия в микробиоте между людьми с проблемами мочевыводящих путей и здоровыми людьми. [72] [73] [75] Чтобы правильно оценить микробиом мочевого пузыря, а не мочеполовой системы, образец мочи следует собирать непосредственно из мочевого пузыря, что часто делается с помощью катетера . [76]
Вагинальная микробиота относится к тем видам и родам, которые колонизируют влагалище. Эти организмы играют важную роль в защите от инфекций и поддержании здоровья влагалища. [77] Наиболее распространенные вагинальные микроорганизмы, обнаруженные у женщин в пременопаузе, относятся к роду Lactobacillus , которые подавляют патогены, производя перекись водорода и молочную кислоту. [47] [77] [78] Видовой состав бактерий и их соотношение варьируются в зависимости от стадии менструального цикла . [79] [80] [ требуется обновленная информация ] Этническая принадлежность также влияет на флору влагалища. Встречаемость лактобацилл, продуцирующих перекись водорода, ниже у афроамериканских женщин, а рН влагалища выше. [81] Другие влиятельные факторы, такие как половой акт и прием антибиотиков, связаны с потерей лактобактерий. [78] Более того, исследования показали, что половой акт с презервативом действительно изменяет уровень лактобактерий и увеличивает уровень Escherichia coli во влагалищной флоре. [78] Изменения в нормальной, здоровой вагинальной микробиоте являются признаком инфекций, [82] таких как кандидоз или бактериальный вагиноз . [78] Candida albicans подавляет рост видов Lactobacillus , в то время как виды Lactobacillus , которые производят перекись водорода, подавляют рост и вирулентность Candida albicans как во влагалище, так и в кишечнике. [45] [47] [48]
Роды грибов, обнаруженные во влагалище, включают Candida , Pichia , Eurotium , Alternaria , Rhodotorula и Cladosporium , среди других. [45]
До недавнего времени плаценту считали стерильным органом, однако были идентифицированы комменсальные непатогенные виды и роды бактерий, обитающие в плацентарной ткани. [83] [84] [85] Однако существование микробиома в плаценте является спорным и подвергается критике в нескольких исследованиях. Так называемый «плацентарный микробиом», вероятно, возник в результате загрязнения регентов, поскольку образцы с низкой биомассой легко контаминируются. [86] [87] [88]
До недавнего времени верхние репродуктивные пути женщины считались стерильной средой. В матке здоровых бессимптомных женщин репродуктивного возраста обитают разнообразные микроорганизмы. Микробиом матки существенно отличается от микробиома влагалища и желудочно-кишечного тракта. [89]
Среда, присутствующая во рту человека, способствует росту обнаруженных там характерных микроорганизмов. Он обеспечивает источник воды и питательных веществ, а также умеренную температуру. [2] Резидентные микробы полости рта прикрепляются к зубам и деснам, чтобы противостоять механическому промыванию изо рта в желудок, где чувствительные к кислоте микробы уничтожаются соляной кислотой . [2] [47]
К анаэробным бактериям полости рта относятся: Actinomyces , Arachnia , Bacteroides , Bifidobacterium , Eubacterium , Fusobacterium , Lactobacillus , Leptotrichia , Peptococcus , Peptostreptococcus , Propionibacterium , Selenomonas , Treponema и Veillonella . [90] [ нужна обновленная информация ] Роды грибов, которые часто встречаются во рту, включают Candida , Cladosporium , Aspergillus , Fusarium , Glomus , Alternaria , Penicillium и Cryptococcus , среди других. [45]
Бактерии накапливаются как на твердых, так и на мягких тканях полости рта в виде биопленки , что позволяет им прикрепляться и перемещаться в среде полости рта, защищая их от факторов окружающей среды и противомикробных агентов. [91] Слюна играет ключевую гомеостатическую роль в биопленке, позволяя бактериям реколонизироваться для формирования и контролировать рост путем отделения накопления биопленки. [92] Он также обеспечивает средства питательных веществ и регулирования температуры. Расположение биопленки определяет тип питательных веществ, которые она получает. [93]
Бактерии полости рта развили механизмы, позволяющие чувствовать окружающую среду и уклоняться от хозяина или изменять его. Однако высокоэффективная врожденная защитная система хозяина постоянно контролирует бактериальную колонизацию и предотвращает бактериальную инвазию в местные ткани. Между бактериями зубного налета и врожденной защитной системой хозяина существует динамическое равновесие . [94]
Эта динамика между полостью рта хозяина и микробами полости рта играет ключевую роль в здоровье и заболевании, поскольку обеспечивает проникновение в организм. [95] Здоровое равновесие представляет собой симбиотические отношения, при которых микробы полости рта ограничивают рост и прикрепление патогенов, в то время как хозяин обеспечивает им среду для процветания. [95] [91] Экологические изменения, такие как изменение иммунного статуса, смена резидентных микробов и доступность питательных веществ, смещают взаимные отношения к паразитическим, что приводит к тому, что хозяин становится склонным к оральным и системным заболеваниям. [91] Системные заболевания, такие как диабет и сердечно-сосудистые заболевания, коррелируют с плохим здоровьем полости рта. [95] Особый интерес представляет роль микроорганизмов полости рта в двух основных стоматологических заболеваниях: кариесе зубов и заболеваниях пародонта . [94] Колонизация патогенов в пародонте вызывает чрезмерный иммунный ответ, приводящий к образованию пародонтального кармана – углубленного пространства между зубом и десной. [91] Это действует как защищенный богатый кровью резервуар с питательными веществами для анаэробных патогенов. [91] Системные заболевания в различных частях тела могут возникнуть в результате попадания микробов полости рта в кровь, минуя пародонтальные карманы и мембраны полости рта. [95]
Постоянная правильная гигиена полости рта является основным методом предотвращения заболеваний полости рта и системных заболеваний. [95] Он снижает плотность биопленки и чрезмерный рост потенциальных патогенных бактерий, приводящих к заболеванию. [93] Однако надлежащей гигиены полости рта может быть недостаточно, поскольку микробиом полости рта, генетика и изменения иммунного ответа играют роль в развитии хронических инфекций. [93] Использование антибиотиков может лечить уже распространяющуюся инфекцию, но неэффективно против бактерий внутри биопленок. [93]
В здоровом микробиоме носа преобладают коринебактерии и стафилококки. Микробиом слизистой оболочки играет решающую роль в модуляции вирусной инфекции. [96]
Как и полость рта, верхняя и нижняя дыхательная система обладают механическими сдерживающими факторами для удаления микробов. Бокаловидные клетки производят слизь, которая улавливает микробы и выводит их из дыхательной системы посредством постоянно движущихся клеток мерцательного эпителия. [2] Кроме того, бактерицидный эффект оказывает носовая слизь, содержащая фермент лизоцим. [2] Верхние и нижние дыхательные пути, по-видимому, имеют свой собственный набор микробиоты. [97] Легочная бактериальная микробиота принадлежит к 9 основным бактериальным родам: Prevotella , Sphingomonas , Pseudomonas , Acinetobacter , Fusobacterium , Megasphaera , Veillonella , Staphylococcus и Streptococcus . Некоторые из бактерий, считающихся «нормальной биотой» дыхательных путей, могут вызывать серьезные заболевания, особенно у людей с ослабленным иммунитетом; к ним относятся Streptococcus pyogenes , Haemophilus influenzae , Streptococcus pneumoniae , Neisseria meningitidis и Staphylococcus aureus . [ нужна цитация ] Роды грибов, составляющие легочный микобиом, включают Candida , Malassezia , Neosartorya , Saccharomyces и Aspergillus , среди других. [45]
Необычное распространение родов бактерий и грибов в дыхательных путях наблюдается у людей, больных муковисцидозом . [45] [98] Их бактериальная флора часто содержит устойчивые к антибиотикам и медленно растущие бактерии, а частота этих патогенов меняется в зависимости от возраста. [98]
Традиционно желчевыводящие пути считались в норме стерильными, а наличие микроорганизмов в желчи является маркером патологического процесса. Это предположение было подтверждено неудачей в выделении бактериальных штаммов из нормального желчного протока. В 2013 году начали появляться статьи, показывающие, что нормальная микробиота желчных путей представляет собой отдельный функциональный слой, который защищает желчные пути от колонизации экзогенными микроорганизмами. [99]
Человеческие тела полагаются на бесчисленные бактериальные гены как на источник необходимых питательных веществ. [100] Как метагеномные, так и эпидемиологические исследования указывают на жизненно важную роль микробиома человека в предотвращении широкого спектра заболеваний, от диабета 2 типа и ожирения до воспалительных заболеваний кишечника, болезни Паркинсона и даже состояний психического здоровья, таких как депрессия. [101] Симбиотические отношения между микробиотой кишечника и различными бактериями могут влиять на иммунный ответ человека. [102] Метаболиты, вырабатываемые кишечными микробами, по-видимому, являются причинными факторами диабета 2 типа. [103] Хотя лечение на основе микробиома находится в зачаточном состоянии, оно также демонстрирует многообещающие результаты, особенно для лечения лекарственно-устойчивой инфекции C. difficile [ мертвая связь ] [104] и лечения диабета. [105]
Подавляющее присутствие бактерий C. difficile приводит к инфекции желудочно-кишечного тракта, обычно связанной с дисбактериозом микробиоты, который, как полагают, вызван приемом антибиотиков. Использование антибиотиков уничтожает полезную кишечную флору в желудочно-кишечном тракте, которая обычно предотвращает доминирование патогенных бактерий. [106] Традиционное лечение инфекций, вызванных C. difficile , включает дополнительный режим приема антибиотиков, однако эффективность в среднем составляет от 20 до 30%. [107] Признавая важность здоровых кишечных бактерий, исследователи обратились к процедуре, известной как трансплантация фекальной микробиоты (FMT), при которой пациенты, страдающие желудочно-кишечными заболеваниями, такими как инфекция C. difficile (CDI), в надежде получают фекалии от здорового человека. восстановления нормального функционирования микробиоты кишечника. [108] Трансплантация фекальной микробиоты эффективна примерно на 85–90% у людей с ИКД, у которых антибиотики не помогли или у которых заболевание рецидивирует после приема антибиотиков. [109] [110] Большинство людей с ИКД выздоравливают после одного курса лечения ТФМ. [111] [106] [112]
Хотя рак, как правило, является заболеванием, обусловленным генетикой хозяина и факторами окружающей среды, около 20% случаев рака у человека связаны с микроорганизмами. [113] В частности, что касается потенциальных факторов рака толстой кишки , плотность бактерий в миллион раз выше, чем в тонкой кишке , и примерно в 12 раз больше случаев рака в толстой кишке по сравнению с тонкой кишкой, что, возможно, устанавливает патогенную роль микробиоты в толстой кишке. и рак прямой кишки. [114] Плотность микроорганизмов может использоваться в качестве прогностического инструмента при оценке колоректального рака. [114]
Микробиота может влиять на канцерогенез тремя основными способами: (i) изменять баланс пролиферации и гибели опухолевых клеток, (ii) регулировать функцию иммунной системы и (iii) влиять на метаболизм факторов, продуктов питания и фармацевтических препаратов, вырабатываемых хозяином. [113] Опухоли, возникающие на пограничных поверхностях, таких как кожа, ротоглотка , дыхательные, пищеварительные и мочеполовые тракты, содержат микробиоту. Значительное присутствие микробов в месте опухоли не позволяет установить ассоциацию или причинно-следственную связь. Вместо этого микробы могут найти благоприятное напряжение кислорода в опухоли или профиль питательных веществ. Снижение популяции определенных микробов или индуцированный окислительный стресс также могут увеличить риски. [113] [114] Из примерно 10 30 микробов на Земле десять определены Международным агентством по исследованию рака как канцерогены для человека. [113] Микробы могут секретировать белки или другие факторы, непосредственно стимулирующие пролиферацию клеток в организме хозяина, или могут повышать или подавлять иммунную систему хозяина, в том числе стимулируя острое или хроническое воспаление, способствующее канцерогенезу. [113]
Что касается взаимосвязи иммунной функции и развития воспаления, поверхностные барьеры слизистой оболочки подвержены рискам окружающей среды и должны быстро восстанавливаться для поддержания гомеостаза . Нарушение устойчивости хозяина или микробиоты также снижает устойчивость к злокачественным новообразованиям, что может вызывать воспаление и рак. Как только барьеры преодолеваются, микробы могут вызывать провоспалительные или иммуносупрессивные программы различными путями. [113] Например, ассоциированные с раком микробы, по-видимому, активируют передачу сигналов NF-κB в микроокружении опухоли. Другие рецепторы распознавания образов, такие как члены семейства нуклеотид-связывающих доменов олигомеризации (NLR) NOD-2 , NLRP3 , NLRP6 и NLRP12 , могут играть роль в опосредовании колоректального рака. [113] Аналогичным образом, Helicobacter pylori, по-видимому, увеличивает риск рака желудка из-за того, что он вызывает хроническую воспалительную реакцию в желудке. [113] [114]
Воспалительное заболевание кишечника состоит из двух разных заболеваний: язвенного колита и болезни Крона, и оба этих заболевания сопровождаются нарушениями микробиоты кишечника (также известными как дисбиоз ). Этот дисбиоз проявляется в виде снижения микробного разнообразия в кишечнике [115] [116] и коррелирует с дефектами в генах хозяина, которые изменяют врожденный иммунный ответ у людей. [115]
Прогрессирование ВИЧ - инфекции влияет на состав и функцию кишечной микробиоты, при этом наблюдаются заметные различия между ВИЧ-отрицательными, ВИЧ-положительными и ВИЧ-позитивными популяциями после АРТ . [ нужна цитация ] ВИЧ снижает целостность барьерной функции эпителия кишечника, воздействуя на плотные соединения . Этот распад позволяет осуществлять транслокацию через эпителий кишечника, что, как полагают, способствует усилению воспаления, наблюдаемого у людей с ВИЧ. [117]
Вагинальная микробиота играет роль в заразности ВИЧ, причем риск заражения и передачи ВИЧ повышается, когда у женщины бактериальный вагиноз — состояние, характеризующееся аномальным балансом вагинальных бактерий. [118] Повышенная инфекционность наблюдается при увеличении количества провоспалительных цитокинов и клеток CCR5 + CD4 + во влагалище. Однако снижение инфекционности наблюдается при повышении уровня вагинальных лактобактерий, что способствует противовоспалительному состоянию. [117]
Люди в возрасте 100 лет и старше, называемые долгожителями , имеют отчетливый кишечный микробиом. Этот микробиом обычно обогащен микроорганизмами , которые способны синтезировать новые вторичные желчные кислоты . [119] Эти вторичные желчные кислоты включают различные изоформы литохолевой кислоты , которые могут способствовать здоровому старению. [119]
Со смертью микробиом живого организма разрушается, и другой состав микроорганизмов, называемый некробиомом , становится важной активной составляющей сложного процесса физического разложения. Считается, что его предсказуемые изменения с течением времени полезны для определения времени смерти. [120] [121]
Исследования 2009 года поставили под сомнение, может ли сокращение биоты (включая микрофауну ) в результате вмешательства человека препятствовать здоровью человека, процедурам безопасности в больницах, дизайну пищевых продуктов и лечению заболеваний. [122]

Гигиена, пробиотики , [123] пребиотики , трансплантация микробиоты ( фекальной или кожной [124] ), лекарства, антибиотики, заболевания, физические упражнения, [125] [126] диета, грудное вскармливание, старение и другие факторы [ необходимы дополнительные объяснения ] могут измениться. микробиом человека в различных анатомических системах или регионах, таких как кожа и кишечник. [ нужна цитата ]
Предварительные исследования показывают, что немедленные изменения в микробиоте могут произойти, когда человек мигрирует из одной страны в другую, например, когда тайские иммигранты поселились в Соединенных Штатах [127] или когда латиноамериканцы иммигрировали в Соединенные Штаты. [128] Потери разнообразия микробиоты были выше у людей с ожирением и детей иммигрантов. [127] [128]
Метагеномный анализ 2023 года предоставил различные комплексные данные и понимание обмена микробами между людьми, обнаружив существенное разделение штаммов среди сожительствующих людей, при этом медианная скорость обмена штаммами для микробиомов кишечника и полости рта составила 12% (34% для матерей и их детей 0–3 лет). -летнего потомства) и 32% (38% для партнеров) в использованных данных. Время, прошедшее с момента совместного проживания, было важнейшим фактором, и совместное использование бактериальных штаммов «лучше резюмировало структуру популяции хозяина [ необходимы разъяснения ] , чем профили на уровне вида». [129] [130]
Микробиом.
Этот термин относится ко всей среде обитания, включая микроорганизмы (бактерии, археи, низшие и высшие эукариоты и вирусы), их геномы (т. е. гены) и условия окружающей среды. Это определение основано на определении «биома», биотических и абиотических факторов данной среды. Другие специалисты в этой области ограничивают определение микробиома совокупностью генов и геномов членов микробиоты. Утверждается, что это определение
метагенома
, который в сочетании с окружающей средой образует микробиом.
мы рассматриваем литературу о триметиламине (ТМА), метаболите, вырабатываемом микробиотой, связанном с развитием атеросклероза.
Триметиламин представляет собой продукт исключительно микробиотного происхождения питательных веществ (лецитин, холин, ТМАО, L-карнитин) из обычного рациона питания, от которого, по-видимому, происходят два заболевания: триметиламинурия (или синдром рыбного запаха) и сердечно-сосудистые заболевания из-за проатерогенного свойства. его окисленной формы, полученной из печени.
Candida
и другие микроорганизмы участвуют в этой сложной грибковой инфекции, но
Candida albicans
продолжает оставаться наиболее распространенной. В последние два десятилетия наблюдаются аномальные разрастания в желудочно-кишечном, мочевыделительном и дыхательном путях не только у пациентов с ослабленным иммунитетом, но также связанные с нозокомиальными инфекциями и даже у здоровых лиц. Существует множество причинных факторов, которые способствуют дрожжевой инфекции, а это означает, что кандидоз является хорошим примером многофакторного синдрома.
Кроме того, грибковая инфекция ЖКТ регистрируется даже среди пациентов с нормальным иммунным статусом. Грибковые инфекции, связанные с пищеварительной системой, могут быть индуцированы как комменсальными условно-патогенными грибами, так и экзогенными патогенными грибами. ...
Кандида
зр. также является наиболее часто выявляемым видом среди пациентов с ИФИ желудка. ... Когда-то считалось, что желудочная кислота может убивать микробы, попадающие в желудок, и что уникальная экологическая среда желудка не подходит для микробной колонизации или инфекции. Однако несколько исследований с использованием культурально-независимых методов подтвердили, что в желудке существует большое количество кислотоустойчивых бактерий, принадлежащих к восьми типам и до 120 видам, таким как
Streptococcus
sp.,
Neisseria
sp. и
Lactobacillus
sp. и т. д.
26, 27
Кроме того,
Candida albicans
может хорошо расти в очень кислой среде,
28
а некоторые генотипы могут увеличивать тяжесть поражений слизистой оболочки желудка.
29
Чрезмерный грибковый рост в тонком кишечнике (SIFO) характеризуется наличием чрезмерного количества грибковых организмов в тонком кишечнике, что связано с желудочно-кишечными симптомами. Известно, что кандидоз вызывает симптомы со стороны желудочно-кишечного тракта, особенно у пациентов с ослабленным иммунитетом или у тех, кто принимает стероиды или антибиотики. Однако лишь недавно появилась литература о том, что чрезмерный рост грибков в тонкой кишке у лиц без иммунодефицита может вызывать необъяснимые симптомы со стороны желудочно-кишечного тракта. Два недавних исследования показали, что 26% (24/94) и 25,3% (38/150) пациентов с необъяснимыми желудочно-кишечными симптомами имели SIFO. Наиболее распространенными симптомами, наблюдавшимися у этих пациентов, были отрыжка, вздутие живота, расстройство желудка, тошнота, диарея и газы. ... Грибково-бактериальное взаимодействие может действовать по-разному и быть синергическим, антагонистическим или симбиотическим [29]. Некоторые бактерии, такие как виды
Lactobacillus
, могут взаимодействовать и подавлять как вирулентность, так и рост видов
Candida
в кишечнике, производя перекись водорода [30]. Любое повреждение слизистого барьера или нарушение микробиоты желудочно-кишечного тракта при химиотерапии или применении антибиотиков, воспалительные процессы, активация иммунных молекул и нарушение восстановления эпителия — все это может вызвать чрезмерный рост грибков [27].
Lactobacillus
spp. превращают триптофан в индол-3-альдегид (I3A) с помощью неидентифицированных ферментов [125].
Clostridium sporogenes
превращают триптофан в IPA [6], вероятно, посредством триптофандезаминазы. ... IPA также эффективно удаляет гидроксильные радикалы.
Было показано, что продукция IPA полностью зависит от присутствия микрофлоры кишечника и может быть установлена путем колонизации бактерией
Clostridium sporogenes
.
[Индол-3-пропионовая кислота (IPA)] ранее была идентифицирована в плазме и спинномозговой жидкости человека, но ее функции неизвестны. ... В экспериментах по кинетической конкуренции с использованием агентов, улавливающих свободные радикалы, способность IPA удалять гидроксильные радикалы превышала способность мелатонина, индоламина, который считается наиболее мощным природным поглотителем свободных радикалов. В отличие от других антиоксидантов, IPA не превращался в реакционноспособные интермедиаты с прооксидантной активностью.
Эти пробиотики показали эффективность в улучшении поведения, связанного с психическими расстройствами, включая тревогу, депрессию, расстройство аутистического спектра (РАС), обсессивно-компульсивное расстройство и способности памяти, включая пространственную и непространственную память. Поскольку многие фундаментальные научные исследования показали некоторую эффективность пробиотиков в отношении функции центральной нервной системы, эти данные могут служить ориентиром и способствовать дальнейшим доклиническим и клиническим исследованиям. ...По качественному анализу текущих исследований можно сделать предварительный вывод, что наиболее эффективными оказались B. longum, B. breve, B. infantis, L. helveticus, L. rhamnosus, L. plantarum и L. casei. в улучшении функции ЦНС, включая функции, связанные с психическими заболеваниями (тревога, депрессия, настроение, реакция на стресс) и способности памяти