Миорелаксант — это препарат, который влияет на функцию скелетных мышц и снижает мышечный тонус . Он может использоваться для облегчения таких симптомов, как мышечные спазмы , боль и гиперрефлексия . Термин «миорелаксант» используется для обозначения двух основных терапевтических групп: нейромышечных блокаторов и спазмолитиков . Нейромышечные блокаторы действуют, вмешиваясь в передачу на нервно-мышечной концевой пластинке и не оказывают воздействия на центральную нервную систему (ЦНС). Они часто используются во время хирургических операций, в интенсивной терапии и неотложной медицине, чтобы вызвать временный паралич . Спазмолитики, также известные как «центрально действующие» миорелаксанты, используются для облегчения мышечно-скелетной боли и спазмов и для уменьшения спастичности при различных неврологических состояниях. Хотя и нейромышечные блокаторы, и спазмолитики часто объединяются в группу миорелаксантов, [1] [2] этот термин обычно используется для обозначения только спазмолитиков. [3] [4]
Самое раннее известное использование миорелаксантов было у аборигенов бассейна Амазонки в Южной Америке, которые использовали отравленные стрелы , которые вызывали смерть от паралича скелетных мышц. Это было впервые задокументировано в 16 веке, когда с ним столкнулись европейские исследователи. Этот яд, известный сегодня как кураре , привел к некоторым из самых ранних научных исследований в фармакологии . Его активный ингредиент, тубокурарин , а также многие синтетические производные, сыграли значительную роль в научных экспериментах по определению функции ацетилхолина в нервно-мышечной передаче . [5] К 1943 году нервно-мышечные блокирующие препараты стали общепринятыми в качестве миорелаксантов в практике анестезии и хирургии . [6]
Управление по контролю за продуктами и лекарствами США (FDA) одобрило использование каризопродола в 1959 году, метаксалона в августе 1962 года и циклобензаприна в августе 1977 года. [7]
Другие релаксанты скелетных мышц этого типа, используемые во всем мире, принадлежат к ряду категорий препаратов, а другие препараты, используемые в первую очередь по этому показанию, включают орфенадрин (антихолинергическое средство), хлорзоксазон , тизанидин ( родственник клонидина ), диазепам , тетразепам и другие бензодиазепины , мефеноксалон , метокарбамол , дантролен , баклофен . [7] Препараты, которые когда-то, но больше не используются или используются очень редко для расслабления скелетных мышц, включают мепробамат , барбитураты , метаквалон , глютетимид и тому подобное; некоторые подкатегории опиоидов обладают свойствами миорелаксантов, а некоторые продаются в комбинированных препаратах с релаксантами скелетных и/или гладких мышц, такими как цельные опиумные продукты, некоторые препараты кетобемидона , пиритрамида и фентанила , а также Эквагезика .

Расслабление мышц и паралич теоретически могут происходить путем прерывания функции в нескольких местах, включая центральную нервную систему , миелинизированные соматические нервы, немиелинизированные двигательные нервные окончания, никотиновые ацетилхолиновые рецепторы , двигательную концевую пластинку и мышечную мембрану или сократительный аппарат. Большинство нейромышечных блокаторов действуют, блокируя передачу на концевой пластинке нервно-мышечного соединения . Обычно нервный импульс поступает в двигательное нервное окончание, инициируя приток ионов кальция , что вызывает экзоцитоз синаптических пузырьков, содержащих ацетилхолин . Затем ацетилхолин диффундирует через синаптическую щель. Он может гидролизоваться ацетилхолинэстеразой (АХЭ) или связываться с никотиновыми рецепторами, расположенными на двигательной концевой пластинке. Связывание двух молекул ацетилхолина приводит к конформационному изменению рецептора, которое открывает натрий-калиевый канал никотинового рецептора. Это позволяет Na+
и Ca2+
ионы проникают в клетку и К+
ионы покидают клетку, вызывая деполяризацию концевой пластинки, что приводит к сокращению мышцы. [8] После деполяризации молекулы ацетилхолина удаляются из области концевой пластинки и ферментативно гидролизуются ацетилхолинэстеразой. [5]
Нормальная функция концевой пластинки может быть заблокирована двумя механизмами. Недеполяризующие агенты, такие как тубокурарин , блокируют агонист ацетилхолин от связывания с никотиновыми рецепторами и их активации, тем самым предотвращая деполяризацию. Альтернативно, деполяризующие агенты, такие как сукцинилхолин , являются агонистами никотиновых рецепторов , которые имитируют Ach, блокируют сокращение мышц путем деполяризации до такой степени, что он десенсибилизирует рецептор, и он больше не может инициировать потенциал действия и вызывать сокращение мышц. [5] Оба этих класса нейромышечных блокирующих препаратов структурно похожи на ацетилхолин, эндогенный лиганд, во многих случаях содержащий две молекулы ацетилхолина, связанные конец к концу жесткой углеродной кольцевой системой, как в панкуронии (недеполяризующий агент). [5]
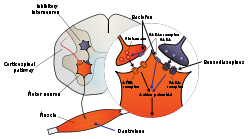
Генерация нейронных сигналов в двигательных нейронах, вызывающих мышечные сокращения, зависит от баланса синаптического возбуждения и торможения, которые получает двигательный нейрон. Спазмолитические агенты обычно работают либо за счет повышения уровня торможения, либо за счет снижения уровня возбуждения. Торможение усиливается путем имитации или усиления действия эндогенных ингибирующих веществ, таких как ГАМК .
Поскольку они могут действовать на уровне коры головного мозга, ствола мозга или спинного мозга, или всех трех областей, их традиционно называют «центрально действующими» миорелаксантами. Однако теперь известно, что не все агенты этого класса обладают активностью ЦНС (например, дантролен ), поэтому это название неточно. [5]
Большинство источников по-прежнему используют термин «миорелаксант центрального действия». Согласно MeSH , дантролен обычно классифицируется как миорелаксант центрального действия. [9] Всемирная организация здравоохранения в своем ATC использует термин «агенты центрального действия», [10] но добавляет отдельную категорию «агенты прямого действия» для дантролена. [11] Использование этой терминологии восходит как минимум к 1973 году. [12]
Термин «спазмолитик» также считается синонимом спазмолитического средства . [13]
Спазмолитики, такие как каризопродол , циклобензаприн , метаксалон и метокарбамол , обычно назначают при болях в пояснице или шее , фибромиалгии , головных болях напряжения и миофасциальном болевом синдроме . [14] Однако они не рекомендуются в качестве препаратов первой линии; при острой боли в пояснице они не более эффективны, чем парацетамол или нестероидные противовоспалительные препараты ( НПВП ), [15] [16] а при фибромиалгии они не более эффективны, чем антидепрессанты . [14] Тем не менее, некоторые (низкокачественные) доказательства свидетельствуют о том, что миорелаксанты могут быть полезны при лечении НПВП. [17] В целом, нет высококачественных доказательств в поддержку их использования. [14] Ни один препарат не показал себя лучше другого, и все они имеют побочные эффекты , в частности головокружение и сонливость . [14] [16] Опасения по поводу возможного злоупотребления и взаимодействия с другими препаратами, особенно если существует риск усиления седации, еще больше ограничивают их использование. [14] Миорелаксант выбирается на основе его профиля побочных эффектов, переносимости и стоимости. [18]
Миорелаксанты (согласно одному исследованию) не рекомендуются при ортопедических заболеваниях, а скорее при неврологических заболеваниях, таких как спастичность при церебральном параличе и рассеянном склерозе . [14] Дантролен, хотя и считается в первую очередь периферически действующим средством, связан с эффектами ЦНС, тогда как активность баклофена строго связана с ЦНС.
Мышечные релаксанты считаются полезными при болезненных расстройствах, основанных на теории, что боль вызывает спазм, а спазм вызывает боль. Однако значительные доказательства противоречат этой теории. [17]
В целом, миорелаксанты не одобрены FDA для длительного использования. Однако ревматологи часто назначают циклобензаприн на ночь ежедневно, чтобы увеличить 4 стадию сна. Увеличивая эту стадию сна, пациенты чувствуют себя более отдохнувшими утром. Улучшение сна также полезно для пациентов, страдающих фибромиалгией. [19]
Миорелаксанты, такие как тизанидин, назначают при лечении головных болей напряжения . [20]
Диазепам и каризопродол не рекомендуются пожилым людям, беременным женщинам , людям, страдающим депрессией , а также лицам, имеющим в анамнезе наркотическую или алкогольную зависимость . [21]
Из-за усиления торможения в ЦНС большинство спазмолитических средств имеют побочные эффекты седации и сонливости и могут вызывать зависимость при длительном применении. Некоторые из этих средств также имеют потенциал злоупотребления, и их назначение строго контролируется. [22] [23] [24]
Бензодиазепины , такие как диазепам , взаимодействуют с рецептором ГАМК А в центральной нервной системе. Хотя его можно использовать у пациентов с мышечным спазмом практически любого происхождения, он вызывает седацию у большинства людей в дозах, необходимых для снижения мышечного тонуса. [5]
Баклофен считается по крайней мере таким же эффективным, как диазепам, в снижении спастичности и вызывает гораздо меньший седативный эффект. Он действует как агонист ГАМК на рецепторах ГАМК В в головном и спинном мозге, что приводит к гиперполяризации нейронов, экспрессирующих этот рецептор, скорее всего, из-за повышенной проводимости ионов калия. Баклофен также подавляет нейронную функцию пресинаптически, уменьшая приток ионов кальция и тем самым уменьшая высвобождение возбуждающих нейротрансмиттеров как в головном, так и в спинном мозге. Он также может уменьшать боль у пациентов, подавляя высвобождение вещества Р в спинном мозге. [5] [25]
Клонидин и другие соединения имидазолина также, как было показано, уменьшают мышечные спазмы за счет своей активности в центральной нервной системе. Тизанидин , возможно, является наиболее тщательно изученным аналогом клонидина и является агонистом α2 -адренорецепторов , но уменьшает спастичность в дозах, которые приводят к значительно меньшей гипотензии, чем клонидин. [26] Нейрофизиологические исследования показывают, что он подавляет возбуждающую обратную связь от мышц, которые обычно увеличивают мышечный тонус, тем самым минимизируя спастичность. [27] [28] Кроме того, несколько клинических испытаний показывают, что тизанидин имеет аналогичную эффективность с другими спазмолитическими средствами, такими как диазепам и баклофен, с другим спектром побочных эффектов. [29]
Производное гидантоина дантролен является спазмолитическим средством с уникальным механизмом действия за пределами ЦНС. Он снижает силу скелетных мышц, ингибируя сопряжение возбуждения-сокращения в мышечном волокне . При нормальном сокращении мышц кальций высвобождается из саркоплазматического ретикулума через канал рианодинового рецептора , что вызывает взаимодействие актина и миозина , генерирующее напряжение . Дантролен препятствует высвобождению кальция, связываясь с рианодиновым рецептором и блокируя эндогенный лиганд рианодин путем конкурентного ингибирования . Мышца, которая сокращается быстрее, более чувствительна к дантролену, чем мышца, которая сокращается медленно, хотя сердечная мышца и гладкая мышца угнетаются лишь незначительно, скорее всего, потому, что высвобождение кальция их саркоплазматическим ретикулумом включает несколько иной процесс. Основные побочные эффекты дантролена включают общую мышечную слабость, седацию и иногда гепатит . [5]
Другие распространенные спазмолитические средства включают: метокарбамол , каризопродол , хлорзоксазон , циклобензаприн , габапентин , метаксалон и орфенадрин .
Тиоколхикозид — миорелаксант с противовоспалительным и анальгезирующим эффектом, механизм действия которого неизвестен. [30] [31] [32] [33] Он действует как конкурентный антагонист ГАМК А и глициновых рецепторов с аналогичной эффективностью , а также никотиновых ацетилхолиновых рецепторов , хотя и в гораздо меньшей степени. [34] [35] Он обладает мощной проконвульсивной активностью и не должен использоваться у лиц, склонных к судорогам . [36] [37] [38]
Пациенты чаще всего сообщают о седации как о главном побочном эффекте миорелаксантов. Обычно люди становятся менее бдительными, когда находятся под воздействием этих препаратов. Людям обычно не рекомендуется управлять транспортными средствами или работать с тяжелой техникой , находясь под воздействием миорелаксантов.
Циклобензаприн вызывает спутанность сознания и летаргию , а также антихолинергические побочные эффекты. При приеме в избытке или в сочетании с другими веществами он также может быть токсичным . Пока организм приспосабливается к этому лекарству, у пациентов могут возникнуть сухость во рту , усталость , головокружение, запор или нечеткость зрения . Могут возникнуть некоторые серьезные, но маловероятные побочные эффекты, включая изменения психики или настроения, возможную спутанность сознания и галлюцинации , а также затрудненное мочеиспускание. В очень немногих случаях могут возникнуть очень серьезные, но редкие побочные эффекты: нерегулярное сердцебиение, пожелтение глаз или кожи, обмороки , боли в животе, включая боли в желудке , тошнота или рвота , отсутствие аппетита , судороги, темная моча или потеря координации. [39]
Пациенты, принимавшие каризопродол в течение длительного времени, сообщали о зависимости , абстиненции и злоупотреблении, хотя большинство этих случаев были зарегистрированы пациентами с историей зависимости. Эти эффекты также были зарегистрированы пациентами, которые принимали его в сочетании с другими препаратами с потенциалом злоупотребления, и в меньшем количестве случаев сообщения о злоупотреблении, связанном с каризопродолом, появлялись при использовании без других препаратов с потенциалом злоупотребления. [40]
Обычные побочные эффекты, в конечном итоге вызванные метаксалоном, включают головокружение, головную боль , сонливость, тошноту, раздражительность , нервозность , расстройство желудка и рвоту . При приеме метаксалона могут возникнуть серьезные побочные эффекты, такие как тяжелые аллергические реакции ( сыпь , крапивница , зуд , затрудненное дыхание, стеснение в груди, отек рта, лица, губ или языка), озноб , лихорадка и боль в горле , которые могут потребовать медицинской помощи. Другие серьезные побочные эффекты включают необычную или сильную усталость или слабость, а также пожелтение кожи или глаз. [41] Когда баклофен вводится интратекально , он может вызвать угнетение ЦНС, сопровождающееся сердечно-сосудистым коллапсом и дыхательной недостаточностью . Тизанидин может снизить артериальное давление . Этот эффект можно контролировать, назначая низкую дозу вначале и постепенно увеличивая ее. [42]