
Реагенты Гриньяра или соединения Гриньяра представляют собой химические соединения с общей формулой R-Mg-X , где X представляет собой галоген , а R представляет собой органическую группу , обычно алкил или арил . Двумя типичными примерами являются хлорид метилмагния Cl-Mg-CH 3 и бромид фенилмагния (C 6 H 5 )-Mg-Br . Они представляют собой подкласс магнийорганических соединений .
Соединения Гриньяра — популярные реагенты в органическом синтезе для создания новых углерод-углеродных связей . Например, при взаимодействии с другим галогенированным соединением R'-X' в присутствии подходящего катализатора они обычно дают R-R' и галогенид магния MgXX' в качестве побочного продукта; и последний нерастворим в обычно используемых растворителях. В этом отношении они аналогичны литийорганическим реагентам .
Реагенты Гриньяра редко выделяют в виде твердых веществ. Вместо этого с ними обычно обращаются в виде растворов в растворителях, таких как диэтиловый эфир или тетрагидрофуран, используя безвоздушные методы . Реагенты Гриньяра представляют собой комплексы с атомом магния, связанным с двумя эфирными лигандами , а также галогенидным и органильным лигандами.
Открытие реакции Гриньяра в 1900 году было отмечено Нобелевской премией, присужденной Виктору Гриньяру в 1912 году.
Традиционно реактивы Гриньяра готовят путем обработки органического галогенида (обычно броморганического соединения) металлическим магнием. Эфиры необходимы для стабилизации магнийорганического соединения . Исключаются вода и воздух, которые быстро разрушают реагент за счет протонолиза или окисления. [1] Хотя реагенты по-прежнему должны быть сухими, ультразвук может позволить реагентам Гриньяра образовываться во влажных растворителях за счет активации магния, так что он поглощает воду. [2]
Как это обычно бывает с реакциями с участием твердых веществ и растворов, образование реактивов Гриньяра часто сопровождается индукционным периодом . На этом этапе пассивирующий оксид магния удаляется. После этого индукционного периода реакции могут быть сильно экзотермическими . Эту экзотермичность необходимо учитывать при масштабировании реакции от лаборатории до производственного предприятия. [3] Большинство галогенорганических соединений будут работать, но связи углерод-фтор обычно нереакционноспособны, за исключением специально активированного магния (через металлы Риеке ).
Обычно реакция образования реактивов Гриньяра включает использование магниевой ленты. Весь магний покрыт пассивирующим слоем оксида магния , который ингибирует реакции с органическими галогенидами. Было разработано множество методов для ослабления этого пассивирующего слоя, тем самым подвергая высокореактивный магний воздействию органического галогенида. Механические методы включают измельчение кусочков магния на месте, быстрое перемешивание и обработку ультразвуком . [4] Йод , йодистый метил и 1,2-дибромэтан являются распространенными активирующими агентами. Использование 1,2-дибромэтана выгодно, поскольку его действие можно контролировать по наблюдению за пузырьками этилена . Кроме того, побочные продукты безобидны:
Количество Mg, потребляемое этими активаторами, обычно незначительно. Небольшое количество хлорида ртути амальгамирует поверхность металла, повышая его реакционную способность . В качестве инициатора часто используют добавление заранее приготовленного реактива Гриньяра.
Специально активированный магний, такой как магний Риеке , позволяет решить эту проблему. [5] Оксидный слой также можно разрушить с помощью ультразвука, используя палочку для перемешивания, чтобы соскоблить окисленный слой, [6] или добавив несколько капель йода или 1,2-дииодэтана . Другой вариант — использовать сублимированный магний или антрацен магния . [7]
« Риеке магний» получают восстановлением безводного хлорида магния калием :
По механизму реакция протекает путем одноэлектронного переноса : [8] [9] [10]
Альтернативное приготовление реактивов Гриньяра включает перенос Mg из предварительно полученного реактива Гриньяра в органический галогенид. Используют и другие магнийорганические реагенты. [11] Преимущество этого метода заключается в том, что перенос Mg допускает многие функциональные группы. Показательная реакция включает хлорид изопропилмагния и арилбромид или иодиды: [12]
Другой метод синтеза реактивов Гриньяра включает реакцию Mg с цинкорганическим соединением . Этот метод использовался для получения реагентов Гриньяра на основе адамантана , которые из-за побочных реакций сочетания CC трудно получить обычным методом из алкилгалогенида и Mg. Восстановительная трансметаллизация обеспечивает: [13]
Поскольку реактивы Гриньяра очень чувствительны к влаге и кислороду, было разработано множество методов проверки качества партии. Типичные тесты включают титрование взвешенными безводными протонными реагентами, например ментолом, в присутствии цветового индикатора. Взаимодействие реактива Гриньяра с фенантролином или 2,2'-бихинолином вызывает изменение цвета. [14]
Реактивы Гриньяра реагируют с различными карбонильными производными. [15]
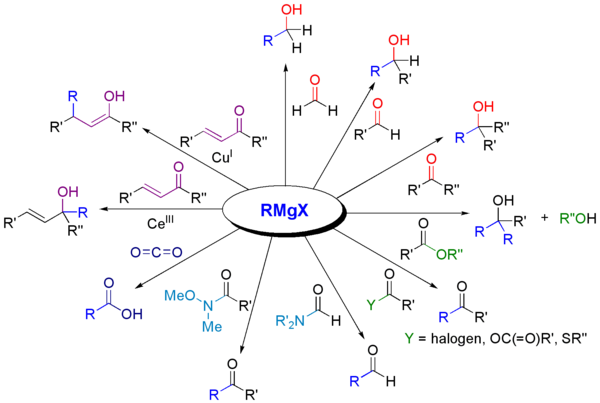
Наиболее распространенным применением реактивов Гриньяра является алкилирование альдегидов и кетонов, т.е. реакция Гриньяра : [16]

Обратите внимание, что ацетальная функциональная группа (защищенный карбонил) не вступает в реакцию.
Такие реакции обычно включают водно-кислотную обработку, хотя этот этап редко показан на схемах реакций. В тех случаях, когда реактив Гриньяра добавляется к альдегиду или прохиральному кетону, модель Фелкина-Аня или правило Крама обычно позволяют предсказать, какой стереоизомер образуется. С легко депротонируемыми 1,3- дикетонами и родственными кислотными субстратами реактив Гриньяра RMgX действует просто как основание, давая енолят- анион и высвобождая алкан RH.
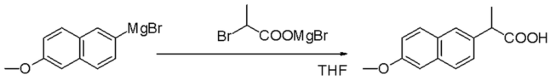
Реагенты Гриньяра представляют собой нуклеофилы в нуклеофильных алифатических замещениях, например, с алкилгалогенидами на ключевом этапе промышленного производства напроксена :
Реагенты Гриньяра также реагируют со многими «карбонилоподобными» соединениями и другими электрофилами:

Реактивы Гриньяра служат основой для непротонных субстратов (на этой схеме не указаны условия обработки, обычно включающие воду). Реактивы Гриньяра являются основными и реагируют со спиртами, фенолами и др. с образованием алкоксидов (ROMgBr). Производное феноксида подвержено формилированию параформальдегидом с образованием салицилового альдегида . [17]
Как и литийорганические соединения , реактивы Гриньяра полезны для образования связей углерод-гетероатом.
Большинство реакций Гриньяра проводят в эфирных растворителях, особенно в диэтиловом эфире и ТГФ . Реагенты Гриньяра реагируют с 1,4-диоксаном с образованием магнийорганических соединений и нерастворимого координационного полимера MgX 2 (диоксан) 2 и (R = органическая группа, X = галогенид):
Эта реакция использует равновесие Шленка , сдвигая его вправо.
Реактивы Гриньяра реагируют с литийорганическими соединениями с образованием атных комплексов (Bu = бутил): [19]
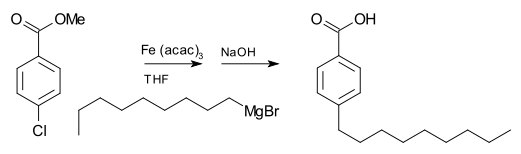
Реактивы Гриньяра обычно не реагируют с органическими галогенидами, в отличие от их высокой реакционной способности с галогенидами других основных групп. Однако в присутствии металлических катализаторов реагенты Гриньяра участвуют в реакциях сочетания CC . Например, бромид нонилмагния реагирует с метил- п -хлорбензоатом с образованием п -нонилбензойной кислоты в присутствии трис(ацетилацетонато)железа(III) (Fe(acac) 3 ) после обработки NaOH для гидролиза сложного эфира , как показано ниже. . Без Fe(acac) 3 реактив Гриньяра будет атаковать сложноэфирную группу , а не арилгалогенид . [20]
Хорошим катализатором для реакции сочетания арилгалогенидов с арилреагентами Гриньяра является также хлорид никеля в тетрагидрофуране (ТГФ). Кроме того, эффективным катализатором реакции сочетания алкилгалогенидов является катализатор Гилмана тетрахлоркупрат лития ( Li 2 CuCl 4 ), приготовленный путем смешивания хлорида лития (LiCl) и хлорида меди (II) ( CuCl 2 ) в ТГФ. Соединение Кумада -Корриу дает доступ к [замещенным] стиролам .
Обработка реактива Гриньяра кислородом дает органопероксид магния. Гидролиз этого материала дает гидроперекиси или спирт. В этих реакциях участвуют радикальные промежуточные соединения.
Простое окисление реактивов Гриньяра с образованием спиртов не имеет большого практического значения, поскольку выходы обычно низкие. Напротив, двухстадийная последовательность через боран ( см. выше ), который впоследствии окисляется до спирта перекисью водорода, имеет синтетическое применение.
Синтетическая полезность окисления Гриньяра может быть увеличена за счет реакции реагентов Гриньяра с кислородом в присутствии алкена с образованием этиленового расширенного спирта . [21] Эта модификация требует арилового или винилового Гриньяра. Добавление только Гриньяра и алкена не приводит к реакции, демонстрирующей, что присутствие кислорода существенно. Единственным недостатком является требование наличия как минимум двух эквивалентов Гриньяра, хотя это можно частично обойти, используя двойную систему Гриньяра с дешевым восстановителем Гриньяра, таким как н-бутилмагнийбромид.

В синтезе олефинов по Борду добавление магния к некоторым β-галогенэфирам приводит к реакции отщепления алкена. Эта реакция может ограничить полезность реакций Гриньяра.

Примером реакции Гриньяра является ключевой этап (нестереоселективного) промышленного производства тамоксифена [22] (в настоящее время используемого для лечения рака молочной железы, положительного по эстрогеновым рецепторам у женщин): [23]

{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )