

Фотосинтез ( / ˌ f oʊ t ə ˈ s ɪ n θ ə s ɪ s / FOH -tə- SINTH -ə-sis ) [1] — биологический процесс , используемый многими клеточными организмами для преобразования световой энергии в химическую энергию , которая Хранятся в органических соединениях , которые позже могут метаболизироваться посредством клеточного дыхания для поддержания деятельности организма. Этот термин обычно относится к оксигенному фотосинтезу , при котором кислород вырабатывается как побочный продукт , а часть вырабатываемой химической энергии сохраняется в молекулах углеводов , таких как сахара , крахмал , гликоген и целлюлоза , которые синтезируются в результате эндергонической реакции углекислого газа с водой . Большинство растений , водорослей и цианобактерий осуществляют фотосинтез; такие организмы называются фотоавтотрофами . Фотосинтез в значительной степени отвечает за производство и поддержание содержания кислорода в атмосфере Земли и обеспечивает большую часть биологической энергии , необходимой для сложной жизни на Земле. [2]
Некоторые бактерии также осуществляют аноксигенный фотосинтез , при котором бактериохлорофилл используется для расщепления сероводорода в качестве восстановителя вместо воды, а в качестве побочного продукта вместо кислорода образуется сера . Археи, такие как Halobacterium, также осуществляют тип аноксигенного фотосинтеза, не связывающего углерод , при котором более простой фотопигмент ретиналь и его микробные производные родопсина используются для поглощения зеленого света и приводят в действие протонные насосы для прямого синтеза аденозинтрифосфата (АТФ). Такой архейный фотосинтез мог быть самой ранней формой фотосинтеза, развившейся на Земле, восходящей еще в палеоархее , предшествовавшей фотосинтезу цианобактерий (см. Гипотезу Пурпурной Земли ).
Хотя фотосинтез у разных видов осуществляется по-разному, процесс всегда начинается, когда энергия света поглощается белками , называемыми реакционными центрами , которые содержат фотосинтетические пигменты или хромофоры . У растений эти белки представляют собой хлорофилл ( производное порфирина , которое поглощает красный и синий спектры света , отражая таким образом зеленый цвет), содержащийся внутри органелл , называемых хлоропластами , которые наиболее распространены в клетках листьев , тогда как у бактерий они встроены в плазму . мембрана . В этих светозависимых реакциях некоторая энергия используется для отрыва электронов от подходящих веществ, таких как вода, с образованием газообразного кислорода. Водород, высвобождаемый при расщеплении воды, используется для создания двух дополнительных соединений, которые служат кратковременными запасами энергии для последующего запуска других реакций: восстановленного никотинамидадениндинуклеотидфосфата (НАДФН) и аденозинтрифосфата (АТФ), «энергетического валюта» ячеек.
В растениях, водорослях и цианобактериях сахара синтезируются посредством последующей последовательности светонезависимых реакций, называемых циклом Кальвина . В цикле Кальвина углекислый газ из атмосферы включается в уже существующие органические соединения углерода, такие как рибулозобисфосфат (RuBP). [3] Используя АТФ и НАДФН, образующиеся в результате светозависимых реакций, полученные соединения затем восстанавливаются и удаляются с образованием дополнительных углеводов, таких как глюкоза . У других бактерий для достижения той же цели используются другие механизмы, такие как обратный цикл Кребса .
Первые фотосинтезирующие организмы, вероятно, возникли на ранних этапах эволюционной истории жизни и, скорее всего, использовали восстановители, такие как водород или сероводород , а не воду, в качестве источников электронов. [4] Цианобактерии появились позже; избыток кислорода, который они производили, непосредственно способствовал насыщению Земли кислородом , [5] что сделало возможной эволюцию сложной жизни . Сегодня средняя скорость захвата энергии фотосинтезом во всем мире составляет примерно 130 тераватт , [6] [7] [8] , что примерно в восемь раз превышает нынешнее энергопотребление человеческой цивилизации . [9] Фотосинтезирующие организмы также преобразуют около 100–115 миллиардов тонн (91–104 петаграмм Пг , или миллиард метрических тонн) углерода в биомассу в год. [10] [11] То, что растения получают некоторую энергию от света – в дополнение к воздуху, почве и воде – было впервые обнаружено в 1779 году Яном Ингенхаузом .
Фотосинтез жизненно важен для климатических процессов, поскольку он улавливает углекислый газ из воздуха, а затем связывает углерод в растениях и далее в почвах и собранных продуктах. По оценкам, только зерновые ежегодно связывают 3,825 Тг (тераграмм) или 3,825 Пг (петаграмм) углекислого газа, т.е. 3,825 миллиарда метрических тонн. [12]

Большинство фотосинтезирующих организмов являются фотоавтотрофами , что означает, что они способны синтезировать пищу непосредственно из углекислого газа и воды, используя энергию света. Однако не все организмы используют углекислый газ в качестве источника атомов углерода для осуществления фотосинтеза; фотогетеротрофы используют в качестве источника углерода органические соединения, а не углекислый газ. [2]
У растений, водорослей и цианобактерий фотосинтез выделяет кислород. Этот кислородный фотосинтез на сегодняшний день является наиболее распространенным типом фотосинтеза, используемым живыми организмами. Некоторые тенелюбивые растения (сциофиты) производят в процессе фотосинтеза настолько мало кислорода, что используют весь его сами, вместо того, чтобы выбрасывать в атмосферу. [13]
Хотя существуют некоторые различия между кислородным фотосинтезом у растений , водорослей и цианобактерий , общий процесс у этих организмов весьма схож. Существует также множество разновидностей аноксигенного фотосинтеза , используемого в основном бактериями, которые потребляют углекислый газ, но не выделяют кислород. [ нужна цитата ]
Углекислый газ превращается в сахара в процессе, называемом фиксацией углерода ; фотосинтез улавливает энергию солнечного света для преобразования углекислого газа в углеводы . Фиксация углерода представляет собой эндотермическую окислительно-восстановительную реакцию. В общих чертах фотосинтез является противоположностью клеточного дыхания : фотосинтез — это процесс восстановления углекислого газа до углеводов, а клеточное дыхание — это окисление углеводов или других питательных веществ до углекислого газа. Питательные вещества, используемые в клеточном дыхании, включают углеводы, аминокислоты и жирные кислоты. Эти питательные вещества окисляются с образованием углекислого газа и воды, а также с выделением химической энергии, необходимой для метаболизма организма .
Фотосинтез и клеточное дыхание — это разные процессы, поскольку они происходят посредством разных последовательностей химических реакций и в разных клеточных компартментах . [ нужна цитата ]
Общее уравнение фотосинтеза, впервые предложенное Корнелисом ван Нилем, выглядит так: [14]
Поскольку вода используется в качестве донора электронов при оксигенном фотосинтезе, уравнение этого процесса имеет вид:
Это уравнение подчеркивает, что вода является одновременно реагентом в светозависимой реакции и продуктом светонезависимой реакции, но сокращение n молекул воды с каждой стороны дает чистое уравнение:
Другие процессы заменяют воду другими соединениями (такими как арсенит ) в качестве источника электронов; например, некоторые микробы используют солнечный свет для окисления арсенита до арсената : [15] Уравнение этой реакции:
Фотосинтез происходит в два этапа. На первом этапе светозависимые реакции или световые реакции улавливают энергию света и используют ее для создания переносчика водорода НАДФН и молекулы-хранилища энергии АТФ . На втором этапе светонезависимые реакции используют эти продукты для улавливания и восстановления углекислого газа.
Большинство организмов, использующих кислородный фотосинтез, используют видимый свет для светозависимых реакций, хотя по крайней мере три используют коротковолновое инфракрасное или, точнее, дальнее красное излучение. [17]
Некоторые организмы используют еще более радикальные варианты фотосинтеза. Некоторые археи используют более простой метод, в котором используется пигмент, аналогичный тем, которые используются для зрения у животных. Бактериородопсин меняет свою конфигурацию в ответ на солнечный свет, действуя как протонный насос. Это создает более непосредственный градиент протонов, который затем преобразуется в химическую энергию. Этот процесс не предполагает фиксации углекислого газа и не выделяет кислород и, по-видимому, развился отдельно от более распространенных типов фотосинтеза. [18]

У фотосинтезирующих бактерий белки, собирающие свет для фотосинтеза, встроены в клеточные мембраны . В простейшей форме это касается мембраны, окружающей саму клетку. [19] Однако мембрана может быть плотно свернута в цилиндрические листы, называемые тилакоидами , [20] или собрана в круглые пузырьки , называемые интрацитоплазматическими мембранами . [21] Эти структуры могут заполнить большую часть внутренней части клетки, придавая мембране очень большую площадь поверхности и, следовательно, увеличивая количество света, которое могут поглощать бактерии. [20]
У растений и водорослей фотосинтез происходит в органеллах , называемых хлоропластами . Типичная растительная клетка содержит от 10 до 100 хлоропластов. Хлоропласт окружен мембраной. Эта мембрана состоит из фосфолипидной внутренней мембраны, фосфолипидной внешней мембраны и межмембранного пространства. Оболочкой окружена водная жидкость, называемая стромой. В строму встроены стопки тилакоидов (гран), которые являются местом фотосинтеза. Тилакоиды имеют вид уплощенных дисков. Сам тилакоид окружен тилакоидной мембраной, а внутри замкнутого объема находится просвет или тилакоидное пространство. В тилакоидную мембрану встроены интегральные и периферические мембранные белковые комплексы фотосинтетической системы.
Растения поглощают свет преимущественно с помощью пигмента хлорофилла . Зеленая часть спектра света не поглощается, а отражается, поэтому большинство растений имеют зеленый цвет. Помимо хлорофилла, растения также используют пигменты, такие как каротины и ксантофиллы . [22] Водоросли также используют хлорофилл, но присутствуют и другие пигменты, такие как фикоцианин , каротины и ксантофиллы в зеленых водорослях , фикоэритрин в красных водорослях (родофитах) и фукоксантин в бурых водорослях и диатомовых водорослях , что приводит к широкому разнообразию цветов.
Эти пигменты встроены в растения и водоросли в комплексы, называемые антенными белками. В таких белках пигменты работают вместе. Такое сочетание белков еще называют светособирающим комплексом . [23]
Хотя все клетки зеленых частей растения имеют хлоропласты, большинство из них находится в специально приспособленных структурах, называемых листьями . Некоторые виды, адаптированные к условиям сильного солнечного света и засушливости , например, многие виды молочайов и кактусов , имеют основные фотосинтетические органы в стеблях. Клетки внутренних тканей листа, называемые мезофиллом , могут содержать от 450 000 до 800 000 хлоропластов на каждый квадратный миллиметр листа. Поверхность листа покрыта водостойкой восковой кутикулой , которая защищает лист от чрезмерного испарения воды и уменьшает поглощение ультрафиолетового или синего света , чтобы свести к минимуму нагревание . Прозрачный слой эпидермиса позволяет свету проходить к клеткам палисадного мезофилла, где происходит большая часть фотосинтеза.

В светозависимых реакциях одна молекула пигмента хлорофилла поглощает один фотон и теряет один электрон . Этот электрон поглощается модифицированной формой хлорофилла, называемой феофитином , которая передает электрон молекуле хинона , запуская поток электронов по цепи переноса электронов , что приводит к окончательному восстановлению НАДФ до НАДФН . Кроме того, это создает протонный градиент (градиент энергии) на мембране хлоропласта , который используется АТФ-синтазой в синтезе АТФ . Молекула хлорофилла в конечном итоге восстанавливает электрон, который она потеряла, когда молекула воды расщепляется в процессе, называемом фотолизом , в результате которого выделяется кислород .
Общее уравнение светозависимых реакций в условиях нециклического потока электронов в зеленых растениях имеет вид: [24]
Не все длины волн света могут поддерживать фотосинтез. Спектр фотосинтетического действия зависит от типа присутствующих дополнительных пигментов . Например, у зеленых растений спектр действия напоминает спектр поглощения хлорофиллов и каротиноидов с пиками поглощения в фиолетово-синем и красном свете . У красных водорослей спектр действия представляет собой сине-зеленый свет, который позволяет этим водорослям использовать синий конец спектра для роста в более глубоких водах, которые отфильтровывают более длинные волны (красный свет), используемые надземными зелеными растениями. Непоглощенная часть светового спектра придает цвет фотосинтезирующим организмам (например, зеленым растениям, красным водорослям, пурпурным бактериям) и наименее эффективна для фотосинтеза в соответствующих организмах.
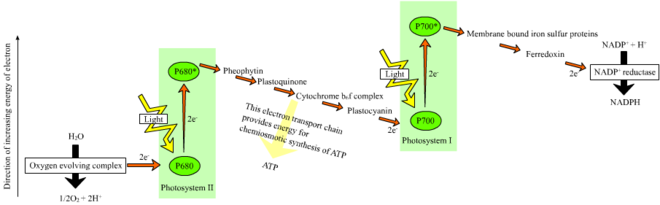
У растений светозависимые реакции происходят в тилакоидных мембранах хлоропластов , где они управляют синтезом АТФ и НАДФН. Светозависимые реакции имеют две формы: циклическую и нециклическую.
В нециклической реакции фотоны захватываются светособирающими антенными комплексами фотосистемы II хлорофиллом и другими вспомогательными пигментами (см . схему справа). Поглощение фотона антенным комплексом ослабляет электрон посредством процесса, называемого фотоиндуцированным разделением заряда . Антенная система лежит в основе молекулы хлорофилла реакционного центра фотосистемы II. Этот освобожденный электрон поглощается первичной молекулой-акцептором электронов феофитином. Когда электроны перемещаются по цепи переноса электронов (так называемая Z-схема, показанная на схеме), хемиосмотический потенциал генерируется за счет перекачки катионов протонов (H + ) через мембрану в пространство тилакоида. Фермент АТФ- синтаза использует этот хемиосмотический потенциал для образования АТФ во время фотофосфорилирования , тогда как НАДФН является продуктом терминальной окислительно-восстановительной реакции в Z-схеме . Электрон входит в молекулу хлорофилла в фотосистеме I. Там он далее возбуждается светом, поглощаемым этой фотосистемой . Затем электрон проходит по цепочке акцепторов электронов , которым он передает часть своей энергии. Энергия, передаваемая акцепторам электронов, используется для перемещения ионов водорода через мембрану тилакоида в просвет. Электрон в конечном итоге используется для восстановления кофермента НАДФ с Н + до НАДФН (который выполняет функции в светонезависимой реакции); в этот момент путь этого электрона заканчивается.
Циклическая реакция аналогична реакции нециклической, но отличается тем, что генерируется только АТФ и восстановленный НАДФ (НАДФН) не образуется. Циклическая реакция происходит только в фотосистеме I. Как только электрон вытесняется из фотосистемы, электрон передается вниз по молекулам-акцепторам электронов и возвращается в фотосистему I, откуда он был испущен, отсюда и название циклической реакции .
Линейный транспорт электронов через фотосистему приводит к окислению реакционного центра этой фотосистемы. Подъем другого электрона сначала потребует повторного восстановления реакционного центра. Возбужденные электроны, потерянные из реакционного центра (Р700) фотосистемы I, замещаются переносом от пластоцианина , электроны которого поступают в результате транспорта электронов через фотосистему II . Фотосистема II, как первая ступень Z-схемы , требует внешнего источника электронов для восстановления окисленного хлорофилла в реакционном центре. Источником электронов для фотосинтеза у зеленых растений и цианобактерий является вода. Две молекулы воды окисляются за счет энергии четырех последовательных реакций разделения зарядов фотосистемы II с образованием молекулы двухатомного кислорода и четырех ионов водорода . Образовавшиеся электроны передаются на редокс-активный остаток тирозина , который окисляется за счет энергии P680 + . Это сбрасывает способность P680 поглощать другой фотон и высвобождать еще один фотодиссоциированный электрон. Окисление воды катализируется в фотосистеме II окислительно-восстановительной структурой, содержащей четыре иона марганца и ион кальция; этот комплекс, выделяющий кислород, связывает две молекулы воды и содержит четыре окислительных эквивалента, которые используются для запуска реакции окисления воды (диаграммы S-состояний Кока). Ионы водорода высвобождаются в просвете тилакоида и, следовательно, способствуют трансмембранному хемиосмотическому потенциалу, который приводит к синтезу АТФ. Кислород является отходом светозависимых реакций, но большинство организмов на Земле используют кислород и его энергию для клеточного дыхания , включая фотосинтезирующие организмы. [25] [26]
В светонезависимых (или «темновых») реакциях фермент RuBisCO захватывает CO 2 из атмосферы и в процессе, называемом циклом Кальвина , использует вновь образовавшийся НАДФН и высвобождает трехуглеродные сахара, которые позже соединяются с образованием сахароза и крахмал. Общее уравнение светонезависимых реакций в зеленых растениях имеет вид [24] : 128.

Фиксация углерода приводит к образованию трехуглеродного промежуточного продукта сахара, который затем превращается в конечные углеводные продукты. Простые углеродные сахара, образующиеся в результате фотосинтеза, затем используются для образования других органических соединений, таких как строительный материал целлюлоза , предшественники биосинтеза липидов и аминокислот или в качестве топлива при клеточном дыхании . Последнее происходит не только у растений, но и у животных , когда углерод и энергия растений передаются по пищевой цепи .
Фиксация или восстановление углекислого газа — это процесс, в котором углекислый газ соединяется с пятиуглеродным сахаром, рибулозо-1,5-бисфосфатом , с образованием двух молекул трехуглеродного соединения, глицерат-3-фосфата , также известного как 3-. фосфоглицерат. Глицерат-3-фосфат в присутствии АТФ и НАДФН , образующихся на светозависимых стадиях, восстанавливается до глицеральдегид-3-фосфата . Этот продукт также называют 3-фосфоглицеральдегидом ( PGAL ) или, в более общем смысле, триозофосфатом . Большая часть (5 из 6 молекул) производимого глицеральдегид-3-фосфата используется для регенерации рибулозо-1,5-бисфосфата, чтобы процесс мог продолжаться. Триозофосфаты, не «переработанные таким образом», часто конденсируются с образованием гексозофосфатов , которые в конечном итоге дают сахарозу , крахмал и целлюлозу , а также глюкозу и фруктозу . Сахара, образующиеся в ходе углеродного метаболизма , образуют углеродные скелеты, которые можно использовать для других метаболических реакций, таких как производство аминокислот и липидов .

В жарких и засушливых условиях растения закрывают устьица , чтобы предотвратить потерю воды. В этих условиях содержание CO 2 будет уменьшаться, а количество газообразного кислорода, образующегося в результате световых реакций фотосинтеза, увеличиваться, вызывая усиление фотодыхания за счет оксигеназной активности рибулозо-1,5-бисфосфаткарбоксилазы/оксигеназы и снижение фиксации углерода. Некоторые растения выработали механизмы увеличения концентрации CO 2 в листьях в этих условиях. [27]
Растения, использующие процесс фиксации углерода C4 , химически фиксируют углекислый газ в клетках мезофилла, добавляя его к трехуглеродной молекуле фосфоенолпирувата (PEP), реакция, катализируемая ферментом под названием PEP-карбоксилаза , создавая четырехуглеродную органическую кислоту. щавелевоуксусная кислота . Щавелосуксусная кислота или малат , синтезированные этим процессом, затем транслоцируются в специализированные клетки оболочки пучка , где расположены фермент RuBisCO и другие ферменты цикла Кальвина, и где CO 2 , высвободившийся в результате декарбоксилирования четырехуглеродных кислот, затем фиксируется активностью RuBisCO на трех -углерод -3-фосфоглицериновые кислоты . Физическое отделение RuBisCO от световых реакций, генерирующих кислород, снижает фотодыхание и увеличивает фиксацию CO 2 и, следовательно, фотосинтетическую способность листа. [28] Растения C 4 могут производить больше сахара, чем растения C 3, в условиях высокой освещенности и температуры. Многие важные сельскохозяйственные культуры являются растениями C 4 , включая кукурузу, сорго, сахарный тростник и просо. Растения, которые не используют PEP-карбоксилазу для фиксации углерода, называются C 3 -растениями , поскольку первичная реакция карбоксилирования, катализируемая RuBisCO, производит трехуглеродные 3-фосфоглицериновые кислоты непосредственно в цикле Кальвина-Бенсона. Более 90% растений используют фиксацию углерода C 3 по сравнению с 3%, которые используют фиксацию углерода C 4 ; [29] однако эволюция C4 в более чем 60 линиях растений делает его ярким примером конвергентной эволюции . [27] Фотосинтез C 2 , который включает концентрацию углерода путем избирательного расщепления фотодыхательного глицина, является одновременно эволюционным предшественником C 4 и полезным CCM сам по себе. [30]
Ксерофиты , такие как кактусы и большинство суккулентов , также используют PEP-карбоксилазу для улавливания углекислого газа в процессе, называемом метаболизмом крассуловой кислоты (CAM). В отличие от метаболизма C 4 , который пространственно отделяет фиксацию CO 2 к PEP от цикла Кальвина, CAM разделяет эти два процесса во времени . Растения CAM имеют анатомию листьев, отличную от растений C 3 , и фиксируют CO 2 ночью, когда их устьица открыты. Растения CAM сохраняют CO 2 в основном в форме яблочной кислоты посредством карбоксилирования фосфоенолпирувата до оксалоацетата, который затем восстанавливается до малата. Декарбоксилирование малата в течение дня приводит к высвобождению CO 2 внутри листьев, что позволяет RuBisCO фиксировать углерод до 3-фосфоглицерата. CAM используется 16 000 видами растений. [31]
Растения, накапливающие оксалат кальция , такие как Amaranthus Hybridus и Colobanthus quitnsis , демонстрируют разновидность фотосинтеза, при которой кристаллы оксалата кальция функционируют как динамические пулы углерода, поставляя углекислый газ ( CO 2 ) в фотосинтезирующие клетки, когда устьица частично или полностью закрыты. Этот процесс получил название тревожного фотосинтеза . В условиях стресса (например, при дефиците воды) оксалат, высвобождаемый из кристаллов оксалата кальция, преобразуется в CO 2 под действием фермента оксалатоксидазы , и образующийся CO 2 может поддерживать реакции цикла Кальвина . Реактивная перекись водорода ( H 2 O 2 ), побочный продукт оксалатоксидазной реакции, может быть нейтрализована каталазой . Сигнальный фотосинтез представляет собой вариант фотосинтеза, добавляемый к хорошо известным путям C4 и CAM . Однако тревожный фотосинтез, в отличие от этих путей, действует как биохимический насос, собирающий углерод из внутренней части органа (или из почвы), а не из атмосферы. [32] [33]
Цианобактерии обладают карбоксисомами , которые увеличивают концентрацию CO 2 вокруг RuBisCO, увеличивая скорость фотосинтеза. Фермент карбоангидраза , расположенный внутри карбоксисомы, высвобождает CO 2 из растворенных ионов гидрокарбоната (HCO−
3). Прежде чем CO 2 диффундирует наружу, он быстро поглощается RuBisCO, который концентрируется внутри карбоксисом. ОЗС−
3ионы образуются из CO 2 вне клетки под действием другой карбоангидразы и активно закачиваются в клетку мембранным белком. Они не могут пересечь мембрану, поскольку заряжены, и внутри цитозоля очень медленно превращаются обратно в CO 2 без помощи карбоангидразы. Это приводит к тому, что HCO−
3ионы накапливаются внутри клетки, откуда они диффундируют в карбоксисомы. [34] Пиреноиды в водорослях и роголистниках также способствуют концентрации CO 2 вокруг RuBisCO. [35]
Общий процесс фотосинтеза проходит в четыре этапа: [11]
Растения обычно преобразуют свет в химическую энергию с эффективностью фотосинтеза 3–6%. [36] [37] Поглощенный свет, который не преобразуется, рассеивается в основном в виде тепла, при этом небольшая часть (1–2%) [38] повторно излучается в виде флуоресценции хлорофилла на более длинных (более красных) длинах волн. Это обстоятельство позволяет измерять световую реакцию фотосинтеза с помощью хлорофилловых флуориметров. [38]
Фактическая эффективность фотосинтеза растений зависит от частоты преобразуемого света, интенсивности света, температуры и доли углекислого газа в атмосфере и может варьироваться от 0,1% до 8%. [39] Для сравнения: солнечные панели преобразуют свет в электрическую энергию с эффективностью примерно 6–20% для панелей массового производства и более 40% для лабораторных устройств. Ученые изучают фотосинтез в надежде получить растения с повышенной урожайностью. [37]
Эффективность как световых, так и темновых реакций можно измерить, но взаимосвязь между ними может быть сложной. [40] Например, энергетические молекулы АТФ и НАДФН, созданные в результате световой реакции, могут использоваться для фиксации углерода или для фотодыхания в растениях C 3 . [40] Электроны также могут перетекать к другим стокам электронов. [41] [42] [43] По этой причине авторы нередко проводят различие между работой, выполняемой в нефотодыхательных условиях и в фотодыхательных условиях. [44] [45] [46]
Флуоресценция хлорофилла фотосистемы II может измерять световую реакцию, а инфракрасные газоанализаторы могут измерять темновую реакцию. [47] Также возможно исследовать оба одновременно, используя интегрированный флуорометр хлорофилла и систему газообмена, или используя вместе две отдельные системы. [48] Инфракрасные газоанализаторы и некоторые датчики влажности достаточно чувствительны для измерения фотосинтетической ассимиляции CO 2 и ΔH 2 O с использованием надежных методов . [49] CO 2 обычно измеряется в мкмоль/(м 2 /с), частях на единицу. миллион или объем на миллион, а H 2 O обычно измеряется в ммоль/(м 2 /с) или в мбарах. [49] Измеряя ассимиляцию CO 2 , ΔH 2 O, температуру листа, барометрическое давление, площадь листа и фотосинтетически активное излучение или ФАР, становится возможным оценить «А» или ассимиляцию углерода «Е» или транспирацию «гс». " или устьичная проводимость, и Ci или внутриклеточный CO 2 . [49] Тем не менее, там, где это возможно, чаще используют флуоресценцию хлорофилла для измерения стресса растений, поскольку наиболее часто используемые параметры FV/FM и Y(II) или F/FM' можно измерить за несколько секунд, что позволяет исследование более крупных популяций растений. [46]
Системы газообмена, обеспечивающие контроль уровня CO 2 выше и ниже уровня окружающей среды, позволяют использовать общепринятую практику измерения кривых A/Ci при различных уровнях CO 2 для характеристики фотосинтетической реакции растения. [49]
Встроенный флуорометр хлорофилла — системы газообмена позволяют более точно измерить реакцию и механизмы фотосинтеза. [47] [48] В то время как стандартные системы газообменного фотосинтеза могут измерять Ci или уровни CO 2 в устьице , добавление интегрированных измерений флуоресценции хлорофилла позволяет более точно измерить CC для замены Ci. [48] [50] Оценка CO 2 в месте карбоксилирования в хлоропластах, или CC , становится возможной при измерении проводимости мезофилла или g m с использованием интегрированной системы. [47] [48] [51]
Системы измерения фотосинтеза не предназначены для прямого измерения количества света, поглощаемого листом. Но анализ флуоресценции хлорофилла, поглощения P700 и P515 и измерений газообмена позволяет получить подробную информацию, например, о фотосистемах, квантовой эффективности и скорости ассимиляции CO 2 . С помощью некоторых инструментов можно анализировать даже зависимость эффективности фотосинтеза от длины волны. [52]
Явление, известное как квантовое блуждание, значительно повышает эффективность переноса энергии света. В фотосинтетической клетке водоросли, бактерии или растения есть светочувствительные молекулы, называемые хромофорами , расположенные в форме антенны, называемой фотокомплексом. Когда фотон поглощается хромофором, он превращается в квазичастицу , называемую экситоном , которая перепрыгивает от хромофора к хромофору к реакционному центру фотокомплекса, совокупности молекул, которые улавливают его энергию в химической форме, доступной для клеточный метаболизм. Волновые свойства экситона позволяют ему покрывать более широкую территорию и опробовать несколько возможных путей одновременно, позволяя мгновенно «выбрать» наиболее эффективный маршрут, по которому он будет иметь наибольшую вероятность прибытия к месту назначения за минимально возможное время.
Поскольку это квантовое блуждание происходит при температурах, намного более высоких, чем обычно происходят квантовые явления, оно возможно только на очень коротких расстояниях. Препятствия в виде деструктивной интерференции заставляют частицу на мгновение терять свои волновые свойства, прежде чем она вновь обретет их после освобождения из заблокированного положения посредством классического «прыжка». Таким образом, движение электрона к фотоцентру рассматривается как серия обычных прыжков и квантовых блужданий. [53] [54] [55]
Возраст окаменелостей того, что считается нитчатыми фотосинтезирующими организмами, составляет 3,4 миллиарда лет. [56] [57] Более поздние исследования также показывают, что фотосинтез мог начаться около 3,4 миллиарда лет назад. [58] [59] , хотя первые прямые доказательства фотосинтеза получены из тилакоидных мембран, сохранившихся в кремнях , возраст которых составлял 1750 миллионов лет назад . [60]
Основным источником кислорода в атмосфере Земли является кислородный фотосинтез , и его появление иногда называют кислородной катастрофой . Геологические данные свидетельствуют о том, что кислородный фотосинтез, например, у цианобактерий , стал важным в палеопротерозойскую эру около 2 миллиардов лет назад. Современный фотосинтез у растений и большинства фотосинтезирующих прокариот является оксигенным, с использованием воды в качестве донора электронов, которая окисляется до молекулярного кислорода в фотосинтетическом реакционном центре .

Несколько групп животных установили симбиотические отношения с фотосинтезирующими водорослями. Они наиболее распространены в кораллах , губках и морских анемонах . Предполагается, что это связано с особенно простым строением тела и большой площадью поверхности по сравнению с их объемами. [61] Кроме того, некоторые морские моллюски Elysia viridis и Elysia chromotica также поддерживают симбиотические отношения с хлоропластами, которые они захватывают из водорослей в своем рационе и затем сохраняют в своем организме (см. Клептопластика ). Это позволяет моллюскам выживать исключительно за счет фотосинтеза в течение нескольких месяцев. [62] [63] Некоторые гены из ядра растительной клетки даже были перенесены слизнякам, так что хлоропласты могут снабжаться белками, необходимыми им для выживания. [64]
Еще более тесная форма симбиоза может объяснить происхождение хлоропластов. Хлоропласты имеют много общего с фотосинтезирующими бактериями, включая кольцевую хромосому , рибосому прокариотического типа и аналогичные белки в фотосинтетическом реакционном центре. [65] [66] Эндосимбиотическая теория предполагает, что фотосинтезирующие бактерии были приобретены (путем эндоцитоза ) ранними эукариотическими клетками, чтобы сформировать первые растительные клетки. Следовательно, хлоропласты могут быть фотосинтезирующими бактериями, приспособившимися к жизни внутри растительных клеток. Как и митохондрии , хлоропласты обладают собственной ДНК, отдельной от ядерной ДНК клеток-хозяев растений, и гены в этой ДНК хлоропластов напоминают гены, обнаруженные у цианобактерий . [67] ДНК в хлоропластах кодирует окислительно-восстановительные белки, подобные тем, которые обнаруживаются в фотосинтетических реакционных центрах. Гипотеза CoRR предполагает, что такое совместное расположение генов с их генными продуктами необходимо для окислительно-восстановительной регуляции экспрессии генов и объясняет устойчивость ДНК в биоэнергетических органеллах. [68]
Исключены симбиотические и клептопластические организмы:
За исключением эвгленид, которые встречаются в пределах Excavata , все они относятся к Diaphoretickes . Археопластида и фотосинтетическая Паулинелла получили свои пластиды, окруженные двумя мембранами, в результате первичного эндосимбиоза в двух отдельных событиях, поглощая цианобактерию. Пластиды во всех других группах имеют происхождение из красных или зеленых водорослей и называются «красными линиями» и «зелеными линиями». Единственным известным исключением является инфузория Pseudoblepharisma tenue , которая помимо пластид, происходящих из зеленых водорослей, имеет в качестве симбионта еще и пурпурную серную бактерию . У динофлагеллят и эвгленид пластиды окружены тремя мембранами, а у остальных линий — четырьмя. Нуклеоморф — остатки исходного ядра водоросли, расположенные между внутренней и наружной мембранами пластиды, имеется у криптофитов (из красной водоросли) и хлорарахниофитов (из зеленой водоросли). [69] Некоторые динофлагелляты, утратившие свою фотосинтетическую способность, позже вновь восстановили ее в результате новых эндосимбиотических событий с различными водорослями. Многие из этих групп эукариот способны осуществлять фотосинтез, но являются миксотрофами и в различной степени гетеротрофны .
Считается , что ранние фотосинтетические системы, такие как у зеленых и пурпурных серных и зеленых и пурпурных несерных бактерий , были аноксигенными и использовали в качестве доноров электронов различные другие молекулы, кроме воды . Считается, что зеленые и пурпурные серные бактерии использовали водород и серу в качестве доноров электронов. Зеленые несерные бактерии использовали в качестве доноров электронов различные аминокислоты и другие органические кислоты . Пурпурные несерные бактерии использовали множество неспецифических органических молекул. Использование этих молекул согласуется с геологическими данными о том, что ранняя атмосфера Земли в то время сильно восстанавливалась . [70]
За возможным исключением Heimdallarchaeota , фотосинтез у архей не обнаружен . [71] Галоархеи фототрофны и могут поглощать энергию Солнца, но не собирают углерод из атмосферы и, следовательно, не фотосинтезируют. [72] Вместо хлорофилла они используют родопсины, которые преобразуют энергию света в ионные градиенты, но не могут опосредовать реакции переноса электронов. [73] [74]
В настоящее время у бактерий известны восемь фотосинтетических линий: [75] [76] [77] [78]
Биохимическая способность использовать воду в качестве источника электронов при фотосинтезе однажды развилась у общего предка современных цианобактерий (ранее называвшихся сине-зелеными водорослями). Геологические данные указывают на то, что это преобразующее событие произошло в начале истории Земли, по крайней мере 2450–2320 миллионов лет назад (млн лет назад), и, как предполагается, намного раньше. [79] [80] Поскольку атмосфера Земли почти не содержала кислорода во время предполагаемого развития фотосинтеза, считается, что первые фотосинтезирующие цианобактерии не производили кислород. [81] Имеющиеся данные геобиологических исследований архейских ( > 2500 млн лет назад) осадочных пород указывают на то, что жизнь существовала 3500 млн лет назад, но вопрос о том, когда появился кислородный фотосинтез, до сих пор остается без ответа. Четкое палеонтологическое окно в эволюцию цианобактерий открылось около 2000 млн лет назад, открыв уже разнообразную биоту цианобактерий. Цианобактерии оставались основными первичными производителями кислорода на протяжении всего протерозойского периода (2500–543 млн лет назад), отчасти потому, что окислительно-восстановительная структура океанов благоприятствовала фотоавтотрофам, способным к фиксации азота . [ нужна ссылка ] Зеленые водоросли присоединились к цианобактериям в качестве основных основных производителей кислорода на континентальных шельфах ближе к концу протерозоя , но только с мезозойской (251–66 млн лет назад) радиацией динофлагеллят, кокколитофорид и диатомей произошло первичное производство кислорода. в морских шельфовых водах принимают современный вид. Цианобактерии по-прежнему имеют решающее значение для морских экосистем как основные производители кислорода в океанических круговоротах, как агенты биологической фиксации азота и, в модифицированной форме, как пластиды морских водорослей. [82]
Хотя некоторые этапы фотосинтеза до сих пор до конца не изучены, общее уравнение фотосинтеза известно с 19 века.

Ян ван Гельмонт начал исследование этого процесса в середине 17 века, когда он тщательно измерил массу почвы , используемой растением, и массу растения по мере его роста. Заметив, что масса почвы изменилась очень мало, он выдвинул гипотезу, что масса растущего растения должна происходить из воды, единственного вещества, которое он добавлял в горшечное растение. Его гипотеза оказалась частично верной — большая часть набранной массы происходит за счет углекислого газа, а также воды. Однако это стало сигналом к идее о том, что основная часть биомассы растения образуется в результате фотосинтеза, а не из самой почвы.
Джозеф Пристли , химик и священник, обнаружил, что когда он изолировал объем воздуха под перевернутой банкой и зажигал в ней свечу (которая выделяла CO 2 ), свеча сгорала очень быстро, задолго до того, как в ней заканчивался воск. . Далее он обнаружил, что мышь может аналогичным образом «повредить» воздух. Затем он показал, что воздух, «испорченный» свечой и мышью, можно восстановить с помощью растения. [83]
В 1779 году Ян Ингенхауз повторил эксперименты Пристли. Он обнаружил, что именно влияние солнечного света на растение может заставить его оживить мышь за считанные часы. [83] [84]
В 1796 году Жан Сенебье , швейцарский пастор, ботаник и натуралист, продемонстрировал, что зеленые растения потребляют углекислый газ и выделяют кислород под воздействием света. Вскоре после этого Николя-Теодор де Соссюр показал, что увеличение массы растения по мере его роста может происходить не только за счет поглощения CO 2 , но и за счет включения воды. Таким образом, была намечена основная реакция, посредством которой фотосинтез используется для производства продуктов питания (например, глюкозы). [85]
Корнелис Ван Ниль сделал ключевые открытия, объясняющие химию фотосинтеза. Изучая пурпурные серобактерии и зеленые бактерии, он первым продемонстрировал, что фотосинтез представляет собой светозависимую окислительно-восстановительную реакцию, в которой водород восстанавливает (отдает свои атомы в виде электронов и протонов) углекислого газа.
Роберт Эмерсон обнаружил две световые реакции, проверяя продуктивность растений с использованием света разной длины волны. Только красный цвет подавлял световые реакции. Когда синий и красный были объединены, результат был гораздо более существенным. Таким образом, существовало две фотосистемы: одна поглощала длины волн до 600 нм, другая — до 700 нм. Первый известен как PSII, второй — PSI. PSI содержит только хлорофилл «а», PSII содержит преимущественно хлорофилл «а» с большей частью доступного хлорофилла «b», среди других пигментов. К ним относятся фикобилины, являющиеся красными и синими пигментами красных и синих водорослей соответственно, и фукоксантол для бурых водорослей и диатомовых водорослей. Процесс наиболее продуктивен, когда поглощение квантов одинаково как в PSII, так и в PSI, гарантируя, что входная энергия от антенного комплекса делится между системами PSI и PSII, что, в свою очередь, приводит в действие фотохимию. [11]
Роберт Хилл считал, что комплекс реакций состоит из промежуточного соединения с цитохромом b 6 (ныне пластохиноном), а другой - с цитохрома f на этап механизмов генерации углеводов. Они связаны пластохиноном, которому требуется энергия для восстановления цитохрома f. Дальнейшие эксперименты, доказывающие, что кислород, образующийся при фотосинтезе зеленых растений, поступает из воды, были проведены Хиллом в 1937 и 1939 годах. Он показал, что изолированные хлоропласты выделяют кислород в присутствии неприродных восстановителей, таких как оксалат железа , феррицианид или бензохинон , после воздействия. осветить. В реакции Хилла: [86]
А – акцептор электронов. Поэтому на свету акцептор электронов восстанавливается и выделяется кислород. Сэмюэль Рубен и Мартин Кеймен использовали радиоактивные изотопы , чтобы определить, что кислород, выделяемый при фотосинтезе, поступает из воды.

Мелвин Кэлвин и Эндрю Бенсон вместе с Джеймсом Башемом выяснили путь ассимиляции углерода (цикл фотосинтетического восстановления углерода) в растениях. Цикл сокращения выбросов углерода известен как цикл Кальвина , но многие ученые называют его циклом Кальвина-Бенсона, Бенсона-Кельвина или даже циклом Кальвина-Бенсона-Башама (или CBB).
Лауреат Нобелевской премии ученый Рудольф А. Маркус позже смог открыть функцию и значение цепи переноса электронов.
Отто Генрих Варбург и Дин Берк открыли I-квантовую реакцию фотосинтеза, которая расщепляет CO 2 , активируемую дыханием. [87]
В 1950 году Отто Кандлер представил первые экспериментальные доказательства существования фотофосфорилирования in vivo, используя интактные клетки хлореллы и интерпретируя свои открытия как светозависимое образование АТФ . [88] В 1954 году Дэниел И. Арнон и др. обнаружил фотофосфорилирование in vitro в изолированных хлоропластах с помощью Р 32 . [89] [90]
Луи Н. М. Дуйсенс и Ян Амес обнаружили, что хлорофилл «а» поглощает один свет и окисляет цитохром f, в то время как хлорофилл «а» (и другие пигменты) поглощают другой свет, но восстанавливают тот же самый окисленный цитохром, заявив, что две световые реакции происходят в ряд.
В 1893 году американский ботаник Чарльз Рид Барнс предложил два термина — фотосинтаксис и фотосинтез — для биологического процесса синтеза сложных соединений углерода из угольной кислоты в присутствии хлорофилла под воздействием света . Термин «фотосинтез» происходит от греческого phōs (φῶς, сияние) и синтеза (σύνθεσις, расположение вместе), [91] [92] [93] , а другое слово, которое он обозначил, было фотосинтакс , от синтаксиса (σύνταξις, конфигурация). Со временем термин фотосинтез вошел в обиход. Позднее открытие аноксигенных фотосинтезирующих бактерий и фотофосфорилирования потребовало переопределения этого термина. [94]
В конце 1940-х годов в Калифорнийском университете в Беркли детали фотосинтетического метаболизма углерода разбирались химиками Мелвином Кэлвином , Эндрю Бенсоном, Джеймсом Бэшемом и множеством студентов и исследователей, использующих методы изотопа углерода-14 и бумажной хроматографии. [95] Путь фиксации CO 2 водорослями хлореллой за долю секунды на свету привел к образованию трехуглеродной молекулы, называемой фосфоглицериновой кислотой (PGA). За эту оригинальную и новаторскую работу Мелвину Кальвину в 1961 году была присуждена Нобелевская премия по химии. Параллельно физиологи растений изучали газообмен листьев, используя новый метод инфракрасного газового анализа и листовую камеру, где чистая скорость фотосинтеза варьировалась от от 10 до 13 мкмоль CO 2 ·м -2 ·с -1 , с выводом, что все наземные растения обладают одинаковыми фотосинтетическими способностями, которые насыщаются светом при менее чем 50% солнечного света. [96] [97]
Позже, в 1958–1963 годах, в Корнельском университете сообщалось, что кукуруза , выращенная в полевых условиях, имеет гораздо более высокую скорость фотосинтеза листьев - 40 мкмоль CO 2 ·м -2 ·с -1 и не насыщается при почти полном солнечном свете. [98] [99] Этот более высокий показатель у кукурузы был почти вдвое выше, чем у других видов, таких как пшеница и соя, что указывает на то, что между высшими растениями существуют большие различия в фотосинтезе. В Университете Аризоны подробное исследование газообмена у более чем 15 видов однодольных и двудольных растений впервые выявило, что различия в анатомии листьев являются решающими факторами в дифференциации фотосинтетических способностей между видами. [100] [101] У тропических трав, включая кукурузу, сорго, сахарный тростник, бермудскую траву и двудольный амарант, скорость фотосинтеза листьев составляла около 38-40 мкмоль CO 2 ·м -2 ·с -1 , а листья имели два типы зеленых клеток, т.е. наружный слой клеток мезофилла, окружающий плотно упакованные хлорофильные клетки оболочки сосудистого пучка. Этот тип анатомии был назван анатомией Кранца в 19 веке ботаником Готлибом Хаберландтом во время изучения анатомии листьев сахарного тростника. [102] Виды растений с наибольшей скоростью фотосинтеза и анатомией Кранца не показали явного фотодыхания, очень низкую точку компенсации CO 2 , высокую оптимальную температуру, высокую устойчивость устьиц и более низкую устойчивость мезофилла к диффузии газа, а также скорость никогда не насыщаются при полном солнечном свете. [103] Исследование в Аризоне было признано Citation Classic в 1986 году. [101] Эти виды позже были названы растениями C4, поскольку первое стабильное соединение, фиксирующее CO 2 на свету, имеет четыре атома углерода в виде малата и аспартата. [104] [105] [106] Другие виды, у которых отсутствует анатомия Кранца, были названы типом C3, например хлопок и подсолнечник, поскольку первым стабильным углеродным соединением является трехуглеродный PGA. При концентрации CO 2 1000 ppm в воздухе растения C3 и C4 имели одинаковую скорость фотосинтеза листьев около 60 мкмоль CO 2 ·м -2 ·с -1 , что указывает на подавление фотодыхания у растений C3. [100] [101]

Есть четыре основных фактора, влияющих на фотосинтез [ нужны разъяснения ] и несколько сопутствующих факторов. Четыре основных: [107]
Общий фотосинтез ограничен рядом факторов окружающей среды. К ним относятся количество доступного света, площадь листьев , которые растение должно улавливать свет (затенение другими растениями является основным ограничением фотосинтеза), скорость, с которой углекислый газ может поступать в хлоропласты для поддержки фотосинтеза, доступность воды и наличие подходящей температуры для проведения фотосинтеза. [108]

Процесс фотосинтеза обеспечивает основной вклад свободной энергии в биосферу и является одним из четырех основных способов, которыми радиация важна для жизни растений. [109]
Радиационный климат внутри растительных сообществ чрезвычайно изменчив как во времени, так и в пространстве.
В начале 20-го века Фредерик Блэкман и Габриэль Маттеи исследовали влияние интенсивности света ( облучения ) и температуры на скорость ассимиляции углерода.
Эти два эксперимента иллюстрируют несколько важных моментов: во-первых, известно, что на фотохимические реакции, как правило, температура не влияет . Однако эти эксперименты ясно показывают, что температура влияет на скорость ассимиляции углерода, поэтому в полном процессе ассимиляции углерода должно происходить два набора реакций. Это светозависимая «фотохимическая» независимая от температуры стадия и светонезависимая, зависящая от температуры стадия. Во-вторых, эксперименты Блэкмана иллюстрируют концепцию ограничивающих факторов . Еще одним ограничивающим фактором является длина волны света. Цианобактерии, обитающие на глубине нескольких метров под водой, не могут получать нужные длины волн, необходимые для фотоиндуцированного разделения зарядов в обычных фотосинтетических пигментах. Для борьбы с этой проблемой у цианобактерий есть светособирающий комплекс, называемый фикобилисомой . [110] Этот комплекс состоит из ряда белков с различными пигментами, окружающих реакционный центр.

По мере роста концентрации углекислого газа скорость образования сахаров в результате светонезависимых реакций увеличивается, пока не будет ограничена другими факторами. RuBisCO , фермент, который захватывает углекислый газ в светонезависимых реакциях, имеет сродство связывания как с углекислым газом, так и с кислородом. Когда концентрация углекислого газа высока, RuBisCO фиксирует углекислый газ. Однако если концентрация углекислого газа низкая, RuBisCO будет связывать кислород вместо углекислого газа. Этот процесс, называемый фотодыханием , использует энергию, но не производит сахара.
Активность оксигеназы RuBisCO невыгодна для растений по нескольким причинам:
Путь утилизации продуктов оксигеназной активности RuBisCO более известен как фотодыхание, поскольку он характеризуется светозависимым потреблением кислорода и выделением углекислого газа.
Это первоначальное включение углерода в органические соединения известно как фиксация углерода.
100 × 10 15 грамм углерода/год фиксируется фотосинтезирующими организмами, что эквивалентно4 × 10 18 кДж/год =4 × 10 21 Дж/год свободной энергии хранится в виде восстановленного углерода.
Средняя глобальная скорость фотосинтеза составляет 130 ТВт.
{{cite web}}: CS1 maint: unfit URL (link)