Цезий ( написание ИЮПАК ; [8] цезий в американском английском ) [примечание 1] — химический элемент ; он имеет символ Cs и атомный номер 55. Это мягкий серебристо-золотистый щелочной металл с температурой плавления 28,5 ° C (83,3 ° F; 301,6 К), что делает его одним из пяти элементарных металлов , которые являются жидкими при температуре или около комнатной температуры . [примечание 2] Цезий имеет физические и химические свойства, аналогичные свойствам рубидия и калия . Он пирофорен и реагирует с водой даже при температуре -116 ° C (-177 ° F). Это наименее электроотрицательный элемент со значением 0,79 по шкале Полинга . Он имеет только один стабильный изотоп — цезий-133 . Цезий добывается в основном из поллуцита . Цезий-137 , продукт деления , добывается из отходов ядерных реакторов . Он имеет самый большой атомный радиус среди всех элементов, радиусы которых были измерены или рассчитаны, — около 260 пикометров .
Немецкий химик Роберт Бунзен и физик Густав Кирхгоф открыли цезий в 1860 году с помощью недавно разработанного метода пламенной спектроскопии . Первые небольшие применения цезия были в качестве « поглотителя » в электронных лампах и фотоэлектрических элементах . В 1967 году, действуя на основании доказательства Эйнштейна , что скорость света является наиболее постоянным измерением во Вселенной, Международная система единиц использовала два конкретных волновых счета из спектра излучения цезия-133 для совместного определения второго и второго. метр . С тех пор цезий широко использовался в высокоточных атомных часах .
С 1990-х годов наибольшее применение этого элемента было в качестве формиата цезия для буровых растворов , но он имеет ряд применений в производстве электроэнергии, в электронике и химии. Радиоактивный изотоп цезий-137 имеет период полураспада около 30 лет и используется в медицине, промышленных датчиках и гидрологии. Нерадиоактивные соединения цезия лишь слегка токсичны , но склонность чистого металла к взрывной реакции с водой означает, что цезий считается опасным материалом, а радиоизотопы представляют значительную опасность для здоровья и окружающей среды.

Из всех элементов, твердых при комнатной температуре, цезий самый мягкий: его твердость составляет 0,2 Мооса. Это очень пластичный , бледный металл, темнеющий в присутствии следовых количеств кислорода . [13] [14] [15] В присутствии минерального масла (где его лучше всего хранить во время транспортировки) оно теряет металлический блеск и приобретает более тусклый, серый вид. Его температура плавления составляет 28,5 °C (83,3 °F), что делает его одним из немногих элементарных металлов, которые находятся в жидком состоянии при температуре около комнатной . Ртуть — единственный стабильный элементный металл с известной температурой плавления ниже, чем у цезия. [примечание 3] [17] Кроме того, металл имеет довольно низкую температуру кипения , 641 ° C (1186 ° F), самую низкую из всех металлов, кроме ртути. [18] Его соединения горят синим [19] [20] или фиолетовым [20] цветом.

Цезий образует сплавы с другими щелочными металлами, золотом и ртутью ( амальгамы ). При температуре ниже 650 °C (1202 °F) он не сплавляется с кобальтом , железом , молибденом , никелем , платиной , танталом или вольфрамом . Он образует четко определенные интерметаллические соединения с сурьмой , галлием , индием и торием , которые являются светочувствительными . [13] Он смешивается со всеми другими щелочными металлами (кроме лития); сплав с молярным распределением 41% цезия, 47% калия и 12% натрия имеет самую низкую температуру плавления среди всех известных металлических сплавов - -78 ° C (-108 ° F). [17] [21] Было изучено несколько амальгам: CsHg
2черный с фиолетовым металлическим блеском , а CsHg — золотистый, также с металлическим блеском. [22]
Золотой цвет цезия обусловлен уменьшением частоты света, необходимого для возбуждения электронов щелочных металлов по мере нисхождения группы. Для лития через рубидий эта частота находится в ультрафиолете, а для цезия она попадает в сине-фиолетовый конец спектра; другими словами, плазмонная частота щелочных металлов становится ниже от лития к цезию. Таким образом, цезий преимущественно пропускает и частично поглощает фиолетовый свет, в то время как другие цвета (имеющие более низкую частоту) отражаются; поэтому он кажется желтоватым. [23]
Цезий существует в виде различных аллотропов, одним из которых является димер, называемый дицезием [24] .
Металлический цезий обладает высокой реакционной способностью и пирофорностью . Он самовозгорается на воздухе и взрывоопасно реагирует с водой даже при низких температурах, в большей степени, чем другие щелочные металлы . [13] Он реагирует со льдом при температуре до -116 ° C (-177 ° F). [17] Из-за своей высокой реакционной способности металлический цезий классифицируется как опасный материал . Его хранят и отправляют в сухих насыщенных углеводородах, таких как минеральное масло . С ним можно работать только в среде инертного газа , например аргона . Однако взрыв воды цезия часто менее мощный, чем взрыв воды натрия с аналогичным количеством натрия. Это связано с тем, что цезий мгновенно взрывается при контакте с водой, оставляя мало времени для накопления водорода . [25] Цезий можно хранить в ампулах из боросиликатного стекла , запаянных под вакуумом . В количествах более 100 граммов (3,5 унции) цезий поставляется в герметично закрытых контейнерах из нержавеющей стали. [13]
Химический состав цезия аналогичен химическому составу других щелочных металлов, в частности рубидия , элемента, расположенного выше цезия в периодической таблице. [26] Как и ожидалось для щелочного металла, единственная общая степень окисления — +1. [примечание 4] Некоторые небольшие различия возникают из-за того, что он имеет более высокую атомную массу и является более электроположительным , чем другие (нерадиоактивные) щелочные металлы. [29] Цезий является наиболее электроположительным химическим элементом. [примечание 5] [17] Ион цезия также больше и менее «твердый», чем ионы более легких щелочных металлов .
Большинство соединений цезия содержат этот элемент в виде катиона Cs .+
, который ионно связывается с широким спектром анионов . Заслуживающим внимания исключением является цезид- анион ( Cs−
), [27] и другие представляют собой несколько субоксидов (см. раздел об оксидах ниже). Совсем недавно было предсказано, что цезий будет вести себя как элемент p-блока и способен образовывать высшие фториды с более высокими степенями окисления (т.е. CsF n с n > 1) под высоким давлением. [31] Это предсказание должно быть подтверждено дальнейшими экспериментами. [32]
Соли Cs + обычно бесцветны, если только сам анион не окрашен. Многие простые соли гигроскопичны , но в меньшей степени, чем соответствующие соли более легких щелочных металлов. Фосфат , [33] ацетат , карбонат , галогениды , оксиды , нитраты и сульфаты растворимы в воде . Его двойные соли часто менее растворимы, и низкая растворимость сульфата алюминия-цезия используется при очистке Cs из руд. Двойные соли сурьмы (например, CsSbCl
4), висмут , кадмий , медь , железо и свинец также плохо растворимы . [13]
Гидроксид цезия (CsOH) гигроскопичен и сильноосновен . [26] Он быстро травит поверхность полупроводников , таких как кремний . [34] CsOH ранее считался химиками «самым сильным основанием», что отражает относительно слабое притяжение между большим ионом Cs + и OH - ; [19] это действительно сильнейшая база Аррениуса ; однако ряд соединений, таких как н -бутиллитий , амид натрия , гидрид натрия , гидрид цезия и т. д., которые не растворяются в воде, поскольку бурно с ней реагируют, а скорее используются только в некоторых безводных полярных апротонных растворителях , являются гораздо более основными. на основе кислотно-основной теории Брёнстеда-Лоури . [26]
Стехиометрическая смесь цезия и золота при нагревании будет реагировать с образованием желтого аурида цезия (Cs + Au - ). Аурид-анион здесь ведет себя как псевдогалоген . Соединение бурно реагирует с водой, образуя гидроксид цезия , металлическое золото и газообразный водород; в жидком аммиаке он может вступать в реакцию с ионообменной смолой, специфичной для цезия, с образованием аурида тетраметиламмония . Аналогичное соединение платины , красный платинид цезия ( Cs2Pt ), содержит ион платинида, который ведет себя как псевдохалькоген . [35]
Как и все катионы металлов, Cs + образует в растворе комплексы с основаниями Льюиса . Из-за своего большого размера Cs + обычно имеет координационные числа, превышающие 6, число, типичное для меньших катионов щелочных металлов. Эта разница проявляется в 8-координации CsCl. Это высокое координационное число и мягкость (склонность к образованию ковалентных связей) являются свойствами, используемыми при отделении Cs + от других катионов при реабилитации ядерных отходов, где 137 Cs + необходимо отделять от больших количеств нерадиоактивного K + . [36]

Фторид цезия (CsF) представляет собой гигроскопичное белое твердое вещество, широко используемое во фторорганической химии в качестве источника фторид- анионов. [38] Фторид цезия имеет структуру галита, что означает, что Cs + и F − упаковываются в кубическую плотнейшую упаковку, как это делают Na + и Cl − в хлориде натрия . [26] Примечательно, что цезий и фтор имеют самую низкую и самую высокую электроотрицательность соответственно среди всех известных элементов.
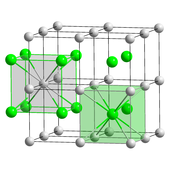
Хлорид цезия (CsCl) кристаллизуется в простой кубической кристаллической системе . Этот структурный мотив , также называемый «структурой хлорида цезия», [29] состоит из примитивной кубической решетки с двухатомной основой, каждый из которых имеет восьмикратную координацию ; атомы хлорида лежат в узлах решетки на краях куба, а атомы цезия лежат в отверстиях в центре кубов. Эта структура является общей с CsBr и CsI , а также многими другими соединениями, не содержащими Cs. Напротив, большинство других щелочных галогенидов имеют структуру хлорида натрия (NaCl). [29] Структура CsCl предпочтительна, поскольку Cs + имеет ионный радиус 174 пм , а Cl−
181 вечера. [39]

В большей степени, чем другие щелочные металлы, цезий образует с кислородом многочисленные бинарные соединения . При горении цезия на воздухе образуется супероксид CsO .
2является основным продуктом. [40] «Нормальный» оксид цезия ( Cs
2O ) образует желто-оранжевые гексагональные кристаллы [41] и является единственным оксидом анти- CdCl .
2тип. [42] Он испаряется при 250 ° C (482 ° F) и разлагается на металлический цезий и пероксид Cs.
2О
2при температуре выше 400 °C (752 °F). Помимо супероксида и озонида CsO3, [43] [44] также были изучены несколько ярко окрашенных субоксидов . [45] К ним относятся Cs
7О , Цс
4О , Цс
11О
3, Кс
3O (темно-зеленый [46] ), CsO, Cs
3О
2, [47] а также Cs
7О
2. [48] [49] Последний можно нагревать в вакууме для получения Cs .
2О. _ [42] Также существуют бинарные соединения с серой , селеном и теллуром . [13]
Цезий имеет 41 известный изотоп , массовое число (т.е. количество нуклонов в ядре) варьируется от 112 до 152. Некоторые из них синтезируются из более легких элементов в процессе медленного захвата нейтронов ( S-процесс ) внутри старых звезд [50] и R-процессом при взрывах сверхновых . [51] Единственным стабильным изотопом цезия является 133 Cs с 78 нейтронами . Хотя он имеет большой ядерный спин (7/2+), исследования ядерного магнитного резонанса позволяют использовать этот изотоп на резонансной частоте 11,7 МГц . [52]

Радиоактивный 135 Cs имеет очень длительный период полураспада — около 2,3 миллиона лет — самый длинный из всех радиоактивных изотопов цезия. Периоды полураспада 137 Cs и 134 Cs составляют 30 и два года соответственно. 137 Cs разлагается до короткоживущего 137m Ba путем бета-распада , а затем до нерадиоактивного бария, а 134 Cs превращается непосредственно в 134 Ba. Изотопы с массовыми числами 129, 131, 132 и 136 имеют период полураспада от одного дня до двух недель, в то время как у большинства других изотопов период полураспада составляет от нескольких секунд до долей секунды. Существует по крайней мере 21 метастабильный ядерный изомер . За исключением 134m Cs (с периодом полураспада чуть менее 3 часов), все они очень нестабильны и распадаются с периодом полураспада несколько минут или меньше. [53] [54]
Изотоп 135 Cs — один из долгоживущих продуктов деления урана , производимого в ядерных реакторах . [55] Однако выход этого продукта деления снижается в большинстве реакторов, поскольку его предшественник, 135 Xe , является мощным нейтронным ядом и часто превращается в стабильный 136 Xe , прежде чем он может распасться до 135 Cs. [56] [57]
Бета -распад от 137 Cs до 137m Ba приводит к гамма-излучению , поскольку 137m Ba релаксирует в основное состояние 137 Ba, при этом испускаемые фотоны имеют энергию 0,6617 МэВ. [58] 137 Cs и 90 Sr являются основными среднеживущими продуктами ядерного деления и основными источниками радиоактивности отработавшего ядерного топлива после нескольких лет охлаждения, продолжающегося несколько сотен лет. [59] Эти два изотопа являются крупнейшим источником остаточной радиоактивности в районе чернобыльской катастрофы . [60] Из-за низкой скорости захвата утилизация 137 Cs путем захвата нейтронов невозможна, и единственное нынешнее решение — позволить ему распасться с течением времени. [61]
Почти весь цезий, образующийся в результате ядерного деления, происходит в результате бета-распада первоначально более богатых нейтронами продуктов деления, проходящих через различные изотопы йода и ксенона . [62] Поскольку йод и ксенон летучи и могут диффундировать через ядерное топливо или воздух, радиоактивный цезий часто образуется вдали от исходного места деления. [63] В ходе испытаний ядерного оружия в 1950-х и 1980-х годах 137 Cs был выброшен в атмосферу и вернулся на поверхность земли в виде компонента радиоактивных осадков . Это готовый маркер движения почвы и отложений того времени. [13]

Цезий — относительно редкий элемент, содержание которого в земной коре оценивается в среднем в 3 части на миллион . [64] Это 45-й по распространенности элемент и 36-й среди металлов. Тем не менее его больше, чем таких элементов, как сурьма , кадмий , олово и вольфрам , и на два порядка больше, чем ртути и серебра ; его содержание на 3,3% меньше, чем у рубидия , с которым он тесно связан химически. [13]
Из-за большого ионного радиуса цезий относится к числу « несовместимых элементов ». [65] Во время кристаллизации магмы цезий концентрируется в жидкой фазе и кристаллизуется последним. Поэтому крупнейшими месторождениями цезия являются зональные пегматитовые рудные тела, образовавшиеся в результате этого процесса обогащения. Поскольку цезий не заменяет калий так легко, как рубидий, минералы щелочного эвапорита сильвит (KCl) и карналлит ( KMgCl
3·6ч
2О ) может содержать всего 0,002% цезия. Следовательно, цезий содержится в немногих минералах. Процентное количество цезия можно найти в берилле ( Be
3Ал
2(SiO
3)
6) и авогадрит ( (K,Cs)BF
4), до 15 мас.% Cs 2 O в близкородственном минерале пеццоттаите ( Cs(Be
2Ли)Ал
2Си
6О
18), до 8,4 мас.% Cs 2 O в редком минерале лондоните ( (Cs,K)Al
4Быть
4(Б, быть)
12О
28), и в меньшей степени – в более распространенном родизите . [13] Единственной экономически значимой рудой для получения цезия является поллуцит Cs(AlSi
2О
6) , который встречается в нескольких местах по всему миру в зональных пегматитах, связанных с более важными с коммерческой точки зрения минералами лития , лепидолитом и петалитом . Большой размер зерен и сильное разделение минералов в пегматитах приводят к получению высококачественной руды для добычи полезных ископаемых. [66]
Самым значительным и богатым известным источником цезия в мире является шахта Танко на озере Берник в Манитобе , Канада, которая, по оценкам, содержит 350 000 метрических тонн поллуцитовой руды, что составляет более двух третей мировых запасов. [66] [67] Хотя стехиометрическое содержание цезия в поллуците составляет 42,6%, чистые образцы поллуцита из этого месторождения содержат лишь около 34% цезия, тогда как среднее содержание составляет 24% масс. [67] Коммерческий поллуцит содержит более 19% цезия. [68] Месторождение пегматита Бикита в Зимбабве добывается из-за петалита, но оно также содержит значительное количество поллуцита . Другой известный источник поллуцита находится в пустыне Карибиб , Намибия . [67] При нынешних темпах мировой добычи полезных ископаемых от 5 до 10 метрических тонн в год запасов хватит на тысячи лет. [13]
Добыча и переработка поллуцитовой руды является селективным процессом и осуществляется в меньших масштабах, чем добыча большинства других металлов. Руду измельчают, сортируют вручную, но обычно не концентрируют, а затем измельчают. Затем цезий извлекают из поллуцита в основном тремя методами: кислотным разложением, щелочным разложением и прямым восстановлением. [13] [69]
При кислотном разложении силикатная поллуцитовая порода растворяется сильными кислотами, такими как соляная (HCl), серная ( H
2ТАК
4), бромистоводородная (HBr) или плавиковая (HF) кислоты. С соляной кислотой образуется смесь растворимых хлоридов, а нерастворимые хлоридные двойные соли цезия осаждаются в виде хлорида цезия и сурьмы ( Cs
4SbCl
7), хлорид цезия иода ( Cs
2ICl ), или гексахлорцерат цезия ( Cs
2(ЦеСл
6) ). После разделения чистая выпавшая в осадок двойная соль разлагается, а чистый CsCl осаждается выпариванием воды.
Метод серной кислоты дает нерастворимую двойную соль непосредственно в виде цезиевых квасцов ( CsAl(SO
4)
2·12 часов
2О ). Компонент сульфата алюминия преобразуется в нерастворимый оксид алюминия путем обжига квасцов углем , а полученный продукт выщелачивается водой с получением Cs.
2ТАК
4решение. [13]
Обжиг поллуцита с карбонатом кальция и хлоридом кальция дает нерастворимые силикаты кальция и растворимый хлорид цезия. Выщелачивание водой или разбавленным аммиаком ( NH
4OH ) дает разбавленный раствор хлорида (CsCl). Этот раствор можно выпарить для получения хлорида цезия или превратить в цезиевые квасцы или карбонат цезия. Хотя это коммерчески неосуществимо, руду можно напрямую восстановить калием, натрием или кальцием в вакууме для непосредственного получения металлического цезия. [13]
Большая часть добытого цезия (в виде солей) напрямую преобразуется в формиат цезия (HCOO − Cs + ) для таких применений, как бурение нефтяных скважин . Для снабжения развивающегося рынка компания Cabot Corporation в 1997 году построила завод по производству раствора формиата цезия на шахте Танко недалеко от озера Берник в Манитобе мощностью 12 000 баррелей (1 900 м 3 ) в год. [70] Основными мелкомасштабными коммерческими соединениями цезия являются хлорид и нитрат цезия . [71]
Альтернативно, металлический цезий может быть получен из очищенных соединений, полученных из руды. Хлорид цезия и другие галогениды цезия можно восстановить при температуре от 700 до 800 ° C (от 1292 до 1472 ° F) с помощью кальция или бария , а из полученного продукта перегнать металлический цезий. Таким же образом алюминат, карбонат или гидроксид можно восстановить магнием . [13]
Металл также можно выделить электролизом плавленого цианида цезия (CsCN). Исключительно чистый и безгазовый цезий может быть получен термическим разложением азида цезия CsN при температуре 390 °C (734 °F ) .
3, который можно получить из водного раствора сульфата цезия и азида бария . [69] В вакууме дихромат цезия может взаимодействовать с цирконием с образованием чистого металлического цезия без других газообразных продуктов. [71]
Цена цезия с чистотой 99,8% (в металлической основе) в 2009 году составляла около 10 долларов за грамм (280 долларов за унцию), но эти соединения значительно дешевле. [67]

В 1860 году Роберт Бунзен и Густав Кирхгоф обнаружили цезий в минеральной воде из Дюркгейма , Германия. Из-за ярких синих линий в спектре излучения они получили название от латинского слова caesius , что означает « голубовато-серый » . [примечание 6] [72] [73] [74] Цезий был первым элементом, который был обнаружен с помощью спектроскопа , который был изобретен Бунзеном и Кирхгофом всего год назад. [17]
Чтобы получить чистый образец цезия, необходимо было выпарить 44 000 литров (9 700 имп галлонов; 12 000 галлонов США) минеральной воды, чтобы получить 240 килограммов (530 фунтов) концентрированного раствора соли. Щелочноземельные металлы осаждаются в виде сульфатов или оксалатов , оставляя щелочной металл в растворе. После перевода в нитраты и экстракции этанолом получали смесь, не содержащую натрия. Из этой смеси литий осаждали карбонатом аммония . Калий, рубидий и цезий образуют с платинохлористоводородной кислотой нерастворимые соли , но эти соли обнаруживают небольшую разницу в растворимости в горячей воде, а менее растворимые гексахлорплатинаты цезия и рубидия ( ( Cs,Rb) 2PtCl6 ) были получены фракционной кристаллизацией . . После восстановления гексахлорплатината водородом цезий и рубидий разделились за счет разницы растворимости их карбонатов в спирте. В результате процесса из первоначальных 44 000 литров минеральной воды было получено 9,2 грамма (0,32 унции) хлорида рубидия и 7,3 грамма (0,26 унции) хлорида цезия. [73]
По хлориду цезия двое ученых оценили атомный вес нового элемента в 123,35 (по сравнению с принятым в настоящее время значением в 132,9). [73] Они попытались получить элементарный цезий электролизом расплавленного хлорида цезия, но вместо металла получили синее однородное вещество, которое «ни невооруженным глазом, ни под микроскопом не показало ни малейшего следа металлического вещества»; в результате они отнесли его к субхлориду ( Cs
2Кл ). На самом деле продукт, вероятно, представлял собой коллоидную смесь металла и хлорида цезия. [75] Электролиз водного раствора хлорида с помощью ртутного катода дал амальгаму цезия, которая легко разлагалась в водных условиях. [73] Чистый металл был в конечном итоге выделен шведским химиком Карлом Сеттербергом , когда он работал над докторской диссертацией вместе с Кекуле и Бунзеном. [74] В 1882 году он произвел металлический цезий путем электролиза цианида цезия , избежав проблем с хлоридом. [76]
Исторически сложилось так, что наиболее важным применением цезия были исследования и разработки, прежде всего в химической и электротехнической областях. Для цезия существовало очень мало применений до 1920-х годов, когда он начал использоваться в радиовакуумных лампах , где у него было две функции; в качестве геттера он удалял лишний кислород после изготовления, а в качестве покрытия на нагретом катоде увеличивал электропроводность . Цезий не был признан высокопроизводительным промышленным металлом до 1950-х годов. [77] Нерадиоактивный цезий применяется в фотоэлектрических элементах , фотоумножителях , оптических компонентах инфракрасных спектрофотометров , катализаторах некоторых органических реакций, кристаллах для сцинтилляционных счетчиков и в магнитогидродинамических генераторах энергии . [13] Цезий также используется в качестве источника положительных ионов во вторичной ионной масс-спектрометрии (ВИМС).
С 1967 года Международная система измерений основывает основную единицу времени, вторую, на свойствах цезия. Международная система единиц (СИ) определяет секунду как продолжительность 9 192 631 770 циклов на микроволновой частоте спектральной линии , соответствующей переходу между двумя уровнями сверхтонкой энергии основного состояния цезия -133 . [78] 13-я Генеральная конференция по мерам и весам 1967 года определила секунду как: «продолжительность 9 192 631 770 циклов микроволнового света, поглощаемого или излучаемого в результате сверхтонкого перехода атомов цезия-133 в их основном состоянии, не подвергающегося воздействию внешних полей».
Наибольшее использование нерадиоактивного цезия в настоящее время приходится на буровые растворы на основе формиата цезия для добывающей нефтяной промышленности . [13] Водные растворы формиата цезия (HCOO - Cs + ), полученные путем взаимодействия гидроксида цезия с муравьиной кислотой , были разработаны в середине 1990-х годов для использования в качестве жидкостей для бурения нефтяных скважин и заканчивания скважин . Функция бурового раствора заключается в смазке буровых долот, выведении шлама на поверхность и поддержании давления на пласт во время бурения скважины. Жидкости для заканчивания способствуют установке контрольно-измерительного оборудования после бурения, но до начала добычи, поддерживая давление. [13]
Высокая плотность рассола формиата цезия (до 2,3 г/см 3 , или 19,2 фунта на галлон) [79] в сочетании с относительно безопасной природой большинства соединений цезия снижает потребность в токсичных взвешенных веществах высокой плотности в буровой раствор — значительное технологическое, инженерное и экологическое преимущество. В отличие от компонентов многих других тяжелых жидкостей, формиат цезия относительно безопасен для окружающей среды. [79] Рассол формиата цезия можно смешать с формиатами калия и натрия, чтобы снизить плотность жидкостей до плотности воды (1,0 г/см 3 , или 8,3 фунта на галлон). Кроме того, он биоразлагаем и может быть переработан, что немаловажно ввиду его высокой стоимости (около 4000 долларов за баррель в 2001 году). [80] Формиаты щелочи безопасны в обращении и не повреждают продуктивный пласт или скважинные металлы, как коррозионная альтернатива рассолам высокой плотности (таким как бромид цинка ZnBr) .
2решения) иногда делают; они также требуют меньше очистки и снижают затраты на утилизацию. [13]

Атомные часы на основе цезия используют в качестве точки отсчета электромагнитные переходы в сверхтонкой структуре атомов цезия-133. Первые точные цезиевые часы были построены Луисом Эссеном в 1955 году в Национальной физической лаборатории Великобритании. [81] За последние полвека цезиевые часы усовершенствовались и считаются «наиболее точной реализацией устройства, которого когда-либо достигло человечество». [78] Эти часы измеряют частоту с погрешностью от 2 до 3 частей на 10 14 , что соответствует точности 2 наносекунд в день или одной секунды за 1,4 миллиона лет. Последние версии точнее, чем 1 часть из 10 15 , примерно 1 секунда за 20 миллионов лет. [13] Цезиевый стандарт является основным стандартом для соответствующих стандартам измерений времени и частоты. [82] Цезиевые часы регулируют время работы сетей сотовой связи и Интернета. [83]
Второй символ s — единица времени в системе СИ. МБМВ подтвердил свое определение на своей 26-й конференции в 2018 году: «[ Второе ] определяется путем принятия фиксированного численного значения частоты цезия Δ ν Cs , невозмущенной частоты сверхтонкого перехода в основное состояние атома цезия-133, как9 192 631 770 в единицах Гц , равных с -1 ». [84]
Термоэмиссионные генераторы на парах цезия представляют собой устройства малой мощности, преобразующие тепловую энергию в электрическую. В двухэлектродном ламповом преобразователе цезий нейтрализует пространственный заряд вблизи катода и усиливает ток. [85]
Цезий также важен своими фотоэмиссионными свойствами, преобразующими свет в поток электронов. Он используется в фотоэлектрических элементах , поскольку катоды на основе цезия, такие как интерметаллическое соединение K
2CsSb имеют низкое пороговое напряжение эмиссии электронов . [86] В число фотоэмиссионных устройств, использующих цезий, входят устройства оптического распознавания символов , фотоумножители и трубки видеокамер . [87] [88] Тем не менее, германий , рубидий, селен, кремний, теллур и некоторые другие элементы могут заменить цезий в светочувствительных материалах. [13]
Кристаллы йодида цезия (CsI), бромида (CsBr) и фторида (CsF) используются в качестве сцинтилляторов в сцинтилляционных счетчиках, широко используемых в разведке полезных ископаемых и исследованиях в области физики элементарных частиц для обнаружения гамма- и рентгеновского излучения. Будучи тяжелым элементом, цезий обеспечивает хорошую останавливающую способность и лучшее обнаружение. Соединения цезия могут обеспечивать более быстрый отклик (CsF) и быть менее гигроскопичными (CsI).
Пары цезия используются во многих распространенных магнитометрах . [89]
Этот элемент используется в качестве внутреннего стандарта в спектрофотометрии . [90] Как и другие щелочные металлы , цезий имеет большое сродство к кислороду и используется в качестве « поглотителя » в вакуумных лампах . [91] Другие области применения металла включают высокоэнергетические лазеры , паровые лампы накаливания и выпрямители пара . [13]
Высокая плотность иона цезия делает растворы хлорида цезия, сульфата цезия и трифторацетата цезия ( Cs(O)
2CCF
3) ) полезен в молекулярной биологии для ультрацентрифугирования в градиенте плотности . [92] Эта технология используется в основном для выделения вирусных частиц , субклеточных органелл и фракций, а также нуклеиновых кислот из биологических образцов. [93]

Относительно немногие химические приложения используют цезий. [94] Легирование соединениями цезия повышает эффективность некоторых металл-ионных катализаторов химического синтеза, таких как акриловая кислота , антрахинон , оксид этилена , метанол , фталевый ангидрид , стирол , мономеры метилметакрилата и различные олефины . Он также используется при каталитической конверсии диоксида серы в триоксид серы при производстве серной кислоты . [13]
Фторид цезия находит широкое применение в органической химии в качестве основания [26] и безводного источника фторид -иона. [95] Соли цезия иногда заменяют соли калия или натрия в органическом синтезе , таком как циклизация , этерификация и полимеризация . Цезий также использовался в дозиметрии термолюминесцентного излучения (ТЛД) : под воздействием радиации он приобретает кристаллические дефекты, которые при нагревании возвращаются с испусканием света, пропорционального полученной дозе. Таким образом, измерение светового импульса с помощью фотоумножителя может позволить количественно оценить накопленную дозу радиации.
Цезий-137 — радиоизотоп , обычно используемый в качестве гамма -излучателя в промышленности. Его преимущества включают период полураспада около 30 лет, его доступность в ядерном топливном цикле и наличие 137 Ба в качестве стабильного конечного продукта. Высокая растворимость в воде является недостатком, который делает его несовместимым с облучателями больших бассейнов для пищевых продуктов и медикаментов. [96] Его использовали в сельском хозяйстве, лечении рака, стерилизации продуктов питания, осадка сточных вод и хирургического оборудования. [13] [97] Радиоактивные изотопы цезия в радиационных устройствах использовались в медицинской сфере для лечения некоторых видов рака, [98] но появление лучших альтернатив и использование водорастворимого хлорида цезия в источниках, которые могли бы создать широкомасштабное загрязнение постепенно вывело некоторые из этих источников цезия из употребления. [99] [100] Цезий-137 использовался в различных промышленных измерительных приборах, включая датчики влажности, плотности, выравнивания и толщиномеры. [101] Он также использовался в устройствах каротажа скважин для измерения электронной плотности горных пород, которая аналогична объемной плотности пород. [102]
Цезий-137 использовался в гидрологических исследованиях, аналогичных исследованиям трития . В качестве дочернего продукта испытаний бомбы деления в период с 1950-х по середину 1980-х годов цезий-137 был выброшен в атмосферу, где он легко абсорбировался в раствор. Известные межгодовые колебания в течение этого периода позволяют провести корреляцию со слоями почвы и отложений. Цезий-134 и, в меньшей степени, цезий-135 также использовался в гидрологии для измерения выхода цезия в атомной энергетике. Хотя они менее распространены, чем цезий-133 или цезий-137, эти изотопы-лидеры производятся исключительно из антропогенных источников. [103]

Цезий и ртуть использовались в качестве топлива в первых ионных двигателях , предназначенных для движения космических кораблей в очень длительных межпланетных или внепланетных полетах. Ионизация топлива осуществлялась контактом с заряженным вольфрамовым электродом. Но коррозия компонентов космического корабля цезием подтолкнула разработку в направлении использования топлива из инертного газа, такого как ксенон , с которым легче обращаться при наземных испытаниях и которые наносят меньший потенциальный ущерб космическому кораблю. [13] Ксенон использовался в экспериментальном космическом корабле Deep Space 1 , запущенном в 1998 году. [104] [105] Тем не менее, были построены автоэмиссионные электрические двигательные установки, которые ускоряют ионы жидких металлов, таких как цезий. [106]
Нитрат цезия используется в качестве окислителя и пиротехнического красителя для сжигания кремния в инфракрасных вспышках , [107] таких как вспышка ЛУУ-19, [108] , поскольку он излучает большую часть своего света в ближнем инфракрасном спектре. [109] Соединения цезия, возможно, использовались в качестве добавок к топливу для уменьшения радиолокационной заметности выхлопных газов в самолете -разведчике ЦРУ Lockheed A-12 . [110] Цезий и рубидий добавляются в стекло в виде карбоната , поскольку они уменьшают электропроводность и улучшают стабильность и долговечность волоконной оптики и приборов ночного видения . Фторид цезия или фторид цезия-алюминия используются во флюсах, предназначенных для пайки алюминиевых сплавов, содержащих магний . [13]
Магнитогидродинамические (МГД) энергогенерирующие системы были исследованы, но не получили широкого распространения. [111] Металлический цезий также рассматривается в качестве рабочего тела в высокотемпературных турбоэлектрических генераторах с циклом Ренкина . [112]
Соли цезия были оценены как противошоковые реагенты после применения препаратов мышьяка . Однако из-за их влияния на сердечный ритм их используют реже, чем соли калия или рубидия. Их также использовали для лечения эпилепсии . [13]
Цезий-133 можно охладить лазером и использовать для исследования фундаментальных и технологических проблем квантовой физики . Он имеет особенно удобный спектр Фешбаха , позволяющий изучать ультрахолодные атомы , требующие настраиваемых взаимодействий. [113]

Нерадиоактивные соединения цезия умеренно токсичны, а нерадиоактивный цезий не представляет значительной опасности для окружающей среды. Поскольку биохимические процессы могут сбить с толку и заменить цезий калием , избыток цезия может привести к гипокалиемии , аритмии и острой остановке сердца , но такие количества обычно не встречаются в природных источниках. [116] [117]
Средняя смертельная доза (LD 50 ) хлорида цезия для мышей составляет 2,3 г на килограмм, что сопоставимо со значениями LD 50 хлорида калия и хлорида натрия . [118] Нерадиоактивный цезий в основном используется в качестве формиата цезия в нефтяных буровых растворах , поскольку он гораздо менее токсичен, чем альтернативы, хотя и более дорог. [79]
Металлический цезий является одним из наиболее реакционноспособных элементов и очень взрывоопасен в присутствии воды. Газообразный водород, образующийся в результате реакции, нагревается за счет выделяющейся при этом тепловой энергии, вызывая возгорание и сильный взрыв. Это может происходить и с другими щелочными металлами, но цезий настолько силен, что эту взрывную реакцию может вызвать даже холодная вода. [13]
Он очень пирофорен : температура самовоспламенения цезия составляет -116 ° C (-177 ° F), и он взрывоопасно воспламеняется на воздухе с образованием гидроксида цезия и различных оксидов. Гидроксид цезия является очень сильным основанием и быстро разъедает стекло. [18]
Изотопы 134 и 137 присутствуют в биосфере в небольших количествах в результате деятельности человека и различаются в зависимости от местоположения. Радиоцезий не накапливается в организме так быстро, как другие продукты деления (такие как радиойод и радиостронций). Около 10% поглощенного радиоцезия относительно быстро вымывается из организма с потом и мочой. Остальные 90% имеют биологический период полураспада от 50 до 150 дней. [119] Радиоцезий следует за калием и имеет тенденцию накапливаться в тканях растений, включая фрукты и овощи. [120] [121] [122] Растения сильно различаются по поглощению цезия, иногда проявляя к нему большую устойчивость. Также хорошо известно, что грибы из загрязненных лесов накапливают радиоцезий (цезий-137) в спорокарпиях грибов . [123] Накопление цезия-137 в озерах стало серьезной проблемой после чернобыльской катастрофы . [124] [125] Эксперименты на собаках показали, что разовая доза 3,8 милликюри (140 МБк , 4,1 мкг цезия-137) на килограмм является летальной в течение трех недель; [126] меньшие количества могут вызвать бесплодие и рак. [127] Международное агентство по атомной энергии и другие источники предупреждают, что радиоактивные материалы, такие как цезий-137, могут использоваться в устройствах радиологического рассеивания или « грязных бомбах ». [128]
{{cite book}}: |journal=проигнорировано ( помощь ) .