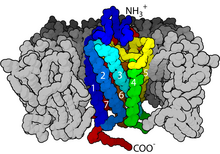
Рецепторы, связанные с G-белком ( GPCR ), также известные как рецепторы семи-(проходного)-трансмембранного домена , 7TM-рецепторы , гептаспиральные рецепторы , серпентиновые рецепторы и рецепторы, связанные с G-белком ( GPLR ), образуют большую группу эволюционно родственных белков , которые представляют собой рецепторы клеточной поверхности , которые обнаруживают молекулы вне клетки и активируют клеточные реакции. Они связаны с G-белками . Они проходят через клеточную мембрану семь раз в виде шести петель [2] (три внеклеточные петли, взаимодействующие с молекулами лигандов , три внутриклеточные петли, взаимодействующие с G-белками, N-концевая внеклеточная область и С-концевая внутриклеточная область [2] ) аминокислотных остатков , поэтому их иногда называют семитрансмембранными рецепторами. [3] Лиганды могут связываться либо с внеклеточным N-концом и петлями (например, глутаматные рецепторы), либо с сайтом связывания внутри трансмембранных спиралей ( родопсин -подобное семейство). Все они активируются агонистами , хотя также наблюдалась спонтанная автоактивация пустого рецептора. [3]
Рецепторы, связанные с G-белком, обнаружены только у эукариот , включая дрожжи , и хоанофлагеллят . [4] Лиганды , которые связывают и активируют эти рецепторы, включают светочувствительные соединения, запахи , феромоны , гормоны и нейротрансмиттеры и различаются по размеру: от небольших молекул до пептидов и крупных белков . Рецепторы, связанные с G-белком, участвуют во многих заболеваниях.
Существует два основных пути передачи сигнала с участием рецепторов, связанных с G-белком:
Когда лиганд связывается с GPCR, он вызывает конформационные изменения в GPCR, что позволяет ему действовать как фактор обмена гуаниновых нуклеотидов (GEF). Затем GPCR может активировать связанный G-белок путем обмена GDP , связанного с G-белком, на GTP . Субъединица α белка G вместе со связанным GTP может затем диссоциировать от субъединиц β и γ для дальнейшего воздействия на внутриклеточные сигнальные белки или целевые функциональные белки, непосредственно в зависимости от типа субъединицы α ( G αs , G αi/o , G αq/ 11 , Gα12 /13 ). [6] : 1160
GPCR являются важной мишенью для лекарств, и примерно 34% [7] всех лекарств, одобренных Управлением по контролю за продуктами и лекарствами (FDA), предназначены для 108 членов этого семейства. Мировой объем продаж этих препаратов оценивается в 180 миллиардов долларов США по состоянию на 2018 год [обновлять]. [7] По оценкам, GPCRs являются мишенями для около 50% лекарств, имеющихся в настоящее время на рынке, в основном из-за их участия в сигнальных путях, связанных со многими заболеваниями, т.е. психическими, метаболическими, включая эндокринологические расстройства, иммунологические, включая вирусные инфекции, сердечно-сосудистые, воспалительные, расстройства чувств и рак. Еще одной динамично развивающейся областью фармацевтических исследований является давно обнаруженная связь между GPCR и многими эндогенными и экзогенными веществами, приводящая, например, к анальгезии. [3]
С определением первой структуры комплекса между рецептором, связанным с G-белком (GPCR) и тримером G-белка (Gαβγ), в 2011 году открылась новая глава исследований GPCR для структурных исследований глобальных переключателей с более чем одним белком. расследуется. Предыдущие открытия включали определение кристаллической структуры первого GPCR, родопсина, в 2000 году и кристаллической структуры первого GPCR с диффундирующим лигандом (β 2 AR) в 2007 году. Способ, которым семь трансмембранных спиралей GPCR соединяются Собрание в пучок было заподозрено на основе модели родопсина лягушки с низким разрешением, полученной в результате исследований двумерных кристаллов с помощью криогенной электронной микроскопии . Кристаллическая структура родопсина, обнаруженная три года спустя, не стала неожиданностью, если не считать наличия дополнительной цитоплазматической спирали H8 и точного расположения петли, охватывающей место связывания с сетчаткой. Однако он предоставил основу, которая, как надеялись, станет универсальной матрицей для моделирования гомологии и разработки лекарств для других GPCR – идея, которая оказалась слишком оптимистичной.
Семь лет спустя кристаллизация β 2 -адренергического рецептора (β 2 АР) с диффундирующим лигандом принесла неожиданные результаты, поскольку выявила совершенно иную форму внеклеточной стороны рецептора, чем у родопсина. Эта область важна, поскольку она отвечает за связывание лигандов и на нее воздействуют многие лекарства. При этом место связывания лиганда было гораздо более просторным, чем в структуре родопсина, и было открыто наружу. В других рецепторах, кристаллизованных вскоре после этого, связывающая сторона была еще более доступна для лиганда. Новые структуры, дополненные биохимическими исследованиями, открыли механизмы действия молекулярных переключателей, которые модулируют структуру рецептора, приводя к состояниям активации для агонистов или к состояниям полной или частичной инактивации для обратных агонистов. [3]
Нобелевская премия по химии 2012 года была присуждена Брайану Кобилке и Роберту Лефковицу за работу, которая «имела решающее значение для понимания того, как функционируют рецепторы, связанные с G-белком». [8] По меньшей мере семь других Нобелевских премий были присуждены за некоторые аспекты передачи сигналов, опосредованной G-белком. По состоянию на 2012 год два из десяти самых продаваемых в мире лекарств ( Advair Diskus и Abilify ) действуют путем воздействия на рецепторы, связанные с G-белком. [9]

Точный размер суперсемейства GPCR неизвестен, но на основе анализа последовательности генома было предсказано, что по крайней мере 831 различный ген человека (или около 4% всего генома , кодирующего белок ) кодирует их . [10] [11] Хотя были предложены многочисленные схемы классификации, суперсемейство было классически разделено на три основных класса (A, B и C) без обнаруживаемой гомологии общих последовательностей между классами.
Самым крупным классом на сегодняшний день является класс А, на который приходится почти 85% генов GPCR. Предполагается, что из GPCR класса А более половины из них кодируют обонятельные рецепторы , в то время как остальные рецепторы связаны известными эндогенными соединениями или классифицируются как орфанные рецепторы . Несмотря на отсутствие гомологии последовательностей между классами, все GPCR имеют общую структуру и механизм передачи сигнала . Очень большая группа родопсина А была подразделена на 19 подгрупп ( А1-А19 ). [12]
Согласно классической системе AF, GPCR можно сгруппировать в шесть классов на основе гомологии последовательностей и функционального сходства: [13] [14] [15] [16]
Совсем недавно для GPCR позвоночных была предложена альтернативная система классификации под названием GRAFS ( глутамат , родопсин , адгезия , вьющиеся / вкус2 , секретин ). [10] Они соответствуют классическим классам C, A, B2, F и B. [17]
Раннее исследование, основанное на доступных последовательностях ДНК, показало, что геном человека кодирует примерно 750 рецепторов, связанных с G-белком, [18] около 350 из которых обнаруживают гормоны, факторы роста и другие эндогенные лиганды. Примерно 150 GPCR, обнаруженных в геноме человека, имеют неизвестные функции.
Некоторые веб-серверы [19] и методы биоинформатического прогнозирования [20] [21] использовались для прогнозирования классификации GPCR только по их аминокислотной последовательности с помощью подхода псевдоаминокислотного состава .
GPCR участвуют в широком спектре физиологических процессов. Некоторые примеры их физиологической роли включают в себя:
GPCRs представляют собой интегральные мембранные белки , которые обладают семью трансмембранными доменами или трансмембранными спиралями . [26] [27] Внеклеточные части рецептора могут быть гликозилированы . Эти внеклеточные петли также содержат два высококонсервативных остатка цистеина , которые образуют дисульфидные связи для стабилизации структуры рецептора. Некоторые семитрансмембранные белки-спирали ( канальный родопсин ), напоминающие GPCR, могут содержать ионные каналы внутри своего белка.
В 2000 году была раскрыта первая кристаллическая структура GPCR млекопитающих — бычьего родопсина ( 1F88 ). [28] В 2007 году была раскрыта первая структура человеческого GPCR. [29] [1] [30] Эта структура человеческого β 2 -адренергического рецептора GPCR оказалась очень похожей на бычий родопсин. Также были определены структуры активированных или связанных с агонистами GPCR. [31] [32] [33] [34] Эти структуры показывают, как связывание лиганда на внеклеточной стороне рецептора приводит к конформационным изменениям на цитоплазматической стороне рецептора. Самым большим изменением является перемещение наружу цитоплазматической части 5-й и 6-й трансмембранных спиралей (TM5 и TM6). Структура активированного бета-2-адренергического рецептора в комплексе с G подтверждает , что Gα связывается с полостью, созданной этим движением. [35]
GPCR имеют структуру, аналогичную некоторым другим белкам с семью трансмембранными доменами , таким как микробные родопсины и рецепторы адипонектина 1 и 2 ( ADIPOR1 и ADIPOR2 ). Однако эти рецепторы и каналы 7TMH (7-трансмембранные спирали) не связываются с G-белками . Кроме того, ADIPOR1 и ADIPOR2 ориентированы в мембране противоположно GPCR (т.е. GPCR обычно имеют внеклеточный N-конец , цитоплазматический C-конец , тогда как ADIPOR инвертированы). [36]
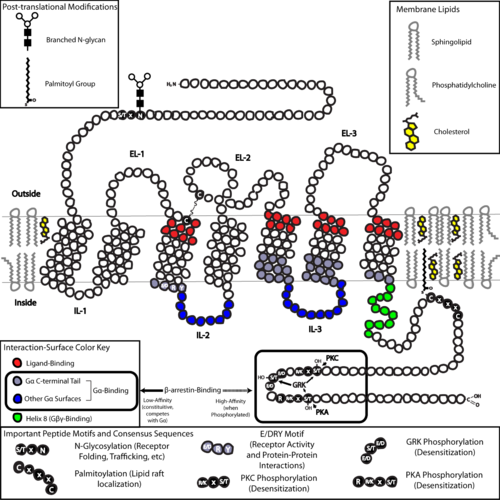
С точки зрения структуры GPCR характеризуются внеклеточным N-концом , за которым следуют семь трансмембранных (7-TM) α-спиралей (TM-1–TM-7), соединенных тремя внутриклеточными (IL-1–IL-3) и три внеклеточные петли (от EL-1 до EL-3) и, наконец, внутриклеточный С-конец . GPCR образует третичную структуру, напоминающую бочонок, с семью трансмембранными спиралями, образующими полость внутри плазматической мембраны, которая обслуживает лиганд -связывающий домен, который часто покрыт EL-2. Однако лиганды могут связываться и в других местах, как в случае с более объемными лигандами (например, белками или большими пептидами ), которые вместо этого взаимодействуют с внеклеточными петлями или, как показано на примере метаботропных глутаматных рецепторов класса C (mGluR), N- конечный хвост. GPCR класса C отличаются большим N-концевым хвостом, который также содержит лиганд-связывающий домен. При связывании глутамата с mGluR N-концевой хвост претерпевает конформационное изменение, которое приводит к его взаимодействию с остатками внеклеточных петель и ТМ-доменами. Конечным эффектом всех трех типов активации, индуцированной агонистом , является изменение относительной ориентации спиралей ТМ (по аналогии с скручивающим движением), приводящее к более широкой внутриклеточной поверхности и «обнаружению» остатков внутриклеточных спиралей и доменов ТМ, имеющих решающее значение. для функции передачи сигнала (т.е. связывания G-белка). Обратные агонисты и антагонисты также могут связываться с рядом различных сайтов, но конечным эффектом должно быть предотвращение этой переориентации спирали ТМ. [3]
Структура N- и C-концевых хвостов GPCR может также выполнять важные функции, помимо связывания лигандов. Например, С-конца мускариновых рецепторов М 3 достаточно, а многоосновный домен из шести аминокислот (KKKRRK) на С-конце необходим для его предварительной сборки с белками Gq . [37] В частности, С-конец часто содержит остатки серина (Ser) или треонина (Thr), которые при фосфорилировании увеличивают сродство внутриклеточной поверхности к связыванию каркасных белков, называемых β- аррестинами (β-arr). [38] После связывания β-аррестины как стерически предотвращают связывание G-белков, так и могут рекрутировать другие белки, что приводит к созданию сигнальных комплексов, участвующих в активации пути киназы, регулируемой внеклеточными сигналами ( ERK ), или эндоцитозе (интернализации) рецепторов. Поскольку фосфорилирование этих остатков Ser и Thr часто происходит в результате активации GPCR, β-arr-опосредованное развязывание G-белка и интернализация GPCRs являются важными механизмами десенсибилизации . [39] Кроме того, существуют интернализованные «мега-комплексы», состоящие из одного GPCR, β-arr (в конформации хвоста), [40] [41] и гетеротримерного G-белка, которые могут отвечать за передачу сигналов белка из эндосом. [42] [43]
Последней общей структурной темой среди GPCRs является пальмитоилирование одного или нескольких участков C-концевого хвоста или внутриклеточных петель. Пальмитоилирование представляет собой ковалентную модификацию остатков цистеина (Cys) посредством добавления гидрофобных ацильных групп и имеет эффект нацеливания рецептора на богатые холестерином и сфинголипидами микродомены плазматической мембраны, называемые липидными рафтами . Поскольку многие из нижестоящих молекул-преобразователей и эффекторов GPCR (включая те, которые участвуют в путях отрицательной обратной связи ) также нацелены на липидные рафты, это способствует быстрой передаче сигналов рецептором.
GPCR реагируют на внеклеточные сигналы, опосредованные огромным разнообразием агонистов, от белков до биогенных аминов и протонов , но все они передают этот сигнал посредством механизма связывания G-белка. Это становится возможным благодаря домену фактора обмена гуанин -нуклеотидов ( GEF ), в первую очередь образованному комбинацией IL-2 и IL-3 вместе с соседними остатками связанных спиралей TM.

Рецептор, связанный с G-белком, активируется внешним сигналом в виде лиганда или другого сигнального медиатора. Это создает конформационные изменения в рецепторе, вызывая активацию G-белка . Дальнейший эффект зависит от типа G-белка. Белки G впоследствии инактивируются белками, активирующими ГТФазу, известными как белки RGS .
GPCR включают один или несколько рецепторов для следующих лигандов: медиаторов сенсорных сигналов (например, молекул, стимулирующих свет и обоняние ); аденозин , бомбезин , брадикинин , эндотелин , γ-аминомасляная кислота ( ГАМК ), фактор роста гепатоцитов ( HGF ), меланокортины , нейропептид Y , опиоидные пептиды, опсины , соматостатин , GH , тахикинины , члены семейства вазоактивных кишечных пептидов и вазопрессин ; биогенные амины (например, дофамин , адреналин , норадреналин , гистамин , серотонин и мелатонин ); глутамат ( метаботропный эффект); глюкагон ; ацетилхолин ( мускариновый эффект); хемокины ; липидные медиаторы воспаления (например, простагландины , простаноиды , фактор активации тромбоцитов и лейкотриены ); пептидные гормоны (например, кальцитонин , анафилатоксин C5a , фолликулостимулирующий гормон [FSH], гонадотропин-высвобождающий гормон [GnRH], нейрокинин , тиреотропин-высвобождающий гормон [TRH] и окситоцин ); и эндоканнабиноиды .
GPCR, которые действуют как рецепторы для стимулов, которые еще не идентифицированы, известны как сиротские рецепторы .
Однако в отличие от других типов рецепторов, которые были изучены, лиганды которых связываются с мембраной снаружи, лиганды GPCR обычно связываются внутри трансмембранного домена. Однако рецепторы, активируемые протеазой, активируются путем отщепления части их внеклеточного домена. [45]

Трансдукция сигнала рецептором через мембрану до конца не изучена. Известно, что в неактивном состоянии GPCR связан с гетеротримерным комплексом G-белка . Связывание агониста с GPCR приводит к конформационному изменению рецептора, которое передается связанной субъединице Gα гетеротримерного G-белка посредством динамики белкового домена . Активированная субъединица Gα обменивает GTP вместо GDP , что, в свою очередь, запускает диссоциацию субъединицы Gα от димера Gβγ и от рецептора. Диссоциированные субъединицы Gα и Gβγ взаимодействуют с другими внутриклеточными белками, продолжая каскад передачи сигнала, в то время как освобожденный GPCR способен повторно связываться с другим гетеротримерным G-белком с образованием нового комплекса, который готов инициировать новый раунд передачи сигнала. [46]
Считается, что молекула рецептора существует в конформационном равновесии между активным и неактивным биофизическими состояниями. [47] Связывание лигандов с рецептором может сместить равновесие в сторону активных состояний рецептора. Существуют три типа лигандов: агонисты — это лиганды, смещающие равновесие в пользу активных состояний; обратные агонисты — лиганды, смещающие равновесие в пользу неактивных состояний; а нейтральные антагонисты представляют собой лиганды, не влияющие на равновесие. Пока неизвестно, чем именно отличаются активное и неактивное состояния друг от друга.

Когда рецептор неактивен, домен GEF может быть связан с также неактивной α-субъединицей гетеротримерного G-белка . Эти «G-белки» представляют собой тример субъединиц α, β и γ (известных как Gα, Gβ и Gγ соответственно), который становится неактивным при обратимом связывании с гуанозиндифосфатом (GDP) (или, альтернативно, без гуанинового нуклеотида). ), но активен при связывании с гуанозинтрифосфатом (ГТФ). При активации рецептора домен GEF, в свою очередь, аллостерически активирует G-белок, способствуя обмену молекулы GDP на GTP в α-субъединице G-белка. В клетке поддерживается соотношение цитозольного ГТФ:ГДП 10:1, поэтому обеспечивается обмен на ГТФ. В этот момент субъединицы G-белка диссоциируют от рецептора, а также друг от друга, образуя мономер Gα-GTP и тесно взаимодействующий димер Gβγ , которые теперь могут модулировать активность других внутриклеточных белков. Однако степень их диффузии ограничена из-за пальмитоилирования Gα и присутствия изопреноидного фрагмента, ковалентно добавленного к C-концам Gγ.
Поскольку Gα также обладает способностью к медленному гидролизу GTP→GDP , неактивная форма α-субъединицы (Gα-GDP) в конечном итоге регенерируется, что позволяет повторно ассоциироваться с димером Gβγ с образованием «покоящегося» G-белка, который может снова связываться с GPCR и дождитесь активации. Скорость гидролиза ГТФ часто ускоряется из-за действия другого семейства аллостерических модулирующих белков, называемых регуляторами передачи сигналов G-белка , или белков RGS, которые представляют собой тип белка, активирующего ГТФазу , или GAP. Фактически, многие из первичных эффекторных белков (например, аденилатциклазы ), которые активируются/инактивируются при взаимодействии с Gα-GTP, также обладают активностью GAP. Таким образом, даже на этой ранней стадии процесса передача сигналов, инициируемая GPCR, обладает способностью к самозавершению.
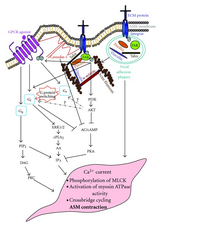
Было показано, что нижестоящие сигналы GPCRs, возможно, взаимодействуют с сигналами интегринов , такими как FAK . [48] Передача сигналов интегрина будет фосфорилировать FAK, что затем может снизить активность GPCR Gαs .

Если рецептор в активном состоянии встречает G-белок , он может активировать его. Некоторые данные свидетельствуют о том, что рецепторы и G-белки на самом деле предварительно связаны. [37] Например, связывание G-белков с рецепторами влияет на сродство рецептора к лигандам. Активированные G-белки связаны с GTP .
Дальнейшая передача сигнала зависит от типа G-белка. Фермент аденилатциклаза является примером клеточного белка, который может регулироваться G-белком, в данном случае G-белком G s . Активность аденилатциклазы активируется, когда она связывается с субъединицей активированного G-белка. Активация аденилатциклазы заканчивается, когда G-белок возвращается в GDP -связанное состояние.
Аденилатциклазы (из которых у человека известны 9 мембраносвязанных и одна цитозольная формы) также могут быть активированы или ингибированы другими способами (например, связыванием Ca2+/ кальмодулина ), что может модифицировать активность этих ферментов аддитивным или синергическим образом. вместе с G-белками.
Сигнальные пути, активируемые посредством GPCR, ограничены первичной последовательностью и третичной структурой самого GPCR, но в конечном итоге определяются конкретной конформацией , стабилизированной конкретным лигандом , а также доступностью молекул -преобразователей . В настоящее время считается, что GPCR используют два основных типа преобразователей: G-белки и β-аррестины . Поскольку β-arr имеют высокое сродство только к фосфорилированной форме большинства GPCR (см. выше или ниже), большая часть передачи сигналов в конечном итоге зависит от активации G-белка. Однако возможность взаимодействия действительно позволяет осуществлять независимую от G-белка передачу сигналов.
Существует три основных сигнальных пути, опосредованных G-белками, опосредованных четырьмя подклассами G-белков, отличающихся друг от друга гомологией последовательностей ( Gαs , Gαi /o , Gαq /11 и Gα12 /13 ) . Каждый подкласс G-белка состоит из множества белков, каждый из которых является продуктом множества генов или вариаций сплайсинга , которые могут придавать им различия в диапазоне от едва заметных до различных в отношении сигнальных свойств, но в целом они кажутся разумно сгруппированными в четыре класса. Поскольку свойства передачи сигналов различных возможных комбинаций βγ, по-видимому, радикально не отличаются друг от друга, эти классы определяются в соответствии с изоформой их α-субъединицы. [6] : 1163
Хотя большинство GPCR способны активировать более одного Gα-подтипа, они также отдают предпочтение одному подтипу над другим. Когда активированный подтип зависит от лиганда, который связан с GPCR, это называется функциональной селективностью (также известной как агонист-направленный транспорт или конформационно-специфичный агонизм). Однако связывание любого отдельного агониста может также инициировать активацию множества различных G-белков, поскольку он может быть способен стабилизировать более чем одну конформацию домена GEF GPCR даже в ходе одного взаимодействия. Кроме того, конформация, которая предпочтительно активирует одну изоформу Gα, может активировать другую, если предпочтительная менее доступна. Более того, пути обратной связи могут приводить к модификациям рецепторов (например, фосфорилированию), которые изменяют предпочтение G-белка. Независимо от этих различных нюансов, предпочтительный партнер для связывания GPCR обычно определяется по G-белку, который наиболее явно активируется эндогенным лигандом в большинстве физиологических или экспериментальных условий.
Приведенные выше описания игнорируют эффекты передачи сигналов Gβγ , которые также могут быть важны, в частности, в случае активированных Gαi /o -связанных GPCR. Первичными эффекторами Gβγ являются различные ионные каналы, такие как регулируемые G-белком внутренне выпрямляющие K + -каналы (GIRK), потенциалзависимые Ca 2+ -каналы P / Q- и N-типа , а также некоторые изоформы AC и PLC вместе с некоторыми изоформами фосфоинозитид-3-киназы (PI3K).
Хотя классически считается, что они работают только вместе, GPCRs могут передавать сигналы посредством независимых от G-белков механизмов, а гетеротримерные G-белки могут играть функциональные роли, независимые от GPCR. GPCRs могут передавать сигналы независимо через многие белки, уже упомянутые в связи с их ролью в G-белкозависимой передаче сигналов, такие как β-arrs , GRKs и Srcs . Было показано, что такая передача сигналов физиологически значима, например, передача сигналов β-аррестина, опосредованная хемокиновым рецептором CXCR3 , была необходима для полной эффективности хемотаксиса активированных Т-клеток. [49] Кроме того, дополнительные каркасные белки, участвующие в субклеточной локализации GPCR (например, белки, содержащие PDZ-домен ), также могут действовать как преобразователи сигнала. Чаще всего эффектор является членом семейства МАПК .
В конце 1990-х годов начали накапливаться данные, позволяющие предположить, что некоторые GPCR способны передавать сигналы без G-белков. Было показано, что митоген -активируемая протеинкиназа ERK2 , ключевой медиатор передачи сигнала после активации рецептора во многих путях, активируется в ответ на опосредованную цАМФ активацию рецептора у слизевика D. discoideum , несмотря на отсутствие связанного с ним G-белка. α- и β-субъединицы. [50]
В клетках млекопитающих было продемонстрировано, что хорошо изученный β 2 -адренорецептор активирует путь ERK2 после опосредованного арестином разобщения передачи сигналов, опосредованной G-белком. Таким образом, вполне вероятно, что некоторые механизмы, которые ранее считались связанными исключительно с десенсибилизацией рецепторов, на самом деле являются примерами переключения рецепторов на свои сигнальные пути, а не просто их выключения.
Было показано , что в клетках почек рецептор брадикинина B2 напрямую взаимодействует с протеинтирозинфосфатазой. Присутствие тирозин-фосфорилированной последовательности ITIM (иммунорецепторный тирозиновый ингибирующий мотив) в рецепторе B2 необходимо для обеспечения этого взаимодействия и, как следствие, антипролиферативного эффекта брадикинина. [51]
Хотя это относительно незрелая область исследований, похоже, что гетеротримерные G-белки также могут принимать участие в передаче сигналов, не связанных с GPCR. Имеются доказательства роли преобразователей сигнала почти во всех других типах рецептор-опосредованной передачи сигналов, включая интегрины , рецепторные тирозинкиназы (RTK), цитокиновые рецепторы ( JAK/STAT ), а также модуляцию различных других «дополнительных» белков, таких как GEF , ингибиторы диссоциации гуанин-нуклеотидов (GDI) и протеинфосфатазы . Могут даже существовать специфические белки этих классов, основная функция которых является частью GPCR-независимых путей, называемых активаторами передачи сигналов G-белка (AGS). Как повсеместное распространение этих взаимодействий, так и важность субъединиц Gα и Gβγ для этих процессов до сих пор неясны.



Существует два основных пути передачи сигнала с участием рецепторов, связанных с G-белком : сигнальный путь цАМФ и сигнальный путь фосфатидилинозитола . [5]
Передача сигнала цАМФ содержит пять основных символов: рецептор стимулирующего гормона (Rs) или рецептор тормозного гормона (Ri); стимулирующий регулятивный G-белок (Gs) или ингибирующий регулятивный G-белок (Gi); аденилатциклаза ; протеинкиназа А (PKA); и цАМФ -фосфодиэстераза .
Рецептор стимулирующего гормона (Rs) представляет собой рецептор, который может связываться со стимулирующими сигнальными молекулами, тогда как рецептор ингибирующего гормона (Ri) представляет собой рецептор, который может связываться с ингибирующими сигнальными молекулами.
Стимулирующий регулятивный G-белок представляет собой G-белок, связанный с рецептором стимулирующего гормона (Rs), и его α-субъединица при активации может стимулировать активность фермента или другой внутриклеточный метаболизм. Напротив, ингибирующий регулятивный G-белок связан с рецептором ингибирующего гормона, и его α-субъединица при активации может ингибировать активность фермента или другой внутриклеточный метаболизм.
Аденилатциклаза представляет собой 12-трансмембранный гликопротеин, катализирующий превращение АТФ в цАМФ с помощью кофактора Mg 2+ или Mn 2+ . Продуцируемый цАМФ является вторичным мессенджером клеточного метаболизма и аллостерическим активатором протеинкиназы А.
Протеинкиназа А является важным ферментом клеточного метаболизма благодаря своей способности регулировать клеточный метаболизм путем фосфорилирования специфических детерминированных ферментов метаболического пути. Он также может регулировать экспрессию специфических генов, клеточную секрецию и проницаемость мембран. Белок-фермент содержит две каталитические субъединицы и две регуляторные субъединицы. При отсутствии цАМФ комплекс неактивен. Когда цАМФ связывается с регуляторными субъединицами, их конформация изменяется, вызывая диссоциацию регуляторных субъединиц, что активирует протеинкиназу А и обеспечивает дальнейшие биологические эффекты.
Эти сигналы затем могут быть прекращены фосфодиэстеразой цАМФ, которая представляет собой фермент, который расщепляет цАМФ до 5'-АМФ и инактивирует протеинкиназу А.
В сигнальном пути фосфатидилинозита внеклеточная сигнальная молекула связывается с рецептором G-белка (Gq ) на поверхности клетки и активирует фосфолипазу C , которая расположена на плазматической мембране . Липаза гидролизует фосфатидилинозитол-4,5-бисфосфат (PIP2) на два вторичных мессенджера: инозитол-1,4,5-трифосфат (IP3) и диацилглицерин ( DAG). IP3 связывается с рецептором IP3 в мембране гладкой эндоплазматической сети и митохондриях, открывая Ca 2+ каналы. DAG помогает активировать протеинкиназу C (PKC), которая фосфорилирует многие другие белки, изменяя их каталитическую активность, что приводит к клеточным реакциям.
Эффекты Ca 2+ также примечательны: он сотрудничает с DAG при активации PKC и может активировать путь киназы CaM , при котором модулированный кальцием белок кальмодулин (CaM) связывает Ca 2+ , претерпевает изменение конформации и активирует киназу CaM. II, который обладает уникальной способностью увеличивать сродство связывания с СаМ путем аутофосфорилирования, что делает СаМ недоступным для активации других ферментов. Затем киназа фосфорилирует целевые ферменты, регулируя их активность. Два сигнальных пути соединены вместе Ca 2+ -CaM, который также является регуляторной субъединицей аденилатциклазы и фосфодиэстеразы в сигнальном пути цАМФ.
GPCR теряют чувствительность при воздействии их лиганда в течение длительного периода времени. Существуют две признанные формы десенсибилизации: 1) гомологичная десенсибилизация , при которой активированный GPCR подавляется; и 2) гетерологичная десенсибилизация , при которой активированный GPCR вызывает подавление другого GPCR. Ключевой реакцией этого подавления является фосфорилирование внутриклеточного (или цитоплазматического ) домена рецептора протеинкиназами .
Циклические АМФ-зависимые протеинкиназы ( протеинкиназа А ) активируются сигнальной цепью, исходящей от белка G (который был активирован рецептором) через аденилатциклазу и циклический АМФ (цАМФ). По механизму обратной связи эти активированные киназы фосфорилируют рецептор. Чем дольше рецептор остается активным, тем больше киназ активируется и тем больше рецепторов фосфорилируется. В β 2 -адренорецепторах это фосфорилирование приводит к переключению связи с класса G s G-белка на класс Gi . [52] цАМФ-зависимое фосфорилирование, опосредованное ПКА, может вызывать гетерологичную десенсибилизацию рецепторов, отличных от активированных. [53]
Киназы рецепторов, связанных с G-белком (GRK), представляют собой протеинкиназы, которые фосфорилируют только активные GPCR. [54] Киназы рецепторов, связанных с G-белками (GRK), являются ключевыми модуляторами передачи сигналов рецепторов, связанных с G-белками (GPCR). Они составляют семейство из семи серин-треониновых протеинкиназ млекопитающих, которые фосфорилируют рецептор, связанный с агонистом. GRK-опосредованное фосфорилирование рецепторов быстро инициирует глубокое нарушение передачи сигналов рецептора и десенсибилизацию. Активность GRK и субклеточное нацеливание жестко регулируется взаимодействием с рецепторными доменами, субъединицами G-белка, липидами, якорными белками и чувствительными к кальцию белками. [55]
Фосфорилирование рецептора может иметь два последствия:
Как упоминалось выше, G-белки могут прекращать собственную активацию из-за присущей им способности гидролиза GTP → GDP . Однако эта реакция протекает с медленной скоростью (≈0,02 раза в секунду), и, таким образом, деактивация любого отдельного G-белка заняла бы около 50 секунд, если бы в игру не вступили другие факторы. Действительно, существует около 30 изоформ белков RGS , которые при связывании с Gα через свой домен GAP ускоряют скорость гидролиза до ≈30 раз/сек. Это 1500-кратное увеличение скорости позволяет клетке реагировать на внешние сигналы с высокой скоростью, а также с пространственным разрешением из-за ограниченного количества вторичного мессенджера , который может быть сгенерирован, и ограниченного расстояния, на которое G-белок может диффундировать за 0,03 секунды. По большей части белки RGS различаются по своей способности деактивировать G-белки, тогда как участие RGS в конкретном сигнальном пути, по-видимому, в большей степени определяется тканью и вовлеченными GPCR, чем чем-либо еще. Кроме того, белки RGS обладают дополнительной функцией увеличения скорости обмена GTP-GDP в GPCR (т.е. в качестве своего рода co-GEF), что дополнительно способствует временному разрешению передачи сигналов GPCR.
Кроме того, GPCR сам может быть десенсибилизирован . Это может произойти как:
Как только β-аррестин связывается с GPCR, он претерпевает конформационные изменения, позволяющие ему служить каркасным белком для адаптерного комплекса, называемого AP-2 , который, в свою очередь, рекрутирует другой белок, называемый клатрином . Если достаточное количество рецепторов в локальной области рекрутируют клатрин таким образом, они агрегируются, и мембрана отпочковывается внутрь в результате взаимодействия между молекулами клатрина в процессе, называемом опсонизацией . После того, как ямка оторвалась от плазматической мембраны под действием двух других белков, называемых амфифизином и динамином , она теперь представляет собой эндоцитарную везикулу . В этот момент молекулы-адаптеры и клатрин диссоциируют , и рецептор либо возвращается к плазматической мембране, либо направляется в лизосомы для деградации .
В любой момент этого процесса β-аррестины могут также рекрутировать другие белки, такие как нерецепторная тирозинкиназа (nRTK), c-SRC , которые могут активировать ERK1/2 или другую митоген-активируемую протеинкиназу (MAPK). передача сигнала, например, посредством фосфорилирования малой ГТФазы Ras или непосредственного рекрутирования белков каскада ERK (т. е. Raf-1 , MEK , ERK-1/2), в этот момент инициируется передача сигнала из-за их непосредственной близости к друг друга. Другой мишенью c-SRC являются молекулы динамина, участвующие в эндоцитозе. Динамины полимеризуются на шейке входящей везикулы, и их фосфорилирование с помощью c-SRC обеспечивает энергию, необходимую для конформационного изменения, позволяющего окончательно «отщепиться» от мембраны.
Десенсибилизация рецептора опосредуется посредством комбинированного фосфорилирования, связывания β-arr и эндоцитоза, как описано выше. Понижение регуляции происходит, когда эндоцитированный рецептор внедряется в эндосому, которая перемещается для слияния с органеллой, называемой лизосомой. Поскольку лизосомальные мембраны богаты протонными насосами, их внутренняя часть имеет низкий pH (≈4,8 по сравнению с pH≈7,2 цитозоля), что приводит к денатурации GPCR. Кроме того, лизосомы содержат множество деградирующих ферментов , включая протеазы, которые могут функционировать только при таком низком pH, поэтому пептидные связи, соединяющие остатки GPCR, могут расщепляться. Доставляется ли данный рецептор в лизосому, задерживается в эндосомах или возвращается обратно на плазматическую мембрану, зависит от множества факторов, включая тип рецептора и величину сигнала. Регуляция GPCR дополнительно опосредуется факторами транскрипции генов. Эти факторы могут увеличивать или уменьшать транскрипцию генов и, таким образом, увеличивать или уменьшать выработку новых рецепторов (повышающая или понижающая регуляция), которые перемещаются к клеточной мембране.
Олигомеризация рецепторов, связанных с G-белком, является широко распространенным явлением. Одним из наиболее изученных примеров является метаботропный рецептор ГАМК В. Этот так называемый конститутивный рецептор образуется путем гетеродимеризации субъединиц GABA BR1 и GABA BR2 . Экспрессия GABA BR1 без GABA BR2 в гетерологичных системах приводит к сохранению субъединицы в эндоплазматическом ретикулуме . Экспрессия только субъединицы GABA B R2, тем временем, приводит к поверхностной экспрессии субъединицы, хотя и без функциональной активности (т.е. рецептор не связывает агонист и не может инициировать ответ после воздействия агониста). Совместная экспрессия двух субъединиц приводит к экспрессии функционального рецептора на плазматической мембране. Показано, что связывание GABA BR2 с GABA BR1 приводит к маскировке сигнала удержания [60] функциональных рецепторов. [61]
Передача сигнала , опосредованная суперсемейством GPCRs, восходит к зарождению многоклеточности . GPCR, подобные млекопитающим, обнаружены в грибах и классифицированы в соответствии с системой классификации GRAFS , основанной на отпечатках пальцев GPCR. [17] Идентификация членов суперсемейства в эукариотическом домене и сравнение специфичных для семейства мотивов показали, что суперсемейство GPCRs имеет общее происхождение. [62] Характерные мотивы указывают на то, что три из пяти семейств GRAFS, Rhodopsin , Adhesion и Frizzled , произошли от цАМФ-рецепторов Dictyostelium discoideum до разделения опистоконтов . Позже семейство секретинов эволюционировало из семейства рецепторов адгезии GPCR еще до разделения нематод . [17] GPCR насекомых, по-видимому, находятся в отдельной группе, а Taste2 идентифицируется как происходящий от Rhodopsin . [62] Обратите внимание, что разделение секретин / адгезия основано на предполагаемой функции, а не на сигнатуре, поскольку классический класс B (7tm_2, Pfam PF00002) используется для идентификации обоих в исследованиях.
Справочник молекулярных и математических моделей первоначального ответа рецептора.
Данные, диаграммы и веб-инструменты для рецепторов, связанных с G-белком (GPCR).; Мунк С., Исберг В., Мордалски С., Харпсё К., Ратаж К., Хаузер А.С. и др. (июль 2016 г.). «GPCRdb: база данных рецепторов, связанных с G-белком - введение». Британский журнал фармакологии . 173 (14): 2195–207. дои : 10.1111/bph.13509. ПМЦ 4919580 . ПМИД 27155948.
классификация GPCR
Инициатива по структуре белка: Сетевой центр биологии, направленный на определение трехмерных структур репрезентативных белков семейства GPCR.