
Митохондрия ( / ˌ m aɪ t ə ˈ k ɒ n d r i ə n / ; [ 1] мн.: митохондрии ) — органелла, обнаруженная в клетках большинства эукариот , таких как животные , растения и грибы . Митохондрии имеют двойную мембранную структуру и используют аэробное дыхание для выработки аденозинтрифосфата (АТФ), который используется в клетке в качестве источника химической энергии . [2] Они были обнаружены Альбертом фон Кёлликером в 1857 году [3] в произвольных мышцах насекомых. Термин «митохондрия» был придуман Карлом Бендой в 1898 году. Митохондрия в народе получила прозвище «электростанция клетки» — фраза, придуманная Филипом Зикевицем в одноименной статье 1957 года. [4]
В некоторых клетках некоторых многоклеточных организмов митохондрии отсутствуют (например, зрелые эритроциты млекопитающих ). Большое количество одноклеточных организмов , таких как микроспоридии , парабазалиды и дипломонады , сократили или трансформировали свои митохондрии в другие структуры . [5] Известно, что эукариоты Monocercomonoides полностью потеряли свои митохондрии, [6] а многоклеточный организм Henneguya salminicola, как известно, сохранил органеллы, связанные с митохондриями, в сочетании с полной потерей своего митохондриального генома. [6] [7] [8]
Митохондрии обычно имеют поперечное сечение от 0,75 до 3 мкм 2 [9] , но значительно различаются по размеру и структуре. Если специально не окрашивать , их не видно. Помимо обеспечения клеточной энергии, митохондрии участвуют в других задачах, таких как передача сигналов , клеточная дифференцировка и гибель клеток , а также поддержание контроля над клеточным циклом и ростом клеток . [10] Митохондриальный биогенез , в свою очередь, во времени координируется с этими клеточными процессами. [11] [12] Митохондрии вовлечены в ряд заболеваний и состояний человека, таких как митохондриальные заболевания , [13] сердечная дисфункция , [14] сердечная недостаточность [15] и аутизм . [16]
Количество митохондрий в клетке может широко варьироваться в зависимости от организма , ткани и типа клеток. Зрелый эритроцит не имеет митохондрий, [17] , тогда как клетка печени может иметь более 2000. [18] [19] Митохондрия состоит из отсеков, которые выполняют специализированные функции. Эти отсеки или области включают внешнюю мембрану, межмембранное пространство , внутреннюю мембрану , кристы и матрикс .
Хотя большая часть ДНК эукариотической клетки содержится в клеточном ядре , митохондрия имеет собственный геном («митогеном»), который существенно похож на бактериальные геномы. [20] Это открытие привело к всеобщему признанию эндосимбиотической гипотезы о том, что свободноживущие прокариотические предки современных митохондрий навсегда слились с эукариотическими клетками в далеком прошлом, эволюционируя таким образом, что современные животные, растения, грибы и другие эукариоты способны дышать , чтобы генерировать клеточную энергию . [21]
Митохондрии могут иметь разную форму. [22] Митохондрия содержит внешнюю и внутреннюю мембраны, состоящие из бислоев фосфолипидов и белков . [18] Две мембраны имеют разные свойства. Из-за этой двухмембранной организации митохондрия состоит из пяти отдельных частей:
Митохондрии имеют складчатость, увеличивающую площадь поверхности, что, в свою очередь, увеличивает выработку АТФ (аденозинтрифосфата). Митохондрии, лишенные внешней мембраны, называются митопластами .
Внешняя митохондриальная мембрана , окружающая всю органеллу, имеет толщину от 60 до 75 ангстрем (Å). Соотношение белков и фосфолипидов в нем аналогично соотношению клеточной мембраны (около 1:1 по массе). Он содержит большое количество интегральных мембранных белков, называемых поринами . Основным транспортным белком является порообразующий потенциал-зависимый анионный канал (VDAC). VDAC является основным переносчиком нуклеотидов , ионов и метаболитов между цитозолем и межмембранным пространством . [23] [24] Он имеет форму бета-цилиндра , охватывающего внешнюю мембрану, аналогично мембране грамотрицательных бактерий . [25] Более крупные белки могут проникать в митохондрии, если сигнальная последовательность на их N-конце связывается с большим мультисубъединичным белком , называемым транслоказой, на внешней мембране , который затем активно перемещает их через мембрану. [26] Митохондриальные пробелки импортируются через специализированные транслокационные комплексы.
Наружная мембрана также содержит ферменты , участвующие в таких разнообразных процессах , как элонгация жирных кислот , окисление адреналина и деградация триптофана . Эти ферменты включают моноаминоксидазу , нечувствительную к ротенону НАДН- цитохром -с-редуктазу, кинуренингидроксилазу и Ко-А- лигазу жирных кислот . Разрушение внешней мембраны позволяет белкам из межмембранного пространства проникать в цитозоль, что приводит к гибели клеток. [27] Внешняя митохондриальная мембрана может соединяться с мембраной эндоплазматического ретикулума (ЭР) в структуре, называемой МАМ (митохондриально-ассоциированная ЭР-мембрана). Это важно для передачи сигналов кальция в ЭР-митохондрии и участвует в переносе липидов между ЭР и митохондриями. [28] За пределами внешней мембраны находятся небольшие (диаметр: 60 Å) частицы, называемые субъединицами Парсона.
Межмембранное пространство митохондрий — это пространство между внешней и внутренней мембранами. Его также называют перимитохондриальным пространством. Поскольку внешняя мембрана свободно проницаема для малых молекул, концентрации малых молекул, таких как ионы и сахара, в межмембранном пространстве такие же, как и в цитозоле . [18] Однако крупные белки должны иметь специфическую сигнальную последовательность для транспортировки через внешнюю мембрану, поэтому белковый состав этого пространства отличается от белкового состава цитозоля . Одним из белков , локализующихся таким образом в межмембранном пространстве, является цитохром с . [27]
Внутренняя мембрана митохондрий содержит белки с тремя типами функций: [18]
Он содержит более 151 различных полипептидов и имеет очень высокое соотношение белка к фосфолипидам (более 3:1 по массе, что составляет примерно 1 белок на 15 фосфолипидов). Внутренняя мембрана содержит около 1/5 всего белка митохондрии. [29] Кроме того, внутренняя мембрана богата необычным фосфолипидом кардиолипином . Этот фосфолипид был первоначально обнаружен в коровьем сердце в 1942 году и обычно характерен для митохондриальных и бактериальных плазматических мембран. [30] Кардиолипин содержит четыре жирные кислоты, а не две, и может помочь сделать внутреннюю мембрану непроницаемой, [18] и ее разрушение может привести к множеству клинических расстройств, включая неврологические расстройства и рак. [31] В отличие от внешней мембраны, внутренняя мембрана не содержит поринов и очень непроницаема для всех молекул. Почти всем ионам и молекулам требуются специальные мембранные транспортеры для входа или выхода из матрикса. Белки переправляются в матрикс через транслоказу комплекса внутренней мембраны (TIM) или через OXA1L . [26] Кроме того, на внутренней мембране существует мембранный потенциал, образованный действием ферментов цепи переноса электронов . Слияние внутренней мембраны опосредуется белком внутренней мембраны OPA1 . [32]

Внутренняя митохондриальная мембрана разделена на многочисленные складки, называемые кристами , которые увеличивают площадь поверхности внутренней митохондриальной мембраны, повышая ее способность вырабатывать АТФ. Для типичных митохондрий печени площадь внутренней мембраны примерно в пять раз больше площади наружной мембраны. Это соотношение является переменным, и митохондрии клеток, которым требуется больше АТФ, например мышечных клеток, содержат еще больше крист. Митохондрии внутри одной и той же клетки могут иметь существенно разную плотность крист, причем те, которые необходимы для производства большего количества энергии, имеют гораздо большую поверхность крист-мембраны. [33] Эти складки усеяны маленькими круглыми телами, известными как частицы F 1 или оксисомы. [34]
Матрица – это пространство, окруженное внутренней мембраной. Он содержит около 2/3 всех белков митохондрии. [18] Матрица важна для производства АТФ с помощью АТФ-синтазы, содержащейся во внутренней мембране. Матрица содержит высококонцентрированную смесь сотен ферментов, особых митохондриальных рибосом , тРНК и нескольких копий генома митохондриальной ДНК . Из ферментов основные функции включают окисление пирувата и жирных кислот , а также цикл лимонной кислоты . [18] Молекулы ДНК упаковываются в нуклеоиды белками, одним из которых является TFAM . [35]
Наиболее важные роли митохондрий заключаются в производстве энергетической валюты клетки, АТФ (т.е. фосфорилировании АДФ ), посредством дыхания и регуляции клеточного метаболизма . [19] Центральный набор реакций, участвующих в производстве АТФ, известен под общим названием цикл лимонной кислоты или цикл Кребса и окислительное фосфорилирование . Однако помимо производства АТФ у митохондрии есть много других функций.
Доминирующей ролью митохондрий является производство АТФ, о чем свидетельствует большое количество белков во внутренней мембране, выполняющих эту задачу. Это осуществляется путем окисления основных продуктов глюкозы : пирувата и НАДН , которые образуются в цитозоле. [19] Этот тип клеточного дыхания , известный как аэробное дыхание , зависит от присутствия кислорода . Когда кислород ограничен, гликолитические продукты будут метаболизироваться посредством анаэробной ферментации , процесса, который не зависит от митохондрий. [19] Производство АТФ из глюкозы и кислорода примерно в 13 раз выше при аэробном дыхании по сравнению с ферментацией. [36] Митохондрии растений также могут производить ограниченное количество АТФ либо за счет расщепления сахара, образующегося во время фотосинтеза, либо без кислорода, используя альтернативный субстрат нитрит . [37] АТФ проникает через внутреннюю мембрану с помощью специфического белка и через внешнюю мембрану через порины . [38] После преобразования АТФ в АДФ путем дефосфорилирования , которое высвобождает энергию, АДФ возвращается тем же путем.
Молекулы пирувата , образующиеся в результате гликолиза , активно транспортируются через внутреннюю митохондриальную мембрану в матрикс, где они могут либо окисляться и соединяться с коферментом А с образованием CO 2 , ацетил-КоА и НАДН [19] , либо карбоксилироваться ( 19) . под действием пируваткарбоксилазы ) с образованием оксалоацетата. Эта последняя реакция «восполняет» количество оксалоацетата в цикле лимонной кислоты и, следовательно, является анаплеротической реакцией , увеличивая способность цикла метаболизировать ацетил-КоА, когда энергетические потребности тканей (например, в мышцах ) внезапно возрастают из-за активности. [39]
В цикле лимонной кислоты все промежуточные продукты (например , цитрат , изоцитрат , альфа-кетоглутарат , сукцинат, фумарат , малат и оксалоацетат) регенерируются во время каждого цикла цикла. Таким образом, добавление большего количества любого из этих промежуточных продуктов в митохондрии означает, что дополнительное количество сохраняется в цикле, увеличивая количество всех других промежуточных продуктов по мере превращения одного в другое. Следовательно, добавление любого из них в цикл имеет анаплеротический эффект, а его удаление – катаплеротический эффект. Эти анаплеротические и катаплеротические реакции в течение цикла будут увеличивать или уменьшать количество оксалоацетата, доступного для соединения с ацетил-КоА с образованием лимонной кислоты. Это, в свою очередь, увеличивает или уменьшает скорость производства АТФ митохондриями и, следовательно, доступность АТФ для клетки. [39]
С другой стороны, ацетил-КоА, получаемый в результате окисления пирувата или бета-окисления жирных кислот , является единственным топливом, вступающим в цикл лимонной кислоты. С каждым оборотом цикла на каждую молекулу оксалоацетата, присутствующую в митохондриальном матриксе, расходуется одна молекула ацетил-КоА и никогда не регенерируется. Именно окисление ацетатной части ацетил-КоА приводит к образованию CO 2 и воды, при этом высвобождаемая энергия улавливается в форме АТФ. [39]
В печени карбоксилирование цитозольного пирувата во внутримитохондриальный оксалоацетат является ранним этапом глюконеогенного пути, который превращает лактат и дезаминированный аланин в глюкозу [19 , 39] под влиянием высоких уровней глюкагона и/или или адреналин в крови. [39] Здесь добавление оксалоацетата к митохондрии не имеет чистого анаплеротического эффекта, поскольку другой промежуточный продукт цикла лимонной кислоты (малат) немедленно удаляется из митохондрии и превращается в цитозольный оксалоацетат и, в конечном итоге, в глюкозу в процессе это почти противоположно гликолизу . [39]
Ферменты цикла лимонной кислоты расположены в митохондриальном матриксе, за исключением сукцинатдегидрогеназы , которая связана с внутренней мембраной митохондрий в составе Комплекса II. [40] Цикл лимонной кислоты окисляет ацетил-КоА до диоксида углерода и в процессе производит восстановленные кофакторы (три молекулы НАДН и одна молекула ФАДН 2 ), которые являются источником электронов для цепи переноса электронов , и молекула ГТФ (которая легко превращается в АТФ). [19]

Электроны от НАДН и ФАДН 2 передаются кислороду (О 2 ) и водороду (протонам) в несколько этапов через цепь переноса электронов. Молекулы НАДН и ФАДН 2 производятся внутри матрикса посредством цикла трикарбоновых кислот и в цитоплазме посредством гликолиза . Восстанавливающие эквиваленты из цитоплазмы могут быть импортированы через малат-аспартатную челночную систему белков- антипортеров или поданы в цепь переноса электронов с использованием глицеринфосфатного челнока . [19]
Основные реакции высвобождения энергии [41] [42] , которые делают митохондрии «электростанцией клетки», происходят в белковых комплексах I, III и IV во внутренней мембране митохондрий ( НАДН-дегидрогеназа (убихинон) , цитохром с-редуктаза и цитохром в-оксидаза ). В комплексе IV О 2 реагирует с восстановленной формой железа в цитохроме с :
высвобождение большого количества свободной энергии [42] [41] из реагентов без разрыва связей органического топлива. Свободная энергия, затрачиваемая на отрыв электрона от Fe 2+ , высвобождается в комплексе III , когда Fe 3+ цитохрома с реагирует с окислением убихинола (QH 2 ):
Образовавшийся убихинон ( Q) в комплексе I реагирует с НАДН:
Хотя реакции контролируются цепью переноса электронов, свободные электроны не входят в число реагентов или продуктов в трех показанных реакциях и, следовательно, не влияют на высвобождаемую свободную энергию, которая используется для перекачки протонов (H + ) в межмембранное пространство. Этот процесс эффективен, но небольшой процент электронов может преждевременно восстанавливать кислород, образуя активные формы кислорода, такие как супероксид . [19] Это может вызвать окислительный стресс в митохондриях и способствовать снижению функции митохондрий, связанному со старением. [43]
По мере увеличения концентрации протонов в межмембранном пространстве через внутреннюю мембрану устанавливается сильный электрохимический градиент . Протоны могут возвращаться в матрикс через АТФ-синтазный комплекс, а их потенциальная энергия используется для синтеза АТФ из АДФ и неорганического фосфата (P i ). [19] Этот процесс называется хемиосмосом и был впервые описан Питером Митчеллом , [44] [45] , который был удостоен Нобелевской премии по химии 1978 года за свою работу. Позже часть Нобелевской премии по химии 1997 года была присуждена Полу Д. Бойеру и Джону Э. Уокеру за разъяснение рабочего механизма АТФ-синтазы. [46]
При определенных условиях протоны могут повторно войти в митохондриальный матрикс, не участвуя в синтезе АТФ. Этот процесс известен как утечка протонов или разобщение митохондрий и обусловлен облегченной диффузией протонов в матрикс. В результате этого процесса неиспользованная потенциальная энергия электрохимического градиента протонов выделяется в виде тепла. [19] Этот процесс опосредован протонным каналом, называемым термогенином , или UCP1 . [47] Термогенин в основном содержится в бурой жировой ткани или буром жире и отвечает за несократительный термогенез. Бурая жировая ткань встречается у млекопитающих, ее самый высокий уровень наблюдается в раннем возрасте и у животных, находящихся в спячке. У человека бурая жировая ткань присутствует при рождении и уменьшается с возрастом. [47]
Синтез митохондриальных жирных кислот (mtFASII) необходим для клеточного дыхания и митохондриального биогенеза. [48] Также считается, что он играет роль медиатора во внутриклеточной передаче сигналов из-за его влияния на уровни биоактивных липидов, таких как лизофосфолипиды и сфинголипиды . [49]
Октаноил-АСР (С8) считается наиболее важным конечным продуктом mtFASII, который также образует стартовый субстрат биосинтеза липоевой кислоты . [50] Поскольку липоевая кислота является кофактором важных митохондриальных ферментных комплексов, таких как комплекс пируватдегидрогеназы (PDC), комплекс α-кетоглутаратдегидрогеназы (OGDC), комплекс дегидрогеназы α-кетокислот с разветвленной цепью (BCKDC) и глицин система расщепления (GCS), mtFASII оказывает влияние на энергетический обмен. [51]
Другие продукты mtFASII играют роль в регуляции митохондриальной трансляции, биогенезе кластеров FeS и сборке комплексов окислительного фосфорилирования. [50]
Кроме того, с помощью mtFASII и ацилированного ACP ацетил-КоА регулирует свое потребление в митохондриях. [50]

Концентрация свободного кальция в клетке может регулировать ряд реакций и важна для передачи сигнала в клетке. Митохондрии могут временно хранить кальций , что способствует гомеостазу кальция в клетках. [52] [53] Их способность быстро поглощать кальций для последующего высвобождения делает их хорошими «цитозольными буферами» для кальция. [54] [55] [56] Эндоплазматический ретикулум (ЭР) является наиболее важным местом хранения кальция, [57] и существует значительное взаимодействие между митохондриями и ЭР в отношении кальция. [58] Кальций поглощается в матрикс митохондриальным унипортером кальция на внутренней митохондриальной мембране . [59] Это в первую очередь обусловлено мембранным потенциалом митохондрий . [53] Высвобождение этого кальция обратно во внутреннюю часть клетки может происходить через натрий-кальциевый обменный белок или через пути «кальций-индуцированного высвобождения кальция». [59] Это может инициировать всплески кальция или волны кальция с большими изменениями мембранного потенциала. Они могут активировать ряд белков системы вторичных мессенджеров , которые могут координировать такие процессы, как высвобождение нейротрансмиттеров в нервных клетках и высвобождение гормонов в эндокринных клетках. [60]
Приток Ca 2+ к митохондриальному матриксу недавно был признан механизмом регуляции дыхательной биоэнергетики , позволяя электрохимическому потенциалу через мембрану временно «пульсировать» от ΔΨ-доминирования к pH-доминированию, способствуя снижению окислительного стресса . [61] В нейронах сопутствующее увеличение цитозольного и митохондриального кальция синхронизирует активность нейронов с митохондриальным энергетическим метаболизмом. Уровни кальция в митохондриальном матриксе могут достигать десятков микромолярных уровней, что необходимо для активации изоцитратдегидрогеназы , одного из ключевых регуляторных ферментов цикла Кребса . [62]
Была исследована связь между клеточной пролиферацией и митохондриями. Опухолевым клеткам требуется достаточное количество АТФ для синтеза биологически активных соединений, таких как липиды , белки и нуклеотиды , для быстрой пролиферации. [63] Большая часть АТФ в опухолевых клетках генерируется посредством пути окислительного фосфорилирования (OxPhos). [64] Взаимодействие с OxPhos вызывает остановку клеточного цикла, что позволяет предположить, что митохондрии играют роль в пролиферации клеток. [64] Производство митохондриального АТФ также жизненно важно для деления и дифференцировки клеток при инфекции [65] в дополнение к основным функциям в клетке, включая регуляцию объема клетки, концентрации растворенных веществ и клеточной архитектуры. [66] [67] [68] Уровни АТФ различаются на разных стадиях клеточного цикла, что позволяет предположить, что существует взаимосвязь между количеством АТФ и способностью клетки вступать в новый клеточный цикл. [69] Роль АТФ в основных функциях клетки делает клеточный цикл чувствительным к изменениям в доступности АТФ, полученного из митохондрий. [69] Вариации уровней АТФ на разных стадиях клеточного цикла подтверждают гипотезу о том, что митохондрии играют важную роль в регуляции клеточного цикла. [69] Хотя конкретные механизмы между митохондриями и регуляцией клеточного цикла не совсем понятны, исследования показали, что низкоэнергетические контрольные точки клеточного цикла контролируют энергетические возможности перед переходом к следующему раунду клеточного деления. [10]
Митохондрии играют центральную роль во многих других метаболических задачах, таких как:
Некоторые митохондриальные функции выполняются только в определенных типах клеток. Например, митохондрии в клетках печени содержат ферменты, которые позволяют им детоксикации аммиака , отхода белкового обмена. Мутация генов, регулирующих любую из этих функций, может привести к митохондриальным заболеваниям .
Митохондриальные белки (белки, транскрибируемые из митохондриальной ДНК) различаются в зависимости от ткани и вида. У человека в митохондриях сердца было идентифицировано 615 различных типов белков [80] , тогда как у крыс сообщалось о 940 белках. [81] Считается, что митохондриальный протеом динамически регулируется. [82]

Митохондрии (или родственные структуры) встречаются у всех эукариот (кроме оксимонад Monocercomonoides ). [6] Хотя их обычно изображают в виде бобовидных структур, они образуют высокодинамическую сеть в большинстве клеток, где постоянно подвергаются делению и слиянию . Популяция всех митохондрий данной клетки составляет хондриому. [83] Митохондрии различаются по количеству и расположению в зависимости от типа клеток. У одноклеточных организмов часто встречается одна митохондрия, тогда как клетки печени человека содержат около 1000–2000 митохондрий на клетку, что составляет 1/5 объема клетки. [18] Содержимое митохондрий в других похожих клетках может существенно различаться по размеру и мембранному потенциалу, [84] причем различия возникают из-за различных источников, включая неравномерное распределение при делении клеток, что приводит к внешним различиям в уровнях АТФ и последующих клеточных процессах. [85] Митохондрии можно найти расположенными между миофибриллами мышц или обернутыми вокруг жгутика спермия . [18] Часто они образуют сложную трехмерную ветвящуюся сеть внутри клетки с цитоскелетом . Ассоциация с цитоскелетом определяет форму митохондрий, которая также может влиять на функцию: [86] различные структуры митохондриальной сети могут предоставлять популяции различные физические, химические и сигнальные преимущества или недостатки. [87] Митохондрии в клетках всегда распределены вдоль микротрубочек, и распределение этих органелл также коррелирует с эндоплазматической сетью . [88] Недавние данные свидетельствуют о том, что виментин , один из компонентов цитоскелета, также имеет решающее значение для связи с цитоскелетом. [89]
Мембрана ЭР, связанная с митохондриями (МАМ), является еще одним структурным элементом, который все чаще признается за его решающую роль в клеточной физиологии и гомеостазе . Когда-то считавшиеся техническим препятствием в методах фракционирования клеток, предполагаемые примеси везикул ЭР, которые неизменно появлялись в митохондриальной фракции, были повторно идентифицированы как мембранные структуры, полученные из МАМ — интерфейса между митохондриями и ЭР. [90] Физическая связь между этими двумя органеллами ранее наблюдалась на электронных микрофотографиях, а совсем недавно была исследована с помощью флуоресцентной микроскопии . [90] По оценкам таких исследований, в МАМ, которая может составлять до 20% внешней мембраны митохондрий, ЭР и митохондрии разделены всего на 10–25 нм и удерживаются вместе белковыми привязывающими комплексами. [90] [28] [91]
Очищенный МАМ, полученный путем субклеточного фракционирования, обогащен ферментами, участвующими в обмене фосфолипидов, в дополнение к каналам, связанным с передачей сигналов Ca 2+ . [90] [91] Эти намеки на выдающуюся роль МАМ в регуляции клеточных липидных запасов и передаче сигналов были подтверждены, что имело значительные последствия для клеточных явлений, связанных с митохондриями, как обсуждается ниже. МАМ не только предоставил понимание механистической основы, лежащей в основе таких физиологических процессов, как внутренний апоптоз и распространение передачи сигналов кальция, но также способствует более точному взгляду на митохондрии. Хотя МАМ часто рассматривается как статичные, изолированные «электростанции», задействованные для клеточного метаболизма посредством древнего эндосимбиотического события, эволюция МАМ подчеркивает степень, в которой митохондрии интегрированы в общую клеточную физиологию, с тесной физической и функциональной связью с эндомембранной системой.
МАМ обогащен ферментами, участвующими в биосинтезе липидов, такими как фосфатидилсеринсинтаза на поверхности ЭР и фосфатидилсериндекарбоксилаза на поверхности митохондрий. [92] [93] Поскольку митохондрии представляют собой динамические органеллы, постоянно подвергающиеся процессам деления и слияния , им требуется постоянное и хорошо регулируемое снабжение фосфолипидами для целостности мембран. [94] [95] Но митохондрии являются не только местом назначения фосфолипидов, синтез которых они завершают; скорее, эта органелла также играет роль в межорганелловом транспорте промежуточных продуктов и продуктов путей биосинтеза фосфолипидов, метаболизме церамидов и холестерина, а также анаболизме гликосфинголипидов. [93] [95]
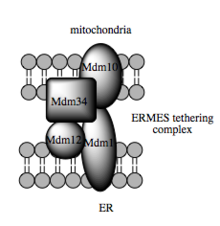
Такая способность транспорта зависит от MAM, который, как было показано, облегчает перенос липидных промежуточных продуктов между органеллами. [92] В отличие от стандартного везикулярного механизма переноса липидов, данные указывают на то, что физическая близость ЭР и митохондриальных мембран в МАМ позволяет осуществлять переворот липидов между противоположными бислоями. [95] Несмотря на этот необычный и, казалось бы, энергетически невыгодный механизм, такой транспорт не требует АТФ. [95] Вместо этого у дрожжей было показано, что это зависит от мультибелковой связывающей структуры, называемой структурой встречи ER-митохондрий, или ERMES, хотя остается неясным, опосредует ли эта структура непосредственно перенос липидов или она необходима для поддержания мембран в достаточно близкое расположение, чтобы снизить энергетический барьер для переворота липидов . [95] [96]
МАМ также может быть частью секреторного пути в дополнение к своей роли во внутриклеточном транспорте липидов. В частности, MAM, по-видимому, является промежуточным пунктом назначения между шероховатым ЭР и Гольджи на пути, который приводит к сборке и секреции липопротеинов очень низкой плотности , или ЛПОНП. [93] [97] Таким образом, МАМ служит важнейшим метаболическим и транспортным узлом в липидном обмене.
Критическая роль ЭР в передаче сигналов кальция была признана еще до того, как такая роль митохондрий получила широкое признание, отчасти потому, что низкое сродство Ca 2+ -каналов, локализованных на внешней митохондриальной мембране, по-видимому, противоречило предполагаемой реакции этой органеллы на изменения внутриклеточной активности. Флюс Са 2+ . [90] [57] Но присутствие MAM разрешает это очевидное противоречие: тесная физическая ассоциация между двумя органеллами приводит к образованию микродоменов Ca 2+ в точках контакта, которые способствуют эффективной передаче Ca 2+ из ЭР в митохондрии. [90] Передача происходит в ответ на так называемые «выбросы Ca 2+ », генерируемые спонтанной кластеризацией и активацией IP3R , канонического Ca 2+ -канала мембраны ЭР. [90] [28]
Судьба этих клубков - в частности, остаются ли они ограниченными изолированными локалями или интегрируются в волны Ca 2+ для распространения по клетке - определяется в значительной степени динамикой MAM. Хотя обратный захват Ca 2+ ЭР (одновременно с его высвобождением) модулирует интенсивность затяжек, тем самым в определенной степени изолируя митохондрии от высокого воздействия Ca 2+ , MAM часто служит брандмауэром, который по существу буферизует затяжки Ca 2+ . действуя как сток, в который могут направляться свободные ионы, высвобождаемые в цитозоль. [90] [98] [99] Это туннелирование Ca 2+ происходит через низкоаффинный Ca 2+ рецептор VDAC1 , который, как недавно было показано, физически связан с кластерами IP3R на мембране ER и обогащен в MAM. [90] [28] [100] Способность митохондрий служить стоком Ca 2+ является результатом электрохимического градиента, возникающего во время окислительного фосфорилирования, что делает туннелирование катиона экзергоническим процессом. [100] Нормальный, умеренный приток кальция из цитозоля в митохондриальный матрикс вызывает временную деполяризацию, которая корректируется путем откачки протонов.
Но передача Ca 2+ не является однонаправленной; скорее, это улица с двусторонним движением. [57] Свойства Ca 2+ насоса SERCA и канала IP3R, присутствующие на мембране ЭР, облегчают регуляцию по обратной связи, координируемую функцией MAM. В частности, клиренс Ca 2+ с помощью MAM позволяет формировать пространственно-временной паттерн передачи сигналов Ca 2+ , поскольку Ca 2+ изменяет активность IP3R двухфазным образом. [90] На SERCA также влияет митохондриальная обратная связь: поглощение Ca 2+ MAM стимулирует выработку АТФ, таким образом обеспечивая энергию, которая позволяет SERCA перезагрузить ER Ca 2+ для продолжения оттока Ca 2+ в MAM. [98] [100] Таким образом, МАМ не является пассивным буфером для слоев Ca 2+ ; скорее это помогает модулировать дальнейшую передачу сигналов Ca 2+ через петли обратной связи, которые влияют на динамику ER.
Регулирование высвобождения Ca 2+ из ER в MAM особенно важно, поскольку только определенное окно поглощения Ca 2+ поддерживает митохондрии и, следовательно, клетку в гомеостазе. Достаточная внутриорганелльная передача сигналов Ca 2+ необходима для стимуляции метаболизма путем активации ферментов дегидрогеназы, имеющих решающее значение для прохождения цикла лимонной кислоты. [101] [102] Однако, как только передача сигналов Ca 2+ в митохондриях достигает определенного порога, она стимулирует внутренний путь апоптоза, частично за счет коллапса потенциала митохондриальной мембраны, необходимого для метаболизма. [90] Исследования, изучающие роль про- и антиапоптотических факторов, подтверждают эту модель; например, было показано, что антиапоптотический фактор Bcl-2 взаимодействует с IP3R, уменьшая заполнение ER Ca 2+ , что приводит к уменьшению оттока в MAM и предотвращает коллапс митохондриальных мембранных потенциальных постапоптотических стимулов. [90] Учитывая необходимость такой точной регуляции передачи сигналов Ca 2+ , возможно, неудивительно, что дисрегуляция митохондриального Ca 2+ вовлечена в несколько нейродегенеративных заболеваний, в то время как каталог опухолевых супрессоров включает несколько, которые обогащены MAM. [100]
Недавние достижения в идентификации связей между митохондриальными и ER мембранами позволяют предположить, что функция каркаса вовлеченных молекулярных элементов является вторичной по отношению к другим, неструктурным функциям. У дрожжей ERMES, мультипротеиновый комплекс взаимодействующих мембранных белков, находящихся в ER и митохондриях, необходим для переноса липидов в MAM и служит примером этого принципа. Например, один из его компонентов также входит в состав белкового комплекса, необходимого для внедрения трансмембранных белков бета-бочонка в липидный бислой. [95] Однако гомолог комплекса ERMES еще не идентифицирован в клетках млекопитающих. Другие белки, вовлеченные в каркас, также имеют функции, независимые от структурной привязки к MAM; например, ER-резидентные и митохондриальные митофузины образуют гетерокомплексы, которые регулируют количество мест контакта между органеллами, хотя митофузины были впервые идентифицированы по их роли в событиях деления и слияния между отдельными митохондриями. [90] Связанный с глюкозой белок 75 (grp75) является еще одним белком с двойной функцией. В дополнение к матричному пулу grp75, часть служит шапероном, который физически связывает митохондриальные и ER Ca 2+ каналы VDAC и IP3R для эффективной передачи Ca 2+ в MAM. [90] [28] Другой потенциальной привязью является Sigma-1R , неопиоидный рецептор, чья стабилизация ER-резидентного IP3R может сохранять связь в MAM во время реакции метаболического стресса. [103] [104]
МАМ является важным узлом передачи сигналов, метаболизма и транспорта в клетке, который обеспечивает интеграцию ЭР и физиологии митохондрий. Связь между этими органеллами является не просто структурной, но и функциональной и имеет решающее значение для общей клеточной физиологии и гомеостаза . Таким образом, MAM предлагает взгляд на митохондрии, который расходится с традиционным представлением об этой органелле как о статической, изолированной единице, предназначенной для метаболических способностей клетки. [105] Вместо этого этот интерфейс митохондрий и ЭР подчеркивает интеграцию митохондрий, продукта эндосимбиотического события, в разнообразные клеточные процессы. Недавно также было показано, что митохондрии и МАМ в нейронах прикреплены к специализированным местам межклеточной коммуникации (так называемым соматическим соединениям). Процессы микроглии контролируют и защищают функции нейронов в этих участках, и предполагается, что MAM-s играют важную роль в этом типе контроля качества клеток. [78]
Существуют две гипотезы происхождения митохондрий: эндосимбиотическая и аутогенная . Эндосимбиотическая гипотеза предполагает, что митохондрии изначально были прокариотическими клетками, способными реализовывать окислительные механизмы, которые были невозможны для эукариотических клеток; они стали эндосимбионтами , живущими внутри эукариот. [21] [106] [107] [108] Согласно аутогенной гипотезе, митохондрии возникли в результате отщепления части ДНК от ядра эукариотической клетки во время расхождения с прокариотами; эта часть ДНК была бы окружена мембранами, через которые белки не могли бы пройти. Поскольку митохондрии имеют много общих черт с бактериями , эндосимбиотическая гипотеза является более широко принятой из двух версий. [108] [109]
Митохондрия содержит ДНК , которая организована в виде нескольких копий одной, обычно кольцевой хромосомы . Эта митохондриальная хромосома содержит гены окислительно-восстановительных белков, например белков дыхательной цепи. Гипотеза CoRR предполагает, что такое совместное расположение необходимо для окислительно-восстановительной регуляции. Митохондриальный геном кодирует некоторые РНК рибосом и 22 тРНК , необходимые для трансляции мРНК в белок. Круглая структура встречается и у прокариот. Протомитохондрия , вероятно, была тесно связана с Rickettsia . [110] [111] Однако точная связь предка митохондрий с альфапротеобактериями и то, образовалась ли митохондрия одновременно с ядром или после ядра, остается спорным. [112] Например, было высказано предположение, что клада бактерий SAR11 имеет относительно недавнего общего предка с митохондриями, [113] в то время как филогеномный анализ показывает, что митохондрии произошли от линии Pseudomonadota , которая тесно связана с альфапротеобактериями или является их членом. . [114] [115] В некоторых статьях митохондрии описываются как сестры альфапротеобактерий, вместе образующие сестринскую группу Marineproteo1, вместе образующие сестру Magnetococcidae . [116] [117] [118] [119]
Рибосомы, кодируемые митохондриальной ДНК, по размеру и структуре аналогичны рибосомам бактерий. [120] Они очень напоминают бактериальную 70S рибосому, а не 80S цитоплазматические рибосомы, которые кодируются ядерной ДНК.
Эндосимбиотические отношения митохондрий с клетками-хозяевами были популяризированы Линн Маргулис . [121] Эндосимбиотическая гипотеза предполагает, что митохондрии произошли от аэробных бактерий, которые каким-то образом пережили эндоцитоз другой клетки и включились в цитоплазму . Способность этих бактерий осуществлять дыхание в клетках-хозяевах, основанных на гликолизе и ферментации , могла бы обеспечить значительное эволюционное преимущество. Эти симбиотические отношения, вероятно, возникли 1,7–2 миллиарда лет назад. [122] [123]

Некоторые группы одноклеточных эукариот имеют только рудиментарные митохондрии или производные структуры: микроспоридии , метамонады и архамебы . [124] Эти группы появляются как наиболее примитивные эукариоты на филогенетических деревьях , построенных с использованием информации рРНК , что однажды позволило предположить, что они появились до возникновения митохондрий. Однако теперь известно, что это результат притяжения длинных ветвей : они представляют собой производные группы и сохраняют гены или органеллы, полученные из митохондрий (например, митосомы и гидрогеносомы ). [5] Гидрогеносомы, митосомы и родственные органеллы, обнаруженные у некоторых лорицифер (например, Spinoloricus ) [125] [126] и миксозоа (например, Henneguya zschokkei ), вместе классифицируются как MRO, органеллы, связанные с митохондриями. [8] [127]
Monocercomonoides, по-видимому, полностью утратили свои митохондрии, и, по крайней мере, некоторые из митохондриальных функций теперь, по-видимому, выполняются цитоплазматическими белками. [6]

Митохондрии содержат собственный геном. Митохондриальный геном человека представляет собой кольцевую двухцепочечную молекулу ДНК длиной около 16 тыс. нуклеотидов . [128] Он кодирует 37 генов: 13 для субъединиц дыхательных комплексов I, III, IV и V, 22 для митохондриальной тРНК (для 20 стандартных аминокислот плюс дополнительный ген для лейцина и серина) и 2 для рРНК (12S и 16S рРНК). [128] Одна митохондрия может содержать от двух до десяти копий своей ДНК. [129] Одна из двух цепей митохондриальной ДНК (мтДНК) имеет непропорционально более высокое соотношение более тяжелых нуклеотидов аденина и гуанина, и это называется тяжелой цепью (или Н-цепью), тогда как другая цепь называется легкой цепью (или Н-цепью). L-прядь). Разница в весе позволяет разделить две нити центрифугированием . мтДНК имеет один длинный некодирующий участок, известный как некодирующая область (NCR), который содержит промотор тяжелой цепи (HSP) и промотор легкой цепи (LSP) для транскрипции РНК, начала репликации H-цепи (OriH). локализованный на L-цепи, трех консервативных последовательностях (CSB 1–3) и последовательности, связанной с терминацией (TAS). Начало репликации L-цепи (OriL) локализовано на H-цепи на 11 000 п.н. ниже OriH, расположенной внутри кластера генов, кодирующих тРНК. [130]
Как и у прокариот, здесь очень высока доля кодирующей ДНК и отсутствуют повторы. Митохондриальные гены транскрибируются в виде мультигенных транскриптов, которые расщепляются и полиаденилируются с образованием зрелых мРНК . Большинство белков, необходимых для функционирования митохондрий, кодируются генами в ядре клетки , и соответствующие белки импортируются в митохондрии. [131] Точное количество генов, кодируемых ядром и митохондриальным геномом, различается у разных видов. Большинство митохондриальных геномов имеют кольцевую форму. [132] Как правило, в митохондриальной ДНК отсутствуют интроны , как и в митохондриальном геноме человека; [131] однако интроны наблюдались в некоторых эукариотических митохондриальных ДНК, [133] таких как ДНК дрожжей [134] и простейших , [135] включая Dictyostelium discoideum . [136] Между областями, кодирующими белок, присутствуют тРНК. Гены митохондриальных тРНК имеют последовательности, отличные от ядерных тРНК, но двойники митохондриальных тРНК были обнаружены в ядерных хромосомах с высоким сходством последовательностей. [137]
У животных митохондриальный геном обычно представляет собой одну кольцевую хромосому длиной примерно 16 т.п.н., содержащую 37 генов. Гены, хотя и высококонсервативны, могут различаться по местоположению. Любопытно, что данная закономерность не обнаружена у человеческой телесной вши ( Pediculus humanus ). Вместо этого этот митохондриальный геном состоит из 18 миникольцевых хромосом, каждая из которых имеет длину 3–4 т.п.н. и содержит от одного до трех генов. [138] Этот образец также встречается у других сосущих вшей , но не у жевательных вшей . Было показано, что рекомбинация происходит между минихромосомами.
Практически отсутствие генетической рекомбинации в митохондриальной ДНК делает ее полезным источником информации для изучения популяционной генетики и эволюционной биологии . [139] Поскольку вся митохондриальная ДНК наследуется как одна единица или гаплотип , взаимоотношения между митохондриальной ДНК разных людей могут быть представлены в виде генного дерева . Закономерности в этих генных деревьях можно использовать для вывода об эволюционной истории популяций. Классическим примером этого является эволюционная генетика человека , где молекулярные часы можно использовать для определения недавней даты появления митохондриальной Евы . [140] [141] Это часто интерпретируется как решительная поддержка недавней современной человеческой экспансии за пределы Африки . [142] Другой человеческий пример — секвенирование митохондриальной ДНК из костей неандертальцев . Относительно большое эволюционное расстояние между последовательностями митохондриальной ДНК неандертальцев и современных людей было интерпретировано как свидетельство отсутствия скрещивания между неандертальцами и современными людьми. [143]
Однако митохондриальная ДНК отражает только историю самок в популяции. Частично это можно преодолеть за счет использования отцовских генетических последовательностей, таких как нерекомбинирующая область Y-хромосомы . [142]
Недавние измерения молекулярных часов митохондриальной ДНК [144] показали значение 1 мутации каждые 7884 года, начиная с самого недавнего общего предка человека и обезьяны, что согласуется с оценками частоты мутаций аутосомной ДНК (10 -8 на 1 база на поколение). [145]
Хотя небольшие вариации стандартного генетического кода были предсказаны ранее [146] , они не были обнаружены до 1979 года, когда исследователи, изучающие митохондриальные гены человека, установили, что они используют альтернативный код. [147] Тем не менее, митохондрии многих других эукариот, включая большинство растений, используют стандартный код. [148] С тех пор было обнаружено множество небольших вариантов, [148] включая различные альтернативные митохондриальные коды. [149] Кроме того, кодоны AUA, AUC и AUU являются допустимыми стартовыми кодонами.
Некоторые из этих различий следует рассматривать как псевдоизменения генетического кода, обусловленные явлением редактирования РНК , которое часто встречается в митохондриях. Считалось, что у высших растений CGG кодирует триптофан , а не аргинин ; однако было обнаружено, что кодоном в обработанной РНК является кодон UGG, что соответствует стандартному генетическому коду триптофана. [150] Следует отметить, что митохондриальный генетический код членистоногих претерпел параллельную эволюцию внутри одного типа, при этом некоторые организмы уникальным образом переводят AGG в лизин. [151]
Митохондрии делятся путем деления митохондрий — формы бинарного деления , которая также осуществляется бактериями [152], хотя этот процесс жестко регулируется эукариотической клеткой-хозяином и включает в себя связь и контакт с несколькими другими органеллами. Регуляция этого деления у эукариот различна. У многих одноклеточных эукариот их рост и деление связаны с клеточным циклом . Например, одна митохондрия может делиться синхронно с ядром. Этот процесс деления и сегрегации необходимо строго контролировать, чтобы каждая дочерняя клетка получила хотя бы одну митохондрия. У других эукариот (например, у млекопитающих) митохондрии могут реплицировать свою ДНК и делиться главным образом в ответ на энергетические потребности клетки, а не в фазе клеточного цикла. Когда энергетические потребности клетки высоки, митохондрии растут и делятся. Когда потребление энергии низкое, митохондрии разрушаются или становятся неактивными. В таких примерах митохондрии, по-видимому, случайным образом распределяются по дочерним клеткам при делении цитоплазмы . Митохондриальная динамика, баланс между слиянием и делением митохондрий , является важным фактором патологий, связанных с некоторыми болезненными состояниями. [153]
Гипотеза бинарного деления митохондрий основана на визуализации с помощью флуоресцентной микроскопии и традиционной просвечивающей электронной микроскопии (ПЭМ). Разрешение флуоресцентной микроскопии (~ 200 нм) недостаточно для различения структурных деталей, таких как двойная митохондриальная мембрана при делении митохондрий, или даже для различения отдельных митохондрий, когда несколько из них расположены близко друг к другу. Обычный ТЕМ также имеет некоторые технические ограничения [ какие? ] при проверке деления митохондрий. Криоэлектронная томография недавно была использована для визуализации деления митохондрий в замороженных гидратированных интактных клетках. Выяснилось, что митохондрии делятся путем почкования. [154]
Митохондриальные гены особи наследуются только от матери, за редким исключением. [155] У людей, когда яйцеклетка оплодотворяется спермой, митохондрии и, следовательно, митохондриальная ДНК обычно происходят только из яйцеклетки. Митохондрии сперматозоида попадают в яйцеклетку, но не несут генетическую информацию эмбриону. [156] Вместо этого отцовские митохондрии помечаются убиквитином , чтобы отобрать их для последующего разрушения внутри эмбриона . [157] Яйцеклетка содержит относительно мало митохондрий, но эти митохондрии делятся, заселяя клетки взрослого организма. Этот режим наблюдается у большинства организмов, включая большинство животных. Однако митохондрии у некоторых видов иногда могут наследоваться по отцовской линии. Это норма для некоторых хвойных растений, но не для сосен и тисов . [158] Для митилид отцовское наследование происходит только у самцов этого вида. [159] [160] [161] Было высказано предположение, что у людей он встречается на очень низком уровне. [162]
Однородительское наследование приводит к ограничению возможностей генетической рекомбинации между различными линиями митохондрий, хотя одна митохондрия может содержать 2–10 копий своей ДНК. [129] Рекомбинация, которая действительно имеет место, поддерживает генетическую целостность, а не разнообразие. Однако есть исследования, показывающие доказательства рекомбинации в митохондриальной ДНК. Понятно, что ферменты, необходимые для рекомбинации, присутствуют в клетках млекопитающих. [163] Кроме того, данные свидетельствуют о том, что митохондрии животных могут подвергаться рекомбинации. [164] Данные более противоречивы у людей, хотя косвенные доказательства рекомбинации существуют. [165] [166]
Можно ожидать, что сущности, претерпевающие однородительское наследование и практически не имеющие рекомбинации, будут подвержены храповому механизму Мюллера — накоплению вредных мутаций до тех пор, пока функциональность не будет потеряна. Популяции митохондрий животных избегают такого накопления благодаря процессу развития, известному как «узкое место» мтДНК . Узкое место использует стохастические процессы в клетке для увеличения межклеточной изменчивости мутантной нагрузки по мере развития организма: одна яйцеклетка с некоторой долей мутантной мтДНК, таким образом, производит эмбрион, в котором разные клетки имеют разную мутантную нагрузку. Затем отбор на уровне клеток может привести к удалению клеток с большим количеством мутантной мтДНК, что приведет к стабилизации или уменьшению мутантной нагрузки между поколениями. Механизм, лежащий в основе узкого места, обсуждается [167] [168] [169] с недавним математическим и экспериментальным метаисследованием, предоставляющим доказательства комбинации случайного разделения мтДНК при клеточных делениях и случайного оборота молекул мтДНК внутри клетки. [170]
Митохондрии могут восстанавливать окислительные повреждения ДНК по механизмам, аналогичным тем, которые происходят в ядре клетки . Белки, участвующие в репарации мтДНК , кодируются ядерными генами и транслоцируются в митохондрии. Пути репарации ДНК в митохондриях млекопитающих включают репарацию вырезания оснований , репарацию двухцепочечного разрыва, прямое обращение и репарацию несоответствия . [171] [172] Альтернативно, повреждение ДНК можно обойти, а не восстановить, путем трансфункционального синтеза.
Из нескольких процессов репарации ДНК в митохондриях наиболее полно изучен путь эксцизионной репарации оснований. [172] Репарация с иссечением оснований осуществляется с помощью последовательности этапов, катализируемых ферментами, которые включают распознавание и вырезание поврежденного основания ДНК, удаление образовавшегося абазисного сайта, обработку концов, заполнение пробелов и лигирование. Распространенным повреждением мтДНК, которое восстанавливается путем эксцизионной репарации оснований, является 8-оксогуанин , образующийся в результате окисления гуанина . [173]
Двухцепочечные разрывы могут быть устранены путем гомологичной рекомбинационной репарации как в мтДНК млекопитающих [174], так и в мтДНК растений. [175] Двухцепочечные разрывы в мтДНК также можно исправить путем микрогомологического соединения концов . [176] Хотя есть доказательства процессов репарации прямого обращения и репарации несоответствий в мтДНК, эти процессы недостаточно хорошо изучены. [172]
Некоторые организмы вообще потеряли митохондриальную ДНК. В этих случаях гены, кодируемые митохондриальной ДНК, теряются или переносятся в ядро. [128] Криптоспоридии имеют митохондрии, в которых отсутствует ДНК, предположительно потому, что все их гены были потеряны или перенесены. [177] У Cryptosporidium митохондрии имеют измененную систему генерации АТФ , которая делает паразита устойчивым ко многим классическим митохондриальным ингибиторам , таким как цианид , азид и атоваквон . [177] Митохондрии, лишенные собственной ДНК, были обнаружены у морских паразитических динофлагеллят из рода Amoebophyra . Этот микроорганизм, A. cerati , имеет функциональные митохондрии, лишенные генома. [178] У родственных видов митохондриальный геном все еще имеет три гена, но у A. cerati обнаружен только один митохондриальный ген — ген цитохром с-оксидазы I ( cox1 ) — и он мигрировал в геном ядра. [179]
Повреждение и последующая дисфункция митохондрий являются важным фактором ряда заболеваний человека из-за их влияния на клеточный метаболизм. Митохондриальные расстройства часто проявляются как неврологические расстройства, включая аутизм . [16] Они также могут проявляться в виде миопатии , диабета , множественной эндокринопатии и множества других системных нарушений. [180] Заболевания, вызванные мутацией мтДНК, включают синдром Кернса-Сейра , синдром MELAS и наследственную оптическую невропатию Лебера . [181] В подавляющем большинстве случаев эти заболевания передаются женщиной своим детям, поскольку зигота получает митохондрии и, следовательно, мтДНК из яйцеклетки. Считается , что такие заболевания, как синдром Кернса-Сейра, синдром Пирсона и прогрессирующая наружная офтальмоплегия , возникают из-за крупномасштабных перестроек мтДНК, тогда как другие заболевания, такие как синдром MELAS, наследственная оптическая нейропатия Лебера, синдром MERRF и другие, возникают из-за точковых мутаций. в мтДНК. [180]
Также сообщалось, что раковые клетки, толерантные к лекарствам, имеют увеличенное количество и размер митохондрий, что предполагает увеличение митохондриального биогенеза. [182] Исследование, проведенное в журнале Nature Nanotechnology в 2022 году , показало, что раковые клетки могут захватывать митохондрии у иммунных клеток с помощью физических туннельных нанотрубок. [183]
При других заболеваниях дефекты ядерных генов приводят к дисфункции митохондриальных белков. Это имеет место при атаксии Фридрейха , наследственной спастической параплегии и болезни Вильсона . [184] Эти заболевания наследуются по принципу доминирования , как и большинство других генетических заболеваний. Различные нарушения могут быть вызваны ядерными мутациями ферментов окислительного фосфорилирования, например, дефицит коэнзима Q10 и синдром Барта . [180] Влияние окружающей среды может взаимодействовать с наследственной предрасположенностью и вызывать митохондриальные заболевания. Например, может существовать связь между воздействием пестицидов и более поздним возникновением болезни Паркинсона . [185] [186] Другие патологии, этиология которых связана с митохондриальной дисфункцией, включают шизофрению , биполярное расстройство , деменцию , болезнь Альцгеймера , [187] [188] болезнь Паркинсона, эпилепсию , инсульт , сердечно-сосудистые заболевания , синдром хронической усталости , пигментный ретинит и сахарный диабет. . [189] [190]
Митохондриально-опосредованный окислительный стресс играет роль в кардиомиопатии у диабетиков 2 типа . Увеличение доставки жирных кислот в сердце увеличивает поглощение жирных кислот кардиомиоцитами, что приводит к усилению окисления жирных кислот в этих клетках. Этот процесс увеличивает количество восстанавливающих эквивалентов, доступных для цепи переноса электронов митохондрий, что в конечном итоге увеличивает выработку активных форм кислорода (АФК). АФК увеличивают разобщающие белки (UCP) и усиливают утечку протонов через транслокатор адениновых нуклеотидов (ANT), комбинация которых разъединяет митохондрии. Затем разобщение увеличивает потребление кислорода митохондриями, что усугубляет усиление окисления жирных кислот. Это создает порочный круг разъединения; более того, даже несмотря на то, что потребление кислорода увеличивается, синтез АТФ не увеличивается пропорционально, поскольку митохондрии разобщены. Уменьшение доступности АТФ в конечном итоге приводит к дефициту энергии, проявляющемуся снижением эффективности работы сердца и сократительной дисфункцией. Проблема усугубляется тем, что нарушение высвобождения кальция саркоплазматическим ретикулумом и снижение обратного захвата митохондрий ограничивают пиковые цитозольные уровни важного сигнального иона во время мышечного сокращения. Снижение внутримитохондриальной концентрации кальция увеличивает активацию дегидрогеназы и синтез АТФ. Таким образом, помимо снижения синтеза АТФ из-за окисления жирных кислот, синтез АТФ также нарушается из-за плохой передачи сигналов кальция, что вызывает проблемы с сердцем у диабетиков. [191]
Митохондрии также модулируют такие процессы, как развитие соматических клеток яичек, дифференциация сперматогониальных стволовых клеток, подкисление просвета, выработка тестостерона в семенниках и многое другое. Таким образом, дисфункция митохондрий сперматозоидов может быть причиной бесплодия. [192]
В целях борьбы с митохондриальными заболеваниями была разработана митохондриальная заместительная терапия (МЗТ). В этой форме экстракорпорального оплодотворения используются донорские митохондрии, что позволяет избежать передачи заболеваний, вызванных мутациями митохондриальной ДНК. [193] Однако эта терапия все еще исследуется и может привести к генетической модификации, а также к проблемам с безопасностью. Эти заболевания редки, но могут быть чрезвычайно изнурительными и прогрессирующими заболеваниями, что ставит сложные этические вопросы перед государственной политикой. [194]
Возможна некоторая утечка электронов, переносимых в дыхательной цепи, с образованием активных форм кислорода . Считалось, что это приводит к значительному окислительному стрессу в митохондриях с высокой скоростью мутаций митохондриальной ДНК. [195] Гипотеза о связи между старением и окислительным стрессом не нова и была предложена в 1956 году, [196] которая позже была уточнена в митохондриальную свободнорадикальную теорию старения . [197] Считалось, что возникает порочный круг, поскольку окислительный стресс приводит к мутациям митохондриальной ДНК, что может привести к ферментативным нарушениям и дальнейшему окислительному стрессу.
В процессе старения в митохондриях может произойти ряд изменений. [198] В тканях пожилых людей наблюдается снижение ферментативной активности белков дыхательной цепи. [199] Однако мутированную мтДНК можно обнаружить только примерно в 0,2% очень старых клеток. [200] Было высказано предположение, что крупные делеции в митохондриальном геноме приводят к высокому уровню окислительного стресса и гибели нейронов при болезни Паркинсона . [201] Также было показано, что митохондриальная дисфункция возникает при боковом амиотрофическом склерозе . [202] [203]
Поскольку митохондрии играют ключевую роль в функции яичников, обеспечивая АТФ, необходимую для развития от зародышевого пузырька до зрелого ооцита , снижение функции митохондрий может привести к воспалению, что приводит к преждевременной недостаточности яичников и ускоренному старению яичников. Возникающая в результате дисфункция затем отражается в количественных (например, число копий мтДНК и делеции мтДНК), качественных (например, мутации и разрывы цепей) и окислительных повреждениях (например, дисфункция митохондрий из-за АФК), которые имеют значение не только для старения яичников, но нарушают перекрестные помехи ооцитов и кумулюсов в яичнике, связаны с генетическими нарушениями (такими как Fragile X) и могут мешать отбору эмбрионов. [204]
Первые наблюдения внутриклеточных структур, которые, вероятно, представляли собой митохондрии, были опубликованы в 1857 году физиологом Альбертом фон Колликером . [205] [206] Ричард Альтманн в 1890 году определил их как клеточные органеллы и назвал их «биобластами». [206] [207] В 1898 году Карл Бенда ввёл термин «митохондрии» от греческого μίτος , mitos , «нить», и χονδρίον , хондрия , «гранулы». [208] [206] [209] Леонор Михаэлис обнаружила, что Янус-зеленый можно использовать в качестве прижизненного красителя для митохондрий в 1900 году. [210] В 1904 году Фридрих Мевес сделал первое зарегистрированное наблюдение митохондрий в растениях в клетках белой кувшинки. , Nymphaea alba , [206] [211] и в 1908 году вместе с Клавдием Рего предположили, что они содержат белки и липиды. Бенджамин Ф. Кингсбери в 1912 году впервые связал их с клеточным дыханием, но почти исключительно на основании морфологических наблюдений. [212] [206] В 1913 году Отто Генрих Варбург связал дыхание с частицами, которые он получил из экстракта печени морской свинки и которые он назвал «грана». [213] Варбург и Генрих Отто Виланд , которые также постулировали аналогичный механизм частиц, разошлись во мнениях относительно химической природы дыхания. Лишь в 1925 году, когда Дэвид Кейлин открыл цитохромы , дыхательная цепь была описана. [206]
В 1939 году эксперименты с использованием измельченных мышечных клеток показали, что клеточное дыхание с использованием одной молекулы кислорода может образовывать четыре молекулы аденозинтрифосфата (АТФ), а в 1941 году Фриц разработал концепцию фосфатных связей АТФ, являющихся формой энергии в клеточном метаболизме. Альберт Липманн . В последующие годы механизм клеточного дыхания получил дальнейшее развитие, хотя его связь с митохондриями не была известна. [206] Введение Альбертом Клодом фракционирования тканей позволило изолировать митохондрии от других клеточных фракций и проводить биохимический анализ только на них. В 1946 году он пришел к выводу, что в митохондриях выделены цитохромоксидаза и другие ферменты, ответственные за дыхательную цепь. Юджин Кеннеди и Альберт Ленинджер в 1948 году обнаружили, что митохондрии являются местом окислительного фосфорилирования у эукариот. Со временем метод фракционирования получил дальнейшее развитие, улучшив качество выделяемых митохондрий, и было установлено, что в митохондриях происходят другие элементы клеточного дыхания . [206]
Первые электронные микрофотографии высокого разрешения появились в 1952 году, заменив окраску Януса Грина в качестве предпочтительного способа визуализации митохондрий. [206] Это привело к более детальному анализу структуры митохондрий, включая подтверждение того, что они окружены мембраной. Исследование также показало наличие второй мембраны внутри митохондрий, которая складывалась в гребни, разделяющие внутреннюю камеру, и что размер и форма митохондрий варьировались от клетки к клетке.
Популярный термин «электростанция клетки» был придуман Филипом Сикевицем в 1957 году. [4] [214]
В 1967 году было обнаружено, что митохондрии содержат рибосомы . [215] В 1968 году были разработаны методы картирования митохондриальных генов, а генетическая и физическая карта митохондриальной ДНК дрожжей была завершена в 1976 году. [206]
Таким образом, митохондриальный биогенез определяется как процесс, посредством которого клетки увеличивают свою индивидуальную митохондриальную массу [3]. ... Биогенез митохондрий происходит путем роста и деления ранее существовавших органелл и временно координируется с событиями клеточного цикла [1].
Митохондриальный биогенез (МБ) является важным механизмом, с помощью которого клетки контролируют количество митохондрий.
п. 344: Немного удивительно, что организмы с несколько разными кодами не сосуществуют.Дальнейшее обсуждение.
{{citation}}: |first4=имеет общее имя ( справка )Общий