Муковисцидоз ( МВ ) – редкое [6] [7] генетическое заболевание , поражающее в основном легкие , но также и поджелудочную железу , печень , почки и кишечник . [1] [8] Отличительной особенностью МВ является накопление густой слизи в различных органах. Долгосрочные проблемы включают затрудненное дыхание и кашель со слизью в результате частых легочных инфекций . [1] Другие признаки и симптомы могут включать инфекции носовых пазух , плохой рост , жирный стул , биение пальцев рук и ног и бесплодие у большинства мужчин. [1] У разных людей симптомы могут быть разной степени тяжести. [1]
Муковисцидоз наследуется по аутосомно-рецессивному типу. [1] Это вызвано наличием мутаций в обеих копиях (аллелях) гена, кодирующего белок регулятора трансмембранной проводимости муковисцидоза (CFTR). [1] Те, у кого есть единственная рабочая копия, являются носителями и в остальном в основном здоровы. [3] CFTR участвует в выработке пота, пищеварительных жидкостей и слизи. [9] Когда CFTR не функционирует, секрет, который обычно жидкий, вместо этого становится густым. [10] Состояние диагностируется с помощью потового теста и генетического тестирования . [1] Тест на пот измеряет концентрацию натрия, поскольку у людей с муковисцидозом пот аномально соленый, вкус которого часто можно почувствовать, когда родители целуют своих детей. Скрининг младенцев при рождении проводится в некоторых регионах мира. [1]
Не существует известного лечения муковисцидоза. [3] Инфекции легких лечат антибиотиками , которые можно вводить внутривенно, ингаляционно или перорально. [1] Иногда антибиотик азитромицин применяют длительное время. [1] Также могут быть полезны ингаляционные гипертонические растворы и сальбутамол . [1] Трансплантация легких может быть вариантом, если функция легких продолжает ухудшаться. [1] Замещение ферментов поджелудочной железы и прием жирорастворимых витаминов важны, особенно у молодых людей. [1] Методы очистки дыхательных путей, такие как физиотерапия грудной клетки , могут иметь некоторую краткосрочную пользу, но долгосрочные эффекты неясны. [11] Средняя продолжительность жизни в развитых странах составляет от 42 до 50 лет , [5] [12] со средним значением 40,7 лет. [13] Проблемы с легкими являются причиной смерти 80% людей с муковисцидозом. [1]
CF наиболее распространен среди людей североевропейского происхождения, у которых он поражает примерно 1 из 3000 новорожденных [1] и среди которых около 1 из 25 человек является носителем. [3] Реже всего оно встречается у африканцев и азиатов, хотя встречается у всех рас . [1] Впервые это заболевание было признано Дороти Андерсен в 1938 году как специфическое заболевание , а описания, соответствующие этому состоянию, появились по крайней мере еще в 1595 году. [8] Название «муковисцидоз» относится к характерному фиброзу и кистам, которые образуют внутри поджелудочной железы . [8] [14]

Муковисцидоз обычно проявляется в раннем возрасте. Новорожденные и младенцы с муковисцидозом, как правило, имеют частый, обильный и жирный стул (результат мальабсорбции ) и имеют недостаточный вес для своего возраста . [15] У 15–20% новорожденных тонкая кишка заблокирована меконием , для исправления которой часто требуется хирургическое вмешательство. [15] У новорожденных иногда возникает неонатальная желтуха из-за закупорки желчных протоков . [15] Дети с муковисцидозом теряют избыток соли с потом, и родители часто замечают кристаллизацию соли на коже или соленый вкус, когда целуют своего ребенка. [15]
Основной причиной заболеваемости и смертности людей с муковисцидозом является прогрессирующее заболевание легких, которое в конечном итоге приводит к дыхательной недостаточности . [16] Обычно это начинается как длительная респираторная инфекция, которая продолжается до тех пор, пока не начато лечение антибиотиками . [16] Хроническая инфекция дыхательных путей почти универсальна у людей с муковисцидозом, причем с течением времени все чаще встречаются Pseudomonas aeruginosa , грибы и микобактерии . [17] Воспаление верхних дыхательных путей приводит к частому насморку и заложенности носа . Полипы носа распространены, особенно у детей и подростков. [16] По мере прогрессирования заболевания у людей появляется одышка и хронический кашель с выделением мокроты . [16] Из-за проблем с дыханием заниматься спортом становится все труднее, а длительная болезнь приводит к тому, что у пострадавших наблюдается недостаточный вес для их возраста. [16] В позднем подростковом или взрослом возрасте у людей начинают развиваться серьезные признаки заболевания легких: свистящее дыхание, удары пальцев , цианоз , кашель с кровью , легочно-сердечная недостаточность и коллапс легкого ( ателектаз или пневмоторакс ). [16]
В редких случаях муковисцидоз может проявляться нарушением свертываемости крови . Витамин К обычно усваивается из грудного молока , молочной смеси, а затем и твердой пищи. Это всасывание нарушено у некоторых пациентов с МВ. Маленькие дети особенно чувствительны к нарушениям всасывания витамина К, поскольку лишь очень небольшое количество витамина К проникает через плаценту, в результате чего у ребенка остаются очень низкие резервы и ограниченная способность усваивать витамин К из пищевых источников после рождения. Поскольку факторы свертывания крови II, VII, IX и X зависят от витамина К, низкий уровень витамина К может привести к проблемам со свертываемостью крови. Следовательно, когда у ребенка появляются необъяснимые синяки, может потребоваться оценка коагуляции, чтобы определить наличие основного заболевания. [18]

Заболевания легких возникают в результате закупорки дыхательных путей из-за накопления слизи, снижения мукоцилиарного клиренса и последующего воспаления . [19] [20] На более поздних стадиях изменения в архитектуре легких, такие как патология основных дыхательных путей ( бронхоэктатическая болезнь ), еще больше усугубляют трудности с дыханием. Другие признаки включают высокое кровяное давление в легких ( легочная гипертензия ), сердечную недостаточность , трудности с поступлением достаточного количества кислорода в организм (гипоксия ) и дыхательную недостаточность, требующую поддержки с помощью дыхательных масок, таких как аппараты двухуровневого положительного давления в дыхательных путях или аппараты искусственной вентиляции легких . [21] Staphylococcus aureus , Haemophilus influenzae и Pseudomonas aeruginosa являются тремя наиболее распространенными микроорганизмами, вызывающими легочные инфекции у пациентов с МВ. [20] : 1254 Кроме того, может возникнуть оппортунистическая инфекция, вызванная комплексом Burkholderia cepacia , особенно при передаче от пациента к пациенту. [22]
Помимо типичных бактериальных инфекций, у людей с МВ чаще развиваются другие виды заболеваний легких. Среди них аллергический бронхолегочный аспергиллез , при котором реакция организма на распространенный гриб Aspergillus fumigatus вызывает ухудшение проблем с дыханием. Другой вариант — заражение комплексом Mycobacterium avium , группой бактерий, связанных с туберкулезом , которые могут вызывать повреждение легких и не реагировать на обычные антибиотики. [23]
Слизь в околоносовых пазухах одинаково густая и может также вызвать закупорку пазух, что приводит к инфекции. Это может вызвать боль в лице, лихорадку, выделения из носа и головные боли . У людей с МВ может развиться чрезмерный разрастание тканей носа ( назальные полипы ) из-за воспаления, вызванного хроническими инфекциями носовых пазух. [24] Рецидивирующие синоназальные полипы могут возникать у 10–25% пациентов с МВ. [20] : 1254 Эти полипы могут блокировать носовые ходы и усугублять трудности с дыханием. [25] [26]
Кардиореспираторные осложнения являются наиболее распространенной причиной смерти (около 80%) пациентов в большинстве центров CF в США. [20] : 1254
Проблемы с пищеварением также распространены у людей с МВ. Примерно у 15–20% новорожденных с диагнозом МВ наблюдается кишечная непроходимость ( мекониевая непроходимость ), а из-за накопления слизи в поджелудочной железе могут возникнуть другие проблемы с пищеварением. [27] Следовательно, происходит нарушение выработки инсулина, что приводит к сахарному диабету, связанному с муковисцидозом. Более того, нарушение транспорта ферментов из поджелудочной железы в кишечник приводит к проблемам с пищеварением, таким как рецидивирующая диарея или потеря веса. [28]
Густая слизь, наблюдаемая в легких, аналогична густым секретам поджелудочной железы — органа, ответственного за выработку пищеварительных соков , которые помогают расщеплять пищу. Эти выделения блокируют экзокринное движение пищеварительных ферментов в двенадцатиперстную кишку и приводят к необратимому повреждению поджелудочной железы, часто с болезненным воспалением ( панкреатит ). [29] В более запущенных случаях протоки поджелудочной железы полностью закупориваются, обычно наблюдаются у детей старшего возраста или подростков. [20] Это вызывает атрофию экзокринных желез и прогрессирующий фиброз. [20]
Кроме того, более распространено выпячивание внутренних оболочек прямой кишки ( выпадение прямой кишки ), встречающееся у 10% детей с МВ [20] и вызванное увеличением объема кала, нарушением питания и повышением внутрибрюшного давления из-за кашляющий. [30]
У людей с CF также возникают трудности с усвоением жирорастворимых витаминов A , D , E и K. [31]
Помимо проблем с поджелудочной железой, люди с МВ чаще страдают изжогой , [31] кишечной непроходимостью вследствие инвагинации и запорами . [32] У пожилых людей с МВ может развиться синдром дистальной кишечной непроходимости , который возникает, когда кал становится густым со слизью ( сгущенным ) и может вызывать вздутие живота, боль и неполную или полную непроходимость кишечника. [33] [31]
Экзокринная недостаточность поджелудочной железы встречается у большинства (85–90%) больных МВ. [20] : 1253 В основном это связано с «тяжелыми» мутациями CFTR, когда оба аллеля полностью нефункциональны (например, ΔF508 /ΔF508). [20] : 1253 Встречается у 10–15% пациентов с одной «тяжелой» и одной «легкой» мутацией CFTR, при которой активность CFTR все еще остается незначительной или существуют две «легкие» мутации CFTR. [20] : 1253 В этих более легких случаях экзокринная функция поджелудочной железы все еще сохраняется, поэтому добавление ферментов не требуется. [20] : 1253 Обычно у фенотипов с достаточной поджелудочной железой не возникает других осложнений со стороны желудочно-кишечного тракта, и в целом такие люди обычно имеют отличный рост и развитие. [20] : 1254 Несмотря на это, идиопатический хронический панкреатит может возникать у части лиц с достаточной поджелудочной железой и МВ и связан с рецидивирующими болями в животе и опасными для жизни осложнениями. [20]
Заболевания печени являются еще одним частым осложнением у пациентов с МВ. Распространенность, наблюдаемая в исследованиях, колебалась от 18% в возрасте двух лет до 41% в возрасте 12 лет без значительного увеличения в дальнейшем. [34] Другое исследование показало, что мужчины с МВ более склонны к заболеваниям печени по сравнению с женщинами, а у пациентов с мекониевой илеусом повышен риск заболеваний печени. [35]
Утолщение секрета также может вызвать проблемы с печенью у пациентов с МВ. Желчь , выделяемая печенью для улучшения пищеварения, может блокировать желчные протоки , что приводит к повреждению печени. Нарушение пищеварения или всасывания липидов может привести к стеаторее . Со временем это может привести к образованию рубцов и узлов ( циррозу печени ). Печень не может очистить кровь от токсинов и не вырабатывает важные белки, например те, которые отвечают за свертывание крови . [36] [37] Заболевания печени являются третьей по частоте причиной смерти, связанной с МВ. [20]
Около 5–7% людей страдают от поражения печени, достаточно серьезного, чтобы вызвать симптомы: обычно камни в желчном пузыре вызывают желчную колику . [38]
Поджелудочная железа содержит островки Лангерганса , которые отвечают за выработку инсулина , гормона, который помогает регулировать уровень глюкозы в крови . Повреждение поджелудочной железы может привести к потере островковых клеток, что приводит к типу диабета, уникальному для людей с этим заболеванием. [39] Этот диабет, связанный с муковисцидозом , имеет общие характеристики с диабетом 1 и 2 типа и является одним из основных нелегочных осложнений МВ. [40]
Витамин D участвует в регуляции кальция и фосфатов . Плохое поступление витамина D из рациона из-за мальабсорбции может привести к заболеванию костей остеопорозу , при котором ослабленные кости более подвержены переломам . [41]
Бесплодию страдают как мужчины, так и женщины. По меньшей мере 97% мужчин с муковисцидозом бесплодны, но не бесплодны и могут иметь детей с помощью вспомогательных репродуктивных технологий. [42] Основной причиной бесплодия у мужчин с муковисцидозом является врожденное отсутствие семявыносящего протока (который обычно соединяет яички с семявыбрасывающими протоками полового члена ), но потенциально также и другие механизмы, вызывающие отсутствие сперматозоидов , сперматозоиды неправильной формы и мало сперматозоидов с плохой подвижностью . [43] Многие мужчины, у которых при обследовании на бесплодие обнаружено врожденное отсутствие семявыносящих протоков, имеют легкую, ранее не диагностированную форму МВ. [44] Хотя женщины с МВ, как правило, фертильны, около 20% женщин с МВ испытывают трудности с фертильностью из-за сгущения цервикальной слизи или недостаточного питания. В тяжелых случаях недостаточное питание нарушает овуляцию и вызывает отсутствие менструации . [45]
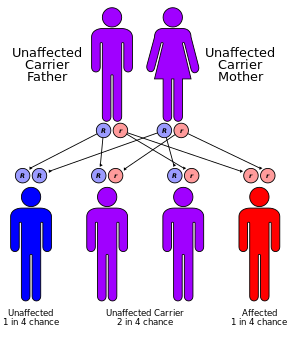
Причиной МВ является отсутствие функциональных копий (аллелей) гена регулятора трансмембранной проводимости муковисцидоза ( CFTR ). По состоянию на 2018 г. описано более 1900 мутаций, приводящих к МВ, но только 5 из них имеют частоту среди пациентов более 1%. Наиболее распространенный мутантный аллель, ΔF508 , представляет собой делецию ( Δ означает делецию) трех нуклеотидов, что приводит к потере аминокислотного остатка фенилаланина (F) в 508-м положении белка. [46] [47] Этот мутантный аллель уже присутствует у 1 из 20–25 человек североевропейского происхождения; на его долю приходится 70% случаев МВ во всем мире и 90% случаев в США ; однако более 700 других мутантных аллелей, некоторые из которых представляют собой новые мутации, могут вызывать МВ. [48] Хотя у большинства людей есть две рабочие копии (аллели) гена CFTR , для предотвращения муковисцидоза необходима только одна. CF развивается, когда ни один из аллелей не может продуцировать функциональный белок CFTR. Таким образом, CF считается аутосомно-рецессивным заболеванием . [49]
Ген CFTR , обнаруженный в локусе q31.2 хромосомы 7 , имеет длину 230 000 пар оснований и кодирует белок длиной 1480 аминокислот . Более конкретно, это место находится между парой оснований 117 120 016 и 117 308 718 на длинном плече хромосомы 7, область 3, полоса 1, поддиапазон 2, представленная как 7q31.2. Структурно CFTR представляет собой тип гена, известный как ген ABC . Продукт этого гена (белок CFTR) представляет собой канал хлорид-ионов, важный для образования пота, пищеварительных соков и слизи. Этот белок обладает двумя АТФ-гидролизующими доменами , что позволяет белку использовать энергию в виде АТФ . Он также содержит два домена, по шесть альфа-спиралей каждый, которые позволяют белку пересекать клеточную мембрану. Регуляторный сайт связывания на белке обеспечивает активацию путем фосфорилирования , главным образом, с помощью цАМФ-зависимой протеинкиназы . [21] Карбоксильный конец белка прикреплен к цитоскелету посредством взаимодействия домена PDZ . [50] Большая часть CFTR в легочных проходах вырабатывается редкими клетками, транспортирующими ионы, которые регулируют свойства слизи. [51]
Кроме того, появляется все больше доказательств того, что генетические модификаторы, помимо CFTR, модулируют частоту и тяжесть заболевания. Одним из примеров является маннан-связывающий лектин , который участвует во врожденном иммунитете , способствуя фагоцитозу микроорганизмов. Полиморфизм в одном или обоих аллелях маннан-связывающего лектина, который приводит к снижению уровня белка в крови, связан с трехкратным увеличением риска терминальной стадии заболевания легких, а также увеличением бремени хронических бактериальных инфекций. [20]
До одного из 25 человек североевропейского происхождения считается генетическим носителем . [52] Заболевание появляется только тогда, когда у двух из этих носителей есть дети, поскольку каждая беременность между ними имеет 25% вероятность рождения ребенка с этим заболеванием. Хотя только один из каждых 3000 новорожденных больных предков страдает МВ, с момента открытия гена CFTR в 1989 году было идентифицировано более 2000 вариантов, но только около 700 из них были признаны ответственными за возникновение МВ. [53] Текущие тесты направлены на выявление наиболее распространенных мутаций. [52]
Мутантные аллели, выявляемые с помощью теста, различаются в зависимости от этнической группы человека или наличия МВ в семье. Более 10 миллионов американцев, в том числе каждый 25-й белый американец, являются носителями одного мутантного аллеля гена CF. CF присутствует и у других рас , хотя и не так часто, как у белых людей. Примерно один из 46 американцев латиноамериканского происхождения, один из 65 афроамериканцев и один из 90 американцев азиатского происхождения являются носителями мутации гена CF. [52]

Ген CFTR регулирует транспорт солей и воды через клеточные мембраны, давая инструкции по созданию пути, позволяющего проходить ионам хлорида. [54] Мутация гена CFTR может нарушить нормальную функцию хлоридных каналов, что приведет к аномальному транспорту ионов хлорида и воды, что приведет к образованию густой и аномальной слизи. [55]
Могут возникнуть несколько мутаций в гене CFTR , и разные мутации вызывают различные дефекты белка CFTR, иногда вызывая более легкое или более тяжелое заболевание. Эти белковые дефекты также являются мишенью для лекарств, которые иногда могут восстановить их функцию. Мутация гена ΔF508-CFTR , которая встречается у более чем 90% пациентов в США, создает белок, который не сворачивается нормально и не транспортируется должным образом к клеточной мембране, что приводит к ее деградации. [56]
Другие мутации приводят к тому, что белки становятся слишком короткими (усеченными), поскольку их производство прекращается преждевременно. Другие мутации производят белки, которые обычно не используют энергию (в форме АТФ), не позволяют хлориду, йодиду и тиоцианату пересекать мембрану должным образом [57] и деградируют быстрее, чем обычно. Мутации также могут привести к образованию меньшего количества копий белка CFTR. [21]
Белок, созданный этим геном, закрепляется на внешней мембране клеток потовых желез , легких, поджелудочной железы и всех остальных экзокринных желез в организме. Белок охватывает эту мембрану и действует как канал , соединяющий внутреннюю часть клетки ( цитоплазму ) с окружающей жидкостью . Этот канал в первую очередь отвечает за контроль движения галогенид-анионов изнутри наружу клетки; однако в потовых протоках он облегчает перемещение хлоридов из потовых протоков в цитоплазму. Когда белок CFTR не резорбирует ионы в потовых протоках, хлорид и тиоцианат [58], выделяемые из потовых желез, задерживаются внутри протоков и перекачиваются в кожу.
Кроме того , гипотиоцианит OSCN не может вырабатываться системой иммунной защиты. [59] [60] Поскольку хлорид заряжен отрицательно , это изменяет электрический потенциал внутри и снаружи клетки, что обычно приводит к проникновению катионов в клетку. Натрий является наиболее распространенным катионом во внеклеточном пространстве. Избыток хлоридов в потовых протоках предотвращает резорбцию натрия эпителиальными натриевыми каналами, а сочетание натрия и хлорида создает соль, которая теряется в больших количествах с потом у людей с МВ. Эта потерянная соль составляет основу теста пота. [21]
Большая часть повреждений при МВ обусловлена закупоркой узких проходов пораженных органов сгущенным секретом. Эти закупорки приводят к ремоделированию и инфекции легких, повреждению накопленными пищеварительными ферментами в поджелудочной железе, закупорке кишечника густыми фекалиями и т. д. Было выдвинуто несколько теорий о том, как дефекты белковой и клеточной функции вызывают клинические эффекты. Самая современная теория предполагает, что нарушение транспорта ионов приводит к обезвоживанию эпителия дыхательных путей, что приводит к сгущению слизи. [61] В эпителиальных клетках дыхательных путей реснички существуют между апикальной поверхностью клетки и слизью в слое, известном как поверхностная жидкость дыхательных путей (ASL). Поток ионов из клетки в этот слой определяется ионными каналами, такими как CFTR. CFTR не только позволяет ионам хлора вытягиваться из клетки в ASL, но также регулирует другой канал, называемый ENac, который позволяет ионам натрия покидать ASL и проникать в респираторный эпителий. CFTR обычно ингибирует этот канал, но если CFTR неисправен, натрий свободно течет из ASL в клетку. [ нужна цитата ]
Поскольку вода следует за натрием, глубина ASL будет истощена и реснички останутся в слизистом слое. [62] Поскольку реснички не могут эффективно двигаться в густой, вязкой среде, мукоцилиарный клиренс недостаточен и происходит накопление слизи, закупоривающие мелкие дыхательные пути. [63] Накопление более вязкой, богатой питательными веществами слизи в легких позволяет бактериям скрываться от иммунной системы организма, вызывая повторные респираторные инфекции. Присутствие тех же белков CFTR в протоках поджелудочной железы и потовых железах кожи также вызывает симптомы в этих системах. [ нужна цитата ]
Легкие людей с муковисцидозом колонизируются и инфицируются бактериями с раннего возраста. Эти бактерии, которые часто распространяются среди людей с МВ, процветают в измененной слизи, которая скапливается в мелких дыхательных путях легких. Эта слизь приводит к образованию бактериальной микросреды, известной как биопленки , в которую трудно проникнуть иммунным клеткам и антибиотикам. Вязкие выделения и стойкие респираторные инфекции неоднократно повреждают легкие, постепенно ремоделируя дыхательные пути, что еще больше затрудняет искоренение инфекции. [64] Естественная история легочных инфекций CF и ремоделирования дыхательных путей плохо изучена, в основном из-за огромной пространственной и временной гетерогенности как внутри, так и между микробиомами пациентов с CF. [65]
С течением времени у людей с МВ изменяются как типы бактерий, так и их индивидуальные характеристики. На начальной стадии распространенные бактерии, такие как S. aureus и H. influenzae, колонизируют и инфицируют легкие. [20] В конце концов, Pseudomonas aeruginosa (а иногда и Burkholderia cepacia ) доминирует. К 18 годам 80% пациентов с классическим МВ являются носителями P. aeruginosa и 3,5% – B. cepacia . [20] Попадая в легкие, эти бактерии адаптируются к окружающей среде и развивают устойчивость к широко используемым антибиотикам. Pseudomonas может развивать особые характеристики, которые позволяют образовывать большие колонии, известные как «мукоидные» Pseudomonas , которые редко наблюдаются у людей, не болеющих МВ. [64] Научные данные свидетельствуют о том, что путь интерлейкина 17 играет ключевую роль в резистентности и модуляции воспалительного ответа во время инфекции P. aeruginosa при МВ. [66] В частности, иммунитет, опосредованный интерлейкином-17, играет обоюдоострую активность во время хронической инфекции дыхательных путей; с одной стороны, он способствует контролю нагрузки P. aeruginosa , а с другой, способствует усилению легочной нейтрофилии и ремоделированию тканей. [66]
Инфекция может распространяться при передаче от одного человека к другому, больному МВ. [67] В прошлом люди с МВ часто участвовали в летних «лагерях МВ» и других развлекательных мероприятиях. [68] [69] В больницах пациенты с МВ группировались в общие помещения, а обычное оборудование (например, небулайзеры ) [70] не подвергалось стерилизации между отдельными пациентами. [71] Это привело к передаче более опасных штаммов бактерий среди групп пациентов. В результате людей с МВ теперь регулярно изолируют друг от друга в медицинских учреждениях, а медицинским работникам рекомендуется носить халаты и перчатки при обследовании пациентов с МВ, чтобы ограничить распространение вирулентных бактериальных штаммов. [72]
У пациентов с МВ дыхательные пути также могут быть хронически колонизированы нитчатыми грибами (такими как Aspergillus fumigatus , Scedosporium apiospermum , Aspergillus terreus ) и/или дрожжами (такими как Candida albicans ); другие нитчатые грибы, выделяемые реже, включают Aspergillus flavus и Aspergillus nidulans (временно встречаются в респираторных секретах CF), а также Exophiala dermatitidis и Scedosporium prolificans (хронические колонизаторы дыхательных путей); некоторые нитчатые грибы, такие как Penicillium emersonii и Acrophialophora fusispora, встречаются у пациентов почти исключительно при МВ. [73] Нарушение мукоцилиарного клиренса, характеризующее МВ, связано с местными иммунологическими нарушениями. Кроме того, длительная терапия антибиотиками и применение кортикостероидов также могут способствовать росту грибков. Хотя клиническая значимость грибковой колонизации дыхательных путей до сих пор остается предметом дискуссий, мицелиальные грибы могут способствовать местной воспалительной реакции и, следовательно, прогрессирующему ухудшению функции легких, как это часто бывает при аллергическом бронхолегочном аспергиллезе – наиболее распространенном грибковом заболевании в легких. контексте МВ, включающем Th2-зависимый иммунный ответ на виды Aspergillus . [73] [74]

Диагноз МВ первоначально основывается на клинических данных, указывающих на респираторные заболевания, различные проблемы с пищеварением, мекониевую непроходимость и многое другое. Окончательный диагноз может включать генетическое тестирование на основе семейного анамнеза или определение концентрации хлоридов в поту, которая у лиц с МВ относительно высока (>60 мэкв/л).
Во многих населенных пунктах всех новорожденных проверяют на муковисцидоз в течение первых нескольких дней жизни, обычно с помощью анализа крови на высокий уровень иммунореактивного трипсиногена . [75] Новорожденные с положительными тестами или те, у кого есть иное подозрение на муковисцидоз на основании симптомов или семейного анамнеза, затем проходят тест на пот . Электрический ток используется для введения пилокарпина в кожу, стимулируя потоотделение. Пот собирается и анализируется на уровень соли. Необычно высокий уровень хлоридов в поте указывает на дисфункцию CFTR ; затем человеку ставят диагноз муковисцидоз. [76] [примечание 1] Также доступно генетическое тестирование для выявления мутаций CFTR, обычно связанных с муковисцидозом. Многие лаборатории могут проверить 30–96 наиболее распространенных мутаций CFTR, которые позволяют выявить более 90% людей с муковисцидозом. [76]
У людей с МВ меньше тиоцианата и гипотиоцианита в слюне [78] и слизи (Banfi et al.). В случае более легких форм МВ могут быть полезны измерения трансэпителиальной разности потенциалов . МВ также можно диагностировать путем выявления мутаций в гене CFTR. [79]
Во многих случаях родители ставят диагноз, потому что у ребенка соленый вкус. [20] Уровни иммунореактивного трипсиногена могут быть повышены у людей, имеющих одну мутированную копию гена CFTR (носители) или, в редких случаях, у людей с двумя нормальными копиями гена CFTR . Из-за этих ложноположительных результатов скрининг новорожденных на МВ может быть спорным. [80] [81]
К 2010 году в каждом штате США были введены программы скрининга новорожденных [82] , а по состоянию на 2016 год [обновлять]21 европейская страна имела такие программы, по крайней мере, в некоторых регионах. [83]
Беременные женщины или пары, планирующие беременность, могут сами пройти тестирование на мутации гена CFTR , чтобы определить риск рождения их ребенка с МВ. Обычно сначала тестирование проводится у одного или обоих родителей, а если риск МВ высок, проводится тестирование на плоде. Американский колледж акушеров и гинекологов рекомендует всем людям, планирующим беременность, пройти тестирование на предмет того, являются ли они носителями. [84]
Поскольку для развития CF у плода требуется, чтобы каждый родитель передал мутированную копию гена CFTR , а тестирование на CF является дорогостоящим, тестирование часто сначала проводится на одном родителе. Если тестирование показывает, что родитель является носителем мутации гена CFTR , другого родителя проверяют, чтобы рассчитать риск того, что у его детей будет МВ. МВ может возникнуть в результате более чем тысячи различных мутаций. [49] По состоянию на 2016 год [обновлять]обычно проверяются только наиболее распространенные мутации, такие как ΔF508. [49] Большинство коммерчески доступных тестов выявляют 32 или менее различных мутаций. Если в семье есть известная необычная мутация, можно провести специальный скрининг на эту мутацию. Поскольку не все известные мутации обнаруживаются в ходе текущих тестов, отрицательный результат скрининга не гарантирует, что у ребенка не будет МВ. [85]
Во время беременности тестирование можно проводить на плаценте ( взятие ворсинок хориона ) или жидкости вокруг плода ( амниоцентез ). Однако при взятии пробы ворсин хориона риск внутриутробной смерти составляет один из 100, а амниоцентез - в одном из 200; [86] недавнее исследование показало, что этот показатель может быть намного ниже, примерно один на 1600. [87]
С экономической точки зрения для пар-носителей муковисцидоза при сравнении преимплантационной генетической диагностики (ПГД) с естественным зачатием (НК) с последующим пренатальным тестированием и абортом пораженной беременности ПГД обеспечивает чистую экономическую выгоду до возраста матери около 40 лет, после чего НК , пренатальное тестирование и аборты имеют более высокую экономическую выгоду. [88]
Лечение МВ разнообразно, адаптировано к различным симптомам и включает в себя различные устройства, ингаляционные препараты для облегчения респираторных затруднений, пероральные ферментные добавки для устранения экзокринной недостаточности поджелудочной железы и, в некоторых случаях, хирургические вмешательства при таких состояниях, как мекониевая непроходимость. [89] Хотя лечение облегчает симптомы и предотвращает потенциальные осложнения, в настоящее время лекарства от этой болезни не существует.
Управление МВ значительно улучшилось за последние 70 лет. В то время как младенцы, родившиеся с этим заболеванием 70 лет назад, вряд ли дожили бы до первого года, современные младенцы, скорее всего, доживут до зрелого возраста. Достижения в лечении муковисцидоза привели к тому, что люди с муковисцидозом могут жить более полноценной жизнью, менее обремененной своим заболеванием. Краеугольными камнями лечения являются превентивное лечение инфекции дыхательных путей , поощрение правильного питания и активного образа жизни. Легочная реабилитация как лечение МВ продолжается на протяжении всей жизни человека и направлена на максимальное улучшение функции органа и, следовательно, качества жизни. [90] Эрготерапевты используют методы энергосбережения в процессе реабилитации пациентов с муковисцидозом. [91] Примерами методов энергосбережения являются эргономические принципы, дыхание через сжатые губы и диафрагмальное дыхание. [92] Люди с МВ, как правило, испытывают утомляемость и одышку из-за хронических легочных инфекций, поэтому уменьшение количества энергии, затрачиваемой во время деятельности, может помочь людям чувствовать себя лучше и обрести большую независимость. [91] Современные методы лечения в лучшем случае замедляют ухудшение функции органов. [ нужна ссылка ] Из-за большого разнообразия симптомов заболевания лечение обычно проводится в специализированных многопрофильных центрах и подбирается индивидуально. Объектами терапии являются легкие, желудочно-кишечный тракт (включая добавки ферментов поджелудочной железы), репродуктивные органы (включая вспомогательные репродуктивные технологии ) и психологическая поддержка. [93]
Наиболее последовательным аспектом терапии МВ является ограничение и лечение повреждений легких, вызванных густой слизью и инфекцией, с целью поддержания качества жизни . Внутривенные , ингаляционные и пероральные антибиотики используются для лечения хронических и острых инфекций. Механические устройства и ингаляционные препараты используются для изменения и очищения загустевшей слизи. Эти методы лечения, хотя и эффективны, могут занять чрезвычайно много времени. Кислородная терапия в домашних условиях рекомендуется людям со значительным низким уровнем кислорода. [94] Многие люди с МВ используют пробиотики , которые, как считается, способны корректировать дисбактериоз и воспаление кишечника, но данные клинических испытаний относительно эффективности пробиотиков для снижения легочных обострений у людей с МВ неопределенны. [95]
Многие люди с МВ постоянно принимают один или несколько антибиотиков, даже когда они здоровы, для профилактического подавления инфекции. Выбор антибиотиков при муковисцидозе зависит от конкретных бактерий, вызывающих инфекцию, а также от возраста, веса и состояния пациента. и другие медицинские условия. [ нужна цитата ] Антибиотики абсолютно необходимы всякий раз, когда подозревается пневмония или наблюдается заметное снижение функции легких, и обычно их выбирают на основе результатов анализа мокроты и прошлой реакции человека. [ нужна цитация ] Эта длительная терапия часто требует госпитализации и установки более постоянной внутривенной инъекции , такой как периферически вставленный центральный катетер или порт-катетер . Ингаляционная терапия антибиотиками, такими как тобрамицин , колистин и азтреонам , часто назначается в течение нескольких месяцев для улучшения функции легких путем предотвращения роста колонизированных бактерий. [96] [97] [98] Ингаляционная антибиотикотерапия помогает функции легких, борясь с инфекцией, но имеет и существенные недостатки, такие как развитие устойчивости к антибиотикам, шум в ушах и изменения голоса. [99] Ингаляционный левофлоксацин можно использовать для лечения Pseudomonas aeruginosa у инфицированных людей с муковисцидозом. [100]
Антибиотики для перорального применения, такие как ципрофлоксацин или азитромицин, назначаются для предотвращения инфекции или для контроля текущей инфекции. [101] Используемые аминогликозидные антибиотики (например, тобрамицин) могут вызвать потерю слуха , повреждение системы баланса внутреннего уха или почечную недостаточность при длительном применении. [102] Чтобы предотвратить эти побочные эффекты , количество антибиотиков в крови регулярно измеряется и соответствующим образом корректируется. [103]
В настоящее время нет надежных данных клинических исследований, подтверждающих эффективность антибиотиков при обострениях легких у людей с муковисцидозом и комплексом Burkholderia cepacia [104] или при использовании антибиотиков для лечения нетуберкулезных микобактерий у людей с МВ. [105]
Для раннего лечения инфекции Pseudomonas aeruginosa обычно предлагается использовать распыляемые антибиотики с пероральными антибиотиками или без них для удаления бактерий из дыхательных путей человека на определенный период времени. [106] При выборе антибиотиков для лечения легочных инфекций, вызванных Pseudomonas aeruginosa , у людей с муковисцидозом до сих пор неясно, должен ли выбор антибиотиков основываться на результатах тестирования антибиотиков отдельно (по одному) или в сочетании с каждым из них. другой. [107] Также неясно, улучшают ли эти подходы к лечению инфекции Pseudomonas aeruginosa качество жизни или продолжительность жизни человека. [106] Отрицательные побочные эффекты антибиотиков при этой инфекции также недостаточно изучены. [106] Было показано , что внутривенная антибиотикотерапия для лечения инфекций, вызванных Pseudomonas aeruginosa, не лучше, чем антибиотики, принимаемые перорально. [106]
Инфекции , вызванные метициллин-резистентным золотистым стафилококком (MRSA), могут быть опасны для людей с муковисцидозом и могут усугубить повреждение легких, что приведет к более быстрому снижению заболеваемости. Раннее лечение антибиотиками является стандартным; однако необходимы дальнейшие исследования для определения долгосрочных эффектов и преимуществ (3–6 месяцев после лечения или дольше), а также показателей выживаемости, связанных с различными вариантами лечения. [108]
Факторы, связанные с применением антибиотиков, хроническим течением заболевания и появлением резистентных бактерий, требуют более тщательного изучения различных стратегий, таких как адъювантная антибиотикотерапия . [109] Антибиотико-адъювантная терапия относится к терапевтическим подходам, целью которых является улучшение действия антибиотиков, таких как фармацевтические агенты или добавки, которые влияют на вирулентность бактерии или изменяют восприимчивость организма к антибиотику, чтобы антибиотики были более эффективными. [109] Нет убедительных доказательств, позволяющих рекомендовать конкретные адъювантные антибиотики, такие как β-каротин , оксид азота , добавки цинка или KB001-A. [109]
Аэрозольные лекарства, которые помогают ослабить секрецию, включают дорназу альфа и гипертонический физиологический раствор . [110] Дорназа представляет собой рекомбинантную человеческую дезоксирибонуклеазу , которая расщепляет ДНК в мокроте, тем самым уменьшая ее вязкость. [111] Дорназа альфа улучшает функцию легких и, вероятно, снижает риск обострений, но недостаточно доказательств, чтобы узнать, является ли она более или менее эффективной, чем другие аналогичные лекарства. [112] Дорназа альфа может улучшить функцию легких; однако нет убедительных доказательств того, что он лучше других гиперосмолярных методов лечения. [112]
Денуфозол , исследуемый препарат, открывает альтернативный хлоридный канал, помогая разжижать слизь. [113] Неясно, полезны ли ингаляционные кортикостероиды , но прекращение терапии ингаляционными кортикостероидами безопасно. [114] Имеются слабые доказательства того, что лечение кортикостероидами может причинить вред, препятствуя росту. [114] По состоянию на 2014 год вакцинация против пневмококка не изучалась [обновлять]. [115] По состоянию на 2014 год [обновлять]в результате рандомизированных контролируемых исследований не было четких доказательств того, что вакцина против гриппа полезна для людей с муковисцидозом. [116]
Ивакафтор — это препарат, принимаемый перорально для лечения МВ из-за ряда специфических мутаций, реагирующих на индуцированное ивакафтором усиление белка CFTR. [117] [118] Он улучшает функцию легких примерно на 10%; однако по состоянию на 2014 год [обновлять]это дорого. [117] В первый год его появления на рынке прейскурантная цена в США превышала 300 000 долларов в год. [117] [ нужна обновленная информация ] В июле 2015 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило люмакафтор/ивакафтор . [119] В 2018 году FDA одобрило комбинацию ивакафтор/тезакафтор ; Производитель объявил прейскурантную цену в 292 000 долларов в год. [120] Тезакафтор помогает переместить белок CFTR в правильное положение на поверхности клетки и предназначен для лечения людей с мутацией F508del . [121]
В 2019 году комбинированный препарат элексакафтор/ивакафтор/тезакафтор, продаваемый в США под названием Трикафта , был одобрен для лечения пациентов с МВ старше 12 лет . [122] [123] В 2021 году его действие было расширено и теперь включает пациентов старше 6 лет. [124] В Европе этот препарат был одобрен в 2020 году и продается как Кафтрио . [125] Он используется у пациентов с мутацией f508del, которая встречается примерно у 90% пациентов с муковисцидозом. [122] [126] По данным Фонда муковисцидоза , «это лекарство представляет собой величайшее терапевтическое достижение в истории МВ, предлагая лечение основной причины заболевания, которое в конечном итоге может обеспечить модуляторную терапию 90 процентам людей с муковисцидозом». КФ». [127] В клиническом исследовании у участников, которым вводили комбинированный препарат, наблюдалось последующее снижение легочных обострений на 63% и снижение концентрации хлоридов в поте на 41,8 ммоль/л. [128] Смягчая набор симптомов, связанных с муковисцидозом, комбинированный препарат также значительно улучшил показатели качества жизни среди пациентов с этим заболеванием. [128] [127] Также известно, что комбинированный препарат взаимодействует с индукторами CYP3A, [129] такими как карбамазепин, используемый при лечении биполярного расстройства, вызывая циркуляцию элексафтора/ивакафтора/тезакафтора в организме в пониженных концентрациях. Таким образом, одновременное применение не рекомендуется. [130] Прейскурантная цена в США составит 311 000 долларов в год; [131] однако страховка может покрыть большую часть стоимости препарата. [132]
Использовалась желчная соль урсодезоксихолевой кислоты ; однако данных недостаточно, чтобы показать, является ли он эффективным. [133]
Неизвестно, влияют ли добавки витамина А или бета-каротина на проблемы с глазами и кожей, вызванные дефицитом витамина А. [134]
Нет убедительных доказательств того, что люди с муковисцидозом могут предотвратить остеопороз , увеличив потребление витамина D. [135]
Есть данные, что у людей с дефицитом витамина Е и муковисцидозом прием добавок витамина Е может повысить уровень витамина Е, хотя до сих пор неясно, какое влияние добавки оказывают на расстройства, связанные с дефицитом витамина Е, или на функцию легких. [136]
По состоянию на 2020 год убедительных данных о влиянии добавок витамина К на людей с муковисцидозом нет. [137]
В различных исследованиях изучалось влияние добавок жирных кислот омега-3 на людей с муковисцидозом, но данные неясны, есть ли у них какие-либо преимущества или побочные эффекты. [138]
Для вытеснения мокроты и стимулирования ее отхаркивания используются несколько механических методов. Одним из методов, подходящих для кратковременного очищения дыхательных путей, является физиотерапия грудной клетки , при которой респираторный терапевт перкустирует грудную клетку человека несколько раз в день, чтобы разжижить выделения. Этот «ударный эффект» можно также осуществлять с помощью специальных устройств, использующих колебание грудной клетки , или внутрилегочного перкуссионного аппарата искусственной вентиляции легких . Другие методы, такие как двухфазная кирасная вентиляция и соответствующий режим очистки, доступные в таких устройствах, включают фазу облегчения кашля, а также фазу вибрации для вытеснения выделений. Они портативны и адаптированы для домашнего использования. [11]
Другой метод — это физиотерапия с положительным давлением на выдохе, которая заключается в создании противодавления в дыхательных путях во время выдоха. Этот эффект обеспечивают устройства, состоящие из маски или мундштука, в которых сопротивление применяется только на фазе выдоха. [139] Принцип действия этого метода, по-видимому, заключается в увеличении давления газа позади слизи посредством коллатеральной вентиляции наряду с временным увеличением функциональной остаточной емкости, предотвращающей ранний коллапс мелких дыхательных путей во время выдоха. [140] [141]
По мере обострения заболевания легких может возникнуть необходимость в механической поддержке дыхания. Людям с МВ, возможно, придется носить специальные маски в ночное время, чтобы облегчить поступление воздуха в легкие. Эти аппараты, известные как аппараты двухуровневого положительного давления в дыхательных путях (BiPAP), помогают предотвратить низкий уровень кислорода в крови во время сна. Неинвазивные аппараты искусственной вентиляции легких можно использовать во время физиотерапии для улучшения выведения мокроты. [142] Неизвестно, влияет ли этот тип терапии на обострения легких или прогрессирование заболевания. [142] Неизвестно, какую роль неинвазивная вентиляционная терапия играет в улучшении способности к физической нагрузке у людей с муковисцидозом. [142] Однако авторы отметили, что «неинвазивная вентиляция может быть полезным дополнением к другим методам очистки дыхательных путей, особенно у людей с муковисцидозом, у которых возникают трудности с отхаркиванием мокроты». [143] При тяжелом заболевании в горло можно вставить трубку (процедура, известная как трахеостома ), чтобы обеспечить дыхание при поддержке аппарата искусственной вентиляции легких. [144] [145]
Предварительные исследования показывают, что массажная терапия для детей может улучшить качество жизни людей и их семей. [146]
Некоторые инфекции легких требуют хирургического удаления инфицированной части легкого. Если это необходимо многократно, функция легких резко снижается. [147] Наиболее эффективные варианты лечения людей с МВ со спонтанным или рецидивирующим пневмотораксом не ясны. [148]
Трансплантация легких может стать необходимой для людей с МВ, поскольку функция легких и толерантность к физической нагрузке снижаются. Хотя трансплантация одного легкого возможна и при других заболеваниях, людям с МВ необходимо заменить оба легких, поскольку оставшееся легкое может содержать бактерии, которые могут инфицировать трансплантированное легкое. Трансплантация поджелудочной железы или печени может быть выполнена одновременно для облегчения заболевания печени и/или диабета. [149] Трансплантация легких рассматривается, когда функция легких снижается до такой степени, что требуется помощь механических устройств или чье-либо выживание находится под угрозой. [150] Согласно Руководству компании Merck , «двусторонняя трансплантация легких при тяжелом заболевании легких становится все более рутинной и успешной благодаря опыту и усовершенствованным методам. Среди взрослых с МВ медиана выживаемости после трансплантации составляет около 9 лет». [151]

Новорожденным с кишечной непроходимостью обычно требуется хирургическое вмешательство, тогда как взрослым с синдромом дистальной кишечной непроходимости обычно этого не требуется. Лечение недостаточности поджелудочной железы путем замены недостающих пищеварительных ферментов позволяет двенадцатиперстной кишке правильно усваивать питательные вещества и витамины, которые в противном случае были бы потеряны с калом. Однако оптимальная дозировка и форма замены ферментов поджелудочной железы неясны, как и риски и долгосрочная эффективность этого лечения. [152]
До настоящего времени не проводилось масштабных исследований, посвященных заболеваемости атеросклерозом и ишемической болезнью сердца у взрослых, больных муковисцидозом. Вероятно, это связано с тем, что подавляющее большинство людей с муковисцидозом не живут достаточно долго, чтобы у них развился клинически значимый атеросклероз или ишемическая болезнь сердца. [153]
Диабет является наиболее частым нелегочным осложнением МВ. Он сочетает в себе признаки диабета 1-го и 2-го типа и признан отдельным заболеванием — диабетом, связанным с муковисцидозом . [40] [154] Хотя иногда используются пероральные противодиабетические препараты , рекомендуемым лечением являются инъекции инсулина или инсулиновая помпа , [155] и, в отличие от диабета 1 и 2 типа, диетические ограничения не рекомендуются. [40] Хотя Stenotropomonasmaltophilia относительно часто встречается у людей с муковисцидозом, данные об эффективности антибиотиков против S.maltophilia неопределенны. [156]
Бисфосфонаты, принимаемые перорально или внутривенно , могут использоваться для улучшения минеральной плотности костей у людей с муковисцидозом, но нет никаких доказательств того, что это уменьшает количество переломов или увеличивает выживаемость. [157] При внутривенном приеме бисфосфатов могут возникнуть побочные эффекты , такие как боль и симптомы гриппа. [157] Побочные эффекты перорального приема бисфосфатов на желудочно-кишечный тракт неизвестны. [157]
Плохого роста можно избежать, вставив зонд для кормления для увеличения энергии пищи за счет дополнительного кормления или путем введения гормона роста . [158]
Инфекции носовых пазух лечатся длительными курсами антибиотиков. Развитие полипов носа или других хронических изменений в носовых ходах может серьезно ограничить поток воздуха через нос и со временем ухудшить обоняние человека. Хирургия носовых пазух часто используется для облегчения заложенности носа и ограничения дальнейших инфекций. Назальные стероиды, такие как флутиказона пропионат , используются для уменьшения воспаления носа. [159]
Женское бесплодие можно преодолеть с помощью технологий вспомогательной репродукции , особенно методов переноса эмбрионов . Мужское бесплодие, вызванное отсутствием семявыносящих протоков, можно преодолеть с помощью экстракции сперматозоидов из яичек , собирая сперматозоиды непосредственно из яичек. Если собранный образец содержит слишком мало сперматозоидов для вероятного спонтанного оплодотворения, можно выполнить интрацитоплазматическую инъекцию сперматозоидов . [160] Репродукция третьим лицом также возможна для женщин с МВ. Неясно, влияет ли прием антиоксидантов на результаты. [161]
Физические упражнения обычно являются частью амбулаторного лечения людей с муковисцидозом. [162] Аэробные упражнения, по-видимому, полезны для аэробной способности к нагрузкам, функции легких и качества жизни, связанного со здоровьем; однако качество доказательств было плохим. [162]
Из-за использования аминогликозидных антибиотиков часто наблюдается ототоксичность. Симптомы могут включать «шум в ушах, потерю слуха, гиперакузия, заложенность слуха, головокружение и головокружение». [163]
Проблемы с желудочно-кишечной системой, включая запоры и непроходимость желудочно-кишечного тракта, включая синдром дистальной кишечной непроходимости, являются частыми осложнениями для людей с муковисцидозом. [33] Лечение желудочно-кишечных проблем необходимо для предотвращения полной непроходимости, уменьшения других симптомов МВ и улучшения качества жизни. [33] Хотя часто предлагаются размягчители стула, слабительные и прокинетики (лечение, ориентированное на желудочно-кишечный тракт), среди экспертов нет четкого консенсуса относительно того, какой подход является лучшим и сопряжен с наименьшими рисками. [33] Для улучшения симптомов иногда также предлагаются муколитики или системное лечение, направленное на дисфункцию CFTR. [164]
Прогноз при муковисцидозе улучшился благодаря более ранней диагностике посредством скрининга, а также более качественному лечению и доступу к медицинской помощи. В 1959 г. средний возраст выживания детей с МВ в США составлял шесть месяцев. [165] В 2010 году продолжительность жизни оценивается в 37 лет для женщин и 40 лет для мужчин. [166] В Канаде медиана выживаемости увеличилась с 24 лет в 1982 году до 47,7 в 2007 году. [167] В США у тех, кто родился с МВ в 2016 году, прогнозируемая продолжительность жизни составляет 47,7 лет при уходе за ними в специализированных клиниках. [168]
В США среди людей с муковисцидозом, которым исполнилось 18 лет по состоянию на 2009 год, 92% окончили среднюю школу, 67% имели хотя бы некоторое высшее образование, 15% были инвалидами, 9% были безработными, 56% были одинокими. , а 39% состояли в браке или жили с партнером. [169]
С хроническими заболеваниями сложно справиться. МВ — это хроническое заболевание, поражающее «пищеварительные и дыхательные пути, приводящее к генерализованному недоеданию и хроническим респираторным инфекциям». [170] Густые выделения закупоривают дыхательные пути легких, что часто вызывает воспаление и тяжелые инфекции легких. [171] [172] Если он нарушен, это влияет на качество жизни человека с МВ и его способность выполнять такие задачи, как повседневная работа. [ нужна цитата ]
По мнению Шмитца и Голдбека (2006), МВ значительно увеличивает эмоциональный стресс как у человека, так и у семьи, «а необходимое трудоемкое ежедневное лечение может иметь дальнейшие негативные последствия для качества жизни». [173] Однако Хаверманс и коллеги (2006) установили, что молодые амбулаторные пациенты с МВ, принявшие участие в пересмотренном опроснике по муковисцидозу, «оценили некоторые области качества жизни выше, чем их родители». [174] Следовательно, амбулаторные пациенты с МВ имеют более позитивный прогноз о себе. Как отмечается в Руководстве Merck , «при соответствующей поддержке большинство пациентов могут адаптироваться к возрасту дома и в школе. Несмотря на множество проблем, образовательные, профессиональные и семейные успехи пациентов впечатляют». [151]
Более того, существует множество способов улучшить качество жизни пациентов с МВ. Упражнения способствуют улучшению функции легких. Включение режима физических упражнений в распорядок дня пациента с МВ может значительно улучшить качество жизни. [175] Никакого окончательного лечения МВ не известно, но используются различные лекарства, такие как муколитики, бронхолитики, стероиды и антибиотики, целью которых является разжижение слизи, расширение дыхательных путей, уменьшение воспаления и борьба с легочными инфекциями соответственно. [176]
Муковисцидоз является наиболее распространенным ограничивающим жизнь аутосомно-рецессивным заболеванием среди людей европейского происхождения. [178] В США около 30 000 человек страдают МВ; большинство из них диагностируются в возрасте шести месяцев. В Канаде около 4000 человек страдают МВ. [179] Примерно 1 из 25 человек европейского происхождения и каждый 30 белых американцев [180] являются носителями мутации CF. Хотя МВ менее распространен в этих группах, примерно один из 46 латиноамериканцев , один из 65 африканцев и один из 90 азиатов являются носителями по крайней мере одного аномального гена CFTR . [181] [182] В Ирландии самый высокий в мире уровень распространенности МВ: один на 1353. [183]
Хотя технически это редкое заболевание, МВ считается одним из наиболее распространенных генетических заболеваний, сокращающих жизнь. Это наиболее распространено среди стран западного мира. Исключением является Финляндия , где только один из 80 человек является носителем мутации CF. [184] Всемирная организация здравоохранения заявляет: «В Европейском Союзе один из 2000–3000 новорожденных страдает МВ». [185] В США один из 3500 детей рождается с МВ. [186] В 1997 году примерно один из 3300 белых детей в США родился с МВ. Напротив, только у одного из 15 000 афроамериканских детей он есть, а среди американцев азиатского происхождения этот показатель был еще ниже – один из 32 000. [187]
Муковисцидоз диагностируется одинаково у мужчин и женщин. По причинам, которые остаются неясными, данные показали, что мужчины, как правило, имеют более высокую продолжительность жизни, чем женщины, [188] [189] , хотя недавние исследования показывают, что этого гендерного разрыва, возможно, больше не существует, возможно, из-за улучшений в медицинских учреждениях. [190] [191] Недавнее исследование, проведенное в Ирландии, выявило связь между женским гормоном эстрогеном и худшими исходами при МВ. [192]
Распределение аллелей CF варьируется среди популяций. Частота носителей ΔF508 оценивается в один из 200 в северной Швеции, один из 143 среди литовцев и один из 38 в Дании. Носителей ΔF508 не обнаружено среди 171 финна и 151 саами . [193] ΔF508 действительно встречается в Финляндии, но там это миноритарный аллель. Известно, что CF встречается только в 20 семьях (родословных) в Финляндии. [194]
По оценкам, мутация ΔF508 произошла около 52 000 лет назад. [195] Было выдвинуто множество гипотез относительно того, почему такой летальный аллель сохранился и распространился в человеческой популяции. Было обнаружено , что другие распространенные аутосомно-рецессивные заболевания, такие как серповидно-клеточная анемия , защищают носителей от других заболеваний - эволюционный компромисс , известный как преимущество гетерозигот . В качестве возможных источников преимущества гетерозигот была предложена устойчивость к следующим факторам:

Предполагается, что МВ возник около 3000 г. до н. э. в результате миграции народов, генных мутаций и новых условий питания. [205] Хотя весь клинический спектр МВ не был известен до 1930-х годов, некоторые аспекты МВ были выявлены гораздо раньше. Действительно, литература Германии и Швейцарии XVIII века предупреждала: «Wehe dem Kind, das beim Kuß auf die Stirn salzig schmeckt, es ist verhext und muss bald sterben» («Горе ребенку, у которого от поцелуя в лоб соленый вкус, ибо он околдован и скоро должен умереть»), признавая связь между потерей соли при МВ и болезнью. [205]
В 19 веке Карл фон Рокитанский описал случай гибели плода при мекониевом перитоните , осложнении мекониевой непроходимости кишечника, связанной с МВ. Мекониевый илеус был впервые описан в 1905 году Карлом Ландштейнером . [205] В 1936 году Гвидо Фанкони описал связь между целиакией , муковисцидозом поджелудочной железы и бронхоэктазами . [206]
В 1938 году Дороти Хансин Андерсен опубликовала в Американском журнале болезней детей статью «Цистозный фиброз поджелудочной железы и его связь с целиакией: клиническое и патологическое исследование» . Она была первой, кто описал характерный муковисцидоз поджелудочной железы и связал его с заболеваниями легких и кишечника, выраженными при МВ. [14] Она также первой предположила, что МВ является рецессивным заболеванием, и впервые использовала заместительную терапию ферментами поджелудочной железы для лечения больных детей. В 1952 году Поль ди Сант'Аньезе обнаружил отклонения в электролитах пота; тест на пот был разработан и усовершенствован в течение следующего десятилетия. [207]
Первая связь между CF и другим маркером ( параоксоназой ) была обнаружена в 1985 году Хансом Эйбергом , что указывает на то, что для CF существует только один локус. [208] В 1988 году первая мутация CF, ΔF508 , была обнаружена Фрэнсисом Коллинзом , Лап-Чи Цуй и Джоном Р. Риорданом в седьмой хромосоме. [209] Последующие исследования выявили более 1000 различных мутаций, вызывающих МВ. [210]
Поскольку мутации в гене CFTR обычно невелики, классические методы генетики не смогли точно определить мутировавший ген. [211] Используя белковые маркеры, исследования генных связей смогли сопоставить мутацию с хромосомой 7. Затем для идентификации и секвенирования гена были использованы методы хромосомного перемещения и хромосомных прыжков . [211] В 1989 году Лап-Чи Цуй возглавил группу исследователей в Больнице для больных детей в Торонто , которая обнаружила ген, ответственный за МВ. [212] CF представляет собой классический пример того, как генетическое заболевание человека было выявлено исключительно с помощью процесса передовой генетики . [211] [213]
Люди с МВ могут быть внесены в реестр заболеваний , который позволит исследователям и врачам отслеживать результаты лечения и выявлять кандидатов для клинических испытаний. [214]
Генная терапия изучалась как потенциальное лекарство от МВ. Результаты клинических испытаний по состоянию на 2016 год показали ограниченный успех [обновлять], и использование генной терапии в качестве рутинной терапии не предлагается. [215] Небольшое исследование, опубликованное в 2015 году, выявило небольшую пользу. [216]
В центре внимания многих исследований генной терапии МВ – попытка поместить нормальную копию гена CFTR в пораженные клетки. Перенос нормального гена CFTR в пораженные эпителиальные клетки приведет к выработке функционального белка CFTR во всех клетках-мишенях без побочных реакций или воспалительной реакции. Для предотвращения легочных проявлений CF необходимо лишь 5–10% нормального количества экспрессии гена CFTR. [217] Для переноса генов было протестировано множество подходов, таких как липосомы и вирусные векторы, на животных моделях и в клинических испытаниях. Однако оба метода оказались относительно неэффективными вариантами лечения [218] , главным образом потому, что очень немногие клетки поглощают вектор и экспрессируют ген, поэтому лечение имеет небольшой эффект. Кроме того, были отмечены проблемы с рекомбинацией кДНК, такие как ген, введенный в результате лечения, становится непригодным для использования. [219] В культуре CFTR с помощью CRISPR/Cas9 произошло функциональное восстановление органоидов кишечных стволовых клеток пациентов с муковисцидозом. [220]
Фаговая терапия изучается для лечения бактерий с множественной лекарственной устойчивостью у людей с МВ. [221] [222]
В стадии разработки находится ряд небольших молекул, целью которых является компенсация различных мутаций гена CFTR . Модуляторы CFTR использовались вместо других типов генетической терапии. Эти методы лечения сосредоточены на проявлении генетической мутации, а не на самом мутировавшем гене. Модуляторы делятся на два класса: потенциаторы и корректоры. Потенциаторы действуют на ионные каналы CFTR, встроенные в клеточную мембрану, и эти типы лекарств помогают открыть канал, обеспечивая трансмембранный поток. Корректоры предназначены для помощи в транспортировке возникающих белков, белков, которые образуются рибосомами до того, как они преобразуются в определенную форму, к поверхности клетки для внедрения в клеточную мембрану. [223]
Большинство из них нацелены на стадию транскрипции генетической экспрессии. Один из подходов заключался в попытке разработать лекарство, которое заставит рибосому преодолевать стоп-кодон и производить полноразмерный белок CFTR. Около 10% случаев МВ возникают в результате преждевременного появления стоп-кодона в ДНК, что приводит к преждевременному прекращению синтеза белка и усечению белков. Эти препараты нацелены на нонсенс-мутации, такие как G542X, в которых аминокислота глицин в положении 542 заменена стоп-кодоном. Аминогликозидные антибиотики мешают синтезу белка и исправлению ошибок. В некоторых случаях они могут заставить клетку преодолеть преждевременный стоп-кодон путем вставки случайной аминокислоты, тем самым обеспечивая экспрессию полноразмерного белка. Будущие исследования этих модуляторов сосредоточены на клеточных мишенях, на которые можно повлиять изменением экспрессии гена. В противном случае генетическая терапия будет использоваться в качестве лечения, когда модуляторная терапия не работает, учитывая, что на 10% людей с муковисцидозом эти препараты не влияют. [224]
Элексакафтор/ивакафтор/тезакафтор был одобрен в США в 2019 году для лечения муковисцидоза. [225] Эта комбинация ранее разработанных препаратов способна вылечить до 90% людей с муковисцидозом. [223] [225] Этот препарат восстанавливает некоторую эффективность белка CFTR, так что он может работать как ионный канал на поверхности клетки. [226]
Ранее было показано, что межвидовые взаимодействия вносят важный вклад в патологию легочных инфекций CF. Примеры включают выработку ферментов, разрушающих антибиотики, таких как β-лактамазы, и выработку побочных продуктов метаболизма, таких как короткоцепочечные жирные кислоты (КЦЖК), анаэробными видами, которые могут усиливать патогенность традиционных патогенов, таких как Pseudomonas aeruginosa . [227] В связи с этим было высказано предположение, что прямое изменение состава микробного сообщества и метаболической функции МВ может стать альтернативой традиционной терапии антибиотиками. [65]
Антисмысловая терапия исследуется для лечения подмножества мутаций, которые имеют ограниченный ответ или вообще не реагируют на модуляторы CFTR. [228] Такие мутации делятся на два класса: сплайсинг (например, c.3718-2477C>T) и нонсенс (например, G542X, W1282X), оба из которых приводят к очень низкой экспрессии белка CFTR, хотя сам белок обычно незатронутый. Это противоречит более распространенным мутациям, таким как ΔF508, которые имеют нормальную экспрессию CFTR, но в нефункциональной форме. Модуляторы служат только для коррекции этих аберрантных белков и практически не приносят никакой пользы в случае недостаточной экспрессии. Антисмысловые олигонуклеотиды (ASO) могут решить эту проблему путем стимулирования деградации мРНК или изменения сплайсинга пре-мРНК, нонсенс-опосредованного распада мРНК или трансляции, тем самым увеличивая экспрессию CFTR.