Серебро — химический элемент ; он имеет символ Ag (от латинского argentum «серебро», производного от протоиндоевропейского *h₂erϵ « блестящий, белый » )) и атомный номер 47. Мягкий, белый, блестящий переходный металл , он демонстрирует высочайшую электропроводность , теплопроводность. проводимость и отражательная способность любого металла . [8] Металл встречается в земной коре в чистой, свободной элементарной форме (« самородное серебро»), в виде сплава с золотом и другими металлами, а также в таких минералах, как аргентит и хлораргирит . Большая часть серебра производится как побочный продукт переработки меди , золота, свинца и цинка .
Серебро издавна ценилось как драгоценный металл . Металлическое серебро используется во многих инвестиционных монетах , иногда вместе с золотом : [9] хотя его больше, чем золота, его гораздо меньше, чем самородного металла . [10] Его чистота обычно измеряется на промилле ; сплав с чистотой 94% описывается как «тонкий 0,940». Серебро , как один из семи металлов древности , играло непреходящую роль в большинстве человеческих культур.
Помимо валюты и инвестиционного средства ( монеты и слитки ), серебро используется в солнечных батареях , фильтрации воды , ювелирных изделиях , украшениях, дорогой посуде и утварях (отсюда и термин « серебряные изделия »), в электрических контактах и проводниках . в специализированных зеркалах, покрытиях для окон, в катализе химических реакций, в качестве красителя в витражах и в специализированных кондитерских изделиях. Его соединения используются в фото- и рентгеновской пленке. Разбавленные растворы нитрата серебра и других соединений серебра применяют как дезинфицирующие средства и микробиоциды ( олигодинамический эффект ), добавляют в повязки , раневые повязки, катетеры и др. медицинский инструментарий .

Серебро по своим физическим и химическим свойствам похоже на двух своих соседей по вертикали в 11-й группе таблицы Менделеева : медь и золото . Его 47 электронов расположены в конфигурации [Kr]4d 10 5s 1 , аналогично меди ([Ar]3d 10 4s 1 ) и золоту ([Xe]4f 14 5d 10 6s 1 ); группа 11 — одна из немногих групп d-блока , имеющая полностью согласованный набор электронных конфигураций. [12] Эта характерная электронная конфигурация с единственным электроном в самой высокой занятой подоболочке s над заполненной подоболочкой d, объясняет многие необычные свойства металлического серебра. [13]
Серебро — относительно мягкий, чрезвычайно пластичный и податливый переходный металл , хотя оно немного менее податливо, чем золото. Серебро кристаллизуется в гранецентрированной кубической решетке с объемным координационным числом 12, в которой делокализован только один 5s-электрон, подобно меди и золоту. [14] В отличие от металлов с неполной d-оболочкой, металлические связи в серебре не имеют ковалентного характера и относительно слабы. Это наблюдение объясняет низкую твердость и высокую пластичность монокристаллов серебра. [15]
Серебро имеет блестящий белый металлический блеск, который можно полировать до блеска [ 16 ] и который настолько характерен, что название самого металла стало названием цвета . [13] Защищенное серебро имеет большую оптическую отражательную способность , чем алюминий , на всех длинах волн длиннее ~450 нм. [17] На длинах волн короче 450 нм отражательная способность серебра уступает отражательной способности алюминия и падает до нуля вблизи 310 нм. [18]
Элементам группы 11 свойственна очень высокая электро- и теплопроводность, поскольку их единственный s-электрон свободен и не взаимодействует с заполненной d-подоболочкой, поскольку такие взаимодействия (которые происходят в предыдущих переходных металлах) снижают подвижность электронов. [19] Теплопроводность серебра одна из самых высоких из всех материалов, хотя теплопроводность углерода (в аллотропе алмаза ) и сверхтекучего гелия-4 выше. [12] Электропроводность серебра самая высокая из всех металлов, даже выше, чем у меди . Серебро также имеет самое низкое контактное сопротивление среди всех металлов. [12] Серебро редко используется из-за его электропроводности из-за его высокой стоимости, хотя исключение составляет радиочастотная техника , особенно на УКВ и более высоких частотах, где серебряное покрытие улучшает электропроводность, поскольку эти токи имеют тенденцию течь по поверхности проводники , а не через внутреннюю часть. Во время Второй мировой войны в США для изготовления электромагнитов в калютронах для обогащения урана было использовано 13540 тонн серебра , главным образом из-за дефицита меди во время войны. [20] [21] [22]
Серебро легко образует сплавы с медью, золотом и цинком . Сплавы цинка с серебром с низкой концентрацией цинка можно рассматривать как гранецентрированные кубические твердые растворы цинка в серебре, поскольку структура серебра практически не меняется, а концентрация электронов возрастает по мере добавления большего количества цинка. Дальнейшее увеличение концентрации электронов приводит к образованию объемноцентрированной кубической (концентрация электронов 1,5), сложной кубической (1,615) и гексагональной плотноупакованных фаз (1,75). [14]
Встречающееся в природе серебро состоит из двух стабильных изотопов : Ag 107 и Ag 109 , при этом Ag 107 встречается немного больше (51,839% естественного содержания ). Такое почти равное содержание редко встречается в периодической таблице. Атомный вес 107,8682(2) u ; [23] [24] это значение очень важно из-за важности соединений серебра, особенно галогенидов, в гравиметрическом анализе . [23] Оба изотопа серебра производятся в звездах посредством s-процесса (медленный захват нейтронов), а также в сверхновых посредством r-процесса (быстрый захват нейтронов). [25]
Охарактеризовано 28 радиоизотопов , наиболее стабильными из которых являются 105 Ag с периодом полураспада 41,29 суток, 111 Ag с периодом полураспада 7,45 суток и 112 Ag с периодом полураспада 3,13 часа. Серебро имеет множество ядерных изомеров , наиболее стабильными из которых являются 108m Ag ( t 1/2 = 418 лет), 110m Ag ( t 1/2 = 249,79 дней) и 106m Ag ( t 1/2 = 8,28 дней). Период полураспада всех остальных радиоактивных изотопов составляет менее часа, а период полураспада большинства из них составляет менее трех минут. [26]
Относительная атомная масса изотопов серебра варьируется от 92,950 ед. ( 93 Ag) до 129,950 ед. ( 130 Ag); [27] первичным режимом распада перед наиболее распространенным стабильным изотопом 107 Ag является захват электрона , а основным режимом после него является бета-распад . Первичными продуктами распада до 107 Ag являются изотопы палладия (46-й элемент), а после — изотопы кадмия (48-й элемент). [26]
Изотоп палладия 107 Pd распадается путем бета-излучения до 107 Ag с периодом полураспада 6,5 миллионов лет. Железные метеориты — единственные объекты с достаточно высоким соотношением палладия к серебру, позволяющим выявить измеримые вариации содержания 107 Ag. Радиогенный 107 Ag был впервые обнаружен в метеорите Санта-Клара в 1978 году. [28] Корреляции 107 Pd– 107 Ag, наблюдаемые в телах, которые явно расплавились со времени аккреции Солнечной системы , должны отражать присутствие нестабильных нуклидов в ранней Солнечной системе. . [29]
Серебро – довольно инертный металл. Это связано с тем, что его заполненная 4d-оболочка не очень эффективно экранирует электростатические силы притяжения ядра к самому внешнему 5s-электрону, и, следовательно, серебро находится в нижней части электрохимического ряда ( E 0 ( Ag + /Ag) = +0,799 В). [13] В группе 11 серебро имеет самую низкую первую энергию ионизации (что указывает на нестабильность 5s-орбитали), но имеет более высокие вторую и третью энергии ионизации, чем медь и золото (что указывает на стабильность 4d-орбиталей), так что химия Серебро преимущественно имеет степень окисления +1, что отражает все более ограниченный диапазон состояний окисления вдоль переходного ряда по мере заполнения и стабилизации d-орбиталей. [31] В отличие от меди , для которой более высокая энергия гидратации Cu 2+ по сравнению с Cu + является причиной того, что первая более стабильна в водных растворах и твердых веществах, несмотря на отсутствие у последней стабильной заполненной d-подоболочки, с серебром этот эффект затмевается его большей второй энергией ионизации. Следовательно, Ag + является стабильной формой в водных растворах и твердых веществах, а Ag2 + гораздо менее стабилен, поскольку окисляет воду. [31]
Большинство соединений серебра имеют значительный ковалентный характер из-за небольшого размера и высокой энергии первой ионизации (730,8 кДж/моль) серебра. [13] Кроме того, электроотрицательность серебра по Полингу , равная 1,93, выше, чем у свинца (1,87), а его сродство к электрону , равное 125,6 кДж/моль, намного выше, чем у водорода (72,8 кДж/моль), и ненамного меньше, чем у кислорода . (141,0 кДж/моль). [32] Из-за своей полной d-подоболочки серебро в своей основной степени окисления +1 проявляет относительно мало свойств собственно переходных металлов из групп с 4 по 10, образуя довольно нестабильные металлоорганические соединения , образуя линейные комплексы с очень низкими координационными числами, такими как 2. и образует амфотерный оксид [33] , а также фазы Цинтла, подобные постпереходным металлам . [34] В отличие от предыдущих переходных металлов, степень окисления серебра +1 стабильна даже в отсутствие π-акцепторных лигандов . [31]
Серебро не вступает в реакцию с воздухом даже при красном калении, поэтому алхимики считали его благородным металлом наряду с золотом. Его реакционная способность занимает промежуточное положение между медью (которая образует оксид меди (I) при нагревании на воздухе до красного каления) и золотом. Подобно меди, серебро реагирует с серой и ее соединениями; в их присутствии серебро тускнеет на воздухе с образованием черного сульфида серебра (вместо этого медь образует зеленый сульфат , а золото не вступает в реакцию). Хотя серебро не подвергается воздействию неокисляющих кислот, металл легко растворяется в горячей концентрированной серной кислоте , а также в разбавленной или концентрированной азотной кислоте . В присутствии воздуха и особенно в присутствии перекиси водорода серебро легко растворяется в водных растворах цианида . [30]
Тремя основными формами порчи исторических серебряных артефактов являются потускнение, образование хлорида серебра вследствие длительного погружения в соленую воду, а также реакция с нитрат- ионами или кислородом. Свежий хлорид серебра имеет бледно-желтый цвет, под воздействием света становится пурпурным; он слегка выступает над поверхностью артефакта или монеты. Осаждение меди в древнем серебре можно использовать для датировки артефактов, поскольку медь почти всегда входит в состав серебряных сплавов. [35]
Металлическое серебро подвергается воздействию сильных окислителей, таких как перманганат калия ( KMnO
4) и дихромат калия ( K
2Кр
2О
7), а также в присутствии бромида калия ( KBr ). Эти соединения используются в фотографии для отбеливания изображений серебра, превращая их в бромид серебра, который можно либо зафиксировать тиосульфатом , либо повторно проявить для усиления исходного изображения. Серебро образует цианидные комплексы ( цианид серебра ), растворимые в воде при наличии избытка цианид-ионов. Растворы цианида серебра используются при гальванике серебра. [36]
Распространенными степенями окисления серебра являются (в порядке общности): +1 (наиболее стабильное состояние; например, нитрат серебра , AgNO 3 ); +2 (высокоокислительные; например, фторид серебра(II) , AgF 2 ); и даже очень редко +3 (чрезвычайно окислительные; например, тетрафтораргентат(III) калия, KAgF 4 ). [37] Для достижения состояния +3 требуются очень сильные окислители, такие как фтор или пероксодисульфат , а некоторые соединения серебра (III) реагируют с атмосферной влагой и разъедают стекло. [38] Действительно, фторид серебра (III) обычно получают путем реакции серебра или монофторида серебра с самым сильным известным окислителем, дифторидом криптона . [39]
Серебро и золото имеют довольно низкое химическое сродство к кислороду, меньшее, чем у меди, и поэтому ожидается, что оксиды серебра термически весьма нестабильны. Растворимые соли серебра(I) при добавлении щелочи выпадают в осадок темно-коричневого оксида серебра(I) Ag 2 O. (Гидроксид AgOH существует только в растворе; в противном случае он самопроизвольно разлагается до оксида.) Оксид серебра (I) очень легко восстанавливается до металлического серебра и при температуре выше 160 ° C разлагается на серебро и кислород. [40] Это и другие соединения серебра(I) могут быть окислены сильным окислителем пероксодисульфатом до черного AgO, смешанного оксида серебра(I,III) формулы Ag I Ag III O 2 . Известны также некоторые другие смешанные оксиды с серебром в нецелых степенях окисления, а именно Ag 2 O 3 и Ag 3 O 4 , а также Ag 3 O, который ведет себя как металлический проводник. [40]
Сульфид серебра(I) Ag 2 S очень легко образуется из составляющих его элементов и является причиной потускнения некоторых старых серебряных предметов. Он также может образовываться в результате реакции сероводорода с металлическим серебром или водными ионами Ag + . Известны многие нестехиометрические селениды и теллуриды ; в частности, AgTe ~3 является низкотемпературным сверхпроводником . [40]

Единственным известным дигалогенидом серебра является дифторид AgF 2 , который можно получить из элементов при нагревании. Сильный, но термически стабильный и, следовательно, безопасный фторирующий агент, фторид серебра (II) часто используется для синтеза гидрофторуглеродов . [41]
В отличие от этого, известны все четыре галогенида серебра (I). Фторид , хлорид и бромид имеют структуру хлорида натрия, но йодид имеет три известные стабильные формы при разных температурах ; что при комнатной температуре это кубическая структура цинковой обманки . Все они могут быть получены путем прямой реакции соответствующих элементов. [41] По мере спуска галогенной группы галогенид серебра приобретает все более и более ковалентный характер, растворимость снижается, а цвет меняется от белого хлорида к желтому йодиду, поскольку энергия, необходимая для переноса заряда лиганд-металл (X - Ag + → XAg) снижается. [41] Фторид является аномальным, поскольку ион фтора настолько мал, что имеет значительную энергию сольватации и, следовательно, хорошо растворим в воде и образует ди- и тетрагидраты. [41] Остальные три галогенида серебра плохо растворяются в водных растворах и очень часто используются в гравиметрических аналитических методах. [23] Все четыре фоточувствительны (хотя монофторид светочувствителен только к ультрафиолетовому свету), особенно бромид и йодид, которые фоторазлагаются до металлического серебра и поэтому использовались в традиционной фотографии . [41] Происходит следующая реакция: [42]
Этот процесс необратим, поскольку высвободившийся атом серебра обычно находится в дефекте кристалла или в месте примеси, так что энергия электрона снижается настолько, что он «захватывается». [42]

Белый нитрат серебра AgNO 3 является универсальным предшественником многих других соединений серебра, особенно галогенидов, и гораздо менее чувствителен к свету. Когда-то его называли лунной едкой, потому что древние алхимики называли серебро луной , веря, что серебро связано с Луной. [43] [44] Его часто используют для гравиметрического анализа, используя нерастворимость более тяжелых галогенидов серебра, распространенным предшественником которых он является. [23] Нитрат серебра используется многими способами в органическом синтезе , например, для снятия защиты и окисления. Ag + обратимо связывает алкены , а нитрат серебра использовался для разделения смесей алкенов путем селективного поглощения. Полученный аддукт можно разложить аммиаком с выделением свободного алкена. [45]
Желтый карбонат серебра Ag 2 CO 3 легко получить взаимодействием водных растворов карбоната натрия с недостатком нитрата серебра. [46] Его основное применение — производство серебряного порошка для использования в микроэлектронике. Его восстанавливают формальдегидом с получением серебра, свободного от щелочных металлов: [47]
Карбонат серебра также используется в качестве реагента в органическом синтезе, например, в реакции Кенигса-Кнорра . При окислении Фетизона карбонат серебра на целите действует как окислитель , образуя лактоны из диолов . Он также используется для превращения алкилбромидов в спирты . [46]
Гремучее серебро , AgCNO, мощное, чувствительное к прикосновению взрывчатое вещество , используемое в капсюлях , производится реакцией металлического серебра с азотной кислотой в присутствии этанола . Другими взрывоопасными соединениями серебра являются азид серебра AgN 3 , образующийся при реакции нитрата серебра с азидом натрия [48] и ацетилид серебра Ag 2 C 2 , образующийся при реакции серебра с газообразным ацетиленом в растворе аммиака. [31] В своей наиболее характерной реакции азид серебра взрывоопасно разлагается с выделением газообразного азота: учитывая фоточувствительность солей серебра, такое поведение можно вызвать, освещая его кристаллы светом. [31]
Комплексы серебра имеют тенденцию быть похожими на комплексы его более легкого гомолога меди. Комплексы серебра (III), как правило, редки и очень легко восстанавливаются до более стабильных низших степеней окисления, хотя они немного более стабильны, чем комплексы меди (III). Например, квадратно-плоские комплексы периодата [Ag(IO 5 OH) 2 ] 5- и теллурата [Ag{TeO 4 (OH) 2 } 2 ] 5- могут быть получены окислением серебра(I) щелочным пероксодисульфатом . Желтый диамагнетик [AgF 4 ] − гораздо менее стабилен, дымит во влажном воздухе и реагирует со стеклом. [38]
Комплексы серебра(II) встречаются чаще. Как и валентные изоэлектронные комплексы меди(II), они обычно имеют плоскую квадратную форму и парамагнитны, что усиливается за счет большего расщепления поля для 4d-электронов, чем для 3d-электронов. Водный Ag 2+ , получаемый окислением Ag + озоном, является очень сильным окислителем даже в кислых растворах: в фосфорной кислоте он стабилизируется за счет комплексообразования. Пероксодисульфатное окисление обычно необходимо для получения более стабильных комплексов с гетероциклическими аминами , такими как [Ag(py) 4 ] 2+ и [Ag(bipy) 2 ] 2+ : они стабильны при условии, что противоион не может восстановить серебро обратно до +1 степень окисления. [AgF 4 ] 2- также известен в виде фиолетовой соли бария, а также некоторых комплексов серебра (II) с N- или O -донорными лигандами, такими как пиридинкарбоксилаты. [49]
Безусловно, наиболее важной степенью окисления серебра в комплексах является +1. Катион Ag + диамагнитен, как и его гомологи Cu + и Au + , поскольку все три имеют электронную конфигурацию с замкнутой оболочкой без неспаренных электронов: его комплексы бесцветны при условии, что лиганды не слишком легко поляризуются, такие как I - . Ag + образует соли с большинством анионов, но он неохотно координируется с кислородом, и поэтому большинство этих солей нерастворимы в воде: исключениями являются нитрат, перхлорат и фторид. Тетракоординированный тетраэдрический водный ион [Ag(H 2 O) 4 ] + известен, но характерная геометрия катиона Ag + является 2-координатной линейной. Например, хлорид серебра легко растворяется в избытке водного аммиака с образованием [Ag(NH 3 ) 2 ] + ; соли серебра растворяются на фотографии за счет образования тиосульфатного комплекса [Ag(S 2 O 3 ) 2 ] 3- ; и цианидная экстракция для серебряных (и золотых) производств путем образования комплекса [Ag(CN) 2 ] - . Цианид серебра образует линейный полимер {Ag–C≡N→Ag–C≡N→}; Тиоцианат серебра имеет аналогичную структуру, но вместо него образует зигзаг из-за sp 3 - гибридизованного атома серы. Хелатирующие лиганды не способны образовывать линейные комплексы, поэтому комплексы серебра (I) с ними имеют тенденцию образовывать полимеры; существует несколько исключений, таких как околотетраэдрические комплексы дифосфина и диарсина [Ag(L–L) 2 ] + . [50]
В стандартных условиях серебро не образует простых карбонилов из-за слабости связи Ag–C. Некоторые из них известны при очень низких температурах около 6–15 К, например, зеленый плоский парамагнитный Ag(CO) 3 , который димеризуется при 25–30 К, вероятно, образуя связи Ag-Ag. Кроме того, известен карбонил серебра [Ag(CO)] [B(OTeF 5 ) 4 ]. Известны полимерные комплексы AgLX с алкенами и алкинами , но их связи термодинамически слабее, чем даже у комплексов платины (хотя они образуются легче, чем у аналогичных комплексов золота): они также весьма несимметричны, демонстрируя слабую π- связь . в группе 11. σ- связи Ag–C также могут образовываться серебром(I), как медь(I) и золото(I), но простые алкилы и арилы серебра(I) еще менее стабильны, чем у меди(I). I) (которые имеют тенденцию взрываться в условиях окружающей среды). Например, плохая термическая стабильность отражается на относительных температурах разложения AgMe (-50 °C) и CuMe (-15 °C), а также PhAg (74 °C) и PhCu (100 °C). [51]
Связь C–Ag стабилизируется перфторалкильными лигандами, например в AgCF(CF 3 ) 2 . [52] Соединения алкенилсеребра также более стабильны, чем их аналоги из алкилсеребра. [53] Комплексы серебро- NHC легко получить и обычно используются для получения других комплексов NHC путем замены лабильных лигандов. Например, реакция комплекса бис(NHC)серебра(I) с дихлоридом бис(ацетонитрил)палладия или хлоридо(диметилсульфид)золотом(I) : [54]

Серебро образует сплавы с большинством других элементов таблицы Менделеева. Элементы 1–3 групп, за исключением водорода , лития и бериллия , хорошо смешиваются с серебром в конденсированной фазе и образуют интерметаллиды; из групп 4–9 смешиваются плохо; элементы 10–14 групп (кроме бора и углерода ) имеют очень сложные фазовые диаграммы Ag–M и образуют наиболее коммерчески важные сплавы; а остальные элементы таблицы Менделеева не имеют согласованности в своих фазовых диаграммах Ag – M. Безусловно, наиболее важными из таких сплавов являются сплавы с медью: большая часть серебра, используемого для чеканки монет и ювелирных изделий, на самом деле представляет собой сплав серебра и меди, а эвтектическая смесь используется при вакуумной пайке . Эти два металла полностью смешиваются в жидком виде, но не в твердом состоянии; их важность в промышленности обусловлена тем фактом, что их свойства, как правило, подходят для широкого диапазона изменений концентрации серебра и меди, хотя большинство полезных сплавов, как правило, богаче серебром, чем эвтектическая смесь (71,9% серебра и 28,1% меди по вес, а также 60,1% серебра и 28,1% меди по атому). [55]
Большинство других бинарных сплавов малопригодны: например, сплавы серебро-золото слишком мягки, а сплавы серебро- кадмий слишком токсичны. Тройные сплавы имеют гораздо большее значение: зубные амальгамы обычно представляют собой сплавы серебро-олово-ртуть, сплавы серебро-медь-золото очень важны в ювелирном деле (обычно богаты золотом) и имеют широкий диапазон твердости и цветов, серебро-медь-золото. медно-цинковые сплавы полезны в качестве легкоплавких припоев, а серебро-кадмий- индий (включающий три соседних элемента в таблице Менделеева) полезен в ядерных реакторах из-за его высокого сечения захвата тепловых нейтронов , хорошей теплопроводности, механическая стабильность и устойчивость к коррозии в горячей воде. [55]
Слово серебро встречается в древнеанглийском языке в различных вариантах написания, например, seolfor и siolfor . Это родственно древневерхненемецкому силабару ; _ Готический силубр ; или древнескандинавское silfr , все они в конечном итоге произошли от протогерманского *silubra . Балто -славянские слова, обозначающие серебро, очень похожи на германские (например, русское серебро [ serebró ], польское srebro , литовское sidãbras ), как и кельтиберийская форма silabur . Они могут иметь общее индоевропейское происхождение, хотя их морфология скорее предполагает неиндоевропейский Wanderwort . [56] [57] Некоторые ученые, таким образом, предположили палео-латиноамериканское происхождение, указывая на баскскую форму zilharr в качестве доказательства. [58]
Химический символ Ag происходит от латинского слова, обозначающего серебро , argentum (сравните древнегреческое ἄργυρος , árgyros ), от протоиндоевропейского корня * h₂erٵ- (ранее реконструированного как *arϵ- ), означающего « белый » или « сияющий ». . Это было обычное протоиндоевропейское слово для обозначения металла, рефлексы которого отсутствуют в германском и балтославянском языках. [57]

Серебро было известно еще в доисторические времена: [59] три металла 11-й группы — медь, серебро и золото — встречаются в природе в элементарной форме и, вероятно, использовались в качестве первых примитивных форм денег , а не простого обмена. [60] Однако, в отличие от меди, серебро не привело к развитию металлургии из-за его низкой структурной прочности и чаще использовалось в качестве украшения или в качестве денег. [61] Поскольку серебро более реакционноспособно, чем золото, запасы самородного серебра были гораздо более ограниченными, чем запасы золота. [60] Например, серебро было дороже золота в Египте примерно до пятнадцатого века до нашей эры: [62] Считается, что египтяне отделяли золото от серебра, нагревая металлы с солью, а затем восстанавливая полученный хлорид серебра до металл. [63]
Ситуация изменилась с открытием купелирования — метода, позволяющего извлекать металлическое серебро из руд. В то время как шлаковые отвалы, обнаруженные в Малой Азии и на островах Эгейского моря, указывают на то, что серебро отделялось от свинца еще в 4-м тысячелетии до нашей эры , [12] а одним из первых центров добычи серебра в Европе была Сардиния в раннем энеолите . период [64] эти методы не получили широкого распространения до тех пор, пока они не распространились по всему региону и за его пределами . [62] Истоки производства серебра в Индии , Китае и Японии почти наверняка были одинаково древними, но недостаточно документированы из-за их большого возраста. [63]

Когда финикийцы впервые пришли на территорию нынешней Испании , они получили так много серебра, что не могли уместить его все на свои корабли, и в результате для утяжеления своих якорей использовали серебро вместо свинца. [62] Ко времени греческой и римской цивилизаций серебряные монеты были основным продуктом экономики: [60] греки уже добывали серебро из галенита к 7 веку до нашей эры, [62] и возвышение Афин было частично обусловлено Это возможно благодаря близлежащим серебряным рудникам в Лаурии , из которых они добывали около 30 тонн в год с 600 по 300 годы до нашей эры. [65] Стабильность римской валюты в значительной степени зависела от поставок серебряных слитков, в основном из Испании, которые римские горняки производили в масштабах, не имеющих себе равных до открытия Нового Света . Достигнув пикового производства в 200 тонн в год, в середине второго века нашей эры в римской экономике обращались примерно 10 000 тонн серебра, что в пять-десять раз больше, чем совокупное количество серебра, доступное средневековой Европе и Аббасидскому халифату. около 800 г. н. э. [66] [67] Римляне также записали добычу серебра в Центральной и Северной Европе в тот же период. Это производство почти полностью остановилось с падением Римской империи и не возобновилось до времен Карла Великого : к тому времени уже были добыты десятки тысяч тонн серебра. [63]
Центральная Европа стала центром производства серебра в средние века , поскольку средиземноморские месторождения, эксплуатируемые древними цивилизациями, были исчерпаны. Серебряные рудники были открыты в Богемии , Саксонии , Эльзасе , регионе Лан , Зигерланде , Силезии , Венгрии , Норвегии , Штирии , Шваце и южном Шварцвальде . Большинство этих руд были весьма богаты серебром, и их можно было просто вручную отделить от оставшейся породы, а затем переплавить; встречены также месторождения самородного серебра. Многие из этих рудников вскоре были исчерпаны, но некоторые из них оставались активными до промышленной революции , до которой мировое производство серебра составляло всего лишь 50 тонн в год. [63] В Америке технология высокотемпературного купелирования серебром и свинцом была разработана цивилизациями до инков еще в 60–120 годах нашей эры; В это время продолжали разрабатывать месторождения серебра в Индии, Китае, Японии и доколумбовой Америке. [63] [68]
С открытием Америки и разграблением серебра испанскими конкистадорами Центральная и Южная Америка стали доминирующими производителями серебра примерно до начала 18 века, особенно Перу , Боливия , Чили и Аргентина : [63] последний из позже эти страны получили свое название от названия металла, составлявшего большую часть их минеральных богатств. [65] Торговля серебром уступила место глобальной сети обмена . Как выразился один историк, серебро «ходило по миру и заставляло мир вращаться». [69] Большая часть этого серебра оказалась в руках китайцев. Португальский купец в 1621 году заметил, что серебро «скитается по всему миру... прежде чем попасть в Китай, где оно остается как бы в своем естественном центре». [70] Тем не менее, большая часть денег пошла в Испанию, что позволило испанским правителям преследовать военные и политические амбиции как в Европе, так и в Америке. «Рудники Нового Света», заключили несколько историков, «поддержали Испанскую империю». [71]
В XIX веке первичное производство серебра переместилось в Северную Америку, особенно в Канаду , Мексику и Неваду в США : некоторое вторичное производство из свинцовых и цинковых руд также имело место в Европе, а также на месторождениях в Сибири и на Дальнем Востоке России . так же как и в Австралии были добыты. [63] Польша стала важным производителем в 1970-х годах после открытия месторождений меди, богатых серебром, прежде чем в следующем десятилетии центр производства вернулся в Америку. Сегодня Перу и Мексика по-прежнему входят в число основных производителей серебра, но распределение производства серебра по всему миру вполне сбалансировано, и около одной пятой поставок серебра поступает за счет переработки, а не нового производства. [63]

Серебро играет определенную роль в мифологии и нашло различное использование в качестве метафоры и в фольклоре. Греческий поэт Гесиод в «Трудах и днях» (строки 109–201) перечисляет разные возрасты человека , названные в честь таких металлов, как золото, серебро, бронза и железо, чтобы объяснить последовательные эпохи человечества. [72] « Метаморфозы » Овидия содержат еще один пересказ истории, содержащий иллюстрацию метафорического использования серебра для обозначения второго лучшего в ряду, лучшего, чем бронза, но хуже, чем золото:
Но когда добрый Сатурн , изгнанный свыше,
Был загнан в ад, мир находился под властью Юпитера .
Последующие времена, серебряный век, вот,
Превосходная латунь, но более превосходящая золото.- Овидий, Метаморфозы , Книга I, пер. Джон Драйден
В фольклоре обычно считалось, что серебро обладает мистическими способностями: например, пуля, отлитая из серебра, часто считается в таком фольклоре единственным оружием, эффективным против оборотня , ведьмы или других монстров . [73] [74] [75] Из этого идиома « серебряная пуля» превратилась в образное обозначение любого простого решения с очень высокой эффективностью или почти чудесными результатами, как в широко обсуждаемой статье по разработке программного обеспечения « Нет серебряной пули ». [76] Другие способности, приписываемые серебру, включают обнаружение яда и облегчение перехода в мифическое царство фей . [75]
Производство серебра также вдохновило образный язык. Явные упоминания о купелировании встречаются в Ветхом Завете Библии , например, в упреке Иеремии Иуде: «Мехи сгорают, свинец сгорает в огне, плавит напрасно, ибо нечестивые не исторгаются». ... Нечестивым серебром назовут их люди, потому что Господь отверг их». (Иеремия 6:19–20) Иеремия также знал о листовом серебре, которое служило примером ковкости и пластичности металла: «Серебро, разложенное на пластины, привозится из Фарсиса, а золото из Уфаза, дело рук и рук основателя: синяя и пурпурная одежда их: все они — дело хитрых людей». (Иеремия 10:9) [62]
Серебро также имеет более негативное культурное значение: идиома тридцать сребреников, относящаяся к награде за предательство, отсылает к взятке, которую, как сказано в Новом Завете, Иуда Искариот взял у еврейских лидеров в Иерусалиме , чтобы передать Иисуса из Назарета солдатам первосвященник Каиафа. [77] С этической точки зрения серебро также символизирует жадность и деградацию сознания; это отрицательный аспект, извращение его ценности. [78]

Содержание серебра в земной коре составляет 0,08 частей на миллион , что почти точно такое же, как у ртути . Чаще всего он встречается в сульфидных рудах, особенно в акантите и аргентите , Ag 2 S. Месторождения аргентита иногда содержат и самородное серебро, когда они встречаются в восстановительных средах, а при контакте с соленой водой превращаются в хлораргирит (в том числе роговое серебро ), AgCl, который распространен в Чили и Новом Южном Уэльсе . [79] Большинство других минералов серебра представляют собой пниктиды или халькогениды серебра ; Обычно это блестящие полупроводники. Большинство настоящих месторождений серебра, в отличие от серебристых месторождений других металлов, произошло в результате вулканизма третичного периода . [80]
Основными источниками серебра являются руды меди, медно-никелевые, свинцовые и свинцово-цинковые руды, добываемые в Перу , Боливии , Мексике , Китае , Австралии , Чили , Польше и Сербии . [12] Перу, Боливия и Мексика добывают серебро с 1546 года и до сих пор являются крупнейшими мировыми производителями. Крупнейшие рудники по добыче серебра — Каннингтон (Австралия), Фреснильо (Мексика), Сан-Кристобаль (Боливия), Антамина (Перу), Рудна (Польша) и Пенаскито (Мексика). [81] Наиболее краткосрочными проектами разработки месторождений до 2015 года являются Паскуа Лама (Чили), Навидад (Аргентина), Хаунисипио (Мексика), Малку Хота (Боливия), [82] и Хакетт Ривер (Канада). [81] Известно , что в Центральной Азии Таджикистан обладает одними из крупнейших месторождений серебра в мире. [83]
Серебро обычно встречается в природе в сочетании с другими металлами или в минералах, содержащих соединения серебра, обычно в форме сульфидов , таких как галенит (сульфид свинца) или церуссит (карбонат свинца). Таким образом, первичное производство серебра требует плавки, а затем купелирования серебристо-свинцовых руд, что является исторически важным процессом. [84] Свинец плавится при 327 °C, оксид свинца — при 888 °C, а серебро — при 960 °C. Для отделения серебра сплав снова плавят при высокой температуре от 960°С до 1000°С в окислительной среде. Свинец окисляется до монооксида свинца , известного тогда как глет , который захватывает кислород из других присутствующих металлов. Жидкий оксид свинца удаляется или впитывается под действием капиллярных сил в футеровку пода. [85] [86] [87]
Сегодня металлическое серебро в основном производится как вторичный побочный продукт электролитического рафинирования меди, свинца и цинка, а также путем применения процесса Паркса к слиткам свинца из руды, которая также содержит серебро. [88] В таких процессах серебро следует за рассматриваемым цветным металлом через его концентрацию и плавку, а затем очищается. Например, при производстве меди очищенная медь электролитически осаждается на катоде, в то время как менее реакционноспособные драгоценные металлы, такие как серебро и золото, собираются под анодом в виде так называемого «анодного шлама». Затем его отделяют и очищают от неблагородных металлов путем обработки горячей аэрированной разбавленной серной кислотой и нагревания с известью или кремнеземным флюсом, после чего серебро очищается до чистоты более 99,9% посредством электролиза в нитратном растворе. [79]
Чистота технического серебра составляет не менее 99,9%, но доступно серебро с чистотой более 99,999%. В 2022 году Мексика была крупнейшим производителем серебра (6300 тонн или 24,2% от мирового объема в 26 000 тонн), за ней следовали Китай (3600 тонн) и Перу (3100 тонн). [88]
Концентрация серебра в морской воде низкая (пмоль/л). Уровни варьируются в зависимости от глубины и между водоемами. Концентрация растворенного серебра колеблется от 0,3 пмоль/л в прибрежных поверхностных водах до 22,8 пмоль/л в пелагических глубоких водах. [89] Анализ присутствия и динамики серебра в морской среде затруднен из-за особенно низких концентраций и сложных взаимодействий в окружающей среде. [90] Несмотря на то, что металл является редким микроэлементом, на его концентрацию сильно влияют речные, эоловые, атмосферные и апвеллинговые поступления, а также антропогенные воздействия через сбросы, удаление отходов и выбросы промышленных компаний. [91] [92] Другие внутренние процессы, такие как разложение органического вещества, могут быть источником растворенного серебра в более глубоких водах, которое поступает в некоторые поверхностные воды посредством апвеллинга и вертикального перемешивания. [92]
В Атлантическом и Тихом океанах концентрации серебра минимальны на поверхности, но возрастают в более глубоких водах. [93] Серебро поглощается планктоном в фотической зоне, ремобилизуется с глубиной и обогащается в глубоких водах. Серебро транспортируется из Атлантики в другие океанические водные массы. [91] В водах северной части Тихого океана серебро ремобилизуется медленнее и все больше обогащается по сравнению с глубокими водами Атлантического океана. Концентрация серебра увеличивается, следуя за основным океаническим конвейером, который перемещает воду и питательные вещества из Северной Атлантики в Южную Атлантику и в северную часть Тихого океана. [94]
Не существует большого количества данных о том, как серебро влияет на морскую жизнь, несмотря на вероятное вредное воздействие, которое оно может оказать на организмы посредством биоаккумуляции , связи с твердыми частицами и сорбции . [89] Лишь примерно в 1984 году учёные начали понимать химические характеристики серебра и его потенциальную токсичность. Фактически, ртуть — единственный микроэлемент, который превосходит по токсичному воздействию серебро; однако полная степень токсичности серебра не ожидается в условиях океана из-за его способности переходить в нереактивные биологические соединения. [95]
В одном исследовании присутствие избытка ионного серебра и наночастиц серебра вызывало эффект биоаккумуляции в органах рыбок данио и изменяло химические пути в их жабрах. [96] Кроме того, очень ранние экспериментальные исследования показали, как токсическое воздействие серебра колеблется в зависимости от солености и других параметров, а также от стадии жизни и различных видов, таких как рыбы, моллюски и ракообразные. [97] Другое исследование обнаружило повышенную концентрацию серебра в мышцах и печени дельфинов и китов, что указывает на загрязнение этого металла в последние десятилетия. Серебро — металл, который нелегко вывести из организма, и повышенные концентрации могут привести к смерти. [98]

Самые ранние известные монеты были отчеканены в Лидийском царстве в Малой Азии около 600 г. до н.э. [99] Монеты Лидии были изготовлены из электрума , который представляет собой природный сплав золота и серебра, который был доступен на территории Лидии. [99] С этого времени серебряные стандарты , в которых стандартной экономической единицей расчета является фиксированный вес серебра, были широко распространены во всем мире вплоть до 20 века. Известные серебряные монеты на протяжении веков включают греческую драхму , [100] римский денарий , [ 101] исламский дирхам , [102] каршапану из древней Индии и рупию времен Империи Великих Моголов (сгруппированные с медными и золотыми монетами для создать триметаллический стандарт), [103] и испанский доллар . [104]
Соотношение количества серебра, используемого для чеканки монет, и количества серебра, используемого для других целей, со временем сильно менялось; например, в военное время больше серебра, как правило, использовалось для чеканки монет для финансирования войны. [105]
Сегодня серебряные слитки имеют код валюты XAG по стандарту ISO 4217 , один из четырех драгоценных металлов , имеющих такой код (остальные — палладий , платина и золото). [106] Серебряные монеты производятся из литых стержней или слитков, прокатываются до нужной толщины, подвергаются термообработке, а затем используются для вырезания заготовок . Эти заготовки затем фрезеруются и чеканятся в чеканном прессе; современные чеканные станки могут производить 8000 серебряных монет в час. [105]
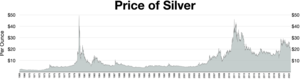
Цены на серебро обычно указываются в тройских унциях . Одна тройская унция равна 31,1034768 грамма. Лондонский фиксинг серебра публикуется каждый рабочий день в полдень по лондонскому времени. [107] Эта цена определяется несколькими крупными международными банками и используется участниками лондонского рынка драгоценных металлов для торгов в этот день. Цены чаще всего указываются в долларах США (USD), фунтах стерлингов (GBP) и евро (EUR).


На протяжении большей части истории серебро, помимо чеканки монет, главным образом использовалось в производстве ювелирных изделий и других предметов общего пользования, и это продолжает оставаться основным применением и сегодня. Примеры включают столовое серебро для столовых приборов, для которого серебро очень подходит из-за его антибактериальных свойств. Западные концертные флейты обычно покрываются серебром или изготавливаются из него ; [109] на самом деле, большая часть серебряных изделий только посеребрена, а не сделана из чистого серебра; серебро обычно наносится гальванопокрытием . Посеребренное стекло (в отличие от металлического) используется для изготовления зеркал, термосов и елочных украшений. [110]
Поскольку чистое серебро очень мягкое, большая часть серебра, используемого для этих целей, легирована медью, причем обычно используются пробы 925/1000, 835/1000 и 800/1000. Одним из недостатков является легкое потускнение серебра в присутствии сероводорода и его производных. Включение драгоценных металлов, таких как палладий, платина и золото, обеспечивает устойчивость к потускнению, но обходится довольно дорого; неблагородные металлы, такие как цинк , кадмий , кремний и германий , не полностью предотвращают коррозию и имеют тенденцию влиять на блеск и цвет сплава. Электролитически очищенное покрытие серебром эффективно повышает устойчивость к потускнению. Обычными решениями для восстановления блеска потускневшего серебра являются окунающие ванны, восстанавливающие поверхность сульфида серебра до металлического серебра, и очистка слоя потускнения пастой; Последний подход также имеет приятный побочный эффект, заключающийся в одновременной полировке серебра. [109]
В медицине серебро добавляют в повязки на раны и используют в качестве антибиотического покрытия в медицинских устройствах. Раневые повязки, содержащие сульфадиазин серебра или наноматериалы серебра , используются для лечения внешних инфекций. Серебро также используется в некоторых медицинских целях, таких как мочевые катетеры (где предварительные данные указывают на то, что оно снижает риск возникновения катетер-ассоциированных инфекций мочевыводящих путей ) и в эндотрахеальных дыхательных трубках (где данные свидетельствуют о том, что оно снижает риск возникновения пневмонии , связанной с аппаратом искусственной вентиляции легких ). [111] [ 112] Ион серебра биоактивен и в достаточной концентрации легко убивает бактерии in vitro . Ионы серебра мешают ферментам бактерий, которые транспортируют питательные вещества, формируют структуры и синтезируют клеточные стенки; эти ионы также связываются с генетическим материалом бактерий. Серебро и наночастицы серебра используются в качестве противомикробного средства в различных отраслях промышленности, здравоохранения и быта: например, наполнение одежды частицами наносеребра позволяет ей дольше оставаться без запаха. [113] [114] Однако бактерии могут развить устойчивость к противомикробному действию серебра. [115] Соединения серебра усваиваются организмом так же, как соединения ртути , но лишены токсичности последних. Серебро и его сплавы применяют в черепной хирургии для замещения кости, амальгамы серебра, олова и ртути — в стоматологии. [110] Фторид диаммина серебра , фторидная соль координационного комплекса с формулой [Ag(NH 3 ) 2 ]F, представляет собой лекарственное средство (лекарство) местного действия, используемое для лечения и профилактики кариеса (полостей) зубов и снижения гиперчувствительности дентина. [116]
Серебро очень важно в электронике для изготовления проводников и электродов из-за его высокой электропроводности, даже если оно потускнело. Объемное серебро и серебряная фольга использовались для изготовления электронных ламп и продолжают использоваться сегодня в производстве полупроводниковых приборов, схем и их компонентов. Например, серебро используется в высококачественных разъемах для ВЧ , УКВ и более высоких частот, особенно в настроенных схемах, таких как резонаторные фильтры , где проводники не могут масштабироваться более чем на 6%. Печатные схемы и RFID- антенны изготавливаются серебряными красками. [12] [117] Порошок серебра и его сплавы используются при приготовлении пасты для проводящих слоев и электродов, керамических конденсаторов и других керамических компонентов. [118]
Серебросодержащие припои используются для пайки металлических материалов, в основном сплавов на основе кобальта , никеля и меди, инструментальных сталей и драгоценных металлов. Основными компонентами являются серебро и медь, а другие элементы выбираются в соответствии с конкретным желаемым применением: например, цинк, олово, кадмий, палладий, марганец и фосфор . Серебро обеспечивает повышенную обрабатываемость и устойчивость к коррозии во время использования. [119]
Серебро полезно при производстве химического оборудования из-за его низкой химической активности, высокой теплопроводности и легкости обработки. Для проведения щелочной плавки применяют серебряные тигли (легированные 0,15% никеля во избежание рекристаллизации металла при красном калении). Медь и серебро также используются при проведении химии с фтором . Оборудование, предназначенное для работы при высоких температурах, часто бывает посеребренным. Серебро и его сплавы с золотом применяют в качестве проволочных или кольцевых уплотнений кислородных компрессоров и вакуумного оборудования. [120]
Металлическое серебро является хорошим катализатором реакций окисления ; на самом деле оно слишком хорошо для большинства целей, поскольку мелкодисперсное серебро имеет тенденцию приводить к полному окислению органических веществ до углекислого газа и воды, и, следовательно, вместо него обычно используется более крупнозернистое серебро. Например, 15%-ное серебро, нанесенное на α-Al 2 O 3 или силикаты, является катализатором окисления этилена в оксид этилена при 230–270 °С. Дегидрирование метанола в формальдегид проводится при 600–720 ° C на серебряной сетке или кристаллах в качестве катализатора, как и дегидрирование изопропанола в ацетон . В газовой фазе гликоль дает глиоксаль , а этанол дает ацетальдегид , а органические амины дегидратируются до нитрилов . [120]
До появления цифровой фотографии , которая сейчас доминирует, светочувствительность галогенидов серебра использовалась для использования в традиционной пленочной фотографии. Светочувствительная эмульсия, используемая в черно-белой фотографии, представляет собой суспензию кристаллов галогенида серебра в желатине , возможно, смешанную с некоторыми соединениями благородных металлов для улучшения светочувствительности, проявления и настройки [ уточнить ] .
Цветная фотография требует добавления специальных компонентов красителей и сенсибилизаторов, так что исходное черно-белое серебряное изображение сочетается с другим компонентом красителя. Оригинальные серебряные изображения отбеливаются, а затем серебро восстанавливается и перерабатывается. Нитрат серебра во всех случаях является исходным материалом. [121]
Рынок нитрата серебра и галогенидов серебра для фотографии быстро сократился с появлением цифровых камер. С пикового мирового спроса на фотосеребро в 1999 году (267 000 000 тройских унций или 8 304,6 тонны ) к 2013 году рынок сократился почти на 70%. [122]
Частицы наносеребра размером от 10 до 100 нанометров используются во многих приложениях. Они используются в проводящих чернилах для печатной электроники и имеют гораздо более низкую температуру плавления, чем более крупные частицы серебра микрометрового размера. [ нужна цитация ] Они также используются в медицинских целях в антибактериальных и противогрибковых средствах почти так же, как и более крупные частицы серебра. [114] Кроме того, по данным Обсерватории наноматериалов Европейского Союза (EUON), наночастицы серебра используются как в пигментах, так и в косметике. [123] [124]

Чистый металл серебра используется в качестве пищевого красителя. Он имеет обозначение E174 и одобрен в Европейском Союзе . [125] Традиционные индийские и пакистанские блюда иногда включают декоративную серебряную фольгу, известную как варк , [126] а в других культурах серебряное драже используется для украшения тортов, печенья и других десертов. [127]
Фотохромные линзы содержат галогениды серебра, поэтому ультрафиолетовый свет при естественном дневном свете высвобождает металлическое серебро, затемняя линзы. Галогениды серебра реформируются при более низкой интенсивности света. Бесцветные пленки хлорида серебра используются в детекторах радиации . Цеолитовые сита, содержащие ионы Ag + , используются для опреснения морской воды во время спасательных операций с использованием ионов серебра для осаждения хлорида в виде хлорида серебра. Серебро также используется из-за его антибактериальных свойств для дезинфекции воды, но его применение ограничено ограничениями на потребление серебра. Коллоидное серебро также используется для дезинфекции закрытых бассейнов; Хотя коллоидное серебро имеет то преимущество, что не выделяет запаха, как обработка гипохлоритом , оно недостаточно эффективно для более загрязненных открытых бассейнов. Маленькие кристаллы йодида серебра используются при засеве облаков , вызывающих дождь. [114]
В 2007 году Законодательное собрание Техаса объявило серебро официальным драгоценным металлом Техаса. [128]
Соединения серебра обладают низкой токсичностью по сравнению с соединениями большинства других тяжелых металлов , поскольку они плохо усваиваются организмом человека при попадании в организм, а то, что усваивается, быстро превращается в нерастворимые соединения серебра или образует комплекс с металлотионеином . Однако фторид серебра и нитрат серебра являются едкими и могут вызвать повреждение тканей, что приводит к гастроэнтериту , диарее , падению артериального давления , судорогам, параличу и остановке дыхания . У животных, неоднократно получавших соли серебра, наблюдалась анемия , замедление роста, некроз печени и жировая дегенерация печени и почек; у крыс, которым имплантировали серебряную фольгу или вводили коллоидное серебро, наблюдалось развитие локализованных опухолей. При парентеральном введении коллоидное серебро вызывает острое отравление серебром. [130] Некоторые водные виды особенно чувствительны к солям серебра и других драгоценных металлов; однако в большинстве ситуаций серебро не представляет серьезной опасности для окружающей среды. [130]
В больших дозах серебро и содержащие его соединения могут всасываться в систему кровообращения и откладываться в различных тканях организма, что приводит к аргирии , приводящей к сине-сероватой пигментации кожи, глаз и слизистых оболочек . Аргирия встречается редко и, насколько известно, не причиняет иного вреда здоровью человека, хотя уродует и обычно необратима. Легкие формы аргирии иногда ошибочно принимают за цианоз — синий оттенок кожи, вызванный недостатком кислорода. [130] [12]
Металлическое серебро, как и медь, является антибактериальным агентом, который был известен древним людям и впервые научно исследован Карлом Нэгели , названным олигодинамическим эффектом . Ионы серебра повреждают метаболизм бактерий даже в таких низких концентрациях, как 0,01–0,1 миллиграмма на литр; металлическое серебро оказывает аналогичный эффект из-за образования оксида серебра. Этот эффект теряется в присутствии серы из-за крайней нерастворимости сульфида серебра. [130]
Некоторые соединения серебра очень взрывоопасны, например, соединения азота азид серебра, амид серебра и гремучее серебро, а также ацетилид серебра , оксалат серебра и оксид серебра (II). Они могут взрываться при нагревании, силе, высыхании, освещении, а иногда и самопроизвольно. Чтобы избежать образования таких соединений, аммиак и ацетилен следует хранить подальше от серебряного оборудования. Соли серебра с сильно окисляющими кислотами, такими как хлорат серебра и нитрат серебра, могут взрываться при контакте с легко окисляющимися материалами, такими как органические соединения, сера и сажа. [130]