Транскрипция – это процесс копирования участка ДНК в РНК. Сегменты ДНК, транскрибируемые в молекулы РНК, которые могут кодировать белки , производят информационную РНК (мРНК). Другие сегменты ДНК транскрибируются в молекулы РНК, называемые некодирующими РНК (нкРНК).
И ДНК, и РНК представляют собой нуклеиновые кислоты , которые используют пары оснований нуклеотидов в качестве дополнительного языка. Во время транскрипции последовательность ДНК считывается РНК- полимеразой , которая производит комплементарную антипараллельную цепь РНК, называемую первичным транскриптом .
В вирусологии термин «транскрипция» также может использоваться применительно к синтезу мРНК из молекулы РНК (т. е. эквивалентному репликации РНК). Например, геном вируса с одноцепочечной РНК с отрицательным смыслом (оцРНК-) может быть матрицей для одноцепочечной РНК с положительным смыслом (оцРНК+). [ необходимы разъяснения ] Это связано с тем, что цепь с положительным смыслом содержит информацию о последовательности, необходимую для трансляции вирусных белков, необходимых для репликации вируса . Этот процесс катализируется вирусной РНК-репликазой . [1] [ нужны разъяснения ]
Единица транскрипции ДНК, кодирующая белок, может содержать как кодирующую последовательность , которая будет транслироваться в белок, так и регуляторные последовательности , которые направляют и регулируют синтез этого белка. Регуляторная последовательность перед кодирующей последовательностью ( выше нее) называется пятью первичными нетранслируемыми областями (5'UTR); последовательность после ( ниже ) кодирующей последовательности называется тремя основными нетранслируемыми областями (3'UTR). [2]
В отличие от репликации ДНК , транскрипция приводит к образованию комплемента РНК, который включает нуклеотид урацил (U) во всех случаях, когда тимин (Т) присутствовал бы в комплементе ДНК. [3]
Только одна из двух цепей ДНК служит матрицей для транскрипции. Антисмысловая цепь ДНК считывается РНК-полимеразой от 3'-конца к 5'-концу во время транскрипции (3' → 5') . Комплементарная РНК создается в противоположном направлении, в направлении 5' → 3', что соответствует последовательности смысловой цепи, за исключением замены урацила на тимин. Такая направленность обусловлена тем, что РНК-полимераза может добавлять нуклеотиды только к 3'-концу растущей цепи мРНК. Такое использование только цепи ДНК 3' → 5' устраняет необходимость во фрагментах Оказаки , которые наблюдаются при репликации ДНК. [2] Это также устраняет необходимость в праймере РНК для инициации синтеза РНК, как это происходит при репликации ДНК.
Нематричная (смысловая) цепь ДНК называется кодирующей цепью , поскольку ее последовательность такая же, как у вновь созданного транскрипта РНК (за исключением замены тимина на урацил) . Это цепь, которая традиционно используется при представлении последовательности ДНК. [4]
Транскрипция имеет некоторые механизмы корректуры, но их меньше и они менее эффективны, чем средства контроля копирования ДНК. В результате транскрипция имеет более низкую точность копирования, чем репликация ДНК. [5]
Транскрипция подразделяется на инициацию , уход от промотора , элонгацию и терминацию . [6]

Настройка транскрипции у млекопитающих регулируется многими цис-регуляторными элементами , включая коровый промотор и проксимальные промоторные элементы , которые расположены вблизи сайтов начала транскрипции генов. Core-промоторы в сочетании с общими факторами транскрипции достаточны для управления инициацией транскрипции, но обычно имеют низкую базальную активность. [7] Другие важные цис-регуляторные модули локализованы в регионах ДНК, удаленных от сайтов начала транскрипции. К ним относятся усилители , глушители , изоляторы и привязывающие элементы. [8] Среди этого созвездия элементов энхансеры и связанные с ними факторы транскрипции играют ведущую роль в инициации транскрипции генов. [9] Энхансер, локализованный в области ДНК, удаленной от промотора гена, может оказывать очень большое влияние на транскрипцию гена, при этом транскрипция некоторых генов увеличивается до 100 раз из-за активированного энхансера. [10]
Энхансеры — это участки генома, которые являются основными генно-регуляторными элементами. Энхансеры контролируют программы транскрипции генов, специфичные для определенного типа клеток, чаще всего путем прохождения больших расстояний, чтобы прийти в физическую близость к промоторам их генов-мишеней. [11] Хотя существуют сотни тысяч областей ДНК энхансеров, [12] для определенного типа ткани только специфические энхансеры приближаются к промоторам, которые они регулируют. При исследовании нейронов коры головного мозга было обнаружено 24 937 петель, приводящих энхансеры к целевым промоторам. [10] Множественные энхансеры, каждый из которых часто находится на десятках или сотнях тысяч нуклеотидов, удаленных от генов-мишеней, соединяются с промоторами гена-мишени и могут координироваться друг с другом, чтобы контролировать транскрипцию общего гена-мишени. [11]
Схематическая иллюстрация в этом разделе показывает, как энхансер движется по кругу, чтобы вступить в тесную физическую близость к промотору целевого гена. Петля стабилизируется димером соединительного белка (например, димером CTCF или YY1 ), причем один член димера прикреплен к своему связывающему мотиву на энхансере, а другой член прикреплен к своему связывающему мотиву на промоторе (представленному красные зигзаги на иллюстрации). [13] Несколько факторов транскрипции, специфичных для клеточных функций (в клетке человека насчитывается около 1600 факторов транскрипции [14] ), как правило, связываются со специфическими мотивами на энхансере [15] и небольшой комбинацией этих связанных с энхансером факторов транскрипции, если их сблизить. к промотору посредством петли ДНК регулируют уровень транскрипции целевого гена. Медиатор (комплекс, обычно состоящий примерно из 26 белков во взаимодействующей структуре) передает регуляторные сигналы от энхансерных ДНК-связанных факторов транскрипции непосредственно ферменту РНК-полимеразы II (pol II), связанному с промотором. [16]
Энхансеры, когда они активны, обычно транскрибируются с обеих цепей ДНК с помощью РНК-полимераз, действующих в двух разных направлениях, образуя две энхансерные РНК (еРНК), как показано на рисунке. [17] Неактивный энхансер может быть связан с неактивным фактором транскрипции. Фосфорилирование фактора транскрипции может активировать его, и этот активированный фактор транскрипции может затем активировать энхансер, с которым он связан (см. маленькую красную звездочку, обозначающую фосфорилирование фактора транскрипции, связанного с энхансером, на иллюстрации). [18] Активированный энхансер начинает транскрипцию своей РНК до активации транскрипции информационной РНК из своего гена-мишени. [19]

Регуляция транскрипции примерно на 60% промоторов также контролируется метилированием цитозинов в динуклеотидах CpG (где за 5'-цитозином следует 3'-гуанин или сайты CpG ). 5-метилцитозин (5-mC) представляет собой метилированную форму цитозина основания ДНК (см. рисунок). 5-mC представляет собой эпигенетический маркер, обнаруживаемый преимущественно в сайтах CpG. В геноме человека встречается около 28 миллионов CpG-динуклеотидов. [20] В большинстве тканей млекопитающих в среднем от 70% до 80% цитозинов CpG метилированы (образуя 5-метилCpG или 5-mCpG). [21] Метилированные цитозины в 3'-последовательностях 5'цитозин-гуанин часто встречаются группами, называемыми CpG-островками . Около 60% последовательностей промоторов имеют островок CpG, тогда как только около 6% последовательностей энхансеров имеют островок CpG. [22] Островки CpG представляют собой регуляторные последовательности, поскольку, если островки CpG метилированы в промоторе гена, это может уменьшить или заглушить транскрипцию гена. [23]
Метилирование ДНК регулирует транскрипцию генов посредством взаимодействия с белками метилсвязывающего домена (MBD), такими как MeCP2, MBD1 и MBD2. Эти белки MBD наиболее прочно связываются с высоко метилированными CpG-островками . [24] Эти белки MBD имеют как метил-CpG-связывающий домен, так и домен репрессии транскрипции. [24] Они связываются с метилированной ДНК и направляют белковые комплексы с ремоделированием хроматина и/или модификацией гистонов на метилированные CpG-островки. Белки MBD обычно репрессируют локальный хроматин, например, катализируя введение репрессивных меток гистонов или создавая общую репрессивную среду хроматина посредством ремоделирования нуклеосом и реорганизации хроматина. [24]

Как отмечалось в предыдущем разделе, факторы транскрипции — это белки, которые связываются со специфическими последовательностями ДНК и регулируют экспрессию гена. Последовательность связывания фактора транскрипции в ДНК обычно имеет длину около 10 или 11 нуклеотидов. Как подытожили в 2009 году Vaquerizas et al. указали, что существует около 1400 различных факторов транскрипции, кодируемых в геноме человека генами, которые составляют около 6% всех генов, кодирующих человеческие белки. [25] Около 94% сайтов связывания транскрипционных факторов (TFBS), которые связаны с сигнально-чувствительными генами, встречаются в энхансерах, тогда как только около 6% таких TFBS встречаются в промоторах. [15]
Белок EGR1 представляет собой особый фактор транскрипции, который важен для регуляции метилирования CpG-островков. Сайт связывания транскрипционного фактора EGR1 часто расположен в последовательностях энхансера или промотора. [26] В геноме млекопитающих имеется около 12 000 сайтов связывания EGR1, и около половины сайтов связывания EGR1 расположены в промоторах, а половина - в энхансерах. [26] Связывание EGR1 с целевым участком связывания ДНК нечувствительно к метилированию цитозина в ДНК. [26]
Хотя в нестимулированных клетках обнаруживаются лишь небольшие количества белка транскрипционного фактора EGR1, трансляция гена EGR1 в белок через час после стимуляции резко увеличивается. [27] Производство белков транскрипционного фактора EGR1 в различных типах клеток может стимулироваться факторами роста, нейротрансмиттерами, гормонами, стрессом и травмой. [27] В головном мозге, когда нейроны активируются, белки EGR1 активируются и связываются (рекрутируют) ранее существовавшие ферменты TET1 , которые производятся в нейронах в больших количествах. Ферменты ТЕТ могут катализировать деметилирование 5-метилцитозина. Когда факторы транскрипции EGR1 доставляют ферменты TET1 к сайтам связывания EGR1 в промоторах, ферменты TET могут деметилировать метилированные островки CpG на этих промоторах. После деметилирования эти промоторы могут затем инициировать транскрипцию своих генов-мишеней. Сотни генов в нейронах дифференциально экспрессируются после активации нейронов посредством рекрутирования EGR1 TET1 на метилированные регуляторные последовательности в их промоторах. [26]
Метилирование промоторов также изменяется в ответ на сигналы. Три метилтрансферазы ДНК млекопитающих (DNMT1, DNMT3A и DNMT3B) катализируют добавление метильных групп к цитозинам в ДНК. Хотя DNMT1 является поддерживающей метилтрансферазой, DNMT3A и DNMT3B могут осуществлять новые метилирования. Существуют также две изоформы сплайсингового белка , полученные из гена DNMT3A : белки ДНК-метилтрансферазы DNMT3A1 и DNMT3A2. [28]
Изоформа сплайсинга DNMT3A2 ведет себя как продукт классического гена немедленной ранней стадии и, например, она устойчиво и временно продуцируется после активации нейронов. [29] То, где изоформа ДНК-метилтрансферазы DNMT3A2 связывается и добавляет метильные группы к цитозинам, по-видимому, определяется посттрансляционными модификациями гистонов. [30] [31] [32]
С другой стороны, нервная активация вызывает деградацию DNMT3A1, сопровождающуюся снижением метилирования по крайней мере одного оцененного целевого промотора. [33]
Транскрипция начинается с связывания РНК-полимеразы и одного или нескольких общих факторов транскрипции с последовательностью промотора ДНК с образованием закрытого комплекса РНК-полимераза-промотор. В закрытом комплексе ДНК промотора все еще полностью двухцепочечная. [6]
РНК-полимераза при помощи одного или нескольких общих факторов транскрипции затем раскручивает примерно 14 пар оснований ДНК с образованием открытого комплекса РНК-полимераза-промотор. В открытом комплексе ДНК промотора частично раскручена и является одноцепочечной. Обнаженная одноцепочечная ДНК называется «пузырем транскрипции». [6]
РНК-полимераза при помощи одного или нескольких общих факторов транскрипции затем выбирает сайт начала транскрипции в пузыре транскрипции, связывается с инициирующим NTP и расширяющим NTP (или коротким праймером РНК и расширяющим NTP), комплементарным последовательности сайта начала транскрипции. и катализирует образование связей с образованием исходного продукта РНК. [6]
У бактерий голофермент РНК- полимеразы состоит из пяти субъединиц: 2 α-субъединицы, 1 β-субъединицы, 1 β'-субъединицы и 1 ω-субъединицы. У бактерий существует один общий фактор транскрипции РНК, известный как сигма-фактор . Основной фермент РНК-полимеразы связывается с бактериальным фактором общей транскрипции (сигма) с образованием голофермента РНК-полимеразы, а затем связывается с промотором. [6] (РНК-полимераза называется голоферментом, когда сигма-субъединица присоединена к основному ферменту, который состоит только из 2 α-субъединицы, 1 β-субъединицы и только 1 β'-субъединицы). В отличие от эукариот, инициирующий нуклеотид возникающей бактериальной мРНК не кэпирован модифицированным гуаниновым нуклеотидом. Инициирующий нуклеотид бактериальных транскриптов несет 5'-трифосфат (5'-PPP), который можно использовать для полногеномного картирования сайтов инициации транскрипции. [35]
У архей и эукариот РНК-полимераза содержит субъединицы, гомологичные каждой из пяти субъединиц РНК-полимеразы у бактерий, а также содержит дополнительные субъединицы. У архей и эукариот функции бактериального общего фактора транскрипции сигма выполняются несколькими общими факторами транскрипции, которые работают вместе. [6] У архей есть три основных фактора транскрипции: TBP , TFB и TFE . У эукариот в транскрипции, зависимой от РНК-полимеразы II , имеется шесть общих факторов транскрипции: TFIIA , TFIIB ( ортолог архейного TFB), TFIID (многосубъединичный фактор, в котором ключевая субъединица, TBP , является ортологом архейного TBP), TFIIE ( ортолог архейного TFE), TFIIF и TFIIH . TFIID является первым компонентом, который связывается с ДНК благодаря связыванию TBP, тогда как TFIIH является последним компонентом, который рекрутируется. У архей и эукариот закрытый комплекс РНК-полимераза-промотор обычно называют « преинициационным комплексом ». [36]
Инициация транскрипции регулируется дополнительными белками, известными как активаторы и репрессоры , а в некоторых случаях ассоциированными коактиваторами или корепрессорами , которые модулируют образование и функцию комплекса инициации транскрипции. [6]
После синтеза первой связи РНК-полимераза должна покинуть промотор. В это время наблюдается тенденция к высвобождению транскрипта РНК и образованию усеченных транскриптов. Это называется абортивной инициацией и характерно как для эукариот, так и для прокариот. [37] Абортивная инициация продолжает происходить до тех пор, пока не будет синтезирован продукт РНК пороговой длины примерно в 10 нуклеотидов, после чего происходит уход от промотора и формируется комплекс элонгации транскрипции. [ нужна цитата ]
Механически ускользание промотора происходит за счет сжатия ДНК , обеспечивая энергию, необходимую для разрыва взаимодействий между голоферментом РНК-полимеразы и промотором. [38]
Исторически считалось, что у бактерий сигма-фактор определенно высвобождается после клиренса промотора. Эта теория была известна как модель обязательного выпуска. Однако более поздние данные показали, что после клиренса промотора сигма-фактор высвобождается в соответствии со стохастической моделью , известной как модель стохастического высвобождения . [39]
У эукариот на промоторе, зависимом от РНК-полимеразы II, после клиренса промотора TFIIH фосфорилирует серин 5 на карбокси-концевом домене РНК-полимеразы II, что приводит к задействованию кэпирующего фермента (CE). [40] [41] Точный механизм того, как CE индуцирует клиренс промотора у эукариот, пока не известен.

Одна цепь ДНК, матричная цепь (или некодирующая цепь), используется в качестве матрицы для синтеза РНК. По мере продолжения транскрипции РНК-полимераза пересекает цепь матрицы и использует комплементарность спаривания оснований с матрицей ДНК для создания копии РНК (которая удлиняется во время прохождения). Хотя РНК-полимераза пересекает цепь матрицы от 3' → 5', кодирующую (нематричную) цепь и вновь образованную РНК также можно использовать в качестве контрольных точек, поэтому транскрипцию можно описать как происходящую 5' → 3'. В результате образуется молекула РНК из 5' → 3', точная копия кодирующей цепи (за исключением того, что тимины заменены урацилами , а нуклеотиды состоят из рибозного (5-углеродного) сахара, где ДНК содержит дезоксирибозу (на один кислород меньше). атом) в его сахарно-фосфатном остове). [3]
Транскрипция мРНК может включать несколько РНК-полимераз на одной матрице ДНК и несколько раундов транскрипции (амплификация определенной мРНК), поэтому из одной копии гена можно быстро получить множество молекул мРНК. [ нужна цитата ] Характерные скорости удлинения у прокариот и эукариот составляют около 10–100 нт/сек. [42] Однако у эукариот нуклеосомы действуют как основные барьеры для транскрипции полимераз во время элонгации транскрипции. [43] [44] У этих организмов пауза, индуцированная нуклеосомами, может регулироваться факторами элонгации транскрипции, такими как TFIIS. [44]
Удлинение также включает в себя механизм корректуры, который может заменить неправильно включенные основы. У эукариот это может соответствовать коротким паузам во время транскрипции, которые позволяют связываться соответствующим факторам редактирования РНК. Эти паузы могут быть присущи РНК-полимеразе или обусловлены структурой хроматина. [ нужна цитата ]
Бактерии используют две разные стратегии терминации транскрипции – Rho-независимую терминацию и Rho-зависимую терминацию. При Rho-независимой терминации транскрипции транскрипция РНК останавливается, когда вновь синтезированная молекула РНК образует шпильку , богатую GC , за которой следует цепочка Us. Когда образуется шпилька, механический стресс разрывает слабые связи ru-dA, которые теперь заполняют гибрид ДНК-РНК. Это вытягивает транскрипт поли-U из активного сайта РНК-полимеразы, прекращая транскрипцию. При Rho-зависимой терминации Rho , белковый фактор, дестабилизирует взаимодействие между матрицей и мРНК, тем самым высвобождая вновь синтезированную мРНК из элонгационного комплекса. [45]
Терминация транскрипции у эукариот менее изучена, чем у бактерий, но включает расщепление нового транскрипта с последующим независимым от матрицы добавлением аденинов к его новому 3'-концу в процессе, называемом полиаденилированием . [46]
Помимо терминации последовательностями терминатора (которые являются частью гена ) , транскрипция также может нуждаться в остановке при возникновении таких условий, как повреждение ДНК или активная репликационная вилка . У бактерий АТФаза Mfd может удалить РНК-полимеразу, застрявшую в повреждении, открыв ее зажим. Он также задействует механизмы эксцизионной репарации нуклеотидов для устранения повреждения. Предполагается, что Mfd также разрешает конфликты между репликацией и транскрипцией ДНК. [47] У эукайротов АТФаза TTF2 помогает подавлять действие РНКП I и II во время митоза , предотвращая ошибки хромосомной сегрегации. [48] Предполагается, что у архей эта-АТФаза играет аналогичную роль. [49]
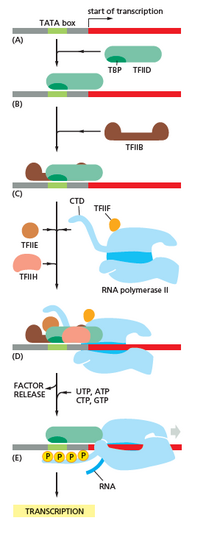
РНК-полимераза играет очень важную роль на всех этапах, включая посттранскрипционные изменения РНК.
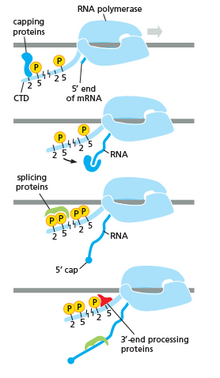
Как показано на изображении справа, очевидно, что CTD (C-концевой домен) представляет собой хвост, который меняет свою форму; этот хвост будет использоваться в качестве носителя сплайсинга, кэпирования и полиаденилирования , как показано на изображении слева. [50]
Ингибиторы транскрипции можно использовать в качестве антибиотиков против, например, патогенных бактерий ( антибактериальные средства ) и грибов ( противогрибковые средства ). Примером такого антибактериального средства является рифампицин , который ингибирует транскрипцию бактериальной ДНК в мРНК путем ингибирования ДНК-зависимой РНК-полимеразы путем связывания ее бета-субъединицы, тогда как 8-гидроксихинолин является противогрибковым ингибитором транскрипции. [51] Эффекты метилирования гистонов также могут ингибировать действие транскрипции. Недавно сообщалось о мощных биоактивных натуральных продуктах, таких как триптолид, которые ингибируют транскрипцию млекопитающих посредством ингибирования субъединицы XPB общего фактора транскрипции TFIIH в качестве конъюгата глюкозы для воздействия на гипоксические раковые клетки с повышенным производством транспортера глюкозы. [52]
У позвоночных большинство промоторов генов содержат островок CpG с многочисленными сайтами CpG . [53] Когда многие сайты CpG промотора гена метилированы, ген становится ингибируемым (заглушенным). [54] Колоректальный рак обычно имеет от 3 до 6 мутаций водителя и от 33 до 66 мутаций автостопщика или пассажира. [55] Однако ингибирование транскрипции (замалчивание) может иметь большее значение, чем мутация, в возникновении прогрессирования рака. Например, при колоректальном раке около 600–800 генов транскрипционно ингибируются метилированием CpG-островков (см. « Регуляция транскрипции при раке »). Репрессия транскрипции при раке может также происходить за счет других эпигенетических механизмов, таких как изменение продукции микроРНК . [56] При раке молочной железы репрессия транскрипции BRCA1 может происходить чаще из-за избыточной продукции микроРНК-182, чем из-за гиперметилирования промотора BRCA1 (см. Низкая экспрессия BRCA1 при раке молочной железы и яичников ). [ нужна цитата ]
Активные единицы транскрипции группируются в ядре в отдельных участках, называемых фабриками транскрипции или эухроматином . Такие сайты можно визуализировать, позволяя вовлеченным полимеразам расширять свои транскрипты в меченых предшественниках (Br-UTP или Br-U) и иммуномаркируя меченую возникающую РНК. Фабрики транскрипции также можно локализовать с помощью флуоресцентной гибридизации in situ или пометить антителами, направленными против полимераз. В нуклеоплазме клетки HeLa имеется ~10 000 фабрик , среди которых ~8 000 фабрик полимеразы II и ~2 000 фабрик полимеразы III. Каждая фабрика полимеразы II содержит ~8 полимераз. Поскольку большинство активных единиц транскрипции связаны только с одной полимеразой, каждая фабрика обычно содержит ~8 различных единиц транскрипции. Эти единицы могут быть связаны через промоторы и/или энхансеры с петлями, образующими «облако» вокруг фактора. [57]
Молекула, которая позволяет генетическому материалу реализоваться в виде белка, была впервые предложена Франсуа Жакобом и Жаком Моно . Северо Очоа получил Нобелевскую премию по физиологии и медицине в 1959 году за разработку процесса синтеза РНК in vitro с помощью полинуклеотидной фосфорилазы , который оказался полезен для взлома генетического кода . Синтез РНК с помощью РНК-полимеразы был установлен in vitro несколькими лабораториями к 1965 году; однако РНК, синтезируемая этими ферментами, обладала свойствами, которые предполагали существование дополнительного фактора, необходимого для правильной терминации транскрипции. [ нужна цитата ]
Роджер Д. Корнберг получил Нобелевскую премию по химии 2006 года «за исследования молекулярных основ эукариотической транскрипции ». [58]

Транскрипцию можно измерить и обнаружить различными способами :

Некоторые вирусы (например , ВИЧ , причина СПИДа ) обладают способностью транскрибировать РНК в ДНК. ВИЧ имеет геном РНК, который обратно транскрибируется в ДНК. Полученная ДНК может быть слита с ДНК генома клетки-хозяина. Основной фермент, ответственный за синтез ДНК из матрицы РНК, называется обратной транскриптазой . [61]
В случае ВИЧ обратная транскриптаза отвечает за синтез цепи ДНК, комплементарной (кДНК) геному вирусной РНК. Затем фермент рибонуклеаза H расщепляет цепь РНК, а обратная транскриптаза синтезирует комплементарную цепь ДНК с образованием структуры двойной спирали ДНК (кДНК). кДНК интегрируется в геном клетки-хозяина с помощью фермента интегразы , который заставляет клетку-хозяина генерировать вирусные белки, которые снова собираются в новые вирусные частицы. При ВИЧ после этого клетка-хозяин подвергается запрограммированной клеточной гибели или апоптозу Т- клеток . [62] Однако у других ретровирусов клетка-хозяин остается интактной, когда вирус отпочковывается из клетки. [ нужна цитата ]
Некоторые эукариотические клетки содержат фермент с активностью обратной транскрипции, называемый теломеразой . Теломераза переносит матрицу РНК, из которой она синтезирует теломеры , повторяющуюся последовательность ДНК, до конца линейных хромосом. Это важно, потому что каждый раз, когда линейная хромосома удваивается, она укорачивается. Поскольку теломеры находятся на концах хромосом, укорочение устраняет часть несущественных повторяющихся последовательностей, а не последовательность ДНК, кодирующую белок, расположенную дальше от конца хромосомы.
Теломераза часто активируется в раковых клетках, чтобы позволить раковым клеткам бесконечно дублировать свои геномы без потери важной последовательности ДНК, кодирующей белок. Активация теломеразы может быть частью процесса, который позволяет раковым клеткам стать бессмертными. Доказано, что иммортизирующий фактор рака посредством удлинения теломер за счет теломеразы встречается в 90% всех канцерогенных опухолей in vivo , а в оставшихся 10% используется альтернативный путь поддержания теломер, называемый АЛТ или альтернативное удлинение теломер. [63]