Алюминий ( алюминий в североамериканском английском ) — химический элемент ; он имеет символ Al и атомный номер 13. Алюминий имеет плотность ниже, чем у других обычных металлов ; примерно на одну треть меньше, чем у стали . Он имеет большое сродство к кислороду , образуя на поверхности защитный слой оксида при воздействии воздуха. Алюминий визуально напоминает серебро как по цвету, так и по своей способности отражать свет. Он мягкий, немагнитный и пластичный . Он имеет один стабильный изотоп: 27 Al, которого очень много, что делает алюминий двенадцатым по распространенности элементом во Вселенной. Радиоактивность 26 Al используется при радиометрическом датировании .
Химически алюминий представляет собой постпереходный металл группы бора ; Как обычно для этой группы, алюминий образует соединения преимущественно со степенью окисления +3 . Катион алюминия Al 3+ имеет небольшой размер и сильно заряжен ; как таковой он обладает большей поляризующей способностью , а связи, образуемые алюминием, имеют более ковалентный характер. Сильное сродство алюминия к кислороду приводит к широкому распространению его оксидов в природе. Алюминий встречается на Земле в основном в горных породах земной коры , где он является третьим по распространенности элементом после кислорода и кремния , а не в мантии , и практически никогда в виде свободного металла . Его получают в промышленных масштабах путем добычи боксита , осадочной породы, богатой минералами алюминия.
Об открытии алюминия объявил в 1825 году датский физик Ганс Кристиан Эрстед . Первое промышленное производство алюминия было инициировано французским химиком Анри Этьеном Сент-Клер Девилем в 1856 году. Алюминий стал гораздо более доступным для общественности благодаря процессу Холла-Эру, разработанному независимо французским инженером Полем Эру и американским инженером Шарлем Мартином Холлом в 1886 году. а массовое производство алюминия привело к его широкому использованию в промышленности и быту. В Первой и Второй мировых войнах алюминий был важнейшим стратегическим ресурсом для авиации . В 1954 году алюминий стал самым производимым цветным металлом , обогнав медь . В 21 веке большая часть алюминия потреблялась в сфере транспорта, машиностроения, строительства и упаковки в США, Западной Европе и Японии.
Несмотря на широкое распространение в окружающей среде, ни один живой организм не использует соли алюминия для метаболизма , но алюминий хорошо переносится растениями и животными. Из-за обилия этих солей потенциальная их биологическая роль представляет интерес, и исследования продолжаются.
Из изотопов алюминия только27
Ал
является стабильным. Такая ситуация характерна для элементов с нечетным атомным номером. [б] Это единственный первичный изотоп алюминия, т.е. единственный, который существовал на Земле в его нынешнем виде с момента образования планеты. Следовательно, это мононуклидный элемент , и его стандартный атомный вес практически такой же, как у изотопа. Это делает алюминий очень полезным для ядерного магнитного резонанса (ЯМР), поскольку его единственный стабильный изотоп обладает высокой чувствительностью ЯМР. [11] Стандартный атомный вес алюминия невелик по сравнению со многими другими металлами. [с]
Все остальные изотопы алюминия радиоактивны . Самым стабильным из них является 26 Al : хотя он присутствовал вместе со стабильным 27 Al в межзвездной среде, из которой сформировалась Солнечная система, и был также произведен в результате звездного нуклеосинтеза , его период полураспада составляет всего 717 000 лет и, следовательно, поддается обнаружению. Сумма не сохранилась со времен образования планеты. [12] Однако мельчайшие следы 26 Al образуются из аргона в атмосфере в результате расщепления, вызванного протонами космических лучей . Отношение 26 Al к 10 Be использовалось для радиодатирования геологических процессов в масштабах времени от 10 5 до 10 6 лет, в частности, переноса, осаждения, хранения отложений , времени захоронения и эрозии. [13] Большинство учёных, изучающих метеориты, считают, что энергия, высвободившаяся при распаде 26 Al, была ответственна за плавление и дифференциацию некоторых астероидов после их образования 4,55 миллиарда лет назад. [14]
Остальные изотопы алюминия с массовыми числами от 22 до 43 имеют период полураспада значительно меньше часа. Известны три метастабильных состояния, все с периодом полураспада менее минуты. [10]
Атом алюминия имеет 13 электронов, расположенных в электронной конфигурации [ Ne ] 3s 2 3p 1 , [ 15] с тремя электронами за пределами стабильной конфигурации благородного газа. Соответственно, объединенные первые три энергии ионизации алюминия намного ниже, чем одна только четвертая энергия ионизации. [16] Такая электронная конфигурация является общей с другими хорошо изученными членами этой группы: бором , галлием , индием и таллием ; это также ожидается для нихония . Алюминий может отдавать свои три крайних электрона во многих химических реакциях (см. ниже). Электроотрицательность алюминия равна 1,61 (по шкале Полинга) . [17]

Свободный атом алюминия имеет радиус 143 пм . [18] При удалении трех крайних электронов радиус уменьшается до 39 пм для 4-координационного атома или до 53,5 пм для 6-координационного атома. [18] При стандартной температуре и давлении атомы алюминия (если на них не влияют атомы других элементов) образуют гранецентрированную кубическую кристаллическую систему , связанную металлической связью, обеспечиваемой внешними электронами атомов; следовательно, алюминий (в этих условиях) является металлом. [19] Эту кристаллическую систему разделяют многие другие металлы, такие как свинец и медь ; размер элементарной ячейки алюминия сравним с размером элементарной ячейки других металлов. [19] Однако эта система не является общей для других членов ее группы; энергия ионизации бора слишком высока, чтобы обеспечить металлизацию, таллий имеет гексагональную плотноупакованную структуру, а галлий и индий имеют необычные структуры, которые не являются плотноупакованными, как структуры алюминия и таллия. Немногие электроны, которые доступны для металлической связи в металлическом алюминии, являются вероятной причиной его мягкости, низкой температуры плавления и низкого удельного электрического сопротивления . [20]
Металлический алюминий имеет внешний вид от серебристо-белого до тускло-серого, в зависимости от шероховатости поверхности . [d] Алюминиевые зеркала являются наиболее отражающими из всех металлических зеркал для ближнего ультрафиолетового и дальнего инфракрасного света и одними из наиболее отражающих в видимом спектре, почти на одном уровне с серебром, и поэтому они оба выглядят одинаково. Алюминий также хорошо отражает солнечную радиацию , хотя длительное воздействие солнечных лучей на воздухе увеличивает износ поверхности металла; этого можно предотвратить, если алюминий анодирован , что создает на поверхности защитный слой оксида.
Плотность алюминия составляет 2,70 г/см 3 , что составляет около 1/3 плотности стали, что намного ниже, чем у других обычно встречающихся металлов, что позволяет легко идентифицировать алюминиевые детали по их легкости. [23] Низкая плотность алюминия по сравнению с большинством других металлов обусловлена тем, что его ядра намного легче, а разница в размерах элементарной ячейки не компенсирует эту разницу. Единственными более легкими металлами являются металлы 1 и 2 групп , которые, за исключением бериллия и магния , слишком реакционноспособны для конструкционного использования (а бериллий очень токсичен). [24] Алюминий не такой прочный и жесткий, как сталь, но низкая плотность компенсирует это в аэрокосмической промышленности и во многих других приложениях, где легкий вес и относительно высокая прочность имеют решающее значение. [25]
Чистый алюминий довольно мягкий и недостаточно прочный. В большинстве случаев вместо них используются различные алюминиевые сплавы из-за их более высокой прочности и твердости. [26] Предел текучести чистого алюминия составляет 7–11 МПа , тогда как алюминиевые сплавы имеют предел текучести от 200 до 600 МПа. [27] Алюминий пластичен , с процентным удлинением 50-70%, [28] и податлив , что позволяет его легко тянуть и экструдировать . [29] Он также легко обрабатывается и отливается . [29]
Алюминий является отличным проводником тепла и электричества , его проводимость составляет около 60% от проводимости меди , как тепловой, так и электрической, при этом его плотность составляет всего 30% от плотности меди. [30] Алюминий обладает сверхпроводимостью , его критическая температура сверхпроводимости составляет 1,2 Кельвина , а критическое магнитное поле составляет около 100 гаусс (10 миллитесл ). [31] Он парамагнитен и поэтому практически не подвержен влиянию статических магнитных полей. [32] Однако высокая электропроводность означает, что на нее сильно влияют переменные магнитные поля за счет индукции вихревых токов . [33]
Алюминий сочетает в себе характеристики металлов до и после перехода. Поскольку у него мало доступных электронов для металлической связи, как и у его более тяжелых собратьев из группы 13 , он обладает характерными физическими свойствами постпереходного металла с более длинными, чем ожидалось, межатомными расстояниями. [20] Кроме того, поскольку Al 3+ представляет собой небольшой и сильно заряженный катион, он обладает сильной поляризацией, и связи в соединениях алюминия имеют тенденцию к ковалентности ; [34] это поведение похоже на поведение бериллия (Be 2+ ), и они демонстрируют пример диагонального отношения . [35]
Базовое ядро под валентной оболочкой алюминия представляет собой ядро предыдущего благородного газа , тогда как ядра его более тяжелых родственников галлия , индия , таллия и нихония также включают заполненную d-подоболочку и в некоторых случаях заполненную f-подоболочку. Следовательно, внутренние электроны алюминия почти полностью экранируют валентные электроны, в отличие от электронов более тяжелых родственников алюминия. Таким образом, алюминий является наиболее электроположительным металлом в своей группе, а его гидроксид фактически более основной, чем гидроксид галлия. [34] [e] Алюминий также имеет незначительное сходство с металлоидным бором из той же группы: соединения AlX 3 валентно изоэлектронны соединениям BX 3 (они имеют одинаковую валентную электронную структуру), и оба ведут себя как кислоты Льюиса и легко образуют аддукты . . [36] Кроме того, одним из основных мотивов химии бора являются правильные икосаэдрические структуры, а алюминий составляет важную часть многих икосаэдрических квазикристаллических сплавов, включая класс Al-Zn-Mg. [37]
Алюминий имеет высокое химическое сродство к кислороду, что делает его пригодным для использования в качестве восстановителя в термитной реакции. Мелкий порошок металлического алюминия взрывается при контакте с жидким кислородом ; однако в нормальных условиях алюминий образует тонкий оксидный слой (около 5 нм при комнатной температуре) [38] , который защищает металл от дальнейшей коррозии кислородом, водой или разбавленной кислотой — процесс, называемый пассивацией . [34] [39] Благодаря своей общей устойчивости к коррозии алюминий является одним из немногих металлов, которые сохраняют серебристую отражательную способность в виде мелкого порошка, что делает его важным компонентом серебристых красок . [40] Алюминий не подвергается воздействию окисляющих кислот из-за его пассивации. Это позволяет использовать алюминий для хранения таких реагентов, как азотная кислота , концентрированная серная кислота и некоторые органические кислоты. [41]
В горячей концентрированной соляной кислоте алюминий реагирует с водой с выделением водорода, а в водном растворе гидроксида натрия или гидроксида калия при комнатной температуре с образованием алюминатов — защитная пассивация в этих условиях незначительна. [42] Царская водка также растворяет алюминий. [41] Алюминий разъедает растворенные хлориды , такие как обычный хлорид натрия , поэтому бытовая сантехника никогда не изготавливается из алюминия. [42] Оксидный слой на алюминии разрушается также при контакте с ртутью вследствие амальгамации или с солями некоторых электроположительных металлов. [34] Таким образом, самые прочные алюминиевые сплавы менее устойчивы к коррозии из-за гальванических реакций с легированной медью , [27] а коррозионная стойкость алюминия значительно снижается под действием водных солей, особенно в присутствии разнородных металлов. [20]
Алюминий реагирует с большинством неметаллов при нагревании, образуя такие соединения, как нитрид алюминия (AlN), сульфид алюминия (Al 2 S 3 ) и галогениды алюминия (AlX 3 ). Он также образует широкий спектр интерметаллических соединений , включающих металлы всех групп периодической таблицы. [34]
Подавляющее большинство соединений, включая все алюминийсодержащие минералы и все коммерчески значимые соединения алюминия, содержат алюминий в степени окисления 3+. Координационное число таких соединений варьируется, но обычно Al 3+ является шести- или четырехкоординационным. Почти все соединения алюминия(III) бесцветны. [34]
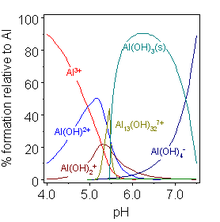
В водном растворе Al 3+ существует в виде гексааква-катиона [Al(H 2 O) 6 ] 3+ , который имеет приблизительное значение K a 10 -5 . [11] Такие растворы являются кислыми, поскольку этот катион может действовать как донор протонов и постепенно гидролизоваться до тех пор, пока не образуется осадок гидроксида алюминия Al(OH) 3 . Это полезно для осветления воды, поскольку осадок образует зародыши на взвешенных частицах в воде, тем самым удаляя их. Дальнейшее повышение pH приводит к повторному растворению гидроксида с образованием алюмината [Al(H 2 O) 2 (OH) 4 ] - .
Гидроксид алюминия образует как соли, так и алюминаты, растворяется в кислотах и щелочах, а также при сплавлении с кислотными и основными оксидами. [34] Такое поведение Al(OH) 3 называется амфотеризмом и характерно для слабоосновных катионов, образующих нерастворимые гидроксиды и гидратированные формы которых также могут отдавать свои протоны. Одним из последствий этого является то, что соли алюминия со слабыми кислотами гидролизуются в воде до водного гидроксида и соответствующего гидрида неметалла: например, сульфид алюминия дает сероводород . Однако некоторые соли, такие как карбонат алюминия, существуют в водных растворах, но сами по себе нестабильны; и только неполный гидролиз имеет место для солей с сильными кислотами, такими как галогениды, нитраты и сульфаты . По тем же причинам безводные соли алюминия не могут быть получены путем нагревания их «гидратов»: гидратированный хлорид алюминия на самом деле представляет собой не AlCl 3 ·6H 2 O, а [Al(H 2 O) 6 ]Cl 3 , а связи Al–O настолько сильные, что нагревания недостаточно, чтобы разорвать их и вместо этого образовать связи Al–Cl: [34]
Все четыре тригалогенида хорошо известны. В отличие от структур трех более тяжелых тригалогенидов, фторид алюминия (AlF 3 ) представляет собой шестикоординированный алюминий, что объясняет его нелетучесть и нерастворимость, а также высокую теплоту образования . Каждый атом алюминия окружен шестью атомами фтора в искаженном октаэдрическом расположении, причем каждый атом фтора находится между углами двух октаэдров. Такие звенья {AlF 6 } также существуют в сложных фторидах, таких как криолит Na 3 AlF 6 . [f] AlF 3 плавится при 1290 °C (2354 °F) и получается в результате реакции оксида алюминия с газообразным фтороводородом при 700 °C (1300 °F). [44]
У более тяжелых галогенидов координационные числа ниже. Остальные тригалогениды являются димерными или полимерными с тетраэдрическими четырехкоординатными алюминиевыми центрами. [g] Трихлорид алюминия (AlCl 3 ) имеет слоистую полимерную структуру ниже температуры плавления 192,4 ° C (378 ° F), но при плавлении превращается в димеры Al 2 Cl 6 . При более высоких температурах они все больше диссоциируют на тригональные плоские мономеры AlCl 3 , аналогичные структуре BCl 3 . Трибромид и трииодид алюминия образуют димеры Al 2 X 6 во всех трех фазах и поэтому не проявляют столь значительных изменений свойств при фазовом переходе. [44] Эти материалы получают путем обработки металлического алюминия галогеном. Тригалогениды алюминия образуют множество аддитивных соединений или комплексов; их кислая природа Льюиса делает их полезными в качестве катализаторов реакций Фриделя-Крафтса . Трихлорид алюминия имеет широкое промышленное применение, связанное с этой реакцией, например, при производстве антрахинонов и стирола ; он также часто используется в качестве предшественника многих других соединений алюминия и в качестве реагента для преобразования фторидов неметаллов в соответствующие хлориды (реакция трансгалогенирования ). [44]
Алюминий образует один стабильный оксид с химической формулой Al 2 O 3 , обычно называемый глиноземом . [45] В природе его можно найти в минерале корунде , α-глиноземе; [46] имеется также фаза γ-оксида алюминия. [11] Его кристаллическая форма, корунд , очень тверда ( твердость по шкале Мооса 9), имеет высокую температуру плавления 2045 °C (3713 °F), имеет очень низкую летучесть, химически инертна и является хорошим электрическим изолятором. часто используется в абразивах (например, в зубной пасте), в качестве огнеупорного материала и в керамике , а также является исходным материалом для электролитического производства металлического алюминия. Сапфир и рубин — это нечистый корунд, загрязненный следами других металлов. [11] Двумя основными оксидами-гидроксидами AlO(OH) являются бемит и диаспор . Существует три основных тригидроксида: байерит , гиббсит и нордстрандит, которые различаются по своей кристаллической структуре ( полиморфам ). Известны также многие другие промежуточные и родственные структуры. [11] Большинство из них производятся из руд различными мокрыми процессами с использованием кислоты и основания. Нагревание гидроксидов приводит к образованию корунда. Эти материалы имеют решающее значение для производства алюминия и сами по себе чрезвычайно полезны. Некоторые смешанные оксидные фазы также очень полезны, например, шпинель (MgAl 2 O 4 ), Na-β-оксид алюминия (NaAl 11 O 17 ) и алюминат трикальция (Ca 3 Al 2 O 6 , важная минеральная фаза в портландцементе ). . [11]
Единственными стабильными халькогенидами при нормальных условиях являются сульфид алюминия (Al 2 S 3 ), селенид (Al 2 Se 3 ) и теллурид (Al 2 Te 3 ). Все три получают путем прямой реакции их элементов при температуре около 1000 ° C (1800 ° F) и быстро полностью гидролизуются в воде с образованием гидроксида алюминия и соответствующего халькогенида водорода . Поскольку алюминий является небольшим атомом по сравнению с этими халькогенами, они имеют четырехкоординированный тетраэдрический алюминий с различными полиморфными модификациями, имеющими структуры, связанные с вюрцитом , с двумя третями возможных металлических участков, занятых либо упорядоченным (α), либо случайным (β) образом. ; сульфид также имеет γ-форму, родственную γ-оксиду алюминия, и необычную высокотемпературную гексагональную форму, в которой половина атомов алюминия имеет тетраэдрическую четырехкоординацию, а другая половина имеет тригонально-бипирамидальную пятикоординацию. [47]
Известны четыре пниктида : нитрид алюминия (AlN), фосфид алюминия (AlP), арсенид алюминия (AlAs) и антимонид алюминия (AlSb). Все они представляют собой полупроводники III-V, изоэлектронные кремнию и германию , все из которых, кроме AlN, имеют структуру цинковой обманки . Все четыре могут быть получены путем прямой реакции составляющих их элементов при высокой температуре (и, возможно, высоком давлении). [47]
Алюминий хорошо сплавляется с большинством других металлов (за исключением большинства щелочных металлов и металлов 13-й группы) и известно более 150 интерметаллидов с другими металлами. Подготовка включает нагревание фиксированных металлов вместе в определенной пропорции с последующим постепенным охлаждением и отжигом . Связь в них преимущественно металлическая и кристаллическая структура в первую очередь зависит от эффективности упаковки. [48]
Соединений с более низкими степенями окисления немного. Существует несколько соединений алюминия (I) : AlF, AlCl, AlBr и AlI существуют в газовой фазе, когда соответствующий тригалогенид нагревается с алюминием и при криогенных температурах. [44] Стабильным производным моноиодида алюминия является циклический аддукт , образующийся с триэтиламином Al 4 I 4 (NEt 3 ) 4 . Al 2 O и Al 2 S также существуют, но они очень нестабильны. [49] Очень простые соединения алюминия(II) возникают или наблюдаются в реакциях металлического Al с окислителями. Например, окись алюминия AlO была обнаружена в газовой фазе после взрыва [50] и в спектрах поглощения звезд. [51] Более тщательно изучены соединения формулы R 4 Al 2 , которые содержат связь Al-Al и где R - крупный органический лиганд . [52]
Существует множество соединений брутто-формулы AlR 3 и AlR 1,5 Cl 1,5 . [53] Триалкилы и триарилы алюминия представляют собой реакционноспособные, летучие и бесцветные жидкости или легкоплавкие твердые вещества. Они самовозгораются на воздухе и реагируют с водой, что требует соблюдения мер предосторожности при обращении с ними. Они часто образуют димеры, в отличие от своих борных аналогов, но эта тенденция уменьшается для алкилов с разветвленной цепью (например, Pri, Bu i , Me 3 CCH 2 ) ; например, триизобутилалюминий существует в виде равновесной смеси мономера и димера. [54] [55] Эти димеры, такие как триметилалюминий (Al 2 Me 6 ), обычно имеют тетраэдрические центры Al, образованные в результате димеризации с некоторым количеством алкильных групп, соединяющих оба атома алюминия. Они представляют собой жесткие кислоты и легко реагируют с лигандами, образуя аддукты. В промышленности они в основном используются в реакциях внедрения алкенов, как обнаружил Карл Циглер , наиболее важно в «реакциях роста», которые образуют длинноцепные неразветвленные первичные алкены и спирты, а также в полимеризации под низким давлением этена и пропена . Существуют также некоторые гетероциклические и кластерные алюминийорганические соединения со связями Al–N. [54]
Наиболее важным в промышленном отношении гидридом алюминия является алюмогидрид лития (LiAlH 4 ), который используется в качестве восстановителя в органической химии . Его можно производить из гидрида лития и трихлорида алюминия . [56] Самый простой гидрид, гидрид алюминия или алан, не так важен. Это полимер формулы (AlH 3 ) n , в отличие от соответствующего гидрида бора, который представляет собой димер с формулой (BH 3 ) 2 . [56]
Содержание алюминия на частицу в Солнечной системе составляет 3,15 частей на миллион (частей на миллион). [57] [h] Это двенадцатый по распространенности среди всех элементов и третий по распространенности среди элементов с нечетными атомными номерами после водорода и азота. [57] Единственный стабильный изотоп алюминия, 27 Al, является восемнадцатым по распространенности ядром во Вселенной. Он почти полностью образуется в результате синтеза углерода в массивных звездах, которые позже станут сверхновыми типа II : в результате этого синтеза образуется 26 Mg, который при захвате свободных протонов и нейтронов становится алюминием. Некоторые меньшие количества 27 Al образуются в горящих водородных оболочках эволюционировавших звезд, где 26 Mg может захватывать свободные протоны. [58] По существу, весь существующий сейчас алюминий представляет собой 27 Al. 26 Al присутствовал в ранней Солнечной системе в количестве 0,005% по сравнению с 27 Al, но его период полураспада в 728 000 лет слишком короток для выживания каких-либо первоначальных ядер; 26 Таким образом, Al вымер . [58] В отличие от 27 Al, горение водорода является основным источником 26 Al, при этом нуклид появляется после того, как ядро 25 Mg захватывает свободный протон. Однако следовые количества 26 Al, которые действительно существуют, являются наиболее распространенным излучателем гамма-лучей в межзвездном газе ; [58] если бы первоначальный 26 Al все еще присутствовал, карты гамма-лучей Млечного Пути были бы ярче. [58]

В целом Земля состоит из алюминия примерно на 1,59% по массе (седьмое место по массе). [59] Алюминий встречается в большей степени в земной коре, чем во Вселенной в целом, потому что алюминий легко образует оксид, связывается с горными породами и остается в земной коре , в то время как менее химически активные металлы оседают в ядро. [58] В земной коре алюминий является наиболее распространенным металлическим элементом (8,23% по массе [28] ) и третьим по распространенности из всех элементов (после кислорода и кремния). [60] Большое количество силикатов в земной коре содержат алюминий. [61] Напротив, мантия Земли состоит всего из 2,38% алюминия по массе. [62] Алюминий также встречается в морской воде в концентрации 2 мкг/кг. [28]
Из-за сильного сродства к кислороду алюминий почти никогда не встречается в элементарном состоянии; вместо этого он содержится в оксидах или силикатах. Полевые шпаты , наиболее распространенная группа минералов в земной коре, представляют собой алюмосиликаты. Алюминий встречается также в минералах берилле , криолите , гранате , шпинели и бирюзе . [63] Примеси в Al 2 O 3 , такие как хром и железо , дают драгоценные камни рубин и сапфир соответственно. [64] Самородный металлический алюминий встречается крайне редко и может быть обнаружен только в качестве второстепенной фазы в средах с низкой фугитивностью кислорода , например, в недрах некоторых вулканов. [65] Самородный алюминий был обнаружен в холодных просачиваниях на северо-восточном континентальном склоне Южно -Китайского моря . Возможно, эти отложения образовались в результате бактериального восстановления тетрагидроксоалюмината Al(OH) 4 - . [66]
Хотя алюминий является обычным и широко распространенным элементом, не все минералы алюминия являются экономически выгодными источниками металла. Практически весь металлический алюминий производится из бокситовой руды (AlO x (OH) 3–2 x ). Боксит возникает как продукт выветривания коренных пород с низким содержанием железа и кремнезема в тропических климатических условиях. [67] В 2017 году большая часть бокситов добывалась в Австралии, Китае, Гвинее и Индии. [68]

История алюминия сформировалась благодаря использованию квасцов . Первое письменное упоминание о квасцах, сделанное греческим историком Геродотом , относится к V веку до нашей эры. [69] Известно, что древние использовали квасцы в качестве протравы для окрашивания и для защиты города. [69] После крестовых походов квасцы, незаменимый товар в европейской тканевой промышленности, [70] стали предметом международной торговли; [71] он был импортирован в Европу из восточного Средиземноморья до середины 15 века. [72]
Природа квасцов осталась неизвестной. Около 1530 года швейцарский врач Парацельс предположил, что квасцы — это соль квасцовой земли. [73] В 1595 году немецкий врач и химик Андреас Либавиус экспериментально подтвердил это. [74] В 1722 году немецкий химик Фридрих Гофман заявил о своей убежденности в том, что основой квасцов является отдельная земля. [75] В 1754 году немецкий химик Андреас Сигизмунд Маргграф синтезировал глинозем путем кипячения глины в серной кислоте и последующего добавления поташа . [75]
Попытки производить металлический алюминий датируются 1760 годом. [76] Однако первая успешная попытка была предпринята в 1824 году датским физиком и химиком Гансом Кристианом Эрстедом . Он прореагировал безводный хлорид алюминия с амальгамой калия , получив кусок металла, похожий на олово. [77] [78] [79] Он представил свои результаты и продемонстрировал образец нового металла в 1825 году. [80] [81] В 1827 году немецкий химик Фридрих Вёлер повторил эксперименты Эрстеда, но не выявил алюминия. [82] (Причина этого несоответствия была обнаружена только в 1921 году.) [83] В том же году он провел аналогичный эксперимент, смешав безводный хлорид алюминия с калием и получив порошок алюминия. [79] В 1845 году он смог изготовить небольшие кусочки металла и описал некоторые физические свойства этого металла. [83] В течение многих лет после этого Вёлер считался первооткрывателем алюминия. [84]

Поскольку метод Велера не мог дать большого количества алюминия, металл оставался редким; его стоимость превышала стоимость золота. [82] Первое промышленное производство алюминия было налажено в 1856 году французским химиком Анри Этьеном Сент-Клер Девилем и его товарищами. [85] Девиль обнаружил, что трихлорид алюминия можно восстановить с помощью натрия, который был более удобным и менее дорогим, чем калий, который использовал Велер. [86] Даже тогда алюминий еще не отличался особой чистотой, и производимый алюминий различался по свойствам в зависимости от образца. [87] Из-за своей электропроводной способности алюминий использовался в качестве крышки Монумента Вашингтона , построенного в 1885 году. Это самое высокое здание в мире того времени, нержавеющая металлическая крышка предназначалась для использования в качестве громоотвода . вершина горы.
Первый промышленный метод крупномасштабного производства был независимо разработан в 1886 году французским инженером Полем Эру и американским инженером Чарльзом Мартином Холлом ; теперь он известен как процесс Холла-Эру . [88] Процесс Холла-Эру превращает глинозем в металл. В 1889 году австрийский химик Карл Йозеф Байер открыл способ очистки боксита для получения глинозема, ныне известный как процесс Байера . [89] Современное производство металлического алюминия основано на процессах Байера и Холла-Эру. [90]
Цены на алюминий упали, и в 1890-х и начале 20-го века алюминий стал широко использоваться в ювелирных изделиях, предметах повседневного обихода, оправах для очков, оптических инструментах, посуде и фольге . Способность алюминия образовывать твердые, но легкие сплавы с другими металлами в то время обеспечивала этому металлу множество применений. [91] Во время Первой мировой войны правительства крупных стран требовали больших поставок алюминия для легких и прочных планеров; [92] Во время Второй мировой войны спрос на авиацию со стороны крупных правительств был еще выше. [93] [94] [95]
К середине 20 века алюминий стал частью повседневной жизни и важным компонентом предметов домашнего обихода. [96] В 1954 году производство алюминия превысило производство меди , [i] исторически уступая по производству только железу, [99] что сделало его самым производимым цветным металлом . В середине 20-го века алюминий появился в качестве материала для гражданского строительства, его можно было использовать как в базовом строительстве, так и в работах по внутренней отделке [100] и все чаще он использовался в военном машиностроении, как для самолетов, так и для двигателей наземных бронетранспортеров. [101] Первый искусственный спутник Земли , запущенный в 1957 году, состоял из двух отдельных соединенных алюминиевых полусфер, и все последующие космические аппараты в той или иной степени использовали алюминий. [90] Алюминиевая банка была изобретена в 1956 году и использовалась в качестве хранилища для напитков в 1958 году. [102]
На протяжении всего ХХ века производство алюминия быстро росло: хотя мировое производство алюминия в 1900 году составляло 6800 метрических тонн, годовой объем производства впервые превысил 100 000 метрических тонн в 1916 году; 1 000 000 тонн в 1941 году; 10 000 000 тонн в 1971 году. [97] В 1970-х годах возросший спрос на алюминий сделал его биржевым товаром; в 1978 году он вошёл на Лондонскую биржу металлов , старейшую промышленную биржу металлов в мире .
Реальная цена на алюминий снизилась с 14 000 долларов за метрическую тонну в 1900 году до 2340 долларов в 1948 году (в долларах США 1998 года). [97] Затраты на добычу и переработку были снижены в связи с технологическим прогрессом и масштабом экономики. Однако необходимость разработки месторождений с более низким содержанием и более низким качеством и использование быстро растущих производственных затрат (прежде всего, энергии) увеличили чистую стоимость алюминия; [103] Реальная цена начала расти в 1970-х годах с ростом стоимости энергии. [104] Производство переместилось из промышленно развитых стран в страны, где продукция была дешевле. [105] Производственные затраты в конце 20 века изменились из-за развития технологий, снижения цен на энергоносители, обменного курса доллара США и цен на глинозем. [106] Совокупная доля стран БРИК в первичном производстве и первичном потреблении существенно выросла в первое десятилетие XXI века. [107] Китай аккумулирует особенно большую долю мирового производства благодаря изобилию ресурсов, дешевой энергии и правительственным стимулам; [108] он также увеличил свою долю потребления с 2% в 1972 году до 40% в 2010 году . [109] В США, Западной Европе и Японии большая часть алюминия потреблялась в сфере транспорта, машиностроения, строительства и упаковки. [110] В 2021 году цены на промышленные металлы, такие как алюминий, взлетели до почти рекордного уровня, поскольку из-за нехватки энергии в Китае растут затраты на электроэнергию. [111]
Названия «алюминий» и «алюминий» происходят от слова «глинозем» , устаревшего термина, обозначающего оксид алюминия , [j] встречающегося в природе оксида алюминия . [113] Глинозем был заимствован из французского языка, который, в свою очередь, получил его от alumen , классического латинского названия квасцов , минерала, из которого он был собран. [114] Латинское слово alumen происходит от протоиндоевропейского корня *alu-, означающего «горький» или «пиво». [115]

Британский химик Хамфри Дэви , который провел ряд экспериментов, направленных на выделение металла, считается человеком, давшим название этому элементу. Первым названием, предложенным для выделения металла из квасцов, было алюминий , которое Дэви предложил в статье 1808 года о своих электрохимических исследованиях, опубликованной в журнале Philosophical Transactions of the Royal Society . [116] Оказалось, что название было создано из английского слова квасцы и латинского суффикса -ium ; но тогда было принято давать элементам имена, происходящие от латыни, поэтому это название не было принято повсеместно. Это название подверглось критике со стороны современных химиков из Франции, Германии и Швеции, которые настаивали на том, чтобы металл был назван в честь оксида алюминия, из которого он будет выделен. [117] Английское название квасцы не происходит напрямую от латыни, тогда как алюминий / глинозем, очевидно, происходит от латинского слова alumen (при склонении alumen меняется на alumin- ).
Одним из примеров был Essai sur la Nomenclature chimique (июль 1811 г.), написанный на французском языке шведским химиком Йонсом Якобом Берцелиусом , в котором название « алюминий» дано элементу, который будет синтезирован из квасцов. [118] [k] (Другая статья в том же номере журнала также упоминает металл, оксид которого является основой сапфира , то есть того же металла, что и алюминий .) [120] Краткое изложение одной из лекций Дэви в январе 1811 года в Королевское общество упомянуло возможное название «алюминий» . [121] В следующем году Дэви опубликовал учебник химии, в котором использовал слово «алюминий» . [122] С тех пор оба варианта написания сосуществовали. В настоящее время их использование носит региональный характер: алюминий доминирует в США и Канаде; алюминий широко распространен в остальном англоязычном мире. [123]
В 1812 году британский учёный Томас Янг [ 124] написал анонимную рецензию на книгу Дэви, в которой предложил название « алюминий» вместо «алюминий », которое, по его мнению, имело «менее классическое звучание». [125] Это имя прижилось: хотя написание -um иногда использовалось в Великобритании, в американском научном языке с самого начала использовалось -ium . [126] Большинство ученых во всем мире использовали -ий в 19 веке; [123] и оно закрепилось в нескольких других европейских языках, таких как французский , немецкий и голландский . [l] В 1828 году американский лексикограф Ной Вебстер ввёл в свой Американский словарь английского языка только написание алюминия . [127] В 1830-х годах написание -um получило распространение в Соединенных Штатах; к 1860-м годам это написание стало более распространенным за пределами науки. [126] В 1892 году Холл использовал написание -um в своей рекламной листовке для своего нового электролитического метода производства металла, несмотря на то, что он постоянно использовал написание -ium во всех патентах, которые он подал в период с 1886 по 1903 год: неизвестно, было ли такое написание введено ошибочно или намеренно; но Холл предпочитал алюминий с момента его появления, потому что он напоминал платину — название престижного металла. [128] К 1890 году оба написания были распространены в Соединенных Штатах, написание -ium было немного более распространенным; к 1895 году ситуация изменилась; к 1900 году алюминий стал в два раза более распространенным, чем алюминий ; в следующем десятилетии написание -um доминировало в американском использовании. В 1925 году Американское химическое общество приняло это написание. [123]
Международный союз теоретической и прикладной химии (IUPAC) принял алюминий в качестве стандартного международного названия элемента в 1990 году. [129] В 1993 году они признали алюминий приемлемым вариантом; [129] самое последнее издание номенклатуры неорганической химии ИЮПАК 2005 года также признает это написание. [130] В официальных публикациях ИЮПАК в качестве основного используется написание -ium , и там, где это уместно, они перечисляют оба варианта. [м]
Производство алюминия начинается с добычи бокситовой породы из земли. Боксит обрабатывается и превращается с помощью процесса Байера в глинозем , который затем обрабатывается с использованием процесса Холла-Эру , в результате чего получается конечный металлический алюминий.
Производство алюминия очень энергозатратно, поэтому производители стремятся размещать плавильные заводы в местах, где электроэнергии много и она недорогая. [133] Для производства одного килограмма алюминия требуется 7 килограммов нефтяного энергетического эквивалента по сравнению с 1,5 килограммами для стали и 2 килограммами для пластика. [134] По состоянию на 2019 год крупнейшие в мире заводы по производству алюминия расположены в Китае, Индии, России, Канаде и Объединенных Арабских Эмиратах, [132] в то время как Китай на сегодняшний день является крупнейшим производителем алюминия с мировой долей в пятьдесят пять процентов.
Согласно отчету Международной группы ресурсов о запасах металлов в обществе , глобальные запасы алюминия на душу населения , используемого в обществе (т.е. в автомобилях, зданиях, электронике и т. д.), составляют 80 кг (180 фунтов). Большая часть этого приходится на более развитые страны (350–500 кг (770–1100 фунтов) на душу населения), а не на менее развитые страны (35 кг (77 фунтов) на душу населения). [135]
Боксит преобразуется в глинозем методом Байера. Боксит смешивают до однородного состава, а затем измельчают. Полученную суспензию смешивают с горячим раствором гидроксида натрия ; затем смесь обрабатывают в варочном котле при давлении значительно выше атмосферного, растворяя гидроксид алюминия в боксите и превращая примеси в относительно нерастворимые соединения: [136]
После этой реакции суспензия имеет температуру выше атмосферной точки кипения. Он охлаждается за счет удаления пара при снижении давления. Остаток боксита отделяют от раствора и выбрасывают. В раствор, свободный от твердых веществ, затравлены мелкие кристаллы гидроксида алюминия; это вызывает разложение ионов [Al(OH) 4 ] - до гидроксида алюминия. После того как примерно половина алюминия выпадет в осадок, смесь отправляют в классификаторы. Маленькие кристаллы гидроксида алюминия собираются и служат в качестве затравки; крупные частицы при нагревании превращаются в оксид алюминия; избыток раствора удаляют выпариванием, (при необходимости) очищают и направляют на переработку. [136]

Превращение глинозема в металлический алюминий достигается с помощью процесса Холла-Эру . В этом энергоемком процессе раствор оксида алюминия в расплавленной (950 и 980 °C (1740 и 1800 °F)) смеси криолита ( Na 3 AlF 6 ) с фторидом кальция подвергается электролизу с получением металлического алюминия. Жидкий металлический алюминий опускается на дно раствора, выливается и обычно отливается в большие блоки, называемые алюминиевыми заготовками, для дальнейшей обработки. [41]
Аноды электролизера изготовлены из углерода — наиболее устойчивого к фторидной коррозии материала — и либо обжигаются в процессе, либо подвергаются предварительному обжигу. Первые, также называемые анодами Содерберга, менее энергоэффективны, а сбор паров, образующихся во время обжига, требует больших затрат, поэтому их заменяют предварительно обожженными анодами, даже несмотря на то, что они экономят электроэнергию, энергию и трудозатраты на предварительный обжиг катодов. Углерод для анодов должен быть предпочтительно чистым, чтобы ни алюминий, ни электролит не были загрязнены золой. Несмотря на устойчивость углерода к коррозии, он все равно расходуется в размере 0,4–0,5 кг на каждый килограмм произведенного алюминия. Катоды изготовлены из антрацита ; высокая чистота для них не требуется, поскольку примеси выщелачиваются очень медленно. Катод расходуется из расчета 0,02–0,04 кг на каждый килограмм производимого алюминия. Ячейка обычно отключается через 2–6 лет после выхода из строя катода. [41]
Процесс Холла-Эру производит алюминий чистотой более 99%. Дальнейшую очистку можно провести с помощью процесса Хупеса . Этот процесс включает электролиз расплавленного алюминия с помощью электролита из фторидов натрия, бария и алюминия. Полученный алюминий имеет чистоту 99,99%. [41] [137]
Электроэнергия составляет от 20 до 40% стоимости производства алюминия, в зависимости от местоположения плавильного завода. Производство алюминия потребляет примерно 5% электроэнергии, вырабатываемой в США. [129] По этой причине были исследованы альтернативы процессу Холла-Эру, но ни одна из них не оказалась экономически целесообразной. [41]

Восстановление металла путем переработки стало важной задачей алюминиевой промышленности. Переработка отходов была малозаметной деятельностью до конца 1960-х годов, когда растущее использование алюминиевых банок для напитков привлекло к этому внимание общественности. [138] Переработка включает в себя плавку лома, процесс, который требует всего 5% энергии, используемой для производства алюминия из руды, хотя значительная часть (до 15% входного материала) теряется в виде шлака (золоподобного оксида). . [139] Плавильная печь для плавления алюминия производит значительно меньше окалины, значения которой, как сообщается, составляют менее 1%. [140]
Белый шлак от производства первичного алюминия и вторичной переработки все еще содержит полезные количества алюминия, который можно извлечь в промышленности . В результате этого процесса производятся алюминиевые заготовки вместе с очень сложными отходами. С этими отходами трудно справиться. Он реагирует с водой, выделяя смесь газов (в том числе водород , ацетилен и аммиак ), которая самопроизвольно воспламеняется при контакте с воздухом; [141] контакт с влажным воздухом приводит к выделению большого количества газообразного аммиака. Несмотря на эти трудности, отходы используются в качестве наполнителя асфальта и бетона . [142]

Мировое производство алюминия в 2016 году составило 58,8 миллиона тонн. Он превысил аналогичный показатель любого другого металла, кроме железа (1,231 млн тонн). [143] [144]
Алюминий почти всегда легирован, что заметно улучшает его механические свойства, особенно при закалке . Например, обычная алюминиевая фольга и банки для напитков представляют собой сплавы с содержанием алюминия от 92% до 99%. [145] Основными легирующими веществами являются медь , цинк , магний , марганец и кремний (например, дюралюминий ) с содержанием других металлов в нескольких процентах по весу. [146] Алюминий, как кованый, так и литой, легирован марганцем , кремнием , магнием , медью и цинком, среди других. [147] Например, семейство сплавов Kynal было разработано британским химическим производителем Imperial Chemical Industries .

Основные области применения металлического алюминия: [148]
Подавляющее большинство (около 90%) оксида алюминия превращается в металлический алюминий. [136] Будучи очень твердым материалом ( твердость по шкале Мооса 9), [149] оксид алюминия широко используется в качестве абразива; [150] будучи чрезвычайно химически инертным, он полезен в высокореактивных средах, таких как натриевые лампы высокого давления. [151] Оксид алюминия обычно используется в качестве катализатора в промышленных процессах; [136] например, процесс Клауса для преобразования сероводорода в серу на нефтеперерабатывающих заводах и для алкилирования аминов . [152] [153] Многие промышленные катализаторы имеют основу из оксида алюминия, а это означает, что дорогой материал катализатора диспергируется по поверхности инертного оксида алюминия. [154] Другое основное применение — в качестве осушителя или абсорбента. [136] [155]

Некоторые сульфаты алюминия имеют промышленное и коммерческое применение. Сульфат алюминия (в его гидратной форме) производится в ежегодном масштабе в несколько миллионов метрических тонн. [156] Около двух третей потребляется на очистку воды . [156] Следующее важное применение — производство бумаги. [156] Он также используется в качестве протравы при крашении, травлении семян, дезодорации минеральных масел, при дублении кожи и при производстве других соединений алюминия. [156] Два вида алюминиевых квасцов, аммонийные квасцы и алюмокалиевые квасцы , раньше использовались в качестве протрав и при дублении кожи, но их использование значительно сократилось после появления сульфата алюминия высокой чистоты. [156] Безводный хлорид алюминия применяется в качестве катализатора в химической и нефтехимической промышленности, красильной промышленности, в синтезе различных неорганических и органических соединений. [156] Гидроксихлориды алюминия используются для очистки воды, в бумажной промышленности и в качестве антиперспирантов . [156] Алюминат натрия используется для очистки воды и в качестве ускорителя затвердевания цемента. [156]
Многие соединения алюминия имеют нишевые применения, например:

Несмотря на широкое распространение в земной коре, алюминий не имеет известной биологической роли. [41] При pH 6–9 (актуально для большинства природных вод) алюминий выпадает в осадок из воды в виде гидроксида и, следовательно, недоступен; большинство элементов, ведущих себя таким образом, не имеют биологической роли или токсичны. [169] Сульфат алюминия имеет ЛД 50 6207 мг/кг (перорально, мышь), что соответствует 435 граммам (около одного фунта) на человека весом 70 кг (150 фунтов). [41]
Алюминий классифицируется Министерством здравоохранения и социальных служб США как неканцероген . [170] [n] В обзоре, опубликованном в 1988 году, говорилось, что существует мало доказательств того, что нормальное воздействие алюминия представляет риск для здорового взрослого человека, [173] а многоэлементный токсикологический обзор 2014 года не смог обнаружить вредного воздействия алюминия, потребляемого в количествах не более 40 мг/день на кг массы тела . [170] Большая часть потребляемого алюминия покидает организм с фекалиями; большая часть небольшой его части, попадающей в кровь, выводится с мочой; [174] тем не менее, некоторое количество алюминия проникает через гематоэнцефалический барьер и преимущественно откладывается в мозге пациентов с болезнью Альцгеймера. [175] [176] Данные, опубликованные в 1989 году, показывают, что на пациентов с болезнью Альцгеймера алюминий может действовать путем электростатического сшивания белков, таким образом подавляя гены в верхней височной извилине . [177]
Алюминий, хотя и редко, может вызывать резистентную к витамину D остеомаляцию , эритропоэтин -резистентную микроцитарную анемию и изменения в центральной нервной системе. Особенно подвержены риску люди с почечной недостаточностью. [170] Хронический прием гидратированных силикатов алюминия (для контроля избыточной кислотности желудка) может привести к связыванию алюминия с содержимым кишечника и повышенному выведению других металлов, таких как железо или цинк ; достаточно высокие дозы (>50 г/день) могут вызвать анемию. [170]

Во время инцидента с загрязнением воды в Кэмелфорде в 1988 году питьевая вода жителей Кэмелфорда была загрязнена сульфатом алюминия в течение нескольких недель. В окончательном отчете об инциденте, опубликованном в 2013 году, сделан вывод о маловероятности того, что это вызвало долгосрочные проблемы со здоровьем. [178]
Предполагалось, что алюминий является возможной причиной болезни Альцгеймера [179] , но исследования в этом направлении, проводимые в течение более 40 лет, по состоянию на 2018 год не выявили [обновлять]убедительных доказательств причинного эффекта. [180] [181]
Алюминий увеличивает экспрессию генов , связанных с эстрогеном , в клетках рака молочной железы человека , культивируемых в лаборатории. [182] В очень высоких дозах алюминий вызывает изменение функции гематоэнцефалического барьера. [183] Небольшой процент людей [184] страдает контактной аллергией на алюминий и испытывает зудящие красные высыпания, головную боль, мышечную боль, боль в суставах, плохую память, бессонницу, депрессию, астму, синдром раздраженного кишечника или другие симптомы при контакте с продуктами. содержащие алюминий. [185]
Воздействие порошкообразного алюминия или сварочных дымов алюминия может вызвать фиброз легких . [186] Мелкий алюминиевый порошок может воспламениться или взорваться, создавая еще одну опасность на рабочем месте. [187] [188]
Продукты питания являются основным источником алюминия. Питьевая вода содержит больше алюминия, чем твердая пища; [170] однако алюминий из продуктов питания может усваиваться лучше, чем алюминий из воды. [189] Основными источниками перорального воздействия алюминия на человека являются пищевые продукты (из-за его использования в пищевых добавках, упаковке продуктов питания и напитков, а также в кухонной утвари), питьевая вода (из-за его использования в муниципальной очистке воды) и алюминийсодержащие лекарства. (особенно антацидные/противоязвенные препараты и буферизованный аспирин). [190] Диетическая экспозиция у европейцев составляет в среднем 0,2–1,5 мг/кг/неделю, но может достигать 2,3 мг/кг/неделю. [170] Более высокие уровни воздействия алюминия в основном ограничиваются шахтерами, работниками производства алюминия и пациентами на диализе . [191]
Потребление антацидов , антиперспирантов, вакцин и косметики указывает на возможные пути заражения. [192] Потребление кислых продуктов или жидкостей, содержащих алюминий, усиливает всасывание алюминия, [193] было показано, что мальтол увеличивает накопление алюминия в нервных и костных тканях. [194]
В случае подозрения на внезапное употребление большого количества алюминия единственным лечением является мезилат дефероксамина , который может быть назначен для выведения алюминия из организма путем хелатирования . [195] [196] Однако это следует применять с осторожностью, поскольку это снижает не только содержание алюминия в корпусе, но и других металлов, таких как медь или железо. [195]

Высокие уровни содержания алюминия наблюдаются вблизи горнодобывающих предприятий; небольшие количества алюминия выбрасываются в окружающую среду на угольных электростанциях или мусоросжигательных заводах . [174] Алюминий, находящийся в воздухе, вымывается дождем или обычно оседает, но мелкие частицы алюминия остаются в воздухе в течение длительного времени. [174]
Кислотные осадки являются основным природным фактором мобилизации алюминия из природных источников [170] и основной причиной воздействия алюминия на окружающую среду; [197] однако основным фактором присутствия алюминия в соленой и пресной воде являются промышленные процессы, которые также выбрасывают алюминий в воздух. [170]
В воде алюминий действует как токсичный агент на животных, дышащих жабрами , таких как рыбы , когда вода кислая, в результате чего алюминий может осаждаться на жабрах, [198] что вызывает потерю ионов плазмы и гемолимфы , что приводит к нарушению осморегуляции . [197] Органические комплексы алюминия могут легко усваиваться и нарушать обмен веществ у млекопитающих и птиц, хотя на практике это происходит редко. [197]
Алюминий занимает первое место среди факторов, снижающих рост растений на кислых почвах. Хотя в почвах с нейтральным pH обычно безвредно для роста растений, в кислых почвах концентрация токсичных катионов Al 3+ увеличивается и нарушает рост и функционирование корней. [199] [200] [201] [202] Пшеница выработала толерантность к алюминию, выделяя органические соединения , которые связываются с вредными катионами алюминия . Считается, что сорго обладает таким же механизмом толерантности. [203]
Производство алюминия сталкивается с собственными проблемами для окружающей среды на каждом этапе производственного процесса. Основной проблемой являются выбросы парниковых газов . [191] Эти газы образуются в результате потребления электроэнергии на плавильных заводах и побочных продуктов переработки. Наиболее мощными из этих газов являются перфторуглероды, образующиеся в процессе плавки. [191] Выброс диоксида серы является одним из основных предшественников кислотных дождей . [191]
Биодеградация металлического алюминия происходит крайне редко; большинство организмов, разъедающих алюминий, не атакуют алюминий напрямую и не потребляют его, а вместо этого производят коррозийные отходы. [204] [205] Гриб Geotrichum candidum может поедать алюминий в компакт-дисках . [206] [207] [208] Бактерия Pseudomonas aeruginosa и грибок Cladosporium resinae обычно обнаруживаются в топливных баках самолетов, в которых используется топливо на основе керосина (не авиационного газа ), а лабораторные культуры могут разлагать алюминий. [209]
Французские химики дали этой чистой земле новое имя; алюминий на французском языке и оксид алюминия на латыни. Признаюсь, мне не нравится этот глинозем.
Происхождение: Сформировано в английском языке путем происхождения. Этимоны: алюминий н. , суффикс -ium , алюминий n.
Этимология: < французский алюминий (LB Guyton de Morveau 1782, Observ. sur la Physique 19 378) < классический латинский alūmin- , alūmen alum n. 1 , после французского суффикса -ine -ine 4 .
Калий, действуя на алюминий и глюцин, образует пирофорные вещества темно-серого цвета, которые горят, выбрасывая блестящие искры, оставляя после себя щелочь и землю и которые, будучи брошены в воду, разлагают ее с большой силой. Результат этого эксперимента не является полностью решающим в отношении существования того, что можно было бы назвать алюминием и глюцинием.
алюминий н. сосуществовал со своим синонимом алюминий n. на протяжении всего 19 в. С начала 20 в. алюминий постепенно стал преобладающей формой в Северной Америке; оно было принято в качестве официального названия металла в США Американским химическим обществом в 1925 году. В других странах алюминий постепенно вытеснялся алюминием , который был принят ИЮПАК в качестве международного стандарта в 1990 году.
{{cite book}}: |journal=игнорируется ( помощь )Артроконидальный гриб типа
Geotrichum
был выделен авторами из поврежденного компакт-диска, найденного в Белизе (Центральная Америка).... В настоящей статье мы сообщаем об очистке и характеристике внеклеточного H
2
O
2
-генерирующего оксидаза, продуцируемая этим грибом, которая разделяет каталитические свойства как с
P. eryngii
AAO, так и с
P. simplicissimum
VAO.
См. также реферат работы Romero et al. 2007.