Болезнь Хантингтона ( БХ ), также известная как хорея Хантингтона , представляет собой неизлечимое нейродегенеративное заболевание [7] , которое в большинстве случаев передается по наследству . [8] Самыми ранними симптомами часто являются едва заметные проблемы с настроением или умственными/психиатрическими способностями. [9] [1] Часто за этим следует общее отсутствие координации и неустойчивая походка . [2] Это также заболевание базальных ганглиев, вызывающее гиперкинетическое двигательное расстройство, известное как хорея . [10] [11] По мере прогрессирования заболевания нескоординированные, непроизвольные движения тела при хорее становятся более очевидными. [1] Физические способности постепенно ухудшаются, пока не становится трудно координировать движения и человек не может говорить. [1] [2] Умственные способности обычно снижаются до деменции , депрессии, апатии и временами импульсивности. [9] [12] [3] Конкретные симптомы у разных людей несколько различаются. [1] Симптомы обычно появляются в возрасте от 30 до 50 лет и могут начаться в любом возрасте, но обычно наблюдаются в возрасте около 40 лет. [12] [9] [3] [4] Заболевание может развиваться раньше в каждом последующем возрасте. поколение . [1] Около восьми процентов случаев начинаются в возрасте до 20 лет и известны как ювенильная HD , которая обычно проявляется медленными симптомами болезни Паркинсона , а не хореи. [3]
БГ обычно наследуется от больного родителя , который несет мутацию в гене хантингтина (HTT). [4] Однако до 10% случаев связаны с новой мутацией. [1] Ген хантингтина предоставляет генетическую информацию о белке хантингтина (Htt). [1] Расширение CAG-повторов цитозин - аденин - гуанин ( известное как расширение тринуклеотидных повторов ) в гене, кодирующем белок хантингтин, приводит к образованию аномального мутантного белка (mHtt), который постепенно повреждает клетки мозга посредством ряда возможных механизмов. . [8] [13] Мутантный белок является доминантным , поэтому наличие одного родителя, являющегося носителем этого признака, достаточно, чтобы вызвать заболевание у их детей. Диагноз ставится с помощью генетического тестирования , которое можно провести в любое время, независимо от наличия симптомов. [5] Этот факт вызывает несколько этических дебатов: возраст, в котором человек считается достаточно зрелым, чтобы выбрать тестирование; имеют ли родители право на тестирование своих детей; а также обеспечение конфиденциальности и раскрытие результатов испытаний. [2]
Лекарство от БГ не известно, и на более поздних стадиях требуется постоянный уход. [2] Лечение может облегчить некоторые симптомы, а в некоторых улучшить качество жизни . [3] Лучшим доказательством лечения двигательных проблем является тетрабеназин . [3] HD поражает от 4 до 15 из 100 000 человек европейского происхождения. [1] [3] Редко встречается среди финнов и японцев, а частота встречаемости в Африке неизвестна. [3] Заболевание одинаково поражает мужчин и женщин. [3] Такие осложнения, как пневмония , болезни сердца и физические травмы в результате падений, сокращают продолжительность жизни; хотя фатальную аспирационную пневмонию обычно называют основной причиной смерти людей с этим заболеванием. [14] [12] [3] Суицид является причиной смерти примерно в 9% случаев. [3] Смерть обычно наступает через 15–20 лет с момента первого обнаружения заболевания. [4]
Самое раннее известное описание болезни было сделано в 1841 году американским врачом Чарльзом Оскаром Уотерсом. [15] Более подробно это состояние было описано в 1872 году американским врачом Джорджем Хантингтоном . [15] Генетическая основа была открыта в 1993 году международным совместным усилием под руководством Фонда наследственных заболеваний . [16] [17] Исследовательские и вспомогательные организации начали формироваться в конце 1960-х годов для повышения осведомленности общественности, оказания поддержки отдельным лицам и их семьям и продвижения исследований. [17] [18] Направления исследований включают определение точного механизма заболевания, улучшение моделей животных для помощи в исследованиях, тестирование лекарств и их доставку для лечения симптомов или замедления прогрессирования заболевания, а также изучение таких процедур, как использование стволовых клеток. терапия с целью замены поврежденных или утраченных нейронов. [16]
Признаки и симптомы болезни Хантингтона чаще всего становятся заметными в возрасте от 30 до 50 лет, но они могут начаться в любом возрасте [4] и проявляться в виде триады двигательных, когнитивных и психиатрических симптомов. [19] Если заболевание развивается на ранней стадии, оно известно как ювенильная болезнь Хантингтона. [20] В 50% случаев первыми появляются психиатрические симптомы. [19] Их прогрессирование часто описывается на ранних, средних и поздних стадиях с более ранней продромальной фазой. [2] На ранних стадиях возникают незначительные изменения личности, проблемы с когнитивными способностями и физическими навыками, раздражительность и перепады настроения, и все это может остаться незамеченным, [21] [22] и обычно предшествует двигательным симптомам. [23] Почти у каждого человека с HD в конечном итоге проявляются схожие физические симптомы, но начало, прогрессирование и степень когнитивных и поведенческих симптомов значительно различаются у разных людей. [24] [25]
Наиболее характерными начальными физическими симптомами являются судорожные, беспорядочные и неконтролируемые движения, называемые хореей . [10] Многие люди не осознают своих непроизвольных движений или того, что они им мешают. [1] Первоначально хорея может проявляться как общее беспокойство, небольшие непреднамеренно инициированные или незавершенные движения, нарушение координации или замедленные саккадические движения глаз . [26] Эти незначительные двигательные нарушения обычно предшествуют более очевидным признакам двигательной дисфункции как минимум на три года. [27] По мере прогрессирования заболевания появляются явные симптомы, такие как ригидность, корчащиеся движения или ненормальная поза . [26] Это признаки того, что поражена система мозга, отвечающая за движение. [28] Психомоторные функции становятся все более нарушенными, так что это влияет на любые действия, требующие мышечного контроля. Когда нарушается мышечный контроль, например возникает ригидность или мышечная контрактура, это называется дистонией . Дистония — это неврологическое гиперкинетическое двигательное расстройство, которое приводит к скручиванию или повторяющимся движениям, которые могут напоминать тремор. Распространенными последствиями являются физическая нестабильность, аномальное выражение лица и трудности с жеванием, глотанием и речью . [26] Нарушения сна и потеря веса также являются сопутствующими симптомами. [29] Проблемы с питанием обычно приводят к потере веса и могут привести к недостаточности питания. [30] [31] Потеря веса часто встречается у людей с болезнью Хантингтона и прогрессирует по мере заболевания. Ювенильная БГ обычно прогрессирует быстрее, с более выраженным снижением когнитивных функций, хорея проявляется кратковременно, если вообще проявляется; Вестфальский вариант замедленности движений , ригидности и тремора более типичен для юношеской ГБ, как и судороги . [26] [29]
Когнитивные способности прогрессивно ухудшаются и обычно переходят в деменцию . [3] Особенно страдают исполнительные функции , которые включают планирование, когнитивную гибкость, абстрактное мышление , усвоение правил, инициирование соответствующих действий и подавление неподходящих действий. Различные когнитивные нарушения включают трудности с концентрацией внимания на задачах, отсутствие гибкости, отсутствие импульсивности, отсутствие осознания собственного поведения и способностей, а также трудности с обучением или обработкой новой информации. По мере прогрессирования заболевания появляются нарушения памяти . Зарегистрированные нарушения варьируются от дефицита кратковременной памяти до проблем с долговременной памятью , включая дефицит эпизодической (память о своей жизни), процедурной (память тела о том, как выполнять какую-либо деятельность) и рабочей памяти . [28]
Сообщаемыми нейропсихиатрическими признаками являются тревога , депрессия , снижение проявления эмоций , эгоцентризм , агрессия , компульсивное поведение , галлюцинации и бред . [32] Другие распространенные психические расстройства могут включать обсессивно-компульсивное расстройство , манию , бессонницу и биполярное расстройство . Также наблюдались трудности с распознаванием негативных высказываний других людей. [28] Распространенность этих симптомов сильно различается в разных исследованиях: по оценкам, распространенность психических расстройств в течение жизни составляет от 33 до 76%. [32] Для многих больных и членов их семей эти симптомы являются одними из наиболее тревожных аспектов заболевания, часто влияя на повседневное функционирование и являясь причиной помещения в специальные учреждения . [32] Ранние поведенческие изменения при ГБ приводят к повышенному риску самоубийства. [10] Часто у людей снижается осознание хореи, когнитивных и эмоциональных нарушений. [33]
Мутантный хантингтин экспрессируется по всему организму и связан с аномалиями в периферических тканях, которые непосредственно вызваны такой экспрессией за пределами мозга. Эти нарушения включают мышечную атрофию , сердечную недостаточность , нарушение толерантности к глюкозе , потерю веса , остеопороз и атрофию яичек . [34]
У каждого есть две копии гена хантингтина ( HTT ), который кодирует белок хантингтина (Htt). HTT также называют геном HD и геном IT15 (интересный транскрипт 15). Часть этого гена представляет собой повторяющийся участок, называемый расширением тринуклеотидных повторов – короткий повтор , длина которого варьируется у разных людей и может меняться в зависимости от поколения. Если повтор присутствует в здоровом гене, динамическая мутация может увеличить количество повторов и привести к дефектному гену. Когда длина этого повторяющегося участка достигает определенного порога, он производит измененную форму белка, называемую мутантным белком хантингтина (mHtt). Различные функции этих белков являются причиной патологических изменений, которые, в свою очередь, вызывают симптомы заболевания. Мутация болезни Хантингтона является генетически доминантной и почти полностью пенетрантной ; Мутация любого из аллелей HTT человека вызывает заболевание. Наследуется не по полу, а по длине повторяющегося участка гена; следовательно, на тяжесть заболевания может влиять пол больного родителя. [26]
HD — одно из нескольких нарушений тринуклеотидных повторов , вызванных длиной повторяющегося участка гена, превышающей нормальный диапазон. [26] Ген HTT расположен на коротком плече хромосомы 4 [26] в районе 4p16.3. HTT содержит последовательность трех оснований ДНК — цитозин-аденин-гуанин (CAG), повторяющуюся несколько раз (т. е.… CAGCAGCAG…), известную как тринуклеотидный повтор. [26] CAG — это трехбуквенный генетический код ( кодон ) аминокислоты глютамин , поэтому серия из них приводит к образованию цепочки глютамина, известной как полиглутаминовый тракт (или полиQ-тракт), и повторяющейся части ген, область полиQ . [35]
.jpg/440px-Huntington's_disease_(5880985560).jpg)
Как правило, у людей имеется менее 36 повторяющихся глютаминов в области PolyQ, что приводит к выработке цитоплазматического белка хантингтина. [26] Однако последовательность из 36 или более глютаминов приводит к образованию белка с различными характеристиками. [26] Эта измененная форма, называемая мутантным хантингтином (mHtt), увеличивает скорость распада определенных типов нейронов . Области мозга имеют различное количество и зависимость от этих типов нейронов и подвергаются соответствующему воздействию. [26] Как правило, количество повторов CAG связано с тем, насколько сильно затронут этот процесс, и составляет около 60% вариаций возраста появления симптомов. Остальные вариации связаны с окружающей средой и другими генами, которые модифицируют механизм БГ. [26] Примерно от 36 до 39 повторений приводят к форме заболевания с пониженной пенетрантностью, с гораздо более поздним началом и более медленным прогрессированием симптомов. В некоторых случаях начало может быть настолько поздним, что симптомы вообще не замечаются. [26] При очень большом количестве повторов (более 60) начало БГ может произойти в возрасте до 20 лет, что известно как ювенильная БГ. Ювенильный БГ обычно относится к вестфальскому варианту, который характеризуется замедленностью движений, ригидностью и тремором. Это составляет около 7% носителей HD. [36] [37]
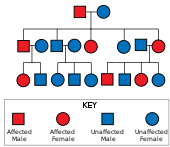
Болезнь Хантингтона имеет аутосомно-доминантное наследование, что означает, что больной человек обычно наследует одну копию гена с расширенным тринуклеотидным повтором (мутантный аллель ) от больного родителя. [26] Поскольку пенетрантность мутации очень высока, заболеванием заболеют те, у кого есть мутированная копия гена. При этом типе наследования каждый потомок больного человека имеет 50% риск унаследовать мутантный аллель, поэтому страдает заболеванием (см. рисунок). Эта вероятность не зависит от пола. [38] Гены, зависящие от пола или сцепленные с полом, — это признаки, которые обнаруживаются в X или Y-хромосомах. [39]
Тринуклеотидные повторы CAG , насчитывающие более 28, нестабильны во время репликации , и эта нестабильность увеличивается с увеличением количества присутствующих повторов. [26] Обычно это приводит к новым расширениям по мере прохождения поколений ( динамические мутации ) вместо воспроизведения точной копии тринуклеотидного повтора. [26] Это приводит к изменению количества повторов в последующих поколениях, так что незатронутый родитель с «промежуточным» количеством повторов (28–35) или «пониженной пенетрантностью» (36–40) может передать копию гена с увеличением числа повторов, что приводит к образованию полностью проникающей HD. [26] Более ранний возраст начала и большая тяжесть заболевания в последующих поколениях из-за увеличения количества повторов известны как генетическое предвосхищение . [1] Нестабильность выше в сперматогенезе , чем в оогенезе ; [26] аллели, унаследованные по материнской линии, обычно имеют одинаковую длину повторов, тогда как аллели, унаследованные по отцовской линии, имеют более высокий шанс увеличения длины. [26] [40] Редко болезнь Хантингтона вызывается новой мутацией , когда ни один из родителей не имеет более 36 повторов CAG. [41]
В редких ситуациях, когда оба родителя имеют расширенный ген HD, риск увеличивается до 75%, а когда у одного из родителей есть две расширенные копии, риск составляет 100% (пострадают все дети). Лица с пораженными обоими генами встречаются редко. Некоторое время считалось, что БГ является единственным заболеванием, для которого наличие второго мутировавшего гена не влияет на симптомы и прогрессирование [42] , но с тех пор было обнаружено, что оно может влиять на фенотип и скорость прогрессирования. [26] [43]
Белок хантингтин взаимодействует с более чем 100 другими белками и, по-видимому, выполняет множество функций. [44] Поведение мутировавшего белка (mHtt) до конца не изучено, но он токсичен для определенных типов клеток, особенно клеток головного мозга . Раннее поражение наиболее очевидно в подкорковых базальных ганглиях , первоначально в полосатом теле , но по мере прогрессирования заболевания поражаются и другие области головного мозга, включая области коры головного мозга . Ранние симптомы обусловлены функциями полосатого тела и его корковых связей, а именно контролем над движением, настроением и высшими когнитивными функциями. [26] Метилирование ДНК также, по-видимому, изменяется при БГ. [45]
Htt экспрессируется во всех клетках, при этом самые высокие концентрации обнаруживаются в мозге и семенниках , а умеренные количества — в печени , сердце и легких . Его функции неясны, но он взаимодействует с белками, участвующими в транскрипции , передаче сигналов в клетках и внутриклеточном транспорте . [46] У животных, генетически модифицированных для проявления HD, было идентифицировано несколько функций Htt. [47] У этих животных Htt важен для эмбрионального развития, поскольку его отсутствие связано с эмбриональной гибелью. Считается, что каспаза , фермент, который играет роль в катализе апоптоза , активируется мутировавшим геном путем повреждения системы убиквитин-протеаза. Он также действует как антиапоптотический агент, предотвращая запрограммированную гибель клеток , и контролирует выработку мозгового нейротрофического фактора — белка, который защищает нейроны и регулирует их создание во время нейрогенеза . Htt также облегчает синаптический везикулярный транспорт и синаптическую передачу и контролирует транскрипцию нейрональных генов. [47] Если экспрессия Htt увеличивается, выживаемость клеток головного мозга улучшается, а эффекты mHtt снижаются, тогда как когда экспрессия Htt снижается, результирующие характеристики больше похожи на те, что наблюдаются в присутствии mHtt. [47] Соответственно, считается, что заболевание вызвано не неадекватным производством Htt, а токсическим усилением функции mHtt в организме. [26]

Токсическое действие mHtt может проявляться и вызывать патологию ГБ через множественные клеточные изменения. [48] [49] В своей мутантной (расширенной полиглутамином) форме белок более склонен к расщеплению, в результате чего образуются более короткие фрагменты, содержащие увеличение полиглутамина. [48] Эти белковые фрагменты склонны подвергаться неправильному сворачиванию и агрегации, образуя фибриллярные агрегаты, в которых ненативные полиглутаминовые β-цепи из нескольких белков связаны друг с другом водородными связями. [13] Эти агрегаты имеют ту же фундаментальную архитектуру перекрестного бета- амилоида , что и при других заболеваниях отложения белка . [50] Со временем агрегаты накапливаются, образуя тельца включения внутри клеток, что в конечном итоге нарушает функцию нейронов. [13] [48] Тельца включения были обнаружены как в ядре клетки , так и в цитоплазме . [48] Тельца включения в клетках головного мозга являются одним из самых ранних патологических изменений, и некоторые эксперименты показали, что они могут быть токсичными для клетки, но другие эксперименты показали, что они могут формироваться как часть защитного механизма организма и помогать защищать клетки. [48]
Было идентифицировано несколько путей, с помощью которых mHtt может вызывать гибель клеток. К ним относятся воздействие на белки-шапероны , которые помогают сворачивать белки и удалять неправильно свернутые; взаимодействие с каспазами , которые играют роль в процессе удаления клеток ; токсическое воздействие глютамина на нервные клетки ; нарушение выработки энергии внутри клеток; и влияние на экспрессию генов. [13] [51]
Было обнаружено, что мутантный белок хантингтин играет ключевую роль в дисфункции митохондрий . [46] Нарушение митохондриального транспорта электронов может привести к более высокому уровню окислительного стресса и выделению активных форм кислорода . [52]
Известно, что глутамин в больших количествах эксайтотоксичен и может вызвать повреждение многочисленных клеточных структур. Избыток глутамина не обнаруживается при БГ, но взаимодействия измененного белка хантингтина с многочисленными белками нейронов приводят к повышенной уязвимости к глютамину. Считается, что повышенная уязвимость приводит к эксайтотоксическим эффектам из-за нормального уровня глютамина. [13]

Первоначально повреждение головного мозга является регионально специфичным: в первую очередь поражается дорсальное полосатое тело в подкорковых базальных ганглиях , а затем вовлекается кора во всех областях. [53] [54] Другие пораженные участки базальных ганглиев включают черную субстанцию ; вовлечение коры включает корковые слои 3, 5 и 6 ; также очевидно вовлечение гиппокампа , клеток Пуркинье в мозжечке , латеральных туберальных ядер гипоталамуса и частей таламуса . [26] Эти области подвергаются воздействию в зависимости от их структуры и типа содержащихся в них нейронов, уменьшаясь в размерах по мере потери клеток. [26] Колючие нейроны стриарного среднего слоя являются наиболее уязвимыми, особенно те, которые проецируются в сторону внешнего бледного шара , при этом вставочные нейроны и шиповидные клетки, выступающие во внутренний бледный шар, поражаются меньше. [26] [55] HD также вызывает аномальное увеличение количества астроцитов и активацию иммунных клеток головного мозга, микроглии . [56]
Базальные ганглии играют ключевую роль в контроле движений и поведения. Их функции до конца не изучены, но теории предполагают, что они являются частью когнитивно- исполнительной системы [28] и двигательного контура. [57] Базальные ганглии обычно подавляют большое количество цепей, генерирующих определенные движения. Чтобы инициировать определенное движение, кора головного мозга посылает сигнал базальным ганглиям, который вызывает прекращение торможения. Повреждение базальных ганглиев может привести к тому, что высвобождение или восстановление торможения будет беспорядочным и неконтролируемым, что приводит к неловкому началу движения или к непреднамеренному инициированию движений или к остановке движения до или после его запланированного завершения. Накапливающееся повреждение этой области вызывает характерные беспорядочные движения, связанные с ГБ, известные как хорея, дискинезия . [57] Из-за неспособности базальных ганглиев сдерживать движения люди, затронутые этим заболеванием, неизбежно испытывают снижение способности произносить речь и глотать пищу и жидкости (дисфагия). [58]
CREB-связывающий белок (CBP), корегулятор транскрипции, необходим для функционирования клеток, поскольку в качестве коактиватора значительного числа промоторов он активирует транскрипцию генов для путей выживания. [51] CBP содержит домен ацетилтрансферазы , с которым HTT связывается через свой полиглутаминсодержащий домен. [59] При аутопсии мозга тех, кто страдал болезнью Хантингтона, также было обнаружено невероятное снижение количества CBP. [60] Кроме того, когда CBP сверхэкспрессируется, смертность, вызванная полиглутамином, уменьшается, что еще раз демонстрирует, что CBP играет важную роль в болезни Хантингтона и нейронах в целом. [51]
Диагноз начала ГБ можно поставить после появления физических симптомов, характерных для заболевания. [26] Генетическое тестирование может быть использовано для подтверждения физического диагноза, если в семейном анамнезе не существует ГБ. Еще до появления симптомов генетическое тестирование может подтвердить, несет ли человек или эмбрион расширенную копию тринуклеотидного повтора (CAG) в гене HTT , вызывающем заболевание. Доступны генетические консультации , которые предоставят советы и рекомендации на протяжении всей процедуры тестирования, а также о последствиях подтвержденного диагноза. Эти последствия включают влияние на психологию человека, карьеру, решения по планированию семьи, родственников и отношения. Несмотря на доступность пресимптоматического тестирования, только 5% из тех, кто подвержен риску наследования БГ, решают это сделать. [26]

Физикальное обследование , иногда в сочетании с психологическим обследованием , позволяет определить, началось ли начало заболевания. [26] Чрезмерные непреднамеренные движения какой-либо части тела часто являются поводом для обращения к врачу. Если они происходят внезапно и имеют случайное время и распределение, они предполагают диагноз ГБ. Когнитивные или поведенческие симптомы редко являются первыми диагностируемыми симптомами; их обычно распознают только задним числом или по мере дальнейшего развития. Насколько далеко продвинулось заболевание, можно измерить с помощью единой шкалы оценки болезни Хантингтона, которая представляет собой общую систему оценок, основанную на двигательных, поведенческих, когнитивных и функциональных оценках. [62] [63] Медицинские методы визуализации , такие как КТ или МРТ , могут выявить атрофию хвостатых ядер на ранних стадиях заболевания, как показано на рисунке справа, но эти изменения сами по себе не являются диагностическими показателями. HD. Церебральная атрофия может наблюдаться на поздних стадиях заболевания. Функциональные методы нейровизуализации, такие как функциональная магнитно-резонансная томография (фМРТ) и позитронно-эмиссионная томография (ПЭТ), могут показать изменения в активности мозга до появления физических симптомов, но они являются экспериментальными инструментами и не используются клинически. [26]
Поскольку БГ наследуется по аутосомно-доминантному типу, у людей, которые подвержены риску ее унаследования, существует сильная мотивация обратиться за диагнозом. Генетический тест на БГ состоит из анализа крови, в ходе которого подсчитывают количество повторов CAG в каждом из аллелей HTT . [64] Предельные значения даны следующим образом:
Тестирование до появления симптомов — это событие, которое меняет жизнь, и это очень личное решение. [26] Основной причиной выбора теста на БГ является помощь в принятии решений о карьере и семье. [26] Прогностическое тестирование на болезнь Хантингтона было доступно с помощью анализа сцепления (который требует тестирования нескольких членов семьи) с 1986 года и с помощью прямого анализа мутаций с 1993 года. [66] В то время исследования показали, что 50–70% людей из группы риска люди были бы заинтересованы в прохождении тестирования, но, поскольку предлагается прогностическое тестирование, гораздо меньше людей решают пройти тестирование. [67] Более 95% людей с риском наследования ГБ не проходят тестирование, главным образом потому, что оно не лечится. [26] Ключевой проблемой является беспокойство, которое человек испытывает из-за незнания, разовьется ли у него в конечном итоге БГ, по сравнению с влиянием положительного результата. [26] Независимо от результата, уровень стресса снижается через два года после тестирования, но риск самоубийства увеличивается после положительного результата теста. [26] Лица, у которых обнаружено не унаследованное расстройство, могут испытывать чувство вины выжившего перед членами семьи, которые пострадали. [26] Другие факторы, принимаемые во внимание при рассмотрении вопроса о тестировании, включают возможность дискриминации и последствия положительного результата, что обычно означает, что у родителя есть пораженный ген и что братья и сестры человека будут подвергаться риску его унаследования. [26] В одном исследовании генетическая дискриминация была обнаружена у 46% людей, подверженных риску болезни Хантингтона. Это происходило чаще в личных отношениях, чем в сфере медицинского страхования или трудовых отношениях. [68] Генетическое консультирование при ГБ может предоставить информацию, советы и поддержку для принятия первоначальных решений, а затем, если это будет выбрано, на всех этапах процесса тестирования. [69] Из-за последствий этого теста пациенты, желающие пройти тестирование, должны пройти три консультации, на которых предоставят информацию о болезни Хантингтона. [70]
Консультации и рекомендации по использованию генетического тестирования на БГ стали моделями для других генетических нарушений, таких как аутосомно-доминантная мозжечковая атаксия . [26] [71] [72] Пресимптоматическое тестирование на БГ также повлияло на тестирование на другие заболевания с генетическими вариантами, такие как поликистоз почек , семейная болезнь Альцгеймера и рак молочной железы . [71] Европейская сеть качества молекулярной генетики опубликовала ежегодную схему внешней оценки качества молекулярно-генетического тестирования на это заболевание и разработала рекомендации по передовой практике генетического тестирования на БГ, чтобы помочь в тестировании и представлении результатов. [73]
Эмбрионы , полученные с помощью экстракорпорального оплодотворения , могут быть генетически протестированы на БГ с использованием преимплантационной генетической диагностики . Этот метод, при котором одна или две клетки извлекаются из эмбриона, состоящего обычно из 4–8 клеток, а затем проверяются на наличие генетических аномалий, может затем использоваться для обеспечения того, чтобы эмбрионы, пораженные генами HD, не были имплантированы, поэтому ни один потомок не унаследует болезнь. Некоторые формы преимплантационной генетической диагностики — тестирование на неразглашение или исключение — позволяют людям из группы риска иметь потомство без БГ, не раскрывая свой собственный родительский генотип, не давая информации о том, предначертано ли им самим развить БГ. При тестировании на исключение ДНК эмбриона сравнивается с ДНК родителей, бабушек и дедушек, чтобы избежать наследования хромосомной области, содержащей ген HD, от больного дедушки и бабушки. При тестировании с сохранением конфиденциальности в матке заменяются только здоровые эмбрионы, при этом родительский генотип и, следовательно, родительский риск развития БГ никогда не раскрываются. [74] [75]
Пренатальная диагностика эмбриона или плода в утробе матери также возможна с использованием генетического материала плода, полученного путем отбора проб ворсин хориона . Амниоцентез можно провести , если беременность продолжается, в течение 14–18 недель. В ходе этой процедуры амниотическая жидкость, окружающая ребенка, исследуется на наличие признаков мутации HD. [76] Это также можно сочетать с тестированием на исключение, чтобы избежать раскрытия родительского генотипа. Пренатальное тестирование можно проводить, если у родителей был диагностирован БГ, когда у них было генетическое тестирование, показывающее экспансию гена HTT , или когда у них есть 50% вероятность унаследовать заболевание. Родители могут быть проконсультированы о возможных вариантах, включая прерывание беременности , а также о трудностях ребенка с выявленным геном. [77] [78]
Кроме того, при беременности из группы риска из-за пораженного партнера-мужчины неинвазивная пренатальная диагностика может быть выполнена путем анализа бесклеточной ДНК плода в образце крови, взятом у матери (через венепункцию ) между 6 и 12 неделями беременности. [65] При этом отсутствует риск выкидыша, связанный с процедурой. [65]
Около 99% диагнозов БГ, основанных на типичных симптомах и семейном анамнезе заболевания, подтверждаются генетическим тестированием на наличие расширенного тринуклеотидного повтора, вызывающего БГ. Большинство из оставшихся называются HDL-подобными (HDL) синдромами . [26] [79] Причина большинства заболеваний ЛПВП неизвестна, но те из них, причины которых известны, обусловлены мутациями в гене прионного белка (ЛПВП1), гене мунктофилина 3 (ЛПВП2), рецессивно наследуемом неизвестном гене (ЛПВП3 — только обнаружен в двух семьях и плохо изучен), а также ген, кодирующий белок, связывающий ТАТА-бокс ( SCA17, иногда называемый HDL4 ). Другими аутосомно-доминантными заболеваниями, которые могут быть ошибочно приняты за БГ, являются дентаторубрально-паллидолуизова атрофия и нейроферритинопатия . Кроме того, некоторые аутосомно-рецессивные заболевания напоминают спорадические случаи БГ. К ним относятся хореальный акантоцитоз и нейродегенерация, связанная с пантотенаткиназой . Одним из Х-сцепленных заболеваний этого типа является синдром МакЛеода . [79]
.pdf/page1-440px-Report_(IA_report00comm_6).pdf.jpg)
Доступны методы лечения, позволяющие уменьшить тяжесть некоторых симптомов ГБ. [80] Для многих из этих методов лечения доказательства, подтверждающие их эффективность в лечении симптомов ГБ, являются неполными. [26] [81] По мере прогрессирования заболевания способность заботиться о себе снижается, и тщательно управляемый междисциплинарный уход становится все более необходимым. [26] Хотя относительно мало исследований упражнений и методов лечения показали, что они полезны для реабилитации когнитивных симптомов ГБ, некоторые данные показывают полезность физиотерапии , трудотерапии и логопеда . [26]
Потеря веса и проблемы с питанием из-за дисфагии и других нарушений координации мышц являются обычным явлением, что делает контроль питания все более важным по мере прогрессирования заболевания. [26] В жидкости можно добавлять загустители , поскольку более густые жидкости легче и безопаснее глотать. [26] Напоминание пострадавшему о необходимости есть медленно и брать в рот небольшие кусочки пищи также может быть полезно для предотвращения удушья. [26] Если прием пищи становится слишком опасным или неудобным, можно использовать чрескожную эндоскопическую гастростомию . Эта трубка для кормления, постоянно прикрепленная через брюшную полость к желудку , снижает риск аспирации пищи и обеспечивает лучший контроль питания. [82] Рекомендуется обследование и лечение у логопедов с опытом работы с болезнью Гентингтона. [26]
Люди с болезнью Хантингтона могут обратиться к физиотерапевту , чтобы узнать о неинвазивных и немедикаментозных способах лечения физических симптомов. Физиотерапевты могут проводить оценку и предотвращение риска падения, а также выполнять упражнения на укрепление, растяжку и сердечно-сосудистые упражнения. При необходимости могут быть назначены средства для ходьбы . Физиотерапевты также назначают дыхательные упражнения и техники очистки дыхательных путей при развитии респираторных проблем. [83] Согласованные рекомендации по физиотерапии при болезни Хантингтона были разработаны Европейской сетью HD. [83] Целью раннего реабилитационного вмешательства является предотвращение потери функции. Участие в программах реабилитации на ранней и средней стадии заболевания может быть полезным, поскольку приводит к долгосрочному поддержанию двигательных и функциональных показателей. Реабилитация на поздней стадии направлена на компенсацию двигательных и функциональных потерь. [84] Для долгосрочного независимого лечения терапевт может разработать программы домашних упражнений для подходящих людей. [85]
Кроме того, все большее число людей с ГБ обращаются к паллиативной помощи , целью которой является улучшение качества жизни посредством лечения симптомов и стресса серьезного заболевания в дополнение к другим методам лечения. [86]
Тетрабеназин был одобрен в 2000 году для лечения хореи при болезни Хантингтона в ЕС и в 2008 году в США. [87] Хотя другие препараты использовались « не по назначению », тетрабеназин был первым одобренным средством лечения болезни Хантингтона в США. Это соединение известно с 1950-х годов. Альтернативой тетрабеназину является амантадин , однако данные о его безопасности и эффективности ограничены. [88]
Другие препараты, которые помогают уменьшить хорею, включают нейролептики и бензодиазепины . [22] Гипокинезию и ригидность, особенно в юношеских случаях, можно лечить противопаркинсоническими препаратами, а миоклоническую гиперкинезию можно лечить вальпроевой кислотой . [22] Предварительные данные показали, что этилэйкозапентаеновая кислота улучшает двигательные симптомы через год. [89] В 2017 году FDA одобрило дейтетрабеназин , более тяжелую форму тетрабеназина для лечения хореи при ГБ. [90] Он продается как Аустедо.
Психиатрические симптомы можно лечить с помощью лекарств, аналогичных тем, которые используются среди населения в целом. [26] [81] Селективные ингибиторы обратного захвата серотонина и миртазапин рекомендуются при депрессии, тогда как атипичные антипсихотики рекомендуются при психозах и поведенческих проблемах. [81] Рекомендуется участие специалиста нейропсихиатра, поскольку людям может потребоваться длительное лечение с применением нескольких препаратов в комбинации. [26]
В аюрведической медицине экспериментировали с рядом альтернативных методов лечения с использованием продуктов растительного происхождения, хотя ни один из них не имеет убедительных доказательств эффективности.
Семьи людей и общество в целом, унаследовавшие БГ или находящиеся под угрозой ее наследования, имеют опыт БГ в течение нескольких поколений, но могут не знать о недавних прорывах в понимании болезни и о доступности генетического тестирования. Генетическое консультирование приносит пользу этим людям, обновляя их знания, стремясь развеять любые необоснованные убеждения, которые у них могут быть, и помогая им обдумать свои будущие варианты и планы. Программа обучения пациентов по поводу болезни Хантингтона была создана, чтобы помочь в обучении членов семьи, лиц, осуществляющих уход, и тех, у кого диагностирована болезнь Хантингтона. [91] Также представлена информация, касающаяся вариантов планирования семьи, организации ухода и других вопросов. [26] [92]
На длину тринуклеотидного повтора приходится 60% вариаций возраста появления симптомов и скорости их прогрессирования. Более длительное повторение приводит к более раннему началу заболевания и более быстрому прогрессированию симптомов. [26] [93] У людей с более чем шестьюдесятью повторами заболевание часто развивается в возрасте до 20 лет, тогда как у людей с менее чем 40 повторами заболевание может оставаться бессимптомным. [94] Остальные вариации обусловлены факторами окружающей среды и другими генами, влияющими на механизм заболевания. [26]
Ожидаемая продолжительность жизни при БГ обычно составляет от 10 до 30 лет после появления видимых симптомов. [26] При ювенильной болезни Гентингтона ожидаемая продолжительность жизни составляет 10 лет после появления видимых симптомов. Большинство опасных для жизни осложнений возникают в результате мышечной координации и, в меньшей степени, поведенческих изменений, вызванных снижением когнитивных функций. Наибольший риск представляет собой пневмония , которая приводит к смерти одной трети пациентов с ГБ. Поскольку способность синхронизировать движения ухудшается, трудности с очисткой легких и повышенный риск аспирации еды или питья увеличивают риск заражения пневмонией . Вторым по величине риском являются болезни сердца , которые являются причиной почти четверти смертей среди людей с ГБ. [95] Самоубийство является третьей по значимости причиной смертности: 7,3% больных ГБ покончили с собой и до 27% пытались это сделать. Неясно, в какой степени на суицидальные мысли влияют поведенческие симптомы, поскольку они означают желание избежать более поздних стадий заболевания. [96] [97] [98] Наибольший риск при этом заболевании представляет суицид до постановки диагноза и на средних стадиях развития на протяжении всего заболевания. Другие связанные с этим риски включают удушье; из-за неспособности глотать, физических травм в результате падений и недоедания. [95] [20]
Позднее начало болезни Хантингтона означает, что она обычно не влияет на репродуктивную функцию. [26] Распространенность ГБ во всем мире составляет 5–10 случаев на 100 000 человек, [99] [100] , но сильно различается географически в результате этнической принадлежности, местной миграции и прошлых иммиграционных моделей. [26] Распространенность одинакова для мужчин и женщин. Уровень заболеваемости самый высокий у людей западноевропейского происхождения, составляя в среднем около семи на 100 000 человек, и ниже в остальном мире; например, один на миллион человек азиатского и африканского происхождения. Эпидемиологическое исследование распространенности болезни Хантингтона в Великобритании в период с 1990 по 2010 год, проведенное в 2013 году, показало, что средний показатель распространенности в Великобритании составил 12,3 на 100 000 человек. [26] [101] Кроме того, в некоторых локализованных районах распространенность гораздо выше, чем в среднем по региону. [26] Один из самых высоких случаев заболеваемости наблюдается в изолированных популяциях региона озера Маракайбо в Венесуэле , где ГБ встречается до 700 на 100 000 человек. [26] [102] Другие области высокой локализации были обнаружены на Тасмании и в отдельных регионах Шотландии , Уэльса и Швеции . [98] Увеличение распространенности в некоторых случаях происходит из-за эффекта местного основателя , исторической миграции носителей в область географической изоляции . [98] [103] Некоторые из этих носителей были прослежены на протяжении сотен лет с помощью генеалогических исследований. [98] Генетические гаплотипы также могут дать представление о географических вариациях распространенности. [98] [104] В Исландии , наоборот, довольно низкая распространенность — 1 на 100 000, несмотря на то, что исландцы как народ произошли от ранних германских племен Скандинавии, которые также дали начало шведам ; все случаи, за исключением одного, произошедшего почти два столетия назад, произошли от потомков пары, жившей в начале 19 века. [105] В Финляндии также низкий уровень заболеваемости – всего 2,2 на 100 000 человек. [106]
До открытия генетического теста статистика могла включать только клинический диагноз , основанный на физических симптомах и семейном анамнезе БГ, исключая тех, кто умер от других причин до постановки диагноза. Эти случаи теперь могут быть включены в статистику; и по мере того, как тест становится более доступным, оценки распространенности и заболеваемости расстройством, вероятно, возрастут. [98] [107]

В прошлые века различные виды хореи иногда назывались такими именами, как танец Святого Витта , практически без понимания их причины или типа в каждом случае.
Первое определенное упоминание о ГБ было в письме Чарльза Оскара Уотерса (1816–1892), опубликованном в первом издании « Практики медицины » Робли Данглисона в 1842 году. [109] Уотерс описал «форму хореи, в просторечии называемую магрумами». ", включая точные описания хореи, ее прогрессирования и сильной наследственности заболевания. [110] В 1846 году Чарльз Роллин Горман (1817–1879) наблюдал, как более высокая распространенность, по-видимому, наблюдалась в локализованных регионах. [111] [110] Независимо от Гормана и Уотерса, обоих студентов Данглисона в Медицинском колледже Джефферсона в Филадельфии, [112] Йохан Кристиан Лунд (1830–1906) также подготовил раннее описание в 1860 году. [110] В частности, он отметили, что в Сетесдалене , уединенной горной долине в Норвегии , высокая распространенность деменции была связана с паттерном подергивания двигательных расстройств, который передавался в семьях. [113]
Первое подробное описание болезни было сделано Джорджем Хантингтоном в 1872 году. Изучая совокупную историю болезни нескольких поколений семей, демонстрирующих схожие симптомы, он понял, что их состояния должны быть связаны между собой; он представил свое подробное и точное определение болезни в качестве своей первой статьи. Хантингтон описал точную картину наследования аутосомно-доминантного заболевания за несколько лет до повторного открытия учеными менделевского наследования .
О его наследственной природе. Когда у одного или обоих родителей наблюдаются проявления болезни... один или несколько потомков почти всегда страдают от этой болезни... Но если случайно эти дети проживут жизнь без нее, нить оборвется и внуки и правнуки первых шейкеров могут быть уверены, что они свободны от этой болезни. [108] [114]
Сэр Уильям Ослер интересовался этим расстройством и хореей в целом и был впечатлен статьей Хантингтона, в которой говорилось: «В истории медицины есть несколько случаев, когда болезнь была описана более точно, более наглядно или более кратко». [115] [110] [116] Постоянный интерес Ослера к ГБ в сочетании с его влиянием в области медицины помог быстро распространить осведомленность и знания об этом расстройстве среди медицинского сообщества. [110] Большой интерес был проявлен учёными в Европе, в том числе Луи Теофилем Жозефом Ландузи , Дезире-Маглуаром Бурневилем , Камилло Гольджи и Жозефом Жюлем Дежерином , и до конца века большая часть исследований ГБ имела европейское происхождение. [110] К концу 19 века исследования и отчеты о ГБ были опубликованы во многих странах, и это заболевание было признано заболеванием во всем мире. [110]
Во время повторного открытия менделевского наследования на рубеже 20-го века БГ экспериментально использовалась как пример аутосомно-доминантного наследования. [110] Английский биолог Уильям Бейтсон использовал родословные затронутых семей, чтобы установить, что БГ имеет аутосомно-доминантный тип наследования. [117] [112] Сильный характер наследования побудил нескольких исследователей, в том числе Смита Эли Джеллиффа , попытаться отследить и связать членов семьи, участвовавших в предыдущих исследованиях. [110] Джеллифф собрал информацию со всего Нью-Йорка и опубликовал несколько статей, касающихся генеалогии БГ в Новой Англии . [118] Исследование Джеллиффа вызвало интерес у его друга по колледжу Чарльза Дэвенпорта , который поручил Элизабет Манси провести первое полевое исследование на восточном побережье Соединенных Штатов семей с HD и построить их родословные. [119] Давенпорт использовал эту информацию, чтобы документировать различный возраст начала и диапазон симптомов ГБ; он утверждал, что большинство случаев ГБ в США можно отнести к небольшому числу людей. [119] Это исследование было дополнительно украшено в 1932 году П.Р. Весси, который популяризировал идею о том, что три брата, покинувшие Англию в 1630 году и направлявшиеся в Бостон , были прародителями ГБ в США. [120] Утверждение о том, что были установлены самые ранние прародители, а также евгеническая предвзятость работ Манси, Давенпорта и Весси способствовали недоразумениям и предрассудкам в отношении БГ. [112] Манси и Давенпорт также популяризировали идею о том, что в прошлом некоторые люди с HD могли считаться одержимыми духами или жертвами колдовства , и иногда их избегали или изгоняли общество. [121] [122] Эта идея не была доказана. Исследователи нашли противоположные доказательства; например, сообщество семьи, которую изучал Джордж Хантингтон, открыто принимало тех, у кого были симптомы ГБ. [112] [121]
Поиск причины этого состояния значительно активизировался в 1968 году, когда Милтоном Векслером , психоаналитиком из Лос-Анджелеса , Калифорния , у чьей жены Леоноры Сабин ранее в том же году была диагностирована болезнь Хантингтона, был создан Фонд наследственных заболеваний (HDF). . [123] Трое братьев жены Векслера также страдали этим заболеванием.
Фонд участвовал в привлечении более 100 ученых для участия в совместном проекте США и Венесуэлы по борьбе с болезнью Хантингтона, который в течение 10 лет, начиная с 1979 года, работал над выяснением генетической причины. [124] Это было достигнуто в 1983 году, когда был приблизительно обнаружен причинный ген, [103] а в 1993 году ген был точно локализован на хромосоме 4 (4p16.3). [125] Исследование было сосредоточено на населении двух изолированных венесуэльских деревень, Барранкитас и Лагунетас, где наблюдалась необычно высокая распространенность ГБ, и охватило более 18 000 человек, в основном из одной большой семьи. Локус аутосомного заболевания обнаружен с помощью анализа генетического сцепления . [125] [126] Помимо других инноваций, в рамках проекта были разработаны методы маркировки ДНК , которые стали важным шагом на пути к реализации проекта «Геном человека» . [124]
В то же время были сделаны ключевые открытия, касающиеся механизмов заболевания, в том числе выводы исследовательской группы Аниты Хардинг о влиянии длины гена. [127]
Моделирование заболевания на различных типах животных, таких как трансгенная мышь, выведенная в 1996 году, позволило провести более масштабные эксперименты. Поскольку у этих животных более быстрый метаболизм и гораздо более короткая продолжительность жизни, чем у людей, результаты экспериментов получаются раньше, что ускоряет исследования. Открытие в 1997 году того, что фрагменты mHtt неправильно сворачиваются, привело к открытию ядерных включений, которые они вызывают. Эти достижения привели к все более обширным исследованиям белков, связанных с этим заболеванием, потенциальных медикаментозных методов лечения, методов ухода и самого гена. [110] [128]
Сети ухода и поддержки, которые сложились в Венесуэле и Колумбии во время исследовательских проектов там в 1970-х и 2000-х годах, в конечном итоге были разрушены различными силами, такими как продолжающийся кризис в Венесуэле и смерть ведущего исследователя в Колумбии (Хорхе Даса Баррига). ). [129] Врачи работают над возрождением этих сетей, потому что люди, которые внесли свой вклад в науку о болезни Хантингтона, участвуя в этих исследованиях, заслуживают надлежащего последующего ухода; общества в других частях мира, которые извлекают выгоду из достигнутых таким образом научных достижений, обязаны по крайней мере этим тем, кто участвовал в исследованиях. [129]
Раньше это состояние называлось хореей Хантингтона, но этот термин был заменен болезнью Хантингтона, поскольку не у всех пациентов развивается хорея, а также из-за важности когнитивных и поведенческих проблем. [130]
Генетическое тестирование болезни Хантингтона подняло несколько этических проблем. Проблемы генетического тестирования включают определение того, насколько зрелым должен быть человек, прежде чем его можно будет считать подходящим для тестирования, обеспечение конфиденциальности результатов и следует ли разрешить компаниям использовать результаты тестов для принятия решений о приеме на работу, страховании жизни или других финансовых вопросах. Возникли разногласия, когда Чарльз Дэвенпорт в 1910 году предложил использовать принудительную стерилизацию и иммиграционный контроль для людей с определенными заболеваниями, включая БГ, в рамках евгенического движения. [131] Экстракорпоральное оплодотворение имеет некоторые проблемы, связанные с использованием эмбрионов. Некоторые исследования БГ имеют этические проблемы из-за использования испытаний на животных и эмбриональных стволовых клеток . [132] [133]
Разработка точного диагностического теста на болезнь Хантингтона вызвала социальные, юридические и этические проблемы по поводу доступа к результатам человека и их использования. [134] [135] Многие руководства и процедуры тестирования предусматривают строгие процедуры раскрытия информации и конфиденциальности, позволяющие людям решать, когда и как получать результаты, а также кому они будут доступны. [26] Страховые компании и предприятия сталкиваются с вопросом, следует ли использовать результаты генетических тестов при оценке человека, например, при страховании жизни или трудоустройстве. Страховые компании Соединенного Королевства договорились с Министерством здравоохранения и социального обеспечения , что до 2017 года клиентам не нужно будет раскрывать им прогностические генетические тесты, но это соглашение прямо исключает одобренный правительством тест для болезни Хантингтона при оформлении полисов на сумму более 500 000 фунтов стерлингов. . [136] [137] Как и в случае с другими неизлечимыми генетическими заболеваниями с более поздним началом, проведение предсимптомного тестирования у ребенка или подростка является этически сомнительным, поскольку для этого человека не будет никакой медицинской пользы. Существует консенсус в отношении тестирования только лиц, которые считаются когнитивно зрелыми, хотя существует контраргумент, согласно которому родители имеют право принимать решение от имени своего ребенка. Из-за отсутствия эффективного лечения тестирование лица, не достигшего совершеннолетия , которое не признано дееспособным, в большинстве случаев считается неэтичным. [49] [138] [139]
Существуют этические проблемы, связанные с пренатальным генетическим тестированием или преимплантационной генетической диагностикой, чтобы гарантировать, что ребенок не родится с данным заболеванием. [140] Например, пренатальное тестирование поднимает вопрос о селективном аборте, который некоторые считают неприемлемым. [140] Поскольку это доминантное заболевание, возникают трудности в ситуациях, когда родитель не хочет знать свой собственный диагноз. Это потребует сохранения частей процесса в секрете от родителя. [140]

В 1968 году, после того как Милтон Векслер столкнулся с HD в семье своей жены, он был вдохновлен созданием Фонда наследственных заболеваний (HDF) с целью лечения генетических заболеваний путем координации и поддержки исследований. [17] Фонд и дочь Векслера, Нэнси Векслер , были ключевыми участниками исследовательской группы в Венесуэле, которая обнаружила ген HD. [17]
Примерно в то же время, когда сформировалась HDF, Марджори Гатри помогла основать комитет по борьбе с болезнью Хантингтона (ныне Американское общество по борьбе с болезнью Хантингтона ) после того, как ее муж, фолк-певец и автор песен Вуди Гатри умер от осложнений HD. [18]
С тех пор во многих странах мира сформировались организации поддержки и исследования, которые помогли повысить осведомленность общественности о БГ. Некоторые из них сотрудничают в зонтичных организациях, таких как Международная ассоциация Хантингтона и Европейская сеть HD. [141] Многие организации поддержки проводят ежегодные мероприятия по повышению осведомленности о БГ, некоторые из которых были одобрены соответствующими правительствами. Например, Сенат США объявил 6 июня «Национальным днем распространения информации о болезни Хантингтона» . [142] Существует множество организаций, поддерживающих и информирующих людей, страдающих ГБ, в том числе Ассоциация по болезни Хантингтона в Великобритании. Крупнейшим спонсором исследований является Фонд инициативы по лечению болезни Хантингтона (CHDI). [143]
Исследования механизма БГ сосредоточены на выявлении функционирования Htt, того, как mHtt отличается или мешает ему, а также патологии головного мозга, вызываемой этим заболеванием. [144] Исследования проводятся с использованием методов in vitro , генетически модифицированных животных (также называемых моделями трансгенных животных ) и людей-добровольцев. Модели на животных имеют решающее значение для понимания фундаментальных механизмов, вызывающих заболевание, а также для поддержки ранних стадий разработки лекарств . [128] Идентификация причинного гена позволила развить многие генетически модифицированные организмы , включая нематод (круглых червей), плодовых мух -дрозофил и генетически модифицированных млекопитающих , включая мышей, крыс, овец, свиней и обезьян, которые экспрессируют мутантный хантингтин и развивают прогрессирующую нейродегенерацию . и HD-подобные симптомы. [128]
В настоящее время проводятся исследования с использованием множества подходов, направленных либо на предотвращение болезни Хантингтона, либо на замедление ее прогрессирования. [144] Стратегии, модифицирующие заболевание, можно разделить на три категории: снижение уровня мутантного белка хантингтина (включая сплайсинг генов и подавление генов ); подходы, направленные на улучшение выживаемости нейронов за счет снижения вреда, наносимого белком конкретным клеточным путям и механизмам (включая гомеостаз белка и ингибирование деацетилазы гистонов ); и стратегии замены потерянных нейронов. Кроме того, разрабатываются новые методы лечения для улучшения функционирования мозга; они направлены на разработку симптоматических, а не модифицирующих заболевание методов лечения и включают ингибиторы фосфодиэстеразы . [145] [146]
Фонд CHDI финансирует множество исследовательских инициатив, публикуя множество публикаций. [147] Фонд CHDI является крупнейшим спонсором исследований болезни Хантингтона в мире и стремится найти и разработать лекарства, которые замедлят прогрессирование ГБ. [143] [148] CHDI ранее был известен как High Q Foundation. В 2006 году компания потратила 50 миллионов долларов на исследования болезни Хантингтона. [143] CHDI сотрудничает со многими академическими и коммерческими лабораториями по всему миру и занимается надзором и управлением исследовательскими проектами, а также финансированием. [149]
Замалчивание генов направлено на снижение продукции мутантного белка, поскольку БХ вызывается единственным доминантным геном , кодирующим токсичный белок. Эксперименты по подавлению генов на моделях мышей показали, что когда экспрессия mHtt снижается, симптомы улучшаются. [150] Безопасность РНК-интерференции и методов подавления генов с помощью аллель-специфических олигонуклеотидов (ASO) была продемонстрирована на мышах и мозге крупных приматов-макак. [151] [152] Аллель-специфическое подавление пытается заставить замолчать мутантный htt, оставляя при этом Htt дикого типа нетронутым. Один из способов добиться этого — идентифицировать полиморфизмы, присутствующие только в одной аллели, и производить препараты, подавляющие гены, которые нацелены на полиморфизмы только в мутантном аллеле. [153] Первое испытание по подавлению генов с участием людей с БГ началось в 2015 году, проверяя безопасность IONIS-HTTRx, произведенного Ionis Pharmaceuticals и возглавляемого Институтом неврологии UCL . [154] [155] Мутантный хантингтин был впервые обнаружен и количественно определен в спинномозговой жидкости носителей мутации болезни Хантингтона в 2015 году с использованием нового иммуноанализа «подсчета одиночных молекул» , [156] обеспечивающего прямой способ оценить, является ли хантингтин Снижающие процедуры достигают желаемого эффекта. [157] [158] Испытание третьей фазы этого соединения, переименованного в томинерсен и спонсируемого Roche Pharmaceuticals , началось в 2019 году, но было остановлено в 2021 году после того, как совет по мониторингу безопасности пришел к выводу, что баланс риска и пользы был неблагоприятным. [159] Испытания генной терапии, снижающие хантингтин, проводимые Uniqure, начались в 2019 году, и было объявлено о нескольких испытаниях перорально вводимых соединений-модуляторов сплайсинга, снижающих хантингтин. [160] Рассматриваются методы сплайсинга генов , чтобы попытаться восстановить геном с ошибочным геном, вызывающим HD, с использованием таких инструментов, как CRISPR/Cas9 . [146]
Другая стратегия снижения уровня мутантного хантингтина заключается в увеличении скорости, с которой клетки способны его выводить. [161] Поскольку mHtt (и многие другие белковые агрегаты ) разрушаются в результате аутофагии , увеличение скорости аутофагии потенциально может снизить уровни mHtt и тем самым улучшить течение заболевания. [162] Фармакологические и генетические индукторы аутофагии были протестированы на различных моделях болезни Хантингтона; Было показано, что многие из них снижают уровни mHtt и снижают токсичность. [161]
Среди подходов, направленных на улучшение выживаемости клеток в присутствии мутантного хантингтина, — коррекция регуляции транскрипции с помощью ингибиторов гистондеацетилазы , модуляция агрегации хантингтина, улучшение метаболизма и функции митохондрий и восстановление функции синапсов . [150]
Терапия стволовыми клетками используется для замены поврежденных нейронов путем трансплантации стволовых клеток в пораженные участки мозга. Эксперименты на животных моделях (только крысы и мыши) дали положительные результаты. [163]
Каким бы ни был их будущий терапевтический потенциал, стволовые клетки уже являются ценным инструментом для изучения болезни Хантингтона в лаборатории. [164]
Ферроптоз — это форма регулируемой гибели клеток, характеризующаяся зависимым от железа накоплением гидроперекисей липидов до летальных уровней. ALOX5 -опосредованный ферроптоз действует как путь гибели клеток при окислительном стрессе при болезни Хантингтона [165] . Ингибиторы ферроптоза защищают модели дегенеративных заболеваний головного мозга, включая болезни Паркинсона, Хантингтона и болезни Альцгеймера. [166]
В 2020 году было проведено 197 клинических исследований , связанных с различными методами лечения и биомаркерами болезни Хантингтона, которые были указаны как находящиеся в стадии реализации, набор или недавно завершенные. [167] Испытанные соединения , которые не смогли предотвратить или замедлить прогрессирование болезни Хантингтона, включают ремасемид , коэнзим Q10 , рилузол , креатин , миноциклин , этил-ЭПК , фенилбутират и димебон . [168]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )