Нейросенсорная тугоухость ( SNHL ) — это тип потери слуха , при котором основная причина лежит во внутреннем ухе , сенсорном органе ( улитке и связанных с ней структурах) или вестибулокохлеарном нерве ( VIII черепном нерве ). SNHL составляет около 90% зарегистрированных случаев потери слуха. [ необходима ссылка ] SNHL обычно является постоянной и может быть легкой, умеренной, тяжелой, глубокой или полной. Могут использоваться различные другие описания в зависимости от формы аудиограммы , такие как высокочастотная, низкочастотная, U-образная, зазубренная, пиковая или плоская.
Сенсорная потеря слуха часто возникает в результате повреждения или недостатка волосковых клеток улитки . [ оспаривается – обсудить ] Волосковые клетки могут быть аномальными при рождении или поврежденными в течение жизни человека. Существуют как внешние причины повреждения, включая инфекцию и ототоксичные препараты, так и внутренние причины, включая генетические мутации . Распространенной причиной или усугубляющим фактором при SNHL является длительное воздействие окружающего шума или потеря слуха, вызванная шумом . Воздействие одного очень громкого шума, такого как выстрел из пистолета или взрыв бомбы, может вызвать потерю слуха, вызванную шумом. Использование наушников на высокой громкости в течение длительного времени или регулярное нахождение в шумной обстановке, например, на громком рабочем месте, на спортивных мероприятиях, концертах и использование шумных машин, также может быть риском потери слуха, вызванной шумом.
Невральная , или «ретрокохлеарная», потеря слуха возникает из-за повреждения кохлеарного нерва (CVIII). Это повреждение может повлиять на инициацию нервного импульса в кохлеарном нерве или передачу нервного импульса по нерву в ствол мозга .
Большинство случаев SNHL сопровождаются постепенным ухудшением порогов слуха, происходящим в течение лет или десятилетий. В некоторых случаях потеря может в конечном итоге затронуть большую часть диапазона частот . Она может сопровождаться другими симптомами, такими как звон в ушах ( тиннитус ) и головокружение или предобморочное состояние ( вертиго ). Наиболее распространенным видом сенсоневральной потери слуха является возрастная потеря слуха ( пресбиакузис ), за которой следует потеря слуха, вызванная шумом (NIHL).
Частыми симптомами SNHL являются потеря остроты различения голосов на переднем плане на шумном фоне, трудности с пониманием по телефону, некоторые виды звуков кажутся чрезмерно громкими или резкими, трудности с пониманием некоторых частей речи ( фрикативных и свистящих ), потеря направленности звука (особенно высокочастотных звуков), ощущение, что люди бормочут во время разговора, и трудности с пониманием речи. Подобные симптомы также связаны с другими видами потери слуха; для различения сенсоневральной потери слуха необходимы аудиометрия или другие диагностические тесты.
Выявление нейросенсорной тугоухости обычно осуществляется путем проведения тональной аудиометрии (аудиограммы), при которой измеряются пороги костной проводимости. Тимпанометрия и речевая аудиометрия могут быть полезны. Тестирование проводится аудиологом .
Не существует проверенного или рекомендуемого лечения или излечения от SNHL; управление потерей слуха обычно осуществляется с помощью слуховых стратегий и слуховых аппаратов. В случаях глубокой или полной глухоты кохлеарный имплант является специализированным устройством, которое может восстановить функциональный уровень слуха. SNHL можно, по крайней мере, частично предотвратить, избегая окружающего шума, ототоксичных химикатов и лекарств, травм головы, а также лечения или вакцинации от определенных провоцирующих заболеваний и состояний, таких как менингит .
Поскольку внутреннее ухо не имеет прямого доступа к инструментам, идентификация осуществляется на основании рассказа пациента о симптомах и аудиометрического тестирования. Из тех, кто обращается к врачу с сенсоневральной потерей слуха, 90% сообщают о снижении слуха, 57% сообщают о чувстве заложенности в ухе и 49% сообщают о звоне в ухе ( тиннитусе ). Около половины сообщают о вестибулярных (вертиго) проблемах. [ необходима цитата ]
Для подробного описания симптомов, полезных для скрининга, Американская академия отоларингологии разработала опросник самооценки , который называется «Опросник нарушений слуха у взрослых» (HHIA). Это опросник из 25 вопросов по субъективным симптомам. [1]
Сенсоневральная потеря слуха может быть генетической или приобретенной (например, в результате болезни, шума, травмы и т. д.). Люди могут иметь потерю слуха с рождения ( врожденная ) или потеря слуха может возникнуть позже. Многие случаи связаны со старостью (возрастная). [ необходима цитата ]
Потеря слуха может быть унаследована. Более 40 генов были вовлечены в причину глухоты. [2] Существует 300 синдромов, связанных с потерей слуха, и каждый синдром может иметь причинные гены. [ необходима цитата ]
Рецессивные , доминантные , сцепленные с Х-хромосомой или митохондриальные генетические мутации могут влиять на структуру или метаболизм внутреннего уха. Некоторые из них могут быть точечными мутациями , тогда как другие вызваны хромосомными аномалиями . Некоторые генетические причины приводят к поздней потере слуха. Митохондриальные мутации могут вызывать SNHL iem1555A>G, что делает человека чувствительным к ототоксическим эффектам аминогликозидных антибиотиков .
Прогрессирующая возрастная потеря остроты слуха или чувствительности может начаться уже в возрасте 18 лет, в первую очередь затрагивая высокие частоты, и больше у мужчин, чем у женщин. [6] Такие потери могут проявиться только в более позднем возрасте. Пресбиакузис является, безусловно, доминирующей причиной нейросенсорной потери слуха в индустриальных обществах. Исследование, проведенное в Судане, где население не подвергалось воздействию громкого шума, выявило значительно меньше случаев потери слуха по сравнению с соответствующими по возрасту случаями из индустриальной страны. [7] Аналогичные результаты были получены в исследовании, проведенном среди населения острова Пасхи, которое сообщило об ухудшении слуха среди тех, кто провел время в индустриальных странах, по сравнению с теми, кто никогда не покидал остров. [8] Исследователи утверждают, что факторы, отличные от различий в воздействии шума, такие как генетический состав, также могли способствовать полученным результатам. [9] Потеря слуха, которая ухудшается с возрастом, но вызвана факторами, отличными от обычного старения, такими как потеря слуха, вызванная шумом, не является пресбиакузисом, хотя дифференциация отдельных эффектов множественных причин потери слуха может быть затруднена. У каждого третьего человека к 65 годам наблюдается значительная потеря слуха; к 75 годам — у каждого второго. Возрастная потеря слуха не является ни предотвратимой, ни обратимой.
Большинство людей, живущих в современном обществе, имеют некоторую степень прогрессирующей сенсоневральной (т. е. постоянной) потери слуха, вызванной шумом (NIHL), в результате перегрузки и повреждения сенсорного или нейронного аппарата слуха во внутреннем ухе. [ требуется ссылка ] NIHL обычно представляет собой выпадение или вырез с центром на частоте 4000 Гц. Как интенсивность (SPL), так и продолжительность воздействия, а также повторяющееся воздействие небезопасных уровней шума способствуют повреждению улитки, что приводит к потере слуха. Чем громче шум, тем короче безопасное количество воздействия. NIHL может быть как постоянным, так и временным, называемым пороговым сдвигом. Небезопасные уровни шума могут составлять всего 70 дБ (примерно в два раза громче обычного разговора) при длительном (24 часа) или непрерывном воздействии. 125 дБ (громкий рок-концерт составляет ~120 дБ) — это уровень боли; звуки выше этого уровня вызывают мгновенное и постоянное повреждение уха. [ требуется ссылка ]
Шум и старение являются основными причинами пресбиакузиса , или возрастной потери слуха, наиболее распространенного вида потери слуха в индустриальном обществе. [10] [ необходима цитата ] Опасности воздействия окружающего и профессионального шума широко признаны. Многочисленные национальные и международные организации установили стандарты безопасных уровней воздействия шума в промышленности, охране окружающей среды, военной сфере, на транспорте, в сельском хозяйстве, горнодобывающей промышленности и других областях. [Примечание 1] Интенсивность звука или уровень звукового давления (SPL) измеряется в децибелах (дБ). Для справки:
Увеличение на 6 дБ представляет собой удвоение SPL или энергии звуковой волны, и, следовательно, ее склонности вызывать повреждение ушей. Поскольку человеческие уши слышат логарифмически, а не линейно, требуется увеличение на 10 дБ, чтобы произвести звук, который воспринимается как в два раза громче. Повреждение ушей из-за шума пропорционально интенсивности звука, а не воспринимаемой громкости, поэтому ошибочно полагаться на субъективное восприятие громкости как на показатель риска для слуха, т. е. оно может значительно недооценивать опасность.
Хотя стандарты умеренно различаются по уровням интенсивности и продолжительности воздействия, которые считаются безопасными, можно вывести некоторые рекомендации. [Примечание 2]
Безопасное количество воздействия уменьшается в 2 раза при каждом увеличении уровня звукового давления на 3 дБ (3 дБ по стандарту NIOSH или 5 дБ по стандарту OSHA ). Например, безопасное ежедневное количество воздействия при 85 дБ (90 дБ по OSHA) составляет 8 часов, в то время как безопасное воздействие при 94 дБ(A) (уровень ночного клуба) составляет всего 1 час. Шумовая травма также может вызвать обратимую потерю слуха, называемую временным пороговым сдвигом. Это обычно происходит у людей, которые подвергаются воздействию выстрелов или петард и слышат звон в ушах после этого события ( тиннитус ).
Некоторые безрецептурные и рецептурные препараты, а также некоторые промышленные химикаты ототоксичны. Воздействие этих веществ может привести к временной или постоянной потере слуха.
Некоторые лекарства вызывают необратимые повреждения уха, и по этой причине их применение ограничено. Наиболее важной группой являются аминогликозиды ( главный член гентамицин ). Редкая митохондриальная мутация m.1555A>G может повысить восприимчивость человека к ототоксическому эффекту аминогликозидов. Известно, что длительное злоупотребление гидрокодоном (викодином) вызывает быстро прогрессирующую сенсоневральную потерю слуха, обычно без вестибулярных симптомов. Метотрексат , химиотерапевтический препарат, также известен тем, что вызывает потерю слуха. В большинстве случаев потеря слуха не восстанавливается после прекращения приема препарата. Как это ни парадоксально, метотрексат также используется при лечении аутоиммунно-индуцированной воспалительной потери слуха. [ необходима цитата ]
Различные другие лекарства могут обратимо ухудшать слух. К ним относятся петлевые диуретики , силденафил (Виагра), высокие или постоянные дозы НПВП ( аспирин , ибупрофен , напроксен и различные рецептурные препараты: целекоксиб и т. д.), хинин и макролидные антибиотики ( эритромицин и т. д.). Цитотоксические агенты, такие как карбоплатин, используемый для лечения злокачественных новообразований, могут вызывать дозозависимую SNHL, как и такие препараты, как десфериоксамин, используемый при гематологических расстройствах, таких как талассемия; пациентам, которым прописаны эти препараты, необходимо контролировать слух. [ необходима цитата ]
Длительное или повторяющееся воздействие ототоксичных химических веществ, связанных с окружающей средой или работой, также может привести к нейросенсорной потере слуха. Некоторые из этих химических веществ:
Может быть повреждено либо само ухо, либо центральные слуховые пути, которые обрабатывают информацию, передаваемую ушами. Люди, получившие травму головы, подвержены потере слуха или шуму в ушах, как временному, так и постоянному. Контактные виды спорта, такие как футбол (US NFL), хоккей и крикет, имеют значительную частоту травм головы (сотрясений мозга). В одном опросе вышедших на пенсию игроков NFL, все из которых сообщили об одном или нескольких сотрясениях мозга во время своей игровой карьеры, 25% имели потерю слуха, а 50% имели шум в ушах. [ необходима цитата ]
Они гораздо чаще встречаются у недоношенных детей, особенно тех, кто весит менее 1500 г при рождении. Преждевременные роды могут быть связаны с проблемами, которые приводят к сенсоневральной потере слуха, такими как аноксия или гипоксия (низкий уровень кислорода), желтуха, внутричерепные кровоизлияния, менингит. Сообщается, что фетальный алкогольный синдром вызывает потерю слуха у 64% младенцев, рожденных от матерей- алкоголичек , из-за ототоксического воздействия на развивающийся плод, а также из-за недоедания во время беременности из-за избыточного потребления алкоголя .
Дефицит йода и эндемический гипотиреоз связаны с потерей слуха. [12] Если беременная мать получает недостаточное количество йода во время беременности, это влияет на развитие внутреннего уха у плода, что приводит к сенсоневральной глухоте. Это происходит в определенных регионах мира, таких как Гималаи, где в почве и, следовательно, в рационе питания наблюдается дефицит йода. В этих регионах высока заболеваемость эндемическим зобом. Эту причину глухоты можно предотвратить, добавляя йод в соль.
Инсульт в области мозга, влияющей на слуховую функцию, например, инфаркт в заднем круге кровообращения, может быть связан с глухотой.
Сенсорная потеря слуха вызвана аномальной структурой или функцией волосковых клеток кортиева органа в улитке . [ оспаривается – обсудить ] Нейрональные нарушения слуха являются следствием повреждения восьмого черепного нерва ( вестибулокохлеарного нерва ) или слуховых трактов ствола мозга . Если затронуты более высокие уровни слухового тракта, это известно как центральная глухота. Центральная глухота может проявляться как сенсоневральная глухота, но ее следует отличать от анамнеза и аудиологической диагностики.
Нарушение слуха может быть связано с повреждением волосковых клеток в улитке. Иногда может наблюдаться полная потеря функции внутренних волосковых клеток (ВВК) в определенной области улитки; это называется «мертвой областью». Область может быть определена в терминах диапазона характеристических частот (ХЧ) ВВК и/или нейронов, непосредственно прилегающих к мертвой области.

Наружные волосковые клетки (НВК) вносят вклад в структуру кортиева органа , который расположен между базилярной мембраной и покровной мембраной внутри улитки (см. рисунок 3). Туннель кортиева органа, который проходит через кортиев орган, разделяет НВК и внутренние волосковые клетки (ВВК). НВК соединены с ретикулярной пластинкой и клетками Дейтерса. В каждом человеческом ухе насчитывается около двенадцати тысяч НВК, и они расположены в пять рядов. Каждый НВК имеет небольшие пучки «волосков», или ресничек, на своей верхней поверхности, известные как стереоцилии , и они также расположены в ряды, которые градуируются по высоте. На каждом НВК имеется около 140 стереоцилий. [13]
Основная роль OHC и IHC заключается в том, чтобы функционировать как сенсорные рецепторы . Основная функция IHC заключается в передаче звуковой информации через афферентные нейроны . Они делают это, преобразуя механические движения или сигналы в нейронную активность. При стимуляции стереоцилии на IHC двигаются, заставляя поток электрического тока проходить через волосковые клетки. Этот электрический ток создает потенциалы действия внутри связанных афферентных нейронов.
OHC отличаются тем, что они фактически вносят вклад в активный механизм улитки. Они делают это, принимая механические сигналы или вибрации вдоль базилярной мембраны и преобразуя их в электрохимические сигналы. Стереоцилии, обнаруженные на OHC, находятся в контакте с текториальной мембраной. Поэтому, когда базилярная мембрана движется из-за вибраций, стереоцилии изгибаются. Направление, в котором они изгибаются, диктует частоту срабатывания слуховых нейронов, связанных с OHC. [14]
Изгиб стереоцилий к базальному тельцу НВК вызывает возбуждение волосковой клетки. Таким образом, происходит увеличение частоты срабатывания слуховых нейронов, связанных с волосковой клеткой. С другой стороны, изгиб стереоцилий от базального тела НВК вызывает торможение волосковой клетки. Таким образом, происходит уменьшение частоты срабатывания слуховых нейронов, связанных с волосковой клеткой. НВК уникальны тем, что они способны сокращаться и расширяться (электромобильность). Поэтому в ответ на электрическую стимуляцию, обеспечиваемую эфферентным нервным питанием, они могут изменять длину, форму и жесткость. Эти изменения влияют на реакцию базилярной мембраны на звук. [13] [14] Поэтому ясно, что НВК играют важную роль в активных процессах улитки. [13] Основная функция активного механизма заключается в тонкой настройке базилярной мембраны и обеспечении ее высокой чувствительности к тихим звукам. Активный механизм зависит от того, находится ли улитка в хорошем физиологическом состоянии. Однако улитка очень восприимчива к повреждениям. [14]
SNHL чаще всего вызывается повреждением OHC и IHC. [ оспаривается – обсудить ] Существует два способа, с помощью которых они могут быть повреждены. Во-первых, может погибнуть вся волосковая клетка. Во-вторых, стереоцилии могут быть искажены или разрушены. Повреждение улитки может произойти несколькими способами, например, вирусной инфекцией, воздействием ототоксичных химических веществ и интенсивным шумовым воздействием. Повреждение OHC приводит либо к менее эффективному активному механизму, либо он может вообще не функционировать. OHC способствуют обеспечению высокой чувствительности к тихим звукам в определенном диапазоне частот (приблизительно 2–4 кГц). Таким образом, повреждение OHC приводит к снижению чувствительности базилярной мембраны к слабым звукам. Поэтому требуется усиление этих звуков, чтобы базилярная мембрана могла эффективно реагировать. IHC менее восприимчивы к повреждению по сравнению с OHC. Однако, если они будут повреждены, это приведет к общей потере чувствительности. [14]
Бегущая волна вдоль базилярной мембраны достигает пика в разных местах вдоль нее, в зависимости от того, является ли звук низкочастотным или высокочастотным. Из-за массы и жесткости базилярной мембраны низкочастотные волны достигают пика в верхушке, в то время как высокочастотные звуки достигают пика в базальном конце улитки. [13] Таким образом, каждое положение вдоль базилярной мембраны тонко настроено на определенную частоту. Эти специально настроенные частоты называются характеристическими частотами (CF). [14]
Если звук, входящий в ухо, смещен с характерной частоты, то сила ответа от базилярной мембраны будет постепенно уменьшаться. Тонкая настройка базилярной мембраны создается за счет ввода двух отдельных механизмов. Первый механизм является линейным пассивным механизмом, который зависит от механической структуры базилярной мембраны и окружающих ее структур. Второй механизм является нелинейным активным механизмом, который в первую очередь зависит от функционирования НВК, а также от общего физиологического состояния самой улитки. Основание и вершина базилярной мембраны различаются по жесткости и ширине, что заставляет базилярную мембрану реагировать на различные частоты по-разному по ее длине. Основание базилярной мембраны узкое и жесткое, в результате чего она лучше всего реагирует на высокочастотные звуки. Вершина базилярной мембраны шире и гораздо менее жесткая по сравнению с основанием, в результате чего она лучше всего реагирует на низкие частоты. [14]
Эту избирательность к определенным частотам можно проиллюстрировать с помощью кривых настройки нейронов. Они демонстрируют частоты, на которые реагирует волокно, показывая пороговые уровни (дБ SPL) волокон слухового нерва как функцию различных частот. Это показывает, что волокна слухового нерва реагируют лучше всего и, следовательно, имеют лучшие пороги на характерной частоте волокна и частотах, непосредственно окружающих его. Базилярная мембрана считается «остро настроенной» из-за острой V-образной кривой, с ее «кончиком», центрированным на характерной частоте слуховых волокон. Эта форма показывает, на сколько частот реагирует волокно. Если бы оно имело более широкую форму «V», оно бы реагировало на большее количество частот (см. рисунок 4). [13]

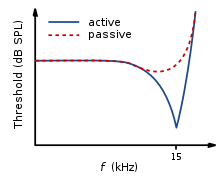
Нормальная кривая настройки нейронов характеризуется широко настроенным низкочастотным «хвостом» с тонко настроенным среднечастотным «кончиком». Однако, если есть частичное или полное повреждение OHC, но с неповрежденными IHC, результирующая кривая настройки будет показывать устранение чувствительности на тихих звуках. То есть там, где кривая настройки нейронов обычно была бы наиболее чувствительной (на «кончике») (см. рисунок 5). [14]
Если повреждены как OHC, так и IHC, то результирующая кривая настройки нейронов покажет устранение чувствительности на «кончике». Однако из-за повреждения IHC вся кривая настройки становится поднятой, что приводит к потере чувствительности на всех частотах (см. рисунок 6). Для устранения тонко настроенного «кончика» достаточно, чтобы был поврежден только первый ряд OHC. Это подтверждает идею о том, что частота повреждения OHC и, следовательно, потери чувствительности к тихим звукам встречается чаще, чем потеря IHC. [14]
Когда IHC или часть базилярной мембраны повреждены или разрушены, так что они больше не функционируют как преобразователи, результатом является «мертвая зона». Мертвые зоны могут быть определены в терминах характерных частот IHC, связанных с определенным местом вдоль базилярной мембраны, где находится мертвая зона. Предполагая, что не было никакого сдвига в характерных частотах, связанных с определенными областями базилярной мембраны, из-за повреждения OHC. Это часто происходит при повреждении IHC. Мертвые зоны также могут быть определены анатомическим местом нефункционирующей IHC (например, «апикальная мертвая зона») или характерными частотами IHC, прилегающими к мертвой зоне. [15]
Мертвые зоны влияют на аудиометрические результаты, но, возможно, не так, как ожидалось. Например, можно ожидать, что пороги не будут получены на частотах в пределах мертвой зоны, но будут получены на частотах, смежных с мертвой зоной. Поэтому, предполагая, что нормальный слух существует вокруг мертвой зоны, это даст аудиограмму , которая имеет резко крутой наклон между частотой, где достигается порог, и частотой, где порог не может быть получен из-за мертвой зоны. [15]


Однако, похоже, это не так. Мертвые зоны не могут быть четко обнаружены с помощью аудиограмм PTA . Это может быть связано с тем, что нейроны, иннервирующие мертвую зону, не могут реагировать на вибрацию на своей характерной частоте. Если вибрация базилярной мембраны достаточно велика, нейроны, настроенные на различные характерные частоты, такие как те, что примыкают к мертвой зоне, будут стимулироваться из-за распространения возбуждения. Следовательно, будет получен ответ от пациента на тестовой частоте. Это называется «слушанием вне места» и также известно как «слушание вне частоты». Это приведет к обнаружению ложного порога. Таким образом, кажется, что у человека лучше слух, чем на самом деле, в результате чего мертвая зона будет пропущена. Следовательно, используя только PTA, невозможно определить протяженность мертвой зоны (см. рисунки 7 и 8). [15]
Следовательно, насколько сильно тон с частотой в пределах мертвой зоны влияет на аудиометрический порог? Это зависит от местоположения мертвой зоны. Пороги в мертвых зонах с низкой частотой более неточны, чем в мертвых зонах с более высокой частотой. Это объясняется тем, что возбуждение, вызванное вибрацией базилярной мембраны, распространяется вверх от апикальных областей базилярной мембраны больше, чем возбуждение распространяется вниз от базальных областей улитки с более высокой частотой. Эта схема распространения возбуждения похожа на явление «восходящего распространения маскировки». Если тон достаточно громкий, чтобы вызвать достаточное возбуждение в нормально функционирующей области улитки, так что он находится выше порога этой области. Тон будет обнаружен из-за прослушивания вне частоты, что приводит к вводящему в заблуждение порогу. [15]
Чтобы помочь преодолеть проблему неточных порогов PTA в мертвых зонах, можно использовать маскировку области за пределами мертвой зоны, которая стимулируется. Это означает, что порог реагирующей зоны достаточно повышен, так что она не может обнаружить распространение возбуждения от тона. Эта техника привела к предположению, что низкочастотная мертвая зона может быть связана с потерей 40-50 дБ. [16] [17] Однако, поскольку одной из целей PTA является определение наличия или отсутствия мертвой зоны, может быть сложно оценить, какие частоты следует маскировать, без использования других тестов. [15]
На основе исследований было высказано предположение, что низкочастотная мертвая зона может вызывать относительно плоскую потерю или очень плавно наклонную потерю в сторону более высоких частот. Поскольку мертвая зона будет менее обнаружима из-за распространения возбуждения вверх. В то время как для высокочастотной мертвой зоны может быть более очевидная круто наклонная потеря на высоких частотах. Хотя вполне вероятно, что наклон представляет собой менее выраженное распространение возбуждения вниз, а не точные пороги для тех частот с нефункционирующими волосковыми клетками. Среднечастотные мертвые зоны с небольшим диапазоном, по-видимому, оказывают меньшее влияние на способность пациента слышать в повседневной жизни и могут вызывать зазубрину в порогах PTA. [15] Хотя очевидно, что PTA не является лучшим тестом для определения мертвой зоны. [18]
Хотя некоторые споры относительно надежности таких тестов продолжаются, [19] было высказано предположение [ weasel words ] , что психоакустические кривые настройки (PTC) и результаты порогового выравнивающего шума (TEN) могут быть полезны для обнаружения мертвых зон, а не PTA. PTC похожи на нейронные кривые настройки. Они иллюстрируют уровень тона маскировщика (дБ SPL) на пороге, как функцию отклонения от центральной частоты (Гц). [13] Они измеряются путем представления фиксированного чистого тона низкой интенсивности с одновременным представлением узкополосного маскировщика с переменной центральной частотой. Уровень маскировщика варьируется, так что уровень маскировщика, необходимый только для маскировки тестового сигнала, находится для маскировщика на каждой центральной частоте. Кончик PTC находится там, где уровень маскировщика, необходимый только для маскировки тестового сигнала, является самым низким. Для людей с нормальным слухом это происходит, когда центральная частота маскировщика наиболее близка к частоте тестового сигнала (см. рисунок 9). [18]
В случае мертвых зон, когда тестовый сигнал лежит в границах мертвой зоны, кончик PTC будет смещен к краю мертвой зоны, к области, которая все еще функционирует и обнаруживает распространение возбуждения от сигнала. В случае мертвой зоны низкой частоты кончик смещен вверх, указывая на мертвую зону низкой частоты, начинающуюся с вершины кривой. Для мертвой зоны высокой частоты кончик смещен вниз от частоты сигнала к функциональной области ниже мертвой зоны. [18] Однако традиционный метод получения PTC непрактичен для клинического использования, и было высказано мнение [ ласкательные слова ] , что TEN недостаточно точны. [18] [19] Был разработан быстрый метод поиска PTC, и он может обеспечить решение. Однако необходимы дополнительные исследования для проверки этого метода, прежде чем его можно будет принять клинически.
Конфигурации аудиограмм не являются хорошими индикаторами того, как мертвая зона будет влиять на человека функционально, в основном из-за индивидуальных различий. [14] Например, наклонная аудиограмма часто присутствует с мертвой зоной из-за распространения возбуждения. Однако человек может быть затронут иначе, чем человек с соответствующей наклонной аудиограммой, вызванной частичным повреждением волосковых клеток, а не мертвой зоной. Они будут воспринимать звуки по-разному, однако аудиограмма предполагает, что у них одинаковая степень потери. Хасс и Мур исследовали, как пациенты с нарушением слуха воспринимают чистые тона, и обнаружили, что они воспринимают тона как шумные и искаженные, больше (в среднем), чем человек без нарушения слуха. Однако они также обнаружили, что восприятие тонов как похожих на шум, не было напрямую связано с частотами в мертвых зонах и, следовательно, не было индикатором мертвой зоны. Следовательно, это говорит о том, что аудиограммы и их плохое представление мертвых зон являются неточными предикторами восприятия пациентом качества чистого тона. [20]
Исследования Клюка и Мура показали, что мертвые области также могут влиять на восприятие пациентом частот за пределами мертвых областей. Наблюдается улучшение способности различать тоны, которые отличаются по частоте совсем немного, в областях сразу за мертвыми областями по сравнению с тонами, расположенными дальше. Объяснением этого может быть то, что произошло корковое перераспределение. В результате чего нейроны, которые обычно стимулировались бы мертвой областью, были переназначены для реагирования на функционирующие области рядом с ней. Это приводит к чрезмерному представлению этих областей, что приводит к повышенной перцептивной чувствительности к небольшим различиям частоты в тонах. [21]
Перед обследованием необходимо собрать анамнез, дающий представление о контексте потери слуха.
Прямое обследование наружного слухового прохода и барабанной перепонки с помощью отоскопа — медицинского прибора, вставляемого в слуховой проход, который с помощью света исследует состояние наружного уха и барабанной перепонки, а также среднего уха через полупрозрачную мембрану.
Дифференциальное тестирование наиболее полезно при односторонней потере слуха и позволяет отличить кондуктивную потерю слуха от сенсоневральной. Оно проводится с помощью низкочастотного камертона, обычно 512 Гц, и контрастных измерений воздушной и костной проводимости звука.
Таблица 1. Таблица сравнения сенсоневральной и кондуктивной тугоухости .
Другие, более сложные, тесты слуховой функции необходимы для различения различных типов потери слуха. Пороги костной проводимости могут дифференцировать сенсоневральную потерю слуха от кондуктивной потери слуха. Другие тесты, такие как отоакустическая эмиссия, акустические стапедиальные рефлексы, речевая аудиометрия и вызванная ответная аудиометрия необходимы для различения сенсорных, нейронных и слуховых нарушений слуха.
Тимпанограмма — это результат теста с помощью тимпанометра. Она проверяет функцию среднего уха и подвижность барабанной перепонки. Она может помочь отличить кондуктивную потерю слуха из-за заболевания среднего уха или барабанной перепонки от других видов потери слуха, включая SNHL.
Аудиограмма — это результат проверки слуха. Наиболее распространенным типом проверки слуха является тональная аудиометрия (ТТА). Она отображает пороги чувствительности слуха на выборке стандартных частот от 250 до 8000 Гц . Существует также высокочастотная тональная аудиометрия, которая проверяет частоты от 8000 до 20 000 Гц. ТТА может использоваться для дифференциации кондуктивной потери слуха, сенсоневральной потери слуха и смешанной потери слуха. Потерю слуха можно описать по ее степени, то есть легкая, умеренная, тяжелая или глубокая, или по ее форме, то есть высокочастотная или наклонная, низкочастотная или восходящая, зазубренная, U-образная или «печенье-кусок», пиковая или плоская.
Существуют также другие виды аудиометрии, предназначенные для проверки остроты слуха, а не чувствительности (речевая аудиометрия), или для проверки передачи слухового нервного пути (вызванная ответная аудиометрия).
МРТ-сканирование может использоваться для выявления грубых структурных причин потери слуха. Оно используется при врожденной потере слуха, когда изменения формы внутреннего уха или слухового нерва могут помочь в диагностике причины потери слуха. Оно также полезно в случаях, когда подозревается опухоль или для определения степени повреждения при потере слуха, вызванной бактериальной инфекцией или аутоиммунным заболеванием. Сканирование не имеет значения при возрастной глухоте.
Пресбиакузис является основной причиной SNHL, прогрессирует и не поддается профилактике, и в настоящее время у нас нет ни соматической, ни генной терапии для борьбы с SNHL, связанной с наследственностью. Но другие причины приобретенной SNHL в значительной степени предотвратимы, особенно причины нозокузисного типа. Это включает в себя избегание окружающего шума и травматического шума, такого как рок-концерты и ночные клубы с громкой музыкой. Использование мер по снижению шума, таких как беруши, является альтернативой, а также изучение уровней шума, которым человек подвергается. В настоящее время существует несколько точных приложений для измерения уровня звука. Сокращение времени воздействия также может помочь контролировать риск от громких воздействий.

Методы лечения делятся на три категории: фармакологические, хирургические и управленческие. Поскольку SNHL является физиологической деградацией и считается постоянной, на данный момент не существует одобренных или рекомендуемых методов лечения.
Были достигнуты значительные успехи в идентификации генов человеческой глухоты и выяснении их клеточных механизмов, а также их физиологической функции у мышей. [22] [23] Тем не менее, возможности фармакологического лечения весьма ограничены и клинически не доказаны. [24] Такие фармацевтические методы лечения, которые применяются, являются скорее паллиативными, чем лечебными, и направлены на основную причину, если ее можно определить, чтобы предотвратить прогрессирующее повреждение.
Глубокая или полная потеря слуха может поддаваться лечению с помощью кохлеарных имплантатов , которые напрямую стимулируют окончания нервов улитки . Кохлеарный имплантат — это хирургическая имплантация электронного медицинского устройства с питанием от батареи во внутреннее ухо. В отличие от слуховых аппаратов , которые делают звуки громче, кохлеарные имплантаты выполняют работу поврежденных частей внутреннего уха (улитки) для передачи звуковых сигналов в мозг. Они состоят как из внутренних имплантированных электродов и магнитов, так и из внешних компонентов. [25] Качество звука отличается от естественного слуха, но может позволить реципиенту лучше распознавать речь и звуки окружающей среды. Из-за риска и расходов такая операция зарезервирована для случаев тяжелого и инвалидизирующего нарушения слуха
Управление сенсоневральной потерей слуха включает в себя использование стратегий для поддержки существующего слуха, таких как чтение по губам, улучшенная коммуникация и т. д. и усиление с помощью слуховых аппаратов . Слуховые аппараты специально настраиваются на индивидуальную потерю слуха, чтобы обеспечить максимальную пользу.
Регенерация волосковых клеток с использованием стволовых клеток и генной терапии станет клинически осуществимой только через несколько лет или десятилетий. [28] Однако в настоящее время ведутся исследования по этому вопросу, и первое одобренное FDA исследование начнется в феврале 2012 года. [29]
Внезапная сенсоневральная потеря слуха (SSHL или SSNHL), обычно известная как внезапная глухота, возникает как необъяснимая, быстрая потеря слуха — обычно на одно ухо — либо сразу, либо в течение нескольких дней. Девять из десяти человек с SSHL теряют слух только на одно ухо. Это следует считать неотложной медицинской ситуацией. Задержка диагностики и лечения может сделать лечение менее эффективным или неэффективным.
По оценкам экспертов, SSHL поражает одного человека из 100 каждый год, как правило, взрослых в возрасте 40–50 лет. Фактическое число новых случаев SSHL каждый год может быть намного выше, поскольку это состояние часто остается недиагностированным.
Многие замечают, что у них ССПЛ, когда просыпаются утром. Другие замечают это впервые, когда пытаются использовать оглохшее ухо, например, когда пользуются телефоном. Третьи замечают громкий, тревожный «хлопок» непосредственно перед тем, как их слух пропадает. Люди с внезапной глухотой часто испытывают головокружение, звон в ушах (тиннитус) или и то, и другое.
SSHL диагностируется с помощью чистотональной аудиометрии. Если тест показывает потерю не менее 30 дБ на трех соседних частотах, потеря слуха диагностируется как SSHL. Например, потеря слуха на 30 дБ сделает разговорную речь более похожей на шепот.
Только 10–15 процентов случаев, диагностированных как SSHL, имеют идентифицируемую причину. Большинство случаев классифицируются как идиопатические , также называемые внезапной идиопатической потерей слуха (SIHL) и идиопатической внезапной сенсоневральной потерей слуха (ISSHL или ISSNHL) [30] [31] Большинство доказательств указывают на некоторый тип воспаления во внутреннем ухе как на наиболее распространенную причину SSNHL.
Потеря слуха полностью восстанавливается примерно у 35–39% пациентов с SSNHL, обычно в течение одной-двух недель с момента начала. [34] Лечение стероидами в течение семи дней, более низкая начальная тяжесть потери слуха, отсутствие головокружения, более молодой возраст пациента и история сердечно-сосудистых заболеваний связаны с полным восстановлением слуха. [35] Восемьдесят пять процентов тех, кто проходит лечение у отоларинголога (иногда называемого ЛОР-хирургом), восстановят часть своего слуха. [ необходима цитата ]
Общая потеря слуха затрагивает около 10% населения мира. [42] Только в Соединенных Штатах ожидается, что 13,5 миллионов американцев имеют сенсоневральную потерю слуха. Из тех, у кого сенсоневральная потеря слуха, примерно 50% имеют врожденную потерю слуха. Остальные 50% вызваны инфекциями матери или плода, послеродовыми инфекциями, вирусными инфекциями, вызванными краснухой или цитомегаловирусом , ототоксичными препаратами, [43] воздействием громких звуков, тяжелой травмой головы и преждевременными родами [44]
Из генетически связанных случаев нейросенсорной потери слуха 75% являются аутосомно-рецессивными , 15-20% аутосомно-доминантными и 1-3% сцепленными с полом. Хотя конкретный ген и белок до сих пор неизвестны, мутации в гене коннексина 26 около локуса DFNB1 хромосомы 13 [45] считаются причиной большинства случаев аутосомно-рецессивной генетической нейросенсорной потери слуха [44]
По крайней мере 8,5 из 1000 детей младше 18 лет страдают сенсоневральной потерей слуха. Общая потеря слуха пропорционально связана с возрастом. По крайней мере 314 из 1000 человек старше 65 лет страдают потерей слуха. Несколько факторов риска сенсоневральной потери слуха были изучены за последнее десятилетие. Остеопороз, операция по стапедэктомии , пневмококковая вакцинация, пользователи мобильных телефонов и гипербилирубинемия при рождении являются одними из некоторых известных факторов риска.
{{cite book}}: |journal=проигнорировано ( помощь )Presbyacusis (или presbyacusis) — это общий термин, который относится к потере слуха у пожилых людей и, как таковой, представляет собой вклад пожизненных повреждений слуховой системы. Из них старение и шумовое повреждение являются главными факторами, а также генетическая восприимчивость, отологические расстройства и воздействие ототоксичных агентов.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка ){{cite journal}}: Цитировать журнал требует |journal=( помощь )