Закись азота (оксид диазота или оксид диазота), широко известный как веселящий газ , закись азота , искусственный воздух и т. д. [4] — это химическое соединение , оксид азота с формулой N
2O. При комнатной температуре это бесцветный негорючий газ , имеющий слегка сладковатый запах и вкус. [4] При повышенных температурах закись азота является мощным окислителем, подобным молекулярному кислороду. [4]
Закись азота имеет важное медицинское применение , особенно в хирургии и стоматологии , благодаря своему анестезирующему и обезболивающему эффекту, [5] и входит в список основных лекарственных средств Всемирной организации здравоохранения . [6] Его разговорное название «веселящий газ», придуманное Хамфри Дэви , описывает эйфорический эффект при вдыхании, который заставляет его использоваться в качестве рекреационного наркотика, вызывающего кратковременный « кайф ». [5] [7] При хроническом злоупотреблении он может вызывать неврологические повреждения из-за инактивации витамина B12 . Он также используется в качестве окислителя в ракетном топливе и топливе для автогонок , а также в качестве вспенивающего газа для взбитых сливок.
Закись азота также является загрязнителем атмосферы , ее концентрация в 2020 году составила 333 части на миллиард (ppb), увеличиваясь на 1 ppb ежегодно. [8] [9] Это основной поглотитель стратосферного озона , воздействие которого сопоставимо с воздействием ХФУ . [10] Около 40% выбросов, вызванных деятельностью человека , приходится на сельское хозяйство , [11] [12] поскольку азотные удобрения перерабатываются в закись азота почвенными микроорганизмами. [13] Будучи третьим по значимости парниковым газом , закись азота вносит существенный вклад в глобальное потепление . [14] [15] Сокращение выбросов является важной целью в политике изменения климата . [16]
Закись азота может использоваться в качестве окислителя в ракетном двигателе. По сравнению с другими окислителями она гораздо менее токсична и более стабильна при комнатной температуре, что облегчает ее хранение и делает ее более безопасной для перевозки в полете. Ее высокая плотность и низкое давление хранения (при поддержании низких температур) делают ее весьма конкурентоспособной по сравнению с системами хранения газа высокого давления. [17] Кроме того, ее можно разложить, образовав воздух для дыхания.
В патенте 1914 года американский пионер ракетной техники Роберт Годдард предложил использовать закись азота и бензин в качестве возможных пропеллентов для жидкотопливной ракеты. [18] Закись азота была выбрана в качестве окислителя в нескольких гибридных конструкциях ракет (использующих твердое топливо с жидким или газообразным окислителем). Сочетание закиси азота с полибутадиеновым топливом с гидроксильным окончанием использовалось SpaceShipOne и другими. Оно также широко используется в любительской и мощной ракетной технике с различными пластиками в качестве топлива.
Закись азота также может быть использована в качестве монотоплива . В присутствии нагретого катализатора при температуре 1070 °F (577 °C) N
2O экзотермически разлагается на безвредные азот и кислород. [19] Из-за большого выделения тепла каталитическое действие быстро становится вторичным, поскольку термическое саморазложение становится доминирующим. В вакуумном двигателе это может обеспечить удельный импульс монотоплива ( I sp ) до 180 с. Хотя это заметно меньше, чем I sp , доступный для двигателей на гидразине (монотопливе или двухтопливе с тетраоксидом диазота ), пониженная токсичность делает закись азота стоящим вариантом.
Воспламенение закиси азота критически зависит от давления. Она дефлагрирует при температуре около 600 °C (1112 °F) при давлении 309 фунтов на квадратный дюйм (21 атмосфера). [20] При 600 фунтах на квадратный дюйм требуемая энергия воспламенения составляет всего 6 джоулей, тогда как при 130 фунтах на квадратный дюйм подводимая энергия воспламенения в 2500 джоулей недостаточна. [21] [22]
В гонках на автомобилях закись азота (часто называемая « нитрос ») увеличивает мощность двигателя , обеспечивая больше кислорода во время сгорания, таким образом позволяя двигателю сжигать больше топлива. Это окислитель, примерно эквивалентный перекиси водорода, и намного сильнее молекулярного кислорода. Закись азота не воспламеняется при низком давлении/температуре, но при температуре около 570 градусов по Фаренгейту (300 °C) ее разложение дает больше кислорода, чем атмосферный воздух. Его часто смешивают с другим топливом, которое легче сгорает.
Закись азота хранится в виде сжатой жидкости. Во впускном коллекторе двигателя испарение и расширение жидкости вызывает значительное падение температуры впускного заряда, что приводит к более плотному заряду и позволяет большему количеству воздушно-топливной смеси поступать в цилиндр. Иногда закись азота впрыскивается во впускной коллектор (или перед ним), тогда как другие системы впрыскивают ее непосредственно перед цилиндром (прямой впрыск в порт).
Эта технология использовалась во время Второй мировой войны самолетами Люфтваффе с системой GM-1 для повышения выходной мощности авиационных двигателей . Первоначально она предназначалась для обеспечения стандартных самолетов Люфтваффе превосходными высотными характеристиками, но технологические соображения ограничили ее применение исключительно большими высотами. Соответственно, она использовалась только специализированными самолетами, такими как высотные разведывательные самолеты , высокоскоростные бомбардировщики и высотные перехватчики . Иногда ее можно было найти на самолетах Люфтваффе, также оснащенных другой системой наддува двигателя, MW 50 , формой впрыска воды для авиационных двигателей, которые использовали метанол для своих возможностей наддува.
Одной из основных проблем окислителя закиси азота в поршневом двигателе является чрезмерная мощность: если механическая структура двигателя не усилена должным образом, она может быть серьезно повреждена или разрушена. Важно при форсировании закисью азота бензиновых двигателей поддерживать надлежащие и равномерно распределенные рабочие температуры и уровни топлива, чтобы предотвратить преждевременное зажигание (также называемое детонацией или стуком). [23] Однако большинство проблем, связанных с закисью азота, возникают не из-за чрезмерной мощности, а из-за избыточного давления, поскольку газ создает гораздо более плотный заряд в цилиндре. Повышенное давление и температура могут расплавить, растрескать или деформировать поршень, клапан и головку цилиндра.
Автомобильная жидкая закись азота немного отличается от медицинской. Небольшое количество диоксида серы ( SO
2) добавляется для предотвращения злоупотребления психоактивными веществами. [24]

Газ одобрен для использования в качестве пищевой добавки ( номер E : E942), в частности, в качестве пропеллента для аэрозольных спреев . Он обычно используется в аэрозольных баллончиках для взбитых сливок и кулинарных спреях .
Газ чрезвычайно растворим в жирных соединениях. В аэрозольных взбитых сливках под давлением он растворяется в жирных сливках до тех пор, пока они не покинут баллончик, где он становится газообразным и таким образом создает пену. Это дает взбитые сливки в четыре раза больше объема жидкости, тогда как взбивание воздуха в сливки дает только в два раза больше объема. В отличие от воздуха, закись азота подавляет прогоркание молочного жира. Диоксид углерода нельзя использовать для взбитых сливок, потому что он кислый в воде, что приведет к свертыванию сливок и придаст им «искру», похожую на сельтерскую воду.
Взбитые сливки, полученные с помощью закиси азота, нестабильны и снова станут жидкими в течение получаса или часа. [25] Таким образом, они не подходят для украшения блюд, которые не будут поданы немедленно.
В декабре 2016 года в США наблюдался дефицит аэрозольных взбитых сливок, а пик потребления консервированных взбитых сливок пришелся на рождественские и праздничные дни из-за взрыва на заводе Air Liquide по производству закиси азота во Флориде в конце августа. Компания отдала приоритет оставшимся поставкам закиси азота медицинским клиентам, а не производству продуктов питания. [26]
Кроме того, в кулинарном спрее, изготовленном из различных масел с эмульгатором лецитином , может использоваться пропеллент закись азота или, в качестве альтернативы, пищевой спирт или пропан .

Закись азота используется в стоматологии и хирургии в качестве анестетика и анальгетика с 1844 года. [27] Вначале газ вводился с помощью простых ингаляторов, состоящих из дыхательного мешка, сделанного из резиновой ткани. [28] Сегодня газ вводится в больницах с помощью автоматизированного аппарата относительной анальгезии с испарителем анестетика и медицинским вентилятором , который подает точно дозированный и активируемый дыханием поток закиси азота, смешанной с кислородом в соотношении 2:1.
Закись азота является слабым общим анестетиком , и поэтому обычно не используется в одиночку при общей анестезии, а используется в качестве газа-носителя (в смеси с кислородом) для более мощных общих анестетиков, таких как севофлюран или десфлуран . Он имеет минимальную альвеолярную концентрацию 105% и коэффициент распределения кровь/газ 0,46. Использование закиси азота при анестезии может увеличить риск послеоперационной тошноты и рвоты. [29] [30] [31]
Стоматологи используют более простую машину, которая выдает только N
2О / О
2Смесь для вдыхания пациентом в сознании, но она должна быть признана специально разработанным относительным анальгезирующим расходомером с минимальным содержанием кислорода 30% в любое время и максимальным верхним пределом 70% закиси азота. Пациент остается в сознании на протяжении всей процедуры и сохраняет достаточные умственные способности, чтобы отвечать на вопросы и инструкции стоматолога. [32]
Вдыхание закиси азота часто используется для облегчения боли, связанной с родами , травмой , хирургией полости рта и острым коронарным синдромом (включая сердечные приступы). Его использование во время родов, как было показано, является безопасной и эффективной помощью для рожениц. [33] Его использование при остром коронарном синдроме имеет неизвестную пользу. [34]
В Канаде и Великобритании энтонокс и нитронокс широко используются бригадами скорой помощи (включая врачей, не имеющих медицинской лицензии) в качестве быстрого и высокоэффективного анальгетического газа.
Пятидесятипроцентный закись азота может рассматриваться для использования обученными непрофессиональными спасателями первой помощи в догоспитальных условиях, учитывая относительную простоту и безопасность применения 50% закиси азота в качестве анальгетика. Быстрая обратимость его эффекта также не позволит ему исключить диагноз. [35]



Рекреационное вдыхание закиси азота , вызывающее эйфорию и легкие галлюцинации , началось в 1799 году среди британского высшего класса на собраниях, известных как «вечеринки веселящего газа». [36]
С 19 века широкая доступность газа для медицинских и кулинарных целей позволила значительно расширить его использование в рекреационных целях по всему миру. В Великобритании по состоянию на 2014 год закись азота, по оценкам, использовалась почти полумиллионом молодых людей в ночных клубах, на фестивалях и вечеринках. [37]
Широкое распространение рекреационного использования препарата по всей Великобритании было показано в документальном фильме Vice 2017 года «Внутри черного рынка веселящего газа» , в котором журналист Мэтт Ши встретился с торговцами препаратом, которые крали его из больниц. [38]
Значительной проблемой, упоминаемой в лондонской прессе, является воздействие мусора из канистр с закисью азота, которое хорошо заметно и вызывает серьезные жалобы со стороны населения. [39]
До 8 ноября 2023 года в Великобритании закись азота подпадала под действие Закона о психоактивных веществах 2016 года, что делало незаконным производство, поставку, импорт или экспорт закиси азота для рекреационного использования. Обновленный закон запрещал хранение закиси азота, классифицируя ее как наркотик класса C в соответствии с Законом о злоупотреблении наркотиками 1971 года. [40]
Хотя большинство потребителей в рекреационных целях считают, что закись азота дает «безопасный кайф», многие не знают, что чрезмерное потребление может вызвать неврологический вред, который, если его не лечить, может привести к необратимому неврологическому повреждению. [41] В Австралии рекреационное использование стало проблемой общественного здравоохранения после роста числа сообщений о нейротоксичности и госпитализации в отделения неотложной помощи . В штате Южная Австралия в 2020 году был принят закон об ограничении продажи баллончиков. [42]
В 2024 году под уличным названием «Галактический газ» закись азота стала пользоваться огромной популярностью среди молодежи для рекреационного использования. Большая часть популярности была создана через TikTok . [43]
Закись азота представляет собой значительную профессиональную опасность для хирургов, стоматологов и медсестер. Поскольку этот газ минимально метаболизируется в организме человека (со скоростью 0,004%), он сохраняет свою активность при выдохе в помещение пациентом и может отравить персонал клиники, если помещение плохо проветривается, с потенциальным хроническим воздействием. Система непрерывной вентиляции свежего воздуха или N
2 Для предотвращения накопления отработанных газов может потребоваться система очистки . [ необходима ссылка ]
Национальный институт охраны труда рекомендует контролировать воздействие закиси азота на работников во время введения анестезирующего газа в медицинских, стоматологических и ветеринарных учреждениях. [44] Он установил рекомендуемый предел воздействия (REL) в размере 25 ppm (46 мг/м3 ) для выделившегося анестетика. [45]
Воздействие закиси азота вызывает кратковременное нарушение познавательных способностей, остроты слуха и зрения, а также нарушение ловкости рук, а также пространственную и временную дезориентацию [46] , подвергая пользователя риску случайной травмы. [47]
Закись азота является нейротоксичной , и среднесрочное или долгосрочное регулярное потребление значительных количеств может вызвать неврологический вред с потенциалом к необратимому повреждению, если его не лечить. [42] [41]
Считается, что, как и другие антагонисты рецепторов NMDA , N
2O вызывает поражения Олни у грызунов при длительном (несколько часов) воздействии. [48] [49] [50] [51]
Однако, поскольку он обычно быстро выводится из организма, он менее вероятно нейротоксичен, чем другие антагонисты NMDAR. [52] У грызунов кратковременное воздействие приводит только к легким повреждениям, которые быстро обратимы, а гибель нейронов наступает только после постоянного и продолжительного воздействия. [48] Закись азота также может вызывать нейротоксичность после длительного воздействия из-за гипоксии . Это особенно касается немедицинских составов, таких как взбитые сливки («whippits» или «nangs»), [53] которые не содержат газообразного кислорода. [54]
В отчетах токсикологических центров у интенсивных пользователей (≥400 г или ≥200 л газа N 2 O за один сеанс) или частых пользователей (регулярно, т. е. ежедневно или еженедельно) развивались признаки периферической невропатии : атаксия (нарушения походки) или парестезия (восприятие ощущений, таких как покалывание, онемение или покалывание, в основном в конечностях). Такие ранние признаки неврологического повреждения указывают на хроническую токсичность . [55]
Закись азота может иметь терапевтическое применение при лечении инсульта . В модели грызунов закись азота в концентрации 75% по объему снижала гибель нейронов, вызванную ишемией, вызванную окклюзией средней мозговой артерии, и снижала вызванный NMDA приток Ca 2+ в культуры нейрональных клеток, что является причиной эксайтотоксичности . [52]
Профессиональное воздействие закиси азота в окружающей среде связано с повреждением ДНК из-за перерывов в синтезе ДНК. [56] Эта корреляция зависит от дозы [57] [58] и, по-видимому, не распространяется на случайное использование в рекреационных целях; однако необходимы дальнейшие исследования для подтверждения уровня воздействия, необходимого для причинения вреда.
Вдыхание чистого оксида азота вызывает кислородное голодание, что приводит к низкому кровяному давлению, обморокам и даже сердечным приступам. Это может произойти, если пользователь вдыхает большие количества непрерывно, как с помощью маски, прикрепленной к газовому баллону или другой ингаляционной системе, или при длительной задержке дыхания. [ необходима цитата ]
Длительное воздействие закиси азота может вызвать дефицит витамина B 12. Это может вызвать серьезную нейротоксичность, если у пользователя уже есть дефицит витамина B 12. [ 59] Он инактивирует кобаламиновую форму витамина B 12 путем окисления. Симптомы дефицита витамина B 12 , включая сенсорную невропатию , миелопатию и энцефалопатию , могут возникнуть в течение нескольких дней или недель после воздействия анестезии закисью азота у людей с субклиническим дефицитом витамина B 12 .
Симптомы лечатся высокими дозами витамина B12 , но выздоровление может быть медленным и неполным. [60]
У людей с нормальным уровнем витамина B 12 есть запасы, которые делают эффекты закиси азота незначительными, если только воздействие не повторяется и не является длительным (злоупотребление закисью азота). Уровни витамина B 12 следует проверять у людей с факторами риска дефицита витамина B 12 перед использованием анестезии закисью азота. [61]
Несколько экспериментальных исследований на крысах показывают, что хроническое воздействие закиси азота на беременных самок может иметь неблагоприятные последствия для развивающегося плода. [62] [63] [64]
При комнатной температуре (20 °C [68 °F]) давление насыщенного пара составляет 50,525 бар, увеличиваясь до 72,45 бар при 36,4 °C (97,5 °F) — критической температуре . Таким образом, кривая давления необычайно чувствительна к температуре. [65]
Как и в случае со многими сильными окислителями, загрязнение деталей топливом было связано с авариями в ракетной технике, когда небольшие количества смесей азота и топлива взрывались из-за эффектов, подобных « гидравлическому удару » (иногда называемых «дизелированием» — нагревание из-за адиабатического сжатия газов может достигать температур разложения). [66] Некоторые обычные строительные материалы, такие как нержавеющая сталь и алюминий, могут выступать в качестве топлива с сильными окислителями, такими как закись азота, как и загрязняющие вещества, которые могут воспламеняться из-за адиабатического сжатия. [67]
Также были случаи, когда разложение закиси азота в водопроводе приводило к взрыву больших резервуаров. [20]
Фармакологический механизм действия ингаляционного N
2O не полностью известен. Однако было показано, что он напрямую модулирует широкий спектр лиганд-управляемых ионных каналов , что, вероятно, играет важную роль. Он умеренно блокирует каналы NMDAR и β 2 -субъединицы , содержащие nACh , слабо ингибирует рецепторы AMPA , каината , GABA C и 5-HT 3 и слегка потенцирует рецепторы GABA A и глицина . [68] [69] Также было показано, что он активирует двухпоровый домен K+
каналы . [70] В то время как N
2O влияет на несколько ионных каналов, его анестезирующий, галлюциногенный и эйфорический эффекты, вероятно, вызваны в основном ингибированием токов, опосредованных рецепторами NMDA. [68] [71] В дополнение к его воздействию на ионные каналы, N
2O2 может действовать аналогично оксиду азота (NO) в центральной нервной системе. [71] Закись азота в 30–40 раз более растворима, чем азот.
Эффекты вдыхания субанестетических доз закиси азота могут непредсказуемо меняться в зависимости от обстановки и индивидуальных различий; [72] [73] однако Джей (2008) [47] предполагает, что это надежно вызывает следующие состояния и ощущения:
Меньшинство пользователей также испытывают неконтролируемые вокализации и мышечные спазмы. Эти эффекты обычно исчезают через несколько минут после удаления источника закиси азота. [47]
В поведенческих тестах на тревожность низкая доза N
2O является эффективным анксиолитиком . Этот противотревожный эффект связан с повышенной активностью рецепторов ГАМК А , поскольку он частично отменяется антагонистами бензодиазепиновых рецепторов . Отражая это, животные, у которых развилась толерантность к анксиолитическому эффекту бензодиазепинов, частично толерантны к N
2О. [74] Действительно, у людей, которым давали 30 % N
2О , антагонисты бензодиазепиновых рецепторов уменьшили субъективные сообщения об ощущении «кайфа», но не изменили психомоторную активность. [75] [76]
Анальгетическое действие N
2O связаны с взаимодействием эндогенной опиоидной системы и нисходящей норадренергической системы. Когда животные получают морфин хронически, у них развивается толерантность к его обезболивающему эффекту, и это также делает животных толерантными к анальгетическому эффекту N
2О. [77] Введение антител , которые связывают и блокируют активность некоторых эндогенных опиоидов (не β-эндорфина ) , также блокирует антиноцицептивные эффекты N
2О . [78] Препараты, которые подавляют распад эндогенных опиоидов, также усиливают антиноцицептивные эффекты N
2О. [78] Несколько экспериментов показали, что антагонисты опиоидных рецепторов, применяемые непосредственно к мозгу, блокируют антиноцицептивные эффекты N
2О , но эти препараты не оказывают никакого эффекта при введении в спинной мозг .
Помимо косвенного действия, закись азота, как и морфин [79], также напрямую взаимодействует с эндогенной опиоидной системой, связываясь с участками связывания опиоидных рецепторов. [80] [81]
Напротив, антагонисты α2 - адренорецепторов блокируют болеутоляющее действие N
2O при введении непосредственно в спинной мозг, но не при введении непосредственно в головной мозг. [82] Действительно, мыши с нокаутированными α 2B -адренорецепторами или животные с дефицитом норадреналина почти полностью устойчивы к антиноцицептивным эффектам N
2О. [83] По-видимому , Н.
2Вызванное O2 высвобождение эндогенных опиоидов вызывает растормаживание норадренергических нейронов ствола мозга , которые высвобождают норадреналин в спинной мозг и подавляют болевую сигнализацию. [84] Как именно N
2Причины высвобождения эндогенных опиоидных пептидов, вызываемые O, остаются неопределенными.
Закись азота — бесцветный газ со слабым сладковатым запахом.
Закись азота поддерживает горение, высвобождая диполярно связанный радикал кислорода, и таким образом может вновь зажечь тлеющую лучину .
Н
2O инертен при комнатной температуре и имеет мало реакций. При повышенных температурах его реакционная способность увеличивается. Например, закись азота реагирует с NaNH
2при 187 °C (369 °F) с образованием NaN3:
Вышеуказанная реакция представляет собой путь, принятый в коммерческой химической промышленности для производства азидных солей, которые используются в качестве детонаторов. [85]
Газ был впервые синтезирован в 1772 году английским натурфилософом и химиком Джозефом Пристли , который назвал его дефлогистированным азотистым воздухом (см. теорию флогистона ) [86] или воспламеняющимся азотистым воздухом . [87] Пристли опубликовал свое открытие в книге « Эксперименты и наблюдения над различными видами воздуха» (1775) , где он описал, как получить препарат «уменьшенного азотистого воздуха» путем нагревания железных опилок, смоченных азотной кислотой . [88]

Первое важное использование закиси азота стало возможным благодаря Томасу Беддоусу и Джеймсу Уатту , которые работали вместе, чтобы опубликовать книгу «Соображения о медицинском использовании и производстве искусственных воздухов» (1794) . Эта книга была важна по двум причинам. Во-первых, Джеймс Уатт изобрел новую машину для производства « искусственных воздухов » (включая закись азота) и новый «дыхательный аппарат» для вдыхания газа. Во-вторых, в книге также были представлены новые медицинские теории Томаса Беддоуса о том, что туберкулез и другие заболевания легких можно лечить с помощью вдыхания «искусственных воздухов». [27]

Машина для производства «искусственных воздухов» состояла из трех частей: печи для сжигания необходимого материала, сосуда с водой, где полученный газ проходил по спиральной трубе (для «смывания» примесей), и, наконец, газового баллона с газометром, где полученный газ, «воздух», можно было подавать в переносные воздушные мешки (изготовленные из воздухонепроницаемого масляного шелка). Дыхательный аппарат состоял из одного из переносных воздушных мешков, соединенных трубкой с мундштуком. С разработкой и производством этого нового оборудования к 1794 году был проложен путь для клинических испытаний , [ необходимо разъяснение ], которые начались в 1798 году, когда Томас Беддоус основал « Пневматический институт для облегчения болезней медицинскими воздухами» в Хотуэллсе ( Бристоль ). В подвале здания крупная машина производила газы под руководством молодого Хэмфри Дэви, которого поощряли экспериментировать с новыми газами для вдыхания пациентами. [27] Первой важной работой Дэви было исследование закиси азота и публикация его результатов в книге: Researches, Chemical and Philosophical (1800) . В этой публикации Дэви отмечает анальгетический эффект закиси азота на странице 465 и ее потенциал для использования при хирургических операциях на странице 556. [89] Дэви придумал название «веселящий газ» для закиси азота. [90]
Несмотря на открытие Дэви, что вдыхание закиси азота может избавить сознательного человека от боли, прошло еще 44 года, прежде чем врачи попытались использовать ее для анестезии . Использование закиси азота в качестве рекреационного наркотика на «вечеринках веселящего газа», в первую очередь устраиваемых для британского высшего класса , стало немедленно успешным, начиная с 1799 года. Хотя воздействие газа обычно заставляет пользователя выглядеть ступорозным, мечтательным и седативным, некоторые люди также «хихикают» в состоянии эйфории и часто взрываются смехом. [91]
Одним из первых коммерческих производителей в США был Джордж По , двоюродный брат поэта Эдгара Аллана По , который также был первым, кто сжижил газ. [92]
Впервые закись азота была использована в качестве анестезирующего средства при лечении пациента, когда дантист Хорас Уэллс , при содействии Гарднера Куинси Колтона и Джона Мэнки Риггса , продемонстрировал нечувствительность к боли при удалении зуба 11 декабря 1844 года. [93] В последующие недели Уэллс лечил первых 12-15 пациентов закисью азота в Хартфорде, штат Коннектикут , и, согласно его собственным записям, потерпел неудачу только в двух случаях. [94] Несмотря на эти убедительные результаты, о которых Уэллс сообщил медицинскому обществу в Бостоне в декабре 1844 года, этот новый метод не был немедленно принят другими дантистами. Причиной этого, скорее всего, было то, что Уэллс в январе 1845 года на своей первой публичной демонстрации медицинскому факультету в Бостоне был частично неудачен, заставив своих коллег сомневаться в его эффективности и безопасности. [95] Метод не получил широкого распространения до 1863 года, когда Гарднер Куинси Колтон успешно начал использовать его во всех своих клиниках «Colton Dental Association», которые он только что основал в Нью-Хейвене и Нью-Йорке . [27] В течение следующих трех лет Колтон и его коллеги успешно вводили закись азота более чем 25 000 пациентов. [28] Сегодня закись азота используется в стоматологии в качестве анксиолитика, как дополнение к местной анестезии .
Однако закись азота не оказалась достаточно сильным анестетиком для использования в крупных хирургических операциях в больницах. Вместо этого диэтиловый эфир , будучи более сильным и мощным анестетиком, был продемонстрирован и принят к использованию в октябре 1846 года, вместе с хлороформом в 1847 году. [27] Однако, когда Джозеф Томас Кловер изобрел «газо-эфирный ингалятор» в 1876 году, в больницах стало обычной практикой начинать все анестезиологические процедуры с небольшого потока закиси азота, а затем постепенно увеличивать анестезию с помощью более сильного эфира или хлороформа. Газо-эфирный ингалятор Кловера был разработан для одновременного снабжения пациента закисью азота и эфиром, при этом точная смесь контролировалась оператором устройства. Он оставался в использовании во многих больницах до 1930-х годов. [28] Хотя сегодня в больницах используются более совершенные анестезиологические аппараты , эти аппараты по-прежнему используют тот же принцип, который был запущен в газоэфирном ингаляторе Кловера, для инициирования анестезии закисью азота перед введением более сильного анестетика.
Популяризация Колтоном закиси азота привела к ее принятию рядом не слишком уважаемых шарлатанов , которые расхваливали ее как лекарство от чахотки , золотухи , катара и других заболеваний крови, горла и легких. Лечение закисью азота проводилось и лицензировалось как патентованное лекарство такими людьми, как CL Blood и Jerome Harris в Бостоне и Charles E. Barney в Чикаго. [96] [97]
Применяются различные методы получения закиси азота. [98]
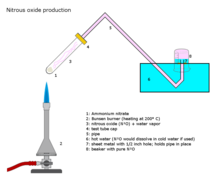
Закись азота получают в промышленных масштабах путем осторожного нагревания нитрата аммония [98] при температуре около 250 °C, который разлагается на закись азота и водяной пар. [99]
Добавление различных фосфатных солей способствует образованию более чистого газа при несколько более низких температурах. Эту реакцию может быть трудно контролировать, что приводит к детонации . [100]
Разложение нитрата аммония также является распространенным лабораторным методом получения газа. Эквивалентно, его можно получить нагреванием смеси нитрата натрия и сульфата аммония : [101]
Другой метод включает реакцию мочевины, азотной кислоты и серной кислоты: [102]
Сообщалось о прямом окислении аммиака с использованием катализатора на основе диоксида марганца и оксида висмута : [103] см . процесс Оствальда .
Хлорид гидроксиламмония реагирует с нитритом натрия , образуя закись азота. Если нитрит добавляется к раствору гидроксиламина, единственным оставшимся побочным продуктом является соленая вода. Однако, если раствор гидроксиламина добавляется к раствору нитрита (нитрит в избытке), то также образуются токсичные высшие оксиды азота:
Лечение HNO
3с SnCl
2и HCl также было продемонстрировано:
Азотистая кислота разлагается на N 2 O и воду с периодом полураспада 16 дней при 25 °C и pH 1–3. [104]
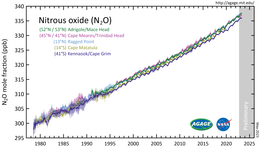



Закись азота является второстепенным компонентом атмосферы Земли и является активной частью планетарного азотного цикла . На основе анализа проб воздуха, собранных по всему миру, его концентрация превысила 330 ppb в 2017 году . [8] Темпы роста около 1 ppb в год также ускорились в течение последних десятилетий. [9] Содержание закиси азота в атмосфере выросло более чем на 20% по сравнению с базовым уровнем около 270 ppb в 1750 году. [106]
Важные атмосферные свойства N
2O обобщены в следующей таблице:
В 2022 году МГЭИК сообщила, что: «Нарушение человеком естественного цикла азота за счет использования синтетических удобрений и навоза, а также осаждение азота в результате земледельческого хозяйства и сжигания ископаемого топлива стали крупнейшим фактором увеличения содержания N2O в атмосфере на 31,0 ± 0,5 ppb (10%) в период с 1980 по 2019 год» [109].
17,0 (от 12,2 до 23,5) миллионов тонн общего среднегодового азота в N
2O был выброшен в атмосферу в 2007–2016 годах. [109] Около 40% N
2Выбросы O происходят от людей , а остальное является частью естественного цикла азота . [110] N
2Выбрасываемый ежегодно человечеством O имеет парниковый эффект, эквивалентный примерно 3 миллиардам тонн углекислого газа: для сравнения, в 2019 году человечество выбросило 37 миллиардов тонн фактического углекислого газа, а метан эквивалентен 9 миллиардам тонн углекислого газа. [111]
Большая часть N
2O, выбрасываемый в атмосферу из природных и антропогенных источников, производится микроорганизмами, такими как денитрифицирующие бактерии и грибы в почвах и океанах. [112] Почвы под естественной растительностью являются важным источником закиси азота, на долю которых приходится 60% всех естественных выбросов. Другие естественные источники включают океаны (35%) и атмосферные химические реакции (5%). [113] Водно-болотные угодья также могут быть источниками закиси азота . [114] [115] Выбросы от таяния вечной мерзлоты могут быть значительными, но по состоянию на 2022 год это не точно. [109]
Основными компонентами антропогенных выбросов являются удобренные сельскохозяйственные почвы и навоз скота (42%), стоки и выщелачивание удобрений (25%), сжигание биомассы (10%), сжигание ископаемого топлива и промышленные процессы (10%), биологическая деградация других азотсодержащих атмосферных выбросов (9%) и человеческие сточные воды (5%). [116] [117] [118] [119] [120] Сельское хозяйство увеличивает производство закиси азота за счет обработки почвы, использования азотных удобрений и переработки отходов животных. [121] Эти виды деятельности стимулируют естественные бактерии производить больше закиси азота. Выбросы закиси азота из почвы может быть сложно измерить, поскольку они заметно меняются во времени и пространстве, [122] и большая часть годовых выбросов может происходить при благоприятных условиях в «горячие моменты» [123] [124] и/или в благоприятных местах, известных как «горячие точки». [125]
Среди промышленных выбросов, производство азотной кислоты и адипиновой кислоты являются крупнейшими источниками выбросов закиси азота. Выбросы адипиновой кислоты возникают, в частности, из-за деградации промежуточного продукта нитрокислоты, полученного из нитрования циклогексанона. [116] [126] [127]
Микробные процессы, которые генерируют закись азота, можно классифицировать как нитрификацию и денитрификацию . В частности, они включают:
На эти процессы влияют химические и физические свойства почвы, такие как наличие минерального азота и органических веществ , кислотность и тип почвы, а также климатические факторы, такие как температура почвы и содержание воды.
Выброс газа в атмосферу в значительной степени ограничен его потреблением внутри клеток, процессом, катализируемым ферментом редуктазой закиси азота . [128]
Глобальный учет N
2Источники и поглотители O за десятилетие, закончившееся в 2016 году, показывают, что около 40% от среднего объема выбросов в 17 ТгN/год ( тераграммов , или миллионов метрических тонн азота в год) были вызваны деятельностью человека, и показывают, что рост выбросов в основном произошел за счет расширения сельского хозяйства . [11] [12]

Закись азота имеет значительный потенциал глобального потепления как парниковый газ . В расчете на молекулу, рассматриваемую в течение 100-летнего периода, закись азота имеет в 265 раз большую способность удерживать тепло в атмосфере, чем углекислый газ ( CO
2). [108] Однако из-за его низкой концентрации (менее 1/1000 концентрации CO
2), его вклад в парниковый эффект составляет менее одной трети от вклада углекислого газа, а также меньше, чем у метана . [129] С другой стороны, поскольку около 40% N
2Попадание O в атмосферу является результатом деятельности человека, [116] контроль закиси азота является частью усилий по ограничению выбросов парниковых газов. [130]
Большая часть антропогенного выброса закиси азота в атмосферу — это выбросы парниковых газов в сельском хозяйстве , когда фермеры добавляют азотные удобрения на поля, а также через разложение навоза животных. Сокращение выбросов может быть горячей темой в политике изменения климата . [131]
Закись азота также выделяется как побочный продукт сжигания ископаемого топлива, хотя количество выделяемого зависит от того, какое топливо использовалось. Она также выделяется при производстве азотной кислоты , которая используется в синтезе азотных удобрений. Производство адипиновой кислоты, предшественника нейлона и других синтетических волокон для одежды, также выделяет закись азота. [132]
Повышение концентрации закиси азота в атмосфере рассматривается как возможный фактор, способствовавший чрезвычайно интенсивному глобальному потеплению во время пограничного события сеномана и турона . [133]
Закись азота также участвует в истончении озонового слоя . Исследование 2009 года показало, что N
2Выбросы O были наиболее значительными выбросами, разрушающими озоновый слой, и, как ожидается, останутся крупнейшими в течение всего 21-го века. [10] [134]
Перекачка закиси азота из баллонов большого объема в меньшие, более транспортабельные баллоны типа Е емкостью 1590 литров [135] является законной, если она предназначена для медицинской анестезии.
Министерство здравоохранения предупредило, что закись азота является рецептурным лекарством, продажа или хранение которого без рецепта является правонарушением в соответствии с Законом о лекарственных средствах. [136] Это, по-видимому, запретит все немедицинские виды использования закиси азота, хотя подразумевается, что под запрет будет подпадать только рекреационное использование.
В августе 2015 года Совет лондонского района Ламбет ( Великобритания ) запретил использование препарата в рекреационных целях, наложив на нарушителей штраф на месте в размере до 1000 фунтов стерлингов. [137]
В сентябре 2023 года правительство объявило, что к концу года закись азота будет объявлена незаконной, а ее хранение может повлечь за собой тюремное заключение сроком до двух лет или неограниченный штраф. [138]
Владение закисью азота является законным в соответствии с федеральным законом и не подлежит компетенции DEA . [139] Однако оно регулируется Управлением по контролю за продуктами питания и лекарственными средствами в соответствии с Законом о пищевых продуктах, лекарственных средствах и косметике; судебное преследование возможно в соответствии с его положениями о «неправильном брендинге», запрещающими продажу или распространение закиси азота с целью потребления человеком без надлежащей медицинской лицензии. Во многих штатах есть законы, регулирующие владение, продажу и распространение закиси азота. Такие законы обычно запрещают распространение среди несовершеннолетних или ограничивают количество, которое может быть продано без специальной лицензии. [ необходима цитата ] Например, в Калифорнии хранение для рекреационного использования запрещено и квалифицируется как правонарушение. [140]
{{cite journal}}: CS1 maint: bot: original URL status unknown (link)...Самостоятельное нагнетание давления (давление паров при 20 °C составляет ~50,1 бар...Нетоксично, низкая реактивность -> отн. безопасное обращение (Общая безопасность ???)...Дополнительная энергия от разложения (как монотопливо: ISP 170 с)...Удельный импульс не сильно меняется с O/F...[страница 2] N
2
O является монотопливом (как H
2
O
2
или гидразин...)
, N2O, текущий при давлении 130 фунтов на квадратный дюйм в эпоксидной композитной трубе, не будет реагировать даже при подаче энергии воспламенения в 2500 Дж. Однако при давлении 600 фунтов на квадратный дюйм требуемая энергия воспламенения составит всего 6 Дж.
{{cite journal}}: CS1 maint: overridden setting (link)