Вирусы иммунодефицита человека ( ВИЧ ) представляют собой два вида лентивирусов (подгруппа ретровирусов ), которые заражают человека. Со временем они вызывают синдром приобретенного иммунодефицита (СПИД), [1] [2] состояние, при котором прогрессирующий отказ иммунной системы приводит к развитию опасных для жизни оппортунистических инфекций и рака . [3] Без лечения среднее время выживания после заражения ВИЧ оценивается в 9–11 лет, в зависимости от подтипа ВИЧ . [4]
В большинстве случаев ВИЧ является инфекцией, передающейся половым путем , и возникает при контакте или передаче крови , предэякулята , спермы и вагинальных выделений . [5] [6] Неполовым путем передача инфекции может произойти от инфицированной матери ее ребенку во время беременности , во время родов при контакте с ее кровью или вагинальной жидкостью, а также через грудное молоко . [7] [8] [9] [10] В этих жидкостях организма ВИЧ присутствует как в виде свободных вирусных частиц, так и в виде вируса внутри инфицированных иммунных клеток . Исследования показали (как для однополых, так и для разнополых пар), что ВИЧ не передается при половом акте без презервативов, если у ВИЧ-положительного партнера постоянно неопределяемая вирусная нагрузка . [5] [6]
ВИЧ инфицирует жизненно важные клетки иммунной системы человека, такие как Т-хелперы (в частности, CD4 + Т-клетки), макрофаги и дендритные клетки . [11] ВИЧ-инфекция приводит к низким уровням CD4 + Т-клеток посредством ряда механизмов, включая пироптоз абортивно инфицированных Т-клеток, [12] апоптоз неинфицированных клеток-свидетелей, [13] прямое вирусное уничтожение инфицированных клеток и уничтожение инфицированные CD4 + Т-клетки цитотоксическими CD8 + лимфоцитами , которые распознают инфицированные клетки. [14] Когда количество CD4 + Т-клеток снижается ниже критического уровня, клеточный иммунитет теряется, и организм становится все более восприимчивым к оппортунистическим инфекциям, что приводит к развитию СПИДа.
ВИЧ является представителем рода Lentivirus , [15] частью семейства Retroviridae . [16] Лентивирусы имеют много общих морфологических и биологических свойств. Многие виды заражены лентивирусами, которые обычно вызывают длительные заболевания с длительным инкубационным периодом . [17] Лентивирусы передаются в виде одноцепочечных РНК-вирусов с положительным смыслом и оболочкой . При попадании в клетку-мишень геном вирусной РНК преобразуется (обратно транскрибируется) в двухцепочечную ДНК с помощью кодируемого вирусом фермента обратной транскриптазы , который транспортируется вместе с вирусным геномом в вирусной частице. Полученная вирусная ДНК затем импортируется в ядро клетки и интегрируется в клеточную ДНК с помощью кодируемого вирусом фермента интегразы и кофакторов хозяина . [18] После интеграции вирус может стать латентным , позволяя вирусу и его клетке-хозяину избегать обнаружения иммунной системой в течение неопределенного периода времени. [19] Вирус может оставаться в спящем состоянии в организме человека до десяти лет после первичного заражения; в этот период вирус не вызывает симптомов. Альтернативно, интегрированная вирусная ДНК может быть транскрибирована , производя новые геномы РНК и вирусные белки, используя ресурсы клетки-хозяина, которые упаковываются и высвобождаются из клетки в виде новых вирусных частиц, которые начинают цикл репликации заново.
Охарактеризованы два типа ВИЧ: ВИЧ-1 и ВИЧ-2. ВИЧ-1 — это вирус, который был первоначально обнаружен и назван как вирусом, ассоциированным с лимфаденопатией (LAV), так и Т-лимфотропным вирусом человека 3 (HTLV-III). ВИЧ-1 более вирулентен и более заразен , чем ВИЧ-2 [20] и является причиной большинства случаев ВИЧ-инфекции во всем мире. Более низкая инфекционность ВИЧ-2 по сравнению с ВИЧ-1 означает, что за один контакт заразится меньше людей, подвергшихся воздействию ВИЧ-2. Из-за относительно низкой способности передачи ВИЧ-2 в основном ограничивается Западной Африкой . [21]

ВИЧ по структуре похож на другие ретровирусы. Он имеет примерно сферическую форму [22] с диаметром около 120 нм , что примерно в 100 000 раз меньше по объему, чем эритроцит . [23] Он состоит из двух копий одноцепочечной РНК с положительным смыслом , которая кодирует девять генов вируса, заключенных в конический капсид , состоящий из 2000 копий вирусного белка p24 . [24] Одноцепочечная РНК прочно связана с белками нуклеокапсида, p7, и ферментами, необходимыми для развития вириона, такими как обратная транскриптаза , протеазы , рибонуклеаза и интеграза . Матрица, состоящая из вирусного белка p17, окружает капсид, обеспечивая целостность частицы вириона. [24]
Он, в свою очередь, окружен вирусной оболочкой , которая состоит из липидного бислоя , взятого из мембраны клетки-хозяина человека, когда вновь образованные вирусные частицы отпочковываются от клетки. Вирусная оболочка содержит белки клетки-хозяина и относительно небольшое количество копий белка оболочки ВИЧ, [24] который состоит из колпачка, состоящего из трех молекул, известных как гликопротеин (gp) 120 , и стебля, состоящего из трех молекул gp41 , которые закрепляют структуры в вирусную оболочку. [25] [26] Белок оболочки, кодируемый геном env ВИЧ , позволяет вирусу прикрепляться к клеткам-мишеням и соединять вирусную оболочку с мембраной клетки- мишени , высвобождая вирусное содержимое в клетку и инициируя инфекционный цикл. [25]
.jpg/440px-Protein_Structure_Diagram_of_Fusion_Peptide_Epitope_on_HIV_Spike_(41863579304).jpg)
Белок оболочки, единственный вирусный белок на поверхности вируса, является основной мишенью для разработки вакцины против ВИЧ . [27] Более половины массы тримерного шипа оболочки составляют N-связанные гликаны . Плотность высока, поскольку гликаны защищают основной вирусный белок от нейтрализации антителами. Это одна из наиболее плотно гликозилированных известных молекул, плотность которой достаточно высока, чтобы предотвратить нормальный процесс созревания гликанов во время биогенеза в эндоплазматическом аппарате и аппарате Гольджи. [28] [29] Таким образом, большинство гликанов остаются незрелыми гликанами с «высоким содержанием маннозы», которые обычно не присутствуют на гликопротеинах человека, которые секретируются или присутствуют на поверхности клеток. [30] Необычная обработка и высокая плотность означают, что почти все широко нейтрализующие антитела, которые были идентифицированы до сих пор (у подгруппы пациентов, которые были инфицированы в течение многих месяцев или лет), связываются с этими оболочками или адаптируются к ним. гликаны. [31]
Молекулярная структура вирусного шипа теперь определена методами рентгеновской кристаллографии [32] и криогенной электронной микроскопии . [33] Эти достижения в структурной биологии стали возможными благодаря разработке стабильных рекомбинантных форм вирусного спайка путем введения межсубъединичной дисульфидной связи и изолейцина с мутацией пролина ( радикальная замена аминокислоты) в gp41. [34] Так называемые тримеры SOSIP не только воспроизводят антигенные свойства нативного вирусного шипа, но также демонстрируют ту же степень незрелых гликанов, что и нативный вирус. [35] Рекомбинантные тримерные вирусные шипы являются многообещающими кандидатами на вакцины, поскольку они содержат меньше ненейтрализующих эпитопов , чем рекомбинантный мономерный gp120, который подавляет иммунный ответ на целевые эпитопы. [36]

Геном РНК состоит как минимум из семи структурных ориентиров ( LTR , TAR , RRE , PE, SLIP, CRS и INS) и девяти генов ( gag , pol и env , tat , rev , nef , vif , vpr , vpu , а иногда и десятый tev , который представляет собой слияние tat , env и rev ), кодирующего 19 белков. Три из этих генов, gag , pol и env , содержат информацию, необходимую для создания структурных белков для новых вирусных частиц. [24] Например, env кодирует белок под названием gp160, который клеточная протеаза разрезает на две части с образованием gp120 и gp41. Шесть оставшихся генов, tat , rev , nef , vif , vpr и vpu (или vpx в случае ВИЧ-2), являются регуляторными генами белков, которые контролируют способность ВИЧ инфицировать клетки, продуцировать новые копии вируса ( копировать) или вызвать заболевание. [24]
Два белка tat (p16 и p14) являются транскрипционными трансактиваторами промотора LTR , действующими путем связывания элемента РНК TAR. TAR также может быть переработан в микроРНК , которые регулируют гены апоптоза ERCC1 и IER3 . [37] [38] Белок rev (p19) участвует в транспортировке РНК из ядра и цитоплазмы путем связывания с элементом РНК RRE . Белок vif (p23) предотвращает действие APOBEC3G (клеточного белка, который дезаминирует цитидин в уридин в одноцепочечной вирусной ДНК и/или препятствует обратной транскрипции [39] ). Белок vpr (p14) останавливает деление клеток на уровне G2/M . Белок nef (p27) подавляет CD4 (основной вирусный рецептор), а также молекулы MHC класса I и класса II . [40] [41] [42]
Nef также взаимодействует с доменами SH3 . Белок vpu (p16) влияет на высвобождение новых вирусных частиц из инфицированных клеток. [24] Концы каждой цепи РНК ВИЧ содержат последовательность РНК, называемую длинным терминальным повтором (LTR). Области LTR действуют как переключатели, контролирующие выработку новых вирусов, и могут запускаться белками ВИЧ или клетки-хозяина. Элемент Psi участвует в упаковке вирусного генома и распознается белками gag и rev . Элемент SLIP (ТТТТТТ) участвует в сдвиге кадра в рамке считывания gag - pol , необходимом для создания функционального pol . [24]
Термин вирусный тропизм относится к типам клеток, которые заражает вирус. ВИЧ может инфицировать различные иммунные клетки, такие как CD4 + Т-клетки , макрофаги и клетки микроглии . Проникновение ВИЧ-1 в макрофаги и CD4 + Т-клетки опосредовано взаимодействием гликопротеинов оболочки вириона (gp120) с молекулой CD4 на мембране клеток-мишеней, а также с хемокиновыми корецепторами . [25] [43]
Макрофаготропные (М-тропные) штаммы ВИЧ-1, или штаммы, не индуцирующие синцитий (NSI; теперь называемые вирусами R5 [44] ), используют рецептор β -хемокина CCR5 для проникновения и, таким образом, способны реплицироваться в как макрофаги, так и CD4 + Т-клетки. [45] Этот корецептор CCR5 используется почти всеми первичными изолятами ВИЧ-1, независимо от генетического подтипа вируса. Действительно, макрофаги играют ключевую роль в нескольких критических аспектах ВИЧ-инфекции. По-видимому, они являются первыми клетками, инфицированными ВИЧ, и, возможно, источником продукции ВИЧ, когда у пациента истощаются клетки CD4 + . Макрофаги и микроглиальные клетки – это клетки центральной нервной системы , инфицированные ВИЧ . В миндалинах и аденоидах ВИЧ-инфицированных пациентов макрофаги сливаются в многоядерные гигантские клетки , которые производят огромное количество вируса.
Т-тропные штаммы ВИЧ-1, или штаммы, индуцирующие синцитии (SI; теперь называемые вирусами Х4 [44] ), реплицируются в первичных CD4 + Т-клетках, а также в макрофагах и используют для проникновения рецептор α -хемокина, CXCR4 . [45] [46] [47]
Двойные тропные штаммы ВИЧ-1 считаются переходными штаммами ВИЧ-1 и, таким образом, способны использовать как CCR5, так и CXCR4 в качестве корецепторов для проникновения вируса.
α - хемокин SDF-1 , лиганд CXCR4, подавляет репликацию Т-тропных изолятов ВИЧ-1. Это происходит за счет снижения экспрессии CXCR4 на поверхности клеток-мишеней ВИЧ. М-тропные изоляты ВИЧ-1, которые используют только рецептор CCR5, называются R5; те, которые используют только CXCR4, называются X4, а те, которые используют оба, X4R5. Однако использование только корецепторов не объясняет вирусный тропизм, поскольку не все вирусы R5 способны использовать CCR5 на макрофагах для продуктивной инфекции [45], а ВИЧ может также инфицировать подтип миелоидных дендритных клеток , [48 ] вероятно, представляют собой резервуар , в котором сохраняется инфекция, когда количество CD4 + Т-клеток снижается до чрезвычайно низкого уровня.
Некоторые люди устойчивы к определенным штаммам ВИЧ. [49] Например, люди с мутацией CCR5-Δ32 устойчивы к заражению вирусом R5, поскольку мутация не позволяет ВИЧ связываться с этим корецептором, снижая его способность инфицировать клетки-мишени.
Половой акт является основным способом передачи ВИЧ. ВИЧ как X4, так и R5 присутствует в семенной жидкости , что позволяет вирусу передаваться от мужчины к его сексуальному партнеру . Затем вирионы могут инфицировать многочисленные клеточные мишени и распространяться по всему организму. Однако процесс отбора [ требуется дальнейшее объяснение ] приводит к преимущественной передаче вируса R5 по этому пути. [50] [51] [52] У пациентов, инфицированных подтипом B ВИЧ-1, на поздних стадиях заболевания часто происходит переключение корецепторов и Т-тропные варианты, которые могут инфицировать различные Т-клетки через CXCR4. [53] Эти варианты затем более агрессивно реплицируются с повышенной вирулентностью, что вызывает быстрое истощение Т-клеток, коллапс иммунной системы и оппортунистические инфекции, которые знаменуют появление СПИДа. [54] ВИЧ-положительные пациенты приобретают чрезвычайно широкий спектр оппортунистических инфекций, что было особенно проблематично до появления ВААРТ ; однако те же самые инфекции наблюдаются среди ВИЧ-инфицированных пациентов, обследованных посмертно после начала антиретровирусной терапии. [3] Таким образом, в ходе инфекции адаптация вируса к использованию CXCR4 вместо CCR5 может быть ключевым этапом в развитии СПИДа. Ряд исследований с участием людей, инфицированных подтипом B, установили, что от 40 до 50 процентов больных СПИДом могут быть носителями вирусов фенотипа SI и, предположительно, X4. [55] [56]
ВИЧ-2 гораздо менее патогенен, чем ВИЧ-1, и его распространение по всему миру ограничено Западной Африкой . Принятие ВИЧ-2 «дополнительных генов» и более беспорядочный характер использования корецепторов (включая независимость от CD4) могут помочь вирусу в его адаптации, чтобы избежать врожденных факторов рестрикции, присутствующих в клетках-хозяевах. Адаптация к использованию обычных клеточных механизмов для обеспечения передачи и продуктивного заражения также способствовала установлению репликации ВИЧ-2 у людей. Стратегия выживания любого инфекционного агента заключается не в том, чтобы убить своего хозяина, а в конечном итоге стать комменсальным организмом. Достигнув низкой патогенности, со временем будут выбраны более успешные при передаче варианты. [57]
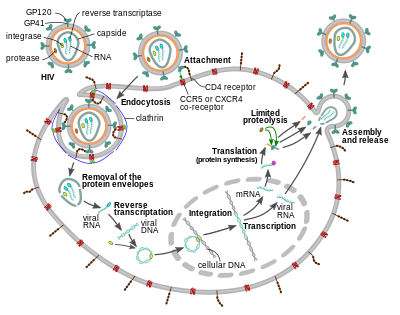

Вирион ВИЧ проникает в макрофаги и CD4 + Т-клетки путем адсорбции гликопротеинов на его поверхности к рецепторам клетки-мишени с последующим слиянием вирусной оболочки с мембраной клетки-мишени и высвобождением капсида ВИЧ в клетку. [58] [59]
Проникновение в клетку начинается посредством взаимодействия комплекса тримерной оболочки ( шип gp160 ) на оболочке вируса ВИЧ, а также CD4 и хемокинового корецептора (обычно либо CCR5 , либо CXCR4 , но известно, что другие взаимодействуют) на поверхности клетки-мишени. [58] [59] Gp120 связывается с интегрином α 4 β 7 , активируя LFA-1 , центральный интегрин, участвующий в создании вирусологических синапсов , которые способствуют эффективному распространению ВИЧ-1 от клетки к клетке. [60] Шип gp160 содержит связывающие домены как для CD4, так и для хемокиновых рецепторов. [58] [59]
Первый этап слияния включает высокоаффинное присоединение CD4-связывающих доменов gp120 к CD4. Как только gp120 связывается с белком CD4, комплекс оболочки претерпевает структурные изменения, обнажая домены связывания хемокинового рецептора gp120 и позволяя им взаимодействовать с целевым хемокиновым рецептором. [58] [59] Это обеспечивает более стабильное двустороннее прикрепление, что позволяет N-концевому слитому пептиду gp41 проникать через клеточную мембрану. [58] [59] Повторяющиеся последовательности в gp41, HR1 и HR2 затем взаимодействуют, вызывая коллапс внеклеточной части gp41 в форму шпильки. Эта петлевая структура сближает вирус и клеточные мембраны, обеспечивая слияние мембран и последующее проникновение вирусного капсида. [58] [59]
После того, как ВИЧ связался с клеткой-мишенью, в клетку вводятся РНК ВИЧ и различные ферменты, включая обратную транскриптазу, интегразу, рибонуклеазу и протеазу. [58] [ не удалось проверить ] Во время транспорта в ядро с помощью микротрубочек геном вирусной одноцепочечной РНК транскрибируется в двухцепочечную ДНК, которая затем интегрируется в хромосому хозяина.
ВИЧ может инфицировать дендритные клетки (ДК) по этому пути CD4-CCR5, но также можно использовать другой путь с использованием маннозоспецифичных лектиновых рецепторов С-типа, таких как DC-SIGN . [61] ДК являются одними из первых клеток, с которыми сталкивается вирус при передаче половым путем. В настоящее время считается, что они играют важную роль, передавая ВИЧ Т-клеткам, когда вирус захватывается в слизистой оболочке ДК. [61] Считается , что наличие FEZ-1 , который естественным образом встречается в нейронах , предотвращает заражение клеток ВИЧ. [62]

Долгое время считалось, что проникновение ВИЧ-1, как и многих других ретровирусов, происходит исключительно через плазматическую мембрану. Однако совсем недавно сообщалось о продуктивном заражении посредством рН -независимого клатрин-опосредованного эндоцитоза ВИЧ-1, который недавно был предложен как единственный путь продуктивного проникновения. [63] [64] [65] [66] [67]

Вскоре после того, как вирусный капсид попадает в клетку, фермент , называемый обратной транскриптазой, освобождает геном одноцепочечной РНК с положительным смыслом от прикрепленных вирусных белков и копирует его в молекулу комплементарной ДНК (кДНК). [68] Процесс обратной транскрипции чрезвычайно подвержен ошибкам, и возникающие в результате мутации могут вызвать устойчивость к лекарствам или позволить вирусу уклониться от иммунной системы организма. Обратная транскриптаза также обладает рибонуклеазной активностью, которая разрушает вирусную РНК во время синтеза кДНК, а также ДНК-зависимой активностью ДНК-полимеразы, которая создает смысловую ДНК из антисмысловой кДНК. [69] Вместе кДНК и ее комплемент образуют двухцепочечную вирусную ДНК, которая затем транспортируется в ядро клетки . Интеграция вирусной ДНК в геном клетки-хозяина осуществляется другим вирусным ферментом, называемым интегразой . [68]
Интегрированная вирусная ДНК может затем находиться в спящем состоянии на латентной стадии ВИЧ-инфекции. [68] Для активной продукции вируса должны присутствовать определенные клеточные факторы транскрипции , наиболее важным из которых является NF- κ B (ядерный фактор каппа B), который активируется, когда Т-клетки активируются. [70] Это означает, что ВИЧ с наибольшей вероятностью попадет в цель, проникнет в него и впоследствии уничтожит те клетки, которые активно борются с инфекцией.
Во время репликации вируса интегрированная ДНК провируса транскрибируется в РНК. Полноразмерные геномные РНК (гРНК) могут быть упакованы в новые вирусные частицы в псевдодиплоидной форме. Селективность упаковки объясняется структурными свойствами димерного конформера гРНК. Димер гРНК характеризуется тандемным трехсторонним соединением внутри мономера гРНК, в котором шпильки SD и AUG , ответственные за сплайсинг и трансляцию соответственно, изолированы, а шпилька DIS (сигнал инициации димеризации) обнажена. Образование димера гРНК опосредовано «целующимся» взаимодействием между шпильками DIS мономеров гРНК. В то же время определенные остатки гуанозина в гРНК становятся доступными для связывания белка нуклеокапсида (NC), что приводит к последующей сборке вириона. [71] Сообщалось также, что лабильный димер гРНК достигает более стабильной конформации после связывания NC, при котором как DIS, так и области U5:AUG гРНК участвуют в обширном спаривании оснований. [72]
РНК также может быть подвергнута процессингу для получения зрелых матричных РНК (мРНК). В большинстве случаев этот процессинг включает сплайсинг РНК для получения мРНК, которые короче полноразмерного генома. Какая часть РНК удаляется во время сплайсинга РНК, определяет, какая из последовательностей, кодирующих белок ВИЧ, транслируется. [73]
Зрелые мРНК ВИЧ экспортируются из ядра в цитоплазму , где транслируются с образованием белков ВИЧ, включая Rev. По мере образования вновь полученного белка Rev он перемещается в ядро, где связывается с полноразмерными несплайсированными копиями вирусных РНК и позволяет им покинуть ядро. [74] Некоторые из этих полноразмерных РНК функционируют как мРНК, которые транслируются с образованием структурных белков Gag и Env. Белки Gag связываются с копиями генома РНК вируса, упаковывая их в новые вирусные частицы. [75] ВИЧ-1 и ВИЧ-2, по-видимому, по-разному упаковывают свою РНК. [76] [77] ВИЧ-1 связывается с любой подходящей РНК. [78] ВИЧ-2 будет преимущественно связываться с мРНК, которая использовалась для создания самого белка Gag. [79]
В каждой частице ВИЧ-1 заключены два генома РНК (см. Строение и геном ВИЧ ). При инфицировании и репликации, катализируемой обратной транскриптазой, может произойти рекомбинация между двумя геномами. [80] [81] Рекомбинация происходит, когда одноцепочечные геномы РНК с положительным смыслом подвергаются обратной транскрипции с образованием ДНК. Во время обратной транскрипции зарождающаяся ДНК может несколько раз переключаться между двумя копиями вирусной РНК. Эта форма рекомбинации известна как выбор копии. События рекомбинации могут происходить по всему геному. В каждом цикле репликации может происходить от двух до 20 событий рекомбинации на геном, и эти события могут быстро перемешивать генетическую информацию, которая передается от родительских геномов к потомству. [81]
Вирусная рекомбинация приводит к генетическим вариациям, которые, вероятно, способствуют развитию устойчивости к антиретровирусной терапии . [82] Рекомбинация в принципе может также способствовать преодолению иммунной защиты хозяина. Тем не менее, для реализации адаптивных преимуществ генетической изменчивости два вирусных генома, упакованные в отдельные инфицирующие вирусные частицы, должны произойти от отдельных родительских вирусов-предшественников различной генетической конституции. Неизвестно, как часто такая смешанная упаковка встречается в естественных условиях. [83]
Бонхеффер и др. [84] предположили, что переключение матрицы с помощью обратной транскриптазы действует как процесс репарации, устраняющий разрывы в геноме одноцепочечной РНК. Кроме того, Ху и Темин [80] предположили, что рекомбинация является адаптацией к восстановлению повреждений в геномах РНК. Переключение цепи (рекомбинация выбора копии) с помощью обратной транскриптазы может генерировать неповрежденную копию геномной ДНК из двух поврежденных копий генома одноцепочечной РНК. Этот взгляд на адаптивную пользу рекомбинации при ВИЧ может объяснить, почему каждая частица ВИЧ содержит два полных генома, а не один. Более того, точка зрения, согласно которой рекомбинация представляет собой процесс репарации, подразумевает, что выгода от репарации может проявляться в каждом цикле репликации и что эта выгода может быть реализована независимо от того, различаются ли два генома генетически. С точки зрения того, что рекомбинация при ВИЧ является процессом репарации, возникновение рекомбинационных вариаций должно быть следствием, но не причиной эволюции переключения шаблонов. [84]
Инфекция ВИЧ-1 вызывает хроническое воспаление и выработку активных форм кислорода . [85] Таким образом, геном ВИЧ может быть уязвим к окислительному повреждению , включая разрывы одноцепочечной РНК. Для ВИЧ, как и для вирусов в целом, успешное заражение зависит от преодоления защитных стратегий хозяина, которые часто включают выработку повреждающих геном активных форм кислорода. Таким образом, Мишо и др. [86] предположили, что рекомбинация вирусов — это адаптация к восстановлению повреждений генома, а рекомбинационные вариации — это побочный продукт, который может принести отдельную пользу.
Последний этап вирусного цикла — сборка новых вирионов ВИЧ-1 — начинается на плазматической мембране клетки-хозяина. Полипротеин Env (gp160) проходит через эндоплазматический ретикулум и транспортируется в аппарат Гольджи , где расщепляется фурином , в результате чего образуются два гликопротеина оболочки ВИЧ, gp41 и gp120 . [87] Они транспортируются к плазматической мембране клетки-хозяина, где gp41 закрепляет gp120 на мембране инфицированной клетки. Полипротеины Gag (p55) и Gag-Pol (p160) также связываются с внутренней поверхностью плазматической мембраны вместе с геномной РНК ВИЧ, когда формирующийся вирион начинает отпочковываться из клетки-хозяина. Почкующийся вирион все еще является незрелым, поскольку полипротеинам gag все еще необходимо расщепиться на настоящий матрикс, капсид и белки нуклеокапсида. Это расщепление опосредовано упакованной вирусной протеазой и может ингибироваться антиретровирусными препаратами класса ингибиторов протеазы . Затем различные структурные компоненты собираются, образуя зрелый вирион ВИЧ. [88] Только зрелые вирионы способны инфицировать другую клетку.

Классический процесс заражения клетки вирионом можно назвать «внеклеточным распространением», чтобы отличить его от недавно признанного процесса, называемого «от клетки к клетке». [89] При бесклеточном распространении (см. рисунок) вирусные частицы отпочковываются от инфицированной Т-клетки, попадают в кровь или внеклеточную жидкость , а затем после случайной встречи заражают другую Т-клетку. [89] ВИЧ также может распространяться путем прямой передачи от одной клетки к другой в процессе распространения от клетки к клетке, для которого описаны два пути. Во-первых, инфицированная Т-клетка может передавать вирус непосредственно Т-клетке-мишени через вирусологический синапс . [60] [90] Во-вторых, антигенпрезентирующая клетка (АПК), такая как макрофаг или дендритная клетка, может передавать ВИЧ Т-клеткам посредством процесса, который либо включает продуктивную инфекцию (в случае макрофагов), либо захват и перенос вирионов в трансе (в случае дендритных клеток). [91] Какой бы путь ни использовался, сообщается, что заражение путем переноса вируса от клетки к клетке гораздо более эффективно, чем бесклеточное распространение вируса. [92] Ряд факторов способствуют такой повышенной эффективности, в том числе поляризованное отпочкование вируса к месту межклеточного контакта, тесное прилегание клеток, что сводит к минимуму диффузию вирионов в жидкой фазе, а также кластеризацию рецепторов входа ВИЧ на целевую ячейку в сторону зоны контакта. [90] Считается, что распространение от клетки к клетке особенно важно в лимфоидных тканях , где CD4 + Т-клетки плотно упакованы и, вероятно, часто взаимодействуют. [89] Исследования прижизненной визуализации подтвердили концепцию вирусологического синапса ВИЧ in vivo . [93] Многие механизмы распространения ВИЧ способствуют непрерывной репликации вируса, несмотря на антиретровирусную терапию. [89] [94]

ВИЧ отличается от многих вирусов тем, что имеет очень высокую генетическую изменчивость . Это разнообразие является результатом его быстрого цикла репликации, при котором ежедневно генерируется около 10 10 вирионов, в сочетании с высокой частотой мутаций примерно 3 x 10 -5 на нуклеотидное основание за цикл репликации и рекомбиногенными свойствами обратной транскриптазы. [95] [96] [97]
Этот сложный сценарий приводит к образованию множества вариантов ВИЧ у одного инфицированного пациента в течение одного дня. [95] Эта изменчивость усугубляется, когда одна клетка одновременно инфицирована двумя или более разными штаммами ВИЧ. При одновременном заражении геном вирионов-потомков может состоять из цепей РНК двух разных штаммов. Этот гибридный вирион затем заражает новую клетку, где он подвергается репликации. Когда это произойдет, обратная транскриптаза, переключаясь между двумя разными матрицами РНК, будет генерировать вновь синтезированную ретровирусную последовательность ДНК , которая является рекомбинантной между двумя родительскими геномами. [95] Эта рекомбинация наиболее очевидна, когда она происходит между подтипами. [95]
Близкородственный вирус иммунодефицита обезьян (SIV) превратился во множество штаммов, классифицированных по естественным видам-хозяевам. Считается , что штаммы SIV африканской зеленой мартышки (SIVagm) и сажистого мангабея (SIVsmm) имеют долгую эволюционную историю со своими хозяевами. Эти хозяева адаптировались к присутствию вируса, [98] который присутствует в высоких концентрациях в крови хозяина, но вызывает лишь умеренный иммунный ответ, [99] не вызывает развития обезьяньего СПИДа, [100] и не не подвергаться обширным мутациям и рекомбинациям, типичным для ВИЧ-инфекции у человека. [101]
Напротив, когда эти штаммы заражают виды, которые не адаптировались к SIV («гетерологичные» или подобные хозяева, такие как макаки-резусы или яванские макаки ), у животных развивается СПИД, и вирус генерирует генетическое разнообразие, подобное тому, что наблюдается при ВИЧ-инфекции человека. [102] SIV шимпанзе (SIVcpz), ближайший генетический родственник ВИЧ-1, связан с повышенной смертностью и СПИД-подобными симптомами у его естественного хозяина. [103] SIVcpz, судя по всему, сравнительно недавно передался популяциям шимпанзе и человека, поэтому их хозяева еще не адаптировались к вирусу. [98] Этот вирус также утратил функцию гена nef , который присутствует у большинства SIV. Для непатогенных вариантов SIV nef подавляет активацию Т-клеток через маркер CD3 . Функция Nef при непатогенных формах ВИО заключается в подавлении экспрессии воспалительных цитокинов MHC-1 и сигналов, влияющих на транспорт Т-клеток. При ВИЧ-1 и SIVcpz nef не ингибирует активацию Т-клеток и утратил эту функцию. Без этой функции более вероятно истощение Т-клеток, что приводит к иммунодефициту. [103] [104]
На основе различий в области оболочки ( env ) ВИЧ-1 были идентифицированы три группы: M, N и O. [105] Группа M является наиболее распространенной и подразделяется на восемь подтипов (или клад ), основанных на по всему геному, которые географически различны. [106] Наиболее распространенными являются подтипы B (в основном в Северной Америке и Европе), A и D (в основном в Африке) и C (в основном в Африке и Азии); эти подтипы образуют ветви филогенетического дерева , представляющие линию М-группы ВИЧ-1. Коинфекция различными подтипами приводит к появлению циркулирующих рекомбинантных форм (CRF). В 2000 году, последнем году, когда был проведен анализ глобальной распространенности подтипа, 47,2% инфекций во всем мире были связаны с подтипом C, 26,7% были с подтипом A/CRF02_AG, 12,3% были с подтипом B, 5,3% были с подтипом D, 3,2% имели CRF_AE, а остальные 5,3% состояли из других подтипов и CRF. [107] Большинство исследований ВИЧ-1 сосредоточено на подтипе B; лишь немногие лаборатории специализируются на других подтипах. [108] Существование четвертой группы, «P», было высказано на основе вируса, выделенного в 2009 году. [109] [110] Штамм, очевидно, произошел от гориллы SIV (SIVgor), впервые выделенной от западных равнинных горилл в 2006. [109]
Ближайшим родственником ВИЧ-2 является SIVsm, штамм SIV, обнаруженный у сажистых мангабей. Поскольку ВИЧ-1 происходит от SIVcpz, а ВИЧ-2 — от SIVsm, генетическая последовательность ВИЧ-2 лишь частично гомологична ВИЧ-1 и более похожа на последовательность SIVsm. [111] [112]
Многие ВИЧ-положительные люди не подозревают, что они инфицированы этим вирусом. [113] Например, в 2001 году менее 1% сексуально активного городского населения в Африке прошли тестирование, а среди сельского населения эта доля еще ниже. [113] Более того, в 2001 году только 0,5% беременных женщин , посещавших городские медицинские учреждения, были консультированы, протестированы или получили результаты анализов. [113] Опять же, в сельских медицинских учреждениях эта доля еще ниже. [113] Поскольку доноры могут не знать о своей инфекции, донорская кровь и продукты крови, используемые в медицине и медицинских исследованиях, регулярно проверяются на ВИЧ. [114]
Тестирование на ВИЧ-1 первоначально проводится с использованием иммуноферментного анализа (ИФА) для выявления антител к ВИЧ-1. Образцы с нереактивным результатом первоначального ИФА считаются ВИЧ-отрицательными, за исключением случаев, когда произошел новый контакт с инфицированным партнером или партнером с неизвестным ВИЧ-статусом. Образцы с реактивным результатом ИФА исследуются повторно в двух экземплярах. [115] Если результат любого повторного теста является реактивным, образец считается повторно реактивным и подвергается подтверждающему тестированию с более специфическим дополнительным тестом (например, полимеразной цепной реакцией (ПЦР), вестерн-блоттингом или, реже, иммунофлуоресценцией) . анализ (ИФА)). ВИЧ-положительными и указывающими на ВИЧ-инфекцию считаются только те образцы, которые повторно реагируют с помощью ELISA и являются положительными с помощью IFA или ПЦР или дают положительный результат с помощью вестерн-блоттинга. Образцы, которые повторно реагируют на ИФА, иногда дают неопределенный результат вестерн-блоттинга, который может быть либо неполным ответом антител на ВИЧ у инфицированного человека, либо неспецифическими реакциями у неинфицированного человека. [116]
Хотя ИФА можно использовать для подтверждения инфекции в этих неоднозначных случаях, этот метод широко не используется. Как правило, второй образец следует собрать более чем через месяц и повторно протестировать у лиц с неопределенными результатами вестерн-блоттинга. Хотя тестирование нуклеиновых кислот (например, метод амплификации вирусной РНК или провирусной ДНК) доступно гораздо реже, оно также может помочь в диагностике в определенных ситуациях. [115] Кроме того, несколько протестированных образцов могут дать неубедительные результаты из-за небольшого количества образцов. В таких ситуациях собирается второй образец и проверяется на ВИЧ-инфекцию.
Современное тестирование на ВИЧ является чрезвычайно точным, если принять во внимание период окна . Один скрининговый тест дает правильный результат более чем в 99% случаев. [118] Вероятность ложноположительного результата при стандартном двухэтапном протоколе тестирования оценивается примерно в 1 на 250 000 в группе низкого риска. [119] Тестирование после заражения рекомендуется проводить немедленно, а затем через шесть недель, три месяца и шесть месяцев. [120]
Последние рекомендации Центров по контролю и профилактике заболеваний США (CDC) показывают, что тестирование на ВИЧ должно начинаться с комбинированного иммунологического анализа на антитела ВИЧ-1 и ВИЧ-2 и антиген p24 . Отрицательный результат исключает заражение ВИЧ, а положительный результат должен сопровождаться иммуноанализом на дифференцировку антител ВИЧ-1/2, чтобы определить, какие антитела присутствуют. Это приводит к четырем возможным сценариям:
Исследования ВИЧ/СПИДа включают все медицинские исследования , направленные на профилактику, лечение или излечение ВИЧ/СПИДа , а также фундаментальные исследования природы ВИЧ как инфекционного агента и СПИДа как заболевания, вызываемого ВИЧ.
Многие правительства и исследовательские институты участвуют в исследованиях по ВИЧ/СПИДу. Эти исследования включают в себя вмешательства в области поведенческого здоровья , такие как исследования в области полового воспитания , и разработку лекарств , таких как исследования микробицидов для лечения заболеваний , передающихся половым путем, вакцин против ВИЧ и антиретровирусных препаратов . [122] Другие области медицинских исследований включают темы доконтактной профилактики , постконтактной профилактики , обрезания и эффектов ускоренного старения .
Лечение ВИЧ/СПИДа обычно включает использование нескольких антиретровирусных препаратов . Во многих частях мира ВИЧ стал хроническим заболеванием, при котором прогрессирование до СПИДа становится все более редким.
Латентный период ВИЧ и, как следствие, вирусный резервуар в CD4 + Т-клетках, дендритных клетках, а также макрофагах являются основным барьером на пути к уничтожению вируса. [19] [123]
Несмотря на высокую вирулентность ВИЧ, передача ВИЧ не происходит половым путем, если ВИЧ-положительный человек имеет постоянно неопределяемую вирусную нагрузку (<50 копий/мл) вследствие антиретровирусного лечения. Впервые об этом заявила Федеральная комиссия Швейцарии по СПИДу/ВИЧ в 2008 году в Заявлении Швейцарии , хотя в то время это заявление вызывало споры. [124] [125] Однако после многочисленных исследований стало ясно, что вероятность передачи ВИЧ половым путем фактически равна нулю, если у ВИЧ-положительного человека постоянно неопределяемая вирусная нагрузка; это известно как U=U, «Необнаружимый = Непередаваемый», также формулируется как «невозможно передать это дальше». [126] [127] Исследования, демонстрирующие U=U: Противоположности притягиваются, [128] ПАРТНЕР 1, [129] ПАРТНЕР 2, [5] [130] (для пар мужчина-мужчина) [131] и HPTN052 [132] (для гетеросексуальных пар), когда «партнер, живущий с ВИЧ, имел стойко подавленную вирусную нагрузку». [131] В эти исследования были включены пары, в которых один партнер был ВИЧ-положительным, а другой ВИЧ-отрицательным, и прошли регулярное тестирование на ВИЧ. Всего в четырех исследованиях приняли участие 4097 пар на четырех континентах и было зарегистрировано 151 880 половых актов без презервативов; не было ни одного филогенетически связанного случая передачи ВИЧ, когда положительный партнер имел неопределяемую вирусную нагрузку. [133] После этого заявление о консенсусе «Н=Н», призывающее к использованию «нулевого риска», было подписано сотнями людей и организаций, включая Центр по контролю и профилактике заболеваний США , Британскую ассоциацию по ВИЧ и медицинский журнал «Ланцет ». [134] Важность окончательных результатов исследования PARTNER 2 была описана медицинским директором Фонда Терренса Хиггинса как «невозможно переоценить», а ведущий автор Элисон Роджер заявила, что сообщение о том, что «неопределяемая вирусная нагрузка делает ВИЧ непередаваемым». ...может помочь положить конец пандемии ВИЧ, предотвращая передачу ВИЧ. [135] Авторы резюмировали свои выводы в журнале The Lancet следующим образом: [5]
Наши результаты предоставляют тот же уровень доказательств в отношении подавления вируса и риска передачи ВИЧ для геев, что и ранее полученный для гетеросексуальных пар, и позволяют предположить, что риск передачи ВИЧ в однополых парах посредством секса без презервативов, когда вирусная нагрузка ВИЧ подавлена, фактически равен нулю. Наши результаты подтверждают идею кампании «Н=Н» (необнаружимое = непередаваемое), а также преимущества раннего тестирования и лечения ВИЧ. [5]
Этот результат согласуется с выводом, представленным Энтони С. Фаучи , директором Национального института аллергии и инфекционных заболеваний Национального института здравоохранения США , и его командой, опубликовавшим точку зрения, опубликованную в Журнале Американской медицинской ассоциации , о том, что U=U – эффективный метод профилактики ВИЧ при сохранении неопределяемой вирусной нагрузки. [6] [131]
Реактивация генитального герпеса (ВПГ-2) у инфицированных вирусом сопровождается увеличением количества CD4+ Т-клеток, обогащенных CCR-5, а также воспалительных дендритных клеток в подслизистой оболочке кожи половых органов. Тропизм ВИЧ к CCR-5-положительным клеткам объясняет двух-трехкратное увеличение заболеваемости ВИЧ среди лиц с генитальным герпесом. Ежедневный прием противовирусных препаратов (например, ацикловира) не уменьшает субклиническое постреактивационное воспаление и, следовательно, не снижает риск заражения ВИЧ. [136] [137]
Первая новость о «новой экзотической болезни» появилась 18 мая 1981 года в гей-газете New York Native . [138]
Впервые СПИД был клинически обнаружен в 1981 году в США. [139] Первые случаи представляли собой группу потребителей инъекционных наркотиков и мужчин-геев без известной причины нарушения иммунитета, у которых проявлялись симптомы пневмоцистной пневмонии (PCP или PJP, последний термин означает, что возбудитель теперь называется Pneumocystis jirovecii ), а редкая оппортунистическая инфекция, которая, как известно, возникает у людей с очень ослабленной иммунной системой. [140] Вскоре после этого исследователи из Медицинской школы Нью-Йоркского университета изучали у мужчин-геев развитие ранее редкого рака кожи, называемого саркомой Капоши (СК). [141] [142] Появилось гораздо больше случаев PJP и KS, что предупредило Центры по контролю и профилактике заболеваний США (CDC), и для мониторинга вспышки была сформирована целевая группа CDC. [143] Считается, что самый ранний ретроспективно описанный случай СПИДа произошел в Норвегии, начиная с 1966 года. [144]
Вначале у CDC не было официального названия заболевания, часто называя его в виде связанных с ним заболеваний, например, лимфаденопатии — заболевания, в честь которого первооткрыватели ВИЧ первоначально назвали вирус. [145] [146] Они также использовали « Саркому Капоши и оппортунистические инфекции» — название, под которым в 1981 году была создана целевая группа. [147] В широкой прессе термин GRID , который обозначал иммунодефицит, связанный с геями , было придумано. [148] Центры по контролю и профилактике заболеваний (CDC), в поисках названия и изучая инфицированные сообщества, придумали «болезнь 4H», поскольку она, казалось, выделяла гомосексуалистов, потребителей героина, больных гемофилией и гаитян . [149] [150] Однако после того, как выяснилось, что СПИД не был изолирован только от гей-сообщества , [147] стало понятно, что термин GRID вводит в заблуждение, и СПИД был представлен на встрече в июле 1982 года. [151] К сентябрю 1982 года CDC начал использовать название СПИД. [152]
В 1983 году две отдельные исследовательские группы во главе с американцем Робертом Галло и французскими исследователями Франсуазой Барре-Синусси и Люком Монтанье независимо друг от друга заявили, что новый ретровирус мог заражать больных СПИДом, и опубликовали свои выводы в том же выпуске журнала Science . [153] [146] [154] Галло утверждал, что вирус, который его группа выделила от человека, больного СПИДом, был поразительно похож по форме на другие человеческие Т-лимфотропные вирусы (HTLV), которые его группа изолировала первыми. В 1987 году Галло признал, что вирус, который, как он утверждал, обнаружил в 1984 году, на самом деле был вирусом, присланным ему из Франции годом ранее. [155] Группа Галло назвала свой недавно выделенный вирус HTLV-III. Группа Монтанье выделила вирус от пациента, у которого наблюдались отек лимфатических узлов шеи и физическая слабость — два классических симптома первичной ВИЧ-инфекции. Вопреки отчету группы Галло, Монтанье и его коллеги показали, что основные белки этого вируса иммунологически отличаются от белков HTLV-I. Группа Монтанье назвала свой изолированный вирус вирусом, ассоциированным с лимфаденопатией (LAV). [143] Поскольку эти два вируса оказались одинаковыми, в 1986 году LAV и HTLV-III были переименованы в ВИЧ. [156]
Другой группой, работавшей одновременно с группами Монтанье и Галло, была группа Джея А. Леви из Калифорнийского университета в Сан-Франциско . Он независимо открыл вирус СПИДа в 1983 году и назвал его СПИД-ассоциированным ретровирусом (АРВ). [157] Этот вирус сильно отличался от вируса, о котором сообщили группы Монтанье и Галло. Штаммы АРВ-препаратов впервые показали гетерогенность изолятов ВИЧ, и некоторые из них остаются классическими примерами вируса СПИДа, обнаруженного в Соединенных Штатах. [158]
Считается, что и ВИЧ-1, и ВИЧ-2 возникли у приматов в западно-центральной Африке и, как полагают, передались человеку (процесс, известный как зооноз ) в начале 20 века. [159] [160]
ВИЧ-1, по-видимому, возник в южном Камеруне в результате эволюции SIVcpz, вируса иммунодефицита обезьян (SIV), который поражает диких шимпанзе (ВИЧ-1 происходит от SIVcpz, эндемичного для подвида шимпанзе Pan troglodytes troglodytes ). [161] [162] Ближайшим родственником ВИЧ-2 является SIVsmm, вирус сажистого мангабея ( Cercocebus atys atys ), обезьяны Старого Света , обитающей в прибрежной части Западной Африки (от южного Сенегала до западного Кот-д'Ивуара ). [21] Обезьяны Нового Света , такие как совиные обезьяны, устойчивы к инфекции ВИЧ-1, возможно, из-за геномного слияния двух генов вирусной устойчивости. [163]
Считается, что ВИЧ-1 преодолевал видовой барьер как минимум трижды, давая начало трем группам вируса: M, N и O. [164]

Есть свидетельства того, что люди, которые участвуют в добыче мяса диких животных в качестве охотников или продавцов мяса диких животных, обычно заражаются ВИО. [165] Однако SIV — слабый вирус, и иммунная система человека обычно подавляет его в течение нескольких недель после заражения. Считается, что необходимо несколько передач вируса от человека к человеку в быстрой последовательности, чтобы дать ему достаточно времени для мутации в ВИЧ. [166] Кроме того, из-за относительно низкой скорости передачи от человека к человеку, он может распространяться среди населения только при наличии одного или нескольких каналов передачи высокого риска, которые, как полагают, отсутствовали в Африке до 20 век.
Конкретные предлагаемые каналы передачи высокого риска, позволяющие вирусу адаптироваться к человеку и распространяться по всему обществу, зависят от предполагаемых сроков скрещивания животного с человеком. Генетические исследования вируса предполагают, что самый последний общий предок группы ВИЧ-1 M датируется ок . 1910 год . [167] Сторонники этой датировки связывают эпидемию ВИЧ с появлением колониализма и ростом крупных колониальных африканских городов, что привело к социальным изменениям, включая различные модели сексуальных контактов (особенно множественные, одновременные партнерства), распространение проституции и сопутствующая высокая частота генитальных язвенных заболеваний (таких как сифилис ) в зарождающихся колониальных городах. [168] Хотя уровень передачи ВИЧ во время вагинального полового акта обычно невелик, он многократно увеличивается, если у одного из партнеров есть инфекция, передающаяся половым путем , приводящая к образованию язв на половых органах. Колониальные города начала 1900-х годов отличались высокой распространенностью проституции и генитальных язв до такой степени, что по состоянию на 1928 год до 45% жительниц восточного Леопольдвилля (ныне Киншаса) считались проститутками, а по состоянию на 1933 год - около 15%. всех жителей одного и того же города были заражены одной из форм сифилиса . [168]
Самый ранний, хорошо документированный случай заражения ВИЧ у человека датируется 1959 годом в Бельгийском Конго . [169] Вирус мог присутствовать в Соединенных Штатах еще в середине-конце 1960-х годов, когда у шестнадцатилетнего мужчины по имени Роберт Рэйфорд появились симптомы в 1966 году, и он умер в 1969 году. [170]
Альтернативная и, вероятно, дополняющая гипотеза указывает на широкое использование небезопасной медицинской практики в Африке в годы после Второй мировой войны, например, нестерильное повторное использование одноразовых шприцев во время массовой вакцинации, использования антибиотиков и кампаний по лечению малярии. [166] [171] [172] Исследования по времени появления самого недавнего общего предка групп M и O ВИЧ-1, а также групп A и B ВИЧ-2, показывают, что SIV привел к появлению трансмиссивных линий ВИЧ во всем мире. двадцатый век. [173] Рассредоточенное время передачи ВИЧ людям означает, что для объяснения межвидовой передачи ВИЧ не требуется какого-либо единого внешнего фактора. Это наблюдение согласуется с двумя преобладающими взглядами на происхождение эпидемии ВИЧ, а именно с передачей ВИО человеку во время забоя или разделки инфицированных приматов, а также с колониальной экспансией африканских городов к югу от Сахары. [173]
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ){{cite web}}: CS1 maint: неподходящий URL ( ссылка )Директор NIAID Энтони С. Фаучи, доктор медицинских наук, и его коллеги обобщают результаты крупных клинических испытаний и когортных исследований, подтверждающих U=U. Знаменательное клиническое исследование HPTN 052, финансируемое НИЗ, показало, что среди ВИЧ-сероразличных гетеросексуальных пар не наблюдалось связанной передачи ВИЧ, когда у партнера, живущего с ВИЧ, была устойчиво подавленная вирусная нагрузка. Впоследствии исследования PARTNER и Opposites Attract подтвердили эти результаты и распространили их на пары мужчина-мужчина. ... Успех Н=Н как метода профилактики ВИЧ зависит от достижения и поддержания неопределяемой вирусной нагрузки путем ежедневного приема АРТ в соответствии с предписаниями.
Доктор Маркс считает, что решающим событием стало появление в Африке миллионов недорогих шприцев массового производства в 1950-х годах. ... подозреваю, что виноват рост колониальных городов. До 1910 года ни в одном городе Центральной Африки не проживало более 10 000 человек. Но городская миграция выросла, увеличивая сексуальные контакты и приводя к появлению кварталов красных фонарей.