
Ковалентная связь — это химическая связь , которая включает в себя совместное использование электронов для образования электронных пар между атомами . Эти электронные пары известны как общие пары или связывающие пары . Стабильный баланс сил притяжения и отталкивания между атомами, когда они совместно используют электроны , известен как ковалентная связь. [1] Для многих молекул совместное использование электронов позволяет каждому атому достичь эквивалента полной валентной оболочки, соответствующей стабильной электронной конфигурации. В органической химии ковалентная связь встречается гораздо чаще, чем ионная связь .
Ковалентная связь также включает в себя множество видов взаимодействий, включая σ-связь , π-связь , связь металл-металл , агостические взаимодействия , изогнутые связи , трехцентровые двухэлектронные связи и трехцентровые четырехэлектронные связи . [2] [3] Термин ковалентная связь появился в 1939 году. [4] Префикс со- означает совместно, ассоциированный в действии, партнерство в меньшей степени и т. д.; таким образом, «ковалентная связь», по сути, означает, что атомы разделяют « валентность », как это обсуждается в теории валентных связей .
В молекуле H
2, атомы водорода делят два электрона через ковалентную связь. [5] Ковалентность наибольшая между атомами с одинаковой электроотрицательностью . Таким образом, ковалентная связь не обязательно требует, чтобы два атома были из одних и тех же элементов, а только чтобы они имели сопоставимую электроотрицательность. Ковалентная связь, которая влечет за собой совместное использование электронов более чем двумя атомами, называется делокализованной .
Термин ковалентность в отношении связи впервые был использован в 1919 году Ирвингом Ленгмюром в статье «Расположение электронов в атомах и молекулах» в журнале Американского химического общества . Ленгмюр писал, что «мы будем обозначать термином ковалентность число пар электронов, которые данный атом делит со своими соседями». [6]
Идея ковалентной связи может быть прослежена за несколько лет до 1919 года до Гилберта Н. Льюиса , который в 1916 году описал совместное использование электронных пар между атомами [7] (а в 1926 году он также ввел термин « фотон » для наименьшей единицы лучистой энергии). Он ввел обозначение Льюиса или обозначение электронной точки или структуру точек Льюиса , в которой валентные электроны (те, что находятся во внешней оболочке) представлены в виде точек вокруг атомных символов. Пары электронов, расположенные между атомами, представляют ковалентные связи. Несколько пар представляют несколько связей, таких как двойные связи и тройные связи . Альтернативная форма представления, не показанная здесь, имеет пары электронов, образующие связи, представленные в виде сплошных линий. [8]
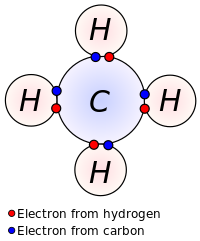
Льюис предположил, что атом образует достаточно ковалентных связей, чтобы сформировать полную (или закрытую) внешнюю электронную оболочку. На диаграмме метана, показанной здесь, атом углерода имеет валентность четыре и, следовательно, окружен восемью электронами ( правило октета ), четырьмя от самого углерода и четырьмя от связанных с ним водородов. Каждый водород имеет валентность один и окружен двумя электронами (правило дуэта) – его собственным одним электроном плюс один от углерода. Количество электронов соответствует полным оболочкам в квантовой теории атома; внешняя оболочка атома углерода – это оболочка n = 2, которая может содержать восемь электронов, тогда как внешняя (и единственная) оболочка атома водорода – это оболочка n = 1, которая может содержать только два. [9]
В то время как идея общих электронных пар обеспечивает эффективную качественную картину ковалентной связи, квантовая механика необходима для понимания природы этих связей и предсказания структур и свойств простых молекул. Уолтеру Гайтлеру и Фрицу Лондону приписывают первое успешное квантово-механическое объяснение химической связи ( молекулярного водорода ) в 1927 году. [10] Их работа основывалась на модели валентной связи, которая предполагает, что химическая связь образуется при хорошем перекрытии между атомными орбиталями участвующих атомов.
Атомные орбитали (за исключением s-орбиталей) обладают специфическими направленными свойствами, приводящими к различным типам ковалентных связей. Сигма-связи (σ) являются самыми сильными ковалентными связями и возникают из-за лобового перекрытия орбиталей на двух разных атомах. Одинарная связь обычно является σ-связью. Пи-связи (π) слабее и возникают из-за бокового перекрытия между p- (или d)-орбиталями. Двойная связь между двумя данными атомами состоит из одной σ- и одной π-связи, а тройная связь — из одной σ- и двух π-связей. [8]
На ковалентные связи также влияет электроотрицательность соединенных атомов, которая определяет химическую полярность связи. Два атома с одинаковой электроотрицательностью образуют неполярные ковалентные связи, такие как H–H. Неравные отношения создают полярную ковалентную связь, такую как H−Cl. Однако полярность также требует геометрической асимметрии , иначе диполи могут нейтрализоваться, что приведет к неполярной молекуле. [8]
Существует несколько типов структур для ковалентных веществ, включая отдельные молекулы, молекулярные структуры , макромолекулярные структуры и гигантские ковалентные структуры. Отдельные молекулы имеют прочные связи, которые удерживают атомы вместе, но, как правило, между молекулами существуют незначительные силы притяжения. Такие ковалентные вещества обычно являются газами, например, HCl , SO2 , CO2 и CH4 . В молекулярных структурах существуют слабые силы притяжения. Такие ковалентные вещества являются жидкостями с низкой температурой кипения (например, этанол ) и твердыми веществами с низкой температурой плавления (например, йод и твердый CO2 ) . Макромолекулярные структуры имеют большое количество атомов, связанных ковалентными связями в цепях, включая синтетические полимеры, такие как полиэтилен и нейлон , и биополимеры, такие как белки и крахмал . Сетчатые ковалентные структуры (или гигантские ковалентные структуры) содержат большое количество атомов, связанных в листы (например, графит ), или трехмерные структуры (например, алмаз и кварц ). Эти вещества имеют высокие температуры плавления и кипения, часто хрупкие и, как правило, имеют высокое электрическое сопротивление . Элементы, которые имеют высокую электроотрицательность и способность образовывать связи из трех или четырех электронных пар, часто образуют такие большие макромолекулярные структуры. [11]

Связи с одним или тремя электронами можно найти в радикальных видах, которые имеют нечетное число электронов. Простейший пример 1-электронной связи можно найти в дигидрогенном катионе , H+
2. Одноэлектронные связи часто имеют около половины энергии связи двухэлектронной связи и поэтому называются «полусвязями». Однако есть исключения: в случае дилития связь на самом деле сильнее для одноэлектронного Li+
2чем для 2-электронного Li 2. Это исключение можно объяснить с точки зрения гибридизации и эффектов внутренней оболочки. [12]
Простейший пример трехэлектронной связи можно найти в катионе димера гелия , He+
2. Она считается «полусвязью», поскольку состоит только из одного общего электрона (а не из двух); [13] в терминах молекулярных орбиталей третий электрон находится на антисвязывающей орбитали, которая отменяет половину связи, образованной двумя другими электронами. Другим примером молекулы, содержащей 3-электронную связь в дополнение к двум 2-электронным связям, является оксид азота , NO. Молекула кислорода, O 2, также может рассматриваться как имеющая две 3-электронные связи и одну 2-электронную связь, что объясняет ее парамагнетизм и формальный порядок связи 2. [14] Диоксид хлора и его более тяжелые аналоги диоксид брома и диоксид йода также содержат трехэлектронные связи.
Молекулы с нечетными электронными связями обычно очень реактивны. Эти типы связей стабильны только между атомами с одинаковой электроотрицательностью. [14]
Существуют ситуации, когда одной структуры Льюиса недостаточно для объяснения электронной конфигурации в молекуле и ее экспериментально определенных свойств, поэтому необходима суперпозиция структур. Те же два атома в таких молекулах могут быть связаны по-разному в разных структурах Льюиса (одинарная связь в одной, двойная связь в другой или даже вообще никакая), что приводит к нецелочисленному порядку связи . Нитрат- ион является одним из таких примеров с тремя эквивалентными структурами. Связь между азотом и каждым кислородом является двойной связью в одной структуре и одинарной связью в двух других, так что средний порядок связи для каждого взаимодействия N–O равен 2 + 1 + 1/3 = 4/3 . [8]
В органической химии , когда молекула с плоским кольцом подчиняется правилу Хюккеля , где число π-электронов соответствует формуле 4 n + 2 (где n — целое число), она достигает дополнительной стабильности и симметрии. В бензоле , прототипичном ароматическом соединении, имеется 6 π-связывающих электронов ( n = 1, 4 n + 2 = 6). Они занимают три делокализованные π-молекулярные орбитали ( теория молекулярных орбиталей ) или образуют сопряженные π-связи в двух резонансных структурах, которые линейно объединяются ( теория валентных связей ), создавая правильный шестиугольник, демонстрирующий большую стабилизацию, чем гипотетический 1,3,5-циклогексатриен. [9]
В случае гетероциклических ароматических соединений и замещенных бензолов различия в электроотрицательности между различными частями кольца могут доминировать над химическим поведением связей ароматического кольца, которые в противном случае эквивалентны. [9]
Некоторые молекулы, такие как дифторид ксенона и гексафторид серы, имеют более высокие координационные числа, чем это было бы возможно из-за строго ковалентной связи в соответствии с правилом октета . Это объясняется моделью трехцентровой четырехэлектронной связи («3c–4e»), которая интерпретирует молекулярную волновую функцию в терминах несвязывающих высших занятых молекулярных орбиталей в теории молекулярных орбиталей и резонанса сигма-связей в теории валентных связей . [15]
В трехцентровых двухэлектронных связях («3c–2e») три атома делят два электрона в связи. Этот тип связи встречается в гидридах бора, таких как диборан (B 2 H 6 ), которые часто описываются как электронно-дефицитные, поскольку в них недостаточно валентных электронов для образования локализованных (2-центровых 2-электронных) связей, соединяющих все атомы. Однако более современное описание с использованием связей 3c–2e действительно обеспечивает достаточное количество связывающих орбиталей для соединения всех атомов, так что молекулы вместо этого можно классифицировать как электронно-точные.
Каждая такая связь (2 на молекулу в диборане) содержит пару электронов, которые соединяют атомы бора друг с другом в форме банана, с протоном (ядром атома водорода) в середине связи, разделяющим электроны с обоими атомами бора. В некоторых кластерных соединениях также постулируются так называемые четырехцентровые двухэлектронные связи . [16]
После развития квантовой механики были предложены две основные теории для квантового описания химической связи: теория валентных связей (ВС) и теория молекулярных орбиталей (МО) . Более позднее квантовое описание [17] дается в терминах атомных вкладов в электронную плотность состояний.
Две теории представляют два способа построения электронной конфигурации молекулы. [18] Для теории валентных связей атомные гибридные орбитали сначала заполняются электронами, чтобы создать полностью связанную валентную конфигурацию, а затем выполняется линейная комбинация способствующих структур ( резонанс ), если их несколько. Напротив, для теории молекулярных орбиталей сначала выполняется линейная комбинация атомных орбиталей , а затем выполняется заполнение полученных молекулярных орбиталей электронами. [8]
Эти два подхода считаются взаимодополняющими, и каждый из них обеспечивает собственное понимание проблемы химической связи. Поскольку теория валентных связей строит молекулярную волновую функцию из локализованных связей, она больше подходит для расчета энергий связей и понимания механизмов реакции . Поскольку теория молекулярных орбиталей строит молекулярную волновую функцию из делокализованных орбиталей, она больше подходит для расчета энергий ионизации и понимания спектральных полос поглощения . [19]
На качественном уровне обе теории содержат неверные предсказания. Простая (Гайтлера–Лондона) теория валентных связей правильно предсказывает диссоциацию гомоядерных двухатомных молекул на отдельные атомы, в то время как простая (Хартри–Фока) теория молекулярных орбиталей неправильно предсказывает диссоциацию на смесь атомов и ионов. С другой стороны, простая теория молекулярных орбиталей правильно предсказывает правило ароматичности Хюккеля , в то время как простая теория валентных связей неправильно предсказывает, что циклобутадиен имеет большую резонансную энергию, чем бензол. [20]
Хотя волновые функции, полученные обеими теориями на качественном уровне, не согласуются и не соответствуют энергии стабилизации по эксперименту, их можно скорректировать с помощью взаимодействия конфигураций . [18] Это делается путем объединения ковалентной функции валентной связи с функциями, описывающими все возможные ионные структуры, или путем объединения функции основного состояния молекулярной орбитали с функциями, описывающими все возможные возбужденные состояния с использованием незанятых орбиталей. Затем можно увидеть, что простой молекулярный орбитальный подход переоценивает вес ионных структур, в то время как простой валентный подход пренебрегает ими. Это также можно описать как утверждение, что простой молекулярный орбитальный подход пренебрегает электронной корреляцией , в то время как простой валентный подход переоценивает ее. [18]
Современные вычисления в квантовой химии обычно начинаются с (но в конечном итоге выходят далеко за рамки) подхода молекулярных орбиталей, а не валентных связей, не из-за какого-либо внутреннего превосходства первого, а скорее потому, что подход МО легче адаптировать к численным расчетам. Молекулярные орбитали ортогональны, что значительно увеличивает осуществимость и скорость компьютерных вычислений по сравнению с неортогональными орбиталями валентных связей.
Оценка ковалентности связи зависит от базисного набора для приближенных квантово-химических методов, таких как COOP (популяция перекрытия кристаллических орбиталей), [21] COHP (популяция гамильтоновской кристаллической орбитали), [22] и BCOOP (популяция перекрытия сбалансированных кристаллических орбиталей). [23] Чтобы преодолеть эту проблему, можно предложить альтернативную формулировку ковалентности связи следующим образом.
Центр масс атомной орбитали с квантовыми числами для атома A определяется как
где - вклад атомной орбитали атома А в общую электронную плотность состояний твердого тела
где внешняя сумма пробегает все атомы A элементарной ячейки. Энергетическое окно выбирается таким образом, чтобы оно охватывало все соответствующие полосы, участвующие в связи. Если диапазон для выбора неясен, его можно определить на практике, исследуя молекулярные орбитали, которые описывают электронную плотность вместе с рассматриваемой связью.
Относительное положение центра масс уровней атома A относительно центра масс уровней атома B задается как
где вклады магнитных и спиновых квантовых чисел суммируются. Согласно этому определению, относительное положение уровней A по отношению к уровням B равно
где для простоты можно опустить зависимость от главного квантового числа в обозначениях, относящихся к
В этом формализме, чем больше значение , тем выше перекрытие выбранных атомных полос, и, таким образом, электронная плотность, описываемая этими орбиталями, дает более ковалентную связь A−B . Величина обозначается как ковалентность связи A−B , которая указывается в тех же единицах энергии .
Аналогичный эффект ковалентной связи, как полагают, происходит в некоторых ядерных системах, с той разницей, что общие фермионы являются кварками, а не электронами. [24] Высокоэнергетическое сечение рассеяния протонов на протонах указывает на то, что обмен кварками либо u, либо d-кварков является доминирующим процессом ядерной силы на коротком расстоянии. В частности, он доминирует над взаимодействием Юкавы , где происходит обмен мезонами . [25] Поэтому ожидается, что ковалентная связь путем обмена кварками будет доминирующим механизмом ядерного связывания на небольшом расстоянии, когда связанные адроны имеют общие ковалентные кварки. [26]