Метастазирование — это распространение патогенного агента из первичного или первичного участка в другой или вторичный участок в организме хозяина; [1] этот термин обычно используется, когда речь идет о метастазах раковой опухоли. [2] Таким образом, новые патологические участки называются метастазами ( метастазы ). [3] [4] Его обычно отличают от инвазии рака , которая представляет собой прямое распространение и проникновение раковых клеток в соседние ткани. [5]
Рак возникает после того, как клетки генетически изменены для быстрого и неограниченного размножения. Эта неконтролируемая пролиферация путем митоза производит первичную гетерогенную опухоль . Клетки, составляющие опухоль, в конечном итоге подвергаются метаплазии , за которой следует дисплазия, а затем анаплазия , что приводит к злокачественному фенотипу. Эта злокачественность допускает вторжение в кровообращение, за которым следует вторжение во второй участок для возникновения опухоли .
Некоторые раковые клетки, известные как циркулирующие опухолевые клетки (ЦОК), способны проникать через стенки лимфатических или кровеносных сосудов и циркулировать через кровоток в другие места и ткани организма. [6] Этот процесс, известный соответственно как лимфатическое или гематогенное распространение, позволяет перемещаться не только отдельным клеткам, но и группам клеток, или кластерам ЦОК . Данные свидетельствуют о том, что кластеры ЦОК могут сохранять свою многоклеточную конфигурацию на протяжении всего метастазирования, что повышает их способность образовывать вторичные опухоли. [7] Эта точка зрения согласуется с гипотезой исхода рака , которая утверждает, что поддержание этой кластерной структуры способствует более высокому метастатическому потенциалу. Метастазирование является одним из признаков рака , отличающим его от доброкачественных опухолей . [8] Большинство видов рака могут метастазировать, хотя и в разной степени. Например, базальноклеточная карцинома редко метастазирует. [8]
Когда опухолевые клетки метастазируют, новая опухоль называется вторичной или метастатической опухолью, и ее клетки похожи на клетки в исходной или первичной опухоли . [9] Это означает, что если рак молочной железы метастазирует в легкие, вторичная опухоль состоит из аномальных клеток молочной железы, а не из аномальных клеток легких. Опухоль в легком тогда называется метастатическим раком молочной железы , а не раком легких . Метастазирование является ключевым элементом в системах стадирования рака , таких как система стадирования TNM , где оно представляет собой «М». В общей группировке стадий метастазирование помещает рак в стадию IV. Возможности излечивающего лечения значительно сокращаются или часто полностью устраняются, когда рак метастазирует.

Сначала поражаются близлежащие лимфатические узлы. [10] Легкие, печень, мозг и кости являются наиболее распространенными местами метастазирования солидных опухолей . [10]
Хотя запущенный рак может вызывать боль , она часто не является первым симптомом.
Однако у некоторых пациентов не проявляются никакие симптомы. [10] Когда орган подвергается метастатическому заболеванию, он начинает уменьшаться в размерах, пока его лимфатические узлы не лопнут или не подвергнутся лизису .
Метастатические опухоли очень распространены на поздних стадиях рака. Распространение метастазов может происходить через кровь или лимфатическую систему или обоими путями. Наиболее распространенными местами метастазов являются легкие , печень , мозг и кости [ 10]
В настоящее время предложено три основные теории для объяснения метастатического пути рака: гипотеза эпителиально-мезенхимального перехода (EMT) и мезенхимально-эпителиального перехода (MET) (1), гипотеза раковых стволовых клеток (2) и гибридная гипотеза слияния макрофагов и раковых клеток (3). Также были предложены некоторые новые гипотезы, а именно, под воздействием определенных биохимических и/или физических стрессоров раковые клетки могут подвергаться ядерному изгнанию с последующим поглощением макрофагами и слиянием с образованием раковых клеток слияния (CFC). [11] Понимание загадки распространения раковых клеток в отдаленные места, что составляет более 90% смертей, связанных с раком, требует всестороннего исследования. Основные нерешенные вопросы вращаются вокруг выживания и миграции раковых клеток, таких как ядро, поскольку они сталкиваются с трудностями при прохождении через капиллярные клапаны и гидродинамическими сдвиговыми силами в системе кровообращения, что делает CTC маловероятным источником метастазов. Более того, понимание того, как раковые клетки адаптируются к метастатической нише и остаются в состоянии покоя (опухолевый покой) в течение длительных периодов времени, представляет собой сложные вопросы, требующие дальнейшего изучения. [11]
Метастазирование включает в себя сложную серию этапов, в ходе которых раковые клетки покидают исходное место опухоли и мигрируют в другие части тела через кровоток, через лимфатическую систему или путем прямого расширения. Для этого злокачественные клетки отрываются от первичной опухоли и прикрепляются к белкам , которые составляют окружающий внеклеточный матрикс (ВКМ), отделяющий опухоль от прилегающих тканей, и разрушают их. Разрушая эти белки, раковые клетки способны прорвать ВКМ и сбежать. Расположение метастазов не всегда случайно, при этом различные типы рака имеют тенденцию распространяться на определенные органы и ткани со скоростью, которая выше, чем ожидается только по статистической случайности. [12] Например, рак груди имеет тенденцию метастазировать в кости и легкие. Эта специфичность, по-видимому, опосредована растворимыми сигнальными молекулами, такими как хемокины [13] и трансформирующий фактор роста бета . [14] Организм сопротивляется метастазам с помощью различных механизмов посредством действия класса белков, известных как супрессоры метастазов , которых известно около дюжины. [15]
Человеческие клетки демонстрируют различные виды движения: коллективную подвижность , движение мезенхимального типа и амебоидное движение . Раковые клетки часто оппортунистически переключаются между различными видами движения. Некоторые исследователи рака надеются найти методы лечения, которые могут остановить или, по крайней мере, замедлить распространение рака, каким-то образом блокируя некоторые необходимые шаги в одном или нескольких видах движения. [16] [17]
Все этапы метастатического каскада включают ряд физических процессов. Миграция клеток требует создания сил, а когда раковые клетки трансмигрируют через сосудистую сеть, это требует образования физических зазоров в кровеносных сосудах. [18] Помимо сил, регуляция различных типов межклеточных и межклеточных адгезий имеет решающее значение во время метастазирования. [ необходима цитата ]
Метастатические этапы критически регулируются различными типами клеток, включая клетки кровеносных сосудов (эндотелиальные клетки), иммунные клетки или стромальные клетки. Рост новой сети кровеносных сосудов, называемый опухолевым ангиогенезом , [19] является важнейшим признаком рака. Поэтому было высказано предположение, что ингибиторы ангиогенеза предотвратят рост метастазов. [8] Было показано, что эндотелиальные клетки-предшественники оказывают сильное влияние на метастазирование и ангиогенез. [20] [21] Эндотелиальные клетки-предшественники играют важную роль в росте опухоли, ангиогенезе и метастазировании и могут быть помечены с помощью ингибитора связывания ДНК 1 (ID1). Это новое открытие означало, что исследователи получили возможность отслеживать эндотелиальные клетки-предшественники от костного мозга до крови, опухолевой стромы и даже включенные в сосудистую сеть опухоли. Эндотелиальные клетки-предшественники, включенные в сосудистую сеть опухоли, предполагают, что этот тип клеток в развитии кровеносных сосудов важен в условиях опухоли и метастазирования. Более того, абляция эндотелиальных прогениторных клеток в костном мозге может привести к значительному снижению роста опухоли и развития сосудистой сети. Таким образом, эндотелиальные прогениторные клетки играют важную роль в биологии опухолей и представляют собой новые терапевтические цели. [22] Иммунная система обычно дерегулирована при раке и влияет на многие стадии прогрессирования опухоли, включая метастазы. [ необходима цитата ]
Эпигенетическая регуляция также играет важную роль в метастатическом разрастании распространенных опухолевых клеток. Метастазы демонстрируют изменения в модификациях гистонов, таких как метилирование H3K4 и метилирование H3K9, по сравнению с соответствующими первичными опухолями. [23] Эти эпигенетические модификации в метастазах могут способствовать пролиферации и выживанию распространенных опухолевых клеток в отдаленных органах. [24]
Недавнее исследование показывает, что PKC-йота способствует инвазии клеток меланомы, активируя виментин во время ЭПТ. Ингибирование или нокдаун PKC-йота приводит к повышению уровней E-кадгерина и RhoA при одновременном снижении общего виментина, фосфорилированного виментина (S39) и Par6 в метастатических клетках меланомы. Эти результаты предполагают, что PKC-ι участвует в сигнальных путях, которые повышают регуляцию ЭПТ в меланоме, тем самым напрямую стимулируя метастазы. [25]
Недавно серия громких экспериментов показала, что кооптация межклеточных перекрестных коммуникаций, опосредованных везикулами экзосом, является критическим фактором, участвующим во всех этапах каскада инвазии-метастазирования. [26]
Метастазирование происходит следующими четырьмя путями:
Распространение злокачественной опухоли в полости тела может происходить через проникновение через поверхность брюшинного , плеврального , перикардиального или субарахноидального пространства. Например, опухоли яичников могут распространяться трансперитонеально на поверхность печени. [ необходима цитата ]
Лимфатическое распространение позволяет переносить опухолевые клетки в региональные лимфатические узлы вблизи первичной опухоли и в конечном итоге в другие части тела. Это называется поражением узлов, положительными узлами или региональным заболеванием. «Положительные узлы» — это термин, который медицинские специалисты используют для описания региональных лимфатических узлов, которые дали положительный результат на злокачественность. Обычной медицинской практикой является тестирование с помощью биопсии по крайней мере одного лимфатического узла вблизи места опухоли при проведении операции по исследованию или удалению опухоли. Затем этот лимфатический узел называется сторожевым лимфатическим узлом . Лимфатическое распространение является наиболее распространенным путем начального метастазирования для карцином . [8] Напротив, саркома редко метастазирует таким путем. Локализованное распространение в региональные лимфатические узлы вблизи первичной опухоли обычно не считается метастазом, хотя это признак худшего исхода . Лимфатическая система в конечном итоге дренируется из грудного протока и правого лимфатического протока в системную венозную систему в венозном углу и в плечеголовные вены , и поэтому эти метастатические клетки в конечном итоге могут также распространяться через гематогенный путь. [ необходима цитата ]

Это типичный путь метастазирования для сарком, но это также предпочтительный путь для некоторых типов карциномы, таких как почечно-клеточная карцинома, возникающая в почке, и фолликулярная карцинома щитовидной железы. Из-за их более тонких стенок вены чаще поражаются, чем артерии, и метастазы имеют тенденцию следовать схеме венозного тока . То есть, гематогенное распространение часто следует различным схемам в зависимости от расположения первичной опухоли. Например, колоректальный рак распространяется в основном через воротную вену в печень. [ необходима цитата ]
Некоторые опухоли, особенно карциномы, могут метастазировать вдоль анатомических канальцевых пространств. К таким пространствам относятся, например, желчные протоки, мочевыделительная система, дыхательные пути и субарахноидальное пространство . Процесс аналогичен процессу трансцеломического распространения. Однако часто остается неясным, являются ли одновременно диагностированные опухоли канальцевой системы одним метастатическим процессом или фактически независимыми опухолями, вызванными одним и тем же агентом ( полевая канцеризация ). [ необходима цитата ]
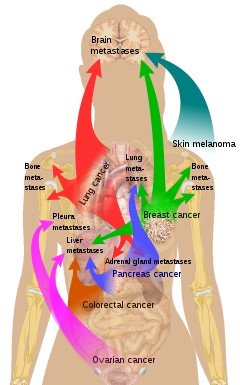
Существует склонность некоторых опухолей к распространению в определенных органах. Впервые это обсуждалось как теория «семени и почвы» Стивеном Пэджетом в 1889 году. [28] Склонность метастатической клетки распространяться в определенный орган называется «органотропизмом». Например, рак простаты обычно метастазирует в кости. Подобным образом рак толстой кишки имеет тенденцию метастазировать в печень. Рак желудка часто метастазирует в яичник у женщин, когда его называют опухолью Крукенберга . [ необходима цитата ]
Согласно теории «семени и почвы», раковым клеткам трудно выживать вне области их происхождения, поэтому для метастазирования они должны найти место со схожими характеристиками. [29] Например, клетки опухоли груди, которые собирают ионы кальция из грудного молока, метастазируют в костную ткань, где они могут собирать ионы кальция из кости. Злокачественная меланома распространяется на мозг, предположительно, потому что нервная ткань и меланоциты возникают из одной и той же клеточной линии в эмбрионе . [30]
В 1928 году Джеймс Юинг бросил вызов теории «семени и почвы» и предположил, что метастазирование происходит исключительно анатомическими и механическими путями. Эта гипотеза была недавно использована для предложения нескольких гипотез о жизненном цикле циркулирующих опухолевых клеток (ЦОК) и для постулирования того, что закономерности распространения можно лучше понять с точки зрения «фильтра и потока». [31] Однако современные данные указывают на то, что первичная опухоль может диктовать органотропные метастазы, вызывая образование пре-метастатических ниш в отдаленных местах, где входящие метастатические клетки могут приживаться и колонизироваться. [26] В частности, было показано, что экзосомальные везикулы, секретируемые опухолями, размещаются в пре-метастатических местах, где они активируют про-метастатические процессы, такие как ангиогенез, и изменяют иммунную структуру, чтобы способствовать созданию благоприятной микросреды для роста вторичной опухоли. [26]
Предполагается, что метастазирование всегда совпадает с первичным раком и, как таковое, является опухолью, которая началась из раковой клетки или клеток в другой части тела. Однако более 10% пациентов, обращающихся в онкологические отделения, будут иметь метастазы без обнаружения первичной опухоли. В этих случаях врачи называют первичную опухоль «неизвестной» или «скрытой», и говорят, что у пациента рак неизвестного первичного происхождения (CUP) или неизвестные первичные опухоли (UPT). [32] По оценкам, 3% всех раковых заболеваний имеют неизвестное первичное происхождение. [33] Исследования показали, что если простой опрос не выявляет источник рака (кашель с кровью — «вероятно, легкое », мочеиспускание с кровью — «вероятно, мочевой пузырь »), сложная визуализация тоже не сможет этого сделать. [33] В некоторых из этих случаев первичная опухоль может появиться позже. [ требуется ссылка ]
Использование иммуногистохимии позволило патологам идентифицировать многие из этих метастазов. Однако визуализация указанной области лишь изредка выявляет первичную опухоль. В редких случаях (например, меланомы ) первичная опухоль не обнаруживается даже при вскрытии . Поэтому считается, что некоторые первичные опухоли могут полностью регрессировать, но оставлять после себя метастазы. В других случаях опухоль может быть просто слишком маленькой и/или находиться в необычном месте для диагностики. [ необходима цитата ]

Клетки в метастатической опухоли напоминают клетки в первичной опухоли. После того, как раковая ткань исследуется под микроскопом для определения типа клеток, врач обычно может сказать, встречается ли этот тип клеток в норме в той части тела, из которой был взят образец ткани. [ необходима цитата ]
Например, клетки рака молочной железы выглядят одинаково, независимо от того, находятся ли они в молочной железе или распространились на другую часть тела. Таким образом, если образец ткани, взятый из опухоли в легком, содержит клетки, которые выглядят как клетки молочной железы, врач определяет, что опухоль легкого является вторичной опухолью. Тем не менее, определение первичной опухоли часто может быть очень сложным, и патологу, возможно, придется использовать несколько вспомогательных методов, таких как иммуногистохимия , FISH ( флуоресцентная гибридизация in situ ) и другие. Несмотря на использование методов, в некоторых случаях первичная опухоль остается неидентифицированной.
Метастатические раковые опухоли могут быть обнаружены одновременно с первичной опухолью или спустя месяцы или годы. Когда у пациента, который в прошлом лечился от рака, обнаруживается вторая опухоль, чаще всего это метастаз, чем другая первичная опухоль.
Ранее считалось, что большинство раковых клеток имеют низкий метастатический потенциал и что существуют редкие клетки, которые развивают способность метастазировать через развитие соматических мутаций. [34] Согласно этой теории, диагностика метастатического рака возможна только после возникновения метастазов. Традиционные средства диагностики рака (например, биопсия ) будут исследовать только субпопуляцию раковых клеток и, скорее всего, не будут брать образцы из субпопуляции с метастатическим потенциалом. [35]
Теория соматической мутации развития метастазов не была подтверждена в раковых заболеваниях человека. Скорее, кажется, что генетическое состояние первичной опухоли отражает способность этой опухоли метастазировать. [35] Исследования, сравнивающие экспрессию генов между первичными и метастатическими аденокарциномами, выявили подмножество генов, экспрессия которых может отличать первичные опухоли от метастатических, названное «метастатической сигнатурой». [35] Гены с повышенной регуляцией в сигнатуре включают: SNRPF , HNRPAB , DHPS и секурин . Снижение регуляции актина , миозина и MHC класса II также было связано с сигнатурой. Кроме того, связанная с метастазами экспрессия этих генов также наблюдалась в некоторых первичных опухолях, что указывает на то, что клетки с потенциалом к метастазированию можно идентифицировать одновременно с диагностикой первичной опухоли. [36] Недавняя работа выявила форму генетической нестабильности при раке, называемую хромосомной нестабильностью (CIN), как движущую силу метастазирования. [37] В агрессивных раковых клетках свободные фрагменты ДНК из нестабильных хромосом попадают в цитозоль, что приводит к хронической активации врожденных иммунных путей, которые захватываются раковыми клетками и распространяются на отдаленные органы.
Экспрессия этой метастатической сигнатуры коррелировала с плохим прогнозом и, как было показано, была постоянной при нескольких типах рака. Было показано, что прогноз был хуже для людей, чьи первичные опухоли выражали метастатическую сигнатуру. [35] Кроме того, было показано, что экспрессия этих метастатически-ассоциированных генов применима к другим типам рака в дополнение к аденокарциноме . Метастазы рака молочной железы , медуллобластомы и рака простаты имели схожие паттерны экспрессии этих метастаз-ассоциированных генов. [35]
Идентификация этой метастаз-ассоциированной сигнатуры дает надежду на идентификацию клеток с метастатическим потенциалом в первичной опухоли и на улучшение прогноза этих метастаз-ассоциированных раковых заболеваний. Кроме того, идентификация генов, экспрессия которых изменяется при метастазах, предлагает потенциальные цели для ингибирования метастазов. [35]
Лечение и выживаемость в значительной степени определяются тем, остается ли рак локализованным или распространяется на другие части тела. Если рак метастазирует в другие ткани или органы, это обычно резко увеличивает вероятность смерти пациента. Некоторые виды рака, такие как некоторые формы лейкемии , рак крови или злокачественные опухоли мозга , могут убивать, вообще не распространяясь.
После того, как рак дал метастазы, его все еще можно лечить с помощью радиохирургии , химиотерапии , лучевой терапии , биологической терапии , гормональной терапии , хирургии или комбинации этих вмешательств («мультимодальная терапия»). Выбор лечения зависит от многих факторов, включая тип первичного рака, размер и расположение метастазов, возраст и общее состояние здоровья пациента, а также типы лечения, которые использовались ранее. У пациентов с диагнозом CUP часто все еще возможно лечить заболевание, даже если первичную опухоль невозможно обнаружить.
Современные методы лечения редко способны вылечить метастатический рак, хотя некоторые опухоли, такие как рак яичек и рак щитовидной железы , обычно поддаются лечению.
Паллиативная помощь , направленная на улучшение качества жизни людей с серьезными заболеваниями, была рекомендована как часть программ лечения метастазов. [38] Результаты систематического обзора литературы по лучевой терапии метастазов в мозг показали, что существует мало доказательств, позволяющих оценить сравнительную эффективность и результаты, ориентированные на пациента, в отношении качества жизни, функционального статуса и когнитивных эффектов. [39]
Хотя метастазы широко признаны как результат миграции опухолевых клеток, существует гипотеза , согласно которой некоторые метастазы являются результатом воспалительных процессов, вызванных аномальными иммунными клетками. [40] Существование метастатического рака при отсутствии первичных опухолей также предполагает, что метастазы не всегда вызваны злокачественными клетками, которые покидают первичные опухоли. [41]
Исследование, проведенное командой Сарны, доказало, что сильно пигментированные клетки меланомы имеют модуль Юнга около 4,93, тогда как у непигментированных он был всего 0,98. [42] В другом эксперименте они обнаружили, что эластичность клеток меланомы важна для ее метастазирования и роста: непигментированные опухоли были больше пигментированных, и им было намного легче распространяться. Они показали, что в опухолях меланомы есть как пигментированные, так и непигментированные клетки , поэтому они оба могут быть устойчивыми к лекарствам и метастатическими. [42]
Первым врачом, сообщившим о возможности локального метастазирования первичного ракового источника в близлежащие ткани, был Ибн Сина . Он описал случай рака груди и метастатического состояния в «Каноне врачебной науки» . Его гипотеза основывалась на клиническом течении заболевания у пациента. [43] [44]
В марте 2014 года исследователи обнаружили старейший полный образец человека с метастатическим раком. Опухоли развились в 3000-летнем скелете, найденном в 2013 году в гробнице в Судане, датируемой 1200 годом до нашей эры. Скелет был проанализирован с помощью рентгенографии и сканирующего электронного микроскопа. Эти результаты были опубликованы в журнале Public Library of Science . [45] [46] [47]
Метастаз – греческое слово, означающее «смещение», от μετά, мета , «следующий», и στάσις, застой , «размещение».
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на октябрь 2024 г. ( ссылка )