Серная кислота ( американское написание и предпочтительное название ИЮПАК ) или серная кислота ( написание Содружества ), известная в древности как купоросное масло , является минеральной кислотой, состоящей из элементов серы , кислорода и водорода , с молекулярной формулой H2SO4 . Это бесцветная, не имеющая запаха и вязкая жидкость, смешивающаяся с водой. [6]

Чистая серная кислота не встречается в природе из-за ее сильного сродства к водяному пару ; она гигроскопична и легко поглощает водяной пар из воздуха . [6] Концентрированная серная кислота очень едкая по отношению к другим материалам, от камней до металлов, поскольку она является окислителем с мощными дегидратирующими свойствами. Пятиокись фосфора является заметным исключением, поскольку она не дегидратируется серной кислотой, а, наоборот, дегидратирует серную кислоту до триоксида серы . При добавлении серной кислоты к воде выделяется значительное количество тепла; таким образом, обратная процедура добавления воды к кислоте обычно избегается, поскольку выделяющееся тепло может закипать раствор, разбрызгивая капли горячей кислоты во время процесса. При контакте с тканями тела серная кислота может вызвать серьезные кислотные химические ожоги и вторичные термические ожоги из-за дегидратации. [7] [8] Разбавленная серная кислота значительно менее опасна без окислительных и дегидратирующих свойств; хотя с ней обращаются с осторожностью из-за ее кислотности.
Серная кислота является очень важным химическим товаром; производство серной кислоты в стране является хорошим показателем ее промышленной мощи. [9] Известно много методов ее производства, включая контактный процесс , мокрый сернокислотный процесс и процесс в свинцовой камере . [10] Серная кислота также является ключевым веществом в химической промышленности . Она чаще всего используется в производстве удобрений [11], но также важна в переработке полезных ископаемых , нефтепереработке , обработке сточных вод и химическом синтезе . Она имеет широкий спектр конечных применений, в том числе в бытовых кислотных очистителях канализации , [12] в качестве электролита в свинцово-кислотных аккумуляторах , в качестве дегидратирующего соединения и в различных чистящих средствах . Серную кислоту можно получить путем растворения триоксида серы в воде.
Хотя можно приготовить почти 100% раствор серной кислоты, последующая потеря SO 3 при температуре кипения доводит концентрацию до 98,3% кислоты. 98,3%-ный сорт, который более стабилен при хранении, является обычной формой того, что описывается как «концентрированная серная кислота». Другие концентрации используются для разных целей. Вот некоторые распространенные концентрации: [13] [14]
«Камерная кислота» и «башенная кислота» были двумя концентрациями серной кислоты, полученными в процессе свинцовой камеры , камерная кислота была кислотой, полученной в самой свинцовой камере (<70%, чтобы избежать загрязнения нитрозилсерной кислотой ), а башенная кислота была кислотой, извлеченной со дна башни Гловера. [13] [14] В настоящее время они устарели как коммерческие концентрации серной кислоты, хотя их можно приготовить в лаборатории из концентрированной серной кислоты, если это необходимо. В частности, «10 M» серная кислота (современный эквивалент камерной кислоты, используемая во многих титрованиях ) готовится путем медленного добавления 98% серной кислоты к равному объему воды при хорошем перемешивании: температура смеси может подняться до 80 °C (176 °F) или выше. [14]
Серная кислота содержит не только молекулы H2SO4 , но на самом деле является равновесием многих других химических веществ, как показано в таблице ниже.
Серная кислота представляет собой бесцветную маслянистую жидкость, давление паров которой составляет <0,001 мм рт. ст. при 25 °C и 1 мм рт. ст. при 145,8 °C [16], а 98% серная кислота имеет давление паров <1 мм рт. ст. при 40 °C [17] .
В твердом состоянии серная кислота представляет собой молекулярное твердое вещество, образующее моноклинные кристаллы с почти тригональными параметрами решетки. Структура состоит из слоев, параллельных плоскости (010), в которых каждая молекула соединена водородными связями с двумя другими. [3] Гидраты H2SO4 · nH2O известны для n = 1 , 2, 3, 4, 6,5 и 8 , хотя большинство промежуточных гидратов устойчивы к диспропорционированию . [18]
Безводная H 2 SO 4 является очень полярной жидкостью, имеющей диэлектрическую проницаемость около 100. Она имеет высокую электропроводность , что является следствием автопротолиза , т.е. самопротонирования : [ 15]
Константа равновесия для автопротолиза (25 °C) равна: [15]
Соответствующая константа равновесия для воды , Kw , равна 10−14 , что в 1010 ( 10 миллиардов) раз меньше.
Несмотря на вязкость кислоты, эффективная проводимость H 3 SO+4и ХСО−4ионы высоки из-за внутримолекулярного механизма переключения протонов (аналогичного механизму Гротгуса в воде), что делает серную кислоту хорошим проводником электричества. Она также является отличным растворителем для многих реакций.

Реакция гидратации серной кислоты является сильно экзотермической , разбавление. [19]
Как показывает константа кислотной диссоциации , серная кислота является сильной кислотой:
Продуктом этой ионизации является HSO.−4, бисульфат- анион. Бисульфат — гораздо более слабая кислота:
Продуктом этой второй диссоциации является SO2−4, сульфат- анион.
Концентрированная серная кислота обладает мощным дегидратирующим свойством, удаляя воду ( H 2 O ) из других химических соединений, таких как столовый сахар ( сахароза ) и другие углеводы , для получения углерода , пара и тепла. Дегидратация столового сахара (сахарозы) является обычной лабораторной демонстрацией. [21] Сахар темнеет по мере образования углерода, и может появиться жесткий столб черного пористого углерода, называемый углеродной змеей [22], как показано на рисунке.
Аналогично, смешивание крахмала с концентрированной серной кислотой дает элементарный углерод и воду. Эффект этого можно увидеть, когда концентрированная серная кислота проливается на бумагу, которая состоит из целлюлозы ; целлюлоза реагирует, давая обгоревший вид, в котором углерод выглядит очень похожим на сажу , которая возникает в результате пожара. Хотя и менее драматично, действие кислоты на хлопок , даже в разбавленной форме, разрушает ткань.
Реакция с сульфатом меди(II) также может продемонстрировать свойство серной кислоты к дегидратации. Синие кристаллы превращаются в белый порошок по мере удаления воды:
Серная кислота реагирует с большинством оснований, образуя соответствующий сульфат или бисульфат.
Серная кислота реагирует с хлоридом натрия , образуя газообразный хлористый водород и гидросульфат натрия :
Сульфат алюминия , также известный как квасцы для производителей бумаги, производится путем обработки бокситов серной кислотой:
Серную кислоту можно также использовать для вытеснения более слабых кислот из их солей. Реакция с ацетатом натрия , например, вытесняет уксусную кислоту , CH 3 COOH , и образует бисульфат натрия :
Аналогично обработка нитрата калия серной кислотой приводит к образованию азотной кислоты .
В сочетании с азотной кислотой серная кислота действует как кислота и дегидратирующий агент, образуя ион нитрония NO+2, что важно в реакциях нитрования , включающих электрофильное ароматическое замещение . Этот тип реакции, где протонирование происходит на атоме кислорода , важен во многих реакциях органической химии , таких как этерификация Фишера и дегидратация спиртов.
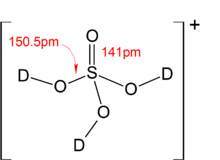
При реакции с суперкислотами серная кислота может действовать как основание и может протонироваться, образуя ион [H 3 SO 4 ] + . Соли [H 3 SO 4 ] + были получены (например, гексафторантимонат(V) тригидроксиоксосульфония [H 3 SO 4 ] + [SbF 6 ] − ) с использованием следующей реакции в жидком HF :
Вышеуказанная реакция термодинамически выгодна из-за высокой энтальпии связи Si–F в побочном продукте. Однако протонирование с использованием просто фторсурьмяной кислоты потерпело неудачу, поскольку чистая серная кислота подвергается самоионизации с образованием ионов [H 3 O] + :
что предотвращает преобразование H 2 SO 4 в [H 3 SO 4 ] + системой HF/ SbF 5. [23]
Даже разбавленная серная кислота реагирует со многими металлами посредством одной реакции замещения, как и другие типичные кислоты , производя водород и соли (сульфат металла). Она атакует химически активные металлы (металлы, стоящие выше меди в ряду реактивности ), такие как железо , алюминий , цинк , марганец , магний и никель .
Концентрированная серная кислота может служить окислителем , выделяя диоксид серы: [7]
Однако свинец и вольфрам устойчивы к серной кислоте.
Горячая концентрированная серная кислота окисляет углерод [24] (как каменный уголь ) и серу :
Бензол подвергается электрофильному ароматическому замещению серной кислотой с образованием соответствующих сульфоновых кислот : [25]
Серную кислоту можно использовать для получения водорода из воды :
Соединения серы и йода восстанавливаются и используются повторно, поэтому процесс называется циклом серы и йода . Этот процесс является эндотермическим и должен происходить при высоких температурах, поэтому необходимо поставлять энергию в виде тепла. Цикл серы и йода был предложен как способ поставки водорода для экономики, основанной на водороде . Он является альтернативой электролизу и не требует углеводородов , как современные методы парового риформинга . Но обратите внимание, что вся доступная энергия в полученном таким образом водороде обеспечивается теплом, используемым для его получения. [26] [27]

Серная кислота редко встречается в природе на Земле в безводной форме из-за ее большого сродства к воде . Разбавленная серная кислота является компонентом кислотных дождей , которые образуются при атмосферном окислении диоксида серы в присутствии воды – т.е. окислении сернистой кислоты . При сжигании серосодержащего топлива, такого как уголь или нефть, диоксид серы является основным побочным продуктом (помимо главных продуктов – оксидов углерода и воды).
Серная кислота образуется естественным образом в результате окисления сульфидных минералов, таких как пирит :
Образующаяся при этом сильнокислотная вода называется кислым шахтным дренажем (КШД) или кислым дренажем горных пород (КДПГ).
Fe 2+ может далее окисляться до Fe 3+ :
Образовавшийся Fe3 + может быть осажден в виде гидроксида или водного оксида железа :
Ион железа(III) («трехвалентное железо») также может окислять пирит:
Когда происходит окисление пирита железом (III), процесс может стать быстрым. Значения pH ниже нуля были измерены в ARD, полученном в результате этого процесса.
ARD также может производить серную кислоту с меньшей скоростью, так что кислотонейтрализующая способность (ANC) водоносного горизонта может нейтрализовать произведенную кислоту. В таких случаях общая концентрация растворенных твердых веществ (TDS) в воде может быть увеличена за счет растворения минералов из реакции кислотонейтрализации с минералами.
Серная кислота используется в качестве защиты некоторыми морскими видами, например, феофитная водоросль Desmarestia munda (отряд Desmarestiales ) концентрирует серную кислоту в вакуолях клеток. [28]
В стратосфере , втором слое атмосферы, который обычно находится на высоте от 10 до 50 км над поверхностью Земли, серная кислота образуется в результате окисления вулканического диоксида серы гидроксильным радикалом : [29]
Поскольку серная кислота достигает пересыщения в стратосфере, она может зародышеобразовать аэрозольные частицы и обеспечивать поверхность для роста аэрозоля посредством конденсации и коагуляции с другими аэрозолями воды и серной кислоты. Это приводит к образованию стратосферного аэрозольного слоя . [29]
Постоянные облака Венеры производят концентрированный кислотный дождь, подобно тому, как облака в атмосфере Земли производят водяной дождь. [30] Считается, что у спутника Юпитера Европы также есть атмосфера, содержащая гидраты серной кислоты. [31]
Серную кислоту получают из серы , кислорода и воды с помощью обычного контактного процесса (DCDA) или мокрого сернокислотного процесса (WSA).
На первом этапе сера сжигается для получения диоксида серы.
Диоксид серы окисляется до триоксида серы кислородом в присутствии катализатора оксида ванадия(V) . Эта реакция обратима, и образование триоксида серы является экзотермическим.
Триоксид серы поглощается 97–98% H 2 SO 4 с образованием олеума ( H 2 S 2 O 7 ), также известного как дымящая серная кислота или пиросерная кислота. Затем олеум разбавляется водой с образованием концентрированной серной кислоты.
Прямое растворение SO3 в воде, называемое « мокрым сернокислотным процессом », практикуется редко, поскольку реакция является чрезвычайно экзотермической и приводит к образованию горячего аэрозоля серной кислоты, требующего конденсации и разделения .
На первом этапе сера сжигается с образованием диоксида серы:
или, в качестве альтернативы, газ сероводорода ( H 2 S ) сжигается до газа SO 2 :
Затем диоксид серы окисляется до триоксида серы с использованием кислорода и оксида ванадия (V) в качестве катализатора .
Триоксид серы гидратируется в серную кислоту H2SO4 :
Последний этап – конденсация серной кислоты в жидкую 97–98% H 2 SO 4 :
Менее известный метод — это метод метабисульфита, в котором метабисульфит помещают на дно стакана и добавляют соляную кислоту с молярной концентрацией 12,6. Полученный газ барботируют через азотную кислоту , которая выделяет коричневые/красные пары диоксида азота по мере протекания реакции. Завершение реакции подтверждается прекращением испарений. Этот метод не дает неотделимого тумана, что весьма удобно.
Исторически применялось сжигание серы вместе с селитрой ( нитрат калия , KNO3 ) в присутствии пара. При разложении селитры сера окисляется до SO3 , который соединяется с водой, образуя серную кислоту.
Альтернативный вариант — растворение диоксида серы в водном растворе соли окисляющего металла, например, хлорида меди (II) или железа (III):
Два менее известных лабораторных метода получения серной кислоты, хотя и в разбавленной форме и требующих дополнительных усилий при очистке. Раствор сульфата меди(II) можно электролизовать с медным катодом и платиновым/графитовым анодом, чтобы получить губчатую медь на катоде и выделение газообразного кислорода на аноде, раствор разбавленной серной кислоты указывает на завершение реакции, когда он меняет цвет с синего на прозрачный (выделение водорода на катоде является еще одним признаком):
Более дорогостоящим, опасным и проблемным, но новым является электробромный метод, который использует смесь серы , воды и бромистоводородной кислоты в качестве электролитического раствора. Сера проталкивается на дно контейнера под кислотным раствором. Затем используются медный катод и платиновый/графитовый анод, причем катод находится вблизи поверхности, а анод располагается на дне электролита для подачи тока. Это может занять больше времени и выделяет токсичные пары брома /бромида серы, но реагентная кислота пригодна для вторичной переработки. В целом, только сера и вода преобразуются в серную кислоту и водород (исключая потери кислоты в виде паров):
До 1900 года большая часть серной кислоты производилась с помощью процесса в свинцовой камере . [32] Еще в 1940 году до 50% серной кислоты, производимой в Соединенных Штатах, производилось на заводах, использующих камерный процесс.
В начале и середине 19 века заводы по производству «купороса» существовали, среди прочего, в Престонпансе в Шотландии, Шропшире и долине Лаган в графстве Антрим в Ирландии, где он использовался в качестве отбеливателя для белья. Раннее отбеливание белья производилось с использованием молочной кислоты из кислого молока, но это был медленный процесс, а использование купороса ускорило процесс отбеливания. [33]

Серная кислота является очень важным химическим товаром, и действительно, производство серной кислоты в стране является хорошим показателем ее промышленной мощи. [9] Мировое производство в 2004 году составило около 180 миллионов тонн со следующим географическим распределением: Азия 35%, Северная Америка (включая Мексику) 24%, Африка 11%, Западная Европа 10%, Восточная Европа и Россия 10%, Австралия и Океания 7%, Южная Америка 7%. [34] Большая часть этого количества (≈60%) потребляется для удобрений, в частности суперфосфатов, фосфата аммония и сульфатов аммония. Около 20% используется в химической промышленности для производства моющих средств, синтетических смол, красителей, фармацевтических препаратов, нефтяных катализаторов, инсектицидов и антифризов , а также в различных процессах, таких как кислотная обработка нефтяных скважин, восстановление алюминия, проклейка бумаги и очистка воды. Около 6% применений связаны с пигментами и включают краски, эмали , типографские краски, ткани с покрытием и бумагу, в то время как остальная часть распределена по множеству применений, таких как производство взрывчатых веществ, целлофана , ацетатных и вискозных тканей, смазочных материалов, цветных металлов и аккумуляторов. [35]
Доминирующее применение серной кислоты — «мокрый метод» производства фосфорной кислоты , используемой для производства фосфатных удобрений . В этом методе используется фосфатная руда, и ежегодно перерабатывается более 100 миллионов тонн. Это сырье показано ниже как фторапатит , хотя точный состав может отличаться. Его обрабатывают 93% серной кислотой для получения сульфата кальция , фтористого водорода (HF) и фосфорной кислоты . HF удаляется в виде плавиковой кислоты . Общий процесс можно представить следующим образом:
Сульфат аммония , важное азотное удобрение, чаще всего производится как побочный продукт коксовых заводов, снабжающих металлургические заводы. Реакция аммиака, полученного при термическом разложении угля , с отходами серной кислоты позволяет кристаллизовать аммиак в виде соли (часто коричневой из-за примесей железа) и продавать его в агрохимической промышленности.
Серная кислота также важна при производстве растворов красителей .
Серная кислота используется в сталелитейной и других металлургических отраслях промышленности в качестве травильного агента для удаления ржавчины и загрязнений . [36] Использованная кислота часто перерабатывается с использованием установок регенерации отработанной кислоты (SAR). Эти установки сжигают отработанную кислоту [ требуется осветление ] с природным газом, нефтезаводским газом, мазутом или другими источниками топлива. Этот процесс сжигания производит газообразный диоксид серы ( SO2 ) и триоксид серы ( SO3 ) , которые затем используются для производства «новой» серной кислоты.
Перекись водорода ( H 2 O 2 ) можно добавлять к серной кислоте для получения раствора пираньи — мощного, но очень токсичного чистящего раствора, с помощью которого можно очищать поверхности подложек. Раствор пираньи обычно используется в микроэлектронной промышленности, а также в лабораторных условиях для очистки стеклянной посуды.
Серная кислота используется для множества других целей в химической промышленности. Например, это обычный кислотный катализатор для превращения циклогексаноноксима в капролактам , используемый для производства нейлона . Она используется для производства соляной кислоты из соли с помощью процесса Мангейма . Много H2SO4 используется в нефтепереработке , например, в качестве катализатора для реакции изобутана с изобутиленом для получения изооктана , соединения, которое повышает октановое число бензина ( бензина ). Серная кислота также часто используется в качестве дегидратирующего или окисляющего агента в промышленных реакциях , таких как дегидратация различных сахаров для образования твердого углерода.
.jpg/440px-Acidic_drain_cleaner_containing_sulfuric_acid_(sulphuric_acid).jpg)
Sulfuric acid acts as the electrolyte in lead–acid batteries (lead-acid accumulator):
At anode:
At cathode:

Overall:
Sulfuric acid at high concentrations is frequently the major ingredient in domestic acidic drain cleaners[12] which are used to remove grease, hair, tissue paper, etc. Similar to their alkaline versions, such drain openers can dissolve fats and proteins via hydrolysis. Moreover, as concentrated sulfuric acid has a strong dehydrating property, it can remove tissue paper via dehydrating process as well. Since the acid may react with water vigorously, such acidic drain openers should be added slowly into the pipe to be cleaned.

The study of vitriols (hydrated sulfates of various metals forming glassy minerals from which sulfuric acid can be derived) began in ancient times. Sumerians had a list of types of vitriol that they classified according to the substances' color. Some of the earliest discussions on the origin and properties of vitriol is in the works of the Greek physician Dioscorides (first century AD) and the Roman naturalist Pliny the Elder (23–79 AD). Galen also discussed its medical use. Metallurgical uses for vitriolic substances were recorded in the Hellenistic alchemical works of Zosimos of Panopolis, in the treatise Phisica et Mystica, and the Leyden papyrus X.[37]
Medieval Islamic chemists like the authors writing under the name of Jabir ibn Hayyan (died c. 806 – c. 816 AD, known in Latin as Geber), Abu Bakr al-Razi (865 – 925 AD, known in Latin as Rhazes), Ibn Sina (980 – 1037 AD, known in Latin as Avicenna), and Muhammad ibn Ibrahim al-Watwat (1234 – 1318 AD) included vitriol in their mineral classification lists.[38]
The Jabirian authors and al-Razi experimented extensively with the distillation of various substances, including vitriols.[39] In one recipe recorded in his Kitāb al-Asrār ('Book of Secrets'), al-Razi may have created sulfuric acid without being aware of it:[40]
Take white (Yemeni) alum, dissolve it and purify it by filtration. Then distil (green?) vitriol with copper-green (the acetate), and mix (the distillate) with the filtered solution of the purified alum, afterwards let it solidify (or crystallise) in the glass beaker. You will get the best qalqadis (white alum) that may be had.[41]
— Abu Bakr al-Razi, Kitāb al-Asrār
In an anonymous Latin work variously attributed to Aristotle (under the title Liber Aristotilis, 'Book of Aristotle'),[42] to al-Razi (under the title Lumen luminum magnum, 'Great Light of Lights'), or to Ibn Sina,[43] the author speaks of an 'oil' (oleum) obtained through the distillation of iron(II) sulfate (green vitriol), which was likely 'oil of vitriol' or sulfuric acid.[44] The work refers multiple times to Jabir ibn Hayyan's Book of Seventy (Liber de septuaginta), one of the few Arabic Jabir works that were translated into Latin.[45] The author of the version attributed to al-Razi also refers to the Liber de septuaginta as his own work, showing that he erroneously believed the Liber de septuaginta to be a work by al-Razi.[46] There are several indications that the anonymous work was an original composition in Latin,[47] although according to one manuscript it was translated by a certain Raymond of Marseilles, meaning that it may also have been a translation from the Arabic.[48]
According to Ahmad Y. al-Hassan, three recipes for sulfuric acid occur in an anonymous Karshuni manuscript containing a compilation taken from several authors and dating from before c. 1100 AD.[49] One of them runs as follows:
The water of vitriol and sulphur which is used to irrigate the drugs: yellow vitriol three parts, yellow sulphur one part, grind them and distil them in the manner of rose-water.[50]
A recipe for the preparation of sulfuric acid is mentioned in Risālat Jaʿfar al-Sādiq fī ʿilm al-ṣanʿa, an Arabic treatise falsely attributed to the Shi'i Imam Ja'far al-Sadiq (died 765). Julius Ruska dated this treatise to the 13th century, but according to Ahmad Y. al-Hassan it likely dates from an earlier period:[51]
Then distil green vitriol in a cucurbit and alembic, using medium fire; take what you obtain from the distillate, and you will find it clear with a greenish tint.[50]
Sulfuric acid was called 'oil of vitriol' by medieval European alchemists because it was prepared by roasting iron(II) sulfate or green vitriol in an iron retort. The first allusions to it in works that are European in origin appear in the thirteenth century AD, as for example in the works of Vincent of Beauvais, in the Compositum de Compositis ascribed to Albertus Magnus, and in pseudo-Geber's Summa perfectionis.[52]
A method of producing oleum sulphuris per campanam, or "oil of sulfur by the bell", was known by the 16th century: it involved burning sulfur under a glass bell in moist weather (or, later, under a moistened bell). However, it was very inefficient (according to Gesner, 5 pounds (2.3 kg) of sulfur converted into less than 1 ounce (0.03 kg) of acid), and the resulting product was contaminated by sulfurous acid (or rather, solution of sulfur dioxide) so most alchemists (including, for example, Isaac Newton) didn't consider it equivalent with the "oil of vitriol".
In the 17th century, Johann Glauber discovered that adding saltpeter (potassium nitrate, KNO3) significantly improves the output, also replacing moisture with steam. As saltpeter decomposes, it oxidizes the sulfur to SO3, which combines with water to produce sulfuric acid. In 1736, Joshua Ward, a London pharmacist, used this method to begin the first large-scale production of sulfuric acid.
In 1746 in Birmingham, John Roebuck adapted this method to produce sulfuric acid in lead-lined chambers, which were stronger, less expensive, and could be made larger than the previously used glass containers. This process allowed the effective industrialization of sulfuric acid production. After several refinements, this method, called the lead chamber process or "chamber process", remained the standard for sulfuric acid production for almost two centuries.[4]
Sulfuric acid created by John Roebuck's process approached a 65% concentration. Later refinements to the lead chamber process by French chemist Joseph Louis Gay-Lussac and British chemist John Glover improved concentration to 78%. However, the manufacture of some dyes and other chemical processes require a more concentrated product. Throughout the 18th century, this could only be made by dry distilling minerals in a technique similar to the original alchemical processes. Pyrite (iron disulfide, FeS2) was heated in air to yield iron(II) sulfate, FeSO4, which was oxidized by further heating in air to form iron(III) sulfate, Fe2(SO4)3, which, when heated to 480 °C, decomposed to iron(III) oxide and sulfur trioxide, which could be passed through water to yield sulfuric acid in any concentration. However, the expense of this process prevented the large-scale use of concentrated sulfuric acid.[4]
In 1831, British vinegar merchant Peregrine Phillips patented the contact process, which was a far more economical process for producing sulfur trioxide and concentrated sulfuric acid. Today, nearly all of the world's sulfuric acid is produced using this method.[53]



Sulfuric acid is capable of causing very severe burns, especially when it is at high concentrations. In common with other corrosive acids and alkali, it readily decomposes proteins and lipids through amide and ester hydrolysis upon contact with living tissues, such as skin and flesh. In addition, it exhibits a strong dehydrating property on carbohydrates, liberating extra heat and causing secondary thermal burns.[7][8] Accordingly, it rapidly attacks the cornea and can induce permanent blindness if splashed onto eyes. If ingested, it damages internal organs irreversibly and may even be fatal.[6] Protective equipment should hence always be used when handling it. Moreover, its strong oxidizing property makes it highly corrosive to many metals and may extend its destruction on other materials.[7] Because of such reasons, damage posed by sulfuric acid is potentially more severe than that by other comparable strong acids, such as hydrochloric acid and nitric acid.
Sulfuric acid must be stored carefully in containers made of nonreactive material (such as glass). Solutions equal to or stronger than 1.5 M are labeled "CORROSIVE", while solutions greater than 0.5 M but less than 1.5 M are labeled "IRRITANT". However, even the normal laboratory "dilute" grade (approximately 1 M, 10%) will char paper if left in contact for a sufficient time.
The standard first aid treatment for acid spills on the skin is, as for other corrosive agents, irrigation with large quantities of water. Washing is continued for at least ten to fifteen minutes to cool the tissue surrounding the acid burn and to prevent secondary damage. Contaminated clothing is removed immediately and the underlying skin washed thoroughly.
Preparation of diluted acid can be dangerous due to the heat released in the dilution process. To avoid splattering, the concentrated acid is usually added to water and not the other way around. A saying used to remember this is "Do like you oughta, add the acid to the water".[54][better source needed] Water has a higher heat capacity than the acid, and so a vessel of cold water will absorb heat as acid is added.
Also, because the acid is denser than water, it sinks to the bottom. Heat is generated at the interface between acid and water, which is at the bottom of the vessel. Acid will not boil, because of its higher boiling point. Warm water near the interface rises due to convection, which cools the interface, and prevents boiling of either acid or water.
In contrast, addition of water to concentrated sulfuric acid results in a thin layer of water on top of the acid. Heat generated in this thin layer of water can boil, leading to the dispersal of a sulfuric acid aerosol or worse, an explosion.
Preparation of solutions greater than 6 M (35%) in concentration is dangerous, unless the acid is added slowly enough to allow the mixture sufficient time to cool. Otherwise, the heat produced may be sufficient to boil the mixture. Efficient mechanical stirring and external cooling (such as an ice bath) are essential.
Reaction rates double for about every 10-degree Celsius increase in temperature.[55] Therefore, the reaction will become more violent as dilution proceeds, unless the mixture is given time to cool. Adding acid to warm water will cause a violent reaction.
On a laboratory scale, sulfuric acid can be diluted by pouring concentrated acid onto crushed ice made from de-ionized water. The ice melts in an endothermic process while dissolving the acid. The amount of heat needed to melt the ice in this process is greater than the amount of heat evolved by dissolving the acid so the solution remains cold. After all the ice has melted, further dilution can take place using water.
Sulfuric acid is non-flammable.
The main occupational risks posed by this acid are skin contact leading to burns (see above) and the inhalation of aerosols. Exposure to aerosols at high concentrations leads to immediate and severe irritation of the eyes, respiratory tract and mucous membranes: this ceases rapidly after exposure, although there is a risk of subsequent pulmonary edema if tissue damage has been more severe. At lower concentrations, the most commonly reported symptom of chronic exposure to sulfuric acid aerosols is erosion of the teeth, found in virtually all studies: indications of possible chronic damage to the respiratory tract are inconclusive as of 1997. Repeated occupational exposure to sulfuric acid mists may increase the chance of lung cancer by up to 64 percent.[56] In the United States, the permissible exposure limit (PEL) for sulfuric acid is fixed at 1 mg/m3: limits in other countries are similar. There have been reports of sulfuric acid ingestion leading to vitamin B12 deficiency with subacute combined degeneration. The spinal cord is most often affected in such cases, but the optic nerves may show demyelination, loss of axons and gliosis.
International commerce of sulfuric acid is controlled under the United Nations Convention Against Illicit Traffic in Narcotic Drugs and Psychotropic Substances, 1988, which lists sulfuric acid under Table II of the convention as a chemical frequently used in the illicit manufacture of narcotic drugs or psychotropic substances.[57]
Clear to turbid oily odorless liquid, colorless to slightly yellow.
{{cite web}}: CS1 maint: unfit URL (link){{cite book}}: CS1 maint: multiple names: authors list (link)