Угарный газ ( химическая формула CO ) — ядовитый, легковоспламеняющийся газ, не имеющий цвета, запаха, вкуса и немного менее плотный, чем воздух. Окись углерода состоит из одного атома углерода и одного атома кислорода , соединенных тройной связью . Это простейший оксид углерода . В координационных комплексах лиганд монооксида углерода называется карбонилом . Это ключевой ингредиент во многих процессах промышленной химии. [5]
Наиболее распространенным источником окиси углерода является частичное сгорание углеродсодержащих соединений. Многочисленные экологические и биологические источники выделяют угарный газ. В промышленности окись углерода играет важную роль в производстве многих соединений, включая лекарства, ароматизаторы и топливо. [6] Выбросы в атмосферу угарного газа влияют на несколько процессов, которые способствуют изменению климата . [7]
Оксид углерода играет важную биологическую роль во всех филогенетических царствах. Его производят многие организмы, в том числе и человек. В физиологии млекопитающих окись углерода является классическим примером гормезиса , при котором низкие концентрации служат эндогенным нейротрансмиттером ( газотрансмиттером ), а высокие концентрации токсичны , приводя к отравлению угарным газом . Он изоэлектронен цианид - аниону CN - .
Люди поддерживают сложные отношения с угарным газом с тех пор, как впервые научились управлять огнем примерно в 800 000 году до нашей эры. Древние люди, вероятно, обнаружили токсичность отравления угарным газом, когда поджигали свои жилища. Раннее развитие металлургии и плавильных технологий, возникшее примерно в 6000 году до нашей эры в бронзовом веке , также пострадало от воздействия угарного газа на человечество. Помимо токсичности угарного газа, коренные индейцы, возможно, испытали на себе нейроактивные свойства угарного газа во время шаманских ритуалов у костра. [8]
Ранние цивилизации разработали мифологические сказки, объясняющие происхождение огня, например, о Прометее из греческой мифологии , который делил огонь с людьми. Аристотель (384–322 до н. э.) впервые зафиксировал, что при горении углей образуются токсичные пары. Греческий врач Гален (129–199 гг. н. э.) предположил, что произошло изменение в составе воздуха, которое причинило вред при вдыхании, и многие другие ученые той эпохи разработали основу знаний об угарном газе в контексте токсичности угольного дыма. Клеопатра, возможно, умерла от отравления угарным газом . [8]
Георг Эрнст Шталь упомянул Carbonarii halitus в 1697 году в связи с токсичными парами, которые считались окисью углерода. Фридрих Гофман провел первое современное научное исследование отравления угарным газом углем в 1716 году. Герман Бурхааве провел первые научные эксперименты по влиянию угарного газа (угольных паров) на животных в 1730-х годах. [8]
Считается, что Джозеф Пристли первым синтезировал угарный газ в 1772 году. Карл Вильгельм Шееле аналогичным образом выделил угарный газ из древесного угля в 1773 году и подумал, что это может быть углеродное вещество, делающее пары токсичными. Торберн Бергман выделил угарный газ из щавелевой кислоты в 1775 году. Позже, в 1776 году, французский химик де Лассон получил CO путем нагревания оксида цинка с коксом , но ошибочно пришел к выводу, что газообразным продуктом был водород , поскольку он горел синим пламенем. В присутствии кислорода, в том числе в атмосферных концентрациях, окись углерода горит синим пламенем с образованием углекислого газа. Антуан Лавуазье провел такие же безрезультатные эксперименты, что и Лассоне, в 1777 году. Уильям Крукшенк в 1800 году идентифицировал газ как соединение, содержащее углерод и кислород . [8] [9]
Томас Беддоуз и Джеймс Уотт в 1793 году признали, что угарный газ (в виде гидрокарбоната ) осветляет венозную кровь. Уотт предположил, что пары угля могут действовать как противоядие от кислорода в крови, а Беддоуз и Уотт также предположили, что гидрокарбонат имеет большее сродство к животной клетчатке, чем к кислороду. в 1796 году. В 1854 году Адриан Шено аналогичным образом предложил угарный газ удалять кислород из крови, а затем окисляться организмом до углекислого газа. [8] Механизм отравления угарным газом широко приписывают Клоду Бернару , в чьих мемуарах, начиная с 1846 года и опубликованных в 1857 году, говорится: «предотвращает превращение артериальной крови в венозную». Феликс Хоппе-Зейлер независимо опубликовал аналогичные выводы в следующем году. [8]
Окись углерода получила признание в качестве важного реагента в 1900-х годах. [5] Три промышленных процесса иллюстрируют его эволюцию в промышленности. В процессе Фишера-Тропша уголь и связанное с ним богатое углеродом сырье преобразуются в жидкое топливо при посредничестве CO. Эта технология, первоначально разработанная в рамках военных усилий Германии, чтобы компенсировать недостаток отечественной нефти, используется и сегодня. Также в Германии было обнаружено, что смесь CO и водорода в сочетании с олефинами дает альдегиды . Этот процесс, называемый гидроформилированием , используется для производства многих крупномасштабных химических веществ, таких как поверхностно-активные вещества , а также специальных соединений, которые являются популярными ароматизаторами и лекарствами. Например , CO используется при производстве витамина А. [10] В третьем важном процессе, приписываемом исследователям из Монсанто , CO соединяется с метанолом, образуя уксусную кислоту . Большая часть уксусной кислоты производится методом Cativa . Гидроформилирование и синтез уксусной кислоты — два из множества процессов карбонилирования .
Оксид углерода является простейшим оксоуглеродом и изоэлектронен другим двухатомным частицам с тройной связью , имеющим 10 валентных электронов, включая цианид- анион, катион нитрозония , монофторид бора и молекулярный азот . Его молярная масса равна 28,0, что, согласно закону идеального газа , делает его немного менее плотным, чем воздух, средняя молярная масса которого равна 28,8.
Углерод и кислород соединены тройной связью , которая состоит из двух пи-связей и одной сигма-связи . Длина связи между атомом углерода и атомом кислорода составляет 112,8 пм . [11] [12] Эта длина связи соответствует тройной связи, как в молекулярном азоте (N 2 ), который имеет аналогичную длину связи (109,76 пм) и почти такую же молекулярную массу . Двойные связи углерод-кислород значительно длиннее: например, в формальдегиде они составляют 120,8 мкм. [13] Точки кипения (82 К) и плавления (68 К) очень похожи на температуры N 2 (77 К и 63 К соответственно). Энергия диссоциации связи, равная 1072 кДж/моль, сильнее, чем у N 2 (942 кДж/моль), и представляет собой самую прочную из известных химических связей. [14]
Основное электронное состояние монооксида углерода является синглетным [15] , поскольку неспаренных электронов нет.
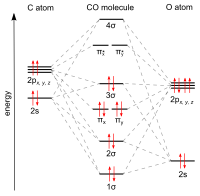
Углерод и кислород вместе имеют в общей сложности 10 электронов в валентной оболочке . Следуя правилу октетов как для углерода, так и для кислорода, два атома образуют тройную связь с шестью общими электронами на трех связывающих молекулярных орбиталях, а не обычную двойную связь, обнаруженную в органических карбонильных соединениях. Поскольку четыре из общих электронов исходят от атома кислорода и только два от углерода, одна связывающая орбиталь занята двумя электронами кислорода, образуя дативную или диполярную связь . Это вызывает поляризацию молекулы C ← O с небольшим отрицательным зарядом углерода и небольшим положительным зарядом кислорода. Каждая из двух других связывающих орбиталей занята одним электроном углерода и одним электроном кислорода, образуя (полярные) ковалентные связи с обратной поляризацией C → O, поскольку кислород более электроотрицательен, чем углерод. В свободной молекуле окиси углерода результирующий отрицательный заряд δ – остается на углеродном конце, и молекула имеет небольшой дипольный момент 0,122 Д. [18]
Таким образом, молекула асимметрична: кислород имеет большую электронную плотность, чем углерод, а также слегка положительно заряжен по сравнению с углеродом, который имеет отрицательный заряд. Напротив, изоэлектронная молекула диазота не имеет дипольного момента.

Рассчитанный дробный порядок связи монооксида углерода равен 2,6, что указывает на то, что «третья» связь важна, но составляет несколько меньшую, чем полная связь. [19] Таким образом, с точки зрения валентной связи, – C≡O + является наиболее важной структурой, в то время как :C=O не является октетной, но имеет нейтральный формальный заряд на каждом атоме и представляет собой второй по важности вкладчик в резонанс. Из-за неподеленной пары и двухвалентности углерода в этой резонансной структуре окись углерода часто считается чрезвычайно стабилизированным карбеном . [20] Изоцианиды — это соединения, в которых O заменен группой NR (R = алкил или арил) и имеют аналогичную схему связей.
Если окись углерода действует как лиганд , полярность диполя может измениться с результирующим отрицательным зарядом на кислородном конце, в зависимости от структуры координационного комплекса . [21] См. также раздел «Координационная химия» ниже.
Теоретические и экспериментальные исследования показывают, что, несмотря на большую электроотрицательность кислорода, дипольный момент направлен от более отрицательного углеродного конца к более положительному кислородному концу. [22] [23] Эти три связи на самом деле представляют собой полярные ковалентные связи , которые сильно поляризованы. Рассчитанная поляризация в сторону атома кислорода составляет 71% для σ-связи и 77% для обеих π-связей . [24]
Степень окисления углерода в угарном газе равна +2 в каждой из этих структур. Он рассчитывается путем подсчета всех связывающих электронов как принадлежащих более электроотрицательному кислороду. Только два несвязывающих электрона углерода принадлежат углероду. В этом случае углерод имеет только два валентных электрона в молекуле по сравнению с четырьмя в свободном атоме.
Окись углерода встречается в различных природных и искусственных средах. Например, при фотохимическом разложении растительных веществ образуется около 60 миллионов тонн в год. [26] Типичные концентрации в частях на миллион следующие:

Оксид углерода (CO) присутствует в небольших количествах (около 80 частей на миллиард) в атмосфере Земли . Большая часть остального приходится на химические реакции с органическими соединениями, выбрасываемыми в результате деятельности человека и природного происхождения в результате фотохимических реакций в тропосфере , которые генерируют около 5 × 10 12 килограммов в год. [34] Другие естественные источники CO включают вулканы, лесные и лесные пожары , а также другие различные формы сгорания, такие как ископаемое топливо . [35] Небольшие количества также выбрасываются из океана и в результате геологической деятельности, поскольку окись углерода растворяется в расплавленной вулканической породе при высоких давлениях в мантии Земли . [36] Поскольку естественные источники окиси углерода меняются из года в год, трудно точно измерить естественные выбросы газа.
Окись углерода оказывает косвенное воздействие на радиационное воздействие за счет повышения концентрации прямых парниковых газов , включая метан и тропосферный озон . CO может вступать в химическую реакцию с другими компонентами атмосферы (в первую очередь с гидроксильным радикалом • OH) , которые в противном случае разрушили бы метан. [37] В результате естественных процессов в атмосфере он окисляется до углекислого газа и озона. Окись углерода недолговечна в атмосфере (средняя продолжительность жизни составляет около одного-двух месяцев), а ее концентрация пространственно варьируется. [38]
Благодаря длительному времени жизни в средней тропосфере окись углерода также используется в качестве индикатора шлейфов загрязняющих веществ. [39]
Оксид углерода является временным загрязнителем атмосферы в некоторых городских районах, главным образом в результате выхлопов двигателей внутреннего сгорания (включая транспортные средства, портативные и резервные генераторы, газонокосилки, моющие машины и т. д.), а также в результате неполного сгорания различных других видов топлива ( включая древесину, уголь, древесный уголь, нефть, парафин, пропан, природный газ и мусор).
Крупные явления загрязнения CO можно наблюдать из космоса над городами. [40]
Угарный газ наряду с альдегидами входит в серию циклов химических реакций, образующих фотохимический смог . Он реагирует с гидроксильным радикалом ( • OH) с образованием промежуточного радикала • HOCO, который быстро переносит свой радикальный водород на O 2 с образованием пероксирадикала (HO 2 • ) и диоксида углерода (CO 2 ). [41] Пероксирадикал впоследствии реагирует с оксидом азота (NO) с образованием диоксида азота (NO 2 ) и гидроксильного радикала. NO 2 дает O( 3 P) посредством фотолиза, тем самым образуя O 3 в результате реакции с O 2 . Поскольку при образовании NO 2 образуется гидроксильный радикал , баланс последовательности химических реакций, начинающихся с оксида углерода и приводящих к образованию озона, таков:
(где hν относится к фотону света, поглощенному молекулой NO 2 в последовательности)
Хотя образование NO 2 является решающим шагом, ведущим к образованию низкого уровня озона , оно также увеличивает содержание озона другим, несколько взаимоисключающим способом, за счет уменьшения количества NO, доступного для реакции с озоном. [42]
В закрытых помещениях концентрация угарного газа может достигать смертельного уровня. В среднем 170 человек в Соединенных Штатах умирают каждый год от угарного газа, выделяемого неавтомобильными потребительскими товарами. [43] К этой продукции относятся неисправные устройства, работающие на топливе, такие как печи, плиты, водонагреватели, а также газовые и керосиновые обогреватели помещений; оборудование с приводом от двигателя, такое как портативные генераторы (и автомобили, оставленные работающими в пристроенных гаражах); камины; и древесный уголь, сжигаемый в домах и других закрытых помещениях. Многие случаи смерти произошли во время отключений электроэнергии из-за суровых погодных условий, таких как ураган Катрина [43] и энергетический кризис в Техасе в 2021 году . [44]
Шахтеры называют угарный газ « белой сыростью » или «тихим убийцей». Его можно найти в закрытых помещениях с плохой вентиляцией как в открытых, так и в подземных шахтах. Наиболее распространенными источниками угарного газа при добыче полезных ископаемых являются двигатели внутреннего сгорания и взрывчатые вещества; однако в угольных шахтах можно обнаружить и окись углерода вследствие низкотемпературного окисления угля. [45] Идиома « Канарейка в угольной шахте » относилась к раннему предупреждению о присутствии угарного газа. [8]
За пределами Земли окись углерода является второй по распространенности двухатомной молекулой в межзвездной среде после молекулярного водорода . Из-за своей асимметрии эта полярная молекула производит гораздо более яркие спектральные линии , чем молекула водорода, что значительно облегчает обнаружение CO. Межзвездный CO был впервые обнаружен с помощью радиотелескопов в 1970 году. Сейчас он является наиболее часто используемым индикатором молекулярного газа вообще в межзвездной среде галактик, поскольку молекулярный водород можно обнаружить только с помощью ультрафиолетового света, для чего необходимы космические телескопы . Наблюдения за угарным газом дают большую часть информации о молекулярных облаках , в которых формируется большинство звезд . [46] [47]
Бета Живописца , вторая по яркости звезда в созвездии Живописца , показывает избыток инфракрасного излучения по сравнению с обычными звездами этого типа, что вызвано большим количеством пыли и газа (в том числе угарного газа) [48] [49] вблизи звезды. .
В атмосфере Венеры угарный газ возникает в результате фотодиссоциации углекислого газа электромагнитным излучением с длиной волны короче 169 нм . Он также был идентифицирован спектроскопически на поверхности спутника Нептуна Тритона . [50]
Твердый угарный газ входит в состав комет . [51] Летучий или «ледяной» компонент кометы Галлея составляет около 15% CO. [52] При комнатной температуре и атмосферном давлении окись углерода на самом деле только метастабильна (см. Реакцию Будуара ), и то же самое справедливо и при низких температурах, когда СО и СО
2тверды, но тем не менее могут существовать в кометах миллиарды лет. В атмосфере Плутона , которая, судя по всему, образовалась из комет, очень мало CO . Это может быть связано с тем, что внутри Плутона есть (или была) жидкая вода.
Оксид углерода может реагировать с водой с образованием углекислого газа и водорода:
Это называется реакцией конверсии вода-газ, когда она протекает в газовой фазе, но она также может происходить (очень медленно) в водном растворе. Если парциальное давление водорода достаточно велико (например, в подземном море), образуется муравьиная кислота :
Эти реакции могут произойти за несколько миллионов лет даже при таких температурах, как на Плутоне. [53]
Оксид углерода имеет широкий спектр функций во всех областях химии. Четыре основные категории реакционной способности включают металл-карбонильный катализ, радикальную химию, химию катионов и анионов . [54]

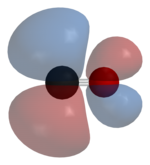
Большинство металлов образуют координационные комплексы , содержащие ковалентно связанную окись углерода. Только металлы в более низких степенях окисления образуют комплексы с лигандами монооксида углерода . Это связано с тем, что должна быть достаточная электронная плотность для облегчения обратного донорства с d xz -орбитали металла на молекулярную орбиталь π * от CO. Неподеленная пара на атоме углерода в CO также передает электронную плотность d x 2 - y 2 на металле, образуя сигма-связь . Это донорство электронов также проявляется в виде цис-эффекта или лабилизации лигандов CO в цис-положении. Карбонил никеля , например, образуется в результате прямого соединения монооксида углерода и металлического никеля :
По этой причине никель в любых трубках или деталях не должен вступать в длительный контакт с окисью углерода. Карбонил никеля легко разлагается обратно на Ni и CO при контакте с горячими поверхностями, и этот метод используется для промышленной очистки никеля в процессе Монда . [55]
В карбониле никеля и других карбонилах электронная пара на углероде взаимодействует с металлом; окись углерода отдает электронную пару металлу. В таких ситуациях окись углерода называется карбонильным лигандом . Одним из важнейших карбонилов металлов является пентакарбонил железа Fe(CO) 5 :
Многие комплексы металл-CO получают путем декарбонилирования органических растворителей, а не из CO. Например, трихлорид иридия и трифенилфосфин реагируют в кипящем 2-метоксиэтаноле или ДМФА с образованием IrCl(CO)(PPh 3 ) 2 .
Карбонилы металлов в координационной химии обычно изучают с помощью инфракрасной спектроскопии .
В присутствии сильных кислот и воды окись углерода реагирует с алкенами с образованием карбоновых кислот в процессе, известном как реакция Коха-Хаафа . [56] В реакции Гаттермана -Коха арены превращаются в производные бензальдегида в присутствии CO, AlCl 3 и HCl . [57] Литийорганические соединения (например, бутиллитий ) реагируют с окисью углерода, но эти реакции имеют мало научного применения.
Хотя CO реагирует с карбокатионами и карбанионами , он относительно инертен по отношению к органическим соединениям без вмешательства металлических катализаторов. [58]
С реагентами основной группы CO вступает в несколько примечательных реакций. Хлорирование CO является промышленным путем получения важного соединения фосгена . С бораном СО образует аддукт H 3 BCO , который изоэлектронен катиону ацетилия [H 3 CCO] + . CO реагирует с натрием с образованием продуктов сочетания C-C, таких как ацетилендиолат натрия 2 Na.+
· С
2О2−
2. Он реагирует с расплавленным калием с образованием смеси металлоорганического соединения - ацетилендиолата калия 2 K.+
· С
2О2−
2, бензолгексолат калия 6 K+
С
6О6−
6, [59] и родизонат калия 2 K+
· С
6О2−
6. [60]
К полимерам монооксида углерода можно отнести соединения циклогексангексон или трихиноил (C 6 O 6 ) и циклопентанпентон или лейконовая кислота (C 5 O 5 ), которые пока получены лишь в следовых количествах. При давлении, превышающем 5 ГПа , окись углерода превращается в поликарбонил , твердый полимер, метастабильный при атмосферном давлении, но взрывоопасный. [61] [62]
Окись углерода удобно получать в лаборатории путем дегидратации муравьиной или щавелевой кислоты , например, концентрированной серной кислотой . [56] [57] [63] Другой метод — нагревание однородной смеси порошкообразного металлического цинка и карбоната кальция , в результате чего выделяется CO и остаются оксид цинка и оксид кальция :
Нитрат серебра и йодоформ также образуют окись углерода:
Наконец, соли оксалатов металлов при нагревании выделяют CO, оставляя карбонат в качестве побочного продукта:
Термическое сжигание является наиболее распространенным источником угарного газа. Окись углерода получается в результате частичного окисления углеродсодержащих соединений; он образуется, когда кислорода недостаточно для образования углекислого газа (CO 2 ), например, при работе печи или двигателя внутреннего сгорания в закрытом помещении.
Большое количество побочного продукта CO образуется в ходе окислительных процессов при производстве химикатов. По этой причине технологические отходящие газы необходимо очищать.
Для производства монооксида углерода было разработано множество методов. [64]
Основным промышленным источником CO является генераторный газ — смесь, содержащая в основном окись углерода и азот, образующаяся при сжигании углерода в воздухе при высокой температуре, когда имеется избыток углерода. В печи воздух пропускают через слой кокса . Первоначально образовавшийся CO 2 уравновешивается с оставшимся горячим углеродом с образованием CO. [65] Реакция CO 2 с углеродом с образованием CO описывается как реакция Будуара . [66] При температуре выше 800 °C преобладающим продуктом является CO:
Другим источником является « водяной газ », смесь водорода и окиси углерода, образующаяся в результате эндотермической реакции пара и углерода:
Другие подобные « синтез-газы » можно получить из природного газа и других видов топлива.
Окись углерода также может быть получена путем высокотемпературного электролиза диоксида углерода в твердооксидных электролизерах . [67] Один метод, разработанный в DTU Energy, использует катализатор на основе оксида церия и не вызывает каких-либо проблем, связанных с загрязнением катализатора. [68] [69]
Окись углерода также является побочным продуктом восстановления металлооксидных руд углеродом , что в упрощенном виде показано следующим образом:
Окись углерода также производится путем прямого окисления углерода в ограниченном количестве кислорода или воздуха.
Поскольку CO представляет собой газ, процесс восстановления можно запустить путем нагревания, используя положительную (благоприятную) энтропию реакции. Диаграмма Эллингема показывает , что при высоких температурах образование CO предпочтительнее, чем CO 2 .
Оксид углерода — это промышленный газ , который имеет множество применений в производстве сыпучих химикатов. [70] Большие количества альдегидов производятся в результате реакции гидроформилирования алкенов , монооксида углерода и H 2 . Гидроформилирование сочетается с процессом получения высших олефинов Shell для получения предшественников моющих средств .
Фосген , полезный для получения изоцианатов, поликарбонатов и полиуретанов, производится путем пропускания очищенного угарного газа и газообразного хлора через слой пористого активированного угля , который служит катализатором . Мировое производство этого соединения оценивалось в 2,74 миллиона тонн в 1989 году. [71]
Метанол получают гидрированием монооксида углерода. В родственной реакции гидрирование моноксида углерода связано с образованием связи C-C, как в процессе Фишера-Тропша , где оксид углерода гидрируется до жидкого углеводородного топлива. Эта технология позволяет превращать уголь или биомассу в дизельное топливо.
В процессе Cativa окись углерода и метанол реагируют в присутствии гомогенного иридиевого катализатора и иодистоводородной кислоты с образованием уксусной кислоты . На этот процесс приходится большая часть промышленного производства уксусной кислоты.
Оксид углерода является сильным восстановителем и с древних времен использовался в пирометаллургии для восстановления металлов из руд . Окись углерода отрывает кислород от оксидов металлов, восстанавливая их до чистого металла при высоких температурах, образуя при этом углекислый газ . Окись углерода обычно не подается в реактор в газообразном виде в чистом виде, а образуется при высокой температуре в присутствии кислородсодержащей руды или углеродосодержащего агента, такого как кокс, и при высокой температуре. Доменный процесс является типичным примером процесса восстановления металла из руды окисью углерода.
Аналогичным образом, доменный газ , собираемый в верхней части доменной печи, по-прежнему содержит от 10% до 30% монооксида углерода и используется в качестве топлива в печах Каупера и печах Сименса-Мартина при мартеновском производстве стали .
Оксид углерода также использовался в качестве лазерной среды в мощных инфракрасных лазерах . [72]
Угарный газ предлагалось использовать в качестве топлива на Марсе. Двигатели на основе угарного газа/кислорода были предложены для раннего использования наземных транспортных средств, поскольку и угарный газ, и кислород могут быть напрямую получены из углекислой атмосферы Марса путем электролиза диоксида циркония , без использования каких-либо ресурсов марсианской воды для получения водорода, который был бы необходим для производства метан или любое топливо на основе водорода. [73]
Окись углерода – это биоактивная молекула, действующая как газообразная сигнальная молекула . Он естественным образом вырабатывается многими ферментативными и неферментативными путями, [74] наиболее изученным из которых является катаболическое действие гемоксигеназы на гем , полученный из гемопротеинов , таких как гемоглобин . [75] После первого сообщения о том, что окись углерода является нормальным нейротрансмиттером в 1993 году, [8] окись углерода привлекла значительное клиническое внимание как биологический регулятор.
Из-за роли угарного газа в организме нарушения его метаболизма связаны с различными заболеваниями, включая нейродегенерацию, гипертонию, сердечную недостаточность и патологическое воспаление. [76] Во многих тканях окись углерода действует как противовоспалительное , сосудорасширяющее средство и стимулирует неоваскулярный рост. [77] В исследованиях на животных окись углерода уменьшала тяжесть экспериментально вызванного бактериального сепсиса , панкреатита, ишемии/реперфузионного повреждения печени, колита, остеоартрита, повреждения легких, отторжения трансплантата легких и нейропатической боли, одновременно способствуя заживлению кожных ран. Таким образом, существует значительный интерес к терапевтическому потенциалу монооксида углерода как фармацевтического агента и клинического стандарта лечения. [78]
Исследования угарного газа проводились во многих лабораториях по всему миру на предмет его противовоспалительных и цитопротекторных свойств. [79] Эти свойства потенциально могут быть использованы для предотвращения развития ряда патологических состояний, включая ишемию-реперфузионное повреждение, отторжение трансплантата, атеросклероз, тяжелый сепсис, тяжелую малярию или аутоиммунитет. [78] Многие фармацевтические инициативы по доставке лекарств разработали методы безопасного введения угарного газа, а последующие контролируемые клинические испытания оценили терапевтический эффект угарного газа. [80]
Микробиота также может использовать окись углерода в качестве газопередатчика . [81] Чувствительность к угарному газу — это сигнальный путь, которому способствуют такие белки, как CooA . [82] [83] [84] Объем биологической роли датчика угарного газа до сих пор неизвестен.
Микробиом человека производит, потребляет и реагирует на окись углерода. [74] Например, у некоторых бактерий окись углерода вырабатывается путем восстановления диоксида углерода ферментом дегидрогеназой моноксида углерода с благоприятной биоэнергетикой для питания последующих клеточных операций. [85] [74] В другом примере окись углерода является питательным веществом для метаногенных архей, которые восстанавливают его до метана с помощью водорода. [86]
Оксид углерода обладает определенными антимикробными свойствами, которые были изучены для лечения инфекционных заболеваний . [74]
Оксид углерода используется в системах упаковки в модифицированной атмосфере в США, в основном для свежих мясных продуктов, таких как говядина, свинина и рыба, чтобы они сохраняли свежий вид. Преимущество двоякое: окись углерода защищает от микробной порчи и улучшает цвет мяса, привлекая потребителя. [87] Окись углерода соединяется с миоглобином , образуя карбоксимиоглобин, ярко-вишнево-красный пигмент. Карбоксимиоглобин более стабилен, чем оксимиоглобин, оксимиоглобин, который может окисляться до коричневого пигмента метмиоглобина . Этот стабильный красный цвет может сохраняться гораздо дольше, чем в обычно упакованном мясе. Типичные уровни угарного газа, используемые на предприятиях, использующих этот процесс, составляют от 0,4% до 0,5%. [87]
Впервые эта технология получила статус « общепризнанной безопасной » (GRAS) Управлением по контролю за продуктами и лекарствами США (FDA) в 2002 году для использования в качестве системы вторичной упаковки и не требует маркировки. В 2004 году FDA одобрило CO в качестве основного метода упаковки, заявив, что CO не маскирует запах порчи. [88] В настоящее время этот процесс несанкционирован во многих других странах, включая Японию, Сингапур и Европейский Союз . [89] [90] [91]
Отравление угарным газом является наиболее распространенным типом смертельного отравления воздуха во многих странах. [92] По оценкам Центров по контролю и профилактике заболеваний , несколько тысяч человек ежегодно обращаются в отделения неотложной помощи больниц для лечения отравления угарным газом. [93] По данным Министерства здравоохранения Флориды , «каждый год более 500 американцев умирают от случайного воздействия угарного газа, и еще тысячам в США требуется неотложная медицинская помощь в случае несмертельного отравления угарным газом». [94] Американская ассоциация центров по контролю за отравлениями (AAPCC) сообщила о 15 769 случаях отравления угарным газом, в результате которых в 2007 году погибло 39 человек. [95] В 2005 году CPSC сообщил о 94 случаях смерти от отравления угарным газом, связанных с генератором. [43]
Угарный газ бесцветен, не имеет запаха и вкуса. Таким образом, его относительно невозможно обнаружить. Он легко соединяется с гемоглобином с образованием карбоксигемоглобина , который потенциально влияет на газообмен ; поэтому воздействие может быть высокотоксичным. Даже такие низкие концентрации, как 667 частей на миллион , могут привести к превращению до 50% гемоглобина организма в карбоксигемоглобин. [96] Уровень карбоксигемоглобина 50% может привести к судорогам, коме и летальному исходу. [97] В Соединенных Штатах OSHA ограничивает уровни долгосрочного воздействия на рабочем месте выше 50 частей на миллион. [98]
Помимо влияния на доставку кислорода, окись углерода также связывается с другими гемопротеинами , такими как миоглобин и митохондриальная цитохромоксидаза , металлическими и неметаллическими клеточными мишенями, влияя на многие клеточные операции.
В древней истории Ганнибал казнил римских пленных дымом угля во время Второй Пунической войны . [8]
Угарный газ использовался для геноцида во время Холокоста в некоторых лагерях смерти , наиболее заметным из которых были газовые фургоны в Хелмно , а также в программе Action T4 « эвтаназия ». [99]
{{cite book}}: CS1 maint: числовые имена: список авторов ( ссылка )Около 80 процентов льда представляет собой водяной лед, а замороженный угарный газ составляет еще 15 процентов.
Описание физиологии угарного газа от Королевского химического общества .