
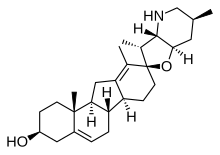
Стероид — это органическое соединение с четырьмя слитыми кольцами (обозначенными A, B, C и D), расположенными в определенной молекулярной конфигурации .
Стероиды выполняют две основные биологические функции: являются важными компонентами клеточных мембран , изменяющими текучесть мембран ; и как сигнальные молекулы . Примеры включают липидный холестерин , половые гормоны эстрадиол и тестостерон , [2] : 10–19 анаболические стероиды и противовоспалительный кортикостероидный препарат дексаметазон . [3] Сотни стероидов обнаружены в грибах , растениях и животных . Все стероиды производятся в клетках из стеринов ланостерина ( опистоконты ) или циклоартенола (растения). Ланостерол и циклоартенол образуются в результате циклизации тритерпенового сквалена . [4]
Стероиды названы в честь стероида холестерина [5] , который был впервые описан в желчных камнях от древнегреческих слов « холе » — « желчь » и «стереос» — «твердый». [6] [7] [8]
Стероидное ядро ( коровая структура ) называется гонаном (циклопентанпергидрофенантрен). [9] Обычно он состоит из семнадцати атомов углерода , связанных в четыре конденсированных кольца: три шестичленных циклогексановых кольца (кольца A, B и C на первой иллюстрации) и одно пятичленное циклопентановое кольцо (кольцо D). Стероиды различаются по функциональным группам , прикрепленным к этому четырехкольцевому ядру, и по степени окисления колец. Стеролы представляют собой формы стероидов с гидроксильной группой в третьем положении и скелетом, полученным из холестана . [1] : 1785f [10] Стероиды также могут быть модифицированы более радикально, например, путем изменения кольцевой структуры, например, путем разрезания одного из колец. Режущее кольцо B производит секостероиды , одним из которых является витамин D3 .


Гонан , также известный как стеран или циклопентанпергидрофенантрен, простейший стероид и ядро всех стероидов и стеринов, [11] [12] состоит из семнадцати атомов углерода в углерод-углеродных связях, образующих четыре слитых кольца в трехмерной форме . Три циклогексановых кольца (A, B и C на первой иллюстрации ) образуют скелет пергидропроизводного фенантрена . Кольцо D имеет циклопентановую структуру. Когда присутствуют две метильные группы и восемь углеродных боковых цепей (в положении C-17, как показано для холестерина), говорят, что стероид имеет холестановый каркас. Две распространенные стереоизомерные формы стероидов 5α и 5β существуют из-за различий в той стороне преимущественно плоской кольцевой системы, к которой присоединен атом водорода (H) при углероде-5, что приводит к изменению конформации A-кольца стероида. Изомеризация боковой цепи C-21 приводит к образованию параллельного ряда соединений, называемых изостероидами. [13]
Примеры стероидных структур:
Помимо разрывов колец (расщеплений), расширений и сжатий (расщепления и повторного замыкания в более крупные или меньшие кольца) — всех вариаций структуры углерод-углеродных связей — стероиды также могут различаться:
Например, стерины, такие как холестерин и ланостерин, имеют гидроксильную группу , присоединенную к положению С-3, тогда как тестостерон и прогестерон имеют карбонильную группу (оксозаместитель) в положении С-3. Среди этих соединений только ланостерин имеет две метильные группы при С-4. Холестерин, имеющий двойную связь от C-5 до C-6, отличается от тестостерона и прогестерона, которые имеют двойную связь от C-4 до C-5.
Почти все биологически значимые стероиды можно представить как производные исходной холестериноподобной углеводородной структуры, служащей скелетом . [14] [15] Эти родительские структуры имеют конкретные названия, такие как прегнан , андростан и т. д. Производные несут различные функциональные группы , называемые суффиксами или префиксами, после соответствующих цифр, указывающих их положение в стероидном ядре. [16] Широко используются тривиальные названия стероидов природного происхождения со значительной биологической активностью, такие как прогестерон , тестостерон или кортизол . Некоторые из этих названий определены в «Номенклатуре стероидов». [17] Эти тривиальные названия также можно использовать в качестве основы для получения новых названий, однако путем добавления только префиксов, а не суффиксов, например, стероид 17α-гидроксипрогестерон имеет гидроксильную группу (-ОН) в положении 17 стероидного ядра. по сравнению с прогестероном.
Буквы α и β [18] обозначают абсолютную стереохимию в хиральных центрах — особую номенклатуру, отличную от соглашения R/S [19] органической химии для обозначения абсолютной конфигурации функциональных групп, известной как правила приоритета Кана-Ингольда-Прелога . Соглашение R/S назначает приоритеты заместителям в хиральном центре на основе их атомного номера. Группа с высшим приоритетом назначается атому с самым высоким атомным номером, а группа с самым низким приоритетом назначается атому с наименьшим атомным номером. Затем молекулу ориентируют так, чтобы группа с наименьшим приоритетом была направлена в сторону от зрителя, а остальные три группы располагались в порядке убывания приоритета вокруг хирального центра. Если это расположение по часовой стрелке, ему присваивается конфигурация R; если против часовой стрелки, ему присваивается конфигурация S. [20] Напротив, в номенклатуре стероидов используются α и β для обозначения стереохимии в хиральных центрах. Обозначения α и β основаны на ориентации заместителей относительно друг друга в конкретной кольцевой системе. В общем, α относится к заместителю, который ориентирован к плоскости кольцевой системы, тогда как β относится к заместителю, который ориентирован от плоскости кольцевой системы. В стероидах, нарисованных со стандартной точки зрения, используемой в этой статье, α-связи изображены на рисунках пунктирными клиньями, а β-связи — сплошными клиньями. [14]
Название « 11-дезоксикортизол » является примером производного названия, в котором кортизол используется в качестве исходной структуры без атома кислорода (отсюда «дезокси»), присоединенного к положению 11 (как часть гидроксигруппы). [14] [21] Нумерация положений атомов углерода в стероидном ядре установлена в шаблоне, найденном в Номенклатуре стероидов [22] , который используется независимо от того, присутствует ли атом в рассматриваемом стероиде. [14]
Ненасыщенные атомы углерода (как правило, входящие в двойную связь) в стероидном ядре обозначаются заменой -ана на -ен. [23] Это изменение традиционно делалось в родительском названии с добавлением префикса для обозначения положения с Δ (греческая заглавная дельта) или без него, который обозначает ненасыщенность, например, 4-прегнен-11β,17α-диол-3,20. -дион (также Δ 4 -прегнен-11β,17α-диол-3,20-дион) или 4-андростен-3,11,17-трион (также Δ 4- андростен-3,11,17-трион). Однако Номенклатура стероидов рекомендует всегда располагать местонахождение двойной связи рядом со слогом, обозначающим ненасыщенность, поэтому использовать его в качестве суффикса, а не префикса, и без использования символа Δ, т.е. прегн-4-. ен-11β,17α-диол-3,20-дион или андрост-4-ен-3,11,17-трион . Двойная связь обозначается атомом углерода с меньшим номером, т.е. «Δ 4- » или «4-ен» означает двойную связь между положениями 4 и 5. Насыщение атомов углерода исходного стероида можно осуществить путем добавления «дигидро» Приставка «-», [24] т.е. насыщение атомов углерода 4 и 5 тестостерона двумя атомами водорода представляет собой 4,5α-дигидротестостерон или 4,5β-дигидротестостерон. Обычно, когда нет двусмысленности, один номер положения водорода стероида с насыщенной связью можно опустить, оставив только положение второго атома водорода, например, 5α-дигидротестостерона или 5β-дигидротестостерона . Δ 5 -стероиды - это стероиды с двойной связью между атомами углерода 5 и 6, а стероиды Δ 4 - это стероиды с двойной связью между атомами углерода 4 и 5. [25] [23]
Такие сокращения, как « P4 » для прогестерона и « A4 » для андростендиона , относятся к Δ4 - стероидам, тогда как « P5 » для прегненолона и « A5 » для андростендиола относятся к Δ5 - стероидам. [14]
Суффикс -ол обозначает гидроксигруппу , а суффикс -он обозначает оксогруппу. Когда две или три одинаковые группы присоединены к базовой структуре в разных положениях, суффикс обозначается как -диол или -триол для гидроксильных групп и -дион или -трион для оксогрупп соответственно. Например, 5α-прегнан-3α,17α-диол-20-он имеет атом водорода в положении 5α (отсюда и префикс «5α-»), две гидроксигруппы (-ОН) в положениях 3α и 17α (отсюда « суффикс «3α,17α-диол») и оксогруппу (=O) в положении 20 (отсюда и суффикс «20-один»). Однако можно встретить ошибочное использование суффиксов, например, «5α-прегнан-17α-диол-3,11,20-трион» [26] [ sic ] — поскольку у него всего одна гидроксигруппа (при 17α), а не две. , то суффикс должен быть -ол, а не -диол, чтобы правильное название было «5α-прегнан-17α-ол-3,11,20-трион».
Согласно правилу, установленному в Номенклатуре стероидов, окончание «е» в названии родительской структуры должно быть опущено перед гласной ( наличие или отсутствие цифры не влияет на такое опущение). [14] [16] Это означает, например, что если суффикс, добавленный непосредственно к имени родительской структуры, начинается с гласной, конечная буква «е» удаляется из этого имени. Примером такого удаления является « 5α-прегнан-17α-ол-3,20-дион », где последняя «е» в слове « прегнан » опускается из-за гласной («о») в начале суффикса — ол. Некоторые авторы неправильно используют это правило, пропуская окончание «е» там, где его следует оставить, или наоборот. [27]
Термин «11-оксигенированный» относится к присутствию атома кислорода в качестве оксо (=O) или гидрокси (-OH) заместителя у углерода 11. «Оксигенированный» постоянно используется в химии стероидов [ 28], поскольку 1950-е годы. [29] В некоторых исследованиях используется термин «11-оксиандрогены» [30] [31] как аббревиатура для 11-оксигенированных андрогенов, чтобы подчеркнуть, что все они имеют атом кислорода, присоединенный к углероду в положении 11. [32] [33] Однако в химической номенклатуре приставка «окси» связана с эфирными функциональными группами, т.е. с соединением , у которого атом кислорода связан с двумя алкильными или арильными группами (ROR), [34] поэтому использование «окси» в названии класс стероидов может вводить в заблуждение. В других областях органической химии можно найти четкие примеры термина «оксигенированный» для обозначения широкого класса органических молекул, содержащих множество кислородсодержащих функциональных групп, [35] , и уместно использовать это соглашение. [14]
Несмотря на то, что «кето» является стандартным префиксом в органической химии, рекомендации Объединенной комиссии по биохимической номенклатуре 1989 года не рекомендуют использовать префикс «кето» для названий стероидов и отдают предпочтение префиксу «оксо» (например, 11-оксостероиды). а не 11-кетостероиды), поскольку «кето» включает углерод, входящий в состав стероидного ядра, и один и тот же атом углерода не следует указывать дважды. [36] [14]
Стероиды встречаются во всех сферах жизни, включая бактерии , археи и эукариоты . У эукариот стероиды встречаются в грибах, растениях и животных. [37] [38]
У прокариот существуют пути биосинтеза тетрациклического стероидного каркаса (например, у миксобактерий ) [39] – где предполагается его происхождение от эукариот [40] – и более распространенного пентациклического тритерпиноидного гопаноидного каркаса. [41]
Грибковые стероиды включают эргостерины , которые участвуют в поддержании целостности клеточной мембраны грибов. Различные противогрибковые препараты , такие как амфотерицин B и азоловые противогрибковые средства , используют эту информацию для уничтожения патогенных грибков. [42] Грибы могут изменять содержание эргостерина (например, за счет потери функции мутаций в ферментах ERG3 или ERG6 , вызывающих истощение эргостерина, или мутаций, которые уменьшают содержание эргостерина) для развития устойчивости к препаратам, нацеленным на эргостерин. [43]
Эргостерин аналогичен холестерину, обнаруженному в клеточных мембранах животных (включая человека), или фитостеринам, содержащимся в клеточных мембранах растений. [43] Все грибы содержат большое количество эргостерина, от десятков до сотен миллиграммов на 100 граммов сухого веса. [43] Кислород необходим для синтеза эргостерина у грибов. [43]
Эргостерин отвечает за содержание витамина D в грибах; Эргостерин химически превращается в провитамин D2 под воздействием ультрафиолетового света . [43] Провитамин D2 спонтанно образует витамин D2. [43] Однако не все грибы используют эргостерин в своих клеточных мембранах; например, патогенный вид грибов Pneumocystis jirovecii этого не делает, что имеет важные клинические последствия (учитывая механизм действия многих противогрибковых препаратов). На примере гриба Saccharomyces cerevisiae другие основные стероиды включают эргоста-5,7,22,24(28)-тетраен-3β-ол, зимостерин и ланостерин . S. cerevisiae использует 5,6-дигидроэргостерин вместо эргостерина в своей клеточной мембране. [43]
Растительные стероиды включают стероидные алкалоиды , обнаруженные у пасленовых [44] и мелантиевых (особенно рода Veratrum ), [ 45] сердечные гликозиды , [46] фитостеролы и брассиностероиды (которые включают несколько растительных гормонов).
Животные стероиды включают соединения позвоночного и насекомого происхождения, причем последние включают экдистероиды, такие как экдистерон (контролирующий линьку у некоторых видов). Примеры позвоночных включают стероидные гормоны и холестерин; последний является структурным компонентом клеточных мембран , который помогает определять текучесть клеточных мембран и является основным компонентом бляшек (участвующих в атеросклерозе ). К стероидным гормонам относятся:
Основными классами стероидных гормонов с известными членами и примерами связанных функций являются: [47] [48]
Дополнительные классы стероидов включают:
А также следующий класс секостероидов (стероиды с открытым кольцом):
Стероиды можно классифицировать по их химическому составу. [49] Один из примеров того, как MeSH выполняет эту классификацию, доступен в каталоге MeSH в Википедии. Примеры этой классификации включают в себя:

В биологии принято называть вышеуказанные классы стероидов по количеству присутствующих атомов углерода, когда речь идет о гормонах: C 18 -стероиды для эстранов (в основном эстрогены), C 19 -стероиды для андростанов (в основном андрогенов) и C 19 -стероиды для эстранов (в основном эстрогенов). 21 -стероиды для прегнанов (в основном кортикостероиды). [50] Классификация « 17-кетостероидов » также важна в медицине.
Гонан (стероидное ядро) представляет собой родительскую молекулу тетрациклического углеводорода с 17 атомами углерода без алкильных боковых цепей. [51]
Секостероиды (лат. seco , «разрезать») представляют собой подкласс стероидных соединений, образующихся биосинтетически или концептуально в результате расщепления (расщепления) родительских стероидных колец (обычно одного из четырех). Основные подклассы секостероидов определяются атомами углерода стероидов, в которых произошло это расщепление. Например, прототип секостероида холекальциферола , витамина D3 ( показан), относится к подклассу 9,10-секостероидов и образуется в результате расщепления атомов углерода C-9 и C-10 стероидного B-кольца; 5,6-секостероиды и 13,14-стероиды схожи. [52]
Норстероиды ( нор- , L.norma ; «нормальный» в химии, указывающий на удаление углерода) [53] и гомостероиды (гомо-, греческий homos ; «тот же», указывающий на присоединение углерода) представляют собой структурные подклассы стероидов, образующихся в результате биосинтетических стадий. Первое включает ферментативные реакции расширения-сокращения кольца , а второе осуществляется ( биомиметически ) или (чаще) посредством замыкания кольца ациклических предшественников с большим (или меньшим) числом атомов в кольце, чем исходный стероидный каркас. [54]
Комбинации этих изменений колец известны в природе. Например, овцы , которые пасутся на кукурузной лилии , потребляют циклопамин (на фото) и вератрамин , два из подсемейства стероидов, у которых C- и D-кольца сжимаются и расширяются соответственно за счет биосинтетической миграции исходного атома C-13. Прием внутрь этих C-nor-D-гомостероидов приводит к врожденным дефектам у ягнят: циклопии из-за циклопамина и деформации ног из-за вератрамина. [55] Еще один C-нор-D-гомостероид (накитерпиозин) выделяется окинавскими цианобактериальными губками . например, Terpios hoshinota , приводящая к гибели кораллов от болезни черных кораллов. [56] Стероиды типа накитерпиозина активны против сигнального пути, включающего сглаженные белки и белки hedgehog , пути, который гиперактивен при ряде видов рака. [ нужна цитата ]
Стероиды и их метаболиты часто функционируют как сигнальные молекулы (наиболее яркими примерами являются стероидные гормоны), а стероиды и фосфолипиды являются компонентами клеточных мембран . [57] Стероиды, такие как холестерин, снижают текучесть мембран . [58] Подобно липидам , стероиды представляют собой высококонцентрированные хранилища энергии. Однако обычно они не являются источниками энергии; у млекопитающих они обычно метаболизируются и выводятся из организма.
Стероиды играют решающую роль в ряде заболеваний, включая злокачественные новообразования, такие как рак простаты , при котором выработка стероидов внутри и снаружи опухоли способствует агрессивности раковых клеток. [59]
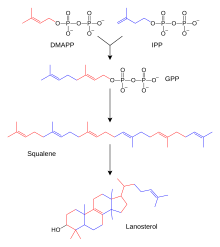
Сотни стероидов, обнаруженных у животных, грибов и растений , состоят из ланостерола (у животных и грибов; см. примеры выше) или циклоартенола (у других эукариот). И ланостерол , и циклоартенол образуются в результате циклизации тритерпеноида сквалена . [4] Ланостерол и циклоартенол иногда называют протостеринами, поскольку они служат исходными соединениями для всех других стероидов.
Биосинтез стероидов — это анаболический путь, при котором стероиды производятся из простых предшественников. У животных наблюдается уникальный путь биосинтеза (по сравнению со многими другими организмами ), что делает этот путь общей мишенью для антибиотиков и других противоинфекционных препаратов. Метаболизм стероидов у человека также является целью препаратов, снижающих уровень холестерина, таких как статины . У людей и других животных биосинтез стероидов происходит по мевалонатному пути, в котором ацетил-КоА используется в качестве строительных блоков для диметилаллилдифосфата (DMAPP) и изопентенилдифосфата (IPP). [60] [ нужен лучший источник ]
На последующих стадиях DMAPP и IPP конъюгируются с образованием фарнезилдифосфата (FPP), который в дальнейшем конъюгируется друг с другом с образованием линейного тритерпеноида сквалена. Биосинтез сквалена катализируется скваленсинтазой , которая принадлежит к семейству сквален/фитоенсинтаз . Последующее эпоксидирование и циклизация сквалена приводят к образованию ланостерола, который является отправной точкой для дополнительных модификаций других стероидов (стероидогенеза). [61] У других эукариот продуктом циклизации эпоксидированного сквалена (оксидосквалена) является циклоартенол.

Мевалонатный путь (также называемый путем ГМГ-КоА-редуктазы) начинается с ацетил-КоА и заканчивается диметилаллилдифосфатом (DMAPP) и изопентенилдифосфатом (IPP).
DMAPP и IPP отдают изопреновые единицы, которые собираются и модифицируются с образованием терпенов и изопреноидов [62] (большой класс липидов, включающий каротиноиды и образующий самый большой класс растительных натуральных продуктов ). [63] Здесь звенья изопрена соединяются, образуя сквален , и сворачиваются в набор колец, образуя ланостерин . [64] Ланостерин затем может быть преобразован в другие стероиды, такие как холестерин и эргостерин . [64] [65]
Два класса препаратов нацелены на мевалонатный путь : статины (например, розувастатин ), которые используются для снижения повышенного уровня холестерина [ 66] и бисфосфонаты (например, золедронат ), которые используются для лечения ряда дегенеративных заболеваний костей. [67]
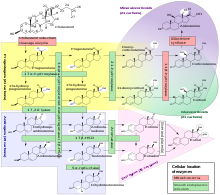
Стероидогенез — это биологический процесс, в ходе которого стероиды образуются из холестерина и превращаются в другие стероиды. [69] Пути стероидогенеза различаются у разных видов . Как отмечалось выше, основными классами стероидных гормонов (с их основными членами и функциями) являются прогестагены , кортикостероиды ( кортикоиды), андрогены и эстрогены . [25] [70] Человеческий стероидогенез этих классов происходит в ряде мест:
У растений и бактерий немевалонатный путь (путь MEP) использует пируват и глицеральдегид-3-фосфат в качестве субстратов для производства IPP и DMAPP. [62] [75]
Во время заболеваний могут использоваться пути, которые в противном случае не имели бы существенного значения для здоровых людей. Например, при одной из форм врожденной гиперплазии надпочечников дефицит ферментативного пути 21-гидроксилазы приводит к избытку 17α-гидроксипрогестерона (17-ОНР) – этот патологический избыток 17-ОНР, в свою очередь, может превращаться в дигидротестостерон (ДГТ, мощный андроген), среди прочего, через 17,20 лиазу (член семейства ферментов цитохрома P450 ), 5α-редуктазу и 3α-гидроксистероиддегидрогеназу . [76]
Стероиды в первую очередь окисляются ферментами оксидазы цитохрома P450 , такими как CYP3A4 . Эти реакции вводят кислород в стероидное кольцо, позволяя другим ферментам расщеплять холестерин на желчные кислоты. [77] Эти кислоты затем могут быть выведены из печени с желчью . [78] Экспрессия гена оксидазы может усиливаться с помощью стероидного датчика PXR при высокой концентрации стероидов в крови. [79] Стероидные гормоны, лишенные боковой цепи холестерина и желчных кислот, обычно гидроксилируются в различных положениях кольца или окисляются в положении 17 , конъюгируются с сульфатом или глюкуроновой кислотой и выводятся с мочой. [80]
Выделение стероидов , в зависимости от контекста, представляет собой выделение химического вещества, необходимого для выяснения химической структуры , химического получения или деградации, биологических испытаний и других исследовательских нужд (обычно от миллиграммов до граммов, но часто и больше [81] или выделение «аналитических величин». » интересующего вещества (когда основное внимание уделяется идентификации и количественному определению вещества (например, в биологической ткани или жидкости). Выделенное количество зависит от аналитического метода, но обычно составляет менее одного микрограмма. [82 ] [ страница нужный ]
Методы выделения для получения продукта двух масштабов различны, но включают экстракцию , осаждение, адсорбцию , хроматографию и кристаллизацию . В обоих случаях выделенное вещество очищают до химической однородности; комбинированные методы разделения и аналитические методы, такие как ЖХ-МС , выбраны как «ортогональные» — их разделение основано на различных способах взаимодействия между веществом и изолирующей матрицей — для обнаружения одного вида в чистом образце.
Определение структуры относится к методам определения химической структуры изолированного чистого стероида с использованием развивающегося набора химических и физических методов, которые включают ЯМР и кристаллографию малых молекул . [2] : 10–19 Методы анализа перекрывают обе вышеуказанные области, уделяя особое внимание аналитическим методам определения присутствия стероида в смеси и определению его количества. [82]
Микробный катаболизм боковых цепей фитостеринов приводит к образованию стероидов C-19, стероидов C-22 и 17-кетостероидов (т.е. предшественников адренокортикальных гормонов и противозачаточных средств ). [83] [84] [85] Добавление и модификация функциональных групп является ключевым моментом при производстве широкого спектра лекарств, доступных в рамках этой химической классификации. Эти модификации осуществляют с использованием традиционных методов органического синтеза и/или биотрансформации . [86] [87]
Полусинтез стероидов часто начинается с таких предшественников, как холестерин , [85] фитостеролы , [ 84] или сапогенины . [88] Компания Syntex , занимающаяся торговлей мексиканскими барбаско , использовала Dioscorea mexicana для производства сапогенина диосгенина на заре фармацевтической промышленности синтетических стероидов . [81]
Некоторые стероидные гормоны экономически выгодно получать только путем полного синтеза из продуктов нефтехимии (например, 13- алкилстероиды ). [85] Например, фармацевтический препарат Норгестрел начинается с метокси - 1-тетралона , нефтехимического продукта, полученного из фенола .
За исследования стероидов был присужден ряд Нобелевских премий , в том числе:
В эту статью включен текст, доступный по лицензии CC BY-SA 3.0.
«Je nommerai cholesterine , de χολη, желчь, et στερεος, Solide, la вещество cristallisée des Calculs biliares humanes,...» (назову холестерин – от χολη (желчь) и στερεος (твердое) – кристаллизованное вещество из желчных камней человека ... )
Структурной основой стероида является стерановое ядро, полициклический стерановый скелет С17, состоящий из трех конденсированных циклогексановых колец в нелинейном или фенантреновом соединении (А, Б и С), и циклопентанового кольца (Г).1,2
3S-1,0.
Определение стероидов и стеролов.
Стероиды представляют собой соединения, имеющие скелет циклопента[а]фенантрена или скелет, полученный из него в результате одного или нескольких разрывов связей или расширения или сжатия кольца.
Метильные группы обычно присутствуют при C-10 и C-13.
Алкильная боковая цепь также может присутствовать у C-17.
Стеролы — это стероиды, несущие гидроксильную группу при С-3 и большую часть скелета холестана.
3С-4.
ФУНКЦИОНАЛЬНЫЕ ГРУППЫ.
3С-4.0.
Общий.
Почти все биологически важные стероиды являются производными исходных углеводородов (см. табл. 1), несущими различные функциональные группы.
[...] К названию насыщенной или ненасыщенной родительской системы добавляются суффиксы (см. 33-2.5), при этом окончание e в -ane, -ene, -yne, -adiene и т. д. опускается перед гласной (наличие или отсутствие цифр не влияет на такие исключения).
3S-4.9.
Тривиальные названия важных стероидов. Примеры тривиальных названий, сохранившихся для важных производных стероидов, которые в основном представляют собой природные соединения, обладающие значительной биологической активностью, приведены в таблице 2.
3S-1.4.
Ориентация формул проекции.
Когда кольца стероида обозначаются как проекции на плоскость бумаги, формулу обычно следует ориентировать, как в пункте 2а.
Атом или группа, прикрепленная к кольцу, изображенному в ориентации 2а, называется α (альфа), если он находится ниже плоскости бумаги, или β (бета), если он лежит над плоскостью бумаги.
P-91.2.1.1 Стереодескрипторы Кана-Ингольда-Прелога (CIP). Некоторые стереодескрипторы, описанные в системе приоритетов Кана-Ингольда-Прелога (CIP), называемые «стереодескрипторы CIP», рекомендуются для определения конфигурации органических соединений, как описано и показано на примерах в этой главе и применяется в главах с P-1 по P-8. и в номенклатуре натуральных продуктов в главе П-10. В качестве предпочтительных стереодескрипторов используются следующие стереодескрипторы (см. P-92.1.2): (a) «R» и «S» для обозначения абсолютной конфигурации тетракоординатных (квадрилигантных) центров хиральности;
P-13.8.1.1 Префикс «de» (не «des»), за которым следует название группы или атома (кроме водорода), означает удаление (или потерю) этой группы и добавление необходимых атомов водорода. , т. е. обмен этой группы на атомы водорода. В виде исключения, «дезокси» применительно к гидроксисоединениям означает удаление атома кислорода из группы –OH с повторным присоединением атома водорода. «Дезокси» широко используется в качестве субтрактивного префикса в номенклатуре углеводов (см. P-102.5.3).
3С-1.1.
Нумерация и кольцевые буквы.
Стероиды пронумерованы, а кольца обозначены буквами, как в формуле 1.
3S-2,5 Ненасыщенность.
Ненасыщенность обозначается заменой -ана на -ен, -адиен, -ин и т. д. или -ан- на -ен-, -адиен-, -ин- и т. д. Примеры: Андрост-5-ен, а не 5-андростен;
5α-холест-6-ен;
5β-холеста-7,9(11)-диен;
5α-холест-6-ен-3β-ол.
Примечания.
1) Теперь рекомендуется, чтобы локант двойной связи всегда находился рядом со слогом, обозначающим ненасыщенность.[...] 3) Не рекомендуется использовать символ Δ (греческая заглавная дельта) для обозначения ненасыщенности в отдельных именах.
Однако его можно использовать и в общих терминах, например, «Δ
5
-стероиды».
П-31.2.2 Общая методология. Префиксы «гидро» и «дегидро» связаны с гидрированием и дегидрированием двойной связи соответственно; таким образом, умножающие префиксы четных значений, такие как «ди», «тетра» и т. д., используются для обозначения насыщения двойной связи (связей), например «дигидро», «тетрагидро»; или создание двойных (или тройных) связей, как «дидегидро» и т. д. В названиях они ставятся непосредственно перед названием родительского гидрида и перед любыми неотделяемыми префиксами. Указанные атомы водорода имеют приоритет над префиксами «гидро» для низких локантов. Если в названии присутствуют указанные атомы водорода, им предшествует префикс «гидро».
окси* –О– П-15.3.1.2.1.1; П-63.2.2.1.1
Префикс оксо- также следует использовать в сочетании с общими терминами, например, 17-оксостероиды.
Термин «17-кетостероиды», часто используемый в медицинской литературе, неверен, поскольку C-17 указывается дважды, поскольку термин «кето» обозначает C=O.