Анаболические стероиды , также известные как анаболически-андрогенные стероиды (ААС), представляют собой класс препаратов, которые структурно родственны тестостерону , основному мужскому половому гормону , и оказывают действие путем связывания с андрогенными рецепторами . Анаболические стероиды имеют ряд медицинских применений [1] , но также используются спортсменами для увеличения размера мышц, силы и производительности.
Риск для здоровья может быть вызван длительным применением или чрезмерными дозами ААС. [2] [3] Эти эффекты включают вредные изменения уровня холестерина (повышение уровня липопротеинов низкой плотности и снижение уровня липопротеинов высокой плотности ), прыщи , высокое кровяное давление , повреждение печени (в основном при приеме большинства пероральных ААС) и гипертрофию левого желудочка . [4] Эти риски еще больше увеличиваются, когда спортсмены принимают стероиды вместе с другими препаратами, что наносит значительно больший вред их организму. [5] Влияние анаболических стероидов на сердце может вызвать инфаркт миокарда и инсульты. [5] Состояния, связанные с гормональным дисбалансом, такие как гинекомастия и уменьшение размера яичек, также могут быть вызваны ААС. [6] У женщин и детей ААС могут вызывать необратимую маскулинизацию . [6]
Эргогенное использование ААС в спорте, гонках и бодибилдинге в качестве препаратов, повышающих работоспособность, является спорным из-за их побочных эффектов и возможности получить преимущество в физических соревнованиях. Их использование считается допингом и запрещено большинством крупных спортивных организаций. Спортсмены искали препараты для улучшения своих спортивных способностей с момента начала Олимпийских игр в Древней Греции. [5] На протяжении многих лет ААС были наиболее часто выявляемыми допинговыми веществами в лабораториях, аккредитованных МОК . [7] [8] Во многих странах анаболические стероиды классифицируются как контролируемые вещества Списка III. [9] В странах, где ААС являются контролируемыми веществами , часто существует черный рынок , на котором потребителям продаются контрабандные, тайно изготовленные или даже поддельные лекарства .

С момента открытия и синтеза тестостерона в 1930-х годах врачи использовали ААС для многих целей с разной степенью успеха. В общих чертах их можно сгруппировать по анаболическим, андрогенным и другим видам применения.

Большинство потребителей стероидов не являются спортсменами. [50] Считается, что в Соединенных Штатах от 1 до 3 миллионов человек (1% населения) использовали ААС. [51] Исследования, проведенные в Соединенных Штатах, показали, что потребителями ААС, как правило, являются в основном мужчины среднего класса со средним возрастом около 25 лет, которые не являются конкурентоспособными бодибилдерами и не спортсменами и используют препараты в косметических целях. [52] «Среди мальчиков в возрасте от 12 до 17 лет употребление стероидов и подобных препаратов выросло на 25 процентов с 1999 по 2000 год, причем 20 процентов заявили, что используют их для красоты, а не для занятий спортом, согласно исследованию страховой компании Blue Cross Blue Shield. (Эйзенхауэр) Другое исследование показало, что немедицинское использование ААС среди студентов колледжей составляло или менее 1%. [53] Согласно недавнему опросу, 78,4% потребителей стероидов были неконкурентными бодибилдерами и неспортсменами, в то время как около 13% сообщили о небезопасных методах инъекций, таких как повторное использование игл, совместное использование игл и совместное использование многодозовых флаконов, [54] хотя исследование 2007 года обнаружили, что совместное использование игл было крайне редким явлением среди лиц, использующих ААС в немедицинских целях, менее 1%. [55] Другое исследование 2007 года показало, что 74% немедицинских пользователей ААС имели высшее образование, большее число окончило колледж и меньшее число не окончило среднюю школу, чем ожидается от населения в целом. [55] То же исследование показало, что люди, использующие ААС в немедицинских целях, имели более высокий уровень занятости и более высокий семейный доход, чем население в целом. [55] Потребители ААС склонны изучать наркотики, которые они принимают, больше, чем другие потребители контролируемых веществ; [ нужна ссылка ] Однако основные источники, к которым обращаются потребители стероидов, включают друзей, немедицинские справочники, интернет-форумы, блоги и журналы о фитнесе, которые могут предоставлять сомнительную или неточную информацию. [56]
Пользователи ААС, как правило, недовольны тем, что в средствах массовой информации и в политике ААС изображают как смертоносное вещество. [57] Согласно одному исследованию, пользователи ААС также не доверяют своим врачам, и в выборке 56% не сообщили своим врачам о своем использовании ААС. [58] Другое исследование 2007 года дало аналогичные результаты: в то время как 66% людей, использующих ААС в немедицинских целях, были готовы обратиться за медицинским наблюдением по поводу употребления стероидов, 58% не доверяли своим врачам, 92% считали, что медицинское наблюдение Знания сообщества о немедицинском использовании ААС отсутствовали, и 99% считали, что общественность имеет преувеличенное представление о побочных эффектах использования ААС. [55] Недавнее исследование также показало, что длительные пользователи ААС с большей вероятностью имели симптомы мышечной дисморфии , а также продемонстрировали более сильную поддержку более традиционных мужских ролей. [59] Недавнее исследование, опубликованное в Журнале психологии здоровья, показало, что многие пользователи считают, что стероиды, используемые в умеренных количествах, безопасны. [60]
ААС использовались мужчинами и женщинами во многих видах профессионального спорта для достижения конкурентного преимущества или для помощи в восстановлении после травм. К этим видам спорта относятся бодибилдинг , тяжелая атлетика , толкание ядра и другие виды легкой атлетики , велоспорт , бейсбол , борьба , смешанные единоборства , бокс , футбол и крикет . Такое использование запрещено правилами руководящих органов большинства видов спорта. Употребление ААС встречается среди подростков, особенно среди тех, кто занимается соревновательными видами спорта. Было высказано предположение, что распространенность употребления наркотиков среди старшеклассников в США может достигать 2,7%. [61]
ААС, которые чаще всего используются в медицине, — это тестостерон и его многочисленные эфиры (но чаще всего ундеканоат тестостерона , энантат тестостерона , ципионат тестостерона и пропионат тестостерона ), [71] эфиры нандролона (обычно деканоат нандролона и фенилпропионат нандролона ), станозолол , и метандиенон (метандростенолон). [72] Другие, которые также были доступны и широко использовались, но в меньшей степени, включают метилтестостерон , оксандролон , местеролон и оксиметолон , а также пропионат дростанолона (пропионат дромостанолона), сложные эфиры метенолона (метиландростенолона) (в частности , ацетат метенолона и энантат метенолона ) . и флюоксиместерон . [72] Дигидротестостерон (ДГТ), известный как андростанолон или станолон при использовании в медицине, и его эфиры также заслуживают внимания, хотя они не получили широкого применения в медицине. [67] Болденона ундециленат и тренболона ацетат используются в ветеринарной медицине . [72]
Дизайнерские стероиды — это ААС, которые не были одобрены и проданы для медицинского использования, но распространяются на черном рынке. [73] Примеры известных дизайнерских стероидов включают 1-тестостерон (дигидроболденон), метастерон , энантат тренболона , дезоксиметилтестостерон , тетрагидрогестринон и метилстенболон . [73]

Существует четыре распространенных формы приема ААС: таблетки для перорального применения; инъекционные стероиды; кремы/гели для местного применения; и пятна на коже. Пероральное введение является наиболее удобным. Тестостерон, принимаемый перорально, быстро всасывается, но в значительной степени превращается в неактивные метаболиты, и только около одной шестой доступна в активной форме. Чтобы быть достаточно активными при пероральном приеме, производные тестостерона алкилируются в положении 17α, например метилтестостерон и флюоксиместерон . Эта модификация снижает способность печени расщеплять эти соединения до того, как они попадут в системный кровоток.
Тестостерон можно вводить парентерально , но он имеет более нерегулярное, продолжительное время всасывания и большую активность в мышцах в форме энантата , ундеканоата или сложного эфира ципионата . Эти производные гидролизуются с высвобождением свободного тестостерона в месте инъекции; Скорость абсорбции (и, следовательно, график инъекций) варьируется в зависимости от разных эфиров, но медицинские инъекции обычно проводятся где-то от полунедели до одного раза в 12 недель. Может быть желательным более частый график, чтобы поддерживать более постоянный уровень гормона в организме. [74] Инъекционные стероиды обычно вводятся в мышцу, а не в вену, чтобы избежать резких изменений количества препарата в кровотоке. Кроме того, поскольку сложный эфир тестостерона растворен в масле, внутривенная инъекция может вызвать опасную эмболию (сгусток) в кровотоке.
Трансдермальные пластыри (клеевые пластыри, наносимые на кожу) также можно использовать для доставки постоянной дозы через кожу в кровоток. Также доступны кремы и гели, содержащие тестостерон, которые ежедневно наносятся на кожу, но абсорбция неэффективна (примерно 10%, в зависимости от человека), и эти методы лечения, как правило, более дорогие. Лица, которые особенно физически активны и/или часто принимают ванну, могут быть неподходящими кандидатами, поскольку лекарство можно смыть, и для полного впитывания может потребоваться до шести часов. Существует также риск того, что интимный партнер или ребенок могут коснуться места нанесения препарата и случайно получить дозу препарата; дети и женщины очень чувствительны к тестостерону, и у них может развиться непреднамеренная маскулинизация и последствия для здоровья даже при приеме небольших доз. Инъекции – наиболее распространенный метод, используемый лицами, вводящими ААС в немедицинских целях. [55]
Традиционные пути введения не оказывают дифференцированного влияния на эффективность препарата. Исследования показывают, что анаболические свойства ААС относительно схожи, несмотря на различия в фармакокинетических принципах, таких как метаболизм первого прохождения . Однако перорально доступные формы ААС могут вызывать повреждение печени в высоких дозах. [8] [75]
Известные возможные побочные эффекты ААС включают: [6] [76] [77] [78] [79]
В зависимости от продолжительности употребления наркотиков существует вероятность повреждения иммунной системы. Большинство этих побочных эффектов являются дозозависимыми, наиболее частым из них является повышение артериального давления , особенно у пациентов с уже существующей гипертонией . [86] Помимо морфологических изменений сердца, которые могут оказывать постоянное неблагоприятное воздействие на эффективность сердечно-сосудистой системы.
Было показано, что ААС изменяют уровень сахара в крови натощак и тесты на толерантность к глюкозе. [87] ААС, такие как тестостерон, также повышают риск сердечно-сосудистых заболеваний [2] или ишемической болезни сердца . [88] [89] Акне довольно распространено среди пользователей ААС, в основном из-за стимуляции сальных желез повышенным уровнем тестостерона. [7] [90] Преобразование тестостерона в ДГТ может ускорить темпы преждевременного облысения у генетически предрасположенных мужчин, но сам тестостерон может вызвать облысение у женщин. [91]
При использовании ААС подростками может возникнуть ряд серьезных побочных эффектов. Например, ААС могут преждевременно остановить удлинение костей (преждевременное сращение эпифизов из-за повышения уровня метаболитов эстрогена ), что приводит к задержке роста . Другие эффекты включают, помимо прочего, ускоренное созревание костей , увеличение частоты и продолжительности эрекций, а также преждевременное половое развитие. Использование ААС в подростковом возрасте также коррелирует с плохим отношением к здоровью. [92]
Организация ВОЗ, Международное агентство по изучению рака (IARC), отнесла ААС к Группе 2А : Вероятно, канцерогенно для человека. [93]
Другие побочные эффекты могут включать изменения в структуре сердца , такие как увеличение и утолщение левого желудочка , что ухудшает его сокращение и расслабление и, следовательно, уменьшает объем выбрасываемой крови. [4] Возможными последствиями этих изменений в сердце являются гипертония, сердечные аритмии , застойная сердечная недостаточность , сердечные приступы и внезапная сердечная смерть . [94] Эти изменения также наблюдаются у спортсменов , не употребляющих наркотики , но использование стероидов может ускорить этот процесс. [95] [96] Однако как связь между изменениями в структуре левого желудочка и снижением сердечной функции, так и связь с употреблением стероидов оспаривается. [97] [98]
Использование ААС может вызвать вредные изменения уровня холестерина : некоторые стероиды вызывают повышение уровня холестерина ЛПНП и снижение уровня холестерина ЛПВП . [99]
Использование ААС у подростков ускоряет созревание костей и может снизить рост взрослых в высоких дозах. [ нужна цитация ] Низкие дозы ААС, такие как оксандролон, используются при лечении идиопатической низкорослости , но это может только ускорить взросление, а не увеличить рост взрослого человека. [100]
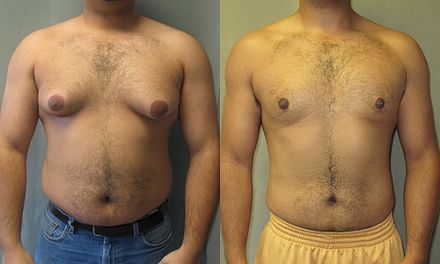
Хотя все анаболические стероиды обладают андрогенным действием, некоторые из них парадоксальным образом приводят к феминизации, например, ткани молочной железы у мужчин, состоянию, называемому гинекомастией . Эти побочные эффекты вызваны естественным превращением тестостерона в эстроген и эстрадиол под действием фермента ароматазы . [101]
Длительное использование андрогенно-анаболических стероидов мужчинами приводит к временному прекращению естественного производства тестостерона из-за ингибирования оси гипоталамус-гипофиз-гонады . Это проявляется в атрофии яичек , угнетении выработки спермы , половой функции и бесплодии . [102] [103] [104] Кратковременное (1–2 месяца) применение андрогенно-анаболических стероидов мужчинами с последующим курсом терапии, повышающей уровень тестостерона (например, кломифена и хорионического гонадотропина человека ), обычно приводит к возвращению к нормальной выработке тестостерона. . [105] )
Побочные эффекты, характерные для женщин, включают увеличение волос на теле , постоянное понижение голоса, увеличение клитора и временное снижение менструальных циклов . Изменение фертильности и кисты яичников также могут возникать у женщин. [106] При приеме во время беременности ААС могут влиять на развитие плода , вызывая развитие мужских признаков у плода женского пола и женских признаков у плода мужского пола. [107]
Анализы почек показали, что у девяти из десяти потребителей стероидов развилось заболевание, называемое фокально-сегментарным гломерулосклерозом , тип рубцов внутри почек. Повреждения почек у бодибилдеров аналогичны тем, которые наблюдаются у пациентов с морбидным ожирением, но кажутся еще более серьезными. [108]
Высокие дозы пероральных соединений ААС могут вызвать повреждение печени . [3] Пелиоз печени все чаще выявляют при использовании ААС.

Обзор 2005 года, опубликованный в журнале CNS Drugs, показал, что «значительные психиатрические симптомы, включая агрессию и насилие, манию , реже психоз и самоубийство, связаны со злоупотреблением стероидами . У лиц, длительное время злоупотребляющих стероидами, могут развиться симптомы зависимости и абстиненции после прекращения приема ААС». [81] Высокие концентрации ААС, сравнимые с теми, которые, вероятно, поддерживаются многими рекреационными потребителями ААС, вызывают апоптотические эффекты на нейроны , [ нужна цитация ] повышая вероятность возможной необратимой нейротоксичности. Рекреационное использование ААС, по-видимому, связано с рядом потенциально длительных психических последствий, включая синдромы зависимости, расстройства настроения и переход к другим формам употребления психоактивных веществ, но распространенность и тяжесть этих различных эффектов остаются плохо изученными. [110] Нет никаких доказательств того, что стероидная зависимость развивается в результате терапевтического использования ААС для лечения заболеваний, но случаи зависимости от ААС были зарегистрированы среди штангистов и бодибилдеров, которые постоянно принимали супрафизиологические дозы. [111] Нарушения настроения (например, депрессия, [гипо-]мания, психотические проявления), вероятно, зависят от дозы и препарата, но зависимость от ААС или эффекты отмены, по-видимому, возникают только у небольшого числа пользователей ААС. [7] Крупномасштабные долгосрочные исследования психиатрического воздействия на потребителей ААС в настоящее время недоступны. [110]
В DSM-IV перечислены общие диагностические критерии для рекомендаций по расстройствам личности: «Этот образец не следует лучше объяснять проявлением другого психического расстройства или прямым физиологическим воздействием вещества (например, лекарства или лекарства) или общим заболеванием. (например, травма головы).». В результате потребители ААС могут получить неверный диагноз у психиатра, не сообщившего об их привычке. [112]
Купер, Ноукс, Данн, Ламберт и Рочфорд установили, что лица, использующие ААС, с большей вероятностью наберут более высокие баллы пограничного ( 4,7 раза), антисоциального (3,8 раза), параноидального (3,4 раза), шизотипического (3,1 раза) и истерического (2,9 раза) характера. раз), пассивно-агрессивный (2,4 раза) и нарциссический (1,6 раза) профили личности, чем непользователи. [113] Другие исследования показали, что антисоциальное расстройство личности несколько более вероятно среди пользователей ААС, чем среди тех, кто не употребляет их (Pope & Katz, 1994). [112] Биполярная дисфункция, [114] зависимость от психоактивных веществ и расстройство поведения также были связаны с использованием ААС. [115]
Аффективные расстройства уже давно признаны осложнением применения ААС. В отчетах о случаях описываются как гипомания, так и мания, а также раздражительность, восторг, безрассудство, скачок мыслей и чувство силы и непобедимости, которые не соответствуют критериям мании/гипомании. [116] Из 53 бодибилдеров, принимавших ААС, 27 (51%) сообщили о неуказанных нарушениях настроения. [117]
С середины 1980-х годов средства массовой информации сообщали о «роидной ярости» как о побочном эффекте ААС. [118] : 23
Обзор 2005 года показал, что некоторые, но не все, рандомизированные контролируемые исследования показали, что использование ААС коррелирует с гипоманией и повышенной агрессивностью, но указало, что попытки определить, вызывает ли использование ААС агрессивное поведение, не увенчались успехом, в первую очередь из-за высокого уровня не- участие. [119] Исследование, проведенное в 2008 году на общенациональной репрезентативной выборке молодых взрослых мужчин в Соединенных Штатах, выявило связь между употреблением ААС в течение всей жизни и за последний год, о которых они сами сообщали, и участием в насильственных действиях. По сравнению с лицами, не принимавшими стероиды, молодые взрослые мужчины, принимавшие ААС, сообщали о большей склонности к агрессивному поведению даже после учета влияния ключевых демографических переменных, предыдущего агрессивного поведения и полинаркомании. [120] Обзор 1996 года, посвященный слепым исследованиям, доступным на тот момент, также показал, что они продемонстрировали связь между агрессией и употреблением стероидов, но указывал, что, по оценкам, в то время в Соединенных Штатах насчитывалось более одного миллиона прошлых или нынешних потребителей стероидов. , чрезвычайно небольшой процент тех, кто употребляет стероиды, по-видимому, испытали психические расстройства, достаточно серьезные, чтобы привести к клиническому лечению или отчетам о медицинских случаях. [121]
Связь между употреблением ААС и депрессией неубедительна. Обзор 1992 года [ требует обновления ] показал, что ААС могут как облегчить, так и вызвать депрессию, и что прекращение или уменьшение использования ААС также может привести к депрессии, но из-за разрозненных данных потребовалось проведение дополнительных исследований. [122]
Андрогены , такие как тестостерон , андростендион и дигидротестостерон , необходимы для развития органов мужской репродуктивной системы , включая семенные пузырьки , придатки яичек , семявыносящие протоки , половой член и простату . [123] ААС — это производные тестостерона, разработанные для максимизации анаболического эффекта тестостерона. [72] ААС потребляют элитные спортсмены, соревнующиеся в таких видах спорта , как тяжелая атлетика , бодибилдинг и легкая атлетика . [124] Мужчины-спортсмены-любители принимают ААС для достижения «улучшенного» внешнего вида . [125]
Потребление ААС нарушает работу гипоталамо-гипофизарно-гонадной оси (ось HPG) у мужчин. [123] В оси HPG гонадотропин-рилизинг-гормон (ГнРГ) секретируется из дугообразного ядра гипоталамуса и стимулирует переднюю долю гипофиза секретировать два гонадотропина : фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). [126] У взрослых мужчин ЛГ стимулирует клетки Лейдига в семенниках вырабатывать тестостерон, который необходим для образования новых сперматозоидов посредством сперматогенеза . [123] Потребление ААС приводит к дозозависимому подавлению высвобождения гонадотропинов за счет подавления ГнРГ из гипоталамуса (механизм с длинной петлей) или за счет прямой отрицательной обратной связи с передней долей гипофиза для ингибирования высвобождения гонадотропинов (механизм с короткой петлей), что приводит к развитию ААС. -индуцированный гипогонадизм . [123]
Фармакодинамика ААС отличается от пептидных гормонов . Водорастворимые пептидные гормоны не могут проникнуть через мембрану жировых клеток и лишь опосредованно воздействуют на ядра клеток- мишеней посредством взаимодействия с поверхностными рецепторами клетки . Однако, как жирорастворимые гормоны, ААС мембранопроницаемы и влияют на ядра клеток прямым действием. Фармакодинамическое действие ААС начинается, когда экзогенный гормон проникает через мембрану клетки-мишени и связывается с андрогенным рецептором (АР), расположенным в цитоплазме этой клетки. Оттуда составной гормон-рецептор диффундирует в ядро, где либо изменяет экспрессию генов [ 128] , либо активирует процессы, которые посылают сигналы в другие части клетки. [129] Различные типы ААС связываются с ААР с разным сродством , в зависимости от их химической структуры. [7]
Влияние ААС на мышечную массу обусловлено как минимум двумя способами: [130] во-первых, они увеличивают выработку белков ; во-вторых, они сокращают время восстановления, блокируя воздействие гормона стресса кортизола на мышечную ткань, в результате чего катаболизм мышц значительно снижается. Была выдвинута гипотеза , что такое снижение распада мышц может происходить за счет ингибирования ААС действия других стероидных гормонов, называемых глюкокортикоидами , которые способствуют распаду мышц. [61] ААС также влияют на количество клеток, которые развиваются в клетки-накопители жира, вместо этого способствуя клеточной дифференцировке в мышечные клетки. [131]
Анаболические стероиды взаимодействуют с АР в различных тканях, включая мышцы, кости и репродуктивную систему. [132] При связывании с AR анаболические стероиды запускают транслокацию комплекса гормон-рецептор в ядро клетки, где они либо изменяют экспрессию генов, либо активируют клеточные сигнальные пути; это приводит к увеличению синтеза белка, усилению мышечного роста и снижению мышечного катаболизма. [133]
Анаболические стероиды влияют на клеточную дифференциацию, благоприятствуя развитию мышечных клеток, а не клеток, накапливающих жир. [134] Исследования в этой области показали, что структурные модификации анаболических стероидов имеют решающее значение для определения их сродства к AR и их анаболической и андрогенной активности. [78] Эти модификации влияют на способность стероидов влиять на экспрессию генов и клеточные процессы, подчеркивая сложные биофизические взаимодействия анаболических стероидов на клеточном уровне. [132]
Как следует из названия, ААС обладают двумя разными, но пересекающимися типами эффектов: анаболическим , что означает, что они способствуют анаболизму (росту клеток), и андрогенным (или вирилизирующим ), что означает, что они влияют на развитие и поддержание мужских характеристик.
Некоторыми примерами анаболического действия этих гормонов являются усиление синтеза белка из аминокислот , повышение аппетита, усиление ремоделирования и роста костей, а также стимуляция костного мозга , что увеличивает выработку эритроцитов . Посредством ряда механизмов ААС стимулируют образование мышечных клеток и, следовательно, вызывают увеличение размеров скелетных мышц , что приводит к увеличению силы. [135] [12] [136]
Андрогенные эффекты ААС многочисленны. В зависимости от продолжительности использования побочные эффекты стероида могут быть необратимыми. Затрагиваемые процессы включают пубертатный рост, выработку масла сальных желез и сексуальность (особенно в развитии плода). Некоторыми примерами вирилизирующих эффектов являются рост клитора у женщин и пениса у детей мужского пола (размер полового члена взрослого не меняется из-за стероидов [ нужна медицинская ссылка ] ), увеличение размера голосовых связок , усиление либидо , подавление естественных половых гормонов . и нарушение выработки спермы . [137] Воздействие на женщин включает снижение голоса, рост волос на лице и, возможно, уменьшение размера груди. У мужчин может развиться увеличение ткани молочной железы, известное как гинекомастия, атрофия яичек и снижение количества сперматозоидов. [ нужна ссылка ] Соотношение андрогенов и анаболиков ААС является важным фактором при определении клинического применения этих соединений. Соединения с высоким соотношением андрогенного и анаболического эффектов являются препаратами выбора при андрогензаместительной терапии (например, при лечении гипогонадизма у мужчин), тогда как соединения с пониженным соотношением андрогенных и анаболических эффектов предпочтительны при анемии и остеопорозе, а также для реверсирования белка. утрата после травмы, хирургического вмешательства или длительной иммобилизации. Определение соотношения андрогенов и анаболиков обычно проводится в исследованиях на животных, что привело к появлению на рынке некоторых соединений, которые, как утверждается, обладают анаболической активностью со слабыми андрогенными эффектами. Эта диссоциация менее выражена у людей, где все ААС обладают значительным андрогенным действием. [74]
Широко используемый протокол определения соотношения андрогенов и анаболиков, принятый еще в 1950-х годах, использует относительный вес вентральной части простаты (VP) и мышцы, поднимающей задний проход (LA) самцов крыс . Вес VP является показателем андрогенного эффекта, тогда как вес LA является показателем анаболического эффекта. Две или более партий крыс кастрируют и не получают лечения и, соответственно, некоторых представляющих интерес ААС. Соотношение LA/VP для ААС рассчитывают как соотношение прироста веса LA/VP, вызванного лечением этим соединением, с использованием кастрированных, но не получавших лечения крыс в качестве исходного уровня: (LA c,t –LA c )/(VP c,t – ВП в ). Коэффициент прибавки веса LA/VP, полученный в экспериментах на крысах, не является единым для тестостерона (обычно 0,3–0,4), но он нормализуется для презентационных целей и используется в качестве основы для сравнения для других ААС, соотношение андрогенов и анаболиков которых масштабировано соответствующим образом ( как показано в таблице выше). [138] [139] В начале 2000-х годов эта процедура была стандартизирована и распространена по всей ОЭСР в так называемом тесте Хершбергера.
Анаболические стероиды заметно влияют на характеристики мышечных волокон, влияя как на размер, так и на тип мышечных волокон. Это изменение значительно способствует увеличению мышечной силы и выносливости. [140] Анаболически-андрогенные стероиды (ААС) вызывают эти изменения, напрямую воздействуя на клеточные компоненты мышечной ткани. Исследования показали, что эти изменения не просто поверхностны, а представляют собой глубокую трансформацию структурных и функциональных свойств мышц. Эта трансформация является ключевым фактором способности стероидов повышать физическую работоспособность и выносливость. [141]
Масса тела у мужчин может увеличиться на 2–5 кг в результате кратковременного (<10 недель) применения ААС, что можно объяснить главным образом увеличением мышечной массы. Исследования на животных также показали, что жировая масса снижается, но большинство исследований на людях не выявили значительного снижения жировой массы. Было показано, что влияние на мышечную массу тела зависит от дозы. Наблюдалась как мышечная гипертрофия , так и образование новых мышечных волокон . Использование ААС не влияет на гидратацию мышечной массы, хотя нельзя исключать небольшое увеличение объема крови. [7]
Верхняя часть тела (грудная клетка, шея, плечи и плечи), по-видимому, более восприимчива к ААС, чем другие области тела, из-за преобладания АР в верхней части тела. [ нужна ссылка ] Самая большая разница в размере мышечных волокон между пользователями и непользователями ААС наблюдалась в мышечных волокнах I типа латеральной широкой мышцы бедра и трапециевидной мышцы в результате длительного самостоятельного приема ААС. После отмены препарата эффекты исчезают медленно, но могут сохраняться более 6–12 недель после прекращения применения ААС. [7]
Улучшение силы составляет от 5 до 20% от исходной силы, в основном в зависимости от используемых препаратов и дозы, а также периода приема. В целом, упражнение, в котором наблюдались наиболее значительные улучшения, — это жим лежа . [7] На протяжении почти двух десятилетий считалось, что ААС оказывают значительный эффект только у опытных силовых спортсменов. [142] [143] Однако рандомизированное контролируемое исследование показало, что даже у начинающих спортсменов 10-недельная программа силовых тренировок, сопровождаемая энантатом тестостерона в дозе 600 мг/неделю, может улучшить силу больше, чем одна тренировка. [7] [144] Этой дозы достаточно, чтобы значительно улучшить мышечную массу по сравнению с плацебо даже у субъектов, которые вообще не занимались спортом. [144] Анаболические эффекты тестостерона энантата сильно зависели от дозы. [7] [145]
Эндогенные/природные ААС, такие как тестостерон и ДГТ, а также синтетические ААС опосредуют свое действие путем связывания и активации АР. [72] На основании биоанализов на животных эффекты этих агентов были разделены на два частично диссоциируемых типа: анаболические (миотрофические) и андрогенные. [72] Диссоциация между соотношениями этих двух типов эффектов по отношению к соотношению, наблюдаемому для тестостерона, наблюдается в биоанализах на крысах с различными ААС. [72] Теории диссоциации включают различия между ААС с точки зрения их внутриклеточного метаболизма , функциональной селективности (дифференцированное рекрутирование коактиваторов ) и негеномных механизмов (т.е. передачи сигналов через мембранные андрогенные рецепторы , не относящиеся к AR , или mAR). [72] Поддержка последних двух теорий ограничена и более гипотетическая, но существует значительная поддержка теории внутриклеточного метаболизма. [72]
Измерение диссоциации между анаболическими и андрогенными эффектами ААС основано в основном на простой, но устаревшей и несложной модели с использованием биоанализа тканей крыс. [72] Его называют « миотрофно-андрогенным индексом ». [72] В этой модели миотрофическая или анаболическая активность измеряется по изменению веса луковично -кавернозной мышцы / поднимающей задний проход крысы, а андрогенная активность измеряется по изменению веса вентральной части простаты крысы (или, альтернативно, семенной мышцы крысы). везикулы ), в ответ на воздействие ААС. [72] Затем измерения сравниваются для формирования соотношения. [72]
Тестостерон метаболизируется в различных тканях под действием 5α-редуктазы в ДГТ, который в 3–10 раз более эффективен в качестве агониста АР, и ароматазы в эстрадиол , который является эстрогеном и не обладает значительным сродством к АР. [72] Кроме того, ДГТ метаболизируется 3α-гидроксистероиддегидрогеназой (3α-HSD) и 3β-гидроксистероиддегидрогеназой (3β-HSD) в 3α-андростандиол и 3β-андростандиол соответственно, которые являются метаболитами с небольшим сродством к AR или вообще без него. [72] 5α-редуктаза широко распространена по всему организму и концентрируется в различной степени в коже (особенно на коже головы, лице и половых органах), предстательной железе, семенных пузырьках, печени и головном мозге. [72] Напротив, экспрессия 5α-редуктазы в скелетных мышцах не обнаруживается. [72] Ароматаза высоко экспрессируется в жировой ткани и головном мозге, а также значительно экспрессируется в скелетных мышцах. [72] 3α-HSD также высоко экспрессируется в скелетных мышцах. [67]
Природные ААС, такие как тестостерон и ДГТ, и синтетические ААС являются аналогами и очень схожи по структуре. [72] По этой причине они обладают способностью связываться и метаболизироваться с помощью одних и тех же ферментов , метаболизирующих стероиды . [72] Согласно объяснению внутриклеточного метаболизма, соотношение андрогенов и анаболиков данного агониста AR связано с его способностью трансформироваться вышеупомянутыми ферментами в сочетании с активностью AR любых полученных продуктов. [72] Например, в то время как AR-активность тестостерона значительно усиливается за счет локального преобразования посредством 5α-редуктазы в ДГТ в тканях, где экспрессируется 5α-редуктаза, ААС, который не метаболизируется 5α-редуктазой или уже 5α-редуктаза, такие как сам ДГТ или его производные (например, местеролон или дростанолон ), не будут подвергаться такому потенцированию в указанных тканях. [72] Более того, нандролон метаболизируется 5α-редуктазой, но в отличие от тестостерона и ДГТ, 5α-восстановленный метаболит нандролона имеет гораздо меньшее сродство к AR, чем сам нандролон, и это приводит к снижению активации AR в 5α. Ткани, экспрессирующие редуктазу. [72] Поскольку так называемые «андрогенные» ткани, такие как кожа/волосяные фолликулы и мужские репродуктивные ткани, имеют очень высокий уровень экспрессии 5α-редуктазы, в то время как скелетные мышцы практически лишены 5α-редуктазы, это может в первую очередь объяснить высокий уровень миотрофно-андрогенной активности. соотношение и диссоциация наблюдаются при приеме нандролона, а также различных других ААС. [72]
Помимо 5α-редуктазы, ароматаза может инактивировать передачу сигналов тестостерона в скелетных мышцах и жировой ткани, поэтому можно ожидать, что ААС, не обладающие сродством к ароматазы, помимо отсутствия потенциального побочного эффекта гинекомастии , будут иметь более высокое миотрофно-андрогенное соотношение в организме. сравнение. [72] Кроме того, ДГТ инактивируется высокой активностью 3α-HSD в скелетных мышцах (и сердечной ткани), и можно ожидать, что ААС, которым не хватает сродства к 3α-HSD, будут иметь более высокое миотрофно-андрогенное соотношение (хотя, возможно, также повышенные долгосрочные сердечно-сосудистые риски). [72] В соответствии с этим, ДГТ, местанолон (17α-метил-ДГТ) и месторолон (1α-метил-ДГТ) описываются как очень плохие анаболические свойства из-за инактивации 3α-HSD в скелетных мышцах, тогда как другие производные ДГТ с другими структурные особенности, такие как метенолон , оксандролон , оксиметолон , дростанолон и станозолол , являются плохими субстратами для 3α-HSD и описываются как мощные анаболики. [67]
Теория внутриклеточного метаболизма объясняет, как и почему может происходить значительная диссоциация между анаболическими и андрогенными эффектами, несмотря на то, что эти эффекты опосредованы одним и тем же сигнальным рецептором, и почему эта диссоциация всегда неполная. [72] В поддержку модели можно привести редкое состояние врожденного дефицита 5α-редуктазы 2 типа , при котором фермент 5α-редуктазы 2 типа дефектен, выработка ДГТ нарушена, а уровни ДГТ низкие, тогда как уровни тестостерона нормальные. [146] [147] Мужчины с этим заболеванием рождаются с неоднозначными гениталиями и сильно недоразвитой или даже отсутствующей предстательной железой. [146] [147] Кроме того, в период полового созревания у таких мужчин развивается нормальная мускулатура, тембр голоса и либидо, но снижается количество волос на лице, женский тип волос на теле (т.е. в основном ограничивается лобковым треугольником и подмышками). ), не было случаев выпадения волос по мужскому типу , а также увеличения простаты или заболеваемости раком простаты . [147] [148] [149] [150] [151] У них также не развивается гинекомастия как следствие их состояния. [149]
Исследование на животных показало, что два разных типа элементов андрогенного ответа могут по-разному реагировать на тестостерон и ДГТ при активации AR. [10] [152] Однако неизвестно, связано ли это с различиями в соотношении анаболического и миотрофического эффекта различных ААС. [10] [152] [72]
Тестостерон передает сигналы не только через ядерный AR, но и через mAR, включая ZIP9 и GPRC6A . [153] [154] Было высказано предположение, что дифференциальная передача сигналов через mAR может участвовать в диссоциации анаболического и андрогенного эффектов ААС. [72] Действительно, ДГТ имеет менее 1% сродства тестостерона к ZIP9, а синтетические ААС метриболон и миболерон также являются неэффективными конкурентами для рецептора. [154] Это указывает на то, что ААС действительно демонстрируют различное взаимодействие с AR и mAR. [154] Однако женщины с синдромом полной нечувствительности к андрогенам (CAIS), у которых есть генотип 46,XY («мужской») и яички , но дефект в AR, так что он нефункционален, бросают вызов этому представлению. [155] Они совершенно нечувствительны к АР-опосредованным эффектам андрогенов, таких как тестостерон, и демонстрируют совершенно женский фенотип , несмотря на то, что уровень тестостерона у них находится на верхнем уровне нормального мужского диапазона. [155] У этих женщин наблюдается незначительное выделение кожного сала или его полное отсутствие, появление прыщей или рост волос на теле (в том числе в лобковой и подмышечной областях). [155] Более того, женщины CAIS имеют безжировую массу тела , которая является нормальной для женщин, но, конечно, значительно ниже, чем у мужчин. [156] Эти наблюдения позволяют предположить, что АР в основном или исключительно ответственен за маскулинизацию и миотрофию, вызванную андрогенами. [155] [156] [157] Однако было обнаружено, что mAR участвуют в некоторых связанных со здоровьем эффектах тестостерона, таких как модуляция риска и прогрессирования рака простаты. [154] [158]
Изменения уровня эндогенного тестостерона также могут способствовать различиям в миотрофно-андрогенном соотношении между тестостероном и синтетическими ААС. [67] Агонисты AR являются антигонадотропными , то есть они дозозависимо подавляют выработку тестостерона гонадами и, следовательно, снижают системные концентрации тестостерона. [67] Подавляя уровни эндогенного тестостерона и эффективно заменяя передачу сигналов AR в организме сигналами экзогенных ААС, миотрофно-андрогенное соотношение данного ААС может быть дополнительно дозозависимо увеличено, и, следовательно, это может быть дополнительным фактором, способствующим различиям в миотрофно-андрогенном соотношении между разными ААС. [67] Кроме того, некоторые ААС, такие как производные 19-нортестостерона, такие как нандролон, также являются мощными прогестагенами , а активация рецептора прогестерона (ПР) является антигонадотропной, как и активация АР. [67] Комбинация достаточной активации AR и PR может подавить уровень циркулирующего тестостерона до кастрационного уровня у мужчин (т.е. полное подавление выработки тестостерона гонадами и уровень циркулирующего тестостерона снижается примерно на 95%). [48] [159] Таким образом, комбинированная прогестагенная активность может способствовать дальнейшему увеличению миотрофно-андрогенного соотношения для данного ААС. [67]
Было обнаружено, что некоторые ААС, такие как тестостерон, ДГТ, станозолол и метилтестостерон, модулируют рецептор ГАМК А аналогично эндогенным нейростероидам , таким как аллопрегнанолон , 3α-андростандиол , сульфат дегидроэпиандростерона и сульфат прегненолона . [72] Было высказано предположение, что это может способствовать альтернативному или дополнительному механизму неврологических и поведенческих эффектов ААС. [72] [160] [161 ] [162] [163] [164] [165]
ААС различаются по-разному, в том числе по их способности метаболизироваться стероидогенными ферментами , такими как 5α-редуктаза , 3-гидроксистероиддегидрогеназы и ароматаза , по тому, усиливается или ослабляется их эффективность в качестве агонистов AR при 5α-восстановлении, а также в их соотношениях . от анаболического / миотрофического до андрогенного действия, по их эстрогенной , прогестагенной и нейростероидной активности, по их пероральной активности и по их способности вызывать гепатотоксичность . [67] [72] [166]
Тестостерон может быть надежно преобразован 5α-редуктазой в ДГТ в так называемых андрогенных тканях, таких как кожа , скальп , простата и семенные пузырьки , но не в мышцах или костях , где 5α-редуктаза либо не экспрессируется, либо экспрессируется лишь минимально. [72] Поскольку ДГТ в 3-10 раз более эффективен в качестве агониста АР, чем тестостерон, активность АР-агониста тестостерона, таким образом, заметно и выборочно усиливается в таких тканях. [72] В отличие от тестостерона, ДГТ и другие 4,5α-дигидрированные ААС уже имеют 5α-восстановление и по этой причине не могут потенцироваться в андрогенных тканях. [72] Производные 19-нортестостерона, такие как нандролон , могут метаболизироваться 5α-редуктазой аналогично тестостерону, но 5α-восстановленные метаболиты производных 19-нортестостерона (например, 5α-дигидронандролон ) имеют тенденцию иметь пониженную активность в качестве агонистов АР, что приводит к снижению андрогенной активности. активность в тканях, экспрессирующих 5α-редуктазу. [72] Кроме того, некоторые производные 19-нортестостерона, в том числе трестолон (7α-метил-19-нортестостерон (MENT)), 11β-метил-19-нортестостерон (11β-MNT) и диметандролон (7α,11β-диметил-19 -нортестостерон), не может быть 5α-восстановлен. [167] И наоборот, некоторые 17α-алкилированные ААС, такие как метилтестостерон, 5α-снижаются и усиливаются в андрогенных тканях, подобно тестостерону. [72] [67] Однако 17α-алкилированные производные ДГТ не могут быть потенцированы посредством 5α-редуктазы, поскольку они уже 4,5α-восстановлены. [72] [67]
Способность метаболизироваться 5α-редуктазой и AR-активность образующихся метаболитов, по-видимому, являются одним из основных, если не самым важным фактором, определяющим андрогенно -миотрофическое соотношение для данного ААС. [72] ААС, которые не усиливаются 5α-редуктазой или ослаблены 5α-редуктазой в андрогенных тканях, имеют меньший риск возникновения андрогенных побочных эффектов, таких как прыщи , андрогенная алопеция (облысение по мужскому типу), гирсутизм (чрезмерное облысение по мужскому типу). рост волос), доброкачественная гиперплазия предстательной железы (увеличение простаты) и рак простаты , в то время как частота и величина других эффектов, таких как гипертрофия мышц , изменения костей, [168] понижение голоса и изменения полового влечения , не имеют различий. [72] [169]
Тестостерон может метаболизироваться ароматазой в эстрадиол , и многие другие ААС также могут метаболизироваться в соответствующие им эстрогенные метаболиты. [72] Например, 17α-алкилированные ААС метилтестостерон и метандиенон превращаются ароматазой в метилэстрадиол . [170] 4,5α-дигидрированные производные тестостерона, такие как ДГТ, не могут быть ароматизированы, тогда как производные 19-нортестостерона, такие как нандролон, могут быть ароматизированы, но в значительно меньшей степени. [72] [171] Некоторые производные 19-нортестостерона, такие как диметандролон и 11β-MNT, не могут ароматизироваться из-за стерических затруднений, обеспечиваемых их 11β-метиловой группой, тогда как близкородственный ААС трестолон (7α-метил-19-нортестостерон) , из-за отсутствия 11β-метильной группы, может ароматизироваться. [171] ААС, 17α-алкилированные (а не 4,5α-восстановленные или 19-деметилированные), также ароматизируются, но в меньшей степени, чем тестостерон. [72] [172] Однако примечательно, что 17α-замещенные эстрогены (например, этинилэстрадиол и метилэстрадиол) обладают заметно повышенной эстрогенной активностью из-за улучшенной метаболической стабильности , [170] и по этой причине 17α-алкилированные ААС могут на самом деле обладают высокой эстрогенностью и сравнительно большим эстрогенным действием, чем тестостерон. [170] [67]
Основным эффектом эстрогенности является гинекомастия (женская грудь). [72] ААС, которые имеют высокий потенциал ароматизации, такие как тестостерон и особенно метилтестостерон, демонстрируют высокий риск гинекомастии при достаточно высоких дозировках, в то время как ААС, которые имеют сниженный потенциал ароматизации, такие как нандролон, демонстрируют гораздо меньший риск (хотя все еще потенциально значимы при высоких дозах). дозировки). [72] Напротив, ААС со сниженным содержанием 4,5α и некоторые другие ААС (например, 11β-метилированные производные 19-нортестостерона) не несут риска гинекомастии. [72] Помимо гинекомастии, ААС с высокой эстрогенностью обладают повышенной антигонадотропной активностью, что приводит к увеличению эффективности подавления гипоталамо-гипофизарно-гонадной оси и продукции тестостерона гонадами . [173]
Многие производные 19-нортестостерона, в том числе нандролон, тренболон , этилэстренол (этилнандрол), метриболон (R-1881), трестолон, 11β-МНТ, диметандролон и другие, являются мощными агонистами рецептора прогестерона (ПР) и, следовательно, являются дополнительно прогестагенами. к ААС. [72] [174] Как и в случае с эстрогенной активностью, прогестагенная активность этих препаратов усиливает их антигонадотропную активность. [174] Это приводит к увеличению активности и эффективности этих ААС в качестве антисперматогенных средств и мужских контрацептивов (или, другими словами, к увеличению активности и эффективности при возникновении азооспермии и обратимого мужского бесплодия ). [174]
Не-17α-алкилированные производные тестостерона, такие как сам тестостерон, ДГТ и нандролон, имеют плохую биодоступность при пероральном приеме из-за интенсивного метаболизма при первом прохождении через печень и, следовательно, не активны при пероральном приеме. [72] Заметным исключением из этого правила являются ААС, которые являются предшественниками андрогенов или прогормонами , включая дегидроэпиандростерон (ДГЭА), андростендиол , андростендион , болдион (андростадиендион), боландиол (норандростендиол), боландион (норандростенедион), диендростион , ментаболан (МЕНТ-дион, трестион). ) и метоксидиенон (метоксигонадиен) (хотя это относительно слабые ААС). [175] [176] ААС, неактивные при пероральном приеме, используются почти исключительно в виде сложных эфиров , вводимых внутримышечно , которые действуют как депо и действуют как пролекарства длительного действия . [72] Примеры включают тестостерон, такой как тестостерон ципионат , тестостерон энантат и тестостерон пропионат , а также нандролон, как нандролон фенилпропионат и нандролон деканоат , среди многих других ( полный список эфиров тестостерона и нандролона см. здесь ). [72] Исключением является очень длинноцепочечный эфир тестостерона ундеканоат , который активен при пероральном приеме, хотя и с очень низкой биодоступностью при пероральном приеме (приблизительно 3%). [177] В отличие от большинства других ААС, 17α-алкилированные производные тестостерона проявляют устойчивость к метаболизму из-за стерических затруднений и активны при пероральном приеме, хотя их можно эстерифицировать и вводить также посредством внутримышечных инъекций. [72]
Помимо перорального действия, 17α-алкилирование также имеет высокий потенциал гепатотоксичности , и все 17α-алкилированные ААС были связаны с этим, хотя и редко и только после длительного применения (по разным оценкам от 1 до 17%) [178] [179] с гепатотоксичностью. [72] [180] [181] Напротив, эфиры тестостерона крайне редко или никогда не были связаны с гепатотоксичностью, [179] и другие не-17α-алкилированные ААС лишь изредка, [ нужна цитация ] , хотя, как сообщается, длительное применение может все же увеличивают риск изменений в печени (но в гораздо меньшей степени, чем 17α-алкилированные ААС, и, как сообщается, не в замещающих дозах). [178] [182] [71] [ необходимы дополнительные ссылки ] В соответствии с этим было обнаружено , что глюкурониды D-кольца тестостерона и ДГТ оказывают холестатическое действие. [183]
За исключением прогормонов и ундеканоата тестостерона, почти все перорально активные ААС являются 17α-алкилированными. [184] Некоторые ААС, не 17α-алкилированные, активны при пероральном приеме. [72] Некоторые примеры включают 17-эфиры тестостерона клоксотестостерон , хинболон и силандрон , [ нужна ссылка ] , которые являются пролекарствами (тестостерону, болденону (Δ 1 -тестостерон) и тестостерону соответственно), 17-эфирам DHT мепитиостану , мезаболон и простанозол (которые также являются пролекарствами), 1-метилированные производные ДГТ местеролон и метенолон (хотя они являются относительно слабыми ААС), [72] [71] и производные 19-нортестостерона диметандролон и 11β-МНТ, которые улучшают устойчивость к метаболизму первого прохождения через печень за счет их 11β-метильных групп (в отличие от них родственный ААС трестолон (7α-метил-19-нортестостерон) не активен при пероральном приеме). [72] [174] Поскольку эти ААС не являются 17α-алкилированными, они демонстрируют минимальный потенциал гепатотоксичности. [72]
ДГТ через свой метаболит 3α-андростандиол (продуцируемый 3α-гидроксистероиддегидрогеназой (3α-HSD)) представляет собой нейростероид , который действует посредством положительной аллостерической модуляции рецептора ГАМК А. [72] Тестостерон, превращаясь в ДГТ, также производит 3α-андростандиол в качестве метаболита и, следовательно, обладает аналогичной активностью. [72] Некоторые ААС, которые являются или могут быть 5α-редуцированы, включая тестостерон, ДГТ, станозолол и метилтестостерон, среди многих других, могут или могут модулировать рецептор ГАМК А , и это может способствовать альтернативному или дополнительному механизму их центрального действия . Влияние на нервную систему с точки зрения настроения, тревоги, агрессии и полового влечения. [72] [160] [161 ] [162] [163] [164] [165]
ААС – это стероиды андростан или эстран . К ним относятся тестостерон (андрост-4-ен-17β-ол-3-он) и его производные с различными структурными модификациями , такие как: [72] [185] [67]
А также другие, такие как 1-дегидрирование (например, метандиенон , болденон ), 1-замещение (например, месторолон , метенолон ), 2-замещение (например, дростанолон , оксиметолон , станозолол ), 4-замещение (например, клостебол , оксаболон ). ) и различные другие модификации. [72] [185] [67]
Превращение в ДГТ, [186] нандролон, [72] метандиенон (Дианабол), [187] хлордегидрометилтестостерон (Туринабол), [188] флуоксиместерон (Халотестин), [189] и болденон (Экипойз): [190]

ДГТ на станозолол (Винстрол), [191] метенолона ацетат (Примоболан), [192] оксиметолон (Анадрол), [193] и метастерон (Супердрол): [194]

Нандролон в трестолон, [195] тренболон, [196] норболетон, [197] и этилэстренол: [198]

Наиболее часто используемым физиологическим образцом человека для выявления употребления ААС является моча, хотя для этой цели исследовались как кровь, так и волосы. ААС, как эндогенного, так и экзогенного происхождения, подвергаются обширной биотрансформации в печени различными ферментативными путями. Первичные метаболиты мочи могут обнаруживаться в течение 30 дней после последнего применения, в зависимости от конкретного препарата, дозы и пути введения. Ряд препаратов имеют общие метаболические пути, и их профили выведения могут перекрывать профили выведения эндогенных стероидов, что делает интерпретацию результатов испытаний очень серьезной проблемой для химика-аналитика. Методы обнаружения веществ или продуктов их выделения в образцах мочи обычно включают газовую хроматографию-масс-спектрометрию или жидкостную хроматографию-масс-спектрометрию. [199] [200] [201] [202]
Использование гонадных стероидов предшествовало их идентификации и выделению. Использование коровьей мочи для лечения асцита, сердечной недостаточности, почечной недостаточности и витилиго было подробно описано в Сушрута Самхите , что позволяет предположить, что древние индийцы имели некоторое представление о стероидных свойствах коровьей мочи примерно в 6 веке до нашей эры. [203] Извлечение гормонов из мочи началось в Китае около 100 г. до н.э. [ нужна цитация ] Медицинское использование экстракта яичек началось в конце 19 века, когда его влияние на силу все еще изучалось. [137] Выделение гонадных стероидов можно проследить до 1931 года, когда Адольф Бутенандт , химик из Марбурга , выделил 15 миллиграммов мужского гормона андростенона из десятков тысяч литров мочи. Этот стероид впоследствии был синтезирован в 1934 году Леопольдом Ружичкой , химиком из Цюриха . [204]
В 1930-х годах уже было известно, что яички содержат более мощный андроген, чем андростенон , и три группы ученых, финансируемые конкурирующими фармацевтическими компаниями в Нидерландах, Германии и Швейцарии, бросились его изолировать. [204] [205] Этот гормон был впервые идентифицирован Кароли Дьюлой Дэвидом, Э. Дингемансом, Дж. Фрейдом и Эрнстом Лакером в статье в мае 1935 года «О кристаллическом мужском гормоне из яичек (тестостерон)». [206] Они назвали гормон тестостерон , от основы яичка и стерола , и суффикса кетона . Химический синтез тестостерона был осуществлен в августе того же года, когда Бутенандт и Г. Ханиш опубликовали статью, описывающую «Метод получения тестостерона из холестерина». [207] Всего через неделю третья группа, Ружичка и А. Веттштейн, объявили о заявке на патент в статье «Об искусственном получении тестикулярного гормона тестостерона (андростен-3-он-17-ол)». [208] Ружичке и Бутенандту была предложена Нобелевская премия по химии 1939 года за их работу, но нацистское правительство вынудило Бутенандта отказаться от этой награды, хотя он принял премию после окончания Второй мировой войны. [204] [205]
Клинические испытания на людях, включающие либо пероральные дозы метилтестостерона , либо инъекции пропионата тестостерона , начались еще в 1937 году. [204] Часто ходят слухи, что немецким солдатам во время Второй мировой войны вводили ААС с целью повысить их агрессию. и выносливость, но это еще не доказано. [118] : 6 Самому Адольфу Гитлеру , по словам его врача, вводили производные тестостерона для лечения различных недугов. [209] ААС использовались в экспериментах, проводимых нацистами над узниками концентрационных лагерей, [209] а позже и союзниками, пытавшимися лечить истощенных жертв, выживших в нацистских лагерях. [118] 6 Президент Джон Ф. Кеннеди принимал стероиды как до, так и во время своего президентства. [210]
Разработка свойств тестостерона для наращивания мышечной массы продолжалась в 1940-х годах в Советском Союзе и в странах Восточного блока , таких как Восточная Германия, где стероидные программы использовались для повышения производительности олимпийских спортсменов и других тяжелоатлетов -любителей . В ответ на успех российских штангистов врач олимпийской сборной США Джон Зиглер работал с химиками-синтетиками над разработкой ААС со сниженным андрогенным действием. [211] Работа Циглера привела к производству метандростенолона , который Ciba Pharmaceuticals продавала как Дианабол. Новый стероид был одобрен для использования в США Управлением по контролю за продуктами и лекарствами (FDA) в 1958 году. Чаще всего его назначали жертвам ожогов и пожилым людям. Потребителями препарата не по назначению были в основном бодибилдеры и тяжелоатлеты. Хотя Зиглер прописывал спортсменам лишь небольшие дозы, он вскоре обнаружил, что у тех, кто использовал Дианабол, развивалась увеличенная простата и атрофированные яички. [212] ААС были внесены в список запрещенных веществ Международного олимпийского комитета (МОК) в 1976 году, а десять лет спустя комитет ввел «внесоревновательные» допинг-тесты, поскольку многие спортсмены использовали ААС в период тренировок, а не во время соревнований. [7]
Три основные идеи определяли модификацию тестостерона во множество ААС: алкилирование в положении C17α метильной или этильной группой создавало POly-активные соединения, поскольку оно замедляло разложение препарата в печени; этерификация тестостерона и нортестостерона по позиции С17β позволяет вводить вещество парентерально и увеличивает продолжительность эффективности, поскольку растворимые в маслянистых жидкостях средства могут присутствовать в организме в течение нескольких месяцев; и изменения кольцевой структуры применялись как для пероральных, так и для парентеральных агентов с целью получения различных соотношений анаболического и андрогенного эффектов. [7]
Андрогены были открыты в 1930-х годах, и их эффекты описывались как андрогенные (т.е. вирилизирующие) и анаболические (например, миотрофические, ренотрофические). [67] [72] Термин «анаболический стероид» можно отнести еще к середине 1940-х годов, когда он использовался для описания тогдашней гипотетической концепции стероида, полученного из тестостерона, с анаболическим эффектом, но с минимальным или отсутствие андрогенных эффектов. [213] Эта концепция была сформулирована на основе наблюдения, что стероиды имеют соотношение ренотрофной и андрогенной активности, которое значительно различается, что позволяет предположить, что анаболические и андрогенные эффекты могут быть несовместимы. [213]
В 1953 году производный от тестостерона стероид, известный как норэтандролон (17α-этил-19-нортестостерон), был синтезирован в компании GD Searle & Company и изучался как прогестин , но не поступил в продажу. [214] Впоследствии, в 1955 году, он был повторно исследован на предмет тестостероноподобной активности на животных, и было обнаружено, что он имеет аналогичную анаболическую активность с тестостероном, но составляет лишь одну шестнадцатую его андрогенной активности. [214] [215] Это был первый обнаруженный стероид с выраженным и благоприятным разделением анаболического и андрогенного действия, и соответственно он был описан как «первый анаболический стероид». [216] [217] Норэтандролон был представлен для медицинского применения в 1956 году, за ним быстро последовали многочисленные аналогичные стероиды, например, нандролон фенилпропионат в 1959 году и станозолол в 1962 году . [216] [217] [218] [219] Благодаря этим разработкам анаболический стероид стал предпочтительным термином для обозначения таких стероидов (а не «андрогеном») и вошел в широкое употребление.
Хотя изначально анаболический стероид был предназначен для описания стероидов, производных тестостерона, с выраженной диссоциацией анаболического и андрогенного действия, сегодня он применяется без разбора ко всем стероидам с анаболическими эффектами, основанными на AR-агонизме, независимо от их андрогенной активности, включая даже несинтетические и андрогенные. непредпочтительно анаболические стероиды, такие как тестостерон. [67] [72] [214] Хотя многие анаболические стероиды обладают меньшей андрогенной активностью по сравнению с анаболической активностью, не существует анаболического стероида, который был бы исключительно анаболическим, и, следовательно, все анаболические стероиды сохраняют по крайней мере некоторую степень андрогенности. [67] [72] [214] (Аналогично, все «андрогены» по своей сути являются анаболическими.) [67] [72] [214] Действительно, вероятно, невозможно полностью отделить анаболические эффекты от андрогенных эффектов, поскольку оба типа эффекты опосредуются одним и тем же сигнальным рецептором, AR. [72] Таким образом, различие между терминами «анаболический стероид» и «андроген» сомнительно, и это является основой для пересмотренного и более современного термина « анаболически-андрогенный стероид» ( ААС ). [67] [72] [214]
Дэвид Хандельсман критиковал терминологию и понимание ААС во многих публикациях. [220] [221] [222] [223] [224] [225] [226] [227] По словам Хандельсмана, фармацевтическая промышленность попыталась разграничить так называемые «андрогенные» и «анаболические» эффекты ААС в середине 20-го века с целью создания немужских анаболических агентов, которые были бы более пригодны для использования у женщин и детей. [220] Однако эта попытка потерпела полную неудачу и была оставлена к 1970-м годам. [220] [221] Эта неудача произошла из-за последующего открытия единственного андрогенного рецептора (AR), опосредующего эффекты ААС как в мышечной, так и в репродуктивной ткани, а также из-за неправильной интерпретации ошибочных биоанализов андрогенов на животных, используемых для различения андрогенных или вирилизирующих эффектов. и анаболические или миотрофические эффекты (т.е. анализ Гершбергера, включающий нерепрезентативную мышцу, поднимающую задний проход). [220] [221] В действительности все ААС обладают по существу схожими АР-опосредованными эффектами, [227] даже если некоторые из них могут в некоторой степени различаться по эффективности в определенных тканях (например, коже, волосяных фолликулах, предстательной железе) в зависимости от чувствительности к 5α-редукция и связанная с ней метаболическая амплификация или инактивация или ее отсутствие. [227] [8] По мнению Хандельсмана, термины «анаболический стероид» и «анаболо-андрогенный стероид» устарели, бессмысленны и ошибочно отличают эти агенты от андрогенов, когда для такого различия нет физиологической основы. [220] [221] Фактически было отмечено, что использование и различие понятий «анаболический» и «андрогенный», а также термина «анаболически-андрогенный стероид» являются оксюморонами, поскольку анаболик относится к наращиванию мышечной массы, а Андрогенный относится к индукции и поддержанию мужских вторичных половых признаков (которые в принципе включают анаболический эффект или эффект наращивания мышечной массы). [220] [221] [228] Хандельсман утверждал, что от этих терминов следует отказаться и вместо этого все ААС следует называть просто «андрогенами», причем он использует этот термин исключительно для обозначения этих агентов в своих публикациях. [220] [221] Хотя термин «анаболически-андрогенный стероид» технически обоснован для описания двух типов действия этих агентов, Хандельсман считает этот термин ненужным и избыточным и сравнивает его с гипотетическими никогда не используемыми терминами, такими как «лютеиново-гестационные прогестины». или «молочно-маточные эстрогены».[220] Хандельсман также отмечает, что «анаболические стероиды» легко и без необходимости спутать с кортикостероидами . [220]Помимо ААС, Хандельсман раскритиковал термин « селективный модулятор андрогенных рецепторов (SARM)», а также утверждения об этих агентах. [222] [220] [221] [226]
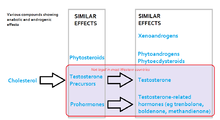
Правовой статус ААС варьируется от страны к стране: в некоторых странах существует более строгий контроль за их использованием или назначением, чем в других, хотя во многих странах они не являются незаконными. В США ААС в настоящее время внесены в список контролируемых веществ Списка III в соответствии с Законом о контролируемых веществах , который делает простое хранение таких веществ без рецепта федеральным преступлением, наказуемым лишением свободы на срок до одного года за первое правонарушение. Незаконное распространение или хранение с целью распространения ААС в качестве первого преступления наказывается лишением свободы на срок до десяти лет. [229] В Канаде ААС и их производные подпадают под действие Закона о контролируемых наркотиках и веществах и относятся к веществам Списка IV , а это означает, что их получение или продажа без рецепта противозаконны; однако хранение не наказуемо, и это последствие касается веществ из списков I, II или III. Виновные в покупке или продаже ААС в Канаде могут быть заключены в тюрьму на срок до 18 месяцев. [230] Импорт и экспорт также влекут за собой аналогичные штрафы.
В Канаде исследователи пришли к выводу, что употребление стероидов среди студентов-спортсменов чрезвычайно широко распространено. Исследование, проведенное в 1993 году Канадским центром спорта без допинга, показало, что около 83 000 канадцев в возрасте от 11 до 18 лет употребляют стероиды. [231] ААС также являются незаконными без рецепта в Австралии, [232] Аргентине, [ нужна ссылка ] Бразилии, [ нужна ссылка ] и Португалии, [ нужна ссылка ] и внесены в список контролируемых препаратов класса C в Соединенном Королевстве. ААС легко доступны без рецепта в некоторых странах, таких как Мексика и Таиланд.
История законодательства США об ААС восходит к концу 1980-х годов, когда Конгресс США рассмотрел вопрос о включении ААС в сферу действия Закона о контролируемых веществах после разногласий по поводу победы Бена Джонсона на летних Олимпийских играх 1988 года в Сеуле . ААС были добавлены в Список III Закона о контролируемых веществах в Законе о контроле над анаболическими стероидами 1990 года . [236]
Этим же законом также были введены более строгие меры контроля и более строгие уголовные наказания за преступления, связанные с незаконным распространением ААС и гормона роста человека. К началу 1990-х годов, после того как ААС были запланированы на продажу в США, несколько фармацевтических компаний прекратили производство или продажу этой продукции в США, в том числе Ciba , Searle , Syntex и другие. В Законе о контролируемых веществах ААС определяются как любые лекарства или гормональные вещества, химически и фармакологически связанные с тестостероном (кроме эстрогенов , прогестинов и кортикостероидов ), которые способствуют росту мышц. В этот закон были внесены поправки Законом о контроле над анаболическими стероидами 2004 года, который добавил прогормоны в список контролируемых веществ , вступивший в силу с 20 января 2005 года. [237]
Несмотря на то, что в США их все еще может назначать врач, использование анаболических стероидов в целях восстановления после травм было табуированной темой даже среди большинства врачей спортивной медицины и эндокринологов.
В Великобритании ААС отнесены к препаратам класса С, что ставит их в один класс с бензодиазепинами . AAS включены в Приложение 4, которое разделено на 2 части; Часть 1 содержит большую часть бензодиазепинов, а часть 2 — ААС.
Препараты Части 1 подлежат полному импортному и экспортному контролю, при этом хранение без соответствующего рецепта считается правонарушением. Ограничений на хранение нет, если он является частью лекарственного препарата. Для ввоза и вывоза препаратов Части 2 требуется лицензия Министерства внутренних дел, за исключением случаев, когда вещество находится в форме лекарственного препарата и предназначено для самостоятельного приема человеком. [238]
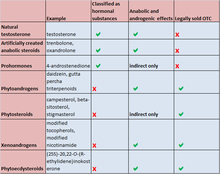
ААС запрещены всеми крупными спортивными организациями, включая Ассоциацию профессиональных теннисистов , Высшую бейсбольную лигу , Международную федерацию футбольных ассоциаций , [239] Олимпийские игры , [240] Национальную баскетбольную ассоциацию , [241] Национальную хоккейную лигу , [242] Мировую борьбу . Развлечения и Национальная футбольная лига . [243] Всемирное антидопинговое агентство (ВАДА) ведет список веществ, улучшающих спортивные результаты, используемых многими крупными спортивными организациями, и включает в себя все анаболические агенты, включая все ААС и прекурсоры, а также все гормоны и родственные им вещества. [244] [245]
Представители федеральных правоохранительных органов США выразили обеспокоенность по поводу использования ААС сотрудниками полиции. «Это большая проблема, и, судя по количеству случаев, это то, что мы не должны игнорировать. Дело не в том, что мы намеревались атаковать полицейских, но когда мы находимся в середине активного расследования стероидов , было довольно много несколько случаев дошли до полицейских», — говорит Лоуренс Пейн, представитель Управления по борьбе с наркотиками США . [246] В Бюллетене правоохранительных органов ФБР говорится, что «злоупотребление анаболическими стероидами со стороны полицейских является серьезной проблемой, которая заслуживает более пристального внимания со стороны департаментов по всей стране». [247] Также считается, что полицейские по всей Великобритании «используют преступников для покупки стероидов», что, по его утверждению, является главным фактором риска коррупции в полиции .
После убийства-самоубийства Криса Бенуа в 2007 году Комитет по надзору и правительственной реформе расследовал использование стероидов в индустрии рестлинга. [248] Комитет расследовал WWE и Total Nonstop Action Wrestling (теперь известный как Impact Wrestling ), запросив документацию о политике их компаний в отношении наркотиков. Генеральный директор и председатель WWE Линда и Винс МакМэхон соответственно дали показания. В документах говорилось, что с 2006 года 75 борцов (примерно 40 процентов) дали положительный результат на употребление наркотиков, чаще всего на стероиды. [249] [250]

ААС часто производятся в фармацевтических лабораториях, но в странах, где действуют более строгие законы, их также производят в небольших самодельных подземных лабораториях, обычно из сырья, импортируемого из-за границы. [251] В этих странах большая часть стероидов приобретается нелегально, посредством торговли на черном рынке . [252] [253] Эти стероиды обычно производятся в других странах, и поэтому их необходимо переправлять контрабандой через международные границы. Как и в большинстве крупных операций по контрабанде, в них участвует организованная преступность . [254]
В конце 2000-х годов мировая торговля незаконными ААС значительно возросла, и власти объявили о рекордных объемах вылова на трех континентах. В 2006 году финские власти объявили о рекордном изъятии 11,8 миллионов таблеток ААС. Год спустя DEA конфисковало 11,4 миллиона единиц ААС в ходе крупнейшей конфискации за всю историю США. За первые три месяца 2008 года австралийская таможня сообщила о рекордных 300 изъятиях партий ААС. [110]
В США, Канаде и Европе нелегальные стероиды иногда покупаются, как и любые другие нелегальные наркотики, через дилеров, которые могут получить наркотики из разных источников. Нелегальные ААС иногда продаются в спортзалах, на соревнованиях, а также по почте, но их также можно приобрести у фармацевтов, ветеринаров и врачей. [255] Кроме того, значительное количество контрафактной продукции продается под видом ААС, в частности, по почте с веб-сайтов, выдающих себя за зарубежные аптеки. В США продолжается черный рынок импорта из Мексики, Таиланда и других стран, где стероиды более доступны, поскольку они легальны. [256]
ААС, отдельно или в сочетании с прогестагенами , изучались как потенциальные мужские гормональные контрацептивы . [48] Двойные ААС и прогестины , такие как трестолон и ундеканоат диметандролона , также изучались в качестве мужских контрацептивов, причем последний находится в стадии активного исследования с 2018 года. [257] [174] [258]
Местные андрогены использовались и изучались при лечении целлюлита у женщин. [259] Было обнаружено, что местное применение андростанолона на животе значительно уменьшает количество подкожного брюшного жира у женщин и, следовательно, может быть полезно для улучшения силуэта тела. [259] Однако мужчины и гиперандрогенные женщины имеют большее количество брюшного жира, чем здоровые женщины, а также было обнаружено, что андрогены увеличивают количество брюшного жира у женщин в постменопаузе и трансгендерных мужчин . [260]
Эндогенные анаболические стероиды, такие как тестостерон и дигидротестостерон, и синтетические анаболические стероиды опосредуют свое действие путем связывания и активации андрогенных рецепторов.
[...] в недавнем исследовании на животных Hsiao et al. (10) обнаружили два разных типа элементов ответа на андрогены, которые могут по-разному реагировать на Т и ДГТ. Следовательно, возможно, что селективная последовательность элемента андрогенного ответа может играть роль в дифференциальной трансактивации T и DHT AR.
Хотя и тестостерон, и дигидротестостерон активируют один и тот же андрогенный рецептор, различия в последовательности элементов андрогенного ответа ответственны за дифференциальную регуляцию этих гормонов (21).
Андрогены, эстрогены и прогестины оказывают эффект отрицательной обратной связи на секрецию ГнРГ и ЛГ, воздействуя на гипофиз и гипоталамус. Большая часть эффекта отрицательной обратной связи андрогенов обусловлена их эстрогенными метаболитами, образующимися в результате ароматизации. 5α-редукция, по-видимому, не является необходимой для эффекта отрицательной обратной связи тестостерона. (Риттмастер и др., 1992; Кумар и др., 1995а; Хейс и др., 2000).
В последние годы несколько лабораторий (Кочакян, Олбрайт, Уилкинс) питали надежду найти белковый анаболический стероид без какого-либо или лишь с незначительным сексуальным действием. Эти исследования получили особый импульс и поддержку благодаря наблюдению Кочакяна о том, что некоторые стероиды обладают более сильным ренотрофическим (анаболическим?), чем андрогенным действием.
Однако третий крупный поиск по разработке невирилизирующего андрогена («анаболического стероида»), подходящего для использования у женщин и детей, основанный на разграничении вирилизирующего и анаболического эффектов андрогенов, полностью потерпел неудачу (36). В настоящее время считается, что эта неудача связана с открытием единственного андрогенного рецептора (АР) вместе с неправильной интерпретацией неспецифических биоанализов андрогенов на животных, используемых для различения анаболического и вирилизирующего эффектов (37). Термин «андроген» используется здесь как для эндогенных, так и для синтетических андрогенов, включая ссылки на химические вещества, называемые в других местах как «анаболические стероиды», «анаболически-андрогенные стероиды» или «специфические модуляторы AR» (SARM), которые продолжают оставаться устаревшими и оксюморонное различие между вирилизирующим и анаболическим действием андрогенов, когда разницы нет (36).
Эти результаты также подчеркивают, насколько устаревшим является термин «анаболический стероид», когда его ошибочно отличают от «андрогена», дихотомии, лишенной физиологического значения и сохраняющейся в основном как медиа-пиньята.10
По определению, все андрогены сочетают в себе присущие анаболические и андрогенные свойства, которые никогда значимо не разделялись [67], проявляющиеся через андрогенный рецептор, белок, кодируемый единственным копийным геном. Следовательно, своеобразие действия андрогенов означает, что термины «анаболический стероид» или «андрогенно-анаболические стероиды» остаются устаревшей терминологией, делающей различие между андрогенными и анаболическими эффектами там, где реальной разницы нет [67]. Эта устаревшая, но широко используемая терминология представляет собой пережиток безуспешных попыток фармацевтической промышленности отделить вирилизирующие свойства от анаболических и остается в общественном сознании в основном как пиньята в средствах массовой информации. В этой главе будет использоваться более подходящий термин, охватывающий незаконное использование всех доступных андрогенов, – злоупотребление андрогенами.
После перерыва во Второй мировой войне разработка синтетических стероидов в фармацевтической промышленности включала преследование цели создания невирилизирующего андрогена («анаболического стероида»), потенциально подходящего для использования для получения фармакологического андрогенного эффекта у женщин и детей. [...] промышленные поиски «анаболических стероидов», основанных на разграничении вирилизирующего и анаболического эффектов андрогенов, потерпели неудачу. Теперь это понятно в свете более позднего открытия единственного AR вместе с ошибочными интерпретациями относительно неспецифических биоанализов на цельных животных, которые затем использовались для скрининга синтетических стероидов на предмет предположительно различных анаболических и вирилизирующих эффектов. Тем не менее, несмотря на отказ отрасли от этого бесплодного начинания к 1980 году и его недавнюю реинкарнацию под предлогом разработки «селективного AR-модулятора» (SARM) [6], пустая концепция «анаболического стероида» сохраняется как нечеткое определение. и вводящая в заблуждение научная терминология [7, 8] . В этой статье более точный и ясный термин «андроген» используется исключительно как для эндогенных, так и для синтетических андрогенов, но включает в себя ссылки на химические вещества, которые в других местах широко определены как «анаболические стероиды» или «анаболикандрогенные стероиды», что сбивает с толку, проводя устаревшее различие, где нет никакой разницы.
Разработка нестероидных андрогенов, продаваемых как «селективные модуляторы андрогенных рецепторов» (SARM), открывает новые возможности для адъювантной фармакологической терапии андрогенами. В отличие от полного спектра андрогенных эффектов тестостерона, такие SARMs будут чистыми андрогенами, не подверженными тканеспецифической активации путем ароматизации до соответствующего эстрогена или усилению андрогенной активности за счет 5а-восстановления. В этом контексте эндогенные чистые андрогены нандролон и ДГТ можно рассматривать как прототипы SARM. SARM не являются современным воплощением так называемых «анаболических стероидов», устаревшего термина, обозначающего гипотетические, но несуществующие невирилизирующие андрогены, нацеленные исключительно на мышцы, — неудачная концепция, не имеющая биологического подтверждения принципа (Handelsman 2011).
Идентификация единственного гена и белка рецептора андрогенов в 1988 г. (584-586) объясняет физиологическое наблюдение о том, что в эквивалентных дозах все андрогены оказывают по существу схожие эффекты (587). Термин «анаболический стероид» был изобретен во время золотого века стероидной фармакологии после Второй мировой войны для определения идеализированного андрогена, лишенного вирилизирующих свойств, но сохраняющего миотрофические свойства, чтобы его можно было безопасно использовать у детей и женщин. Хотя этот поиск оказался иллюзорным и был оставлен после того, как все усилия отрасли не смогли идентифицировать такой гипотетический синтетический андроген, устаревший термин «анаболический стероид» сохраняется в основном как мрачное описание в популярных средствах массовой информации, несмотря на то, что продолжают проводить ложное различие там, где нет разницы. Лучшее понимание метаболической активации андрогенов посредством 5α-восстановления и ароматизации в тканях-мишенях, а также тканеспецифичных свойств частичных агонистов/антагонистов некоторых синтетических андрогенов может привести к более физиологическим концепциям тканеспецифического действия андрогенов («специфический модулятор андрогенных рецепторов»). ) регулируется физиологическими процессами пререцепторной активации андрогенов, а также пострецепторным взаимодействием с белками-корегуляторами, аналогичными развитию синтетических частичных агонистов эстрогена с тканевой специфичностью («специфический модулятор эстрогеновых рецепторов») (588). Потенциал новых клинических терапевтических показаний новых тканеселективных андрогенов в клинической разработке еще предстоит полностью оценить (589).
Анаболически-андрогенные стероиды (ААС) представляют собой класс природных и синтетических гормонов, которые получили свое название благодаря своей химической структуре (стероидное ядро, см. Рисунок 1) и биологическим эффектам (анаболическим и андрогенным), которые они вызывают. Под анаболизмом понимаются свойства ААС в наращивании скелетных мышц, тогда как под андрогенным подразумевается индукция и поддержание мужских вторичных половых признаков (что в принципе включает в себя анаболическое действие, что делает этот термин оксюмороном (1)).