
Карбонат кальция представляет собой химическое соединение с химической формулой Ca CO 3 . Это обычное вещество, встречающееся в горных породах в виде минералов кальцита и арагонита , особенно в меле и известняке , яичной скорлупе , панцирях брюхоногих моллюсков , скелетах моллюсков и жемчуге . Материалы, содержащие много карбоната кальция или напоминающие его, называются известковыми . Карбонат кальция является активным ингредиентом сельскохозяйственной извести и образуется, когда ионы кальция в жесткой воде реагируют с ионами карбоната , образуя известковый налет . Он используется в медицинских целях в качестве добавки кальция или антацида , но чрезмерное употребление может быть опасным и вызвать гиперкальциемию и проблемы с пищеварением. [8]
Карбонат кальция разделяет типичные свойства других карбонатов . Примечательно, что
Карбонат кальция реагирует с водой, насыщенной углекислым газом, с образованием растворимого бикарбоната кальция .
Эта реакция важна при эрозии карбонатных пород , образуя каверны , и приводит к образованию жесткой воды во многих регионах.
Необычной формой карбоната кальция является гексагидрат икаита CaCO 3 · 6H 2 O. Икаит стабилен только при температуре ниже 8 °C.
Подавляющее большинство карбоната кальция, используемого в промышленности, добывается в горнодобывающей промышленности. Чистый карбонат кальция (например, для пищевых или фармацевтических целей) можно производить из чистого карьерного источника (обычно мрамора ).
Альтернативно карбонат кальция получают из оксида кальция . Добавляют воду, чтобы получить гидроксид кальция , затем через этот раствор пропускают диоксид углерода для осаждения желаемого карбоната кальция, называемого в промышленности осажденным карбонатом кальция (PCC). Этот процесс называется карбонатацией : [9]
В лаборатории карбонат кальция можно легко кристаллизовать из хлорида кальция (CaCl 2 ), поместив водный раствор CaCl 2 в эксикатор рядом с карбонатом аммония (NH4) 2 CO 3 . [10] В эксикаторе карбонат аммония подвергается воздействию воздуха и разлагается на аммиак, углекислый газ и воду. Затем диоксид углерода диффундирует в водный раствор хлорида кальция, реагирует с ионами кальция и водой и образует карбонат кальция.
Термодинамически стабильной формой CaCO 3 при нормальных условиях является гексагональный β- CaCO 3 (минерал кальцит ). Могут быть получены и другие формы: более плотная (2,83 г/см 3 ) ромбическая λ- CaCO 3 (минерал арагонит ) и гексагональная µ- CaCO 3 , встречающаяся в виде минерала ватерита . Форму арагонита можно получить осаждением при температуре выше 85 °С; форму ватерита можно получить осаждением при 60 °C. Кальцит содержит атомы кальция, координированные шестью атомами кислорода; в арагоните они координированы девятью атомами кислорода. [ нужна цитация ] Структура ватерита до конца не изучена. [11] Карбонат магния ( MgCO 3 ) имеет структуру кальцита, тогда как карбонат стронция ( SrCO 3 ) и карбонат бария ( BaCO 3 ) принимают структуру арагонита, что отражает их больший ионный радиус . [ нужна цитата ]
Карбонат кальция кристаллизуется в трех безводных полиморфах , [12] [13] из которых кальцит термодинамически наиболее стабилен при комнатной температуре, арагонит лишь немного менее устойчив, а ватерит является наименее стабильным. [14]
Кристаллическая структура кальцита тригональная , с пространственной группой (№ 167 в Международных таблицах кристаллографии [15] ) и символом Пирсона . [16] Арагонит ромбический , с пространственной группой ( № 62) и символом Пирсона . [17] Ватерит состоит как минимум из двух различных сосуществующих кристаллографических структур. Основная структура демонстрирует гексагональную симметрию в пространственной группе , второстепенная структура до сих пор неизвестна. [18]

Все три полиморфные модификации кристаллизуются одновременно из водных растворов в условиях окружающей среды. [14] В водных растворах без добавок кальцит легко образуется в качестве основного продукта, тогда как арагонит появляется только в качестве второстепенного продукта.
При высоком насыщении ватерит обычно выделяется первой фазой, за которой следует превращение ватерита в кальцит. [19] Такое поведение, по-видимому, соответствует правилу Оствальда , согласно которому сначала кристаллизуется наименее стабильная полиморфная модификация, за которой следует кристаллизация различных полиморфных модификаций через последовательность все более стабильных фаз. [20] Однако арагонит, чья стабильность находится между стабильностью ватерита и кальцита, по-видимому, является исключением из этого правила, поскольку арагонит не образуется в качестве предшественника кальцита в условиях окружающей среды. [14]

Арагонит возникает в большинстве случаев, когда условия реакции препятствуют образованию кальцита и/или способствуют зародышеобразованию арагонита. Например, образованию арагонита способствует присутствие ионов магния [21] или использование белков и пептидов, полученных из биологического карбоната кальция. [22] Было показано , что некоторые полиамины, такие как кадаверин и поли(этиленимин), способствуют образованию арагонита поверх кальцита. [14]
Организмы, такие как моллюски и членистоногие , продемонстрировали способность выращивать все три кристаллические полиморфы карбоната кальция, главным образом, в качестве защиты (оболочки) и прикрепления мышц. [23] Более того, они демонстрируют замечательную способность выбирать фазу по сравнению с кальцитом и арагонитом, и некоторые организмы могут переключаться между двумя полиморфами. Способность выбора фазы обычно объясняется использованием такими организмами специфических макромолекул или комбинаций макромолекул. [24] [25] [26]

Кальцит , арагонит и ватерит представляют собой чистые минералы карбоната кальция. Промышленно важные материнские породы, состоящие преимущественно из карбоната кальция, включают известняк , мел , мрамор и травертин .

Яичная скорлупа , раковины улиток и большинство морских ракушек состоят преимущественно из карбоната кальция и могут использоваться в качестве промышленных источников этого химического вещества. [28] Раковины устриц в последнее время получили признание как источник пищевого кальция, но также являются практическим промышленным источником. [29] [30] Темно- зеленые овощи, такие как брокколи и капуста , содержат значительное количество карбоната кальция с точки зрения диеты, но они непрактичны в качестве промышленного источника. [31]
За пределами Земли убедительные данные свидетельствуют о присутствии карбоната кальция на Марсе . Признаки карбоната кальция были обнаружены более чем в одном месте (особенно в кратерах Гусева и Гюйгенса ). Это дает некоторые доказательства присутствия жидкой воды в прошлом. [32] [33]

Карбонат часто встречается в геологических условиях и представляет собой огромный резервуар углерода . Карбонат кальция встречается в виде арагонита , кальцита и доломита и является важными компонентами кальциевого цикла . Карбонатные минералы образуют породы: известняк , мел , мрамор , травертин , туф и другие.

В теплых и чистых тропических водах кораллов больше, чем на полюсах, где вода холодная. Карбонат кальция, в том числе планктон (например, кокколиты и планктонные фораминиферы ), коралловые водоросли , губки , брахиоподы , иглокожие , мшанки и моллюски , обычно встречаются на мелководье, где больше солнечного света и фильтруемой пищи. Холодноводные карбонаты действительно существуют в более высоких широтах, но имеют очень медленную скорость роста. Процессы кальцификации сменяются закислением океана .
Там, где океаническая кора погружается под континентальную плиту, осадки будут переноситься в более теплые зоны астеносферы и литосферы . В этих условиях карбонат кальция разлагается с образованием углекислого газа , который вместе с другими газами вызывает взрывные извержения вулканов .
Глубина компенсации карбоната (CCD) — это точка в океане, где скорость осаждения карбоната кальция уравновешивается скоростью растворения в зависимости от существующих условий. Глубоко в океане температура падает, а давление увеличивается. Повышение давления также увеличивает растворимость карбоната кальция. Карбонат кальция необычен тем, что его растворимость увеличивается с понижением температуры. [34] Глубина компенсации карбонатов колеблется от 4000 до 6000 метров ниже уровня моря в современных океанах, а различные полиморфы (кальцит, арагонит) имеют разные глубины компенсации в зависимости от их стабильности. [35]
Карбонат кальция может сохранять окаменелости посредством перминерализации . Большинство окаменелостей позвоночных формации Ту Медисин — геологической формации , известной своими яйцами утконосых динозавров — сохранились благодаря перминерализации CaCO 3 . [36] Этот тип консервации сохраняет высокий уровень детализации, даже вплоть до микроскопического уровня. Однако это также делает образцы уязвимыми для атмосферных воздействий при воздействии на поверхность. [36]
Когда-то считалось, что популяции трилобитов составляли большую часть водной жизни в кембрийском периоде из-за того, что их богатые карбонатом кальция панцири легче сохранялись, чем панцири других видов [37] , которые имели чисто хитиновые панцири.
Карбонат кальция в основном используется в строительной промышленности, либо в качестве строительного материала, либо в качестве заполнителя известняка для дорожного строительства, в качестве ингредиента цемента или в качестве исходного материала для приготовления строительной извести путем обжига в печи . Однако из-за выветривания, вызванного главным образом кислотными дождями , [38] карбонат кальция (в форме известняка) больше не используется в строительных целях сам по себе, а только в качестве первичного сырья для строительных материалов.
Карбонат кальция применяется также при очистке железа из железной руды в доменной печи . Карбонат прокаливают на месте с получением оксида кальция , который образует шлак с различными примесями и отделяется от очищенного железа. [39]
В нефтяной промышленности карбонат кальция добавляют в буровые растворы в качестве агента, закупоривающего пласт и фильтрационной корки; это также утяжелитель, который увеличивает плотность буровых растворов для контроля забойного давления. Карбонат кальция добавляется в бассейны в качестве корректора pH для поддержания щелочности и компенсации кислотных свойств дезинфицирующего средства . [40]
Он также используется в качестве сырья при рафинировании сахара из сахарной свеклы ; его прокаливают в печи с антрацитом для получения оксида кальция и углекислого газа. Эту жженую известь затем гасят в пресной воде для получения суспензии гидроксида кальция для осаждения примесей в сыром соке во время карбонизации . [41]
Карбонат кальция в виде мела традиционно был основным компонентом мела для школьных досок. Однако современный мел, выпускаемый в основном, представляет собой гипс , гидрат сульфата кальция CaSO 4 ·2H 2 O. Карбонат кальция является основным источником для выращивания биокамней . Осажденный карбонат кальция (PCC), предварительно диспергированный в форме суспензии , является распространенным наполнителем для латексных перчаток с целью достижения максимальной экономии материалов и производственных затрат. [42]
Мелкоизмельченный карбонат кальция (GCC) является важным ингредиентом микропористой пленки, используемой в подгузниках и некоторых строительных пленках, поскольку поры зарождаются вокруг частиц карбоната кальция во время изготовления пленки путем двухосного растяжения. GCC и PCC используются в качестве наполнителя бумаги , поскольку они дешевле древесного волокна . Бумага для печати и письма может содержать 10–20% карбоната кальция. В Северной Америке карбонат кальция начал заменять каолин при производстве глянцевой бумаги . В Европе уже несколько десятилетий практикуется производство щелочной или бескислотной бумаги. PCC, используемый для наполнителя бумаги и покрытия бумаги, осаждается и приготавливается различных форм и размеров, имеющих характерный узкий гранулометрический состав и эквивалентные сферические диаметры от 0,4 до 3 микрометров. [ нужна цитата ]
Карбонат кальция широко используется в качестве наполнителя в красках , [43] в частности, в матовых эмульсионных красках , где обычно 30% по весу краски составляет мел или мрамор. Это также популярный наполнитель пластмасс. [43] Некоторые типичные примеры включают от 15 до 20% загрузки мела в водосточные трубы из непластифицированного поливинилхлорида (НПВХ) , от 5% до 15% загрузки мела или мрамора, покрытого стеаратом , в оконный профиль ПВХ. В кабелях из ПВХ можно использовать карбонат кальция при нагрузке до 70 частей на сто частей смолы для улучшения механических свойств (прочности на разрыв и удлинения) и электрических свойств (объемного удельного сопротивления). [ нужна цитата ] Полипропиленовые соединения часто наполняются карбонатом кальция для увеличения жесткости, требование, которое становится важным при высоких температурах использования. [44] Здесь процент часто составляет 20–40%. Он также обычно используется в качестве наполнителя в термореактивных смолах (листовых и объемных формовочных компаундах) [44] , а также смешивается с АБС-пластиком и другими ингредиентами для формирования некоторых типов «глиняных» фишек для покера, полученных прессованием . [45] Осажденный карбонат кальция, полученный путем добавления оксида кальция в воду, используется сам по себе или с добавками в качестве белой краски, известной как побелка . [46] [47]
Карбонат кальция добавляется во многие клеи , герметики и отделочные шпатлевки своими руками . [43] Клеи для керамической плитки обычно содержат от 70% до 80% известняка. Заполнители для декоративных трещин содержат аналогичные уровни мрамора или доломита. Его также смешивают с замазкой при установке витражей и в качестве резиста, чтобы предотвратить прилипание стекла к полкам печи при обжиге глазурей и красок при высоких температурах. [48] [49] [50] [51]
При производстве керамической глазури карбонат кальция известен как белила [ 43] и является распространенным ингредиентом для многих глазурей в форме белого порошка. Когда глазурь, содержащую этот материал, обжигается в печи, белила действуют как флюс в глазури. Молотый карбонат кальция представляет собой абразив (как в качестве чистящего порошка, так и в качестве ингредиента бытовых чистящих кремов), особенно в его кальцитовой форме, который имеет относительно низкий уровень твердости (3 по шкале Мооса ) и поэтому не царапает стекло и большинство другая керамика , эмаль , бронза , железо и сталь , а также оказывают умеренное воздействие на более мягкие металлы, такие как алюминий и медь . Для очистки серебра от потускнения можно использовать пасту из карбоната кальция и деионизированной воды . [52]

Карбонат кальция широко используется в медицине как недорогая пищевая добавка кальция в качестве желудочного антацида [53] (например, Tums и Eno ). Его можно использовать в качестве фосфатсвязывающего средства для лечения гиперфосфатемии (прежде всего у пациентов с хронической почечной недостаточностью ). Его используют в фармацевтической промышленности в качестве инертного наполнителя для таблеток и других фармацевтических препаратов . [54]
Карбонат кальция используется в производстве оксида кальция, а также зубной пасты, и вновь стал использоваться в качестве пищевого консерванта и фиксатора цвета при использовании в таких продуктах, как органические яблоки, или вместе с ними. [55]
Карбонат кальция применяется в терапевтических целях в качестве фосфатсвязывающего средства у пациентов, находящихся на поддерживающем гемодиализе . Это наиболее распространенная форма фосфатсвязывающих препаратов, особенно при недиализной хронической болезни почек. Карбонат кальция является наиболее часто используемым фосфатсвязывающим средством, но врачи все чаще назначают более дорогие фосфатсвязывающие средства, не содержащие кальция, особенно севеламер .
Избыток кальция в пищевых добавках, обогащенных продуктах и диетах с высоким содержанием кальция может вызвать молочно-щелочной синдром , который имеет серьезную токсичность и может привести к летальному исходу. В 1915 году Бертрам Сиппи ввел «режим Сиппи», заключающийся в ежечасном приеме молока и сливок и постепенном добавлении яиц и приготовленных хлопьев в течение 10 дней в сочетании со щелочными порошками, что обеспечивало симптоматическое облегчение язвенной болезни. В течение следующих нескольких десятилетий режим Сиппи приводил к почечной недостаточности , алкалозу и гиперкальциемии , в основном у мужчин с язвенной болезнью. Эти побочные эффекты были устранены после прекращения приема препарата, но у некоторых пациентов с длительной рвотой это привело к летальному исходу. Молочно-щелочной синдром уменьшился у мужчин после появления эффективных методов лечения язвенной болезни. С 1990-х годов о нем чаще всего сообщалось у женщин, принимающих добавки кальция в дозах, превышающих рекомендуемый диапазон от 1,2 до 1,5 граммов в день, для профилактики и лечения остеопороза [56] [57] и усугубляющееся обезвоживанием . Кальций добавляется в безрецептурные продукты, что способствует непреднамеренному его чрезмерному потреблению. Чрезмерное потребление кальция может привести к гиперкальциемии, осложнениями которой являются рвота, боли в животе и изменение психического статуса. [58]
В качестве пищевой добавки он имеет обозначение E170 , [59] и номер INS 170. Используется в качестве регулятора кислотности , противослеживающего агента , стабилизатора или красителя . Он одобрен для использования в ЕС, [60] США [61] и Австралия и Новая Зеландия . [62] Он «добавляется по закону во всю муку из молотого хлеба в Великобритании, кроме цельнозерновой». [63] [64] Он используется в некоторых соевых и миндальных молочных продуктах в качестве источника пищевого кальция; по крайней мере, одно исследование предполагает, что карбонат кальция может быть таким же биодоступным , как и кальций в коровьем молоке . [65] Карбонат кальция также используется в качестве укрепляющего агента во многих консервированных и бутилированных овощных продуктах.
Было документально подтверждено, что несколько составов добавок кальция содержат химический элемент свинец , [66] что представляет собой проблему для общественного здравоохранения . [67] Свинец обычно содержится в природных источниках кальция. [66]
Сельскохозяйственная известь , порошкообразный мел или известняк используются как дешевый метод нейтрализации кислой почвы , что делает ее пригодной для посадки, а также используется в аквакультуре для регулирования pH почвы пруда перед началом выращивания. [68] Существует интерес к пониманию того, может ли это повлиять на адсорбцию и десорбцию пестицидов в известковой почве. [69]
Карбонат кальция является ключевым ингредиентом многих бытовых чистящих порошков, таких как Comet , и используется в качестве чистящего средства.
В 1989 году исследователь Кен Симмонс ввел CaCO 3 в ручей Уэтстоун в Массачусетсе . [70] Он надеялся, что карбонат кальция нейтрализует кислоту в ручье от кислотных дождей и спасет форель, которая перестала нереститься. Хотя его эксперимент увенчался успехом, он увеличил количество ионов алюминия в той части ручья, которая не была обработана известняком. Это показывает, что CaCO 3 можно добавлять для нейтрализации воздействия кислотных дождей на речные экосистемы. В настоящее время карбонат кальция используется для нейтрализации кислой среды как в почве, так и в воде. [71] [72] [73] С 1970-х годов такое известкование практикуется в больших масштабах в Швеции для смягчения закисления, и несколько тысяч озер и ручьев известковываются неоднократно. [74]
Карбонат кальция также используется для обессеривания дымовых газов , устраняя вредные выбросы SO 2 и NO 2 из угля и других видов ископаемого топлива, сжигаемых на крупных электростанциях, работающих на ископаемом топливе. [71]
Обжиг известняка с использованием древесного угля для получения негашеной извести практиковался с древних времен в культурах всего мира . Температура, при которой известняк образует оксид кальция, обычно составляет 825 ° C, но указание абсолютного порога вводит в заблуждение. Карбонат кальция существует в равновесии с оксидом кальция и углекислым газом при любой температуре. При каждой температуре существует парциальное давление углекислого газа, находящееся в равновесии с карбонатом кальция. При комнатной температуре равновесие в подавляющем большинстве благоприятствует карбонату кальция, поскольку равновесное давление CO 2 составляет лишь небольшую часть парциального давления CO 2 в воздухе, которое составляет около 0,035 кПа.
При температуре выше 550 °С равновесное давление СО 2 начинает превышать давление СО 2 в воздухе. Так, при температуре выше 550°C карбонат кальция начинает выделять CO2 в воздух. Однако в печи, работающей на угле, концентрация CO 2 будет намного выше, чем в воздухе. Действительно, если весь кислород в печи израсходуется при пожаре, то парциальное давление CO 2 в печи может достигать 20 кПа. [75]
Из таблицы видно, что это парциальное давление не достигается до тех пор, пока температура не достигнет почти 800 °C. Чтобы выделение CO 2 из карбоната кальция происходило с экономически выгодной скоростью, равновесное давление должно значительно превышать давление CO 2 в окружающей среде . И чтобы это произошло быстро, равновесное давление должно превысить общее атмосферное давление в 101 кПа, что происходит при 898 °C.

Карбонат кальция плохо растворяется в чистой воде (47 мг/л при нормальном атмосферном парциальном давлении CO 2 , как показано ниже).
Равновесие его раствора задается уравнением (с растворенным карбонатом кальция справа):
где произведение растворимости [Ca 2+ ][CO2-3] задается где угодно от K sp =3,7 × 10 −9 до K sp =8,7 × 10–9 при 25 ° C , в зависимости от источника данных. [76] [77] Это уравнение означает, что произведение молярной концентрации ионов кальция ( молей растворенного Ca 2+ на литр раствора) на молярную концентрацию растворенного CO2-3не может превышать значения K sp . Это, казалось бы, простое уравнение растворимости, однако, необходимо рассматривать наряду с более сложным уравнением равновесия углекислого газа с водой (см. Угольная кислота ). Некоторые из CO2-3соединяется с Н + в растворе по
ОЗС−3известен как бикарбонат- ион. Бикарбонат кальция во много раз более растворим в воде, чем карбонат кальция, и действительно существует только в растворе.
Некоторые из ОХС−3соединяется с Н + в растворе по
Часть H 2 CO 3 распадается на воду и растворенный углекислый газ согласно
А растворенный углекислый газ находится в равновесии с углекислым газом атмосферы согласно
Для окружающего воздуха PCO 2 составляет около3,5 × 10 −4 атмосфер (или что эквивалентно 35 Па ). Последнее уравнение выше определяет концентрацию растворенного CO 2 как функцию P CO 2 независимо от концентрации растворенного CaCO 3 . При атмосферном парциальном давлении CO 2 концентрация растворенного CO 2 равна1,2 × 10 −5 моль на литр. Уравнение перед этим фиксирует концентрацию H 2 CO 3 как функцию концентрации CO 2 . Для [ CO 2 ] =1,2 × 10 −5 , это приводит к тому, что [H 2 CO 3 ] =2,0 × 10 −8 моль на литр. Если известно [H 2 CO 3 ] , остальные три уравнения вместе с
(что справедливо для всех водных растворов), а также тот факт, что раствор должен быть электрически нейтральным, т. е. общий заряд растворенных положительных ионов [Ca 2+ ] + 2 [H + ] должен уравновешиваться общим зарядом растворенные отрицательные ионы [HCO−3] + [КО2-3] + [OH − ] , позволяют одновременно решить оставшиеся пять неизвестных концентраций (упомянутая ранее форма нейтральности действительна только в том случае, если карбонат кальция был приведен в контакт с чистой водой или раствором с нейтральным pH; в В случае, когда исходный pH водного растворителя не является нейтральным, баланс не является нейтральным).
В соседней таблице показаны результаты для [Ca 2+ ] и [H + ] (в виде pH) в зависимости от парциального давления CO 2 окружающей среды ( K sp =Для расчета принято 4,47 × 10-9 ) .
Эффект последнего особенно заметен в повседневной жизни людей, имеющих жесткую воду. Вода в подземных водоносных горизонтах может подвергаться воздействию CO 2 в уровнях , значительно превышающих атмосферные. Когда такая вода просачивается через карбонат кальция, CaCO 3 растворяется по второй тенденции. Когда та же самая вода затем выходит из крана, со временем она приходит в равновесие с уровнем CO 2 в воздухе, выделяя избыток CO 2 . В результате карбонат кальция становится менее растворимым, а его избыток выпадает в осадок в виде известкового налета. Этот же процесс ответственен за образование сталактитов и сталагмитов в известняковых пещерах.
Две гидратированные фазы карбоната кальция, моногидрокальцит CaCO 3 ·H 2 O и икаит CaCO 3 ·6H 2 O , могут осаждаться из воды в условиях окружающей среды и сохраняться в виде метастабильных фаз.
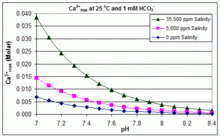
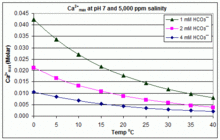
В отличие от описанного выше сценария открытого равновесия, управление многими плавательными бассейнами осуществляется путем добавления примерно 2 мМ бикарбоната натрия ( NaHCO 3 ) в качестве буфера, а затем контроля pH с помощью HCl, NaHSO 4 , Na 2 CO 3 , NaOH или хлорсодержащие составы, кислые или основные. В этой ситуации растворенный неорганический углерод ( общий неорганический углерод ) находится далеко от равновесия с атмосферным CO 2 . Прогресс к равновесию за счет выделения CO 2 замедляется
В этой ситуации константы диссоциации для гораздо более быстрых реакций
позволяют прогнозировать концентрацию каждого растворенного неорганического углерода в растворе на основе добавленной концентрации HCO .−3(что составляет более 90% видов участка Бьеррум с pH от 7 до pH 8 при 25 °C в пресной воде). [79] Добавление HCO−3увеличит CO2-3концентрация при любом pH. Переставляя приведенные выше уравнения, видим, что [Ca 2+ ] =К сп/[ Колорадо2-3]и [ CO2-3"="K a2 [ HCO−3]/[ Ч + ]. Поэтому, когда ОХС−3концентрация известна, максимальную концентрацию ионов Ca 2+ до отложения через осаждение CaCO 3 можно предсказать по формуле:
Произведение растворимости CaCO 3 ( K sp ) и константы диссоциации растворенных неорганических частиц углерода (включая K a2 ) существенно зависят от температуры и солености [79] с общим эффектом, что [ Ca 2+ ] max увеличивается с пресной воды в соленую и уменьшается с повышением температуры, pH или добавленного уровня бикарбоната, как показано на прилагаемых графиках.
Тенденции являются показательными для управления пулом, но возникновение отложений также зависит от других факторов, включая взаимодействие с Mg 2+ , [B(OH) 4 ] - и другими ионами в пуле, а также эффекты пересыщения. [80] [81] Отложения накипи обычно наблюдаются в электролитических генераторах хлора, где наблюдается высокий уровень pH вблизи поверхности катода, а отложение накипи еще больше повышает температуру. Это одна из причин, по которой некоторые операторы бассейнов предпочитают борат бикарбонату в качестве основного буфера pH и избегают использования химикатов для бассейнов, содержащих кальций. [82]
В продаже имеются растворы сильной ( HCl ), умеренно сильной ( сульфаминовой ) или слабой ( уксусной , лимонной , сорбиновой , молочной , фосфорной ) кислот. Их обычно используют в качестве средств для удаления накипи . Максимальное количество CaCO 3 , которое можно «растворить» в одном литре раствора кислоты, можно рассчитать с помощью приведенных выше уравнений равновесия.


{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ){{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )