Индий — химический элемент ; он имеет символ In и атомный номер 49. Это серебристо-белый постпереходный металл и один из самых мягких элементов. По химическому составу индий подобен галлию и таллию , а его свойства в значительной степени являются промежуточными между ними. [9] Он был открыт в 1863 году Фердинандом Райхом и Иеронимом Теодором Рихтером с помощью спектроскопических методов и назван в честь синей линии индиго в его спектре. [10]
Индий — технологически важный элемент , используемый в основном в производстве плоских дисплеев в виде оксида индия и олова (ITO) , прозрачного и проводящего покрытия, наносимого на стекло. [11] [12] [13] Индий также используется в полупроводниковой промышленности , [14] в легкоплавких металлических сплавах , таких как припои и высоковакуумные уплотнения из мягких металлов. Его получают исключительно как побочный продукт при переработке руд других металлов, главным образом сфалерита и других сульфидных цинковых руд . [15]
Индий не играет биологической роли, а его соединения токсичны при вдыхании или попадании в кровоток, хотя при проглатывании они плохо всасываются. [16] [17]

Индий — серебристо-белый, очень пластичный постпереходный металл с ярким блеском . [18] Он настолько мягкий ( твердость по шкале Мооса 1,2), что его можно резать ножом, и при растирании на бумаге он оставляет видимые линии. [19] Он входит в 13-ю группу периодической таблицы , и его свойства в основном занимают промежуточное положение между его вертикальными соседями галлием и таллием . Как и олово , при сгибании индия слышен пронзительный крик – потрескивающий звук из-за двойникования кристаллов . [18] Как и галлий, индий способен смачивать стекло. Как и оба, индий имеет низкую температуру плавления - 156,60 ° C (313,88 ° F); выше, чем у его более легкого гомолога галлия, но ниже, чем у его более тяжелого гомолога таллия, и ниже, чем у олова. [20] Температура кипения составляет 2072 ° C (3762 ° F), что выше, чем у таллия, но ниже, чем у галлия, в отличие от общей тенденции температур плавления, но аналогично тенденциям снижения других групп постпереходных металлов, потому что о слабости металлической связи с небольшим количеством делокализованных электронов . [21]
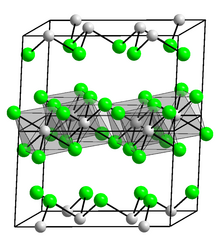
Плотность индия 7,31 г/см 3 также больше, чем у галлия, но ниже, чем у таллия. Ниже критической температуры 3,41 К индий становится сверхпроводником . Индий кристаллизуется в объемноцентрированной тетрагональной кристаллической системе в пространственной группе I 4/ ммм ( параметры решетки : а = 325 пм , с = 495 пм): [20] это слегка искаженная гранецентрированная кубическая структура, где каждый индий У атома есть четыре соседа на расстоянии 15:24 и восемь соседей чуть дальше (336:00). [22] Индий обладает большей растворимостью в жидкой ртути, чем любой другой металл (более 50 массовых процентов индия при 0 ° C). [23] Индий демонстрирует пластичную вязкопластическую реакцию, которая, как выяснилось, не зависит от размера при растяжении и сжатии. Однако он имеет размерный эффект при изгибе и вдавливании, связанный с длиной порядка 50–100 мкм [24] , что значительно больше по сравнению с другими металлами.
Индий имеет 49 электронов с электронной конфигурацией [ Kr ]4d 10 5s 2 5p 1 . В соединениях индий чаще всего отдает три крайних электрона, превращаясь в индий (III), In 3+ . В некоторых случаях пара 5s-электронов не отдается, в результате чего образуется индий(I), In + . Стабилизация одновалентного состояния объясняется эффектом инертной пары , при котором релятивистские эффекты стабилизируют 5s-орбиталь, наблюдаемую в более тяжелых элементах. Таллий (более тяжелый гомолог индия ) демонстрирует еще более сильный эффект, в результате чего окисление до таллия (I) более вероятно, чем до таллия (III) [25] , тогда как галлий (более легкий гомолог индия) обычно показывает только степень окисления +3. Таким образом, хотя таллий (III) является умеренно сильным окислителем , индий (III) им не является, а многие соединения индия (I) являются мощными восстановителями . [26] Хотя энергия, необходимая для включения s-электронов в химическую связь, является самой низкой для индия среди металлов группы 13, энергии связи уменьшаются вниз по группе, так что у индия энергия, высвобождаемая при образовании двух дополнительных связей и достижении +3 состояния не всегда достаточно, чтобы перевесить энергию, необходимую для участия 5s-электронов. [27] Оксид и гидроксид индия (I) являются более основными, а оксид и гидроксид индия (III) более кислыми. [27]
Для индия [28] приводится ряд стандартных электродных потенциалов в зависимости от исследуемой реакции , отражающих пониженную стабильность степени окисления +3: [22]
Металлический индий не реагирует с водой, но окисляется более сильными окислителями, такими как галогены, с образованием соединений индия (III). Он не образует борида , силицида или карбида , а гидрид InH 3 в лучшем случае имеет временное существование в эфирных растворах при низких температурах, будучи достаточно нестабильным, чтобы самопроизвольно полимеризоваться без координации. [26] Индий является довольно основным в водных растворах, проявляя лишь незначительные амфотерные характеристики, и в отличие от своих более легких гомологов алюминия и галлия, он нерастворим в водных щелочных растворах. [29]
Индий имеет 39 известных изотопов , массовое число которых варьируется от 97 до 135. Только два изотопа встречаются в природе в виде первичных нуклидов : индий-113, единственный стабильный изотоп , и индий-115, период полураспада которого составляет 4,41 × 10 .14 лет, что на четыре порядка превышает возраст Вселенной и почти в 30 000 раз превышает период полураспада тория-232 . [30] Период полураспада 115 In очень велик, поскольку бета-распад до 115 Sn запрещен по спину . [31] Индий-115 составляет 95,7% всего индия. Индий — один из трех известных элементов (остальные — теллур и рений ), стабильный изотоп которых менее распространен в природе, чем долгоживущие первичные радиоизотопы. [32]
Самый стабильный искусственный изотоп — индий-111 с периодом полураспада примерно 2,8 дня. Все остальные изотопы имеют период полураспада менее 5 часов. Индий также имеет 47 метасостояний, среди которых индий-114m1 (период полураспада около 49,51 дня) является наиболее стабильным, более стабильным, чем основное состояние любого изотопа индия, кроме первичного. Весь распад происходит путем изомерного перехода . Изотопы индия легче 113 In преимущественно распадаются в результате захвата электронов или эмиссии позитронов с образованием изотопов кадмия , тогда как изотопы индия тяжелее 113 In преимущественно распадаются в результате бета-минус-распада с образованием изотопов олова. [30]
Оксид индия(III) In 2 O 3 образуется при сгорании металлического индия на воздухе или при нагревании гидроксида или нитрата. [33] In 2 O 3 имеет структуру, подобную оксиду алюминия , и является амфотерным, то есть способен реагировать как с кислотами, так и с основаниями. Индий реагирует с водой с образованием растворимого гидроксида индия (III) , который также является амфотерным; со щелочами с получением индатов(III); и с кислотами для получения солей индия (III):
Известны также аналогичные сескви-халькогениды с серой , селеном и теллуром . [34] Индий образует ожидаемые тригалогениды . Хлорирование, бромирование и йодирование In дают бесцветные InCl 3 , InBr 3 и желтый InI 3 . Соединения представляют собой кислоты Льюиса , чем-то похожие на более известные тригалогениды алюминия. Опять же, как и родственное соединение алюминия, InF 3 является полимерным. [35]
Прямая реакция индия с пниктогенами приводит к образованию серых или полуметаллических полупроводников III–V . Многие из них медленно разлагаются во влажном воздухе, что обусловливает необходимость бережного хранения полупроводниковых соединений во избежание контакта с атмосферой. Нитрид индия легко подвергается воздействию кислот и щелочей. [36]
Соединения индия (I) встречаются нечасто. Хлорид, бромид и йодид имеют глубокую окраску, в отличие от исходных тригалогенидов, из которых они получены. Фторид известен только как нестабильное газообразное соединение. [37] Черный порошок оксида индия (I) образуется при разложении оксида индия (III) при нагревании до 700 °C. [33]
Реже индий образует соединения со степенью окисления +2 и даже дробными степенями окисления. Обычно такие материалы имеют связь In-In, особенно в галогенидах In 2 X 4 и [In 2 X 6 ] 2- , [38] и различных субхалькогенидах, таких как In 4 Se 3 . [39] Известно несколько других соединений, объединяющих индий(I) и индий(III), например In I 6 (In III Cl 6 )Cl 3 , [40] In I 5 (In III Br 4 ) 2 (In III Бр 6 ), [41] и В I В III Бр 4 . [38]
Индийорганические соединения содержат связи In–C. Большинство из них являются производными In(III), но циклопентадиенилиндий(I) является исключением. Это было первое известное индийорганическое соединение [42] и оно является полимерным, состоящим из зигзагообразных цепочек чередующихся атомов индия и циклопентадиенильных комплексов . [43] Пожалуй, самым известным индийорганическим соединением является триметилиндий In(CH 3 ) 3 , используемый для приготовления некоторых полупроводниковых материалов. [44] [45]
В 1863 году немецкие химики Фердинанд Райх и Иероним Теодор Рихтер тестировали руду из рудников вокруг Фрайберга, Саксония . Они растворяли минералы пирит , арсенопирит , галенит и сфалерит в соляной кислоте и перегоняли сырой хлорид цинка . Райх, который был дальтоником , нанял Рихтера в качестве помощника для обнаружения цветных спектральных линий. Зная, что руды этого региона иногда содержат таллий , они искали зеленые линии спектра излучения таллия. Вместо этого они обнаружили ярко-синюю линию. Поскольку эта синяя линия не соответствовала ни одному известному элементу, они предположили, что в минералах присутствует новый элемент. Они назвали элемент индием по цвету индиго , наблюдаемому в его спектре, в честь латинского indicum , что означает « Индийский ». [46] [10] [47] [48]
Рихтер продолжил изолировать металл в 1864 году. [49] Слиток весом 0,5 кг (1,1 фунта) был представлен на Всемирной выставке 1867 года. [50] Райх и Рихтер позже поссорились, когда последний заявил, что является единственным первооткрывателем. [48]

Индий создается в результате длительного (до тысяч лет) s-процесса (медленного захвата нейтронов) в звездах малой и средней массы (диапазон масс от 0,6 до 10 масс Солнца ). Когда атом серебра-109 захватывает нейтрон, он превращается в серебро-110, которое затем подвергается бета-распаду и становится кадмием-110. Захватывая дальнейшие нейтроны, он превращается в кадмий-115, который распадается до индия-115 в результате еще одного бета-распада . Это объясняет, почему радиоактивного изотопа больше, чем стабильного. [51] Стабильный изотоп индия, индий-113, является одним из p-ядер , происхождение которого до конца не изучено; хотя известно, что индий-113 производится непосредственно в s- и r-процессах (быстрый захват нейтронов), а также как дочка очень долгоживущего кадмия-113, период полураспада которого составляет около восьми квадриллионов лет, это не может объяснить весь индий-113. [52] [53]
Индий является 68-м по распространенности элементом в земной коре (около 50 частей на миллиард ). Это похоже на изобилие в земной коре серебра , висмута и ртути . Он очень редко образует собственные минералы или встречается в элементарной форме. Известно менее 10 минералов индия, таких как рокезит (CuInS 2 ), и ни один из них не встречается в концентрациях, достаточных для экономической добычи. [54] Вместо этого индий обычно является микроэлементом более распространенных рудных минералов, таких как сфалерит и халькопирит . [55] [56] Из них его можно извлечь в качестве побочного продукта во время плавки. [15] Хотя обогащение индия в этих месторождениях является высоким по сравнению с его содержанием в земной коре, при нынешних ценах оно недостаточно для поддержки добычи индия как основного продукта. [54]
Существуют разные оценки количества индия, содержащегося в рудах других металлов. [57] [58] Однако эти количества невозможно извлечь без добычи исходных материалов (см. «Производство и доступность»). Таким образом, доступность индия в основном определяется скоростью добычи этих руд, а не их абсолютным количеством. Этот аспект часто забывается в текущих дебатах, например, группой Гределя в Йельском университете в своих оценках критичности [59] , объясняя парадоксально низкие времена истощения, на которые ссылаются некоторые исследования. [60] [15]

Индий производится исключительно как побочный продукт при переработке руд других металлов. Его основным источником являются сульфидно-цинковые руды, в которых он преимущественно содержится сфалеритом. [15] Незначительные количества также извлекаются из сульфидных медных руд. Во время процесса обжига-выщелачивания-электролиза при выплавке цинка индий накапливается в богатых железом остатках. Из них его можно извлечь разными способами. Его также можно извлечь непосредственно из технологических растворов. Дальнейшая очистка осуществляется электролизом . [62] Точный процесс зависит от режима работы металлургического завода. [18] [15]
Его статус побочного продукта означает, что производство индия ограничено количеством сульфидных цинковых (и медных) руд, добываемых каждый год. Поэтому его наличие необходимо обсуждать с точки зрения потенциала поставок. Потенциал предложения побочного продукта определяется как количество, которое экономически можно извлечь из исходных материалов в год при текущих рыночных условиях (т. е. технологии и цене). [63] Запасы и ресурсы не имеют отношения к побочной продукции, поскольку их нельзя извлечь независимо от основной продукции. [15] По последним оценкам, потенциал поставок индия составляет как минимум 1300 т/год из сульфидных цинковых руд и 20 т/год из сульфидных медных руд. [15] Эти цифры значительно превышают текущий объем производства (655 т в 2016 г.). [64] Таким образом, значительное будущее увеличение производства побочной продукции индия будет возможно без значительного увеличения производственных затрат или цен. Средняя цена на индий в 2016 году составила 240 долларов США /кг по сравнению с 705 долларами США /кг в 2014 году. [65]
Китай является ведущим производителем индия (290 тонн в 2016 году), за ним следуют Южная Корея (195 тонн), Япония (70 тонн) и Канада (65 тонн). [64] Нефтеперерабатывающий завод Teck Resources в Трейле, Британская Колумбия , является крупным производителем индия из одного источника с объемом производства 32,5 тонны в 2005 году, 41,8 тонны в 2004 году и 36,1 тонны в 2003 году.
Основным потреблением индия во всем мире является производство ЖК-дисплеев . Спрос быстро рос с конца 1990-х по 2010 год благодаря популярности компьютерных ЖК-мониторов и телевизоров, на которые сейчас приходится 50% потребления индия. [13] Повышение эффективности производства и переработки (особенно в Японии) поддерживают баланс между спросом и предложением. По данным ЮНЕП , уровень переработки индия по окончании срока службы составляет менее 1%. [66]

В 1924 году было обнаружено, что индий обладает ценным свойством стабилизации цветных металлов , и это стало первым значительным применением этого элемента. [67] Первым крупномасштабным применением индия было покрытие подшипников высокопроизводительных авиационных двигателей во время Второй мировой войны для защиты от повреждений и коррозии ; это больше не является основным использованием элемента. [62] Новые применения были найдены в легкоплавких сплавах , припоях и электронике . В 1950-х годах крошечные шарики индия использовались для изготовления эмиттеров и коллекторов PNP -транзисторов со сплавным переходом . В середине и конце 1980-х годов большой интерес вызвала разработка полупроводников на основе фосфида индия и тонких пленок оксида индия и олова для жидкокристаллических дисплеев (ЖКД). К 1992 году применение тонких пленок стало крупнейшим конечным применением. [68] [69]
Оксид индия (III) и оксид индия-олова (ITO) используются в качестве прозрачного проводящего покрытия на стеклянных подложках в электролюминесцентных панелях. [70] Оксид индия и олова используется в качестве светофильтра в натриевых лампах низкого давления . Инфракрасное излучение отражается обратно в лампу, что повышает температуру внутри трубки и улучшает работу лампы. [69]
Индий имеет множество применений, связанных с полупроводниками . Некоторые соединения индия, такие как антимонид индия и фосфид индия , [71] являются полупроводниками с полезными свойствами: одним из прекурсоров обычно является триметилиндий (TMI), который также используется в качестве полупроводниковой легирующей примеси в полупроводниках соединений II – VI . [72] InAs и InSb используются для низкотемпературных транзисторов, а InP — для высокотемпературных транзисторов. [62] Полупроводниковые соединения InGaN и InGaP используются в светоизлучающих диодах (LED) и лазерных диодах. [73] Индий используется в фотогальванике в качестве полупроводникового селенида меди, индия, галлия (CIGS), также называемого солнечными элементами CIGS , типом тонкопленочных солнечных элементов второго поколения . [74] Индий используется в транзисторах с биполярным переходом PNP с германием : при пайке при низкой температуре индий не оказывает воздействия на германий. [62]

Индиевая проволока используется в качестве вакуумного уплотнения и теплопроводника в криогенике и сверхвысоком вакууме , а также в таких производственных приложениях, как прокладки , которые деформируются для заполнения зазоров. [75] Благодаря большой пластичности и адгезии к металлам листы индия иногда используются для холодной пайки в СВЧ- схемах и соединениях волноводов , где прямая пайка затруднена. Индий является ингредиентом галинстана из сплава галлий-индий-олово , который является жидким при комнатной температуре и заменяет ртуть в некоторых термометрах . [76] Другие сплавы индия с висмутом , кадмием , свинцом и оловом , которые имеют более высокие, но все же низкие температуры плавления (от 50 до 100 ° C), используются в спринклерных системах пожаротушения и регуляторах тепла. [62]
Индий является одним из многих заменителей ртути в щелочных батареях , предотвращающих коррозию цинка и выделение газообразного водорода. [77] Индий добавляют в некоторые сплавы стоматологической амальгамы , чтобы уменьшить поверхностное натяжение ртути, уменьшить содержание ртути и облегчить амальгамацию. [78]
Высокое сечение захвата тепловых нейтронов Индием делает его пригодным для использования в стержнях управления ядерных реакторов , обычно в сплаве, состоящем из 80% серебра , 15% индия и 5% кадмия . [79] В ядерной энергетике (n,n')-реакции 113 In и 115 In используются для определения величин нейтронных потоков. [80]
В 2009 году профессор Мас Субраманиан и бывший аспирант Эндрю Смит из Университета штата Орегон обнаружили, что индий можно объединить с иттрием и марганцем , образуя интенсивно синий , нетоксичный, инертный, устойчивый к выцветанию пигмент YInMn blue , первый новый неорганический пигмент. синий пигмент открыт через 200 лет. [81]
Индий не играет метаболической роли ни в одном организме. Подобно солям алюминия, ионы индия (III) могут быть токсичными для почек при инъекционном введении. [17] Оксид индия-олова и фосфид индия наносят вред легочной и иммунной системам, преимущественно через ионный индий, [83] хотя гидратированный оксид индия более чем в сорок раз токсичен при инъекции, если судить по количеству введенного индия. [17] Радиоактивный индий-111 (в очень небольших количествах по химическому составу) используется в тестах ядерной медицины в качестве радиофармпрепарата для отслеживания движения меченых белков и лейкоцитов в организме. [84] [85] Соединения индия в основном не всасываются при проглатывании и лишь умеренно всасываются при вдыхании; они, как правило, временно сохраняются в мышцах , коже и костях , прежде чем выводятся из организма, а биологический период полураспада индия у человека составляет около двух недель. [86]
Люди могут подвергаться воздействию индия на рабочем месте при вдыхании, проглатывании, контакте с кожей и глазами. Индиевые легкие — это заболевание легких, характеризующееся легочным альвеолярным протеинозом и фиброзом легких, впервые описанное японскими исследователями в 2003 году. По состоянию на 2010 год [обновлять]было описано 10 случаев, хотя более чем у 100 рабочих, работающих с индием, были зарегистрированы респираторные нарушения. [16] Национальный институт безопасности и гигиены труда установил рекомендуемый предел воздействия (REL) на уровне 0,1 мг/м 3 в течение восьмичасового рабочего дня. [87]
{{cite book}}: CS1 maint: числовые имена: список авторов ( ссылка )