
Кишечная микробиота , кишечный микробиом или кишечная флора — это микроорганизмы , включая бактерии , археи , грибы и вирусы , которые живут в пищеварительном тракте животных . [1] [2] Желудочно-кишечный метагеном представляет собой совокупность всех геномов кишечной микробиоты . [3] [ 4] Кишечник является основным местом расположения микробиома человека . [5] Микробиота кишечника оказывает широкое влияние, включая влияние на колонизацию , устойчивость к патогенам , поддержание эпителия кишечника , метаболизм пищевых и фармацевтических соединений, контроль иммунной функции и даже поведение через ось кишечник-мозг .
Микробный состав кишечной микробиоты варьируется в зависимости от отдела пищеварительного тракта. Толстая кишка содержит самую высокую плотность микробов среди всех изученных на данный момент микробных сообществ, связанных с человеком, и включает от 300 до 1000 различных видов . [6] Бактерии являются крупнейшим и на сегодняшний день наиболее изученным компонентом, а 99% кишечных бактерий относятся примерно к 30 или 40 видам. [7] До 60% сухой массы фекалий составляют бактерии. [8] Более 99% бактерий в кишечнике являются анаэробами , но в слепой кишке аэробные бактерии достигают высокой плотности. [5] Подсчитано, что микробиота кишечника человека содержит примерно в сто раз больше генов , чем в геноме человека .

У человека микробиота кишечника содержит наибольшее количество и виды бактерий по сравнению с другими областями тела. [9] Примерное количество бактерий, составляющих микробиоту кишечника, составляет около 10 13 –10 14 . [10] У человека кишечная флора формируется через один-два года после рождения, и к этому времени кишечный эпителий и барьер слизистой оболочки кишечника , который он секретирует, совместно развиваются таким образом, что становятся толерантными и даже поддерживают кишечную флору, что также обеспечивает барьер для патогенных организмов. [11] [12]
Отношения между некоторой кишечной микробиотой и людьми являются не просто комменсальными (безвредное сосуществование), а скорее мутуалистическими отношениями. [5] : 700 Некоторые кишечные микроорганизмы человека приносят пользу хозяину, ферментируя пищевые волокна в короткоцепочечные жирные кислоты (КЦЖК), такие как уксусная кислота и масляная кислота , которые затем усваиваются хозяином. [9] [13] Кишечные бактерии также играют роль в синтезе витамина B и витамина K , а также в метаболизме желчных кислот , стеринов и ксенобиотиков . [5] [13] Системное значение SCFAs и других соединений, которые они производят, аналогично гормонам , а сама кишечная флора, по-видимому, функционирует как эндокринный орган . [13] Нарушение регуляции кишечной флоры коррелирует с множеством воспалительных и аутоиммунных состояний. [9] [14]
Состав микробиоты кишечника человека меняется со временем, когда меняется диета и общее состояние здоровья. [9] [14] В систематическом обзоре 2016 года были изучены доклинические и небольшие исследования на людях, которые были проведены с некоторыми коммерчески доступными штаммами пробиотических бактерий, и были выявлены те из них, которые имели наибольший потенциал быть полезными при определенных заболеваниях центральной нервной системы . [15]
Микробный состав кишечной микробиоты варьируется в зависимости от пищеварительного тракта. В желудке и тонком кишечнике обычно присутствует относительно небольшое количество видов бактерий. [6] [16] Толстая кишка , напротив, содержит самую высокую плотность микробов среди всех изученных до сих пор микробных сообществ, связанных с человеком [17] : от 10 10 до 10 11 клеток на грамм кишечного содержимого. [18] Эти бактерии представляют от 300 до 1000 различных видов . [6] [16] Однако 99% бактерий относятся примерно к 30 или 40 видам. [7] Вследствие обилия бактерий в кишечнике они также составляют до 60% сухой массы фекалий . [8] Грибы , протисты , археи и вирусы также присутствуют во флоре кишечника, но об их деятельности известно меньше. [19]
Более 99% бактерий в кишечнике являются анаэробами , но в слепой кишке аэробные бактерии достигают высокой плотности. [5] Подсчитано, что эта кишечная флора содержит примерно в сто раз больше генов , чем в геноме человека . [20]
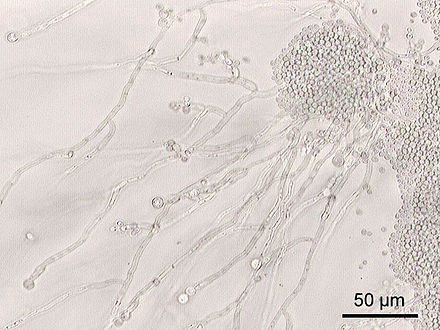
Многие виды, обитающие в кишечнике, не изучались вне их хозяев, поскольку их невозможно культивировать . [16] [7] [21] Хотя существует небольшое количество основных видов микробов, общих для большинства людей, популяции микробов могут сильно различаться. [22] Внутри человека микробная популяция остается довольно постоянной с течением времени, с некоторыми изменениями, происходящими из-за изменений в образе жизни, диете и возрасте. [6] [23] Целью проекта «Микробиом человека» было лучшее описание микробиоты кишечника человека и других частей тела. [ нужна цитата ]
Четырьмя доминирующими бактериальными типами в кишечнике человека являются Bacillota (Firmicutes), Bacteroidota , Actinomycetota и Pseudomonadota . [24] Большинство бактерий принадлежат к родам Bacteroides , Clostridium , Faecalibacterium , [6] [7] Eubacterium , Ruminococcus , Peptococcus , Peptostreptococcus и Bifidobacterium . [6] [7] Другие роды, такие как Escherichia и Lactobacillus , присутствуют в меньшей степени. [6] Одни только виды рода Bacteroides составляют около 30% всех бактерий в кишечнике, что позволяет предположить, что этот род особенно важен для функционирования организма хозяина. [16]
Роды грибов, обнаруженные в кишечнике, включают Candida , Saccharomyces , Aspergillus , Penicillium , Rhodotorula , Trametes , Pleospora , Sclerotinia , Bullera и Galactomyces , среди других. [25] [26] Rhodotorula чаще всего встречается у людей с воспалительными заболеваниями кишечника, тогда как Candida чаще всего встречается у людей с циррозом печени и хроническим гепатитом B. [25]
Археи представляют собой еще один крупный класс кишечной флоры, играющий важную роль в метаболизме бактериальных продуктов ферментации.
Индустриализация связана с изменениями в микробиоте, и сокращение разнообразия может привести к исчезновению некоторых видов; в 2018 году исследователи предложили создать биобанк микробиоты человека. [27]
Энтеротип — это классификация живых организмов, основанная на их бактериологической экосистеме в микробиоме кишечника человека, не продиктованная возрастом, полом, массой тела или национальной принадлежностью . [28] Есть признаки того, что длительная диета влияет на энтеротип. [29] Было предложено три человеческих энтеротипа, [28] [30] , но их ценность была поставлена под сомнение. [31]
Из-за высокой кислотности желудка большинство микроорганизмов не могут там выжить. Основные бактерии микробиоты желудка относятся к пяти основным типам: Firmicutes , Bacteroidetes , Actinobacteria , Fusobacteriota и Proteobacteria . Доминирующие роды — Prevotella , Streptococcus , Veillonella , Rothia , Haemophilus . [32] Взаимодействие ранее существовавшей микробиоты желудка с введением H. pylori может влиять на прогрессирование заболевания . [32] При наличии H. pylori он становится доминантом микробиоты. [33]
Тонкая кишка содержит следовые количества микроорганизмов из-за близости и влияния желудка. Грамположительные кокки и палочковидные бактерии являются преобладающими микроорганизмами, обнаруживаемыми в тонком кишечнике. [5] Однако в дистальной части тонкой кишки щелочные условия поддерживают грамотрицательные бактерии Enterobacteriaceae . [5] Бактериальная флора тонкой кишки способствует выполнению широкого спектра функций кишечника. Бактериальная флора обеспечивает регуляторные сигналы, которые обеспечивают развитие и полезность кишечника. Чрезмерный рост бактерий в тонком кишечнике может привести к кишечной недостаточности. [35] Кроме того, толстая кишка содержит крупнейшую бактериальную экосистему в организме человека. [5] Около 99% флоры толстого кишечника и фекалий состоят из облигатных анаэробов, таких как бактероиды и бифидобактерии. [36] Факторы, нарушающие популяцию микроорганизмов толстого кишечника, включают антибиотики, стресс и паразитов. [5]
Бактерии составляют большую часть флоры толстой кишки [ 37] и 60% сухой массы фекалий . [6] Этот факт делает фекалии идеальным источником кишечной флоры для любых тестов и экспериментов путем извлечения нуклеиновой кислоты из образцов фекалий, а последовательности бактериального гена 16S рРНК генерируются с помощью бактериальных праймеров. Эта форма тестирования также часто предпочтительнее более инвазивных методов, таких как биопсия.
В микробиоте кишечника доминируют пять типов : Bacteroidota , Bacillota (Firmicutes), Actinomycetota , Pseudomonadota и Verrucomicrobiota – при этом Bacteroidota и Bacillota составляют 90% состава. [38] В кишечнике обитает от 300 [6] до 1000 различных видов , [16] по большинству оценок около 500. [39] [40] Однако вполне вероятно, что 99% бактерий происходят от примерно 30 или 40 видов, причем наиболее распространенными видами у здоровых взрослых являются Faecalibacterium prausnitzii (тип Firmicutes). [7] [41]
Исследования показывают, что отношения между кишечной флорой и людьми являются не просто комменсальными (безвредное сосуществование), а, скорее, мутуалистическими , симбиотическими отношениями. [16] Хотя люди могут выжить и без кишечной флоры, [39] микроорганизмы выполняют множество полезных функций, таких как ферментация неиспользованных энергетических субстратов, тренировка иммунной системы с помощью конечных продуктов метаболизма, таких как пропионат и ацетат , предотвращение роста вредных видов. , регулируя развитие кишечника, производя витамины для хозяина (такие как биотин и витамин К ) и производя гормоны, направляющие хозяина на хранение жиров. [5] Обширные модификации и дисбаланс микробиоты кишечника и его микробиома или коллекции генов связаны с ожирением. [42] Однако при определенных условиях считается, что некоторые виды способны вызывать заболевание , вызывая инфекцию или увеличивая риск рака у хозяина. [6] [37]
Грибы и протисты также составляют часть кишечной флоры, но об их деятельности известно меньше. [43]
Виром человека состоит в основном из бактериофагов . [44]
Существуют общие закономерности эволюции состава микробиома в течение жизни. [45] В целом разнообразие состава микробиоты образцов фекалий значительно выше у взрослых, чем у детей, хотя межличностные различия у детей выше, чем у взрослых. [46] Большая часть созревания микробиоты до конфигурации, подобной взрослой, происходит в течение трех первых лет жизни. [46]
По мере изменения состава микробиома меняется и состав бактериальных белков, вырабатываемых в кишечнике. В микробиомах взрослых обнаружена высокая распространенность ферментов, участвующих в ферментации, метаногенезе и метаболизме аргинина, глутамата, аспартата и лизина. Напротив, в микробиомах младенцев доминирующие ферменты участвуют в метаболизме цистеина и путях ферментации. [46]
Состав кишечного микробиома зависит от географического происхождения популяций. Вариации в компромиссе Prevotella , репрезентации гена уреазы и репрезентации генов, кодирующих глутаматсинтазу/деградацию или другие ферменты, участвующие в деградации аминокислот или биосинтезе витаминов, демонстрируют значительные различия между популяциями из США, Малави или индейцев. источник. [46]
В популяции США широко представлены ферменты, кодирующие расщепление глютамина , и ферменты, участвующие в биосинтезе витаминов и липоевой кислоты ; тогда как в популяциях Малави и американских индейцев высока представленность ферментов, кодирующих глутаматсинтазу, а также в их микробиомах преобладает α-амилаза . Поскольку рацион населения США более богат жирами, чем рацион индейцев или малавийцев, рацион которого богат кукурузой, диета, вероятно, является основным фактором, определяющим бактериальный состав кишечника. [46]
Дальнейшие исследования показали большую разницу в составе микробиоты между европейскими и сельскими африканскими детьми. Фекальные бактерии детей из Флоренции сравнили с бактериями детей из небольшой сельской деревни Булпон в Буркина-Фасо . Рацион типичного ребенка, живущего в этой деревне, в значительной степени лишен жиров и животных белков и богат полисахаридами и растительными белками. В фекальных бактериях европейских детей доминировали Firmicutes , что демонстрировало заметное снижение биоразнообразия, в то время как в фекальных бактериях детей Булпона доминировали Bacteroidetes . Повышенное биоразнообразие и различный состав кишечного микробиома у африканских популяций могут способствовать перевариванию обычно неперевариваемых растительных полисахаридов, а также могут привести к снижению заболеваемости неинфекционными заболеваниями толстой кишки. [47]
В меньшем масштабе было показано, что совместное использование многочисленных общих воздействий окружающей среды в семье является сильным определяющим фактором индивидуального состава микробиома. Этот эффект не имеет генетического влияния и постоянно наблюдается в культурно разных популяциях. [46]
У недоедающих детей менее зрелая и менее разнообразная микробиота кишечника, чем у здоровых детей, а изменения в микробиоме, связанные с нехваткой питательных веществ, в свою очередь, могут быть патофизиологической причиной недоедания. [48] [49] У недоедающих детей также обычно больше потенциально патогенной кишечной флоры и больше дрожжевых грибков во рту и горле. [50] Изменение диеты может привести к изменениям в составе и разнообразии кишечной микробиоты. [51]
Исследователи из Американского проекта кишечника и Проекта микробиома человека обнаружили, что численность двенадцати семейств микробов различается в зависимости от расы или этнической принадлежности человека. Сила этих ассоциаций ограничена небольшим размером выборки: Американский проект кишечника собрал данные от 1375 человек, 90% из которых были белыми. [52] Исследование «Здоровая жизнь в городских условиях» (HELIUS) в Амстердаме показало, что у людей голландского происхождения был самый высокий уровень разнообразия кишечной микробиоты, в то время как у выходцев из Южной Азии и Суринама было самое низкое разнообразие. Результаты исследования показали, что люди одной расы или этнической принадлежности имеют более схожие микробиомы, чем люди разного расового происхождения. [52]
По состоянию на 2020 год как минимум два исследования продемонстрировали связь между социально-экономическим статусом человека (СЭС) и его кишечной микробиотой. Исследование, проведенное в Чикаго, показало, что люди в районах с более высоким SES имеют большее разнообразие микробиоты. У жителей районов с более высоким СЭС также было больше бактерий Bacteroides . Аналогичным образом, исследование близнецов в Великобритании показало, что более высокий SES также связан с большим разнообразием кишечника. [52]
Формирование кишечной флоры имеет решающее значение для здоровья взрослого человека, а также для функционирования желудочно-кишечного тракта. [53] У людей кишечная флора, аналогичная флоре взрослого человека, формируется в течение одного-двух лет после рождения, поскольку микробиота приобретается путем передачи от родителей к ребенку и передачи из пищи, воды и других источников окружающей среды. [54] [11]

Традиционный взгляд на желудочно-кишечный тракт нормального плода состоит в том, что он стерилен, хотя в последние несколько лет эта точка зрения была подвергнута сомнению. [ временные рамки? ] [55] Начали появляться многочисленные доказательства того, что во внутриутробной среде могут находиться бактерии. Исследования на людях показали, что микробная колонизация может происходить у плода [56] , при этом одно исследование показало, что виды Lactobacillus и Bifidobacterium присутствовали в биоптатах плаценты. [57] Несколько исследований на грызунах продемонстрировали наличие бактерий в околоплодных водах и плаценте, а также в меконии детей , рожденных в результате стерильного кесарева сечения. [58] [59] В другом исследовании исследователи вводили культуру бактерий перорально беременным мышам и обнаружили бактерии у потомства, вероятно, в результате передачи между пищеварительным трактом и околоплодными водами через кровоток. [60] Однако исследователи предупреждают, что источник этих внутриутробных бактерий, живы ли они и их роль, еще не изучены. [61] [57]
Во время рождения и вскоре после него бактерии матери и окружающей среды колонизируют кишечник ребенка. [11] Точные источники бактерий до конца не изучены, но могут включать родовые пути, других людей (родителей, братьев и сестер, работников больницы), грудное молоко, пищу и общую среду, с которой взаимодействует ребенок. [62] Исследования показали, что микробиом детей, рожденных естественным путем , значительно отличается от микробиома детей, рожденных путем кесарева сечения, и что дети, рожденные естественным путем, получили большую часть кишечных бактерий от своей матери, в то время как микробиота детей, рожденных путем кесарева сечения, содержала больше бактерий. связанные с больничной средой. [63]
В течение первого года жизни состав кишечной флоры обычно прост, сильно меняется со временем и неодинаков у разных людей. [11] Исходная бактериальная популяция обычно представляет собой факультативные анаэробные организмы ; Исследователи полагают, что эти первоначальные колонизаторы снижают концентрацию кислорода в кишечнике, что, в свою очередь, позволяет облигатно анаэробным бактериям, таким как Bacteroidota , Actinomycetota и Bacillota , прижиться и процветать. [11] У детей, находящихся на грудном вскармливании, начинают преобладать бифидобактерии , возможно, из-за содержания бифидобактериальных факторов роста в грудном молоке, а также из-за того, что грудное молоко содержит пребиотические компоненты, способствующие здоровому росту бактерий. [57] [64] Грудное молоко также содержит более высокий уровень иммуноглобулина А (IgA), который способствует толерантности и регуляции иммунной системы ребенка. [65] Напротив, микробиота детей, находящихся на искусственном вскармливании , более разнообразна, с большим количеством Enterobacteriaceae , энтерококков , бифидобактерий, Bacteroides и клостридий. [66]
Кесарево сечение, антибиотики и искусственное вскармливание могут изменить состав микробиома кишечника. [57] Дети, получающие антибиотики, имеют менее стабильные и менее разнообразные цветочные сообщества. [67] Было показано, что кесарево сечение препятствует передаче бактерий от матери к потомству, что влияет на общее состояние здоровья потомства, повышая риск таких заболеваний, как целиакия , астма и диабет 1 типа . [57] Это еще раз доказывает важность здорового микробиома кишечника. Изучаются различные методы восстановления микробиома, обычно включающие воздействие на ребенка содержимого влагалища матери и пероральные пробиотики. [57]
Когда в 1995 году началось изучение кишечной флоры [68] , считалось, что она выполняет три ключевые роли: прямую защиту от патогенов , усиление защиты хозяина за счет ее роли в развитии и поддержании кишечного эпителия и индукции там выработки антител, а также метаболизма иным образом. неперевариваемые соединения в пище. Последующие работы обнаружили его роль в тренировке развивающейся иммунной системы, а дальнейшие работы были сосредоточены на его роли в оси кишечник-мозг . [69]
Сообщество кишечной флоры играет непосредственную роль в защите от патогенов, полностью колонизируя пространство, используя все доступные питательные вещества и секретируя соединения, известные как цитокины , которые убивают или подавляют нежелательные организмы, которые будут конкурировать с ним за питательные вещества. [70] Различные штаммы кишечных бактерий вызывают выработку разных цитокинов. Цитокины — это химические соединения, вырабатываемые нашей иммунной системой для инициации воспалительной реакции против инфекций. Нарушение кишечной флоры позволяет утвердиться конкурирующим организмам, таким как Clostridium difficile , которые в противном случае остаются бездействующими. [70]
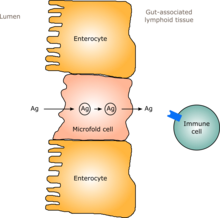
У человека кишечная флора, аналогичная взрослой, формируется в течение одного-двух лет после рождения. [11] По мере того, как формируется кишечная флора, слизистая оболочка кишечника – кишечный эпителий и барьер слизистой оболочки кишечника, который он секретирует – также развивается таким образом, что становится толерантным и даже поддерживает комменсалистические микроорганизмы в определенных условиях. степени, а также обеспечивает барьер для патогенных. [11] В частности, бокаловидные клетки , которые производят слизистую оболочку, пролиферируют, и слой слизистой оболочки утолщается, образуя внешний слой слизистой оболочки, в котором «дружественные» микроорганизмы могут закрепляться и питаться, и внутренний слой, через который даже эти организмы не могут проникнуть. [11] [12] Кроме того, в то время, когда кишечная флора развивается и укореняется, появляется и развивается лимфоидная ткань, связанная с кишечником (GALT), которая составляет часть кишечного эпителия и которая обнаруживает патогены и реагирует на них. [11] Развивающийся GALT толерантен к видам кишечной флоры, но не к другим микроорганизмам. [11] GALT также обычно становится толерантным к еде, с которой контактирует ребенок, а также к продуктам пищеварения и метаболитам кишечной флоры (молекулам, образующимся в результате метаболизма), вырабатываемым из пищи. [11]
Иммунная система человека вырабатывает цитокины , которые могут заставить иммунную систему вызывать воспаление, чтобы защитить себя, и которые могут подавлять иммунный ответ для поддержания гомеостаза и обеспечения заживления после оскорбления или травмы. [11] Было показано, что различные виды бактерий, которые появляются во флоре кишечника, способны стимулировать иммунную систему избирательно вырабатывать цитокины; например, Bacteroides fragilis и некоторые виды Clostridia , по-видимому, вызывают противовоспалительную реакцию, в то время как некоторые сегментированные нитчатые бактерии стимулируют выработку воспалительных цитокинов. [11] [71] Кишечная флора также может регулировать выработку антител иммунной системой. [11] [72] Одной из функций этой регуляции является переключение класса B-клеток на IgA . В большинстве случаев В-клеткам необходима активация Т-хелперов , чтобы вызвать переключение класса ; однако по другому пути кишечная флора вызывает передачу сигналов NF-kB эпителиальными клетками кишечника, что приводит к секреции дополнительных сигнальных молекул. [73] Эти сигнальные молекулы взаимодействуют с В-клетками, вызывая переключение класса на IgA. [73] IgA — важный тип антител, который используется в слизистой оболочке, например в кишечнике. Было доказано, что IgA может помочь разнообразить кишечное сообщество и избавиться от бактерий, вызывающих воспалительные реакции. [74] В конечном итоге, IgA поддерживает здоровую среду между хозяином и кишечными бактериями. [74] Эти цитокины и антитела могут оказывать действие за пределами кишечника, в легких и других тканях. [11]
Иммунная система также может быть изменена из-за способности кишечных бактерий производить метаболиты , которые могут влиять на клетки иммунной системы. Например, короткоцепочечные жирные кислоты (КЦЖК) могут вырабатываться некоторыми кишечными бактериями посредством ферментации . [75] SCFAs стимулируют быстрое увеличение производства клеток врожденного иммунитета, таких как нейтрофилы , базофилы и эозинофилы . [75] Эти клетки являются частью врожденной иммунной системы, которая пытается ограничить распространение инфекции.
Без кишечной флоры человеческий организм не смог бы использовать некоторые из непереваренных углеводов, которые он потребляет, поскольку некоторые типы кишечной флоры содержат ферменты , которых не хватает человеческим клеткам для расщепления определенных полисахаридов . [13] Грызунам, выращенным в стерильной среде и лишенным кишечной флоры, необходимо потреблять на 30% больше калорий , чтобы оставаться в том же весе, что и их нормальные собратья. [13] Углеводы, которые люди не могут переваривать без помощи бактерий, включают определенные крахмалы , клетчатку , олигосахариды и сахара , которые организм не может переварить и усвоить, например лактозу в случае непереносимости лактозы , а также сахарные спирты , слизь , вырабатываемую кишечником, и белки. [9] [13]
Бактерии превращают ферментированные ими углеводы в жирные кислоты с короткой цепью посредством формы ферментации, называемой сахаролитической ферментацией. [40] Продукты включают уксусную кислоту , пропионовую кислоту и масляную кислоту . [7] [40] Эти материалы могут использоваться клетками-хозяевами, обеспечивая их основным источником энергии и питательных веществ. [40] Газы (которые участвуют в передаче сигналов [80] и могут вызывать метеоризм ) и органические кислоты , такие как молочная кислота , также производятся в результате ферментации. [7] Уксусная кислота используется мышцами , пропионовая кислота способствует выработке АТФ в печени , а масляная кислота обеспечивает клетки кишечника энергией. [40]
Кишечная флора также синтезирует витамины, такие как биотин и фолиевая кислота , и способствует усвоению пищевых минералов , включая магний, кальций и железо. [6] [23] Methanobrevibacter smithii уникален, поскольку не является видом бактерий, а скорее членом домена Archaea , и является наиболее распространенным видом архей, производящих метан , в желудочно-кишечной микробиоте человека. [81]
Микробиота кишечника также служит источником витаминов К и В 12 , которые не вырабатываются организмом или производятся в небольших количествах. [82] [83]
Метагеном человека (т.е. генетический состав человека и всех микроорганизмов, обитающих на теле человека или внутри него) значительно различается у разных людей. [84] [85] Поскольку общее количество микробных клеток в организме человека (более 100 триллионов) значительно превышает численность клеток Homo sapiens (десятки триллионов), [примечание 1] [84] [86] существует значительный потенциал для взаимодействия между лекарства и микробиом человека, включая: лекарства, изменяющие состав микробиома человека , метаболизм лекарств под действием микробных ферментов, модифицирующих фармакокинетический профиль лекарства , и микробный метаболизм лекарств, влияющий на клиническую эффективность и профиль токсичности лекарства . [84] [85] [87]
Помимо углеводов, микробиота кишечника может также метаболизировать другие ксенобиотики , такие как лекарства, фитохимические вещества и пищевые токсиканты. Было показано, что более 30 лекарств метаболизируются микробиотой кишечника. [88] Микробный метаболизм лекарств иногда может инактивировать препарат. [89]
Микробиота кишечника представляет собой богатое сообщество, содержащее разнообразные гены с огромными биохимическими способностями модифицировать лекарства, особенно те, которые принимаются перорально. [90] Микробиота кишечника может влиять на метаболизм лекарств посредством прямых и косвенных механизмов. [91] Прямой механизм опосредован микробными ферментами, которые могут изменять химическую структуру вводимых лекарств. [92] И наоборот, непрямой путь опосредован микробными метаболитами, которые влияют на экспрессию метаболизирующих ферментов хозяина, таких как цитохром P450 . [93] [91] Влияние микробиоты кишечника на фармакокинетику и биодоступность препарата было исследовано несколько десятилетий назад. [94] [95] [96] Эти эффекты можно варьировать; он может активировать неактивные препараты, такие как ловастатин, [97] инактивировать активный препарат, такой как дигоксин [98] , или вызывать токсичность препарата, как в случае иринотекана . [99] С тех пор влияние кишечной микробиоты на фармакокинетику многих лекарств было тщательно изучено. [100] [90]
Микробиота кишечника человека играет решающую роль в модуляции воздействия вводимых лекарств на человека. Непосредственно микробиота кишечника может синтезировать и высвобождать ряд ферментов, способных метаболизировать лекарства, такие как микробная биотрансформация L-дофа с помощью ферментов декарбоксилазы и дегидроксилазы. [92] Напротив, микробиота кишечника может также изменять метаболизм лекарств, модулируя метаболизм лекарств в организме хозяина. Этот механизм может быть опосредован микробными метаболитами или модификацией метаболитов хозяина, которые, в свою очередь, изменяют экспрессию ферментов, метаболизирующих хозяина. [93]
Большое количество исследований продемонстрировало метаболизм более 50 лекарств кишечной микробиотой. [100] [91] Например, ловастатин (средство, снижающее уровень холестерина), который является пролекарством лактона, частично активируется микробиотой кишечника человека, образуя активные кислотные гидроксилированные метаболиты. [97] И наоборот, дигоксин (препарат, используемый для лечения застойной сердечной недостаточности) инактивируется членом микробиоты кишечника (например, Eggerthella lanta ). [101] Eggerthella lanta имеет оперон, кодирующий цитохром, активируемый дигоксином и связанный с инактивацией дигоксина. [101] Микробиота кишечника также может модулировать эффективность и токсичность химиотерапевтических агентов, таких как иринотекан. [102] Этот эффект обусловлен кодируемыми микробиомом ферментами β-глюкуронидазой, которые восстанавливают активную форму иринотекана, вызывающую желудочно-кишечную токсичность. [103]
Это микробное сообщество в кишечнике обладает огромной биохимической способностью производить отдельные вторичные метаболиты, которые иногда образуются в результате метаболического преобразования пищевых продуктов, таких как клетчатка , эндогенные биологические соединения, такие как индол или желчные кислоты . [104] [105] [106] Микробные метаболиты, особенно короткоцепочечные жирные кислоты (КЦЖК) и вторичные желчные кислоты (ЖК), играют важную роль для человека в состоянии здоровья и болезненных состояниях. [107] [108] [109]
Одним из наиболее важных бактериальных метаболитов, вырабатываемых микробиотой кишечника, являются вторичные желчные кислоты (ЖК). [106] Эти метаболиты образуются в результате бактериальной биотрансформации первичных желчных кислот, таких как холевая кислота (CA) и хенодезоксихолевая кислота (CDCA), во вторичные желчные кислоты (BA) литохолевая кислота (LCA) и дезоксихолевая кислота (DCA) соответственно. [110] Первичные желчные кислоты, которые синтезируются гепатоцитами и хранятся в желчном пузыре, обладают гидрофобными свойствами. Эти метаболиты впоследствии метаболизируются микробиотой кишечника во вторичные метаболиты с повышенной гидрофобностью. [110] Гидролазы солей желчных кислот (BSH), которые консервативны во всех типах микробиоты кишечника, таких как Bacteroides , Firmicutes и Actinobacteria , ответственных за первый этап вторичного метаболизма желчных кислот. [110] Было продемонстрировано, что вторичные желчные кислоты (ЖК), такие как DCA и LCA, ингибируют как прорастание, так и рост Clostridium difficile . [109]
Микробиота кишечника важна для поддержания гомеостаза в кишечнике. Развитие рака кишечника связано с дисбалансом естественной микрофлоры (дисбиозом). [111] Вторичная желчная кислота, дезоксихолевая кислота , связана с изменениями микробного сообщества, которые приводят к усилению канцерогенеза в кишечнике. [111] Повышенное воздействие на толстую кишку вторичных желчных кислот в результате дисбактериоза может вызвать повреждение ДНК , и такое повреждение может вызвать канцерогенные мутации в клетках толстой кишки. [112] Высокая плотность бактерий в толстой кишке (около 10 12 на мл), подверженных дисбиозу, по сравнению с относительно низкой плотностью в тонкой кишке (около 10 2 на мл), может составлять более 10- заболеваемость раком толстой кишки в несколько раз выше, чем тонкой. [112]
Ось кишечник-мозг представляет собой биохимическую передачу сигналов, которая происходит между желудочно-кишечным трактом и центральной нервной системой . [69] Этот термин был расширен и теперь включает роль кишечной флоры во взаимодействии; Термин «ось микробиом-мозг» иногда используется для описания парадигм, явно включающих кишечную флору. [69] [113] [114] В широком смысле ось кишечник-мозг включает центральную нервную систему, нейроэндокринную и нейроиммунную системы, включая ось гипоталамо-гипофиз-надпочечники (ось HPA), симпатические и парасимпатические ветви вегетативной нервной системы , включая кишечная нервная система , блуждающий нерв и кишечная микробиота . [69] [114]
Систематический обзор 2016 года изучил доклинические и небольшие исследования на людях, которые были проведены с некоторыми коммерчески доступными штаммами пробиотических бактерий , и обнаружил, что среди протестированных были роды Bifidobacterium и Lactobacillus ( B. longum , B. breve , B. infantis , L. helveticus , L. rhamnosus , L. plantarum и L. casei ), имели наибольший потенциал быть полезными при некоторых заболеваниях центральной нервной системы . [15]
Изменение количества кишечных бактерий, например, путем приема антибиотиков широкого спектра действия , может повлиять на здоровье хозяина и его способность переваривать пищу. [115] Антибиотики могут вызывать антибиотикоассоциированную диарею , непосредственно раздражая кишечник , изменяя уровень микробиоты или позволяя патогенным бактериям расти. [7] Еще одним вредным эффектом антибиотиков является увеличение числа устойчивых к антибиотикам бактерий, обнаруживаемых после их применения, которые, проникая в организм хозяина, вызывают заболевания, которые трудно лечить антибиотиками. [115]
Изменение количества и видов кишечной микробиоты может снизить способность организма ферментировать углеводы и метаболизировать желчные кислоты и может вызвать диарею . Нерасщепляемые углеводы могут поглощать слишком много воды и вызывать жидкий стул, а недостаток SCFAs, вырабатываемых кишечной микробиотой, может вызвать диарею. [7]
Снижение уровня местных видов бактерий также нарушает их способность подавлять рост вредных видов, таких как C. difficile и Salmonella kedougou , и эти виды могут выйти из-под контроля, хотя их чрезмерный рост может быть случайным, а не истинной причиной диарея. [6] [7] [115] Новые протоколы лечения инфекций, вызванных C. difficile, включают трансплантацию фекальной микробиоты донорских фекалий (см. Трансплантация кала ). [116] Первоначальные отчеты о лечении описывают уровень успеха в 90% с небольшим количеством побочных эффектов. Предполагается, что эффективность обусловлена восстановлением бактериального баланса бактерий классов бактероидов и фирмикутов. [117]
Состав микробиома кишечника также меняется при тяжелых заболеваниях не только из-за применения антибиотиков, но и из-за таких факторов, как ишемия кишечника, отказ от приема пищи и ослабление иммунитета . Негативные последствия этого привели к интересу к селективной деконтаминации пищеварительного тракта, лечению, которое убивает только патогенные бактерии и позволяет восстановить здоровые. [118]
Антибиотики изменяют популяцию микробиоты в желудочно-кишечном тракте , и это может изменить метаболические взаимодействия внутри сообщества, изменить потребление калорий за счет использования углеводов и глобально повлиять на метаболический, гормональный и иммунный гомеостаз хозяина. [119]
Имеются убедительные доказательства того, что прием пробиотиков, содержащих виды Lactobacillus , может помочь предотвратить диарею, связанную с антибиотиками, и что прием пробиотиков с Saccharomyces (например, Saccharomyces boulardii ) может помочь предотвратить инфекцию Clostridium difficile после системного лечения антибиотиками. [120]
Микробиота кишечника женщины меняется по мере развития беременности , причем изменения аналогичны тем, которые наблюдаются при метаболических синдромах , таких как диабет. Изменение микробиоты кишечника не вызывает никаких побочных эффектов. Микробиота кишечника новорожденного напоминает образцы матери в первом триместре. Разнообразие микробиома уменьшается с первого по третий триместр по мере увеличения численности определенных видов. [57] [121]
Пробиотики — это микроорганизмы , которые, как полагают, приносят пользу для здоровья при употреблении. [122] [123] Что касается кишечной микробиоты, пребиотики обычно представляют собой неперевариваемые соединения клетчатки , которые проходят непереваренными через верхнюю часть желудочно -кишечного тракта и стимулируют рост или активность полезной кишечной флоры, действуя для них в качестве субстрата . [40] [124]
Синбиотики — это пищевые ингредиенты или пищевые добавки , сочетающие пробиотики и пребиотики в форме синергизма . [125]
Термин «фармабиотики» используется по-разному и означает: фармацевтические составы (стандартизованное производство, которое может получить одобрение регулирующих органов в качестве лекарственного средства) пробиотиков, пребиотиков или синбиотиков ; [126] пробиотики, которые были генетически сконструированы или иным образом оптимизированы для достижения наилучших результатов (срок годности, выживаемость в пищеварительном тракте и т. д.); [127] и натуральные продукты метаболизма кишечной флоры (витамины и т. д.). [128]
Есть некоторые доказательства того, что лечение некоторыми пробиотическими штаммами бактерий может быть эффективным при синдроме раздраженного кишечника [129] [130] и хроническом идиопатическом запоре . К микроорганизмам, которые с наибольшей вероятностью приведут к уменьшению симптомов, относятся:
Фекалии примерно 10–15% людей постоянно плавают в туалетной воде («плавают»), в то время как у остальных фекалии тонут («грузила»), а выделение газа заставляет фекалии всплывать. [134] В то время как обычные мыши часто производят «поплавки», гнотобиотические безмикробные мыши без кишечной микробиоты (выращенные в стерильном изоляторе) образуют «грузила», а колонизация кишечной микробиоты у безмикробных мышей приводит к трансформации пищи в микробную биомассу и обогащению множеством газогенных видов бактерий. это превращает «грузила» в «плавающие». [135]
Тесты на то, могут ли неантибиотические препараты влиять на кишечные бактерии человека, были проведены путем анализа in vitro более чем 1000 имеющихся на рынке лекарств против 40 штаммов кишечных бактерий, продемонстрировав, что 24% лекарств ингибировали рост по крайней мере одного из бактериальных штаммов. . [136]
Недавно было показано, что кишечная микробиота и физические упражнения взаимосвязаны. Как умеренные, так и интенсивные упражнения обычно являются частью режима тренировок спортсменов, занимающихся выносливостью, но они оказывают различное влияние на здоровье. Взаимосвязь между кишечной микробиотой и видами спорта, требующими выносливости, зависит от интенсивности тренировок и статуса тренировок. [137]
Бактерии в пищеварительном тракте могут по-разному способствовать возникновению заболеваний и подвергаться им. Присутствие или переизбыток некоторых видов бактерий может способствовать воспалительным заболеваниям, таким как воспалительные заболевания кишечника . [6] Кроме того, метаболиты некоторых представителей кишечной флоры могут влиять на сигнальные пути хозяина, способствуя таким расстройствам, как ожирение и рак толстой кишки . [6] Альтернативно, в случае разрушения эпителия кишечника , проникновение компонентов кишечной флоры в другие компартменты хозяина может привести к сепсису . [6]
Инфекция Helicobacter pylori может инициировать образование язв желудка, когда бактерии проникают в эпителиальную оболочку желудка, вызывая затем воспалительную фагоцитарную реакцию . [138] В свою очередь, воспаление повреждает париетальные клетки, которые выделяют в желудок избыточное количество соляной кислоты и производят меньше защитной слизи. [139] Повреждение слизистой оболочки желудка, приводящее к язвам , развивается, когда желудочная кислота подавляет защитные свойства клеток и ингибирует синтез эндогенных простагландинов , уменьшает секрецию слизи и бикарбоната, уменьшает кровоток слизистой оболочки и снижает устойчивость к травмам. [139] Снижение защитных свойств слизистой оболочки желудка повышает уязвимость к дальнейшему повреждению и образованию язв под действием желудочной кислоты, пепсина и солей желчных кислот. [138] [139]
В норме комменсальные бактерии могут нанести вред хозяину, если они выходят из кишечного тракта. [11] [12] Транслокация, которая возникает, когда бактерии покидают кишечник через слизистую оболочку, может возникать при ряде различных заболеваний. [12] Если кишечник перфорирован, бактерии проникают в интерстиций , вызывая потенциально смертельную инфекцию . [5] : 715
Двумя основными типами воспалительных заболеваний кишечника , болезнью Крона и язвенным колитом , являются хронические воспалительные заболевания кишечника; причины этих заболеваний неизвестны, и к этим состояниям причастны проблемы с кишечной флорой и ее взаимоотношениями с хозяином. [14] [140] [141] [142] Кроме того, оказывается, что взаимодействие кишечной флоры с осью кишечник-мозг играет роль в воспалительных заболеваниях кишечника, при этом физиологический стресс, опосредованный через ось гипоталамус-гипофиз-надпочечники, вызывает изменения в эпителии кишечника. а кишечная флора, в свою очередь, высвобождает факторы и метаболиты, которые запускают передачу сигналов в кишечной нервной системе и блуждающем нерве . [4]
Разнообразие кишечной флоры, по-видимому, значительно уменьшено у людей с воспалительными заболеваниями кишечника по сравнению со здоровыми людьми; кроме того, у людей с язвенным колитом, по-видимому, доминируют протеобактерии и актинобактерии; у людей с болезнью Крона, по-видимому, чрезмерно представлены Enterococcus faecium и некоторые протеобактерии. [4]
Имеются убедительные доказательства того, что исправление дисбаланса кишечной флоры путем приема пробиотиков с лактобактериями и бифидобактериями может уменьшить висцеральную боль и воспаление кишечника при ВЗК. [120]
Синдром раздраженного кишечника является результатом стресса и хронической активации оси HPA; его симптомы включают боль в животе, изменения в дефекации и увеличение количества провоспалительных цитокинов. В целом исследования показали, что микробиота просвета и слизистой оболочки изменяется у людей с синдромом раздраженного кишечника, и эти изменения могут быть связаны с типом раздражения, таким как диарея или запор . Также наблюдается уменьшение разнообразия микробиома с низким уровнем фекальных лактобацилл и бифидобактерий, высоким уровнем факультативных анаэробных бактерий , таких как Escherichia coli , и повышенным соотношением Firmicutes: Bacteroidetes. [114]
Что касается астмы, были выдвинуты две гипотезы, объясняющие ее растущую распространенность в развитых странах. Гигиеническая гипотеза утверждает, что дети в развитых странах не подвергаются воздействию достаточного количества микробов и, следовательно, могут содержать меньшую распространенность определенных бактериальных таксонов, которые играют защитную роль. [143] Вторая гипотеза фокусируется на диете западного образца , в которой отсутствуют цельнозерновые продукты и клетчатка , а также имеется избыток простых сахаров . [14] Обе гипотезы сходятся во мнении о роли короткоцепочечных жирных кислот (КЦЖК) в иммуномодуляции . Эти метаболиты бактериальной ферментации участвуют в передаче иммунных сигналов, что предотвращает возникновение астмы, а более низкие уровни SCFAs связаны с этим заболеванием. [143] [144] Отсутствие защитных родов, таких как Lachnospira , Veillonella , Rothia и Faecalibacterium , связано со снижением уровней SCFAs. [143] Кроме того, SCFAs являются продуктом бактериальной ферментации клетчатки, которой в рационе западного типа мало. [14] [144] SCFAs обеспечивают связь между кишечной флорой и иммунными нарушениями, и по состоянию на 2016 год это была активная область исследований. [14] Подобные гипотезы также были выдвинуты в отношении роста пищевой и других аллергий. [145]
Связь между кишечной микробиотой и сахарным диабетом 1 типа также связана с КЦЖК, такими как бутират и ацетат. Диеты, содержащие бутират и ацетат в результате бактериальной ферментации, демонстрируют повышенную экспрессию T reg . [146] T- reg- клетки подавляют эффекторные T-клетки , что, в свою очередь, снижает воспалительную реакцию в кишечнике. [147] Бутират является источником энергии для клеток толстой кишки. Диеты, содержащие бутират, таким образом, уменьшают проницаемость кишечника , обеспечивая достаточно энергии для образования плотных соединений . [148] Кроме того, было показано, что бутират снижает резистентность к инсулину, что позволяет предположить, что кишечные сообщества с низким содержанием микробов, продуцирующих бутират, могут увеличить вероятность заражения сахарным диабетом 2 типа . [149] Диеты с содержанием бутирата также могут иметь потенциальный эффект подавления колоректального рака . [148]
Кишечная флора вовлечена в ожирение и метаболический синдром из-за ключевой роли в пищеварительном процессе; Диета западного образца, по-видимому, стимулирует и поддерживает изменения во флоре кишечника, которые, в свою очередь, меняют количество энергии, получаемой из пищи, и то, как эта энергия используется. [142] [150] Одним из аспектов здорового питания , которого часто не хватает в диете западного образца, является клетчатка и другие сложные углеводы, необходимые для процветания здоровой кишечной флоры; Изменения кишечной флоры в ответ на диету западного образца, по-видимому, увеличивают количество энергии, вырабатываемой кишечной флорой, что может способствовать ожирению и метаболическому синдрому. [120] Существуют также доказательства того, что микробиота влияет на пищевое поведение, основанное на предпочтениях микробиоты, что может привести к тому, что хозяин будет потреблять больше пищи, что в конечном итоге приведет к ожирению. В целом замечено, что при более высоком разнообразии микробиома кишечника микробиота будет тратить энергию и ресурсы на конкуренцию с другой микробиотой и меньше на манипулирование хозяином. Обратное наблюдается с разнообразием микробиома нижнего отдела кишечника, и эти микробиоты могут работать вместе, вызывая у хозяина тягу к пище. [51]
Кроме того, печень играет доминирующую роль в гомеостазе глюкозы в крови , поддерживая баланс между поглощением и хранением глюкозы посредством метаболических путей гликогенеза и глюконеогенеза . Кишечные липиды регулируют гомеостаз глюкозы, задействуя ось кишечник-мозг-печень. Прямое введение липидов в верхний отдел кишечника повышает уровень длинноцепочечного жирного ацил-кофермента А (LCFA-CoA) в верхних отделах кишечника и подавляет выработку глюкозы даже при поддиафрагмальной ваготомии или деафферентации вагуса кишечника . Это прерывает нейронную связь между мозгом и кишечником и блокирует способность липидов верхних отделов кишечника ингибировать выработку глюкозы. Ось кишечник-мозг-печень и состав микробиоты кишечника могут регулировать гомеостаз глюкозы в печени и предоставлять потенциальные терапевтические методы для лечения ожирения и диабета. [151]
Точно так же, как кишечная флора может функционировать по принципу обратной связи, что может способствовать развитию ожирения, существуют доказательства того, что ограничение потребления калорий (т. е. диета ) может привести к изменениям в составе кишечной флоры. [142]
Состав микробиома кишечника человека аналогичен составу микробиома других человекообразных обезьян. Однако биота кишечника человека уменьшилась в разнообразии и изменилась по составу с тех пор, как мы эволюционно отделились от Пана . [152] У людей наблюдается увеличение количества Bacteroidetes, типа бактерий, связанного с диетой с высоким содержанием животных белков и жиров, и снижение количества Methanobrevibacter и Fibrobacter, групп, которые ферментируют сложные растительные полисахариды. [152] Эти изменения являются результатом совокупных диетических, генетических и культурных изменений, которые люди претерпели с момента эволюционного отклонения от Пана . [ нужна цитата ]
Помимо людей и позвоночных, у некоторых насекомых также есть сложная и разнообразная кишечная микробиота, которая играет ключевую питательную роль. [2] Микробные сообщества, связанные с термитами , могут составлять большую часть веса особей и выполнять важную роль в переваривании лигноцеллюлозы и фиксации азота . [153] Эти сообщества специфичны для хозяина, и близкородственные виды насекомых имеют сопоставимое сходство в составе микробиоты кишечника. [154] [155] Было показано, что у тараканов кишечная микробиота собирается детерминированным образом, независимо от инокулята ; [156] причина этой специфичной для хозяина сборки остается неясной. Бактериальные сообщества, связанные с такими насекомыми, как термиты и тараканы, определяются сочетанием факторов, в первую очередь диетой, но есть некоторые признаки того, что филогения хозяина также может играть роль в выборе линий. [154] [155]
Уже более 51 года известно, что введение низких доз антибактериальных средств способствует росту сельскохозяйственных животных и увеличению привеса. [119]
В исследовании, проведенном на мышах, соотношение Firmicutes и Lachnospiraceae было значительно повышено у животных, получавших субтерапевтические дозы различных антибиотиков. Анализируя калорийность фекалий и концентрацию короткоцепочечных жирных кислот (КЦЖК) в желудочно-кишечном тракте, был сделан вывод, что изменения в составе микробиоты приводят к увеличению способности извлекать калории из неперевариваемых в противном случае компонентов, а также к увеличение производства SCFAs. Эти результаты свидетельствуют о том, что антибиотики нарушают не только состав микробиома желудочно-кишечного тракта, но и его метаболические возможности, особенно в отношении SCFAs. [119]
группа ученых теперь сообщает только о трех различных экосистемах в кишечнике людей, которых они изучали.
Lactobacillus
spp.
превращают триптофан в индол-3-альдегид (I3A) с помощью неидентифицированных ферментов [125].
Clostridium sporogenes
превращают триптофан в IPA [6], вероятно, посредством триптофандезаминазы.
... IPA также эффективно удаляет гидроксильные радикалы.
Было показано, что продукция IPA полностью зависит от присутствия микрофлоры кишечника и может быть установлена путем колонизации бактерией
Clostridium sporogenes
.
[Индол-3-пропионовая кислота (IPA)] ранее была идентифицирована в плазме и спинномозговой жидкости человека, но ее функции неизвестны.
... В экспериментах по кинетической конкуренции с использованием агентов, улавливающих свободные радикалы, способность IPA удалять гидроксильные радикалы превышала способность мелатонина, индоламина, который считается наиболее мощным природным поглотителем свободных радикалов.
В отличие от других антиоксидантов, IPA не превращался в реакционноспособные интермедиаты с прооксидантной активностью.
Состав микробиома варьируется в зависимости от анатомического участка (рис. 1).
Главным детерминантом состава сообщества является анатомическое расположение: межличностные вариации значительны
23,24
и выше, чем временная изменчивость, наблюдаемая в большинстве мест у одного человека
25
.