Сигнальные пути Wnt представляют собой группу путей передачи сигнала , которые начинаются с белков , которые передают сигналы в клетку через рецепторы клеточной поверхности . Имя Wnt представляет собой сумку , созданную из названий Wingless и Int-1. [1] Сигнальные пути Wnt используют либо близлежащую межклеточную связь ( паракринная ), либо межклеточную связь ( аутокринную ). Они высоко эволюционно консервативны у животных, а это означает, что они схожи у всех видов животных, от плодовых мух до людей. [2] [3]
Охарактеризованы три сигнальных пути Wnt: канонический путь Wnt , неканонический путь полярности плоских клеток и неканонический путь Wnt/кальций . Все три пути активируются путем связывания лиганда белка Wnt с рецептором семейства Frizzled , который передает биологический сигнал белку Disheveled внутри клетки. Канонический путь Wnt приводит к регуляции транскрипции генов и, как полагают, частично отрицательно регулируется геном SPATS1 . [4] Неканонический путь планарной клеточной полярности регулирует цитоскелет , который отвечает за форму клетки. Неканонический путь Wnt/кальций регулирует кальций внутри клетки.
Передача сигналов Wnt была сначала идентифицирована из-за ее роли в канцерогенезе , затем из-за ее функции в эмбриональном развитии . Эмбриональные процессы, которые он контролирует, включают формирование паттерна оси тела , спецификацию клеточной судьбы , клеточную пролиферацию и миграцию клеток . Эти процессы необходимы для правильного формирования важных тканей, включая кости, сердце и мышцы. Его роль в эмбриональном развитии была обнаружена, когда генетические мутации в белках пути Wnt привели к образованию аномальных эмбрионов плодовых мух . Более поздние исследования показали, что гены, ответственные за эти аномалии, также влияют на развитие рака молочной железы у мышей. Передача сигналов Wnt также контролирует регенерацию тканей костного мозга, кожи и кишечника взрослых. [5]
Клиническое значение этого пути было продемонстрировано мутациями , которые приводят к различным заболеваниям, включая рак молочной железы и простаты , глиобластому , диабет II типа и другие. [6] [7] В последние годы исследователи сообщили о первом успешном использовании ингибиторов пути Wnt на мышиных моделях заболеваний. [8]
На открытие передачи сигналов Wnt повлияли исследования онкогенных (вызывающих рак) ретровирусов . В 1982 году Роэл Нусс и Гарольд Вармус заразили мышей вирусом опухоли молочной железы , чтобы мутировать мышиные гены и увидеть, какие мутировавшие гены могут вызывать опухоли молочной железы. Они идентифицировали новый мышиный протоонкоген, который назвали int1 (интеграция 1). [3] [9]
Int1 высоко консервативен у многих видов, включая человека и дрозофилу . Его присутствие у D. melanogaster привело исследователей к открытию в 1987 году, что ген int1 у дрозофилы на самом деле был уже известным и охарактеризованным геном дрозофилы , известным как Wingless (Wg). [3] Поскольку предыдущие исследования Кристианы Нюсляйн-Фольхард и Эрика Вишауса (которые принесли им Нобелевскую премию по физиологии и медицине в 1995 году) уже установили функцию Wg как гена полярности сегментов , участвующего в формировании оси тела во время эмбрионального развития . развития , исследователи определили, что int1 млекопитающих, обнаруженный у мышей, также участвует в эмбриональном развитии. [10]
Продолжение исследований привело к открытию дополнительных генов, связанных с int1; однако, поскольку эти гены не были идентифицированы таким же образом, как int1, номенклатура генов int была неадекватной. Таким образом, семейство int/Wingless стало семейством Wnt, а семейство int1 стало Wnt1. Имя Wnt представляет собой сочетание int и Wg и означает «сайт интеграции, связанный с Wingless». [3]
Wnt включает разнообразное семейство секретируемых липид -модифицированных сигнальных гликопротеинов длиной 350–400 аминокислот . [11] Липидная модификация всех Wnts представляет собой пальмитолеоилирование одного полностью консервативного остатка цистеина. [12] Пальмитолеоилирование необходимо, поскольку оно необходимо для того, чтобы Wnt связывался со своим белком-носителем Wntless (WLS), чтобы его можно было транспортировать к плазматической мембране для секреции [13] , и это позволяет белку Wnt связываться с его рецептором Frizzled [14] [15] Белки Wnt также подвергаются гликозилированию , которое прикрепляет углеводы для обеспечения правильной секреции. [16] При передаче сигналов Wnt эти белки действуют как лиганды , активируя различные пути Wnt паракринными и аутокринными путями. [2] [7]
Эти белки высококонсервативны у разных видов. [3] Их можно найти у мышей, людей, Xenopus , рыбок данио , дрозофилы и многих других. [17]
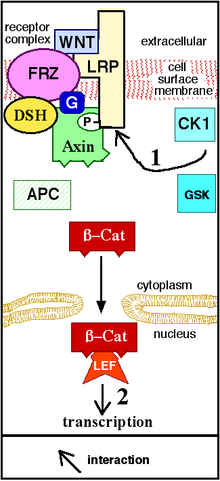

Передача сигналов Wnt начинается, когда белок Wnt связывается с N-концевым внеклеточным, богатым цистеином доменом рецептора семейства Frizzled (Fz). [19] Эти рецепторы охватывают плазматическую мембрану семь раз и составляют отдельное семейство рецепторов, связанных с G-белком (GPCR). [20] Однако для облегчения передачи сигналов Wnt наряду с взаимодействием между белком Wnt и рецептором Fz могут потребоваться корецепторы . Примеры включают белок, родственный рецептору липопротеина ( LRP )-5/6, рецепторную тирозинкиназу (RTK) и ROR2 . [7] При активации рецептора сигнал отправляется на фосфопротеин Растрепанный ( Dsh), который расположен в цитоплазме . Этот сигнал передается посредством прямого взаимодействия между Fz и Dsh. Белки Dsh присутствуют во всех организмах, и все они имеют следующие высококонсервативные белковые домены : аминоконцевой домен DIX, центральный домен PDZ и карбоксиконцевой домен DEP . Эти разные домены важны, поскольку после Dsh сигнал Wnt может разветвляться на множество путей, и каждый путь взаимодействует с различной комбинацией трех доменов. [21]
Тремя наиболее охарактеризованными сигнальными путями Wnt являются канонический путь Wnt, неканонический путь полярности плоских клеток и неканонический путь Wnt/кальций. Как следует из их названий, эти пути принадлежат к одной из двух категорий: каноническим и неканоническим. Разница между категориями заключается в том, что канонический путь включает белок бета-катенин (β-катенин), тогда как неканонический путь действует независимо от него. [19]

Канонический путь Wnt (или путь Wnt/β-катенин) — это путь Wnt, который вызывает накопление β-катенина в цитоплазме и его возможную транслокацию в ядро , чтобы действовать как коактиватор транскрипции транскрипционных факторов , принадлежащих TCF / Семья ЛЕФ . Без Wnt β-катенин не накапливался бы в цитоплазме, поскольку комплекс деструкции обычно разрушает его. В этот комплекс разрушения входят следующие белки: аксин , аденоматозная полипозная палочка (APC), протеинфосфатаза 2А (PP2A), киназа гликогенсинтазы 3 (GSK3) и казеинкиназа 1α (CK1α). [22] [23] Он разрушает β-катенин, направляя его на убиквитинирование , которое впоследствии отправляет его в протеасому для переваривания. [19] [24] Однако, как только Wnt связывает Fz и LRP5 / 6 , функция комплекса разрушения нарушается. Это связано с тем, что Wnt вызывает транслокацию негативного регулятора Wnt, аксина, и деструктивного комплекса на плазматическую мембрану. Фосфорилирование другими белками комплекса разрушения впоследствии связывает аксин с цитоплазматическим хвостом LRP5/6. Аксин дефосфорилируется, его стабильность и уровень снижаются. Затем Dsh активируется посредством фосфорилирования, и его домены DIX и PDZ ингибируют активность GSK3 деструктивного комплекса. Это позволяет β-катенину накапливаться и локализоваться в ядре, а затем вызывать клеточный ответ посредством трансдукции гена наряду с транскрипционными факторами TCF/LEF (фактор усиления Т-клеток/лимфоидный фактор) [25] . [24] β-катенин рекрутирует другие коактиваторы транскрипции, такие как BCL9 , Pygopus [26] и Parafibromin/Hyrax. [27] Сложность транскрипционного комплекса, собранного β-катенином , начинает проявляться благодаря новым высокопроизводительным протеомным исследованиям. [28] Однако единая теория того, как β-катенин управляет экспрессией целевых генов, до сих пор отсутствует, и тканеспецифичные игроки могут помочь β-катенину определить его гены-мишени. [29] Экстенсивность β-катенинавзаимодействующие белки усложняют наше понимание: β-катенин может напрямую фосфорилироваться по Ser552 с помощью Akt, что вызывает его диссоциацию от межклеточных контактов и накопление в цитозоле, после чего 14-3-3ζ взаимодействует с β-катенином (pSer552) и усиливает его ядерную активность. транслокация. [30] Сообщалось, что BCL9 и Pygopus фактически обладают несколькими β-catenin -независимыми функциями (следовательно, вероятно, независимыми от передачи сигналов Wnt). [31] [32] [33]
Путь неканонической планарной клеточной полярности (PCP) не включает β-катенин. Он не использует LRP-5/6 в качестве корецептора и, как полагают, использует NRH1, Ryk, PTK7 или ROR2 . Путь PCP активируется посредством связывания Wnt с Fz и его корецептором. Затем рецептор рекрутирует Dsh , который использует свои домены PDZ и DIX для формирования комплекса с Dishavelled-ассоциированным активатором морфогенеза 1 ( DAAM1 ). Затем Daam1 активирует небольшой G-белок Rho посредством фактора обмена гуанина . Rho активирует Rho-ассоциированную киназу (ROCK), которая является одним из основных регуляторов цитоскелета . Dsh также образует комплекс с rac1 и опосредует связывание профилина с актином . Rac1 активирует JNK и также может приводить к полимеризации актина . Связывание профилина с актином может привести к реструктуризации цитоскелета и гаструляции . [7] [34]

Неканонический путь Wnt/кальций также не включает β-катенин. Его роль заключается в том, чтобы помочь регулировать высвобождение кальция из эндоплазматического ретикулума (ЭР), чтобы контролировать внутриклеточные уровни кальция. Как и другие пути Wnt, при связывании лиганда активированный рецептор Fz напрямую взаимодействует с Dsh и активирует специфические домены белка Dsh. Домены, участвующие в передаче сигналов Wnt/кальций, представляют собой домены PDZ и DEP. [7] Однако, в отличие от других путей Wnt, рецептор Fz напрямую взаимодействует с тримерным G-белком. Эта совместная стимуляция Dsh и G-белка может привести к активации либо PLC , либо цГМФ-специфической ФДЭ . Если PLC активирован, компонент плазматической мембраны PIP2 расщепляется на DAG и IP3 . Когда IP3 связывает свой рецептор на ЭР, высвобождается кальций. Повышенные концентрации кальция и DAG могут активировать Cdc42 через PKC . Cdc42 является важным регулятором формирования вентрального паттерна. Повышенное содержание кальция также активирует кальциневрин и CaMKII . CaMKII индуцирует активацию транскрипционного фактора NFAT , который регулирует клеточную адгезию, миграцию и разделение тканей. [7] Кальцинеурин активирует киназу TAK1 и NLK , которая может мешать передаче сигналов TCF/β-катенина в каноническом пути Wnt. [35] Однако, если ФДЭ активирована, высвобождение кальция из ЭР ингибируется. ФДЭ опосредует это посредством ингибирования ПКГ, что впоследствии вызывает ингибирование высвобождения кальция. [7]
Бинарное различие канонических и неканонических сигнальных путей Wnt подверглось тщательному изучению, и был предложен интегрированный, конвергентный путь Wnt. [36] Некоторые доказательства этого были найдены для одного лиганда Wnt (Wnt5A). [37] Доказательства конвергентного сигнального пути Wnt, который демонстрирует интегрированную активацию передачи сигналов Wnt/Ca2+ и Wnt/β-катенина для множественных лигандов Wnt, были описаны в клеточных линиях млекопитающих. [38]
Передача сигналов Wnt также регулирует ряд других сигнальных путей, которые еще не так подробно изучены. Один из таких путей включает взаимодействие между Wnt и GSK3. Во время роста клеток Wnt может ингибировать GSK3, чтобы активировать mTOR в отсутствие β-катенина. Однако Wnt также может служить негативным регулятором mTOR посредством активации опухолевого супрессора TSC2 , который активируется посредством взаимодействия Dsh и GSK3. [39] Во время миогенеза Wnt использует PA и CREB для активации генов MyoD и Myf5 . [40] Wnt также действует совместно с Ryk и Src , обеспечивая регуляцию отталкивания нейронов во время наведения аксонов . Wnt регулирует гаструляцию , когда CK1 служит ингибитором Rap1-АТФазы для модуляции цитоскелета во время гаструляции. Дальнейшая регуляция гаструляции достигается, когда Wnt использует ROR2 вместе с путем CDC42 и JNK для регулирования экспрессии PAPC . Dsh также может взаимодействовать с aPKC, Pa3, Par6 и LGl, чтобы контролировать полярность клеток и развитие цитоскелета микротрубочек . Хотя эти пути перекрываются с компонентами, связанными с передачей сигналов PCP и Wnt/кальция, они считаются отдельными путями, поскольку вызывают разные ответы. [7]
Чтобы обеспечить правильное функционирование, передача сигналов Wnt постоянно регулируется в нескольких точках сигнальных путей. [41] Например, белки Wnt пальмитоилированы . Белок дикобраза опосредует этот процесс, а это означает, что он помогает регулировать момент секреции лиганда Wnt, определяя, когда он полностью сформирован. Секреция дополнительно контролируется с помощью белков, таких как GPR177 (wntless), и равномерности прерывания, а также комплексов, таких как ретромерный комплекс. [7] [24]
При секреции лиганду можно предотвратить достижение своего рецептора за счет связывания белков, таких как стабилизаторы Dally и глипикан 3 (GPC3), которые ингибируют диффузию. В раковых клетках как цепи гепарансульфата [42] [43], так и основной белок [44] [45] GPC3 участвуют в регуляции связывания Wnt и активации пролиферации клеток. [46] [47] Wnt распознает структуру гепарансульфата на GPC3, которая содержит IdoA2S и GlcNS6S, а 3-O-сульфатирование в GlcNS6S3S усиливает связывание Wnt с гепарансульфатглипиканом. [48] Было идентифицировано, что богатый цистеином домен в N-доле GPC3 образует Wnt-связывающую гидрофобную бороздку, включающую фенилаланин-41, который взаимодействует с Wnt. [45] [49] Блокирование связывающего домена Wnt с помощью нанотела под названием HN3 может ингибировать активацию Wnt. [45]
Связывание с рецептором Fz белков, отличных от Wnt, может противодействовать передаче сигналов. Конкретные антагонисты включают Dickkopf (Dkk), Wnt-ингибирующий фактор 1 (WIF-1), [50] [51] секретируемые Frizzled-родственные белки (SFRP), Cerberus , Frzb , Wise , SOST и Naked Cuticle . Они представляют собой ингибиторы передачи сигналов Wnt. Однако другие молекулы также действуют как активаторы. Норрин и R-спондин2 активируют передачу сигналов Wnt в отсутствие лиганда Wnt.
Взаимодействия между сигнальными путями Wnt также регулируют передачу сигналов Wnt. Как упоминалось ранее, путь Wnt/кальций может ингибировать TCF/β-катенин, предотвращая передачу сигналов канонического пути Wnt. [7] [24] Простагландин E2 (PGE2) является важным активатором канонического сигнального пути Wnt. Взаимодействие PGE2 с его рецепторами E2/E4 стабилизирует β-катенин посредством фосфорилирования, опосредованного цАМФ/ПКА. Синтез PGE2 необходим для процессов, опосредованных передачей сигналов Wnt, таких как регенерация тканей и контроль популяции стволовых клеток у рыбок данио и мышей. [5] Интересно, что неструктурированные области нескольких крупных внутренне неупорядоченных белков играют решающую роль в регуляции передачи сигналов Wnt. [52]
Передача сигналов Wnt играет решающую роль в эмбриональном развитии. Он действует как на позвоночных , так и на беспозвоночных , включая человека, лягушек, рыбок данио, C. elegans , дрозофилу и других. Впервые он был обнаружен в полярности сегментов дрозофилы, где он помогает установить переднюю и заднюю полярности. Он участвует в других процессах развития . Как предполагает его функция у дрозофилы , он играет ключевую роль в формировании осей тела , особенно в формировании переднезадней и дорсовентральной осей. Он участвует в индукции дифференцировки клеток , что приводит к образованию важных органов, таких как легкие и яичники . Wnt также обеспечивает развитие этих тканей посредством правильной регуляции пролиферации и миграции клеток . Функции передачи сигналов Wnt можно разделить на формирование паттерна оси, спецификацию клеточной судьбы, клеточную пролиферацию и клеточную миграцию. [53]
На раннем этапе развития эмбриона формирование основных осей тела является решающим шагом в установлении общего плана тела организма. Оси включают переднезаднюю ось, дорсовентральную ось и право-левую ось. Передача сигналов Wnt участвует в формировании переднезадней и дорсовентральной (DV) осей. Активность передачи сигналов Wnt в передне-заднем развитии можно наблюдать у млекопитающих, рыб и лягушек. У млекопитающих примитивная полоска и другие окружающие ткани продуцируют морфогенные соединения Wnts, BMPs , FGFs , Nodal и ретиноевую кислоту для образования задней области во время поздней гаструлы . Эти белки образуют градиенты концентрации. Области с наибольшей концентрацией определяют заднюю область, а области с наименьшей концентрацией указывают на переднюю область. У рыб и лягушек β-catenin, продуцируемый посредством канонической передачи сигналов Wnt, вызывает образование организующих центров, которые, наряду с BMPs, вызывают образование задних частей. Участие Wnt в формировании оси DV можно увидеть по активности образования организатора Спемана , который устанавливает дорсальную область. Каноническая передача сигналов Wnt вырабатывает β-катенин, индуцируя образование этого организатора посредством активации генов Twin и Siamois. [36] [53] Аналогичным образом, при гаструляции птиц клетки серпа Коллера экспрессируют различные мезодермальные маркерные гены, которые обеспечивают дифференциальное движение клеток во время формирования примитивной полоски. За это движение отвечает передача сигналов Wnt, активируемая FGF. [54] [55]
Передача сигналов Wnt также участвует в формировании осей определенных частей тела и систем органов на более поздних стадиях развития. У позвоночных морфогенетические сигнальные градиенты sonic hedgehog (Shh) и Wnt устанавливают дорсовентральную ось центральной нервной системы во время формирования осевого паттерна нервной трубки . Высокая передача сигналов Wnt устанавливает дорсальную область, тогда как высокая передача сигналов Shh указывает на вентральную область. [56] Wnt участвует в формировании DV центральной нервной системы посредством участия в наведении аксонов . Белки Wnt направляют аксоны спинного мозга в передне-заднем направлении. [57] Wnt также участвует в формировании оси DV конечности. В частности, Wnt7a помогает создавать дорсальный паттерн развивающейся конечности. [36] [53]
В модели развития волн эмбриональной дифференцировки Wnt играет решающую роль как часть сигнального комплекса в компетентных клетках, готовых к дифференцировке. Wnt реагирует на активность цитоскелета, стабилизируя первоначальные изменения, вызванные проходящей волной сокращения или расширения, и одновременно сигнализирует ядру, используя различные сигнальные пути, о том, в какой волне участвовала отдельная клетка. Таким образом, активность Wnt усиливается. механическая передача сигналов, возникающая во время развития. [58] [59]
Спецификация клеточной судьбы или дифференцировка клеток — это процесс, при котором недифференцированные клетки могут стать более специализированным типом клеток. Передача сигналов Wnt индуцирует дифференцировку плюрипотентных стволовых клеток в клетки-предшественники мезодермы и энтодермы . [60] Эти клетки-предшественники далее дифференцируются в типы клеток, такие как эндотелиальные, сердечные и сосудистые гладкомышечные линии. [61] Передача сигналов Wnt индуцирует образование крови из стволовых клеток. В частности, Wnt3 приводит к образованию мезодермальных коммитированных клеток с гемопоэтическим потенциалом. [62] Wnt1 противодействует нейрональной дифференцировке и является основным фактором самообновления нервных стволовых клеток. Это обеспечивает регенерацию клеток нервной системы, что является еще одним доказательством его роли в пролиферации нервных стволовых клеток. Передача сигналов Wnt участвует в детерминации зародышевых клеток , спецификации тканей кишечника , развитии волосяных фолликулов , развитии легочной ткани, дифференцировке клеток ствола нервного гребня , развитии нефронов , развитии яичников и определении пола . [53] Передача сигналов Wnt также противодействует формированию сердца, и было показано, что ингибирование Wnt является критическим индуктором сердечной ткани во время развития, [63] [64] [65] и низкомолекулярные ингибиторы Wnt обычно используются для производства кардиомиоцитов из плюрипотентных стволовых клеток. . [66] [67]
Для того чтобы произошла массовая дифференциация клеток, необходимая для формирования определенных клеточных тканей разных организмов, должны иметь место пролиферация и рост эмбриональных стволовых клеток . Этот процесс опосредован канонической передачей сигналов Wnt, которая увеличивает ядерный и цитоплазматический β-катенин. Увеличение β-катенина может инициировать транскрипционную активацию белков, таких как циклин D1 и c-myc , которые контролируют фазовый переход G1 в S в клеточном цикле . Переход в фазу S вызывает репликацию ДНК и, в конечном итоге , митоз , которые отвечают за пролиферацию клеток. [68] Это увеличение пролиферации напрямую связано с дифференцировкой клеток, поскольку по мере пролиферации стволовые клетки также дифференцируются. Это обеспечивает общий рост и развитие определенных тканевых систем во время эмбрионального развития. Это очевидно в таких системах, как система кровообращения, где Wnt3a приводит к пролиферации и расширению гемопоэтических стволовых клеток, необходимых для образования эритроцитов. [69]
Биохимия раковых стволовых клеток немного отличается от биохимии других опухолевых клеток. Эти так называемые Wnt-зависимые клетки захватывают и зависят от постоянной стимуляции пути Wnt, способствуя их неконтролируемому росту, выживанию и миграции. При раке передача сигналов Wnt может стать независимой от обычных стимулов за счет мутаций в нижестоящих онкогенах и генах-супрессорах опухолей, которые становятся постоянно активированными, даже если нормальный рецептор не получил сигнала. β-катенин связывается с факторами транскрипции, такими как белок TCF4 , и в сочетании молекулы активируют необходимые гены. LF3 сильно ингибирует это связывание in vitro, в клеточных линиях и снижает рост опухоли на мышиных моделях. Это предотвратило репликацию и снизило их способность к миграции, не затрагивая при этом здоровые клетки. После лечения раковых стволовых клеток не осталось. Это открытие стало результатом « рациональной разработки лекарств » с использованием технологий AlphaScreens и ELISA. [70]
Миграция клеток во время эмбрионального развития позволяет устанавливать оси тела, формировать ткани, индукцию конечностей и некоторые другие процессы. Передача сигналов Wnt помогает опосредовать этот процесс, особенно во время конвергентного расширения. Передача сигналов как от пути Wnt PCP, так и от канонического пути Wnt необходима для правильного конвергентного расширения во время гаструляции. Конвергентное расширение дополнительно регулируется путем Wnt/кальций, который блокирует конвергентное расширение при активации. Передача сигналов Wnt также индуцирует миграцию клеток на более поздних стадиях развития посредством контроля миграционного поведения нейробластов , клеток нервного гребня , миоцитов и клеток трахеи. [71]
Передача сигналов Wnt участвует в другом ключевом процессе миграции, известном как эпителиально-мезенхимальный переход (EMT). Этот процесс позволяет эпителиальным клеткам трансформироваться в мезенхимальные клетки, так что они больше не удерживаются на месте в ламинине . Он включает в себя подавление кадгерина, благодаря чему клетки могут отделяться от ламинина и мигрировать. Передача сигналов Wnt является индуктором ЕМТ, особенно при развитии молочных желез. [72]

Инсулин — это пептидный гормон , участвующий в гомеостазе глюкозы в некоторых организмах. В частности, это приводит к активации транспортеров глюкозы в клеточной мембране с целью увеличения поглощения глюкозы из кровотока . Этот процесс частично опосредован активацией передачи сигналов Wnt/β-катенина, которая может повышать чувствительность клеток к инсулину. В частности, Wnt10b представляет собой белок Wnt, который повышает чувствительность клеток скелетных мышц. [73]
С момента своего первоначального открытия передача сигналов Wnt была связана с раком . Когда был открыт Wnt1, он был впервые идентифицирован как протоонкоген на мышиной модели рака молочной железы. Тот факт, что Wnt1 является гомологом Wg, показывает, что он участвует в эмбриональном развитии, которое часто требует быстрого деления и миграции клеток. Неправильная регуляция этих процессов может привести к развитию опухоли за счет избыточной пролиферации клеток. [3]
Активность канонического пути Wnt участвует в развитии доброкачественных и злокачественных опухолей молочной железы. Роль пути Wnt в химиорезистентности опухоли также хорошо документирована, а также его роль в поддержании отдельной субпопуляции клеток, инициирующих рак. [74] Его присутствие выявляется по повышенным уровням β-катенина в ядре и/или цитоплазме, что можно обнаружить с помощью иммуногистохимического окрашивания и вестерн-блоттинга . Повышенная экспрессия β-катенина коррелирует с плохим прогнозом у пациентов с раком молочной железы. Это накопление может быть связано с такими факторами, как мутации в β-катенине, дефицит комплекса разрушения β-катенина, чаще всего из-за мутаций в структурно нарушенных участках APC , сверхэкспрессия лигандов Wnt, потеря ингибиторов и/или снижение активности регуляторных пути (такие как путь Wnt/кальций). [52] [75] [76] Опухоли молочной железы могут метастазировать из-за участия Wnt в ЕМТ. Исследования метастазирования базальноподобного рака молочной железы в легкие показали, что репрессия передачи сигналов Wnt/β-катенина может предотвратить ЕМТ, которая может ингибировать метастазирование. [77]
Передача сигналов Wnt вовлечена в развитие других видов рака, а также в десмоидный фиброматоз . [78] Изменения в экспрессии CTNNB1 , гена, кодирующего β-катенин, можно измерить при раке молочной железы, колоректальном раке , меланоме , предстательной железе , раке легких и других видах рака. Повышенная экспрессия белков-лигандов Wnt, таких как Wnt1, Wnt2 и Wnt7A, наблюдалась при развитии глиобластомы , рака пищевода и рака яичников соответственно. Другие белки, которые вызывают несколько типов рака при отсутствии правильного функционирования, включают ROR1, ROR2, SFRP4 , Wnt5A, WIF1 и белки семейства TCF/LEF. [79] Передача сигналов Wnt также участвует в патогенезе костных метастазов рака молочной железы и простаты, при этом исследования предполагают дискретные состояния включения и выключения. Wnt подавляется на стадии покоя с помощью аутокринного DKK1 , чтобы избежать иммунного надзора [80] , а также на стадиях диссеминации с помощью внутриклеточного Dact1. [81] Между тем, Wnt активируется во время ранней фазы роста с помощью E-селектина . [82]
Связь между PGE2 и Wnt предполагает, что связанное с хроническим воспалением увеличение PGE2 может привести к активации пути Wnt в различных тканях, что приводит к канцерогенезу . [5]
Сахарный диабет 2 типа — распространенное заболевание, вызывающее снижение секреции инсулина и повышение инсулинорезистентности на периферии. Это приводит к повышению уровня глюкозы в крови или гипергликемии , которая при отсутствии лечения может привести к летальному исходу. Поскольку передача сигналов Wnt участвует в чувствительности к инсулину, это может быть связано с нарушением работы его пути. Например, сверхэкспрессия Wnt5b может повысить восприимчивость из-за его роли в адипогенезе , поскольку ожирение и диабет II типа имеют высокую коморбидность . [83] Передача сигналов Wnt является сильным активатором митохондриального биогенеза . Это приводит к увеличению производства активных форм кислорода (АФК), которые, как известно, вызывают повреждение ДНК и клеток. [84] Это повреждение, вызванное АФК, является значительным, поскольку оно может вызвать острую печеночную резистентность к инсулину или резистентность к инсулину, вызванную повреждением. [85] Мутации в транскрипционных факторах, связанных с передачей сигналов Wnt, таких как TCF7L2 , связаны с повышенной восприимчивостью. [86]
{{cite book}}: |website=игнорируется ( помощь )