Углерод (от латинского carbo «уголь») — химический элемент ; он имеет символ C и атомный номер 6. Он неметаллический и четырехвалентный , что означает, что его атомы способны образовывать до четырех ковалентных связей из-за его валентной оболочки , содержащей 4 электрона. Он принадлежит к 14 группе периодической таблицы . [16] Углерод составляет около 0,025 процента земной коры. [17] В природе встречаются три изотопа : 12 C и 13 C являются стабильными, а 14 C представляет собой радионуклид , распадающийся с периодом полураспада 5700 лет. [18] Углерод — один из немногих элементов, известных с древности . [19]
Углерод — 15-й по распространенности элемент в земной коре и четвертый по массе элемент во Вселенной после водорода , гелия и кислорода . Обилие углерода, его уникальное разнообразие органических соединений и его необычная способность образовывать полимеры при температурах, обычно встречающихся на Земле, позволяют этому элементу служить общим элементом всей известной жизни . Это второй по распространенности элемент в организме человека по массе (около 18,5%) после кислорода. [20]
Атомы углерода могут связываться друг с другом разными способами, в результате чего образуются различные аллотропы углерода . Хорошо известные аллотропы включают графит , алмаз , аморфный углерод и фуллерены . Физические свойства углерода сильно различаются в зависимости от аллотропной формы. Например, графит непрозрачен и имеет черный цвет, а алмаз очень прозрачен . Графит достаточно мягок, чтобы образовывать полосы на бумаге (отсюда и его название, от греческого глагола «γράφειν», что означает «писать»), а алмаз — самый твердый из известных природных материалов. Графит является хорошим электропроводником , а алмаз имеет низкую электропроводность . В обычных условиях алмаз, углеродные нанотрубки и графен обладают самой высокой теплопроводностью среди всех известных материалов. Все аллотропы углерода при нормальных условиях представляют собой твердые вещества, при этом графит является наиболее термодинамически стабильной формой при стандартных температуре и давлении. Они химически устойчивы и требуют высокой температуры для реакции даже с кислородом.
Наиболее распространенная степень окисления углерода в неорганических соединениях — +4, а +2 встречается в карбонильных комплексах монооксида углерода и переходных металлов . Крупнейшими источниками неорганического углерода являются известняки , доломиты и углекислый газ , однако значительные его количества встречаются в органических отложениях угля , торфа , нефти и клатратах метана . Углерод образует огромное количество соединений , около двухсот миллионов из которых описаны и проиндексированы; [21], и тем не менее это число составляет лишь часть числа теоретически возможных соединений в стандартных условиях.
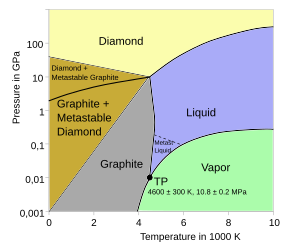
Аллотропы углерода включают графит , одно из самых мягких известных веществ, и алмаз , самое твердое вещество, встречающееся в природе. Он легко связывается с другими небольшими атомами, включая другие атомы углерода, и способен образовывать множественные стабильные ковалентные связи с подходящими многовалентными атомами. Углерод является составным элементом подавляющего большинства всех химических соединений , около двухсот миллионов примеров которого описано в опубликованной химической литературе. [21] Углерод также имеет самую высокую точку сублимации среди всех элементов. При атмосферном давлении он не имеет точки плавления, так как его тройная точка составляет 10,8 ± 0,2 мегапаскаля (106,6 ± 2,0 атм; 1566 ± 29 фунтов на квадратный дюйм) и 4600 ± 300 К (4330 ± 300 ° C; 7820 ± 540 ° F), [ 5] [6] , поэтому он сублимирует при температуре около 3900 К (3630 °C; 6560 °F). [23] [24] Графит гораздо более реакционноспособен, чем алмаз в стандартных условиях, несмотря на то, что он более термодинамически стабилен, поскольку его делокализованная пи-система гораздо более уязвима для атак. Например, графит можно окислить горячей концентрированной азотной кислотой при стандартных условиях до меллитовой кислоты C 6 (CO 2 H) 6 , которая сохраняет гексагональные звенья графита, разрушая при этом более крупную структуру. [25]
Углерод сублимируется в углеродной дуге, температура которой составляет около 5800 К (5530 °C или 9980 °F). Таким образом, независимо от своей аллотропной формы, углерод остается твердым при более высоких температурах, чем металлы с самой высокой температурой плавления, такие как вольфрам или рений . Несмотря на термодинамическую склонность к окислению, углерод сопротивляется окислению более эффективно, чем такие элементы, как железо и медь, которые при комнатной температуре являются более слабыми восстановителями.
Углерод — шестой элемент с электронной конфигурацией основного состояния 1s 2 2s 2 2p 2 , из которой четыре внешних электрона являются валентными электронами . Его первые четыре энергии ионизации: 1086,5, 2352,6, 4620,5 и 6222,7 кДж/моль намного выше, чем у более тяжелых элементов 14-й группы. Электроотрицательность углерода составляет 2,5, что значительно выше, чем у более тяжелых элементов группы 14 (1,8–1,9), но близко к большинству близлежащих неметаллов, а также к некоторым переходным металлам второго и третьего ряда . Ковалентные радиусы углерода обычно принимают равными 77,2 пм (C-C), 66,7 пм (C=C) и 60,3 пм (C≡C), хотя они могут варьироваться в зависимости от координационного числа и того, с чем связан углерод. Как правило, ковалентный радиус уменьшается с меньшим координационным числом и более высоким порядком связи. [26]
Соединения на основе углерода составляют основу всей известной жизни на Земле, а цикл углерод-азот-кислород обеспечивает небольшую часть энергии, производимой Солнцем, и большую часть энергии более крупных звезд (например, Сириуса ). Хотя он образует необычайное разнообразие соединений, большинство форм углерода сравнительно нереакционноспособны при нормальных условиях. При стандартной температуре и давлении он устойчив ко всем окислителям, кроме самых сильных. Не реагирует с серной кислотой , соляной кислотой , хлором и любыми щелочами . При повышенных температурах углерод реагирует с кислородом с образованием оксидов углерода и отбирает кислород у оксидов металлов, оставляя элементарный металл. Эта экзотермическая реакция используется в черной металлургии для выплавки железа и контроля содержания углерода в стали :
Углерод реагирует с серой с образованием сероуглерода , а также с паром в реакции уголь-газ, используемой при газификации угля :
Углерод соединяется с некоторыми металлами при высоких температурах с образованием металлических карбидов, таких как карбид железа в стали и карбид вольфрама , широко используемый в качестве абразива и для изготовления твердых наконечников режущих инструментов.
Система аллотропов углерода охватывает ряд крайностей:
Атомный углерод — очень недолговечный вид, и поэтому углерод стабилизируется в различных многоатомных структурах с разнообразными молекулярными конфигурациями, называемыми аллотропами . Три относительно хорошо известных аллотропа углерода — это аморфный углерод , графит и алмаз. Когда-то считавшиеся экзотическими, фуллерены в настоящее время широко синтезируются и используются в исследованиях; они включают в себя бакиболы , [32] [33] углеродные нанотрубки , [34] углеродные нанопочки [35] и нановолокна . [36] [37] Также было обнаружено несколько других экзотических аллотропов, таких как лонсдейлит , [38] стеклоуглерод , [39] углеродная нанопена [40] и линейный ацетиленовый углерод (карбин). [41]
Графен представляет собой двумерный лист углерода, атомы которого расположены в гексагональной решетке. По состоянию на 2009 год графен оказался самым прочным материалом, когда-либо испытанным. [42] Процесс отделения его от графита потребует дальнейшего технологического развития, прежде чем он станет экономически выгодным для промышленных процессов. [43] В случае успеха графен можно будет использовать в конструкции космического лифта . Его также можно использовать для безопасного хранения водорода для использования в водородных двигателях автомобилей. [44]

Аморфная форма представляет собой набор атомов углерода в некристаллическом, неправильном, стеклообразном состоянии, не удерживаемый в кристаллической макроструктуре. Он присутствует в виде порошка и является основным компонентом таких веществ, как древесный уголь, ламповая сажа (сажа) и активированный уголь . При нормальном давлении углерод принимает форму графита, в котором каждый атом тригонально связан с тремя другими в плоскости, состоящей из сросшихся шестиугольных колец, как в ароматических углеводородах . [45] Полученная сетка является двухмерной, а полученные плоские листы укладываются друг на друга и свободно соединяются посредством слабых сил Ван-дер-Ваальса . Это придает графиту мягкость и раскалывающие свойства (листы легко скользят друг по другу). Из-за делокализации одного из внешних электронов каждого атома с образованием π-облака графит проводит электричество , но только в плоскости каждого ковалентно связанного листа. Это приводит к более низкой объемной электропроводности углерода, чем для большинства металлов. Делокализация также объясняет энергетическую стабильность графита по отношению к алмазу при комнатной температуре.

При очень высоких давлениях углерод образует более компактный аллотроп — алмаз, плотность которого почти вдвое превышает плотность графита. Здесь каждый атом тетраэдрически связан с четырьмя другими, образуя трехмерную сеть сморщенных шестичленных колец атомов. Алмаз имеет ту же кубическую структуру , что и кремний и германий , и из-за прочности связей углерод-углерод он является самым твердым природным веществом, измеряемым по устойчивости к царапинам . Вопреки распространенному мнению, что «алмазы вечны» , они термодинамически нестабильны ( Δ f G ° (алмаз, 298 К) = 2,9 кДж/моль [46] ) при нормальных условиях (298 К, 10 5 Па) и теоретически должны превратиться в графит. [47] Но из-за высокого энергетического барьера активации переход в графит при нормальной температуре настолько медленный, что незаметен. Однако при очень высоких температурах алмаз превращается в графит, и алмазы могут сгореть при пожаре в доме. Левый нижний угол фазовой диаграммы углерода экспериментально не исследовался. Хотя вычислительное исследование с использованием методов теории функционала плотности привело к выводу, что при T → 0 К и p → 0 Па алмаз становится более стабильным, чем графит, примерно на 1,1 кДж/моль, [48] более поздние и окончательные экспериментальные и вычислительные исследования показывают, что графит более стабилен, чем алмаз при Т < 400 К , без приложенного давления, на 2,7 кДж/моль при Т = 0 К и на 3,2 кДж/моль при Т = 298,15 К. [49] При некоторых условиях углерод кристаллизуется в виде лонсдейлита , а гексагональная кристаллическая решетка , все атомы которой связаны ковалентно, и свойства аналогичны свойствам алмаза. [38]
Фуллерены представляют собой синтетические кристаллические образования с графитоподобной структурой, но вместо только плоских шестиугольных ячеек некоторые из ячеек, из которых образуются фуллерены, могут представлять собой пятиугольники, неплоские шестиугольники или даже семиугольники из атомов углерода. Таким образом, листы деформируются в сферы, эллипсы или цилиндры. Свойства фуллеренов (расщепленных на бакиболлы, бакитрубки и нанопочки) еще не полностью проанализированы и представляют собой интенсивную область исследований в области наноматериалов . Названия фуллерен и бакибол даны в честь Ричарда Бакминстера Фуллера , популяризатора геодезических куполов , напоминающих по структуре фуллерены. Баккиболлы представляют собой довольно крупные молекулы, полностью состоящие из углеродных связей, образующих сфероиды (наиболее известным и простым является бакминстерфуллерен C 60 в форме футбольного мяча ). [32] Углеродные нанотрубки (бакитрубки) структурно похожи на бакиболлы, за исключением того, что каждый атом связан тригонально в изогнутом листе, который образует полый цилиндр . [33] [34] Впервые о нанопочках было сообщено в 2007 году. Они представляют собой гибридные материалы из бакитрубок и бакиболов (бакиболы ковалентно связаны с внешней стенкой нанотрубки), которые сочетают в себе свойства обоих в единой структуре. [35]

Из других обнаруженных аллотропов углеродная нанопена представляет собой ферромагнитный аллотроп, открытый в 1997 году. Он состоит из кластерной сборки низкой плотности из атомов углерода, связанных вместе в рыхлую трехмерную паутину, в которой атомы соединены тригонально в шести- и семичленные кольца. Это одно из самых легких известных твердых веществ с плотностью около 2 кг/м 3 . [50] Точно так же стеклоуглерод содержит высокую долю закрытой пористости , [39] но, в отличие от обычного графита, графитовые слои не уложены друг на друга, как страницы в книге, а имеют более случайное расположение. Линейный ацетиленовый углерод [41] имеет химическую структуру [41] −(C≡C) n − . Углерод в этой модификации является линейным с sp- орбитальной гибридизацией и представляет собой полимер с чередующимися одинарными и тройными связями. Этот карбин представляет значительный интерес для нанотехнологий , поскольку его модуль Юнга в 40 раз больше, чем у самого твердого из известных материалов – алмаза. [51]
В 2015 году команда из Университета штата Северная Каролина объявила о разработке еще одного аллотропа, который они назвали Q-углеродом , созданного с помощью высокоэнергетического лазерного импульса малой длительности на аморфной углеродной пыли. Сообщается, что Q-углерод обладает ферромагнетизмом, флуоресценцией и твердостью, превосходящей алмазы. [52]
В паровой фазе часть углерода находится в форме высокореакционноспособного двухатомного диуглерода ( C 2 ). В возбужденном состоянии этот газ светится зеленым.


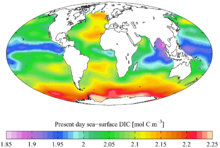
Углерод является четвертым по массе химическим элементом в наблюдаемой Вселенной после водорода, гелия и кислорода. Углерод в изобилии содержится на Солнце, звездах, кометах и в атмосферах большинства планет. [53] Некоторые метеориты содержат микроскопические алмазы, которые образовались, когда Солнечная система еще была протопланетным диском . [54] Микроскопические алмазы также могут образовываться под воздействием сильного давления и высокой температуры в местах ударов метеоритов. [55]
В 2014 году НАСА объявило о значительно обновленной базе данных для отслеживания полициклических ароматических углеводородов (ПАУ) во Вселенной. Более 20% углерода во Вселенной может быть связано с ПАУ — комплексными соединениями углерода и водорода без кислорода. [56] Эти соединения фигурируют в мировой гипотезе ПАУ , где предполагается, что они играют роль в абиогенезе и формировании жизни. ПАУ, судя по всему, образовались «через пару миллиардов лет» после Большого взрыва , широко распространены по всей Вселенной и связаны с новыми звездами и экзопланетами . [53]
Было подсчитано, что твердая Земля в целом содержит 730 частей на миллион углерода, из них 2000 частей на миллион в ядре и 120 частей на миллион в совокупности мантии и коры. [57] Поскольку масса Земли равна5,972 × 10 24 кг , это будет означать 4360 миллионов гигатонн углерода. Это намного больше, чем количество углерода в океанах или атмосфере (ниже).
В сочетании с кислородом в углекислом газе углерод содержится в атмосфере Земли (около 900 гигатонн углерода — каждая ppm соответствует 2,13 Гт) и растворен во всех водоемах (около 36 000 гигатонн углерода). Углерод в биосфере оценивается в 550 гигатонн, но с большой неопределенностью, главным образом из-за огромной неопределенности в количестве наземных глубоко подземных бактерий . [58] Углеводороды (такие как уголь, нефть и природный газ) также содержат углерод. «Запасы» угля (а не «ресурсы») составляют около 900 гигатонн и, возможно, 18 000 Гт ресурсов. [59] Запасы нефти составляют около 150 гигатонн. Доказанные источники природного газа175 × 10 12 кубических метров (содержащих около 105 гигатонн углерода), но исследования оценивают другое900 × 10 12 кубических метров «нетрадиционных» месторождений, таких как сланцевый газ , представляют собой около 540 гигатонн углерода. [60]
Углерод также содержится в гидратах метана в полярных регионах и под морями. По разным оценкам, это количество углерода составляет от 500, 2500, [61] до 3000 Гт. [62]
По данным одного источника, в период с 1751 по 2008 год около 347 гигатонн углерода было выброшено в атмосферу в виде углекислого газа в результате сжигания ископаемого топлива. [63] Другой источник оценивает количество, поступившее в атмосферу за период с 1750 года, в 879 Гт, а общее количество, поступившее в атмосферу, море и на сушу (например, в торфяные болота ), составило почти 2000 Гт. [64]
Углерод входит в состав (около 12% по массе) очень крупных масс карбонатных пород ( известняка , доломита , мрамора и других). Уголь очень богат углеродом ( 92–98% антрацита ) [65] и является крупнейшим коммерческим источником минерального углерода, на его долю приходится 4000 гигатонн или 80% ископаемого топлива . [66]
Что касается отдельных аллотропов углерода, то графит в больших количествах встречается в США (в основном в Нью-Йорке и Техасе ), России, Мексике, Гренландии и Индии. Природные алмазы встречаются в горной породе кимберлита , обнаруженной в древних вулканических «шеях» или «трубках». Большинство месторождений алмазов находится в Африке, особенно в Южной Африке, Намибии, Ботсване, Республике Конго и Сьерра-Леоне. Месторождения алмазов также обнаружены в Арканзасе , Канаде, Российской Арктике, Бразилии, а также в Северной и Западной Австралии. Сейчас алмазы добывают и со дна океана у мыса Доброй Надежды . Алмазы встречаются в природе, но около 30% всех промышленных алмазов, используемых в США, в настоящее время производятся.
Углерод-14 образуется в верхних слоях тропосферы и стратосферы на высотах 9–15 км в результате реакции, вызываемой космическими лучами . [67] Возникают тепловые нейтроны , которые сталкиваются с ядрами азота-14, образуя углерод-14 и протон. Как таковой,1,5% × 10-10 углекислого газа в атмосфере содержит углерод-14 . [68]
Богатые углеродом астероиды относительно преобладают во внешних частях пояса астероидов Солнечной системы. Ученые еще не брали образцы с этих астероидов. Астероиды могут быть использованы для гипотетической добычи углерода в космосе , что возможно в будущем, но в настоящее время технологически невозможно. [69]
Изотопы углерода — это атомные ядра , содержащие шесть протонов плюс несколько нейтронов (от 2 до 16). У углерода есть два стабильных природных изотопа. [70] Изотоп углерод-12 ( 12 C) образует 98,93% углерода на Земле, а углерод-13 ( 13 C) образует оставшиеся 1,07%. [70] Концентрация 12 C в биологических материалах еще больше увеличивается, поскольку биохимические реакции дискриминируют 13 C. [71] В 1961 году Международный союз теоретической и прикладной химии (IUPAC) принял изотоп углерода-12 в качестве основы для атомных весы . [72] Идентификация углерода в экспериментах по ядерному магнитному резонансу (ЯМР) проводится с помощью изотопа 13 C.
Углерод-14 ( 14 C) — природный радиоизотоп , созданный в верхних слоях атмосферы (нижней стратосфере и верхней тропосфере ) в результате взаимодействия азота с космическими лучами. [73] Он встречается в следовых количествах на Земле в размере 1 части на триллион (0,0000000001%) или более, в основном в атмосфере и поверхностных отложениях, особенно в торфе и других органических материалах. [74] Этот изотоп распадается на β - испускание с энергией 0,158 МэВ . Из-за относительно короткого периода полураспада5700 ± 30 лет, [18] 14 С практически отсутствует в древних породах. Количество 14 С в атмосфере и в живых организмах практически постоянно, но после смерти в их организме предсказуемо уменьшается. Этот принцип используется при радиоуглеродном датировании , изобретенном в 1949 году и широко используемом для определения возраста углеродистых материалов возрастом примерно до 40 000 лет. [75] [76]
Известно 15 изотопов углерода, самый короткоживущий из них — 8 C, который распадается за счет испускания протонов и имеет период полураспада 3,5 × 10–21 с. [18] Экзотический 19 C имеет ядерное гало , что означает, что его радиус значительно больше, чем можно было бы ожидать, если бы ядро представляло собой сферу постоянной плотности. [77]
Формирование атомного ядра углерода происходит внутри гигантской или сверхгигантской звезды посредством процесса тройного альфа . Это требует почти одновременного столкновения трех альфа-частиц (ядер гелия), поскольку продукты дальнейших реакций ядерного синтеза гелия с водородом или другим ядром гелия производят соответственно литий-5 и бериллий-8 , оба из которых крайне нестабильны и почти распадаются. мгновенно обратно в более мелкие ядра. [78] Процесс тройного альфа происходит в условиях температур более 100 мегакельвинов и концентрации гелия, которая была запрещена быстрым расширением и охлаждением ранней Вселенной, и поэтому во время Большого взрыва не было создано значительного количества углерода.
Согласно современной теории физической космологии, углерод образуется в недрах звезд на горизонтальной ветви . [79] Когда массивные звезды умирают как сверхновые, углерод рассеивается в космосе в виде пыли. Эта пыль становится компонентным материалом для формирования звездных систем следующего поколения с аккрецированными планетами. [53] [80] Солнечная система — одна из таких звездных систем с обилием углерода, обеспечивающим существование жизни в том виде, в каком мы ее знаем. По мнению большинства ученых, весь углерод в Солнечной системе и Млечном Пути происходит от умирающих звезд. [81] [82] [83]
Цикл CNO — это дополнительный механизм синтеза водорода, который питает звезды, в котором углерод действует как катализатор.
Вращательные переходы различных изотопных форм окиси углерода (например, 12 СО, 13 СО и 18 СО) обнаруживаются в субмиллиметровом диапазоне длин волн и используются при изучении вновь образующихся звезд в молекулярных облаках . [84]
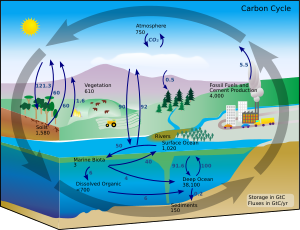
В земных условиях превращение одного элемента в другой происходит очень редко. Следовательно, количество углерода на Земле практически постоянно. Таким образом, процессы, в которых используется углерод, должны откуда-то его получать и где-то утилизировать. Пути прохождения углерода в окружающей среде образуют углеродный цикл . [85] Например, фотосинтезирующие растения извлекают углекислый газ из атмосферы (или морской воды) и превращают его в биомассу, как в цикле Кальвина , процессе фиксации углерода . [86] Некоторая часть этой биомассы съедается животными, а часть углерода выдыхается животными в виде углекислого газа. Углеродный цикл значительно сложнее этой короткой петли; например, некоторое количество углекислого газа растворено в океанах; если бактерии не потребляют его, мертвые растения или животные могут превратиться в нефть или уголь, которые при сжигании выделяют углерод. [87] [88]


Углерод может образовывать очень длинные цепочки взаимосвязанных углерод-углеродных связей , это свойство называется катенацией . Углерод-углеродные связи прочны и стабильны. Посредством цепной связи углерод образует бесчисленное количество соединений. Подсчет уникальных соединений показывает, что больше из них содержат углерод, чем нет. [89] Аналогичное утверждение можно сделать и в отношении водорода, поскольку большинство органических соединений содержат водород, химически связанный с углеродом или другим обычным элементом, таким как кислород или азот.
Простейшей формой органической молекулы является углеводород — большое семейство органических молекул, состоящих из атомов водорода, связанных с цепочкой атомов углерода. Углеводородная основная цепь может быть заменена другими атомами, известными как гетероатомы . Общие гетероатомы, которые появляются в органических соединениях, включают кислород, азот, серу, фосфор и нерадиоактивные галогены, а также металлы литий и магний. Органические соединения, содержащие связи с металлом, известны как металлоорганические соединения ( см. ниже ). Определенные группы атомов, часто включающие гетероатомы, встречаются в большом количестве органических соединений. Эти коллекции, известные как функциональные группы , определяют общие закономерности реакционной способности и позволяют систематически изучать и классифицировать органические соединения. Длина цепи, форма и функциональные группы влияют на свойства органических молекул. [90]
В большинстве стабильных соединений углерода (и почти во всех стабильных органических соединениях) углерод подчиняется правилу октетов и является четырехвалентным , что означает, что атом углерода образует в общей сложности четыре ковалентные связи (которые могут включать двойные и тройные связи). Исключения составляют небольшое количество стабилизированных карбокатионов (три связи, положительный заряд), радикалов (три связи, нейтральный), карбанионов (три связи, отрицательный заряд) и карбенов (две связи, нейтральный заряд), хотя эти виды гораздо чаще оказываются встречаются как нестабильные, реактивные промежуточные продукты.
Углерод встречается во всей известной органической жизни и является основой органической химии . В соединении с водородом он образует различные углеводороды, важные для промышленности в качестве хладагентов, смазочных материалов, растворителей, химического сырья для производства пластмасс и нефтехимии, а также в качестве ископаемого топлива.
В сочетании с кислородом и водородом углерод может образовывать множество групп важных биологических соединений, включая сахара, лигнаны , хитины , спирты, жиры, ароматические сложные эфиры , каротиноиды и терпены . С азотом образует алкалоиды , а с добавлением серы также образует антибиотики, аминокислоты и резиновые изделия. При добавлении фосфора к этим другим элементам он образует ДНК и РНК , носители химического кода жизни, и аденозинтрифосфат (АТФ), наиболее важную молекулу-переносчик энергии во всех живых клетках. [91] Норман Горовиц , руководитель миссий «Маринер» и «Викинг» на Марс (1965–1976), считал, что уникальные характеристики углерода делают маловероятным, что какой-либо другой элемент сможет заменить углерод, даже на другой планете, для создания биохимии, необходимой для жизнь. [92]
Обычно углеродсодержащие соединения, связанные с минералами или не содержащие связей с другими атомами углерода, галогенами или водородом, рассматривают отдельно от классических органических соединений; определение не является жестким, и классификация некоторых соединений может варьироваться от автора к автору (см. справочные статьи выше). К ним относятся простые оксиды углерода. Наиболее известным оксидом является диоксид углерода (CO 2 ). Когда-то это была основная составляющая палеоатмосферы , но сегодня она является второстепенным компонентом атмосферы Земли . [93] Растворяясь в воде, образует угольную кислоту ( H
2СО
3), но, как и большинство соединений с несколькими одинарными атомами кислорода на одном углероде, он нестабилен. [94] Однако через это промежуточное соединение образуются резонансно-стабилизированные карбонат -ионы . Некоторыми важными минералами являются карбонаты, особенно кальцит . Сероуглерод ( CS
2) аналогично. [25] Тем не менее, из-за своих физических свойств и связи с органическим синтезом сероуглерод иногда классифицируется как органический растворитель.
Другой распространенный оксид — окись углерода (CO). Он образуется при неполном сгорании и представляет собой бесцветный газ без запаха. Каждая молекула содержит тройную связь и достаточно полярна , что приводит к тенденции к постоянному связыванию с молекулами гемоглобина, вытесняя кислород, который имеет более низкую аффинность связывания. [95] [96] Цианид (CN - ) имеет аналогичную структуру, но ведет себя во многом как ион галогенида ( псевдогалоген ). Например, он может образовывать молекулу нитрида циана ((CN) 2 ), подобную двухатомным галогенидам. Аналогично, более тяжелый аналог цианида, циафид (CP- ) , также считается неорганическим, хотя большинство простых производных очень нестабильны. Другими необычными оксидами являются субоксид углерода ( C
3О
2), [97] нестабильный монооксид диуглерода (C 2 O), [98] [99] триоксид углерода (CO 3 ), [100] [101] циклопентанпентон (C 5 O 5 ), [102] циклогексангексон (C 6 O 6 ), [102] и меллитовый ангидрид (C 12 O 9 ). Однако меллитовый ангидрид представляет собой тройной ациловый ангидрид меллитовой кислоты; более того, он содержит бензольное кольцо. Таким образом, многие химики считают его органическим.
С химически активными металлами, такими как вольфрам , углерод образует либо карбиды (C 4- ), либо ацетилиды ( C2−
2) для образования сплавов с высокими температурами плавления. Эти анионы также связаны с метаном и ацетиленом , обеими очень слабыми кислотами. При электроотрицательности 2,5 [103] углерод предпочитает образовывать ковалентные связи . Некоторые карбиды имеют ковалентную решетку, например карборунд (SiC), напоминающий алмаз. Тем не менее, даже самые полярные и солеподобные карбиды не являются полностью ионными соединениями. [104]
Металлоорганические соединения по определению содержат по крайней мере одну ковалентную связь углерод-металл. Существует широкий спектр таких соединений; основные классы включают простые алкилметаллические соединения (например, тетраэтилсвинец ), η 2 -алкеновые соединения (например, соль Цейзе ) и η 3 -аллильные соединения (например, димер хлорида аллилпалладия ); металлоцены, содержащие циклопентадиенильные лиганды (например, ферроцен ); и карбеновые комплексы переходных металлов . Существует множество карбонилов металлов и цианидов металлов (например, тетракарбонилникель и феррицианид калия ); некоторые исследователи считают карбонильные и цианидные комплексы металлов без других углеродных лигандов чисто неорганическими, а не металлоорганическими. Однако большинство химиков-металлоргаников считают металлокомплексы с любым углеродным лигандом, даже «неорганическим углеродом» (например, карбонилами, цианидами и некоторыми типами карбидов и ацетилидов), металлоорганическими по своей природе. Металлокомплексы, содержащие органические лиганды без ковалентной связи углерод-металл (например, карбоксилаты металлов), называются металлоорганическими соединениями.
Хотя считается, что углерод предпочитает образование четырех ковалентных связей, известны и другие экзотические схемы связывания. Карбораны представляют собой высокостабильные додекаэдрические производные звена [B 12 H 12 ] 2- , в которых один BH заменен на CH + . Таким образом, углерод связан с пятью атомами бора и одним атомом водорода. Катион [(Ph 3 PAu) 6 C] 2+ содержит октаэдрический углерод, связанный с шестью фосфин-золотыми фрагментами. Это явление связывают с аурофильностью золотых лигандов, которые обеспечивают дополнительную стабилизацию лабильных частиц. [105] В природе железомолибденовый кофактор ( FeMoco ), ответственный за микробную фиксацию азота, также имеет октаэдрический углеродный центр (формально карбид C(-IV)) связанный с шестью атомами железа. В 2016 году было подтверждено, что, в соответствии с более ранними теоретическими предсказаниями, дикатион гексаметилбензола содержит атом углерода с шестью связями. Более конкретно, дикатион можно описать структурно формулой [MeC(η 5 -C 5 Me 5 )] 2+ , что делает его «органическим металлоценом », в котором фрагмент MeC 3+ связан с η 5 -C 5 Me 5 – фрагментируется по всем пяти атомам углерода кольца. [106]
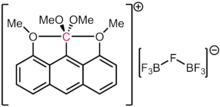
Важно отметить, что в рассмотренных выше случаях каждая из связей с углеродом содержит менее двух формальных электронных пар. Таким образом, формальное количество электронов этих видов не превышает октета. Это делает их гиперкоординированными, но не гипервалентными. Даже в случаях предполагаемых видов 10-C-5 (то есть углерода с пятью лигандами и формальным числом электронов, равным десяти), как сообщает Акиба и его коллеги [107] , расчеты электронной структуры заключают, что популяция электронов вокруг углерода по-прежнему меньше восьми, как и в случае других соединений с четырехэлектронной трехцентровой связью .

Английское название «углерод» происходит от латинского carbo , обозначающего уголь и древесный уголь, [108] откуда также происходит французское charbon , означающее древесный уголь. На немецком, голландском и датском языках названия углерода — Kohlenstoff , koolstof и kulstof соответственно, что буквально означает «угольное вещество».
Углерод был обнаружен в доисторические времена и был известен в виде сажи и древесного угля самым ранним человеческим цивилизациям. Алмазы были известны в Китае, вероятно, еще в 2500 году до нашей эры, а углерод в форме древесного угля производился с помощью того же химического процесса, что и сегодня, путем нагревания древесины в пирамиде, покрытой глиной, чтобы исключить доступ воздуха. [109] [110]

В 1722 году Рене Антуан Фершо де Реомюр продемонстрировал, что железо превращается в сталь в результате поглощения некоторого вещества, теперь известного как углерод. [111] В 1772 году Антуан Лавуазье показал, что алмазы представляют собой форму углерода; когда он сжег образцы древесного угля и алмаза и обнаружил, что ни один из них не образует воды и что оба выделяют одинаковое количество углекислого газа на грамм. В 1779 году [112] Карл Вильгельм Шееле показал, что графит, который считался разновидностью свинца, на самом деле идентичен древесному углю, но с небольшой примесью железа, и что он дает «воздушную кислоту» (его название углерода). диоксид) при окислении азотной кислотой. [113] В 1786 году французские ученые Клод Луи Бертолле , Гаспар Монж и К.А. Вандермонд подтвердили, что графит состоит в основном из углерода, окислив его кислородом почти так же, как Лавуазье сделал с алмазом. [114] Снова осталось немного железа, которое, по мнению французских ученых, было необходимо для структуры графита. В своей публикации они предложили название карбон (лат. Carbonum ) для элемента графита, который выделялся в виде газа при горении графита. Затем Антуан Лавуазье включил углерод в свой учебник 1789 года как элемент. [113]
Новый аллотроп углерода, фуллерен , открытый в 1985 году [115], включает наноструктурированные формы, такие как бакиболы и нанотрубки . [32] Их первооткрыватели – Роберт Керл , Гарольд Крото и Ричард Смолли – получили Нобелевскую премию по химии в 1996 году. [116] Возобновившийся интерес к новым формам привел к открытию дальнейших экзотических аллотропов, включая стеклообразный углерод и осознание того, что « аморфный углерод » не является строго аморфным . [39]
Коммерчески жизнеспособные природные месторождения графита встречаются во многих частях мира, но наиболее важные с экономической точки зрения источники находятся в Китае, Индии, Бразилии и Северной Корее. [ нужна ссылка ] [117] Графитовые месторождения имеют метаморфическое происхождение, встречаются в сочетании с кварцем , слюдой и полевым шпатом в сланцах, гнейсах и метаморфизованных песчаниках и известняках в виде линз или жил , иногда толщиной в один метр и более. Месторождения графита в Борроудейле , Камберленд , Англия, поначалу были настолько большими и чистыми, что до 19 века карандаши изготавливались путем распиливания блоков природного графита на полосы перед их помещением в древесину. Сегодня меньшие залежи графита получают путем дробления материнской породы и выплавления более легкого графита в воду. [118]
Существует три типа природного графита: аморфный, чешуйчатый или кристаллический чешуйчатый, прожилковый или кусковый. Аморфный графит имеет самое низкое качество и наиболее распространен. Вопреки науке, в промышленности термин «аморфный» означает очень маленький размер кристаллов, а не полное отсутствие кристаллической структуры. Аморфный используется для производства графитовых изделий с более низкой стоимостью и является самым дешевым графитом. Крупные месторождения аморфного графита обнаружены в Китае, Европе, Мексике и США. Чешуйчатый графит встречается реже и более высокого качества, чем аморфный; он встречается в виде отдельных пластин, кристаллизовавшихся в метаморфической породе. Чешуйчатый графит может стоить в четыре раза дороже аморфного. Чешуйки хорошего качества можно перерабатывать в расширяемый графит для различных целей, например, в качестве антипиренов . Крупнейшие месторождения находятся в Австрии, Бразилии, Канаде, Китае, Германии и на Мадагаскаре. Жилчатый или кусковый графит — самый редкий, ценный и высококачественный вид природного графита. Он встречается в жилах вдоль интрузивных контактов в виде твердых глыб и в промышленных масштабах добывается только в Шри-Ланке. [118]
По данным Геологической службы США , мировое производство природного графита в 2010 году составило 1,1 миллиона тонн, из которых Китай внес 800 000 тонн, Индия 130 000 тонн, Бразилия 76 000 тонн, Северная Корея 30 000 тонн и Канада 25 000 тонн. Сообщается, что в Соединенных Штатах не было добыто природного графита, но в 2009 году было произведено 118 000 тонн синтетического графита оценочной стоимостью 998 миллионов долларов. [118]

Цепочка поставок алмазов контролируется ограниченным числом влиятельных предприятий, а также сильно сконцентрирована в небольшом количестве мест по всему миру (см. рисунок).
Лишь очень небольшая часть алмазной руды состоит из настоящих алмазов. Руда измельчается, при этом необходимо соблюдать осторожность, чтобы предотвратить разрушение более крупных алмазов в этом процессе, а затем частицы сортируются по плотности. Сегодня алмазы располагаются в богатой алмазами фракции плотности с помощью рентгеновской флуоресценции , после чего финальные этапы сортировки выполняются вручную. До того, как использование рентгеновских лучей стало обычным явлением, разделение осуществлялось с помощью смазочных лент; алмазы имеют более сильную тенденцию прилипать к жиру, чем другие минералы в руде. [119]
Исторически известно, что алмазы можно найти только в аллювиальных месторождениях на юге Индии. [120] Индия лидировала в мире по добыче алмазов с момента их открытия примерно в 9 веке до нашей эры [121] до середины 18 века нашей эры, но коммерческий потенциал этих источников был исчерпан к концу 18 века и в На тот момент Индию затмила Бразилия, где в 1725 году были найдены первые неиндийские алмазы. [122]
Добыча алмазов коренных месторождений (кимберлитов и лампроитов) началась только в 1870-х годах после открытия месторождений алмазов в Южной Африке. Производство со временем увеличивалось, и с этой даты в общей сложности было добыто более 4,5 миллиардов каратов. [123] Наиболее коммерчески жизнеспособные месторождения алмазов находились в России, Ботсване, Австралии и Демократической Республике Конго. [124] К 2005 году Россия производила почти одну пятую мировой добычи алмазов (в основном на территории Якутии ; например, трубки «Мир» и трубка «Удачная» ), но единственным крупнейшим источником стал рудник Аргайл в Австралии, добывший 14 миллионов каратов в 2018 году. [ 125] [126] Новые находки, канадские рудники в Дьявике и Экати , как ожидается, станут еще более ценными благодаря производству камней ювелирного качества. [127]
В Соединенных Штатах алмазы были найдены в Арканзасе, Колорадо и Монтане. [128] В 2004 году поразительное открытие микроскопического алмаза в Соединенных Штатах [129] привело к массовому отбору проб в январе 2008 года из кимберлитовых трубок в отдаленной части Монтаны. [130]






Углерод необходим для всех известных живых систем, и без него жизнь в том виде, в котором мы ее знаем, не могла бы существовать (см. альтернативную биохимию ). Основное экономическое использование углерода, помимо продуктов питания и древесины, происходит в форме углеводородов, в первую очередь ископаемого топлива, метана и сырой нефти (нефти). Сырая нефть перегоняется на нефтеперерабатывающих заводах нефтехимической промышленности для производства бензина, керосина и других продуктов. Целлюлоза — это природный углеродсодержащий полимер, вырабатываемый растениями в виде древесины, хлопка, льна и конопли . Целлюлоза используется в первую очередь для поддержания структуры растений. К коммерчески ценным углеродным полимерам животного происхождения относятся шерсть, кашемир и шелк. Пластмассы изготавливаются из синтетических углеродных полимеров, часто с атомами кислорода и азота, включенными через равные промежутки в основную полимерную цепь. Сырьем для многих из этих синтетических веществ является сырая нефть.
Применение углерода и его соединений чрезвычайно разнообразно. Он может образовывать сплавы с железом, из которых наиболее распространена углеродистая сталь . Графит в сочетании с глинами образует «грифель», используемый в карандашах для письма и рисования. Он также используется в качестве смазки и пигмента, как формовочный материал при производстве стекла, в электродах для сухих батарей, при гальванике и гальванопластике , в щётках для электродвигателей и как замедлитель нейтронов в ядерных реакторах .
Древесный уголь используется в качестве материала для рисования в произведениях искусства, при приготовлении барбекю, выплавке железа и во многих других областях. Древесина, уголь и нефть используются в качестве топлива для производства энергии и отопления. Алмаз ювелирного качества используется в ювелирных изделиях, а технические алмазы используются в инструментах для сверления, резки и полировки металлов и камня. Пластмассы производятся из ископаемых углеводородов, а углеродное волокно , полученное пиролизом синтетических полиэфирных волокон, используется для армирования пластмасс с целью формирования современных легких композитных материалов.
Углеродное волокно производится пиролизом экструдированных и растянутых нитей полиакрилонитрила (ПАН) и других органических веществ. Кристаллографическая структура и механические свойства волокна зависят от типа исходного материала и последующей обработки. Углеродные волокна, изготовленные из ПАН, имеют структуру, напоминающую узкие нити графита, но термическая обработка может изменить структуру в непрерывный прокатанный лист. В результате получаются волокна с более высокой удельной прочностью на разрыв , чем у стали. [131]
Углеродная сажа используется в качестве черного пигмента в печатной краске, художественных масляных красках и акварельных красках, копировальной бумаге , автомобильных покрытиях, чернилах и тонере для лазерных принтеров . Углеродная сажа также используется в качестве наполнителя в резиновых изделиях, таких как шины, и в пластиковых соединениях. Активированный уголь используется в качестве абсорбента и адсорбента в фильтрующем материале в таких разнообразных применениях, как противогазы, очистка воды и кухонные вытяжки , а также в медицине для поглощения токсинов, ядов или газов из пищеварительной системы. Углерод используется при химическом восстановлении при высоких температурах. Кокс используется для восстановления железной руды в железо (плавка). Цементация стали достигается путем нагрева готовых стальных деталей в углеродном порошке. Карбиды кремния , вольфрама , бора и титана являются одними из самых твердых известных материалов и используются в качестве абразивов в режущих и шлифовальных инструментах. Углеродные соединения составляют большую часть материалов, используемых в одежде, таких как натуральный и синтетический текстиль и кожа, а также почти все внутренние поверхности в искусственной среде, за исключением стекла, камня, гипсокартона и металла.
Алмазная промышленность делится на две категории: одна занимается алмазами ювелирного качества, а другая — алмазами промышленного качества . Несмотря на то, что существует большая торговля обоими типами бриллиантов, эти два рынка функционируют совершенно по-разному.
В отличие от драгоценных металлов, таких как золото или платина, драгоценные алмазы не торгуются как товар. При продаже алмазов существует значительная наценка, а рынок перепродажи бриллиантов не очень активен.
Промышленные алмазы ценятся главным образом за их твердость и теплопроводность, при этом геммологические качества чистоты и цвета практически не имеют значения. Около 80% добытых алмазов (около 100 миллионов каратов или 20 тонн в год) непригодны для использования в качестве драгоценных камней и направляются для промышленного использования (известного как борт ) . [132] Синтетические алмазы , изобретенные в 1950-х годах, практически сразу же нашли промышленное применение; Ежегодно производится 3 миллиарда каратов (600 тонн ) синтетических алмазов. [133]
Преобладающее промышленное использование алмаза — огранка, сверление, шлифовка и полировка. Большинство этих приложений не требуют крупных алмазов; Фактически, большинство алмазов ювелирного качества, за исключением их небольшого размера, можно использовать в промышленных целях. Алмазы встраивают в наконечники сверл или пильные полотна или измельчают в порошок для использования при шлифовке и полировке. [134] Специализированные применения включают использование в лабораториях в качестве защитной оболочки для экспериментов под высоким давлением (см. ячейку с алмазной наковальней ), высокопроизводительные подшипники и ограниченное использование в специализированных окнах. [135] [136] С продолжающимся прогрессом в производстве синтетических алмазов, новые применения становятся возможными. Большое волнение вызывает возможность использования алмаза в качестве полупроводника , подходящего для микрочипов , а также, благодаря его исключительной теплопроводности, в качестве радиатора в электронике. [137]


Чистый углерод имеет чрезвычайно низкую токсичность для человека, и с ним можно безопасно обращаться в виде графита или древесного угля. Он устойчив к растворению или химическому воздействию даже в кислом содержимом пищеварительного тракта. Следовательно, попав в ткани организма, он, скорее всего, останется там на неопределенный срок. Углеродная сажа, вероятно, была одним из первых пигментов, которые стали использовать для татуировок, и у Эци Ледяного человека были обнаружены углеродные татуировки, которые сохранились при его жизни и в течение 5200 лет после его смерти. [138] Вдыхание угольной пыли или сажи (технического углерода) в больших количествах может быть опасным, поскольку раздражает ткани легких и вызывает застойную болезнь легких — пневмокониоз угольщиков . Алмазная пыль, используемая в качестве абразива, может быть вредной при проглатывании или вдыхании. Микрочастицы углерода образуются в выхлопных газах дизельных двигателей и могут накапливаться в легких. [139] В этих примерах вред может быть вызван загрязнителями (например, органическими химикатами, тяжелыми металлами), а не самим углеродом.
Углерод обычно малотоксичен для жизни на Земле; но углеродные наночастицы смертельны для дрозофилы . [140]
Углерод может энергично и ярко гореть в присутствии воздуха при высоких температурах. Большие скопления угля, которые оставались инертными в течение сотен миллионов лет в отсутствие кислорода, могут самопроизвольно воспламеняться под воздействием воздуха в отвалах угольных шахт, грузовых трюмах кораблей и угольных бункерах, [141] [142] и отвалах хранения. .
В ядерных приложениях, где графит используется в качестве замедлителя нейтронов , может произойти накопление энергии Вигнера с последующим внезапным спонтанным высвобождением. Отжиг до температуры как минимум 250 ° C может безопасно высвободить энергию, хотя при пожаре в Виндскейле процедура пошла не так, что привело к возгоранию других материалов реактора.
Большое разнообразие углеродных соединений включает такие смертельные яды, как тетродотоксин , лектин рицин из семян клещевины Ricinus communis , цианид (CN- ) и окись углерода; и такие необходимые для жизни вещества, как глюкоза и белок.