Хлорофилл — это любой из нескольких родственных зеленых пигментов , обнаруженных в цианобактериях и в хлоропластах водорослей и растений . [2] Его название происходит от греческих слов χλωρός , хлорос («бледно-зеленый») и φύλλον , филлон («лист»). [3] Хлорофилл позволяет растениям поглощать энергию света.
Хлорофиллы наиболее сильно поглощают свет в синей части электромагнитного спектра , а также в красной части. [4] И наоборот, он плохо поглощает зеленую и околозеленую части спектра. Следовательно, ткани, содержащие хлорофилл, кажутся зелеными, потому что зеленый свет, диффузно отражаемый такими структурами, как клеточные стенки, меньше поглощается. [1] В фотосистемах зеленых растений существуют два типа хлорофилла: хлорофилл а и b . [5]
Хлорофилл был впервые выделен и назван Жозефом Бьенеме Каванту и Пьером Жозефом Пеллетье в 1817 году . [6] Присутствие магния в хлорофилле было обнаружено в 1906 году [7] и стало первым обнаружением этого элемента в живых тканях. [8]
После первоначальной работы, проделанной немецким химиком Рихардом Вильштеттером с 1905 по 1915 год, общая структура хлорофилла а была выяснена Гансом Фишером в 1940 году. К 1960 году, когда большая часть стереохимии хлорофилла а была известна, Роберт Бернс Вудворд опубликовал полный синтез. молекулы. [8] [9] В 1967 году последнее оставшееся стереохимическое объяснение было завершено Яном Флемингом , [10] а в 1990 году Вудворд и соавторы опубликовали обновленный синтез. [11] В 2010 году было объявлено, что хлорофилл f присутствует в цианобактериях и других оксигенных микроорганизмах, образующих строматолиты ; [12] [13] на основе ЯМР, оптических и масс-спектров установлены молекулярная формула C 55 H 70 O 6 N 4 Mg и строение (2- формил )-хлорофилла а . [14]

Хлорофилл жизненно важен для фотосинтеза , который позволяет растениям поглощать энергию света . [15]
Молекулы хлорофилла располагаются внутри и вокруг фотосистем , встроенных в тилакоидные мембраны хлоропластов . [16] В этих комплексах хлорофилл выполняет три функции:
Двумя принятыми в настоящее время единицами фотосистемы являются фотосистема I и фотосистема II , которые имеют свои собственные реакционные центры, называемые P700 и P680 соответственно. Эти центры названы в честь длины волны (в нанометрах ) их максимума поглощения красного пика. Идентичность, функции и спектральные свойства типов хлорофилла в каждой фотосистеме различны и определяются друг другом и окружающей их белковой структурой.
Функция реакционного центра хлорофилла — поглощать световую энергию и передавать ее другим частям фотосистемы. Поглощенная энергия фотона передается электрону в процессе, называемом разделением зарядов. Отрыв электрона от хлорофилла является реакцией окисления. Хлорофилл отдает электрон высокой энергии ряду молекулярных промежуточных продуктов, называемых цепью переноса электронов . Заряженный реакционный центр хлорофилла (P680 + ) затем восстанавливается обратно в основное состояние, принимая электрон, оторванный от воды. Электрон, восстанавливающий P680 +, в конечном итоге возникает в результате окисления воды до O2 и H + через несколько промежуточных продуктов. Эта реакция — то, как фотосинтезирующие организмы, такие как растения, производят газ O 2 и является источником практически всего O 2 в атмосфере Земли. Фотосистема I обычно работает последовательно с Фотосистемой II; таким образом, P700 + Фотосистемы I обычно восстанавливается, поскольку он принимает электрон через множество промежуточных продуктов в тилакоидной мембране электронами, поступающими, в конечном итоге, из Фотосистемы II. Однако реакции переноса электрона в тилакоидных мембранах сложны, и источник электронов, используемых для восстановления P700 + , может варьироваться.
Поток электронов, создаваемый пигментами хлорофилла реакционного центра, используется для перекачки ионов H + через тилакоидную мембрану, создавая протондвижущую силу — хемиосмотический потенциал, используемый в основном для производства АТФ (запасённой химической энергии) или для восстановления НАДФ + до НАДФН . НАДФН – универсальный агент , используемый для восстановления CO 2 до сахаров, а также в других реакциях биосинтеза.
Комплексы хлорофилл-белок реакционного центра способны напрямую поглощать свет и осуществлять процессы разделения заряда без помощи других пигментов хлорофилла, но вероятность того, что это произойдет при заданной интенсивности света, мала. Таким образом, все остальные хлорофиллы в фотосистеме и белки-пигменты антенн совместно поглощают и направляют световую энергию в реакционный центр. Помимо хлорофилла а , в этих антенных комплексах пигмент-белок встречаются и другие пигменты, называемые акцессорными пигментами .
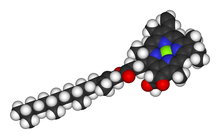
Известно несколько хлорофиллов. Все они определяются как производные исходного хлорина по наличию пятого кетонсодержащего кольца помимо четырех пирролоподобных колец. Большинство хлорофиллов классифицируются как хлорины , которые являются восстановленными родственниками порфиринов (содержащихся в гемоглобине ). Они имеют общий путь биосинтеза с порфиринами, включая предшественника уропорфириногена III . В отличие от гема, который содержит железо, связанное с центром N4, большинство хлорофиллов связывают магний . Осевые лиганды , присоединенные к центру Mg 2+ , часто для ясности опускаются. К хлориновому кольцу присоединены различные боковые цепи, обычно включающие длинную фитильную цепь ( C 20 H 39 O ). Наиболее широко распространенной формой у наземных растений является хлорофилл а . Единственная разница между хлорофиллом а и хлорофиллом b заключается в том, что первый имеет метильную группу, а второй — формильную группу. Эта разница вызывает значительную разницу в спектре поглощения, позволяя растениям поглощать большую часть видимого света.
Структуры хлорофиллов кратко описаны ниже: [17] [18]
Хлорофилл e зарезервирован для пигмента, который был извлечен из водорослей в 1966 году, но не описан химически. Помимо буквенных хлорофиллов, в дикой природе известно множество модификаций боковой цепи хлорофилла. Например, цианобактерия Prochromococcus использует 8-винил Chl a и b . [19]

Хлорофиллы можно экстрагировать из белка органическими растворителями. [20] [21] [22] Таким образом можно оценить концентрацию хлорофилла в листе. [23] Также существуют методы разделения хлорофилла a и хлорофилла b .
В диэтиловом эфире хлорофилл а имеет приблизительные максимумы поглощения 430 и 662 нм, тогда как хлорофилл b имеет приблизительные максимумы 453 и 642 нм. [24] Пики поглощения хлорофилла а находятся при 465 нм и 665 нм. Хлорофилл а флуоресцирует при 673 нм (максимум) и 726 нм. Пиковый молярный коэффициент поглощения хлорофилла а превышает 10 5 М -1 см -1 , что является одним из самых высоких значений для низкомолекулярных органических соединений. [25] В 90% ацетон-воде пиковые длины волн поглощения хлорофилла а составляют 430 нм и 664 нм; пики хлорофилла b – 460 нм и 647 нм; пики хлорофилла с 1 составляют 442 нм и 630 нм; пики хлорофилла с 2 составляют 444 нм и 630 нм; пики хлорофилла d составляют 401 нм, 455 нм и 696 нм. [26]
Отношение эмиссии флуоресценции можно использовать для измерения содержания хлорофилла. При возбуждении флуоресценции хлорофилла на более низкой длине волны соотношение эмиссии флуоресценции хлорофилла при705 ± 10 нм иДлина волны 735 ± 10 нм может обеспечить линейную зависимость содержания хлорофилла по сравнению с химическим тестированием. Соотношение F 735 / F 700 обеспечивало значение корреляции r 2 0,96 по сравнению с химическими испытаниями в диапазоне от 41 мг м -2 до 675 мг м -2 . Гительсон также разработал формулу для прямого определения содержания хлорофилла в мг м -2 . Формула обеспечила надежный метод измерения содержания хлорофилла от 41 мг м- 2 до 675 мг м -2 со значением корреляции r 2 0,95. [27]
В некоторых растениях хлорофилл образуется из глутамата и синтезируется по разветвленному пути биосинтеза , который является общим с гемом и сирогемой . [28] [29] [30] Хлорофиллсинтаза [31] — фермент, завершающий биосинтез хлорофилла а : [32] [33]
В результате этого преобразования образуется сложный эфир группы карбоновой кислоты в хлорофиллиде а с 20-углеродным дитерпеновым спиртом фитолом . Хлорофилл b производится тем же ферментом, который действует на хлорофиллид b . То же самое известно о хлорофиллах d и f , которые оба состоят из соответствующих хлорофиллидов, в конечном итоге полученных из хлорофиллида а . [34]
У покрытосеменных растений более поздние этапы пути биосинтеза зависят от света. Такие растения бледны ( этиолированы ), если выращиваются в темноте. Несосудистые растения и зеленые водоросли имеют дополнительный светонезависимый фермент и растут зелеными даже в темноте. [35]
Хлорофилл связан с белками . Протохлорофиллид , один из промежуточных продуктов биосинтеза, встречается преимущественно в свободной форме и в условиях освещения действует как фотосенсибилизатор , образуя свободные радикалы , которые могут быть токсичными для растения. Следовательно, растения регулируют количество этого предшественника хлорофилла. У покрытосеменных эта регуляция достигается на стадии аминолевулиновой кислоты (АЛК) – одного из промежуточных соединений пути биосинтеза. Растения, получающие АЛК, накапливают высокие и токсичные уровни протохлорофиллида; то же самое делают и мутанты с поврежденной регуляторной системой. [36]
Процесс старения растений включает в себя деградацию хлорофилла: например, фермент хлорофиллаза ( EC 3.1.1.14) гидролизует фитильную боковую цепь, обращая вспять реакцию, в которой хлорофиллы биосинтезируются из хлорофиллида a или b . Поскольку хлорофиллид а может быть преобразован в хлорофиллид b , а последний может быть повторно этерифицирован в хлорофилл b , эти процессы позволяют совершать циклический цикл между хлорофиллами a и b . Более того, хлорофилл b может быть напрямую восстановлен (через 7 1 -гидроксихлорофилл a ) обратно в хлорофилл a , завершая цикл. [37] [38] На более поздних стадиях старения хлорофиллиды превращаются в группу бесцветных тетрапирролов , известных как нефлуоресцентные катаболиты хлорофилла (NCC), с общей структурой:
Эти соединения также были обнаружены в созревающих плодах и придают лиственным растениям характерную осеннюю окраску . [38] [39]
Карты хлорофилла показывают миллиграммы хлорофилла на кубический метр морской воды каждый месяц. Места, где количество хлорофилла было очень низким, что указывает на очень низкую численность фитопланктона , отмечены синим цветом. Места, где концентрация хлорофилла была высокой, а это означает, что росло много фитопланктона, отмечены желтым цветом. Наблюдения происходят с помощью спектрорадиометра визуализации среднего разрешения (MODIS) на спутнике НАСА Aqua. Земля окрашена в темно-серый цвет, а места, где MODIS не смог собрать данные из-за морского льда, полярной тьмы или облаков, — светло-серого цвета. Самая высокая концентрация хлорофилла, где процветают крошечные обитающие на поверхности океанские растения , наблюдается в холодных полярных водах или в местах, где океанские течения выносят холодную воду на поверхность, например, вокруг экватора и вдоль берегов континентов. Не сама холодная вода стимулирует фитопланктон. Вместо этого низкие температуры часто являются признаком того, что вода поднимается на поверхность из более глубоких слоев океана, неся с собой питательные вещества, накопившиеся с течением времени. В полярных водах питательные вещества накапливаются в поверхностных водах в темные зимние месяцы, когда растения не могут расти. Когда весной и летом солнечный свет возвращается, растения процветают в высоких концентрациях. [40]
Синтетический хлорофилл зарегистрирован в качестве красителя пищевой добавки, его номер E — E140 . Повара используют хлорофилл для придания зеленого цвета различным продуктам питания и напиткам, таким как макароны и спиртные напитки. Абсент приобретает свой зеленый цвет естественным образом благодаря хлорофиллу, вносимому в него из большого количества трав, используемых при его производстве. [41] Хлорофилл не растворяется в воде, поэтому его сначала смешивают с небольшим количеством растительного масла , чтобы получить желаемый раствор . [ нужна цитата ]
Исследование 2002 года показало, что «листья, подвергнутые сильному свету, содержат деградированные основные антенные белки , в отличие от тех, которые хранятся в темноте, что согласуется с исследованиями освещения изолированных белков ». Это показалось авторам подтверждением гипотезы о том, что « активные формы кислорода играют роль in vivo » в кратковременном поведении растений. [42]
Из стр. 49:
«Hauptproduct der щелочного гидролиза может быть окрашен в щелочную среду. В его комплексе магния есть металл, который содержится в щелочи, а также при более высоких температурах, более широких, чем энтальпия».
(Темно-зеленые щелочные соли образуют основной продукт щелочного гидролиза. В них присутствуют сложные соединения магния, содержащие металл в связи, необычайно устойчивой к щелочам даже при высокой температуре.)
{{cite book}}: |website=игнорируется ( помощь )