Органическая химия — это раздел химии , включающий научное изучение структуры, свойств и реакций органических соединений и органических материалов , т. е. веществ в их различных формах, содержащих атомы углерода . [1] Изучение структуры определяет их структурную формулу . Изучение свойств включает физические и химические свойства , а также оценку химической реакционной способности для понимания их поведения. Изучение органических реакций включает химический синтез природных продуктов , лекарств и полимеров , а также изучение отдельных органических молекул в лабораторных условиях и посредством теоретического ( in silico ) исследования.
Диапазон химических веществ, изучаемых в органической химии, включает углеводороды (соединения, содержащие только углерод и водород ), а также соединения на основе углерода, но также содержащие другие элементы, [1] [2] [3] особенно кислород , азот , серу , фосфор (входит во многие биохимические вещества ) и галогены . Металлоорганическая химия изучает соединения, содержащие связи углерод- металл .
Кроме того, современные исследования сосредоточены на органической химии с участием других металлоорганических соединений , включая лантаноиды , но особенно переходных металлов: цинка, меди, палладия , никеля, кобальта, титана и хрома.
Органические соединения составляют основу всей земной жизни и составляют большинство известных химических веществ. Модели связей углерода с его валентностью четыре — формальные одинарные, двойные и тройные связи, плюс структуры с делокализованными электронами — делают множество органических соединений структурно разнообразными, а их спектр применения огромным. Они составляют основу или являются составными частями многих коммерческих продуктов, включая фармацевтические препараты ; нефтехимические и агрохимические продукты ; и продукты, изготовленные из них, включая смазочные материалы , растворители ; пластмассы ; топливо и взрывчатые вещества . Изучение органической химии пересекается с металлоорганической химией и биохимией , а также с медицинской химией , полимерной химией и материаловедением . [1]
Органическую химию обычно преподают на уровне колледжа или университета. [4] Это считается очень сложным курсом, но он также стал доступным для студентов. [5]

До XVIII века химики в целом считали, что соединения, полученные из живых организмов, наделены жизненной силой, которая отличает их от неорганических соединений . Согласно концепции витализма (теории жизненной силы), органическое вещество наделено «жизненной силой». [6] В первой половине XIX века были опубликованы некоторые из первых систематических исследований органических соединений. Около 1816 года Мишель Шеврёль начал изучать мыла, изготовленные из различных жиров и щелочей . Он отделил кислоты, которые в сочетании со щелочью давали мыло. Поскольку все это были отдельные соединения, он продемонстрировал, что можно вносить химические изменения в различные жиры (которые традиционно поступают из органических источников), получая новые соединения без «жизненной силы». В 1828 году Фридрих Вёлер получил органическое химическое вещество мочевину (карбамид), составную часть мочи , из неорганических исходных материалов (солей цианата калия и сульфата аммония ), в том, что сейчас называется синтезом Вёлера . Хотя сам Вёлер был осторожен в своих заявлениях об опровержении витализма, это был первый случай, когда вещество, считавшееся органическим, было синтезировано в лаборатории без биологических (органических) исходных материалов. Это событие в настоящее время общепризнанно как действительно опровергающее доктрину витализма. [7]
После Вёлера над организацией органической химии работал Юстус фон Либих , считающийся одним из ее главных основателей. [8]
В 1856 году Уильям Генри Перкин , пытаясь изготовить хинин , случайно получил органический краситель , ныне известный как лиловый краситель Перкина . Его открытие, получившее широкую известность благодаря своему финансовому успеху, значительно повысило интерес к органической химии. [9]
Решающим прорывом в органической химии стала концепция химической структуры, разработанная независимо в 1858 году Фридрихом Августом Кекуле и Арчибальдом Скоттом Купером . [10] Оба исследователя предположили, что четырехвалентные атомы углерода могут соединяться друг с другом, образуя углеродную решетку, и что подробные закономерности атомных связей можно распознать с помощью умелой интерпретации соответствующих химических реакций. [11]
Эпоха фармацевтической промышленности началась в последнее десятилетие XIX века, когда немецкая компания Bayer впервые произвела ацетилсалициловую кислоту, более известную как аспирин . [12] К 1910 году Пауль Эрлих и его лабораторная группа начали разрабатывать арсенамин на основе мышьяка (сальварсан) в качестве первого эффективного лекарственного средства для лечения сифилиса и тем самым положили начало медицинской практике химиотерапии . Эрлих популяризировал концепции «волшебных пулей» и систематического улучшения лекарственной терапии. [13] [14] Его лаборатория внесла решающий вклад в разработку антисыворотки для дифтерии и стандартизацию терапевтических сывороток. [15]

Ранние примеры органических реакций и приложений часто находили благодаря сочетанию удачи и подготовки к неожиданным наблюдениям. Однако вторая половина 19-го века стала свидетелем систематических исследований органических соединений. Развитие синтетического индиго является показательным. Производство индиго из растительных источников сократилось с 19 000 тонн в 1897 году до 1000 тонн к 1914 году благодаря синтетическим методам, разработанным Адольфом фон Байером . В 2002 году из нефтехимических продуктов было произведено 17 000 тонн синтетического индиго . [17]
В начале XX века было показано, что полимеры и ферменты представляют собой крупные органические молекулы, а нефть имеет биологическое происхождение.
Многоступенчатый синтез сложных органических соединений называется полным синтезом. Полный синтез сложных природных соединений увеличился по сложности до глюкозы и терпинеола . Например, холестерин -родственные соединения открыли пути синтеза сложных человеческих гормонов и их модифицированных производных. С начала 20-го века сложность полных синтезов увеличилась, включив молекулы высокой сложности, такие как лизергиновая кислота и витамин B 12 . [18]

Открытие нефти и развитие нефтехимической промышленности стимулировали развитие органической химии. Преобразование отдельных нефтяных соединений в типы соединений с помощью различных химических процессов привело к органическим реакциям, позволяющим производить широкий спектр промышленных и коммерческих продуктов, включая, среди (многих) других: пластмассы , синтетический каучук , органические клеи и различные модифицирующие свойства нефтяные добавки и катализаторы .
Большинство химических соединений, встречающихся в биологических организмах, являются углеродными соединениями, поэтому связь между органической химией и биохимией настолько тесна, что биохимию можно рассматривать как по сути ветвь органической химии. Хотя история биохимии может охватывать около четырех столетий, фундаментальное понимание этой области начало развиваться только в конце 19 века, а сам термин биохимия был придуман около начала 20 века. Исследования в этой области увеличивались на протяжении всего двадцатого века, без каких-либо признаков замедления темпов роста, что можно подтвердить, проверив службы абстракции и индексации, такие как BIOSIS Previews и Biological Abstracts , которые начинались в 1920-х годах как единый ежегодный том, но выросли так резко, что к концу 20 века они были доступны только обычному пользователю как онлайновая электронная база данных . [19]
Поскольку органические соединения часто существуют в виде смесей , были разработаны различные методы оценки чистоты; методы хроматографии особенно важны для этого применения и включают в себя ВЭЖХ и газовую хроматографию . Традиционные методы разделения включают дистилляцию , кристаллизацию , выпаривание , магнитное разделение и экстракцию растворителем .
Органические соединения традиционно характеризовались различными химическими тестами, называемыми «мокрыми методами», но такие тесты были в значительной степени вытеснены спектроскопическими или другими компьютерными методами анализа. [20] Перечисленные в приблизительном порядке полезности, основные аналитические методы следующие:
Традиционные спектроскопические методы, такие как инфракрасная спектроскопия , оптическое вращение и УФ/видимая спектроскопия, предоставляют относительно неспецифическую структурную информацию, но остаются в использовании для определенных приложений. Показатель преломления и плотность также могут быть важны для идентификации веществ.
Физические свойства органических соединений, как правило, представляют интерес, включая как количественные, так и качественные характеристики. Количественная информация включает температуру плавления, температуру кипения, растворимость и показатель преломления. Качественные свойства включают запах, консистенцию и цвет.
Органические соединения обычно плавятся, а многие кипят. Напротив, хотя неорганические материалы обычно можно расплавить, многие не кипят, а вместо этого имеют тенденцию к разложению. В прежние времена точка плавления (т. пл.) и точка кипения (т. к.) давали важную информацию о чистоте и идентичности органических соединений. Температуры плавления и кипения коррелируют с полярностью молекул и их молекулярной массой. Некоторые органические соединения, особенно симметричные, сублимируются . Хорошо известным примером сублимируемого органического соединения является пара-дихлорбензол , пахучий компонент современных нафталиновых шариков. Органические соединения обычно не очень стабильны при температурах выше 300 °C, хотя существуют некоторые исключения.
Нейтральные органические соединения, как правило, гидрофобны ; то есть они менее растворимы в воде, чем неорганические растворители. Исключения включают органические соединения, которые содержат ионизируемые группы, а также низкомолекулярные спирты , амины и карбоновые кислоты , где происходит образование водородных связей . В противном случае органические соединения имеют тенденцию растворяться в органических растворителях . Растворимость широко варьируется в зависимости от органического растворенного вещества и органического растворителя.
Различные специализированные свойства молекулярных кристаллов и органических полимеров с сопряженными системами представляют интерес в зависимости от приложений, например, термомеханические и электромеханические, такие как пьезоэлектричество , электропроводность (см. проводящие полимеры и органические полупроводники ), и электрооптические (например, нелинейная оптика ) свойства. По историческим причинам такие свойства в основном являются предметом изучения областей науки о полимерах и материаловедения .

Названия органических соединений являются либо систематическими, логически вытекающими из набора правил, либо несистематическими, следующими различным традициям. Систематическая номенклатура предусмотрена спецификациями IUPAC (Международного союза теоретической и прикладной химии). Систематическая номенклатура начинается с названия родительской структуры в интересующей молекуле. Затем это родительское название модифицируется префиксами, суффиксами и числами, чтобы однозначно передать структуру. Учитывая, что известны миллионы органических соединений, строгое использование систематических названий может быть обременительным. Таким образом, рекомендации IUPAC более строго соблюдаются для простых соединений, но не для сложных молекул. Чтобы использовать систематическое наименование, необходимо знать структуры и названия родительских структур. Родительские структуры включают незамещенные углеводороды, гетероциклы и их монофункциональные производные.
Несистематическая номенклатура проще и однозначнее, по крайней мере для химиков-органиков. Несистематические названия не указывают на структуру соединения. Они обычны для сложных молекул, которые включают большинство природных продуктов. Так, неформально названный диэтиламид лизергиновой кислоты систематически называется (6a R ,9 R )- N , N -диэтил-7-метил-4,6,6a,7,8,9-гексагидроиндоло-[4,3- fg ] хинолин-9-карбоксамид.
С ростом использования вычислений появились другие методы именования, предназначенные для интерпретации машинами. Два популярных формата — SMILES и InChI .
Органические молекулы чаще всего описываются рисунками или структурными формулами , комбинациями рисунков и химических символов. Формула «линия-угол» проста и недвусмысленна. В этой системе конечные точки и пересечения каждой линии представляют один углерод, а атомы водорода могут быть либо обозначены явно, либо предполагаться присутствующими, как подразумевается четырехвалентным углеродом.

К 1880 году произошел взрыв в количестве открытых химических соединений, чему способствовали новые синтетические и аналитические методы. Гриньяр описал ситуацию как "chaos le plus complet" (полный хаос), из-за отсутствия соглашения стало возможным иметь несколько названий для одного и того же соединения. Это привело к созданию Женевских правил в 1892 году. [21]
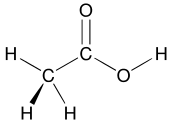
Концепция функциональных групп является центральной в органической химии, как в качестве средства для классификации структур, так и для прогнозирования свойств. Функциональная группа является молекулярным модулем, и предполагается, что реакционная способность этой функциональной группы в определенных пределах одинакова в различных молекулах. Функциональные группы могут оказывать решающее влияние на химические и физические свойства органических соединений. Молекулы классифицируются на основе их функциональных групп. Например, все спирты имеют субъединицу COH. Все спирты, как правило, несколько гидрофильны , обычно образуют сложные эфиры и обычно могут быть преобразованы в соответствующие галогениды . Большинство функциональных групп содержат гетероатомы (атомы, отличные от C и H). Органические соединения классифицируются в соответствии с функциональными группами, спиртами, карбоновыми кислотами, аминами и т. д. [22] Функциональные группы делают молекулу более кислой или основной из-за их электронного влияния на окружающие части молекулы.
По мере увеличения p K a ( основности ) молекулярной присоединения/функциональной группы, существует соответствующий диполь , при измерении которого увеличивается сила. Диполь, направленный к функциональной группе (более высокий p K a , следовательно, основная природа группы), указывает на нее и уменьшается в силе с увеличением расстояния. Дипольное расстояние (измеряемое в ангстремах ) и стерическое препятствие по отношению к функциональной группе оказывают межмолекулярное и внутримолекулярное влияние на окружающую среду и уровень pH .
Различные функциональные группы имеют различные значения p K a и прочность связи (одинарная, двойная, тройная), что приводит к повышенной электрофильности с более низким p K a и повышенной нуклеофильной прочности с более высоким p K a . Более основные/нуклеофильные функциональные группы стремятся атаковать электрофильную функциональную группу с более низким p K a на другой молекуле (межмолекулярная) или внутри той же молекулы (внутримолекулярная). Любая группа с чистым кислотным p K a , которая попадает в диапазон, например, ацильная или карбонильная группа, является честной игрой. Поскольку вероятность быть атакованным уменьшается с увеличением p K a , компоненты ацилхлорида с самыми низкими измеренными значениями p K a с наибольшей вероятностью будут атакованы, за ними следуют карбоновые кислоты (p K a = 4), тиолы (13), малонаты (13), спирты (17), альдегиды (20), нитрилы (25), сложные эфиры (25), затем амины (35). [23] Амины очень основные и являются прекрасными нуклеофилами/атакующими агентами.
Алифатические углеводороды подразделяются на три группы гомологических рядов в зависимости от степени их насыщения :
Остальная часть группы классифицируется в соответствии с присутствующими функциональными группами. Такие соединения могут быть «прямоцепочечными», разветвленными или циклическими. Степень разветвленности влияет на характеристики, такие как октановое число или цетановое число в нефтехимии.
Как насыщенные ( алициклические ) соединения, так и ненасыщенные соединения существуют в виде циклических производных. Наиболее стабильные кольца содержат пять или шесть атомов углерода, но распространены большие кольца (макроциклы) и меньшие кольца. Наименьшее семейство циклоалканов — это трехчленный циклопропан ((CH 2 ) 3 ). Насыщенные циклические соединения содержат только одинарные связи, тогда как ароматические кольца имеют чередующуюся (или сопряженную) двойную связь. Циклоалканы не содержат кратных связей, тогда как циклоалкены и циклоалкины содержат.
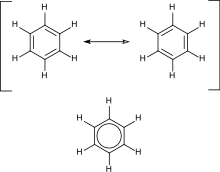
Ароматические углеводороды содержат сопряженные двойные связи. Это означает, что каждый атом углерода в кольце находится в состоянии sp2-гибридизации, что обеспечивает дополнительную стабильность. Наиболее важным примером является бензол , структура которого была сформулирована Кекуле , который первым предложил принцип делокализации или резонанса для объяснения его структуры. Для «обычных» циклических соединений ароматичность обеспечивается наличием 4n + 2 делокализованных пи-электронов, где n — целое число. Особая нестабильность ( антиароматичность ) обеспечивается наличием 4n сопряженных пи-электронов.
Характеристики циклических углеводородов снова изменяются, если присутствуют гетероатомы, которые могут существовать либо как заместители, присоединенные снаружи к кольцу (экзоциклические), либо как член самого кольца (эндоциклические). В последнем случае кольцо называется гетероциклом. Пиридин и фуран являются примерами ароматических гетероциклов, в то время как пиперидин и тетрагидрофуран являются соответствующими алициклическими гетероциклами. Гетероатом гетероциклических молекул обычно является кислородом, серой или азотом, причем последний особенно распространен в биохимических системах.
Гетероциклы обычно встречаются в широком спектре продуктов, включая анилиновые красители и лекарства. Кроме того, они распространены в широком спектре биохимических соединений, таких как алкалоиды , витамины, стероиды и нуклеиновые кислоты (например, ДНК, РНК).
Кольца могут сливаться с другими кольцами на краю, образуя полициклические соединения . Пуриновые нуклеозидные основания являются известными полициклическими ароматическими гетероциклами. Кольца также могут сливаться на «углу» так, что один атом (почти всегда углерод) имеет две связи, идущие к одному кольцу, и две — к другому. Такие соединения называются спиро и играют важную роль в нескольких природных продуктах .

Одним из важных свойств углерода является то, что он легко образует цепи или сети, которые связаны углерод-углеродными (углерод-углеродными) связями. Процесс связывания называется полимеризацией , а цепи или сети называются полимерами . Исходное соединение называется мономером .
Существуют две основные группы полимеров : синтетические полимеры и биополимеры . Синтетические полимеры производятся искусственно и обычно называются промышленными полимерами . [24] Биополимеры встречаются в почтительно естественной среде или без вмешательства человека.
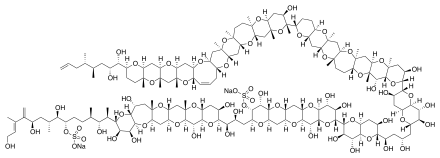
Биомолекулярная химия является основной категорией в органической химии, которую часто изучают биохимики . Многие сложные многофункциональные групповые молекулы важны для живых организмов. Некоторые из них являются длинноцепочечными биополимерами , и к ним относятся пептиды , ДНК , РНК и полисахариды, такие как крахмалы у животных и целлюлозы у растений. Другими основными классами являются аминокислоты (мономерные строительные блоки пептидов и белков), углеводы (включая полисахариды), нуклеиновые кислоты (включая ДНК и РНК в качестве полимеров) и липиды . Кроме того, биохимия животных содержит много небольших молекулярных промежуточных соединений, которые помогают в производстве энергии через цикл Кребса и производят изопрен , наиболее распространенный углеводород у животных. Изопрены у животных образуют важные стероидные структурные ( холестерин ) и стероидные гормональные соединения; и в растениях образуют терпены , терпеноиды , некоторые алкалоиды и класс углеводородов, называемых биополимерными полиизопреноидами, присутствующими в латексе различных видов растений, который является основой для изготовления резины . Биологи обычно классифицируют вышеупомянутые биомолекулы на четыре основные группы, т. е. белки, липиды, углеводы и нуклеиновые кислоты. Нефть и ее производные считаются органическими молекулами, что согласуется с тем фактом, что эта нефть происходит от окаменения живых существ, т. е. биомолекул. [25] См. также: синтез пептидов , синтез олигонуклеотидов и синтез углеводов .

В фармакологии важной группой органических соединений являются малые молекулы , также называемые «малыми органическими соединениями». В этом контексте малая молекула — это небольшое органическое соединение, которое биологически активно, но не является полимером . На практике малые молекулы имеют молярную массу менее примерно 1000 г/моль.
Фуллерены и углеродные нанотрубки , углеродные соединения со сфероидальной и трубчатой структурой, стимулировали множество исследований в смежной области материаловедения . Первый фуллерен был открыт в 1985 году сэром Гарольдом В. Крото из Великобритании и Ричардом Э. Смолли и Робертом Ф. Керлом-младшим из США. Используя лазер для испарения графитовых стержней в атмосфере гелия, эти химики и их помощники получили молекулы, похожие на клетки, состоящие из 60 атомов углерода (C60), соединенных одинарными и двойными связями, чтобы сформировать полую сферу с 12 пятиугольными и 20 шестиугольными гранями — конструкция, которая напоминает футбольный мяч. В 1996 году трио было удостоено Нобелевской премии за свои новаторские усилия. Молекула C60 была названа бакминстерфуллереном (или, проще говоря, бакиболом) в честь американского архитектора Р. Бакминстера Фуллера, чей геодезический купол построен по тем же структурным принципам.
Органические соединения, содержащие связи углерода с азотом, кислородом и галогенами, обычно не группируются отдельно. Другие иногда объединяются в основные группы в рамках органической химии и обсуждаются под такими названиями, как сероорганическая химия , металлоорганическая химия , фосфорорганическая химия и кремнийорганическая химия .
Органические реакции — это химические реакции с участием органических соединений . [26] Многие из этих реакций связаны с функциональными группами. Общая теория этих реакций включает тщательный анализ таких свойств, как электронное сродство ключевых атомов, прочность связей и стерические препятствия . Эти факторы могут определять относительную стабильность короткоживущих реактивных промежуточных продуктов , которые обычно напрямую определяют путь реакции.
Основные типы реакций: реакции присоединения , реакции элиминирования , реакции замещения , перициклические реакции , реакции перегруппировки и окислительно-восстановительные реакции . [27] Примером распространенной реакции является реакция замещения, записанная как:
где X — некоторая функциональная группа , а Nu — нуклеофил .
Число возможных органических реакций бесконечно. Однако наблюдаются некоторые общие закономерности, которые можно использовать для описания многих распространенных или полезных реакций. Каждая реакция имеет пошаговый механизм реакции, который объясняет, как она происходит в последовательности, хотя подробное описание шагов не всегда ясно из одного только списка реагентов.
Поэтапный ход любого заданного механизма реакции можно представить с помощью методов протягивания стрелок , в которых изогнутые стрелки используются для отслеживания движения электронов при переходе исходных материалов через промежуточные соединения в конечные продукты.

Синтетическая органическая химия является прикладной наукой , поскольку она граничит с инженерией , «проектированием, анализом и/или конструированием работ для практических целей». [28] Органический синтез нового соединения является задачей решения проблем, где синтез разрабатывается для целевой молекулы путем выбора оптимальных реакций из оптимальных исходных материалов. Сложные соединения могут иметь десятки стадий реакции, которые последовательно строят желаемую молекулу. Синтез происходит путем использования реакционной способности функциональных групп в молекуле. Например, карбонильное соединение может быть использовано в качестве нуклеофила путем преобразования его в енолят , или в качестве электрофила ; сочетание этих двух называется альдольной реакцией . Разработка практически полезных синтезов всегда требует проведения фактического синтеза в лаборатории. Научная практика создания новых синтетических путей для сложных молекул называется полным синтезом . [29]
Стратегии проектирования синтеза включают ретросинтез , популяризированный EJ Corey , который начинается с целевой молекулы и разделяет ее на части в соответствии с известными реакциями. Части или предлагаемые предшественники получают одинаковую обработку, пока не будут достигнуты доступные и в идеале недорогие исходные материалы. Затем ретросинтез записывается в обратном направлении, чтобы получить синтез. Можно построить «синтетическое дерево», поскольку каждое соединение, а также каждый предшественник имеет несколько синтезов.
{{cite web}}: CS1 maint: numeric names: authors list (link)