В молекулярной биологии [ 1] [2] [3] репликация ДНК — это биологический процесс создания двух идентичных копий ДНК из одной исходной молекулы ДНК . [4] Репликация ДНК происходит во всех живых организмах, выступая в качестве наиболее важной части биологического наследования . Это необходимо для деления клеток во время роста и восстановления поврежденных тканей, а также гарантирует, что каждая из новых клеток получит свою собственную копию ДНК. [5] Клетка обладает отличительным свойством деления, что делает репликацию ДНК необходимой.
ДНК состоит из двойной спирали из двух комплементарных нитей . Двойная спираль описывает внешний вид двухцепочечной ДНК, которая, таким образом, состоит из двух линейных нитей, которые идут напротив друг друга и скручиваются вместе, образуя. [6] Во время репликации эти нити разделяются. Каждая нить исходной молекулы ДНК затем служит шаблоном для производства своего аналога, процесс, называемый полуконсервативной репликацией . В результате полуконсервативной репликации новая спираль будет состоять из исходной нити ДНК, а также из вновь синтезированной нити. [7] Механизмы клеточной проверки и проверки ошибок обеспечивают почти идеальную точность репликации ДНК. [8] [9]
В клетке репликация ДНК начинается в определенных местах, или точках начала репликации , [10] в геноме [11], который содержит генетический материал организма. [12] Раскручивание ДНК в точке начала и синтез новых цепей, осуществляемый ферментом, известным как геликаза , приводит к тому, что репликационные вилки растут в двух направлениях от точки начала. Ряд белков связаны с репликационной вилкой, чтобы помочь в инициировании и продолжении синтеза ДНК . Наиболее заметно, что ДНК-полимераза синтезирует новые цепи, добавляя нуклеотиды , которые дополняют каждую (шаблонную) цепь. Репликация ДНК происходит во время S-стадии интерфазы . [13]
Репликация ДНК (амплификация ДНК) также может быть выполнена in vitro (искусственно, вне клетки). [14] ДНК-полимеразы, выделенные из клеток, и искусственные праймеры ДНК могут быть использованы для запуска синтеза ДНК в известных последовательностях в молекуле ДНК-матрицы. Примерами являются полимеразная цепная реакция (ПЦР), лигазная цепная реакция (ЛЦР) и транскрипционно-опосредованная амплификация (ТМА). В марте 2021 года исследователи сообщили о доказательствах, свидетельствующих о том, что предварительная форма транспортной РНК , необходимый компонент трансляции , биологического синтеза новых белков в соответствии с генетическим кодом , могла быть самой репликаторной молекулой на самом раннем этапе развития жизни, или абиогенеза . [15] [16]
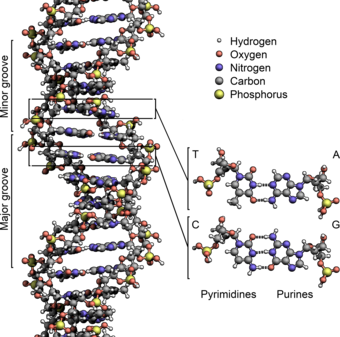
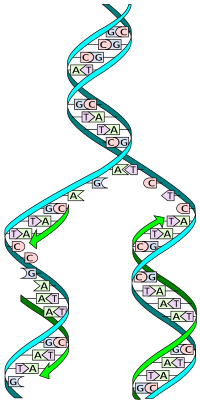
ДНК существует как двухцепочечная структура, в которой обе нити скручены вместе, образуя характерную двойную спираль . Каждая отдельная нить ДНК представляет собой цепочку из четырех типов нуклеотидов . Нуклеотиды в ДНК содержат дезоксирибозный сахар, фосфат и нуклеиновое основание . Четыре типа нуклеотидов соответствуют четырем нуклеиновым основаниям : аденину , цитозину , гуанину и тимину , обычно сокращенно обозначаемым как A, C, G и T. Аденин и гуанин являются пуриновыми [17] основаниями, тогда как цитозин и тимин являются пиримидинами . Эти нуклеотиды образуют фосфодиэфирные связи , создавая фосфатно-дезоксирибозный остов двойной спирали ДНК с нуклеиновыми основаниями, направленными внутрь (т. е. к противоположной цепи). Азотистые основания сопоставляются между цепями посредством водородных связей , образуя пары оснований . Аденин образует пару с тимином (две водородные связи), а гуанин – с цитозином (три водородные связи ). [18]
Цепи ДНК имеют направленность , и разные концы одной цепи называются «3′ (три-штрих) концом» и «5′ (пять-штрих) концом». По соглашению, если дана последовательность оснований одной цепи ДНК, левый конец последовательности является 5′ концом, в то время как правый конец последовательности является 3′ концом. Цепи двойной спирали являются антипараллельными, причем одна находится 5′ к 3′, а противоположная цепь 3′ к 5′. Эти термины относятся к атому углерода в дезоксирибозе, к которому присоединяется следующий фосфат в цепи. Направленность имеет последствия в синтезе ДНК, поскольку ДНК-полимераза может синтезировать ДНК только в одном направлении, добавляя нуклеотиды к 3′ концу цепи ДНК.
Спаривание комплементарных оснований в ДНК (посредством водородных связей ) означает, что информация, содержащаяся в каждой нити, избыточна. Фосфодиэфирные (внутринитевые) связи прочнее водородных (межнитевых) связей. Фактическая работа фосфодиэфирных связей заключается в том, что в полимерах ДНК 5'-атом углерода одного нуклеотида соединяется с 3'-атомом углерода другого нуклеотида, в то время как водородные связи стабилизируют двойные спирали ДНК поперек оси спирали, но не в направлении оси. [19] Это позволяет отделить нити друг от друга. Поэтому нуклеотиды на одной нити можно использовать для реконструкции нуклеотидов на вновь синтезированной партнерской нити. [20]

ДНК-полимеразы — это семейство ферментов , которые осуществляют все формы репликации ДНК. [22] ДНК-полимеразы в целом не могут инициировать синтез новых цепей, а могут только удлинять существующую цепь ДНК или РНК, спаренную с цепью-шаблоном. Чтобы начать синтез, короткий фрагмент РНК, называемый праймером , должен быть создан и спарен с цепью-шаблоном ДНК.
ДНК-полимераза добавляет новую цепь ДНК, удлиняя 3'-конец существующей нуклеотидной цепи, добавляя новые нуклеотиды, соответствующие шаблонной цепи, по одному за раз, посредством создания фосфодиэфирных связей . Энергия для этого процесса полимеризации ДНК поступает от гидролиза высокоэнергетических фосфатных (фосфоангидридных) связей между тремя фосфатами, прикрепленными к каждому неинкорпорированному основанию . Свободные основания с прикрепленными к ним фосфатными группами называются нуклеотидами ; в частности, основания с тремя прикрепленными фосфатными группами называются нуклеозидтрифосфатами . Когда нуклеотид добавляется к растущей цепи ДНК, образование фосфодиэфирной связи между проксимальным фосфатом нуклеотида к растущей цепи сопровождается гидролизом высокоэнергетической фосфатной связи с высвобождением двух дистальных фосфатных групп в виде пирофосфата . Ферментативный гидролиз полученного пирофосфата в неорганический фосфат расходует вторую высокоэнергетическую фосфатную связь и делает реакцию фактически необратимой. [Примечание 1]
В целом, ДНК-полимеразы очень точны, с собственной частотой ошибок менее одной ошибки на каждые 10 7 добавленных нуклеотидов. [23] Некоторые ДНК-полимеразы также могут удалять нуклеотиды с конца развивающейся цепи, чтобы исправить несовпадающие основания. Это известно как корректура. Наконец, механизмы исправления несовпадений после репликации контролируют ДНК на наличие ошибок, будучи способными отличать несовпадения в недавно синтезированной цепи ДНК от исходной последовательности цепи. Вместе эти три шага дискриминации обеспечивают точность репликации менее одной ошибки на каждые 10 9 добавленных нуклеотидов. [23]
Скорость репликации ДНК в живой клетке была впервые измерена как скорость удлинения ДНК фага Т4 в инфицированной фагом E. coli . [24] В период экспоненциального увеличения ДНК при 37 °C скорость составляла 749 нуклеотидов в секунду. Скорость мутации на пару оснований на репликацию во время синтеза ДНК фага Т4 составляет 1,7 на 10 8 . [25]

Репликация ДНК, как и все биологические процессы полимеризации, протекает в три ферментативно катализируемых и координируемых этапа: инициация, удлинение и терминация.
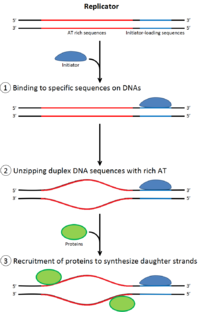

Для деления клетки она должна сначала реплицировать свою ДНК. [26] Репликация ДНК — это процесс «все или ничего»; как только репликация начинается, она продолжается до завершения. После завершения репликации она не происходит снова в том же клеточном цикле. Это становится возможным благодаря разделению инициации пререпликационного комплекса .
В позднем митозе и ранней фазе G1 большой комплекс белков-инициаторов собирается в комплекс пре-репликации в определенных точках ДНК, известных как « истоки ». [11] [10] В E. coli первичным белком-инициатором является Dna A ; в дрожжах это комплекс распознавания ориджина . [27] Последовательности, используемые белками-инициаторами, как правило, «богаты AT» (богаты основаниями аденина и тимина), поскольку пары оснований AT имеют две водородные связи (а не три, образованные в паре CG) и, таким образом, их легче разделить на нити. [28] У эукариот комплекс распознавания ориджина катализирует сборку белков-инициаторов в комплекс пре-репликации. Кроме того, недавний отчет предполагает, что ORC почкующихся дрожжей димеризуется в зависимости от клеточного цикла, чтобы контролировать лицензирование. [29] [30] В свою очередь, процесс димеризации ORC опосредован циклом димеризации Noc3p, зависящим от клеточного цикла in vivo, и эта роль Noc3p отделима от его роли в биогенезе рибосом. Существенный цикл димеризации Noc3p опосредует образование двойного гексамера ORC при лицензировании репликации. ORC и Noc3p непрерывно связаны с хроматином на протяжении всего клеточного цикла. [31] Затем Cdc6 и Cdt1 связываются со связанным комплексом распознавания начала в начале, чтобы сформировать более крупный комплекс, необходимый для загрузки комплекса Mcm на ДНК. У эукариот комплекс Mcm является геликазой, которая разделит спираль ДНК на репликационных вилках и началах. Комплекс Mcm рекрутируется на поздней фазе G1 и загружается комплексом ORC-Cdc6-Cdt1 на ДНК посредством АТФ-зависимого ремоделирования белка. Загрузка комплекса Mcm на исходную ДНК знаменует завершение формирования пререпликационного комплекса. [32]
Если условия окружающей среды подходят для поздней фазы G1, активируются комплексы циклин G1 и G1/S - Cdk , которые стимулируют экспрессию генов, кодирующих компоненты синтетического аппарата ДНК. Активация G1/S-Cdk также способствует экспрессии и активации комплексов S-Cdk, которые могут играть роль в активации точек начала репликации в зависимости от вида и типа клеток. Контроль этих Cdk варьируется в зависимости от типа клеток и стадии развития. Эта регуляция лучше всего изучена в почкующихся дрожжах , где S-циклины Clb5 и Clb6 в первую очередь отвечают за репликацию ДНК. [33] Комплексы Clb5,6-Cdk1 напрямую запускают активацию точек начала репликации и, следовательно, необходимы на протяжении всей фазы S для прямой активации каждой точки начала. [32]
Аналогичным образом Cdc7 также требуется через S-фазу для активации точек начала репликации. Cdc7 не активен на протяжении всего клеточного цикла, и его активация строго рассчитана по времени, чтобы избежать преждевременного начала репликации ДНК. В конце G1 активность Cdc7 резко возрастает в результате ассоциации с регуляторной субъединицей DBF4 , которая напрямую связывает Cdc7 и способствует его протеинкиназной активности. Было обнаружено, что Cdc7 является регулятором, ограничивающим скорость активности точек начала репликации. Вместе G1/S-Cdks и/или S-Cdks и Cdc7 сотрудничают для прямой активации точек начала репликации, что приводит к началу синтеза ДНК. [32]
В ранней S-фазе активация S-Cdk и Cdc7 приводит к сборке комплекса преинициации, массивного белкового комплекса, образованного в начале. Формирование комплекса преинициации вытесняет Cdc6 и Cdt1 из комплекса репликации начала, инактивируя и разбирая комплекс пре-репликации. Загрузка комплекса преинициации на начало активирует геликазу Mcm, вызывая раскручивание спирали ДНК. Комплекс преинициации также загружает α-праймазу и другие ДНК-полимеразы на ДНК. [32]
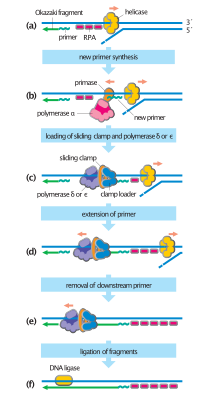
После того, как α-праймаза синтезирует первые праймеры, соединения праймер-матрица взаимодействуют с загрузчиком зажима, который загружает скользящий зажим на ДНК, чтобы начать синтез ДНК. Компоненты комплекса преинициации остаются связанными с репликационными вилками, поскольку они выходят из источника. [32]
ДНК-полимераза имеет 5′–3′ активность. Все известные системы репликации ДНК требуют свободной 3′ гидроксильной группы, прежде чем синтез может быть инициирован (примечание: шаблон ДНК считывается в направлении от 3′ к 5′, тогда как новая цепь синтезируется в направлении от 5′ к 3′ — это часто путают). Распознаются четыре различных механизма синтеза ДНК:
Клеточные организмы используют первый из этих путей, поскольку он наиболее известен. В этом механизме, как только две нити разделены, праймаза добавляет РНК-праймеры к нитям матрицы. Ведущая нить получает один РНК-праймер, а отстающая нить получает несколько. Ведущая нить непрерывно удлиняется от праймера ДНК-полимеразой с высокой процессивностью , в то время как отстающая нить удлиняется прерывисто от каждого праймера, образуя фрагменты Оказаки . РНКаза удаляет фрагменты РНК праймера, и ДНК-полимераза с низкой процессивностью, отличная от репликативной полимеразы, входит, чтобы заполнить пробелы. Когда это завершено, можно обнаружить один надрез на ведущей нити и несколько надрезов на отстающей нити. Лигаза работает, чтобы заполнить эти надрезы, таким образом завершая новую реплицированную молекулу ДНК.
Праймаза, используемая в этом процессе, значительно отличается у бактерий и архей / эукариот . Бактерии используют праймазу, принадлежащую к суперсемейству белков DnaG , которая содержит каталитический домен типа складки TOPRIM. [34] Складка TOPRIM содержит α/β-ядро с четырьмя консервативными цепями в топологии, подобной Россманну . Эта структура также обнаружена в каталитических доменах топоизомеразы Ia, топоизомеразы II, нуклеаз семейства OLD и белков репарации ДНК, связанных с белком RecR.
Праймаза, используемая археями и эукариотами, напротив, содержит высокопроизводную версию мотива распознавания РНК (RRM). Эта праймаза структурно похожа на многие вирусные РНК-зависимые РНК-полимеразы, обратные транскриптазы, циклические нуклеотид-генерирующие циклазы и ДНК-полимеразы семейств A/B/Y, которые участвуют в репликации и репарации ДНК. В эукариотической репликации праймаза образует комплекс с Pol α. [35]
Несколько ДНК-полимераз играют разные роли в процессе репликации ДНК. В E. coli ДНК Pol III является ферментом-полимеразой, в первую очередь отвечающим за репликацию ДНК. Он собирается в репликационный комплекс на репликационной вилке, которая проявляет чрезвычайно высокую процессивность, оставаясь нетронутой в течение всего цикла репликации. Напротив, ДНК Pol I является ферментом, отвечающим за замену РНК-праймеров на ДНК. ДНК Pol I обладает 5′-3′ экзонуклеазной активностью в дополнение к своей полимеразной активности и использует свою экзонуклеазную активность для деградации РНК-праймеров перед собой по мере удлинения цепи ДНК позади себя в процессе, называемом ник-трансляцией . Pol I гораздо менее процессивен, чем Pol III, потому что его основная функция в репликации ДНК заключается в создании множества коротких участков ДНК, а не нескольких очень длинных участков.
У эукариот фермент с низкой процессивностью, Pol α, помогает инициировать репликацию, поскольку он образует комплекс с праймазой. [36] Считается, что у эукариот синтез ведущей цепи осуществляется Pol ε; однако эта точка зрения недавно была подвергнута сомнению, что предполагает роль Pol δ. [37] Удаление праймера завершается Pol δ [38] , тогда как восстановление ДНК во время репликации завершается Pol ε.
По мере продолжения синтеза ДНК исходные нити ДНК продолжают раскручиваться с каждой стороны пузыря, образуя репликационную вилку с двумя зубцами. У бактерий, имеющих одну точку начала репликации на своей кольцевой хромосоме, этот процесс создает « тета-структуру » (напоминающую греческую букву тета: θ). Напротив, эукариоты имеют более длинные линейные хромосомы и инициируют репликацию в нескольких точках начала репликации внутри них. [39]
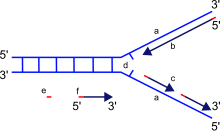

Репликационная вилка — это структура, которая формируется внутри длинной спиральной ДНК во время репликации ДНК. Она производится ферментами, называемыми геликазами, которые разрывают водородные связи, удерживающие нити ДНК вместе в спирали. Полученная структура имеет два разветвляющихся «зубца», каждый из которых состоит из одной нити ДНК. Эти две нити служат шаблоном для лидирующей и отстающей нитей, которые будут созданы, когда ДНК-полимераза сопоставляет комплементарные нуклеотиды с шаблонами; шаблоны можно правильно называть шаблоном лидирующей нити и шаблоном отстающей нити.
ДНК считывается ДНК-полимеразой в направлении от 3' к 5', то есть новая цепь синтезируется в направлении от 5' к 3'. Поскольку шаблоны лидирующей и отстающей цепи ориентированы в противоположных направлениях в репликационной вилке, основной проблемой является то, как добиться синтеза новой отстающей цепи ДНК, направление синтеза которой противоположно направлению растущей репликационной вилки.
Лидирующая цепь — это цепь новой ДНК, которая синтезируется в том же направлении, что и растущая репликационная вилка. Этот вид репликации ДНК является непрерывным.
Отстающая цепь — это цепь новой ДНК, направление синтеза которой противоположно направлению растущей репликационной вилки. Из-за своей ориентации репликация отстающей цепи сложнее, чем репликация ведущей цепи. Вследствие этого ДНК-полимераза на этой цепи «отстает» от другой цепи.
Отстающая цепь синтезируется короткими, разделенными сегментами. На шаблоне отстающей цепи праймаза «считывает» шаблон ДНК и инициирует синтез короткого комплементарного праймера РНК . ДНК-полимераза удлиняет праймерные сегменты, образуя фрагменты Оказаки . Затем праймеры РНК удаляются и заменяются ДНК, а фрагменты ДНК соединяются ДНК -лигазой .
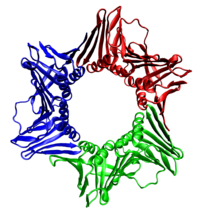
Во всех случаях геликаза состоит из шести полипептидов, которые обвивают только одну цепь реплицируемой ДНК. Две полимеразы связаны с гексамером геликазы. У эукариот геликаза обвивает ведущую цепь, а у прокариот — отстающую цепь. [40]
Когда геликаза раскручивает ДНК на репликационной вилке, ДНК впереди вынуждена вращаться. Этот процесс приводит к накоплению изгибов в ДНК впереди. [41] Это накопление создает крутильную нагрузку, которая в конечном итоге остановит репликационную вилку. Топоизомеразы — это ферменты, которые временно разрывают нити ДНК, снимая натяжение, вызванное раскручиванием двух нитей спирали ДНК; топоизомеразы (включая ДНК-гиразу ) достигают этого, добавляя отрицательные супервитки к спирали ДНК. [42]
Голая одноцепочечная ДНК имеет тенденцию складываться сама на себя, образуя вторичные структуры ; эти структуры могут мешать движению ДНК-полимеразы. Чтобы предотвратить это, одноцепочечные связывающие белки связываются с ДНК до тех пор, пока не синтезируется вторая цепь, предотвращая образование вторичной структуры. [43]
Двухцепочечная ДНК намотана вокруг гистонов , которые играют важную роль в регуляции экспрессии генов, поэтому реплицированная ДНК должна быть намотана вокруг гистонов в тех же местах, что и исходная ДНК. [44] Чтобы обеспечить это, шапероны гистонов разбирают хроматин перед его репликацией и заменяют гистоны в правильном месте. Некоторые этапы этой повторной сборки несколько спекулятивны. [45]
Зажимные белки действуют как скользящий зажим на ДНК, позволяя ДНК-полимеразе связываться с ее шаблоном и способствовать процессивности. Внутренняя поверхность зажима позволяет ДНК проходить через него. Как только полимераза достигает конца шаблона или обнаруживает двухцепочечную ДНК, скользящий зажим претерпевает конформационное изменение, которое высвобождает ДНК-полимеразу. Загрузочные белки зажима используются для первоначальной загрузки зажима, распознавая соединение между шаблоном и праймерами РНК. [9] :274-5
На репликационной вилке многие ферменты репликации собираются на ДНК в сложную молекулярную машину, называемую реплисомой . Ниже приведен список основных ферментов репликации ДНК, которые участвуют в реплисоме: [46]
Эксперименты in vitro с отдельными молекулами (с использованием оптического и магнитного пинцетов ) обнаружили синергетические взаимодействия между ферментами реплисомы ( хеликазой , полимеразой и одноцепочечным ДНК-связывающим белком ) и с репликационной вилкой ДНК , усиливающие раскручивание и репликацию ДНК. [14] Эти результаты приводят к разработке кинетических моделей, учитывающих синергетические взаимодействия и их стабильность. [14]

Аппараты репликации состоят из факторов, участвующих в репликации ДНК и появляющихся на шаблонных одноцепочечных ДНК. Аппараты репликации включают примомоторы — ферменты репликации; ДНК-полимеразу, ДНК-хеликазы, ДНК-зажимы и ДНК-топоизомеразы, а также белки репликации; например, белки, связывающие одноцепочечную ДНК (SSB). В аппаратах репликации эти компоненты координируются. У большинства бактерий все факторы, участвующие в репликации ДНК, расположены на репликационных вилках, и комплексы остаются на вилках во время репликации ДНК. Аппараты репликации также называются реплисомами или системами репликации ДНК. Эти термины являются общими для белков, расположенных на репликационных вилках. В эукариотических и некоторых бактериальных клетках реплисомы не образуются.
На альтернативном рисунке ДНК-фабрики похожи на проекторы, а ДНК похожи на кинопленки, постоянно проходящие через проекторы. В модели репликационной фабрики после того, как ДНК-хеликазы для ведущих и отстающих цепей загружены на шаблонные ДНК, геликазы бегут вдоль ДНК друг в друга. Хеликазы остаются связанными на протяжении оставшейся части процесса репликации. Питер Мейстер и др. наблюдали непосредственно сайты репликации в почкующихся дрожжах , отслеживая ДНК-полимеразы, помеченные зеленым флуоресцентным белком (GFP) α. Они обнаружили репликацию ДНК пар помеченных локусов, расположенных симметрично от начала репликации, и обнаружили, что расстояние между парами заметно уменьшается со временем. [48] Это открытие предполагает, что механизм репликации ДНК идет с ДНК-фабриками. То есть пары репликационных фабрик загружаются на начала репликации, а фабрики связаны друг с другом. Кроме того, шаблонные ДНК перемещаются в фабрики, что приводит к выдавливанию шаблонных одноцепочечных ДНК и новых ДНК. Открытие Мейстера является первым прямым доказательством модели фабрики репликации. Последующие исследования показали, что ДНК-хеликазы образуют димеры во многих эукариотических клетках, а бактериальные репликационные аппараты остаются в одном внутриядерном месте во время синтеза ДНК. [49]
Факторы репликации распутывают сестринские хроматиды. Распутывание необходимо для распределения хроматид в дочерние клетки после репликации ДНК. Поскольку сестринские хроматиды после репликации ДНК удерживают друг друга кольцами когезина , существует единственный шанс для распутывания при репликации ДНК. Закрепление механизмов репликации в качестве фабрик репликации может повысить успешность репликации ДНК. Если репликационные вилки свободно перемещаются в хромосомах, сцепление ядер ухудшается и препятствует митотической сегрегации. [48]
Эукариоты инициируют репликацию ДНК в нескольких точках хромосомы, поэтому репликационные вилки встречаются и заканчиваются во многих точках хромосомы. Поскольку у эукариот линейные хромосомы, репликация ДНК не может достичь самого конца хромосом. Из-за этой проблемы ДНК теряется в каждом цикле репликации с конца хромосомы. Теломеры — это области повторяющейся ДНК, близкие к концам, и помогают предотвратить потерю генов из-за этого укорочения. Укорочение теломер — нормальный процесс в соматических клетках . Это укорачивает теломеры дочерней ДНК-хромосомы. В результате клетки могут делиться только определенное количество раз, прежде чем потеря ДНК предотвратит дальнейшее деление. (Это известно как предел Хейфлика .) В линии зародышевых клеток , которая передает ДНК следующему поколению, теломераза удлиняет повторяющиеся последовательности области теломер, чтобы предотвратить деградацию. Теломераза может стать ошибочно активной в соматических клетках, что иногда приводит к образованию рака . Повышенная активность теломеразы является одним из признаков рака.
Терминация требует, чтобы прогресс репликационной вилки ДНК остановился или был заблокирован. Терминация в определенном локусе, когда она происходит, включает взаимодействие между двумя компонентами: (1) последовательностью сайта терминации в ДНК и (2) белком, который связывается с этой последовательностью, чтобы физически остановить репликацию ДНК. У различных видов бактерий это называется белком, связывающим сайт терминации репликации ДНК, или белком Ter .
Поскольку у бактерий кольцевые хромосомы, прекращение репликации происходит, когда две репликационные вилки встречаются друг с другом на противоположном конце родительской хромосомы. E. coli регулирует этот процесс с помощью терминирующих последовательностей, которые, будучи связанными с белком Tus , позволяют проходить только одному направлению репликационной вилки. В результате репликационные вилки ограничены тем, чтобы всегда встречаться в области терминации хромосомы. [50]

У эукариот репликация ДНК контролируется в контексте клеточного цикла . По мере того, как клетка растет и делится, она проходит стадии клеточного цикла; репликация ДНК происходит во время фазы S (фазы синтеза). Прохождение эукариотической клетки через цикл контролируется контрольными точками клеточного цикла . Прохождение контрольных точек контролируется посредством сложных взаимодействий между различными белками, включая циклины и циклинзависимые киназы . [51] В отличие от бактерий, эукариотическая ДНК реплицируется в пределах ядра. [52]
Контрольная точка G1/S (контрольная точка рестрикции) регулирует, вступают ли эукариотические клетки в процесс репликации ДНК и последующего деления. Клетки, не прошедшие эту контрольную точку, остаются на стадии G0 и не реплицируют свою ДНК.
После того, как ДНК прошла тест "G1/S", она может быть скопирована только один раз в каждом клеточном цикле. Когда комплекс Mcm удаляется от начала, пререпликационный комплекс разбирается. Поскольку новый комплекс Mcm не может быть загружен в начало, пока пререпликационные субъединицы не будут реактивированы, одно начало репликации не может быть использовано дважды в одном и том же клеточном цикле. [32]
Активация S-Cdks в ранней S-фазе способствует разрушению или ингибированию отдельных компонентов пререпликационного комплекса, предотвращая немедленную повторную сборку. S- и M-Cdks продолжают блокировать сборку пререпликационного комплекса даже после завершения S-фазы, гарантируя, что сборка не может произойти снова, пока вся активность Cdk не будет снижена в позднем митозе. [32]
У почкующихся дрожжей ингибирование сборки вызвано Cdk-зависимым фосфорилированием компонентов пререпликационного комплекса. В начале S-фазы фосфорилирование Cdc6 с помощью Cdk1 вызывает связывание Cdc6 с SCF- убиквитин-протеинлигазой , что вызывает протеолитическое разрушение Cdc6. Cdk-зависимое фосфорилирование белков Mcm способствует их экспорту из ядра вместе с Cdt1 во время S-фазы, предотвращая загрузку новых комплексов Mcm в ориджинах в течение одного клеточного цикла. Cdk-фосфорилирование репликационного комплекса ориджин также ингибирует сборку пререпликационного комплекса. Отдельного присутствия любого из этих трех механизмов достаточно для ингибирования сборки пререпликационного комплекса. Однако мутации всех трех белков в одной и той же клетке вызывают повторную инициацию во многих ориджинах репликации в течение одного клеточного цикла. [32] [53]
В клетках животных белок геминин является ключевым ингибитором сборки пререпликационного комплекса. Геминин связывает Cdt1, предотвращая его связывание с комплексом распознавания источника. В G1 уровни геминина поддерживаются на низком уровне с помощью APC, который убиквитинирует геминин, чтобы нацелить его на деградацию. Когда геминин разрушается, Cdt1 высвобождается, позволяя ему функционировать в сборке пререпликационного комплекса. В конце G1 APC инактивируется, позволяя геминину накапливаться и связываться с Cdt1. [32]
Репликация хлоропластных и митохондриальных геномов происходит независимо от клеточного цикла, посредством процесса репликации D-петли .
В клетках позвоночных сайты репликации концентрируются в позициях, называемых фокусами репликации . [48] Сайты репликации можно обнаружить с помощью иммуноокрашивания дочерних цепей и ферментов репликации, а также мониторинга факторов репликации, помеченных GFP. С помощью этих методов обнаружено, что фокусы репликации различного размера и положения появляются в S-фазе деления клетки, и их количество на ядро намного меньше количества геномных репликационных вилок.
P. Heun et al. , [48] (2001) отслеживали очаги репликации, помеченные GFP, в почкующихся дрожжевых клетках и выявили, что точки начала репликации постоянно перемещаются в фазах G1 и S, а динамика значительно снижается в фазе S. [48] Традиционно сайты репликации фиксировались в пространственной структуре хромосом ядерным матриксом или ламинами . Результаты Heun опровергли традиционные концепции, почкующиеся дрожжи не имеют ламинов, и подтверждают, что точки начала репликации самоорганизуются и образуют очаги репликации.
Формирование репликационных фокусов регулируется путем активации репликационных ориджинов, контролируемых пространственно и временно. DA Jackson et al. (1998) обнаружили, что в клетках млекопитающих соседние ориджины активируются одновременно. [48] Пространственное сопоставление репликационных сайтов приводит к кластеризации репликационных вилок. Кластеризация спасает застрявшие репликационные вилки и способствует нормальному прогрессу репликационных вилок. Прогресс репликационных вилок тормозится многими факторами: столкновением с белками или комплексами, прочно связывающимися с ДНК, дефицитом dNTP, надрезами на шаблонах ДНК и т. д. Если репликационные вилки застревают, а остальные последовательности из застрявших вилок не копируются, то дочерние нити получают надрезы надрезы нереплицированные сайты. Нереплицированные сайты на одной родительской нити удерживают вместе другую нить, но не дочерние нити. Следовательно, полученные сестринские хроматиды не могут отделиться друг от друга и не могут разделить на 2 дочерние клетки. Когда соседние начала активируются, а вилка из одного начала останавливается, вилка из другого начала получает доступ в противоположном направлении от остановившейся вилки и дублирует нереплицированные сайты. В качестве другого механизма спасения есть применение спящих начал репликации , которые не активируют избыточные начала при нормальной репликации ДНК.
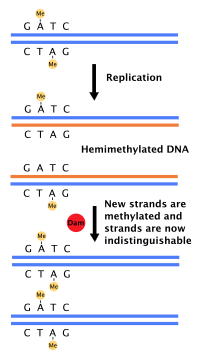
Большинство бактерий не проходят четко определенный клеточный цикл, а вместо этого непрерывно копируют свою ДНК; во время быстрого роста это может привести к одновременному возникновению нескольких раундов репликации. [54] У E. coli , наиболее охарактеризованной бактерии, репликация ДНК регулируется несколькими механизмами, включая: гемиметилирование и секвестрацию исходной последовательности, соотношение аденозинтрифосфата (АТФ) к аденозиндифосфату (АДФ) и уровни белка DnaA. Все они контролируют связывание инициирующих белков с исходными последовательностями. [55]
Поскольку E. coli метилирует последовательности ДНК GATC, синтез ДНК приводит к образованию полуметилированных последовательностей. Эта полуметилированная ДНК распознается белком SeqA , который связывает и изолирует последовательность происхождения; кроме того, DnaA (необходимый для инициации репликации) хуже связывается с полуметилированной ДНК. В результате вновь реплицированные источники не могут немедленно инициировать другой раунд репликации ДНК. [56]
АТФ накапливается, когда клетка находится в богатой среде, запуская репликацию ДНК, как только клетка достигает определенного размера. АТФ конкурирует с АДФ за связывание с DnaA, и комплекс DnaA-АТФ способен инициировать репликацию. Определенное количество белков DnaA также требуется для репликации ДНК — каждый раз, когда копируется начало, количество сайтов связывания для DnaA удваивается, требуя синтеза большего количества DnaA для обеспечения еще одной инициации репликации.
У быстрорастущих бактерий, таких как E. coli , репликация хромосом занимает больше времени, чем деление клетки. Бактерии решают эту проблему, инициируя новый раунд репликации до того, как предыдущий будет завершен. [57] Новый раунд репликации сформирует хромосому клетки, которая родится через два поколения после делящейся клетки. Этот механизм создает перекрывающиеся циклы репликации.
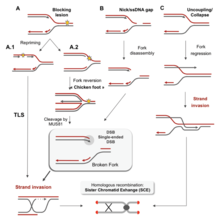
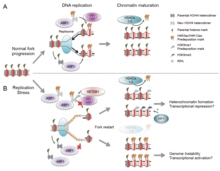
Существует множество событий, которые способствуют репликативному стрессу, в том числе: [58]
Исследователи обычно реплицируют ДНК in vitro с помощью полимеразной цепной реакции (ПЦР). ПЦР использует пару праймеров для охвата целевой области в шаблонной ДНК, а затем полимеризует партнерские цепи в каждом направлении от этих праймеров с помощью термостабильной ДНК-полимеразы . Повторение этого процесса в течение нескольких циклов амплифицирует целевую область ДНК. В начале каждого цикла смесь шаблона и праймеров нагревается, разделяя вновь синтезированную молекулу и шаблон. Затем, по мере охлаждения смеси, обе они становятся шаблонами для отжига новых праймеров, и полимераза расширяется от них. В результате количество копий целевой области удваивается с каждым раундом, увеличиваясь экспоненциально . [59]