Иридий — химический элемент ; он имеет символ Ir и атомный номер 77. Очень твердый, хрупкий, серебристо-белый переходный металл платиновой группы , он считается вторым по плотности встречающимся в природе металлом (после осмия ) с плотностью 22,56 г/см3 ( 0,815 фунта/куб. дюйм) [9] , как определено экспериментальной рентгеновской кристаллографией . [a] 191 Ir и 193 Ir — единственные два встречающихся в природе изотопа иридия, а также единственные стабильные изотопы ; последний является более распространенным. Это один из самых коррозионно -стойких металлов, [12] даже при температурах до 2000 °C (3630 °F).
Иридий был обнаружен в 1803 году в кислотонерастворимых остатках платиновых руд английским химиком Смитсоном Теннантом . Название иридий , происходящее от греческого слова iris (радуга), относится к различным цветам его соединений. Иридий является одним из самых редких элементов в земной коре , с предполагаемым годовым производством всего 6800 килограммов (15000 фунтов) в 2023 году. [13]
Доминирующими применениями иридия являются сам металл и его сплавы, как в высокопроизводительных свечах зажигания , тиглях для перекристаллизации полупроводников при высоких температурах и электродах для производства хлора в хлорщелочном процессе . Важными соединениями иридия являются хлориды и иодиды в промышленном катализе . Иридий является компонентом некоторых OLED .
Иридий содержится в метеоритах в гораздо большем количестве, чем в земной коре. [14] По этой причине необычно высокое содержание иридия в глинистом слое на границе мелового и палеогенового периодов породило гипотезу Альвареса о том, что удар массивного внеземного объекта вызвал вымирание нептичьих динозавров и многих других видов 66 миллионов лет назад , что, как теперь известно, было вызвано ударом, образовавшим кратер Чиксулуб . Аналогичным образом, аномалия иридия в образцах керна из Тихого океана предполагает удар Элтанина около 2,5 миллионов лет назад. [15]

Член платиновой группы металлов, иридий — белый, напоминающий платину, но с легким желтоватым оттенком. Из-за своей твердости, хрупкости и очень высокой температуры плавления твердый иридий трудно обрабатывать, формовать или обрабатывать; поэтому вместо него обычно используется порошковая металлургия . [16] Это единственный металл, сохраняющий хорошие механические свойства на воздухе при температурах выше 1600 °C (2910 °F). [17] Он имеет 10-ю самую высокую температуру кипения среди всех элементов и становится сверхпроводником при температурах ниже 0,14 К (−273,010 °C; −459,418 °F). [18]
Модуль упругости иридия является вторым по величине среди металлов, уступая только осмию . [17] Это, вместе с высоким модулем сдвига и очень низким значением коэффициента Пуассона (отношение продольной деформации к поперечной ), указывает на высокую степень жесткости и сопротивления деформации, которые сделали его изготовление в полезные компоненты делом большой трудности. Несмотря на эти ограничения и высокую стоимость иридия, был разработан ряд приложений, где механическая прочность является существенным фактором в некоторых из чрезвычайно тяжелых условий, встречающихся в современной технологии. [17]
Измеренная плотность иридия лишь немного ниже (примерно на 0,12%), чем у осмия, самого плотного из известных металлов . [19] [20] Возникла некоторая двусмысленность относительно того, какой из двух элементов был плотнее, из-за небольшой разницы в плотности и трудностей в ее точном измерении, [21] но, с увеличением точности коэффициентов, используемых для расчета плотности, данные рентгеновской кристаллографии дали плотности 22,56 г/см 3 (0,815 фунта/куб. дюйм) для иридия и 22,59 г/см 3 (0,816 фунта/куб. дюйм) для осмия. [22]
Иридий чрезвычайно хрупок, вплоть до того, что его трудно сваривать , поскольку в зоне термического влияния появляются трещины, но его можно сделать более пластичным, добавив небольшие количества титана и циркония (по-видимому, 0,2% каждого из них работают хорошо). [23]
Твердость по Виккерсу чистой платины составляет 56 HV, тогда как платина с 50% иридия может достигать более 500 HV. [24] [25]
Иридий — самый коррозионно-стойкий из известных металлов. [26] Он не подвержен воздействию кислот , включая царскую водку , но может растворяться в концентрированной соляной кислоте в присутствии перхлората натрия. [13] В присутствии кислорода он реагирует с солями цианида . [27] Традиционные окислители также реагируют, включая галогены и кислород [28] при более высоких температурах. [29] Иридий также напрямую реагирует с серой при атмосферном давлении, образуя дисульфид иридия . [30]
Иридий имеет два природных стабильных изотопа , 191 Ir и 193 Ir, с естественным содержанием 37,3% и 62,7% соответственно. [31] Также было синтезировано по крайней мере 37 радиоизотопов , массовые числа которых варьируются от 164 до 202. 192 Ir , который находится между двумя стабильными изотопами, является наиболее стабильным радиоизотопом с периодом полураспада 73,827 дня и находит применение в брахитерапии [32] и в промышленной радиографии , в частности, для неразрушающего контроля сварных швов в стали в нефтяной и газовой промышленности; источники иридия-192 были задействованы в ряде радиологических аварий. Три других изотопа имеют период полураспада не менее суток — 188 Ir, 189 Ir и 190 Ir. [31] Изотопы с массой ниже 191 распадаются посредством некоторой комбинации β + распада , α распада и (редко) испускания протонов , за исключением 189 Ir, который распадается посредством электронного захвата . Синтетические изотопы тяжелее 191 распадаются посредством β − распада , хотя 192 Ir также имеет второстепенный путь распада с электронным захватом. [31] Все известные изотопы иридия были открыты между 1934 и 2008 годами, причем последними открытиями являются 200–202 Ir. [33]
Было охарактеризовано не менее 32 метастабильных изомеров с массовым числом от 164 до 197. Наиболее стабильным из них является 192m2 Ir, который распадается путем изомерного перехода с периодом полураспада 241 год, [31] что делает его более стабильным, чем любой из синтетических изотопов иридия в их основных состояниях. Наименее стабильным изомером является 190m3 Ir с периодом полураспада всего 2 мкс. [31] Изотоп 191 Ir был первым из всех элементов, для которого было показано наличие эффекта Мёссбауэра . Это делает его полезным для мёссбауэровской спектроскопии в исследованиях в области физики, химии, биохимии , металлургии и минералогии . [34]
Иридий образует соединения в степенях окисления от −3 до +9, но наиболее распространенными степенями окисления являются +1, +2, +3 и +4. [16] Хорошо охарактеризованные соединения, содержащие иридий в степени окисления +6, включают IrF 6 и оксиды Sr 2 MgIrO 6 и Sr 2 CaIrO 6 . [16] [35] Оксид иридия (VIII) ( IrO 4 ) был получен в условиях матричной изоляции при 6 К в аргоне . [36] Самая высокая степень окисления (+9), которая также является самой высокой зарегистрированной для любого элемента, обнаружена в газообразном [IrO 4 ] + . [5]
Иридий не образует бинарных гидридов . Только один бинарный оксид хорошо охарактеризован: диоксид иридия , IrO
2. Это сине-черное твердое вещество, которое принимает структуру флюорита . [16] Полуторный оксид , Ir
2О
3, описывается как сине-черный порошок, который окисляется до IrO
2по HNO
3[28] Известны соответствующие дисульфиды , диселениды , сесквисульфиды и сесквиселениды, а также IrS
3. [16]
Бинарные тригалогениды, IrX
3, известны для всех галогенов. [16] Для степеней окисления +4 и выше известны только тетрафторид , пентафторид и гексафторид . [16] Гексафторид иридия, IrF
6, представляет собой летучее желтое твердое вещество, состоящее из октаэдрических молекул. Разлагается в воде и восстанавливается до IrF4. [16] Пентафторид иридия также является сильным окислителем, но это тетрамер , Ir
4Ф
20, образованный четырьмя октаэдрами, имеющими общие вершины. [16]
x.jpg/440px-IrCl3(aq)x.jpg)
Иридий имеет обширную координационную химию .
Иридий в своих комплексах всегда низкоспиновый . Ir(III) и Ir(IV) обычно образуют октаэдрические комплексы . [16] Полигидридные комплексы известны для степеней окисления +5 и +3. [37] Одним из примеров является IrH 5 (P i Pr 3 ) 2 ( i Pr = изопропил ). [38] Тройной гидрид Mg
6Ир
2ЧАС
11считается, что он содержит как IrH4−
5и 18-электронный IrH5−
4анион. [39]
Иридий также образует оксианионы со степенями окисления +4 и +5. K
2ИрО
3и КИрО
3может быть получен из реакции оксида калия или супероксида калия с иридием при высоких температурах. Такие твердые вещества не растворяются в обычных растворителях. [40]
Как и многие элементы, иридий образует важные хлоридные комплексы. Гексахлориридиевая (IV) кислота, H
2IrCl
6, и его аммонийная соль являются распространенными соединениями иридия как с промышленной, так и с препаративной точки зрения. [41] Они являются промежуточными продуктами при очистке иридия и используются в качестве прекурсоров для большинства других соединений иридия, а также при приготовлении анодных покрытий. IrCl2−
6ион имеет интенсивный темно-коричневый цвет и может быть легко восстановлен до более светлого IrCl3−
6и наоборот. [41] Трихлорид иридия , IrCl
3, который может быть получен в безводной форме прямым окислением порошка иридия хлором при 650 °C, [41] или в гидратированной форме растворением Ir
2О
3в соляной кислоте часто используется в качестве исходного материала для синтеза других соединений Ir(III). [16] Другим соединением, используемым в качестве исходного материала, является гексахлориридат(III) калия, K 3 IrCl 6 . [42]

Органические соединения иридия содержат связи иридий- углерод . Ранние исследования выявили очень стабильный тетраиридий додекакарбонил , Ir
4(Колорадо)
12. [16] В этом соединении каждый из атомов иридия связан с тремя другими, образуя тетраэдрический кластер. Открытие комплекса Васки ( IrCl(CO)[P(C
6ЧАС
5)
3]
2) открыл дверь для реакций окислительного присоединения , процесса, фундаментального для полезных реакций. Например, катализатор Крэбтри , гомогенный катализатор для реакций гидрирования . [43] [44]

Комплексы иридия сыграли ключевую роль в развитии активации связи углерод-водород (активация C–H), которая обещает обеспечить функционализацию углеводородов , которые традиционно считаются нереакционноспособными . [47]

Открытие иридия тесно связано с открытием платины и других металлов платиновой группы . Первое европейское упоминание платины появляется в 1557 году в трудах итальянского гуманиста Юлия Цезаря Скалигера как описание неизвестного благородного металла, найденного между Дарьеном и Мексикой, «который ни огонь, ни какое-либо испанское изобретение не смогли превратить в жидкость ». [48] С первых встреч с платиной испанцы обычно считали этот металл своего рода примесью в золоте и обращались с ним как с таковым. Его часто просто выбрасывали, и существовал официальный указ, запрещающий подделку золота примесями платины. [49]


В 1735 году Антонио де Ульоа и Хорхе Хуан-и-Сантасилия увидели, как коренные американцы добывают платину, пока испанцы путешествовали по Колумбии и Перу в течение восьми лет. Ульоа и Хуан нашли шахты с беловатыми металлическими самородками и привезли их домой в Испанию. Ульоа вернулся в Испанию и основал первую в Испании минералогическую лабораторию и был первым, кто систематически изучал платину, что произошло в 1748 году. Его исторический отчет об экспедиции включал описание платины как не поддающейся ни разделению , ни прокаливанию . Ульоа также предвидел открытие платиновых рудников. После публикации отчета в 1748 году Ульоа не продолжил исследование нового металла. В 1758 году его отправили руководить операциями по добыче ртути в Уанкавелике . [48]
В 1741 году Чарльз Вуд [50] , британский металлург , нашел на Ямайке различные образцы колумбийской платины, которые он отправил Уильяму Браунриггу для дальнейшего исследования.
В 1750 году, после изучения платины, присланной ему Вудом, Браунригг представил Королевскому обществу подробный отчет о металле , заявив, что он не видел никаких упоминаний о нем в каких-либо предыдущих отчетах об известных минералах. [51] Браунригг также отметил чрезвычайно высокую температуру плавления платины и ее тугоплавкое поведение по отношению к буре . Другие химики по всей Европе вскоре начали изучать платину, включая Андреаса Сигизмунда Маргграфа , [52] Торберна Бергмана , Йенса Якоба Берцелиуса , Уильяма Льюиса и Пьера Маккера . В 1752 году Хенрик Шеффер опубликовал подробное научное описание металла, который он назвал «белым золотом», включая отчет о том, как ему удалось сплавить платиновую руду с помощью мышьяка . Шеффер описал платину как менее пластичную , чем золото, но с аналогичной устойчивостью к коррозии . [48]
Химики, изучавшие платину, растворяли ее в царской водке (смесь соляной и азотной кислот ) для создания растворимых солей. Они всегда наблюдали небольшое количество темного, нерастворимого остатка. [17] Жозеф Луи Пруст считал, что остаток был графитом . [17] Французские химики Виктор Колле-Дескотиль , Антуан Франсуа, граф де Фуркрой и Луи Николя Воклен также наблюдали черный остаток в 1803 году, но не получили достаточного количества для дальнейших экспериментов. [17]
В 1803 году британский ученый Смитсон Теннант (1761–1815) проанализировал нерастворимый остаток и пришел к выводу, что он должен содержать новый металл. Воклен обработал порошок попеременно щелочью и кислотами [26] и получил летучий новый оксид, который, как он считал, принадлежал этому новому металлу, и который он назвал птеном , от греческого слова πτηνός ptēnós , « крылатый ». [53] [54] Теннант, у которого было преимущество в виде гораздо большего количества остатка, продолжил свои исследования и идентифицировал два ранее не открытых элемента в черном остатке, иридий и осмий . [17] [26] Он получил темно-красные кристаллы (вероятно, Na
2[IrCl
6]· н Н
2O ) путем последовательности реакций с гидроксидом натрия и соляной кислотой . [54] Он назвал иридий в честь Ириды ( Ἶρις ), греческой крылатой богини радуги и посланницы олимпийских богов , потому что многие из полученных им солей были сильно окрашены. [c] [55] Открытие новых элементов было задокументировано в письме в Королевское общество 21 июня 1804 года. [17] [56]
Британский ученый Джон Джордж Чилдрен был первым, кто расплавил образец иридия в 1813 году с помощью «величайшей гальванической батареи, которая когда-либо была построена» (на тот момент). [17] Первым, кто получил иридий высокой чистоты, был Роберт Хэр в 1842 году. Он обнаружил, что его плотность составляет около 21,8 г/см 3 (0,79 фунта/куб. дюйм), и отметил, что металл почти нековкий и очень твердый. Первая плавка в заметном количестве была осуществлена Анри Сент-Клером Девилем и Жюлем Анри Дебреем в 1860 году. Им потребовалось сжечь более 300 литров (79 галлонов США) чистого O
2и Н
2газа на каждый 1 килограмм (2,2 фунта) иридия. [17]
Эти экстремальные трудности в плавлении металла ограничивали возможности работы с иридием. Джон Айзек Хокинс искал способ получить тонкий и твердый кончик для перьев перьевых ручек , и в 1834 году ему удалось создать золотую ручку с иридиевым кончиком. В 1880 году Джон Холланд и Уильям Лофланд Дадли смогли расплавить иридий, добавив фосфор , и запатентовали этот процесс в Соединенных Штатах; британская компания Johnson Matthey позже заявила, что они использовали аналогичный процесс с 1837 года и уже представляли плавленый иридий на ряде всемирных выставок . [17] Первое использование сплава иридия с рутением в термопарах было сделано Отто Фойсснером в 1933 году. Они позволили измерять высокие температуры в воздухе до 2000 °C (3630 °F). [17]
В Мюнхене , Германия, в 1957 году Рудольф Мёссбауэр в ходе одного из «знаковых экспериментов в физике двадцатого века» [57] открыл резонансное и безоткатное испускание и поглощение гамма-лучей атомами в твердом металлическом образце, содержащем только 191 Ir . [58] Это явление, известное как эффект Мёссбауэра, привело к присуждению ему Нобелевской премии по физике в 1961 году в возрасте 32 лет, всего через три года после публикации своего открытия. [59]
Наряду со многими элементами, имеющими атомный вес выше, чем у железа, иридий естественным образом образуется только в результате r-процесса (быстрого захвата нейтронов ) при слиянии нейтронных звезд и, возможно, редких типах сверхновых. [60] [61] [62]
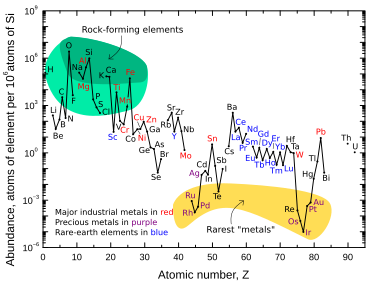

Иридий является одним из девяти наименее распространенных стабильных элементов в земной коре , имея среднюю массовую долю 0,001 ppm в земной породе; золото в 4 раза более распространено, платина в 10 раз более распространена, серебро и ртуть в 80 раз более распространены. [16] Осмий , теллур , рутений , родий и рений примерно так же распространены, как и иридий. [64] В отличие от его низкой распространенности в земной породе, иридий относительно распространен в метеоритах , с концентрациями 0,5 ppm или более. [65] Считается, что общая концентрация иридия на Земле намного выше, чем та, что наблюдается в земных породах, но из-за плотности и сидерофильного («железолюбивого») характера иридия он спустился под кору и в ядро Земли , когда планета была еще расплавлена . [41]
Иридий встречается в природе как не связанный элемент или в природных сплавах , особенно в сплавах иридия с осмием osmiridium (богатый осмием) и iridosmium (богатый иридием). [26] В месторождениях никеля и меди металлы платиновой группы встречаются в виде сульфидов , теллуридов , антимонидов и арсенидов . Во всех этих соединениях платина может обмениваться с небольшим количеством иридия или осмия. Как и все металлы платиновой группы, иридий может быть найден в природе в сплавах с сырым никелем или сырой медью . [66] Известен ряд минералов с преобладанием иридия , в которых иридий является видообразующим элементом. Они чрезвычайно редки и часто представляют собой иридиевые аналоги приведенных выше. Примерами являются ирарсит и купроиридсит, если упомянуть некоторые. [67] [68] [69] В земной коре иридий в самых высоких концентрациях встречается в трех типах геологической структуры: магматические отложения (внедрения земной коры снизу), ударные кратеры и отложения, переработанные из одной из бывших структур. Самые большие известные первичные запасы находятся в магматическом комплексе Бушвельд в Южной Африке [70] (рядом с самой большой известной ударной структурой, ударной структурой Вредефорт ), хотя крупные медно -никелевые месторождения около Норильска в России и бассейн Садбери (также ударный кратер) в Канаде также являются значительными источниками иридия. Меньшие запасы обнаружены в Соединенных Штатах. [70] Иридий также обнаружен во вторичных отложениях в сочетании с платиной и другими металлами платиновой группы в аллювиальных отложениях. Аллювиальные отложения, использовавшиеся доколумбовыми людьми в департаменте Чоко в Колумбии, по-прежнему являются источником металлов платиновой группы. По состоянию на 2003 год мировые запасы не были оценены. [26]
Иридий содержится в морских организмах, отложениях и водной толще. Содержание иридия в морской воде [71] и организмах [72] относительно невелико, поскольку он не образует хлоридные комплексы . [72] Содержание в организмах составляет около 20 частей на триллион, или примерно на пять порядков меньше, чем в осадочных породах на границе мела и палеогена (K–T) . [72] Концентрация иридия в морской воде и морских отложениях чувствительна к морской оксигенации , температуре морской воды и различным геологическим и биологическим процессам. [73]
Иридий в отложениях может поступать из космической пыли , вулканов, осадков из морской воды, микробных процессов или гидротермальных источников , [73] и его обилие может быть сильным указанием на источник. [74] [73] Он имеет тенденцию ассоциироваться с другими черными металлами в марганцевых конкрециях . [71] Иридий является одним из характерных элементов внеземных пород и, наряду с осмием, может использоваться в качестве элемента-индикатора для метеоритного материала в отложениях. [75] [76] Например, образцы керна из Тихого океана с повышенным уровнем иридия предполагают воздействие Элтанина около 2,5 миллионов лет назад. [15]
Некоторые из массовых вымираний , такие как меловое вымирание , можно идентифицировать по аномально высоким концентрациям иридия в осадочных породах, и их можно связать с крупными падениями астероидов . [77]

Граница мелового и палеогенового периодов 66 миллионов лет назад, отмечающая временную границу между меловым и палеогеновым периодами геологического времени , была идентифицирована по тонкому слою глины, богатой иридием . [78] Группа под руководством Луиса Альвареса в 1980 году предположила внеземное происхождение этого иридия, приписав его удару астероида или кометы . [78] Их теория, известная как гипотеза Альвареса , в настоящее время широко принята для объяснения вымирания нептичьих динозавров. Позднее под тем, что сейчас является полуостровом Юкатан, была обнаружена большая погребенная ударная кратерная структура с предполагаемым возрастом около 66 миллионов лет ( кратер Чиксулуб ). [79] [80] Дьюи М. Маклин и другие утверждают, что иридий мог иметь вулканическое происхождение, поскольку ядро Земли богато иридием, а активные вулканы, такие как Питон-де-ла-Фурнез на острове Реюньон , все еще выделяют иридий. [81] [82]
Мировое производство иридия составило около 7300 килограммов (16 100 фунтов) в 2018 году. [84] Цена высокая и изменчивая (см. таблицу). Иллюстративные факторы, которые влияют на цену, включают избыточное предложение Ir-тиглей [83] [85] и изменения в светодиодной технологии. [86]
Платиновые металлы встречаются вместе в виде разбавленных руд. Иридий является одним из самых редких платиновых металлов: на каждые 190 тонн платины, полученных из руд, выделяется только 7,5 тонн иридия. [87] Чтобы разделить металлы, их сначала необходимо перевести в раствор . Два метода перевода руд, содержащих Ir, в растворимое состояние: (i) сплавление твердого вещества с перекисью натрия с последующей экстракцией полученного стекла в царской водке и (ii) экстракция твердого вещества смесью хлора с соляной кислотой . [41] [70] Из растворимых экстрактов иридий выделяют путем осаждения твердого гексахлориридата аммония ( (NH
4)
2IrCl
6) или путем извлечения IrCl2−
6с органическими аминами. [88] Первый метод похож на процедуру, которую Теннант и Волластон использовали для своего первоначального разделения. Второй метод может быть спланирован как непрерывная экстракция жидкость-жидкость и поэтому больше подходит для промышленного производства. В любом случае продукт, соль хлорида иридия, восстанавливается водородом, давая металл в виде порошка или губки , который поддается методам порошковой металлургии . [89] [90] Иридий также получают в коммерческих целях как побочный продукт при добыче и переработке никеля и меди. Во время электрорафинирования меди и никеля благородные металлы, такие как серебро, золото и металлы платиновой группы , а также селен и теллур, оседают на дне ячейки в виде анодного шлама , который является отправной точкой для их извлечения. [83]
Благодаря стойкости иридия к коррозии он имеет промышленное применение. Основные области использования — электроды для производства хлора и других едких продуктов, OLED , тигли, катализаторы (например, уксусная кислота ) и наконечники зажигания для свечей зажигания. [87]
Устойчивость к воздействию тепла и коррозии является основой многочисленных областей применения иридия и его сплавов.
Благодаря своей высокой температуре плавления, твердости и коррозионной стойкости иридий используется для изготовления тиглей. Такие тигли используются в процессе Чохральского для производства оксидных монокристаллов (таких как сапфиры ) для использования в запоминающих устройствах компьютеров и в твердотельных лазерах. [92] [93] Кристаллы, такие как гадолиний-галлиевый гранат и иттрий-галлиевый гранат, выращиваются путем плавления предварительно спеченных шихт смешанных оксидов в окислительных условиях при температурах до 2100 °C (3810 °F). [17]
Некоторые долговечные детали авиационных двигателей изготавливаются из иридиевого сплава, а иридиево- титановый сплав используется для глубоководных труб из-за его коррозионной стойкости. [26] Иридий используется для многопористых фильер , через которые экструдируется расплав пластикового полимера для формирования волокон, таких как вискоза . [94] Осмий-иридий используется для компасных подшипников и для балансиров. [17]
Из-за своей устойчивости к дуговой эрозии некоторые производители используют иридиевые сплавы для изготовления центральных электродов свечей зажигания [92] [95], а свечи зажигания на основе иридия особенно широко используются в авиации.
Соединения иридия используются в качестве катализаторов в процессе Cativa для карбонилирования метанола с целью получения уксусной кислоты . [96] [97]
Комплексы иридия часто активны для асимметричного гидрирования как традиционным гидрированием . [98] так и трансферным гидрированием . [99] Это свойство является основой промышленного пути к хиральному гербициду (S)-метолахлору. Как практикуется Syngenta в масштабе 10 000 тонн/год, комплекс [Ir(COD)Cl] 2 в присутствии лигандов Josiphos . [100]
Радиоизотоп иридий-192 является одним из двух важнейших источников энергии для использования в промышленной γ-радиографии для неразрушающего контроля металлов. [101] [102] Кроме того,192
Ир
используется как источник гамма-излучения для лечения рака с помощью брахитерапии , формы радиотерапии, при которой запечатанный радиоактивный источник помещается внутрь или рядом с областью, требующей лечения. Конкретные методы лечения включают высокодозную брахитерапию простаты, брахитерапию желчных протоков и внутриполостную брахитерапию шейки матки. [26] Иридий-192 обычно производится путем нейтронной активации изотопа иридия-191 в природном металлическом иридии. [103]
Комплексы иридия являются ключевыми компонентами белых OLED . Аналогичные комплексы используются в фотокатализе . [104]

Сплав 90% платины и 10% иридия был использован в 1889 году для создания Международного прототипа метра и килограмма массы, хранящихся в Международном бюро мер и весов недалеко от Парижа. [26] Метровая планка была заменена в качестве определения фундаментальной единицы длины в 1960 году линией в атомном спектре криптона , [d] [105] но прототип килограмма оставался международным стандартом массы до 20 мая 2019 года , когда килограмм был переопределен в терминах постоянной Планка . [106]

Сплавы иридия и осмия использовались в наконечниках перьев перьевых ручек . Первое крупное применение иридия было в 1834 году в перьях, закрепленных на золоте. [17] Начиная с 1944 года, знаменитая перьевая ручка Parker 51 была оснащена пером, наконечник которого был изготовлен из сплава рутения и иридия (с 3,8% иридия). Материал наконечника в современных перьевых ручках по-прежнему традиционно называется «иридий», хотя в нем редко встречается иридий; его место заняли другие металлы, такие как рутений , осмий и вольфрам . [107]
Для затравочных отверстий или вентиляционных отверстий пушек использовался сплав иридия и платины . Согласно отчету Парижской выставки 1867 года , один из экспонатов, представленных Джонсоном и Мэтти , «использовался в орудии Уитворта более 3000 выстрелов и до сих пор не имеет признаков износа. Те, кто знает о постоянных проблемах и расходах, которые возникают из-за износа вентиляционных отверстий пушек во время активной службы, оценят это важное приспособление». [108]
Пигмент иридиевый черный , состоящий из очень тонко измельченного иридия, используется для окраски фарфора в интенсивный черный цвет; было сказано, что «все другие цвета черного фарфора кажутся серыми рядом с ним». [109]
Иридий в виде металлического насыпного вещества не является биологически важным или опасным для здоровья из-за отсутствия у него реакции с тканями; в тканях человека содержится всего около 20 частей на триллион иридия. [26] Как и большинство металлов, тонкодисперсный порошок иридия может быть опасен в обращении, так как он является раздражителем и может воспламениться на воздухе. [70] В остальном иридий относительно безопасен, единственным эффектом от приема иридия внутрь является раздражение пищеварительного тракта . [110] Однако растворимые соли, такие как галогениды иридия, могут быть опасны из-за элементов, отличных от иридия, или из-за самого иридия. [32] В то же время большинство соединений иридия нерастворимы, что затрудняет всасывание в организм. [26]
Радиоизотоп иридия,192
Ir , опасен, как и другие радиоактивные изотопы. Единственные зарегистрированные травмы, связанные с иридием, касаются случайного воздействия радиации от192
Ir используется в брахитерапии . [32] Высокоэнергетическое гамма-излучение от192
Ir может увеличить риск рака. Внешнее воздействие может вызвать ожоги, отравление радиацией и смерть. Проглатывание 192 Ir может вызвать ожог слизистой оболочки желудка и кишечника. [111] 192 Ir, 192m Ir и 194m Ir имеют тенденцию откладываться в печени и могут представлять опасность для здоровья как из-за гамма- , так и бета -излучения. [65]