
Борорганическая химия или химия органоборанов изучает борорганические соединения , также называемые органоборанами . Эти химические соединения сочетают в себе бор и углерод ; обычно они представляют собой органические производные борана (BH 3 ), как, например, триалкилбораны. [1] [2]
Органобораны и -бораты обеспечивают множество химических превращений в органической химии , в первую очередь гидроборирование и карбоборирование . В большинстве реакций нуклеофильный заместитель бора переносится к электрофильному центру либо меж-, либо внутримолекулярно . В частности, α,β -ненасыщенные бораты и бораты с уходящей α-группой весьма подвержены внутримолекулярной 1,2-миграции группы из бора в электрофильное α-положение. Окисление или протонолиз полученных органоборанов приводит к образованию многих органических продуктов, включая спирты, карбонильные соединения, алкены и галогениды. [3]
Связь CB имеет низкую полярность ( электроотрицательность 2,55 для углерода и 2,04 для бора). Алкильные соединения бора в целом стабильны, хотя и легко окисляются.
Бор часто образует электронодефицитные соединения без полного октета , такие как триорганобораны. Эти соединения являются сильными электрофилами , но обычно слишком стерически затруднены для димеризации . Донорство электронов от винильных и арильных групп может придать связи CB некоторый характер двойной связи .

Наиболее изученный класс борорганических соединений имеет формулу BR n H 3−n . Эти соединения представляют собой катализаторы, реагенты и синтетические промежуточные продукты. Триалкильные и триарильные производные имеют тригонально-планарный борный центр, который обычно является слабокислотным по Льюису . За исключением нескольких объемистых производных, гидриды (n = 1 или 2) димеризуются, как и сам диборан . Трехзамещенные производные, например триэтилбор , являются мономерами. [5]
Соединения типа БР n (OR) 3-n называются эфирами борной кислоты (n = 2), эфирами бороновой кислоты (n = 1) и боратами (n = 0). Бороновые кислоты играют ключевую роль в реакции Сузуки . Триметилборат , спорно не являющийся борорганическим соединением, является промежуточным продуктом в производстве борогидрида натрия.
Бор известен кластерными видами , например, додекаборатом [B 12 H 12 ] 2- . Такие кластеры имеют множество органических производных. Одним из примеров является [B 12 (CH 3 ) 12 ] 2- и его радикальное производное [B 12 (CH 3 ) 12 ] - . [6] Родственные кластерные соединения с углеродными вершинами – карбораны ; наиболее известным является ортокарборан C 2 B 10 H 12 . Карбораны имеют мало коммерческого применения. Анионные производные, такие как [C 2 B 9 H 11 ] 2- , называемые дикарболлидами, лигируются аналогично циклопентадиениду .
В борабензоле бор замещает один центр CH в бензоле. Борабензол и его производные неизменно появляются в виде аддуктов, например C 5 H 5 B-пиридин.
Циклическое соединение борол — структурный аналог пиррола — не выделено, но известны замещенные производные (боролы).
Циклическое соединение борепин является ароматическим.
Металлоорганические соединения со связями металл-бор (M–BR 2 ) представляют собой борильные комплексы, соответствующие условному борильному аниону R 2 B − . Родственные лиганды – борилены (M–B(R)–M).
Сильные основания не депротонируют бораны R 2 BH. Вместо этого в результате этих реакций образуется октетно-полный аддукт R 2 HB-основание. [7]
Известны соединения , изоэлектронные N-гетероциклическим карбенам. Необычное соединение получено восстановлением предшественника бромида бора: [8] [9]
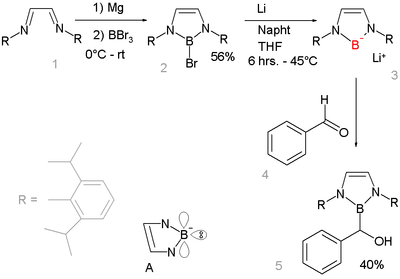
Алкилиденбораны (RB=CRR) с двойной бор-углеродной связью встречаются редко. Одним из примеров является борабензол . Исходное соединение HB=CH 2 можно обнаружить при низкой температуре. Производное CH 3 B=C(SiMe 3 ) 2 достаточно стабильно, но склонно к циклодимеризации. [10]
NHC и бораны образуют стабильные аддукты NHC-боран . [11] Аддукты триэтилборана можно синтезировать непосредственно из соли имидазолия и триэтилборгидрида лития .
Двойные связи бор-бор чрезвычайно редки. В 2007 году Грегори Робинсон из Университета Джорджии представил первый нейтральный диборен (RHB = BHR): [12] [13]

Каждый атом бора имеет присоединенный протон и координирован с карбеном NHC . Исходная структура с дополнительными карбеновыми лигандами представляет собой диборан(2) . [14] [15]
Сообщаемый диборин основан на аналогичном химическом составе.
Простые органобораны, такие как триэтилборан или трис(пентафторфенил)бор, можно получить из трифторборана (в эфире ) и этилового или пентафторфенильного реактива Гриньяра . Дальнейшее добавление карбаниона приведет к образованию бората (R 4 B - ).
Бороновые кислоты RB(OH) 2 реагируют с бифторидом калия K[HF 2 ] с образованием трифторборатных солей K[RBF 3 ], [16] - предшественников нуклеофильных алкил- и арилдифторидов бора ArBF 2 : [17]

При гидроборировании алкены встраиваются в связи борана BH с антимарковниковской стереохимией. Гидроборирование происходит стереоспецифично син — на одной и той же алкеновой грани. Переходное состояние этой согласованной реакции можно представить в виде квадрата, углы которого заняты углеродом, углеродом, водородом и бором, что максимально увеличивает перекрытие между p-орбиталями олефина и пустой орбиталью бора.
Гидроборирование борановыми (BH 3 ) эквивалентами превращает в продукт только 33% исходного олефина, остальное потребляют борсодержащие побочные продукты . Хелатный эффект улучшает это соотношение для циклических борсодержащих реагентов. Одним из распространенных циклических борорганических реагентов является 9-BBN . [18] [19]
Реакции борилирования , катализируемые металлами, производят борорганическое соединение из алифатических или ароматических сигма-связей CH через катализатор на основе переходного металла. Распространенным реагентом является бис(пинаколато)дибор .
Окись углерода реагирует с алкилборанами с образованием нестабильного карбонила борана . Затем алкильный заместитель мигрирует от бора к карбонильному углероду. Например, гомологированные первичные спирты образуются из органоборанов, оксида углерода и восстановителя (здесь боргидрида натрия ): [20]
Алкинилбораны атакуют электрофилы с образованием транс- алкенилборанов [21] , как и на первой стадии синтеза олефинов:
Ключевым свойством органоборанов (R 3 B) и боратов (R 4 B- , образующихся при присоединении R- к R 3 B) является их склонность к реорганизации . Эти соединения обладают связями бор-углерод, поляризованными в сторону углерода. Углерод, присоединенный к бору, является нуклеофильным; [22] в боратах нуклеофность достаточна для межмолекулярного перехода к электрофилу. [23] [3]
Сами по себе бораны обычно недостаточно нуклеофильны для межмолекулярного переноса группы R. Вместо этого группа 1,2 мигрирует к электрофильному углероду, присоединенному к бору, особенно если этот углерод ненасыщен или имеет хорошую уходящую группу: [23]
Склонность органической группы к миграции зависит от ее способности стабилизировать отрицательный заряд: алкинил > арил ≈ алкенил > первичный алкил > вторичный алкил > третичный алкил. [24] По этой причине бис(норборнил)боран и 9-BBN часто являются реагентами гидроборирования - только гидроборированный олефин может мигрировать при нуклеофильной активации.
Миграция сохраняет конфигурацию мигрирующего углерода [25] и инвертирует ее на (предположительно sp 3 -гибридизированном ) конце. [26] Полученный реорганизованный боран затем можно окислить или протолизовать до конечного продукта.
Органобораны неустойчивы к кислотам Бренстеда-Лоури , деборонизируясь в пользу протона. Следовательно, органобораны легко удаляются из алканового или алкенового субстрата, как и на второй стадии синтеза олефинов: [21]
Еноляты α-галогена являются обычными нуклеофилами при реорганизации борана. После нуклеофильной атаки бора образующийся кетоборонат отщепляет галоген и таутомеризуется до нейтрального енолборана. Функционализированное карбонильное соединение затем получается в результате протонолиза [27] или тушения другими электрофилами:
Поскольку миграция стереоспецифична, этим методом синтезируются энантиочистые α-алкил- или -арилкетоны. [28]
Еноляты α-галогенэфиров присоединяются аналогично боранам, но с меньшими выходами: [29]
Диазоэфиры и диазокетоны устраняют необходимость во внешнем основании. [30] α,α'-дигалоиденоляты реагируют с боранами с образованием α-галогенкарбонильных соединений, которые могут быть дополнительно функционализированы в α-положении. [31]
При аллилборировании аллилборан присоединяется к альдегиду или кетону с аллильным сдвигом и затем может быть преобразован в гомоаллильный спирт во время обработки . Реакция с кетонами протекает гораздо медленнее, чем с альдегидами. [32] Например, в синтезе эпотилонов Николау асимметричное аллилборирование (с аллилбораном, полученным из хирального альфа -пинена ) является первым шагом в двухуглеродной гомологации ацетогенина : [33]
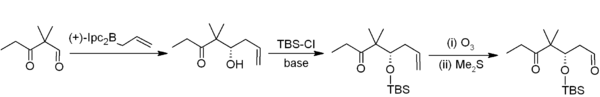
Соли трифторбората более стабильны, чем бороновые кислоты, и селективно алкилируют альдегиды : [34]

Реакционная пара гидроборирования -окисления окисляет боран до спирта перекисью водорода или до карбонильной группы оксидом хрома .
Окисление алкенилборана дает енол, не содержащий бора. [35]
Активация органоборанов гидроксидом или алкоксидом и обработка Х 2 дают галогеналканы. При избытке основания две из трех алкильных групп, присоединенных к атому бора, могут превратиться в галогенид, но дисиамилборан допускает только галогенирование гидроборированного олефина: [36]
Обработка алкенилборана йодом или бромом вызывает миграцию органической группы, связанной с бором. Алкинильные группы мигрируют избирательно, образуя енины после обработки ацетатом натрия и перекисью водорода: [37]
Борорганические соединения также легко трансметаллируются , особенно в палладийорганические соединения. В реакции Сузуки арил- или винилбороновая кислота соединяется с арил- или винилгалогенидом через комплексный катализатор палладия (0) : [ 38 ]
Гидриды борана, такие как 9-BBN и L-селектрид (три( втор-бутил )боргидрид лития), являются восстановителями . Асимметричным катализатором восстановления карбонила является катализатор CBS , который основан на координации бора с карбонильным кислородом.
Гомологированные первичные спирты получаются в результате обработки органоборанов окисью углерода и гидридом: [39]
Третичные спирты с двумя идентичными группами, присоединенными к углероду спирта, могут быть синтезированы путем двойной миграции алкинилборана: [35]
Органоборатные анионы восстанавливают ацилгалогениды. Здесь борат был получен из три(циклопентил)борана и фениллития; три циклопентильные группы существенно не мигрируют: [40]
Борорганическая химия имеет преимущественно коммерческое значение в фармацевтической промышленности.
Триэтилборан использовался для воспламенения топлива JP-7 двигателей с регулируемым циклом Pratt & Whitney J58, установленных на Lockheed SR-71 Blackbird .
Борорганические соединения уже давно обсуждаются на предмет использования в качестве агентов доставки бора в нейтронозахватной терапии рака . [41]