Хлор — химический элемент ; он имеет символ Cl и атомный номер 17. Второй по легкости из галогенов , он занимает место между фтором и бромом в периодической таблице, и его свойства в основном занимают промежуточное положение между ними. Хлор представляет собой желто-зеленый газ при комнатной температуре. Это чрезвычайно реакционноспособный элемент и сильный окислитель : среди элементов он имеет самое высокое сродство к электрону и третье место по электроотрицательности по пересмотренной шкале Полинга , уступая только кислороду и фтору.
Хлор играл важную роль в экспериментах, проводимых средневековыми алхимиками , которые обычно включали нагревание хлоридных солей , таких как хлорид аммония ( аммиачная соль ) и хлорид натрия ( обычная соль ), с получением различных химических веществ, содержащих хлор, таких как хлористый водород , ртуть (II). ) хлорид (едкая сулема) и царская водка . Однако природа газообразного свободного хлора как отдельного вещества была признана только около 1630 года Яном Баптистом ван Гельмонтом . Карл Вильгельм Шееле в 1774 году описал газообразный хлор, предполагая, что это оксид нового элемента. В 1809 году химики предположили, что газ может быть чистым элементом, и это было подтверждено сэром Хамфри Дэви в 1810 году, который назвал его в честь древнегреческого χλωρός ( khlōrós , «бледно-зеленый») из-за его цвета.
Из-за своей большой реакционной способности весь хлор в земной коре находится в форме ионных хлоридных соединений, к которым относится поваренная соль. Это второй по распространенности галоген (после фтора) и двадцать первый по распространенности химический элемент в земной коре. Тем не менее, эти отложения земной коры затмеваются огромными запасами хлоридов в морской воде.
Элементарный хлор в промышленных масштабах получают из рассола электролизом , преимущественно хлорщелочным способом . Высокий окислительный потенциал элементарного хлора привел к разработке коммерческих отбеливателей и дезинфицирующих средств , а также реагента для многих процессов в химической промышленности. Хлор используется в производстве широкого спектра потребительских товаров, около двух третей из которых составляют органические химикаты, такие как поливинилхлорид (ПВХ), многие промежуточные продукты для производства пластмасс и другие конечные продукты, не содержащие этот элемент. В качестве обычного дезинфицирующего средства элементарный хлор и хлоргенерирующие соединения используются непосредственно в плавательных бассейнах для поддержания их санитарного состояния . Элементарный хлор в высоких концентрациях чрезвычайно опасен и ядовит для большинства живых организмов. В качестве боевого отравляющего вещества хлор впервые был использован во время Первой мировой войны в качестве отравляющего газа .
В форме хлорид- ионов хлор необходим всем известным видам жизни. Другие типы соединений хлора редки в живых организмах, а искусственно созданная хлорированная органика варьируется от инертной до токсичной. В верхних слоях атмосферы хлорсодержащие органические молекулы, такие как хлорфторуглероды, участвуют в разрушении озона . Небольшие количества элементарного хлора образуются в результате окисления ионов хлора в нейтрофилах как часть реакции иммунной системы против бактерий.
Самое распространенное соединение хлора — хлорид натрия — известно с древних времен; археологи нашли доказательства того, что каменная соль использовалась еще в 3000 году до нашей эры, а рассол - еще в 6000 году до нашей эры. [7]
Около 900 г. авторы арабских сочинений, приписываемых Джабиру ибн Хайяну (лат. Гебер) и персидскому врачу и алхимику Абу Бакру ар-Рази ( ок. 865–925, латынь: Разес) экспериментировали с нашатырным спиртом ( хлоридом аммония ) . , который при перегонке вместе с купоросом (гидратированными сульфатами различных металлов) давал хлороводород . [8] Однако, похоже, что в этих ранних экспериментах с хлоридными солями газообразные продукты были отброшены, и хлористый водород мог образовываться много раз, прежде чем было обнаружено, что его можно использовать в химических целях. [9] Одним из первых таких применений был синтез хлорида ртути(II) (коррозионный сулем), производство которого путем нагрева ртути либо с квасцами и хлоридом аммония, либо с купоросом и хлоридом натрия, было впервые описано в De aluminibus et al. salibus («О квасцах и солях», арабский текст одиннадцатого или двенадцатого века, ложно приписываемый Абу Бакру ар-Рази и переведенный на латынь во второй половине двенадцатого века Герардом Кремонским , 1144–1187). [10] Еще одним важным достижением стало открытие псевдо-Гебером (в книге De Invente Veritatis , «Об открытии истины», после ок. 1300 г.), что при добавлении хлорида аммония к азотной кислоте получается сильный растворитель, способный растворять золото (10). т. е. царская водка ). [11] Хотя царская водка представляет собой нестабильную смесь, которая постоянно выделяет пары, содержащие свободный газообразный хлор, этот газообразный хлор, по-видимому, игнорировался до тех пор, пока c. 1630 год, когда его природа как отдельного газообразного вещества была признана брабантским химиком и врачом Яном Баптистом ван Гельмонтом . [12] [ru 1]

Элемент был впервые подробно изучен в 1774 году шведским химиком Карлом Вильгельмом Шееле , и ему приписывают открытие. [13] [14] Шееле получил хлор путем реакции MnO 2 (как минерал пиролюзит ) с HCl: [12]
Шееле наблюдал несколько свойств хлора: отбеливающее действие на лакмус , губительное действие на насекомых, желто-зеленый цвет и запах, похожий на царскую водку . [15] Он назвал его « воздухом дефлогистированной соляной кислоты », поскольку это газ (тогда называвшийся «воздухами») и полученный из соляной кислоты (тогда известной как «соляная кислота»). [14] Ему не удалось определить хлор как элемент. [14]
Общая химическая теория того времени утверждала, что кислота — это соединение, содержащее кислород (остатки этого содержания сохранились в немецких и голландских названиях кислорода : sauerstoff или zuurstof , оба переводятся на английский как кислотное вещество ), поэтому ряд химиков, в том числе Клод Бертолле предположил, что дефлогистированный солянокислый воздух Шееле должен представлять собой комбинацию кислорода и еще не открытого элемента muriaticum . [16] [17]
В 1809 году Жозеф Луи Гей-Люссак и Луи-Жак Тенар попытались разложить дефлогистированную соляную кислоту в воздухе , вступив в реакцию с древесным углем, чтобы высвободить свободный элемент muriaticum (и углекислый газ). [14] Им это не удалось, и они опубликовали отчет, в котором рассмотрели возможность того, что дефлогистированный воздух соляной кислоты является элементом, но это не убедило их. [18]
В 1810 году сэр Хамфри Дэви повторил тот же эксперимент и пришел к выводу, что вещество представляет собой элемент, а не соединение. [14] Он объявил свои результаты Королевскому обществу 15 ноября того же года. [12] Тогда он назвал этот новый элемент «хлором» от греческого слова χλωρος ( chlōros , «зелено-желтый»), учитывая его цвет. [19] Название « галоген », что означает «производитель соли», первоначально было использовано для хлора в 1811 году Иоганном Саломо Кристофом Швайггером . [20] Этот термин позже использовался как общий термин для описания всех элементов семейства хлора (фтор, бром, йод) после предложения Йёнса Якоба Берцелиуса в 1826 году . [21] [22] В 1823 году Майкл Фарадей впервые сжиженный хлор [23] [24] [25] и продемонстрировал, что то, что тогда было известно как «твердый хлор», имело структуру гидрата хлора (Cl 2 ·H 2 O). [12]
Газообразный хлор был впервые использован французским химиком Клодом Бертолле для отбеливания тканей в 1785 году . Париж , Франция), пропуская газообразный хлор через раствор карбоната натрия. Полученная жидкость, известная как « Eau de Javel » (« Жавельская вода »), представляла собой слабый раствор гипохлорита натрия . Этот процесс был не очень эффективным, и стали искать альтернативные методы производства. Шотландский химик и промышленник Чарльз Теннант сначала получил раствор гипохлорита кальция («хлорированная известь»), затем твердый гипохлорит кальция (хлорную известь). [26] Эти соединения производят низкие уровни элементарного хлора и могут транспортироваться более эффективно, чем гипохлорит натрия, который оставался в виде разбавленных растворов, поскольку при очистке от воды он становился опасно мощным и нестабильным окислителем. Ближе к концу девятнадцатого века Э.С. Смит запатентовал метод производства гипохлорита натрия, включающий электролиз рассола для получения гидроксида натрия и газообразного хлора, которые затем смешивались с образованием гипохлорита натрия. [28] Это известно как хлорщелочной процесс , впервые внедренный в промышленном масштабе в 1892 году и в настоящее время являющийся источником большей части элементарного хлора и гидроксида натрия. [29] В 1884 году компания Chemischen Fabrik Griesheim из Германии разработала еще один хлорщелочной процесс , который поступил в коммерческое производство в 1888 году. [30]
Растворы элементарного хлора, растворенные в химически основной воде ( гипохлоритах натрия и кальция ), впервые были использованы в качестве противогнилостных и дезинфицирующих средств в 1820-х годах во Франции, задолго до создания микробной теории болезней . Эту практику впервые применил Антуан-Жермен Лабаррак , который адаптировал отбеливатель Бертолле «Жавель» и другие препараты хлора. [31] С тех пор элементарный хлор постоянно используется в местной антисептике (растворы для орошения ран и т.п.) и в общественной санитарии, особенно в воде для купания и питья. [15]
Газообразный хлор был впервые использован в качестве оружия 22 апреля 1915 года во второй битве при Ипре немецкой армией . [32] [33] Эффект для союзников был разрушительным, поскольку существующие противогазы было трудно развернуть и они не были широко распространены. [34] [35]


Хлор — второй галоген , неметалл 17 группы таблицы Менделеева. Таким образом, его свойства аналогичны свойствам фтора , брома и йода и в значительной степени являются промежуточными между свойствами первых двух. Хлор имеет электронную конфигурацию [Ne]3s 2 3p 5 , где семь электронов в третьей и самой внешней оболочке действуют как его валентные электроны . Таким образом, как и у всех галогенов, ему не хватает одного электрона до полного октета, и, следовательно, он является сильным окислителем, реагирующим со многими элементами, чтобы завершить свою внешнюю оболочку. [36] В соответствии с периодическими тенденциями , он занимает промежуточное положение по электроотрицательности между фтором и бромом (F: 3,98, Cl: 3,16, Br: 2,96, I: 2,66) и менее реакционноспособен, чем фтор, и более реакционноспособен, чем бром. Это также более слабый окислитель, чем фтор, но более сильный, чем бром. И наоборот, хлорид- ион является более слабым восстановителем, чем бромид, но более сильным, чем фторид. [36] По атомному радиусу он занимает промежуточное положение между фтором и бромом, и это приводит к тому, что многие его атомные свойства аналогичным образом продолжают тенденцию от йода к брому вверх, такие как первая энергия ионизации , сродство к электрону , энтальпия диссоциации молекулы X 2 (X = Cl, Br, I), ионный радиус и длина связи X–X. (Фтор аномален из-за своего небольшого размера.) [36]
Все четыре стабильных галогена испытывают межмолекулярные силы Ван-дер-Ваальса притяжения, и их сила увеличивается вместе с числом электронов среди всех гомоядерных двухатомных молекул галогена. Таким образом, температуры плавления и кипения хлора являются промежуточными между температурами плавления и кипения фтора и брома: хлор плавится при -101,0 °С и кипит при -34,0 °С. В результате увеличения молекулярной массы галогенов в группе плотность и теплота плавления и испарения хлора снова становятся промежуточными между плотностью и теплотой плавления и испарения брома и фтора, хотя все их теплоты испарения довольно низкие (что приводит к высокой летучести). благодаря их двухатомной молекулярной структуре. [36] Галогены темнеют по мере убывания группы: таким образом, хотя фтор представляет собой бледно-желтый газ, хлор отчетливо желто-зеленый. Эта тенденция возникает потому, что длины волн видимого света, поглощаемого галогенами, увеличиваются по группе. [36] В частности, цвет галогена, такого как хлор, является результатом электронного перехода между самой высокой занятой разрыхляющей молекулярной орбиталью π g и самой низкой вакантной разрыхляющей молекулярной орбиталью σ u . [37] Цвет тускнеет при низких температурах, поэтому твердый хлор при температуре -195 °C практически бесцветен. [36]
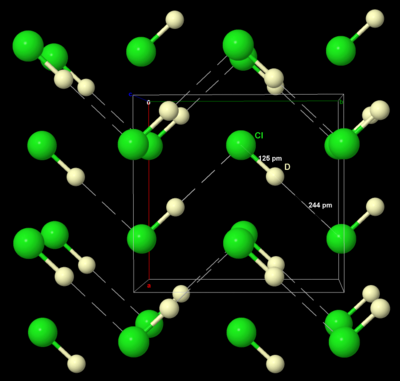
Подобно твердым брому и йоду, твердый хлор кристаллизуется в ромбической кристаллической системе , в слоистой решетке молекул Cl 2 . Расстояние Cl–Cl составляет 198 пм (близко к расстоянию Cl–Cl в газе, равному 199 пм), а расстояние Cl···Cl между молекулами составляет 332 пм внутри слоя и 382 пм между слоями (сравните радиус Ван-дер-Ваальса хлор, 180 вечера). Такая структура означает, что хлор является очень плохим проводником электричества, и его проводимость настолько низка, что ее практически невозможно измерить. [36]
Хлор имеет два стабильных изотопа: 35 Cl и 37 Cl. Это единственные два его природных изотопа, встречающиеся в большом количестве: 35 Cl составляет 76% природного хлора, а 37 Cl составляет оставшиеся 24%. Оба синтезируются в звездах в процессах сжигания кислорода и кремния . [38] Оба имеют ядерный спин 3/2+ и, таким образом, могут использоваться для ядерного магнитного резонанса , хотя величина спина, превышающая 1/2, приводит к несферическому распределению ядерного заряда и, таким образом, к расширению резонанса в результате ненулевого ядерного квадрупольный момент и результирующая квадрупольная релаксация. Все остальные изотопы хлора радиоактивны, их период полураспада слишком короток, чтобы изначально встречаться в природе . Из них наиболее часто используемые в лаборатории 36 Cl ( t 1/2 = 3,0×10 5 лет) и 38 Cl ( t 1/2 = 37,2 мин), которые могут быть получены нейтронной активацией природного хлора. [36]
Самый стабильный радиоизотоп хлора — 36 Cl. Основным способом распада изотопов легче 35 Cl является захват электронов на изотопы серы ; изотопов тяжелее 37 Cl — бета-распад до изотопов аргона ; и 36 Cl может распадаться любым способом до стабильных 36 S или 36 Ar. [39] 36 Cl встречается в природе в следовых количествах в виде космогенного нуклида в соотношении примерно (7–10) × 10 −13 к 1 со стабильными изотопами хлора: он образуется в атмосфере при расщеплении 36 Ar при взаимодействии с Протоны космических лучей . В верхних метрах литосферы 36 Cl образуется в основном за счет активации 35 Cl тепловыми нейтронами и расщепления 39 K и 40 Ca. В подземной среде захват мюонов 40 Ca становится более важным как способ генерации 36 Cl. [40] [41]
Хлор занимает промежуточное положение по реакционной способности между фтором и бромом и является одним из наиболее реакционноспособных элементов. Хлор — более слабый окислитель, чем фтор, но более сильный, чем бром или йод. Это видно из стандартных электродных потенциалов пар X 2 /X - (F - +2,866 В; Cl - +1,395 В; Br - +1,087 В; I - +0,615 В; At - примерно +0,3 В). Однако эта тенденция не проявляется в энергиях связи, поскольку фтор уникален из-за своего небольшого размера, низкой поляризуемости и неспособности проявлять гипервалентность . Еще одним отличием является то, что хлор имеет значительную химию в положительных степенях окисления, а фтор - нет. Хлорирование часто приводит к более высоким степеням окисления, чем бромирование или йодирование, но к более низким степеням окисления, чем фторирование. Хлор имеет тенденцию реагировать с соединениями, включая связи M–M, M–H или M–C, с образованием связей M–Cl. [37]
Учитывая, что Е°(1/2O 2 /H 2 O) = +1,229 В, что меньше +1,395 В, следовало бы ожидать, что хлор должен быть способен окислять воду до кислорода и соляной кислоты. Однако кинетика этой реакции неблагоприятна, и необходимо также учитывать эффект пузырькового перенапряжения , так что при электролизе водных растворов хлоридов выделяется газообразный хлор, а не газообразный кислород, что очень полезно для промышленного производства хлора. [42]
Простейшим соединением хлора является хлористый водород , HCl, основной химикат в промышленности, а также в лаборатории, как в виде газа, так и растворенный в воде в виде соляной кислоты . Его часто получают путем сжигания газообразного водорода в газообразном хлоре или как побочный продукт хлорирования углеводородов . Другой подход заключается в обработке хлорида натрия концентрированной серной кислотой для получения соляной кислоты, также известной как процесс «солевого кека»: [43]
В лаборатории газообразный хлористый водород можно получить путем высушивания кислоты концентрированной серной кислотой. Хлорид дейтерия, DCl, можно получить путем взаимодействия бензоилхлорида с тяжелой водой (D 2 O). [43]
При комнатной температуре хлористый водород представляет собой бесцветный газ, как и все галогениды водорода, кроме фтористого водорода , поскольку водород не может образовывать прочные водородные связи с более крупным электроотрицательным атомом хлора; однако слабая водородная связь присутствует в твердокристаллическом хлористом водороде при низких температурах, подобно структуре фторида водорода, прежде чем при повышении температуры начинает преобладать беспорядок. [43] Соляная кислота является сильной кислотой (p K a = -7), поскольку водородные связи с хлором слишком слабы, чтобы ингибировать диссоциацию. В системе HCl/H 2 O имеется множество гидратов HCl· n H 2 O для n = 1, 2, 3, 4 и 6. За пределами смеси HCl и H 2 O в соотношении 1:1 система полностью разделяется на две отдельные жидкие фазы. Соляная кислота образует азеотроп с температурой кипения 108,58 °С при 20,22 г HCl на 100 г раствора; таким образом, соляную кислоту нельзя сконцентрировать выше этой точки путем перегонки. [44]
В отличие от фтористого водорода, с безводным жидким хлористым водородом трудно работать как растворителем, поскольку его температура кипения низкая, он имеет небольшой интервал жидкого состояния, его диэлектрическая проницаемость мала и он не диссоциирует в заметной степени на H 2 Cl + и HCl .−
2ионы – последние, во всяком случае, гораздо менее стабильны, чем ионы бифторида ( HF−
2) из-за очень слабой водородной связи между водородом и хлором, хотя его соли с очень крупными и слабополяризующимися катионами, такими как Cs + и NR+
4(R = Me , Et , Bu n ) все еще могут быть изолированы. Безводный хлористый водород — плохой растворитель, способный растворять только низкомолекулярные соединения, такие как нитрозилхлорид и фенол , или соли с очень низкой энергией решетки , такие как галогениды тетраалкиламмония. Он легко протонирует электрофилы , содержащие неподеленные пары или π-связи. В растворе хлористого водорода хорошо изучены сольволиз , реакции замены лигандов и окисления: [45]
-chloride-hexahydrate-sample.jpg/440px-Nickel(II)-chloride-hexahydrate-sample.jpg)
Почти все элементы таблицы Менделеева образуют бинарные хлориды. Исключения составляют решительно меньшинство и обусловлены в каждом случае одной из трех причин: крайней инертностью и нежеланием участвовать в химических реакциях (благородные газы , за исключением ксенона в весьма нестабильных XeCl 2 и XeCl 4 ); крайняя ядерная нестабильность, затрудняющая химические исследования до распада и трансмутации (многие из самых тяжелых элементов, помимо висмута ); и иметь электроотрицательность выше, чем у хлора ( кислорода и фтора ), так что образующиеся бинарные соединения формально являются не хлоридами, а скорее оксидами или фторидами хлора. [46] Несмотря на то, что азот в NCl 3 несет отрицательный заряд, это соединение обычно называют трихлоридом азота .
Хлорирование металлов с помощью Cl 2 обычно приводит к более высокой степени окисления, чем бромирование с помощью Br 2 , когда доступны несколько степеней окисления, например, в MoCl 5 и MoBr 3 . Хлориды могут быть получены путем реакции элемента или его оксида, гидроксида или карбоната с соляной кислотой, а затем обезвожены при умеренно высоких температурах в сочетании с низким давлением или безводным газообразным хлористым водородом. Эти методы работают лучше всего, когда хлоридный продукт устойчив к гидролизу; в противном случае возможности включают высокотемпературное окислительное хлорирование элемента хлором или хлористым водородом, высокотемпературное хлорирование оксида металла или другого галогенида хлором, летучим хлоридом металла, четыреххлористым углеродом или органическим хлоридом. Например, диоксид циркония реагирует с хлором при стандартных условиях с образованием тетрахлорида циркония , а триоксид урана реагирует с гексахлорпропеном при нагревании с обратным холодильником с образованием тетрахлорида урана . Второй пример также включает снижение степени окисления , которого также можно достичь путем восстановления более высокого хлорида с использованием водорода или металла в качестве восстановителя. Этого также можно достичь путем термического разложения или диспропорционирования следующим образом: [46]
Большинство хлоридов металлов, в которых металл находится в низких степенях окисления (от +1 до +3), являются ионными. Неметаллы имеют тенденцию образовывать ковалентные молекулярные хлориды, как и металлы с высокими степенями окисления от +3 и выше. Для металлов со степенью окисления +3 известны как ионные, так и ковалентные хлориды (например, хлорид скандия в основном ионный, а хлорид алюминия - нет). Хлорид серебра очень нерастворим в воде и поэтому часто используется в качестве качественного теста на хлор. [46]
Хотя дихлор является сильным окислителем с высокой первой энергией ионизации, в экстремальных условиях он может окисляться с образованием катиона [Cl 2 ] + . Он очень нестабилен и характеризуется своим электронным спектром только при производстве в разрядной трубке низкого давления. Желтый катион [Cl 3 ] + более стабилен и может быть получен следующим образом: [47]
Реакцию проводят в окислительном растворителе пентафториде мышьяка . Трихлорид-анион [Cl 3 ] - также был охарактеризован; он аналогичен трииодиду . [48]
Три фторида хлора образуют подгруппу межгалогенных соединений, все из которых являются диамагнитными . [48] Известны некоторые катионные и анионные производные, такие как ClF.−
2, КФ−
4, КФ+
2и Cl 2 F + . [49] Также известны некоторые псевдогалогениды хлора, такие как хлорид циана (ClCN, линейный), цианат хлора (ClNCO), тиоцианат хлора (ClSCN, в отличие от его кислородного аналога) и азид хлора (ClN 3 ). [48]
Монофторид хлора (ClF) чрезвычайно термостабилен и коммерчески продается в стальных лекционных флаконах по 500 граммов. Это бесцветный газ, который плавится при температуре -155,6 °С и кипит при температуре -100,1 °С. Его можно получить реакцией его элементов при 225 ° C, но затем его необходимо отделить и очистить от трифторида хлора и его реагентов. Его свойства в основном занимают промежуточное положение между свойствами хлора и фтора. Он вступает в реакцию со многими металлами и неметаллами при температуре от комнатной и выше, фторируя их и выделяя хлор. Он также будет действовать как хлорфторирующий агент, добавляя хлор и фтор по кратной связи или путем окисления: например, он будет атаковать окись углерода с образованием карбонилхлорфторида, COFCl. Он будет реагировать аналогичным образом с гексафторацетоном (CF 3 ) 2 CO и катализатором из фторида калия с образованием гептафторизопропилгипохлорита (CF 3 ) 2 CFOCl; с нитрилами RCN с получением RCF 2 NCl 2 ; и с оксидами серы SO 2 и SO 3 с получением ClSO 2 F и ClOSO 2 F соответственно. Он также будет экзотермически реагировать с соединениями, содержащими группы –OH и –NH, такими как вода: [48]
Трифторид хлора (ClF 3 ) представляет собой летучую бесцветную молекулярную жидкость, которая плавится при -76,3 °С и кипит при 11,8 °С. Его можно получить путем прямого фторирования газообразного хлора или монофторида хлора при 200–300 ° C. Одно из наиболее реакционноспособных известных химических соединений, список элементов, которые оно поджигает, разнообразен, содержит водород , калий , фосфор , мышьяк , сурьму , серу , селен , теллур , бром , йод , а также порошкообразный молибден , вольфрам , родий , иридий. и железо . Он также воспламеняет воду, а также многие вещества, которые в обычных обстоятельствах считались бы химически инертными, например асбест , бетон, стекло и песок. При нагревании он разъедает даже благородные металлы, такие как палладий , платина и золото , и даже благородные газы ксенон и радон не избегают фторирования. Непроницаемый слой фторида образован натрием , магнием , алюминием , цинком , оловом и серебром , которые можно удалить нагреванием. Контейнеры из никеля , меди и стали обычно используются из-за их высокой устойчивости к воздействию трифторида хлора, обусловленной образованием нереакционноспособного слоя фторида металла. Его реакция с гидразином с образованием газов фтористого водорода, азота и хлора использовалась в экспериментальном ракетном двигателе, но имеет проблемы, в основном связанные с его чрезвычайной гиперголичностью , приводящей к воспламенению без какой-либо измеримой задержки. Сегодня он в основном используется при переработке ядерного топлива, для окисления урана до гексафторида урана с целью его обогащения и отделения его от плутония , а также в полупроводниковой промышленности, где он используется для очистки камер химического осаждения из паровой фазы . [50] Он может действовать как донор или акцептор фторид-ионов (основание Льюиса или кислота), хотя он не диссоциирует в значительной степени на ClF.+
2и КФ−
4ионы. [51]
Пентафторид хлора (ClF 5 ) получают в больших масштабах прямым фторированием хлора избытком газообразного фтора при 350 °С и 250 атм, а в небольших масштабах - путем взаимодействия хлоридов металлов с газообразным фтором при 100–300 °С. Он плавится при -103 °С и кипит при -13,1 °С. Это очень сильный фторирующий агент, хотя он все же не так эффективен, как трифторид хлора. Охарактеризовано лишь несколько конкретных стехиометрических реакций. Пентафторид мышьяка и пентафторид сурьмы образуют ионные аддукты вида [ClF 4 ] + [MF 6 ] - (M = As, Sb) и вода бурно реагирует следующим образом: [52]
Продукт, хлорилфторид , является одним из пяти известных фторидов оксида хлора. Они варьируются от термически нестабильного FClO до химически нереактивного перхлорилфторида (FClO 3 ), остальные три — FClO 2 , F 3 ClO и F 3 ClO 2 . Все пять ведут себя аналогично фторидам хлора, как структурно, так и химически, и могут действовать как кислоты или основания Льюиса, присоединяя или теряя ионы фтора соответственно, или как очень сильные окислители и фторирующие агенты. [53]


Оксиды хлора, несмотря на свою нестабильность, хорошо изучены (все они являются эндотермическими соединениями). Они важны, поскольку образуются, когда хлорфторуглероды подвергаются фотолизу в верхних слоях атмосферы и вызывают разрушение озонового слоя. Ни один из них не может быть получен путем прямого взаимодействия элементов. [54]
Монооксид дихлора (Cl 2 O) представляет собой коричнево-желтый газ (красно-коричневый в твердом или жидком состоянии), который можно получить путем реакции газообразного хлора с желтым оксидом ртути (II) . Он хорошо растворим в воде, в которой находится в равновесии с хлорноватистой кислотой (HOCl), ангидридом которой он является. Таким образом, он является эффективным отбеливателем и в основном используется для производства гипохлоритов . Он взрывается при нагревании, искрении или в присутствии газообразного аммиака. [54]
Диоксид хлора (ClO 2 ) был первым оксидом хлора, открытым в 1811 году Хамфри Дэви . Это желтый парамагнитный газ (темно-красный в твердом или жидком состоянии), как и ожидалось, поскольку он имеет нечетное количество электронов: он устойчив к димеризации из-за делокализации неспаренного электрона. Он взрывается при температуре выше -40 °C в виде жидкости и под давлением в виде газа, поэтому его необходимо производить в низких концентрациях для отбеливания древесной массы и очистки воды. Обычно его получают восстановлением хлората следующим образом: [54]
Таким образом, его производство тесно связано с окислительно-восстановительными реакциями оксокислот хлора. Это сильный окислитель, реагирующий с серой , фосфором , галогенидами фосфора и боргидридом калия . Он экзотермически растворяется в воде с образованием темно-зеленых растворов, которые очень медленно разлагаются в темноте. Кристаллические клатратные гидраты ClO 2 · n H 2 O ( n ≈ 6–10) выделяются при низких температурах. Однако в присутствии света эти растворы быстро фоторазлагаются с образованием смеси хлорной и соляной кислот. Фотолиз отдельных молекул ClO 2 приводит к образованию радикалов ClO и ClOO, тогда как при комнатной температуре образуются преимущественно хлор, кислород и некоторое количество ClO 3 и Cl 2 O 6 . Cl 2 O 3 также образуется при фотолизе твердого вещества при -78 °C: это темно-коричневое твердое вещество, которое взрывается при температуре ниже 0 °C. Радикал ClO приводит к истощению атмосферного озона и, таким образом, важен для окружающей среды следующим образом: [54]
Перхлорат хлора (ClOClO 3 ) представляет собой бледно-желтую жидкость, менее стабильную, чем ClO 2 , и разлагается при комнатной температуре с образованием хлора, кислорода и гексоксида дихлора (Cl 2 O 6 ). [54] Перхлорат хлора также можно рассматривать как производное хлора хлорной кислоты (HOClO 3 ), аналогичное термически нестабильным производным хлора других оксокислот: примеры включают нитрат хлора (ClONO 2 , энергично реактивный и взрывоопасный) и фторсульфат хлора (ClOSO). 2 F, более стабильный, но все же чувствительный к влаге и обладающий высокой реакционной способностью). [55] Гексоксид дихлора представляет собой темно-красную жидкость, которая при замерзании образует твердое вещество, которое становится желтым при -180 ° C: обычно его получают в результате реакции диоксида хлора с кислородом. Несмотря на попытки рационализировать его как димер ClO 3 , он реагирует больше, как если бы это был хлорилперхлорат, [ClO 2 ] + [ClO 4 ] - , что, как было подтверждено, является правильной структурой твердого вещества. В воде он гидролизуется с образованием смеси хлорной и хлорной кислот: аналогичная реакция с безводным фтористым водородом не протекает до конца. [54]
Гептоксид дихлора (Cl 2 O 7 ) представляет собой ангидрид хлорной кислоты (HClO 4 ) и может быть легко получен из него путем дегидратации фосфорной кислотой при -10 °C и последующей перегонки продукта при -35 °C и 1 мм рт. ст. Это чувствительная к ударам бесцветная маслянистая жидкость. Это наименее реакционноспособный из оксидов хлора и единственный, который не поджигает органические материалы при комнатной температуре. Его можно растворять в воде для регенерации хлорной кислоты или в водных щелочах для регенерации перхлоратов. Однако при термическом взрыве он разлагается, разрывая одну из центральных связей Cl–O, образуя радикалы ClO 3 и ClO 4 , которые сразу же разлагаются на элементы через промежуточные оксиды. [54]
Хлор образует четыре оксокислоты: хлорноватистой кислоты (HOCl), хлорноватой кислоты (HOClO), хлорной кислоты (HOClO 2 ) и хлорной кислоты (HOClO 3 ). Как видно из окислительно-восстановительных потенциалов, приведенных в соседней таблице, хлор гораздо более устойчив к диспропорционированию в кислых растворах, чем в щелочных: [42]
Ионы гипохлорита также диспропорционируются с образованием хлорида и хлората (3 ClO − ⇌ 2 Cl − + ClO−
3), но эта реакция протекает довольно медленно при температуре ниже 70 °C, несмотря на очень благоприятную константу равновесия 10 27 . Хлорат-ионы сами по себе могут диспропорционироваться с образованием хлорида и перхлората (4 ClO−
3⇌ Cl − + 3 ClO−
4), но это все еще очень медленно даже при 100 ° C, несмотря на очень благоприятную константу равновесия 10 20 . Скорость реакции оксианионов хлора увеличивается по мере уменьшения степени окисления хлора. Сила оксикислот хлора увеличивается очень быстро по мере увеличения степени окисления хлора из-за увеличения делокализации заряда все большего и большего количества атомов кислорода в их сопряженных основаниях. [42]
Большинство хлороксокислот можно получить, используя реакции диспропорционирования. Хлорноватистая кислота (HOCl) очень реакционноспособна и весьма нестабильна; его соли в основном используются из-за их отбеливающих и стерилизующих свойств. Они являются очень сильными окислителями, передавая атом кислорода большинству неорганических веществ. Хлористая кислота (HOClO) еще более нестойка и не может быть выделена или сконцентрирована без разложения: она известна по разложению водного диоксида хлора. Однако хлорит натрия является стабильной солью и полезен для отбеливания и очистки тканей, в качестве окислителя и источника диоксида хлора. Хлорная кислота (HOClO 2 ) — сильная кислота, достаточно устойчивая в холодной воде до 30% концентрации, но при нагревании дает хлор и диоксид хлора. Испарение при пониженном давлении позволяет сконцентрировать его примерно до 40%, но затем он разлагается на хлорную кислоту, хлор, кислород, воду и диоксид хлора. Его наиболее важной солью является хлорат натрия , который в основном используется для производства диоксида хлора для отбеливания бумажной массы. Разложение хлората на хлорид и кислород — распространенный способ получения кислорода в небольших масштабах в лаборатории. Хлорид и хлорат могут пропорционально образовывать хлор следующим образом: [56]
Перхлораты и хлорная кислота (HOClO 3 ) являются наиболее стабильными оксосоединениями хлора, что соответствует тому факту, что соединения хлора наиболее стабильны, когда атом хлора находится в самой низкой (-1) или самой высокой (+7) возможных степенях окисления. . Хлорная кислота и водные перхлораты являются энергичными, а иногда и сильными окислителями при нагревании, что резко контрастирует с их в основном неактивной природой при комнатной температуре из-за высоких энергий активации этих реакций по кинетическим причинам. Перхлораты получают путем электролитического окисления хлората натрия, а хлорную кислоту получают путем реакции безводного перхлората натрия или перхлората бария с концентрированной соляной кислотой, отфильтровывания выпавшего хлорида и перегонки фильтрата для его концентрирования. Безводная хлорная кислота представляет собой бесцветную подвижную жидкость, чувствительную к ударам, которая взрывается при контакте с большинством органических соединений, поджигает йодистый водород и тионилхлорид и даже окисляет серебро и золото. Хотя это слабый лиганд, более слабый, чем вода, некоторые соединения, включающие координированный ClO,−
4известны. [56] В таблице ниже представлены типичные степени окисления элемента хлора, данные в средних школах или колледжах. Так или иначе в вузовских курсах химии следует указывать, что существуют более сложные химические соединения, строение которых можно объяснить только с помощью современных квантово-химических методов, например, кластерный хлорид технеция [(CH 3 ) 4 N] 3 [Tc 6 Cl 14 ], в котором 6 из 14 атомов хлора формально двухвалентны, а степени окисления дробные [1]. [57] Кроме того, все приведенные выше химические закономерности справедливы для «нормальных» или близких к нормальным условий, тогда как при сверхвысоких давлениях (например, в ядрах крупных планет) хлор может проявлять степень окисления -3. , образуя с натрием соединение Na3Cl, что не укладывается в традиционные представления о химии. [58]

Как и другие связи углерод-галоген, связь C-Cl представляет собой общую функциональную группу, которая является частью основной органической химии . Формально соединения с этой функциональной группой можно считать органическими производными хлорид-аниона. Из-за разницы электроотрицательности хлора (3,16) и углерода (2,55) углерод в связи C–Cl является электронодефицитным и, следовательно, электрофильным . Хлорирование изменяет физические свойства углеводородов несколькими способами: хлоруглероды обычно плотнее воды из-за более высокого атомного веса хлора по сравнению с водородом, а алифатические хлорорганические соединения являются алкилирующими агентами, поскольку хлорид является уходящей группой . [59]
Алканы и арилалканы можно хлорировать в условиях свободных радикалов УФ-светом. Однако степень хлорирования трудно контролировать: реакция не является региоселективной и часто приводит к смеси различных изомеров с разной степенью хлорирования, хотя это может быть допустимо, если продукты легко разделяются. Арилхлориды могут быть получены галогенированием Фриделя-Крафтса с использованием хлора и катализатора кислоты Льюиса . [59] Галоформная реакция с использованием хлора и гидроксида натрия также способна генерировать алкилгалогениды из метилкетонов и родственных соединений. Хлор также присоединяется к кратным связям алкенов и алкинов , образуя ди- или тетрахлорсоединения. Однако из-за дороговизны и реакционной способности хлора хлорорганические соединения чаще получают с использованием хлористого водорода или хлорирующих агентов, таких как пентахлорид фосфора (PCl 5 ) или тионилхлорид (SOCl 2 ). Последнее очень удобно в лаборатории, поскольку все побочные продукты газообразны и их не нужно отгонять. [59]
Многие хлорорганические соединения были выделены из природных источников, от бактерий до человека. [60] [61] Хлорированные органические соединения встречаются почти во всех классах биомолекул, включая алкалоиды , терпены , аминокислоты , флавоноиды , стероиды и жирные кислоты . [60] [62] Органохлориды, в том числе диоксины , производятся в условиях высоких температур лесных пожаров, а диоксины были обнаружены в сохранившейся золе от пожаров, вызванных молниями, которые предшествовали синтетическим диоксинам. [63] Кроме того, из морских водорослей были выделены различные простые хлорированные углеводороды, включая дихлорметан, хлороформ и четыреххлористый углерод . [64] Большая часть хлорметана в окружающей среде образуется естественным путем в результате биологического разложения, лесных пожаров и вулканов. [65]
Некоторые типы хлорорганических соединений, хотя и не все, обладают значительной токсичностью для растений и животных, включая человека. Диоксины, образующиеся при сжигании органических веществ в присутствии хлора, и некоторые инсектициды, такие как ДДТ , являются стойкими органическими загрязнителями , которые представляют опасность при попадании в окружающую среду. Например, ДДТ, который широко использовался для борьбы с насекомыми в середине 20 века, также накапливается в пищевых цепях и вызывает репродуктивные проблемы (например, истончение яичной скорлупы) у некоторых видов птиц. [66] Из-за готового гомолитического деления связи C–Cl с образованием радикалов хлора в верхних слоях атмосферы, хлорфторуглероды были постепенно вытеснены из-за вреда, который они наносят озоновому слою. [54]

Хлор слишком реакционноспособен, чтобы встречаться в природе в виде свободного элемента, но его очень много в виде хлоридных солей. Это двадцать первый по распространенности элемент в земной коре, его содержание составляет 126 частей на миллион благодаря крупным месторождениям хлоридных минералов, особенно хлорида натрия , которые испарились из водоемов. Все это меркнет по сравнению с запасами ионов хлорида в морской воде: меньшие количества ионов с более высокими концентрациями встречаются в некоторых внутренних морях и подземных соляных колодцах, таких как Большое Соленое озеро в штате Юта и Мертвое море в Израиле. [67]
Небольшие партии газообразного хлора готовят в лаборатории путем соединения соляной кислоты и диоксида марганца , но необходимость возникает редко из-за его легкой доступности. В промышленности элементарный хлор обычно получают электролизом растворенного в воде хлорида натрия. Этот метод, хлорщелочной процесс , промышленно реализованный в 1892 году, в настоящее время обеспечивает большую часть промышленного газообразного хлора. [29] Наряду с хлором в результате этого метода получаются газообразный водород и гидроксид натрия , который является наиболее ценным продуктом. Процесс протекает по следующему химическому уравнению : [68]
Электролиз растворов хлоридов протекает по следующим уравнениям:
При электролизе с диафрагменной ячейкой диафрагма из асбеста (или полимерного волокна) разделяет катод и анод , предотвращая повторное смешивание хлора, образующегося на аноде, с гидроксидом натрия и водородом, образующимся на катоде. [69] Раствор соли (рассол) непрерывно подается в анодное отделение и через диафрагму поступает в катодное отделение, где образуется едкая щелочь и частично обедняется рассол. Диафрагменные методы производят разбавленную и слегка загрязненную щелочь, но они не отягощены проблемой утилизации ртути и более энергоэффективны. [29]
В мембранном электролизе в качестве ионообменника используется проницаемая мембрана . Насыщенный раствор хлорида натрия (или калия) пропускают через анодное отделение, оставляя его с более низкой концентрацией . Этот метод также дает очень чистый гидроксид натрия (или калия), но имеет тот недостаток, что требует очень чистого рассола при высоких концентрациях. [70]
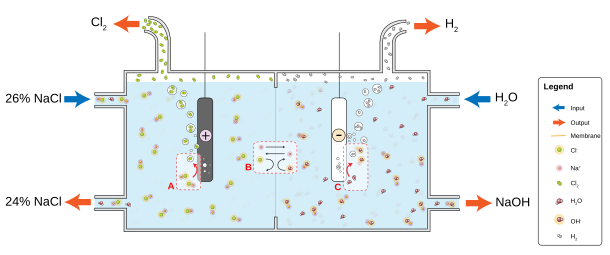
В процессе Дикона хлористый водород, получаемый при производстве хлорорганических соединений , восстанавливается в виде хлора. Процесс основан на окислении с использованием кислорода:
Реакция требует катализатора. Как сообщил Дикон, ранние катализаторы были основаны на меди. Коммерческие процессы, такие как хлорный процесс Mitsui MT, перешли на катализаторы на основе хрома и рутения. [71] Производимый хлор поставляется в баллонах емкостью от 450 г до 70 кг, а также в бочках (865 кг), вагонах-цистернах (15 тонн по дорогам, 27–90 тонн по железной дороге) и баржах (600–90 тонн по железной дороге). 1200 тонн). [72]
Хлорид натрия является наиболее распространенным соединением хлора и основным источником хлора для нужд химической промышленности. На рынке находится около 15 000 хлорсодержащих соединений, в том числе такие разнообразные соединения, как хлорированный метан , этаны , винилхлорид , поливинилхлорид (ПВХ), трихлорид алюминия для катализа , хлориды магния , титана , циркония и гафния , являющиеся предшественниками хлорсодержащих соединений. производя чистую форму этих элементов. [15]
В количественном отношении из всего производимого элементарного хлора около 63% используется в производстве органических соединений, а 18% — в производстве неорганических соединений хлора. [73] Около 15 000 соединений хлора используются в коммерческих целях. [74] Остальные 19% производимого хлора используется для производства отбеливателей и дезинфицирующих средств. [72] Наиболее значимыми из органических соединений по объему производства являются 1,2-дихлорэтан и винилхлорид , полупродукты в производстве ПВХ . Другими особенно важными хлорорганическими соединениями являются метилхлорид , метиленхлорид , хлороформ , винилиденхлорид , трихлорэтилен , перхлорэтилен , аллилхлорид , эпихлоргидрин , хлорбензол , дихлорбензолы и трихлорбензолы . Основные неорганические соединения включают HCl, Cl 2 O, HOCl, NaClO 3 , хлорированные изоцианураты, AlCl 3 , SiCl 4 , SnCl 4 , PCl 3 , PCl 5 , POCl 3 , AsCl 3 , SbCl 3 , SbCl 5 , BiCl 3 и ZnCl 2 . [72]
Во Франции (как и везде) кишки животных перерабатывали для изготовления струн музыкальных инструментов, кожи Голдбитера и других изделий. Это делалось на «кишечных фабриках» ( boyauderies ), и это был вонючий и нездоровый процесс. Примерно в 1820 году Общество поощрения национальной промышленности объявило премию за открытие химического или механического метода отделения перитонеальной оболочки кишечника животных без гниения . [75] [76] Премия досталась Антуану-Жермену Лабарраку , 44-летнему французскому химику и фармацевту, который обнаружил, что хлорированные отбеливающие растворы Бертолле (« Жавель ») не только уничтожают запах гниения животных. разложение тканей, но и фактически замедлило разложение. [76] [31]
Исследования Лабаррака привели к использованию в бояродериях хлоридов и гипохлоритов извести ( гипохлорита кальция ) и натрия ( гипохлорита натрия ) . Было обнаружено, что одни и те же химические вещества полезны при повседневной дезинфекции и дезодорации уборных , канализационных сетей , рынков, скотобоен , анатомических театров и моргов. [77] Они имели успех в госпиталях , лазаретах , тюрьмах , лазаретах (как на суше, так и на море), магнариях , конюшнях , коровниках и т. д.; и они были полезны во время эксгумации , [78] бальзамирования , вспышек эпидемических заболеваний, лихорадки и черной ножки у крупного рогатого скота. [75]
Растворы хлорированной извести и соды Лабаррака пропагандировались с 1828 года для предотвращения инфекции (так называемой «инфекционной инфекции», предположительно передаваемой « миазмами ») и для лечения гниения существующих ран, включая гнойные раны. [79] В своей работе 1828 года Лабаррак рекомендовал врачам дышать хлором, мыть руки хлорной известью и даже посыпать хлорированной известью кровати пациентов в случаях «заразной инфекции». В 1828 году распространение инфекций было хорошо известно, хотя действие микроба было обнаружено только более чем полвека спустя.
Во время вспышки холеры в Париже в 1832 году для дезинфекции столицы использовались большие количества так называемой хлорной извести . Это был не просто современный хлорид кальция , а газообразный хлор, растворенный в известковой воде (разбавленный гидроксид кальция ) с образованием гипохлорита кальция (хлорированной извести). Открытие Лабаррака помогло устранить ужасный запах разложения из больниц и анатомических кабинетов и тем самым эффективно дезодорировало Латинский квартал Парижа. [80] Многие считали, что эти «гнилостные миазмы» вызывают распространение «заразы» и «инфекции» — оба слова использовались до микробной теории инфекции. Хлорид извести использовался для уничтожения запахов и «гнилых веществ». Один источник утверждает, что хлорид извести использовался доктором Джоном Сноу для дезинфекции воды из зараженного холерой колодца, который питал насос на Брод-стрит в Лондоне в 1854 году [81], хотя три других авторитетных источника, описывающих эту знаменитую эпидемию холеры, не упоминают Инцидент. [82] [83] [84] Одна ссылка ясно показывает, что хлорид извести использовался для дезинфекции отходов и грязи на улицах вокруг насоса на Брод-стрит - обычная практика в Англии середины девятнадцатого века. [82] : 296

Пожалуй, самое известное применение растворов хлора и химической основы Лабаррака произошло в 1847 году, когда Игнац Земмельвейс использовал хлор-воду (хлор, растворенный в чистой воде, который был дешевле, чем растворы хлорной извести) для дезинфекции рук австрийских врачей, что Земмельвейс заметил еще переносил зловоние разложения из кабинетов вскрытия в кабинеты осмотра пациентов. Задолго до появления микробной теории болезней Земмельвейс предположил, что «трупные частицы» передают гниение от свежих медицинских трупов живым пациентам, и использовал хорошо известные «растворы Лабаррака» как единственный известный метод удаления запаха разложения и тканей. разложение (которое, как он обнаружил, мыла нет). Растворы оказались гораздо более эффективными антисептиками, чем мыло (Земмельвейс также знал об их большей эффективности, но не о причине), и это привело к знаменитому успеху Земмельвейса в прекращении передачи родильной лихорадки ( «послеродовой горячки») в родильных домах. палаты Венской больницы общего профиля в Австрии , 1847 год. [85]
Намного позже, во время Первой мировой войны в 1916 году, Генри Дрисдейл Дакин (который полностью отдал должное предыдущим работам Лабаррака в этой области) разработал стандартизированную и разбавленную модификацию раствора Лабаррака, содержащую гипохлорит (0,5%) и борную кислоту в качестве кислотного стабилизатора. . Названный раствором Дакина , метод орошения ран хлорированными растворами позволил провести антисептическую обработку самых разных открытых ран задолго до современной эры антибиотиков. Модифицированная версия этого раствора продолжает использоваться для орошения ран и в наше время, где она остается эффективной против бактерий, устойчивых к множеству антибиотиков (см. Century Pharmaceuticals ). [86]

Первое непрерывное применение хлорирования питьевой воды в США было установлено в Джерси-Сити , штат Нью-Джерси, в 1908 году. [87] К 1918 году Министерство финансов США призвало дезинфицировать всю питьевую воду хлором. В настоящее время хлор является важным химическим веществом для очистки воды (например, на водоочистных станциях), в дезинфицирующих средствах и отбеливателях . Даже небольшие запасы воды в настоящее время регулярно хлорируются. [88]
Хлор обычно используется (в форме хлорноватистой кислоты ) для уничтожения бактерий и других микробов в системах питьевого водоснабжения и общественных плавательных бассейнах. В большинстве частных бассейнов используется не сам хлор, а гипохлорит натрия , образующийся из хлора и гидроксида натрия , или твердые таблетки хлорированных изоциануратов. Недостаток использования хлора в бассейнах заключается в том, что хлор вступает в реакцию с аминокислотами белков в волосах и коже человека. Вопреки распространенному мнению, характерный «аромат хлора», связанный с плавательными бассейнами, является результатом не самого элементарного хлора, а хлорамина , химического соединения, образующегося в результате реакции свободного растворенного хлора с аминами в органических веществах, в том числе в моче и поте. . [89] В качестве дезинфицирующего средства в воде хлор более чем в три раза эффективнее против кишечной палочки , чем бром , и более чем в шесть раз эффективнее йода . [90] Сам монохлорамин все чаще добавляется непосредственно в питьевую воду в целях дезинфекции – процесс, известный как хлораминирование . [91]
Зачастую нецелесообразно хранить и использовать ядовитый газообразный хлор для очистки воды, поэтому используются альтернативные методы добавления хлора. К ним относятся растворы гипохлорита , которые постепенно выделяют хлор в воду, и такие соединения, как дихлор-s-триазинтрион натрия (дигидрат или безводный), иногда называемый «дихлор», и трихлор-s-триазинтрион , иногда называемый «трихлор». . Эти соединения стабильны в твердом состоянии и могут использоваться в порошкообразной, гранулированной или таблетированной форме. При добавлении в небольших количествах в воду в бассейне или в промышленные водные системы атомы хлора гидролизуются от остальной части молекулы, образуя хлорноватистую кислоту (HOCl), которая действует как общий биоцид , убивая микробы, микроорганизмы, водоросли и так далее. [92] [93]
Газообразный хлор, также известный как бертолит, впервые был использован Германией в качестве оружия в Первой мировой войне 22 апреля 1915 года во Второй битве при Ипре . [94] [95] По словам солдат, он имел характерный запах смеси перца и ананаса. [ нужна цитация ] Он также имел металлический привкус и жалил заднюю часть горла и грудь. Хлор вступает в реакцию с водой в слизистой оболочке легких с образованием соляной кислоты , разрушительной для живых тканей и потенциально смертельной. Дыхательные системы человека можно защитить от газообразного хлора противогазами с активированным углем или другими фильтрами, что делает газообразный хлор гораздо менее смертоносным, чем другое химическое оружие. Его впервые применил немецкий ученый, позже ставший нобелевским лауреатом, Фриц Хабер из Института кайзера Вильгельма в Берлине в сотрудничестве с немецким химическим конгломератом IG Farben , который разработал методы использования газообразного хлора против укоренившегося врага. [96] После первого применения обе стороны конфликта использовали хлор в качестве химического оружия, но вскоре он был заменен более смертоносными фосгеном и горчичным газом . [97]
Газообразный хлор также использовался во время войны в Ираке в провинции Анбар в 2007 году, когда повстанцы загружали бомбы в грузовиках минометными снарядами и резервуарами с хлором. В результате взрывов погибли два человека и более 350 человек заболели. Большинство смертей было вызвано силой взрывов, а не воздействием хлора, поскольку токсичный газ легко рассеивается и разбавляется в атмосфере взрывом. В результате некоторых взрывов более сотни мирных жителей были госпитализированы из-за проблем с дыханием. Иракские власти усилили меры безопасности в отношении элементарного хлора, который необходим для обеспечения населения безопасной питьевой водой. [98] [99]
23 октября 2014 года сообщалось, что Исламское Государство Ирака и Леванта применило газообразный хлор в городе Дулуйя, Ирак . [100] Лабораторный анализ образцов одежды и почвы подтвердил применение газообразного хлора против курдских сил Пешмерга при нападении с использованием самодельного взрывного устройства на автомобиле 23 января 2015 года на перекрестке шоссе 47 Киске недалеко от Мосула. [101]
Другая страна на Ближнем Востоке, Сирия , использовала хлор в качестве химического оружия [102] , доставляемого из бочковых бомб и ракет. [103] [104] В 2016 году Совместный механизм расследований ОЗХО-ООН пришел к выводу, что сирийское правительство использовало хлор в качестве химического оружия в трех отдельных атаках. [105] Позднее расследование Группы по расследованию и идентификации ОЗХО пришло к выводу, что сирийские ВВС несут ответственность за атаки с использованием хлора в 2017 и 2018 годах. [106]
Хлорид - анион является важным питательным веществом для обмена веществ. Хлор необходим для производства соляной кислоты в желудке и для функций клеточного насоса. [107] Основным пищевым источником является поваренная соль или хлорид натрия. Чрезмерно низкая или высокая концентрация хлоридов в крови является примером электролитных нарушений . Гипохлоремия (слишком мало хлоридов) редко возникает при отсутствии других отклонений. Иногда это связано с гиповентиляцией . [108] Это может быть связано с хроническим респираторным ацидозом . [109] Гиперхлоремия (избыток хлоридов) обычно не вызывает симптомов. Когда симптомы действительно возникают, они имеют тенденцию напоминать симптомы гипернатриемии (избытка натрия ). Снижение содержания хлоридов в крови приводит к обезвоживанию мозга; Симптомы чаще всего вызваны быстрой регидратацией, которая приводит к отеку мозга . Гиперхлоремия может повлиять на транспорт кислорода. [110]
Хлор — токсичный газ, поражающий дыхательную систему, глаза и кожу. [113] Поскольку он плотнее воздуха, он имеет тенденцию скапливаться внизу плохо вентилируемых помещений. Газообразный хлор является сильным окислителем, который может вступать в реакцию с легковоспламеняющимися материалами. [114] [115]
Хлор обнаруживается с помощью измерительных приборов в концентрациях всего 0,2 частей на миллион (ppm) и по запаху при 3 ppm. Кашель и рвота могут возникнуть при концентрации 30 частей на миллион, а повреждение легких – при концентрации 60 частей на миллион. Около 1000 частей на миллион могут быть смертельными после нескольких глубоких вдохов газа. [15] Концентрация IDLH (непосредственно опасного для жизни и здоровья) составляет 10 ppm. [116] Вдыхание более низких концентраций может ухудшить работу дыхательной системы, а воздействие газа может вызвать раздражение глаз. [117] При вдыхании хлора в концентрациях, превышающих 30 частей на миллион, он вступает в реакцию с водой в легких, образуя соляную кислоту (HCl) и хлорноватистую кислоту (HOCl).
При использовании в определенных количествах для дезинфекции воды реакция хлора с водой не представляет серьезной проблемы для здоровья человека. Другие материалы, присутствующие в воде, могут образовывать побочные продукты дезинфекции , которые оказывают негативное воздействие на здоровье человека. [118] [119]
В США Управление по охране труда (OSHA) установило допустимый предел воздействия элементарного хлора на уровне 1 ppm, или 3 мг/м 3 . Национальный институт безопасности и гигиены труда установил рекомендуемый предел воздействия 0,5 ppm в течение 15 минут. [116]
В быту несчастные случаи происходят, когда растворы гипохлоритного отбеливателя вступают в контакт с некоторыми кислотными очистителями канализации с образованием газообразного хлора. [120] Гипохлоритный отбеливатель (популярная добавка для стирки ) в сочетании с аммиаком (еще одна популярная добавка для стирки) приводит к образованию хлораминов , еще одной токсичной группы химикатов. [121]
Хлор широко используется для очистки воды, особенно питьевой воды и воды, используемой в плавательных бассейнах. Несколько катастрофических обрушений потолков бассейнов произошли в результате коррозионного растрескивания под напряжением подвесных стержней из нержавеющей стали , вызванного хлором. [122] Некоторые полимеры также чувствительны к воздействию, в том числе ацетальная смола и полибутен . Оба материала использовались в бытовой сантехнике с горячей и холодной водой, а коррозионное растрескивание под напряжением вызвало массовые неисправности в США в 1980-х и 1990-х годах. [123]

Элемент железо может соединяться с хлором при высоких температурах в результате сильной экзотермической реакции, создавая пожар хлор-железо . [124] [125] Пожары, вызванные хлором и железом, представляют собой опасность на химических заводах, где большая часть трубопроводов, по которым поступает газообразный хлор, изготовлена из стали. [124] [125]
{{cite web}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка ){{cite web}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка )