Хлорофилл — один из нескольких родственных зеленых пигментов, обнаруженных в цианобактериях и хлоропластах водорослей и растений . [ 2] Его название происходит от греческих слов χλωρός ( khloros , «бледно-зеленый») и φύλλον ( phyllon , «лист»). [3] Хлорофилл позволяет растениям поглощать энергию света.
Хлорофиллы сильнее всего поглощают свет в синей части электромагнитного спектра , а также в красной части. [4] И наоборот, они плохо поглощают зеленую и близкую к зеленой части спектра. Поэтому ткани, содержащие хлорофилл, кажутся зелеными, поскольку зеленый свет, диффузно отраженный такими структурами, как клеточные стенки, поглощается меньше. [1] В фотосистемах зеленых растений существуют два типа хлорофилла: хлорофилл a и b . [5]
Хлорофилл был впервые выделен и назван Жозефом Бьенеме Каванту и Пьером Жозефом Пеллетье в 1817 году. [6] Присутствие магния в хлорофилле было обнаружено в 1906 году, [7] и это было первое обнаружение этого элемента в живой ткани. [8]
После первоначальной работы, проделанной немецким химиком Рихардом Вильштеттером с 1905 по 1915 год, общая структура хлорофилла a была выяснена Гансом Фишером в 1940 году. К 1960 году, когда большая часть стереохимии хлорофилла a была известна, Роберт Бернс Вудворд опубликовал полный синтез молекулы. [8] [9] В 1967 году последнее оставшееся стереохимическое выяснение было завершено Яном Флемингом , [10] а в 1990 году Вудворд и соавторы опубликовали обновленный синтез. [11] В 2010 году было объявлено, что хлорофилл f присутствует в цианобактериях и других кислородных микроорганизмах, которые образуют строматолиты ; [12] [13] Молекулярная формула C 55 H 70 O 6 N 4 Mg и структура (2- формил )-хлорофилла а были выведены на основе ЯМР, оптических и масс-спектров. [14]

Хлорофилл жизненно важен для фотосинтеза , который позволяет растениям поглощать энергию света . [15]
Молекулы хлорофилла расположены внутри и вокруг фотосистем , которые встроены в тилакоидные мембраны хлоропластов . [16] В этих комплексах хлорофилл выполняет три функции:
Две в настоящее время принятые единицы фотосистемы — это фотосистема I и фотосистема II , которые имеют свои собственные отдельные реакционные центры, называемые P700 и P680 соответственно. Эти центры названы в честь длины волны (в нанометрах ) их максимума поглощения красного пика. Идентичность, функция и спектральные свойства типов хлорофилла в каждой фотосистеме различны и определяются друг другом и структурой белка, окружающего их.
Функция реакционного центра хлорофилла заключается в поглощении энергии света и передаче ее в другие части фотосистемы. Поглощенная энергия фотона передается электрону в процессе, называемом разделением зарядов. Удаление электрона из хлорофилла представляет собой реакцию окисления. Хлорофилл отдает электрон с высокой энергией ряду молекулярных промежуточных продуктов, называемых цепью переноса электронов . Заряженный реакционный центр хлорофилла (P680 + ) затем восстанавливается обратно в свое основное состояние, принимая электрон, отнятый у воды. Электрон, который восстанавливает P680 + , в конечном итоге поступает из окисления воды в O 2 и H + через несколько промежуточных продуктов. Эта реакция является тем, как фотосинтетические организмы, такие как растения, производят газ O 2 , и является источником практически всего O 2 в атмосфере Земли. Фотосистема I обычно работает последовательно с фотосистемой II; таким образом, P700 + Фотосистемы I обычно восстанавливается, поскольку она принимает электрон через множество промежуточных продуктов в тилакоидной мембране, электронами, поступающими, в конечном счете, из Фотосистемы II. Однако реакции переноса электронов в тилакоидных мембранах сложны, и источник электронов, используемых для восстановления P700 +, может варьироваться.
Поток электронов, создаваемый пигментами хлорофилла реакционного центра, используется для перекачивания ионов H + через тилакоидную мембрану, создавая протондвижущую силу — хемиосмотический потенциал, используемый в основном для производства АТФ (запасенной химической энергии) или для восстановления НАДФ + до НАДФН . НАДФН — универсальный агент, используемый для восстановления CO2 до сахаров, а также для других биосинтетических реакций.
Комплексы хлорофилл-белок реакционного центра способны напрямую поглощать свет и выполнять события разделения заряда без помощи других пигментов хлорофилла, но вероятность того, что это произойдет при заданной интенсивности света, мала. Таким образом, другие хлорофиллы в фотосистеме и пигментные белки антенны все кооперативно поглощают и направляют энергию света в реакционный центр. Помимо хлорофилла a , существуют и другие пигменты, называемые вспомогательными пигментами , которые встречаются в этих комплексах пигмент-белок антенны.
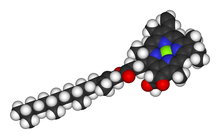
Известно несколько хлорофиллов. Все они определяются как производные родительского хлорина по наличию пятого, содержащего кетон кольца за пределами четырех пирролподобных колец. Большинство хлорофиллов классифицируются как хлорины , которые являются восстановленными родственниками порфиринов (встречаются в гемоглобине ). Они разделяют общий биосинтетический путь с порфиринами, включая предшественника уропорфириногена III . В отличие от гемов, которые содержат железо, связанное с центром N4, большинство хлорофиллов связывают магний . Аксиальные лиганды, присоединенные к центру Mg2 + , часто опускаются для ясности. К кольцу хлорина присоединены различные боковые цепи, обычно включающие длинную фитильную цепь (C20H39O ) . Наиболее широко распространенной формой в наземных растениях является хлорофилл a . Единственное различие между хлорофиллом a и хлорофиллом b заключается в том, что у первого есть метильная группа , а у второго — формильная группа . Это различие приводит к существенной разнице в спектре поглощения, что позволяет растениям поглощать большую часть видимого света.
Структуры хлорофиллов суммированы ниже: [17] [18]
Хлорофилл е зарезервирован для пигмента, который был извлечен из водорослей в 1966 году, но не описан химически. Помимо буквенных хлорофиллов, в дикой природе известно большое разнообразие модификаций боковой цепи в структурах хлорофилла. Например, Prochlorococcus , цианобактерия, использует 8-винил Chl a и b . [19]

Хлорофиллы можно извлечь из белка в органические растворители. [20] [21] [22] Таким образом можно оценить концентрацию хлорофилла в листе. [23] Существуют также методы разделения хлорофилла a и хлорофилла b .
В диэтиловом эфире хлорофилл a имеет приблизительные максимумы поглощения 430 нм и 662 нм, в то время как хлорофилл b имеет приблизительные максимумы 453 нм и 642 нм. [24] Пики поглощения хлорофилла a находятся при 465 нм и 665 нм. Хлорофилл a флуоресцирует при 673 нм (максимум) и 726 нм. Пиковый молярный коэффициент поглощения хлорофилла a превышает 10 5 М -1 см -1 , что является одним из самых высоких значений для низкомолекулярных органических соединений. [25] В 90% ацетоне-воде пиковые длины волн поглощения хлорофилла a составляют 430 нм и 664 нм; пики для хлорофилла b составляют 460 нм и 647 нм; пики для хлорофилла c 1 составляют 442 нм и 630 нм; Пики для хлорофилла c 2 составляют 444 нм и 630 нм; пики для хлорофилла d составляют 401 нм, 455 нм и 696 нм. [26]
Коэффициент флуоресцентного излучения может быть использован для измерения содержания хлорофилла. Возбуждая флуоресценцию хлорофилла а на более низкой длине волны, коэффициент флуоресцентного излучения хлорофилла на705 ± 10 нм и735 ± 10 нм может обеспечить линейную зависимость содержания хлорофилла при сравнении с химическим тестированием. Отношение F 735 / F 700 обеспечило значение корреляции r 2 0,96 по сравнению с химическим тестированием в диапазоне от 41 мг м −2 до 675 мг м −2 . Гительсон также разработал формулу для прямого считывания содержания хлорофилла в мг м −2 . Формула обеспечила надежный метод измерения содержания хлорофилла от 41 мг м −2 до 675 мг м −2 со значением корреляции r 2 0,95. [27]
Dualex — оптический датчик , используемый в растениеводстве и сельском хозяйстве для оценки содержания хлорофилла в листьях. Это устройство позволяет исследователям проводить измерения в режиме реального времени и без разрушения. [28]
В некоторых растениях хлорофилл образуется из глутамата и синтезируется по разветвленному биосинтетическому пути , который является общим с гемом и сирогемом . [29] [30] [31] Хлорофиллсинтаза [32] — это фермент, который завершает биосинтез хлорофилла a : [33] [34]
Это преобразование образует сложный эфир карбоксильной группы в хлорофиллиде a с 20-углеродным дитерпеновым спиртом фитолом . Хлорофилл b производится тем же ферментом, который действует на хлорофиллид b . То же самое известно для хлорофилла d и f , оба производятся из соответствующих хлорофиллидов, в конечном итоге производимых из хлорофиллида a . [35]
У покрытосеменных растений последние этапы биосинтетического пути зависят от света. Такие растения бледнеют ( этиолируются ), если растут в темноте. Несосудистые растения и зеленые водоросли имеют дополнительный светонезависимый фермент и зеленеют даже в темноте. [36]
Хлорофилл связан с белками . Протохлорофиллид , один из промежуточных продуктов биосинтеза, встречается в основном в свободной форме и при освещении действует как фотосенсибилизатор , образуя свободные радикалы , которые могут быть токсичными для растения. Следовательно, растения регулируют количество этого предшественника хлорофилла. У покрытосеменных растений эта регуляция достигается на этапе аминолевулиновой кислоты (АЛК), одного из промежуточных соединений в пути биосинтеза. Растения, питающиеся АЛК, накапливают высокие и токсичные уровни протохлорофиллида; то же самое делают мутанты с поврежденной регуляторной системой. [37]
Процесс старения растений включает деградацию хлорофилла: например, фермент хлорофиллаза ( EC 3.1.1.14) гидролизует фитильную боковую цепь, чтобы обратить реакцию, в которой хлорофиллы биосинтезируются из хлорофиллида a или b . Поскольку хлорофиллид a может быть преобразован в хлорофиллид b , а последний может быть повторно этерифицирован в хлорофилл b , эти процессы позволяют осуществлять цикл между хлорофиллами a и b . Более того, хлорофилл b может быть напрямую восстановлен (через 7 1 -гидроксихлорофилл a ) обратно в хлорофилл a , завершая цикл. [38] [39] На более поздних стадиях старения хлорофиллиды преобразуются в группу бесцветных тетрапирролов, известных как нефлуоресцентные катаболиты хлорофилла (NCC) с общей структурой:
Эти соединения также были обнаружены в созревающих плодах, и они придают характерную осеннюю окраску лиственным растениям. [39] [40]
Карты хлорофилла показывают миллиграммы хлорофилла на кубический метр морской воды каждый месяц. Места, где количество хлорофилла было очень низким, что указывает на очень низкое количество фитопланктона , показаны синим цветом. Места, где концентрация хлорофилла была высокой, что означает, что росло много фитопланктона, показаны желтым цветом. Наблюдения получены с помощью спектрорадиометра умеренного разрешения (MODIS) на спутнике NASA Aqua. Суша темно-серая, а места, где MODIS не мог собрать данные из-за морского льда, полярной темноты или облаков, светло-серые. Самые высокие концентрации хлорофилла, где процветают крошечные обитающие на поверхности океанические растения , находятся в холодных полярных водах или в местах, где океанские течения приносят холодную воду на поверхность, например, вокруг экватора и вдоль берегов континентов. Сама по себе холодная вода не стимулирует фитопланктон. Вместо этого, низкие температуры часто являются признаком того, что вода поднялась на поверхность из глубины океана, неся питательные вещества, которые накопились со временем. В полярных водах питательные вещества накапливаются в поверхностных водах в темные зимние месяцы, когда растения не могут расти. Когда солнечный свет возвращается весной и летом, растения расцветают в высоких концентрациях. [41]
Синтетический хлорофилл зарегистрирован как пищевая добавка-краситель, и его номер E — E140 . Повара используют хлорофилл для окрашивания в зеленый цвет различных продуктов и напитков, таких как паста и спиртные напитки. Абсент приобретает свой зеленый цвет естественным образом из-за хлорофилла, введенного через большое количество трав, используемых при его производстве. [42] Хлорофилл не растворяется в воде, и его сначала смешивают с небольшим количеством растительного масла , чтобы получить желаемый раствор . [ требуется цитата ]
Исследование 2002 года показало, что «листья, подвергшиеся воздействию яркого света, содержали деградировавшие основные антенные белки , в отличие от тех, которые содержались в темноте, что согласуется с исследованиями по освещению изолированных белков ». Это показалось авторам подтверждением гипотезы о том, что « активные формы кислорода играют роль in vivo » в краткосрочном поведении растений. [43]
Из стр. 49:
«Hauptproduct der щелочного гидролиза может быть окрашен в алкализирующий состав. В его комплексе с магнием есть металл, который содержится в щелочи, а также в более широких температурных условиях».
(Основным продуктом щелочного гидролиза являются темно-зеленые щелочные соли. В них присутствуют сложные соединения магния, содержащие металл в связи, которая необычайно устойчива к щелочам даже при высокой температуре.)