Иммунотерапия рака ( иммуноонкотерапия ) — это стимуляция иммунной системы для лечения рака , улучшающая естественную способность иммунной системы бороться с болезнью. [1] Это применение фундаментальных исследований в области иммунологии рака ( иммуноонкологии ) и растущей специальности онкологии .
Иммунотерапия рака использует тот факт, что раковые клетки часто имеют на своей поверхности опухолевые антигены — молекулы, которые могут связываться с белками антител или рецепторами Т-клеток , вызывая реакцию иммунной системы. Опухолевые антигены часто представляют собой белки или другие макромолекулы (например, углеводы ). Обычные антитела связываются с внешними патогенами, а модифицированные иммунотерапевтические антитела связываются с опухолевыми антигенами, маркируя и идентифицируя раковые клетки, которые иммунная система может ингибировать или уничтожать. Клинический успех иммунотерапии рака сильно варьируется в зависимости от различных форм рака; например, некоторые подтипы рака желудка хорошо реагируют на этот подход, тогда как иммунотерапия не эффективна для других подтипов. [2]
В 2018 году американский иммунолог Джеймс П. Эллисон и японский иммунолог Тасуку Хондзё получили Нобелевскую премию по физиологии и медицине за открытие терапии рака путем ингибирования негативной иммунной регуляции. [3]
"В 17-18 веках получили широкое распространение различные формы иммунотерапии рака... В 18-19 веках для лечения рака применялись септические повязки, охватывающие язвенные опухоли. Хирургические раны оставляли открытыми, чтобы облегчить развитие инфекции. , а гнойные язвы создавались намеренно... Об одном из наиболее известных эффектов микроорганизмов на... рак было сообщено в 1891 году, когда американский хирург Уильям Коли привил пациентам с неоперабельными опухолями [ Streptococcus pyogenes ]». [4] «Коли [был] тщательно просмотрел имеющуюся на тот момент литературу и нашел 38 сообщений о больных раком со случайной или ятрогенной лихорадочной рожей . У 12 пациентов саркома или карцинома полностью исчезли; у остальных состояние значительно улучшилось. Коли решил попытаться терапевтическое использование ятрогенной рожи...» [5] «Коли разработал токсин, который содержал убитые нагреванием бактерии [ Streptococcus pyogenes и Serratia marcescens ]. До 1963 года этот метод лечения использовался для лечения саркомы». [4] «Коли ввел более 1000 больных раком бактерии или бактериальные продукты». [6] 51,9% пациентов [Коли] с неоперабельными саркомами мягких тканей показали полную регрессию опухоли и выжили более 5 лет, а у 21,2% пациентов не было клинических признаков опухоли по крайней мере через 20 лет после этого лечения... « [4] Исследования продолжались в 20 веке под руководством Марии О'Коннор Хорнунг в Медицинской школе Тулейна [7] [8]
Существует несколько типов иммунотерапии, используемых для лечения рака: [9] [10]
Иммунотерапию можно разделить на активную и пассивную в зависимости от ее способности воздействовать на иммунную систему хозяина против рака. [11] [12] Активная иммунотерапия специфически воздействует на опухолевые клетки через иммунную систему. Примеры включают терапевтические вакцины против рака (также известные как лечебные вакцины, [13] которые предназначены для усиления иммунной системы организма для борьбы с раком), CAR-T-клетки и таргетную терапию антителами. Напротив, пассивная иммунотерапия не воздействует напрямую на опухолевые клетки, но повышает способность иммунной системы атаковать раковые клетки. Примеры включают ингибиторы контрольных точек и цитокины .
Активная клеточная терапия направлена на уничтожение раковых клеток путем распознавания отдельных маркеров, известных как антигены . Целью противораковых вакцин является создание иммунного ответа на эти антигены с помощью вакцины. В настоящее время одобрена только одна вакцина ( сипулейцел-Т от рака простаты). При клеточно-опосредованной терапии, такой как терапия CAR-T-клетками, иммунные клетки извлекаются из организма пациента, подвергаются генетической инженерии для распознавания опухолеспецифических антигенов и возвращаются пациенту. Типы клеток, которые можно использовать таким образом, включают естественные клетки-киллеры (NK) , активированные лимфокинами клетки-киллеры , цитотоксические Т-клетки и дендритные клетки . Наконец, можно разработать специфические антитела, которые распознают раковые клетки и нацеливают их на уничтожение иммунной системой. Примеры таких антител включают ритуксимаб (нацеленный на CD-20), трастузумаб (нацеленный на HER-2) и цетуксимаб (нацеленный на EGFR).
Терапия пассивными антителами направлена на повышение активности иммунной системы без специфического воздействия на раковые клетки. Например, цитокины напрямую стимулируют иммунную систему и повышают иммунную активность. Ингибиторы контрольных точек нацелены на белки ( иммунные контрольные точки ), которые обычно ослабляют иммунный ответ. Это повышает способность иммунной системы атаковать раковые клетки. Текущие исследования идентифицируют новые потенциальные цели для улучшения иммунной функции. К одобренным ингибиторам контрольных точек относятся такие антитела, как ипилимумаб , ниволумаб и пембролизумаб .

Терапия дендритными клетками провоцирует противоопухолевые реакции, заставляя дендритные клетки представлять опухолевые антигены лимфоцитам, что активирует их, побуждая их убивать другие клетки, презентирующие антиген. Дендритные клетки представляют собой антигенпрезентирующие клетки (АПК) иммунной системы млекопитающих. [14] При лечении рака они помогают нацеливаться на раковые антигены. [15] Единственной одобренной клеточной терапией рака, основанной на дендритных клетках, является сипулейцел-Т .
Одним из методов стимулирования дендритных клеток к представлению опухолевых антигенов является вакцинация аутологичными опухолевыми лизатами [16] или короткими пептидами (небольшими частями белка, которые соответствуют белковым антигенам на раковых клетках). Эти пептиды часто назначаются в сочетании с адъювантами ( высокоиммуногенными веществами) для усиления иммунного и противоопухолевого ответа. Другие адъюванты включают белки или другие химические вещества, которые привлекают и/или активируют дендритные клетки, такие как гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF). Наиболее распространенными источниками антигенов, используемых для дендритно-клеточной вакцины при глиобластоме (ГБМ) как агрессивной опухоли головного мозга, были лизат цельной опухоли, РНК антигена ЦМВ и опухолеассоциированные пептиды, такие как EGFRvIII . [17]
Дендритные клетки также можно активировать in vivo , заставляя опухолевые клетки экспрессировать GM-CSF. Этого можно достичь либо путем генной инженерии опухолевых клеток для производства GM-CSF, либо путем инфицирования опухолевых клеток онколитическим вирусом, экспрессирующим GM-CSF.
Другая стратегия — удалить дендритные клетки из крови пациента и активировать их вне организма. Дендритные клетки активируются в присутствии опухолевых антигенов, которые могут представлять собой один опухолеспецифический пептид/белок или лизат опухолевых клеток (раствор разрушенных опухолевых клеток). Эти клетки (с необязательными адъювантами) вводятся и вызывают иммунный ответ.
Терапия дендритных клеток включает использование антител, которые связываются с рецепторами на поверхности дендритных клеток. Антигены могут быть добавлены к антителу и могут индуцировать созревание дендритных клеток и обеспечить иммунитет к опухоли. В качестве мишеней антител использовались рецепторы дендритных клеток, такие как TLR3 , TLR7 , TLR8 или CD40 . [15] Интерфейс дендритных клеток и NK-клеток также играет важную роль в иммунотерапии. Разработка новых стратегий вакцинации на основе дендритных клеток должна также учитывать эффективность стимуляции NK-клеток. Крайне важно систематически включать мониторинг NK-клеток в качестве результата в противоопухолевые клинические исследования на основе ДК. [ нужна цитата ]
Сипулейцел-Т (Provenge) был одобрен для лечения бессимптомного или минимально симптоматического метастатического кастрационно-резистентного рака простаты в 2010 году. Лечение заключается в удалении антигенпрезентирующих клеток из крови с помощью лейкафереза и выращивании их с помощью слитого белка PA2024, полученного из ГМ- СМЖ и простатспецифическая кислая фосфатаза простаты (ПАР) и реинфузия. Этот процесс повторяется три раза. [18] [19] [20] [21]

Адоптивная Т-клеточная терапия представляет собой форму пассивной иммунизации путем переливания Т-клеток. Они обнаруживаются в крови и тканях и обычно активируются при обнаружении чужеродных патогенов . Активация происходит, когда поверхностные рецепторы Т-клеток сталкиваются с клетками, которые отображают части чужеродных белков (либо на своей поверхности, либо внутриклеточно). Это могут быть как инфицированные клетки, так и другие антигенпрезентирующие клетки (АПК). Последние обнаруживаются в нормальной ткани и в опухолевой ткани, где они известны как инфильтрирующие опухоль лимфоциты (TIL). Они активируются присутствием АПК, таких как дендритные клетки, которые представляют опухолевые антигены . Хотя эти клетки могут атаковать опухоли, микроокружение опухоли обладает сильным иммунодепрессивным действием, препятствуя иммуноопосредованной гибели опухоли. [22]
Было разработано множество способов получения Т-клеток, разрушающих опухоли. Чаще всего Т-клетки, специфичные к опухолевому антигену, можно удалить из образца опухоли (TIL) или отфильтровать из крови. Т-клетки можно дополнительно модифицировать различными способами, культивировать и вводить пациентам. Т-клетки можно модифицировать с помощью генной инженерии, производя CAR-T-клетки или TCR-Т-клетки, или подвергая Т-клетки воздействию опухолевых антигенов в неиммуносупрессивной среде, которые они распознают как чужеродные и учатся атаковать.
Другой подход — передача гаплоидентичных γδ Т-клеток или естественных клеток-киллеров от здорового донора. [23] Основным преимуществом этого подхода является то, что эти клетки не вызывают реакцию «трансплантат против хозяина» . Недостатком является то, что перенесенные клетки часто имеют нарушенную функцию. [24]
Самый простой пример включает удаление TIL из опухоли, их культивирование, но не модификацию, и введение результата обратно в опухоль. Первая терапия этого типа, Лифилеуцел , получила одобрение FDA в феврале 2024 года.
Суть иммунотерапии CAR-T заключается в модификации Т-клеток для распознавания раковых клеток с целью их нацеливания и уничтожения. Ученые собирают Т-клетки у людей, генетически изменяют их, добавляя химерный антигенный рецептор (CAR), который специфически распознает раковые клетки, а затем вводят полученные CAR-T-клетки пациентам, чтобы атаковать их опухоли.
Тисагенлеклейцел (Кимрия), терапия химерными антигенными рецепторами (CAR-T), была одобрена FDA в 2017 году для лечения острого лимфобластного лейкоза (ОЛЛ). [25] Это лечение удаляет CD19- положительные клетки (В-клетки) из организма (включая больные клетки, а также нормальные клетки, продуцирующие антитела).
Axicabtagene ciloleucel ( Yescarta ) — еще один терапевтический препарат CAR-T, одобренный в 2017 году для лечения диффузной крупноклеточной B-клеточной лимфомы (DLBCL). [26]
Многофункциональные альгинатные каркасы для инженерии и высвобождения Т-клеток (MASTER) — это метод инженерии in situ , репликации и высвобождения генно-инженерных Т-клеток. Это эволюция CAR-Т-клеточной терапии. Т-клетки извлекаются из организма пациента и смешиваются с генно-инженерным вирусом, содержащим ген, нацеленный на рак (как в случае с CAR T). Затем смесь добавляют к МАСТЕРУ (каркасу), который их поглощает. МАСТЕР содержит антитела , которые активируют Т-клетки, и интерлейкины , запускающие пролиферацию клеток. Затем МАСТЕР имплантируется пациенту. Активированные Т-клетки взаимодействуют с вирусами, превращаясь в CAR-Т-клетки. Интерлейкины стимулируют пролиферацию этих CAR T-клеток, и CAR T-клетки выходят из MASTER, чтобы атаковать рак. Техника занимает часы, а не недели. А поскольку клетки моложе, они дольше сохраняются в организме, демонстрируют более высокую эффективность против рака и имеют меньше признаков истощения. Эти возможности были продемонстрированы на моделях мышей. Лечение было более эффективным и длительным в отношении лимфомы . [27] [28]
Т-клеточная терапия с использованием Т-клеточных рецепторов (TCR-T) — это тип адоптивной Т-клеточной терапии , нацеленной на некоторые виды рака. В терапии TCR-T используются гетеродимеры , состоящие из альфа- и бета- пептидных цепей, для распознавания молекул полипептидных фрагментов , представленных MHC . В отличие от CAR-T, который использует антигены клеточной поверхности, TCR-T может распознавать больший набор внутриклеточных антигенных фрагментов MHC. Однако терапия TCR-T-клетками зависит от молекул MHC, что ограничивает ее полезность. [29] [30]
TCR каждой Т-клетки специфичен к одному антигену и находится на поверхности Т-клетки. Сродство TCR человека к опухолевым антигенам относительно низкое, что делает их неспособными эффективно распознавать и уничтожать опухолевые клетки. Модифицированные Т-клетки обладают гораздо более высоким сродством, что усиливает как распознавание, так и сродство, поддерживающее распознавание опухолевых клеток. [29]
По состоянию на 2021 год ни один метод лечения TCR-T не получил одобрения регулирующих органов. [29]
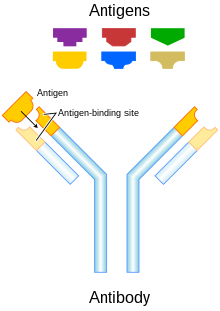
При лечении рака используются два типа: [32]
Способность Fc связывать рецепторы Fc важна, поскольку она позволяет антителам активировать иммунную систему. Fc-области разнообразны: они существуют в многочисленных подтипах и могут быть дополнительно модифицированы, например, с добавлением сахаров в процессе, называемом гликозилированием . Изменения в области Fc могут изменить способность антитела взаимодействовать с рецепторами Fc и, в более широком смысле, будут определять тип иммунного ответа, который вызывает антитело. [35] Например, блокаторы иммунных контрольных точек , нацеленные на PD-1, представляют собой антитела, предназначенные для связывания PD-1, экспрессируемого Т-клетками, и реактивации этих клеток для устранения опухолей . [36] Препараты против PD-1 содержат не только Fab-область, которая связывает PD-1, но и Fc-область. Экспериментальные работы показывают, что Fc-часть препаратов для иммунотерапии рака может влиять на результат лечения. Например, препараты против PD-1 с областями Fc, которые связывают ингибирующие рецепторы Fc, могут иметь пониженную терапевтическую эффективность. [37] Визуализирующие исследования также показали, что Fc-область препаратов против PD-1 может связывать Fc-рецепторы, экспрессируемые опухолеассоциированными макрофагами. Этот процесс удаляет лекарства из их намеченных целей (т.е. молекул PD-1, экспрессируемых на поверхности Т-клеток) и ограничивает терапевтическую эффективность. [38] Кроме того, антитела, нацеленные на костимулирующий белок CD40, требуют взаимодействия с селективными рецепторами Fc для оптимальной терапевтической эффективности. [39] В совокупности эти исследования подчеркивают важность статуса Fc в стратегиях нацеливания на иммунные контрольные точки на основе антител.
Антитела могут происходить из различных источников, включая клетки человека, мышей и их комбинацию (химерные антитела). Различные источники антител могут провоцировать разные виды иммунных реакций. Например, иммунная система человека может распознавать мышиные антитела (также известные как мышиные антитела) и запускать против них иммунный ответ. Это может снизить эффективность лечения антителами и вызвать иммунную реакцию. Химерные антитела пытаются снизить иммуногенность мышиных антител путем замены части антитела соответствующим человеческим аналогом. Гуманизированные антитела почти полностью человеческие; только области, определяющие комплементарность вариабельных областей , получены из мышиных источников. Человеческие антитела были произведены с использованием немодифицированной человеческой ДНК. [33]

Антителозависимая клеточно-опосредованная цитотоксичность (ADCC) требует, чтобы антитела связывались с поверхностями клеток-мишеней. Антитела состоят из связывающей области (Fab) и области Fc, которые могут быть обнаружены клетками иммунной системы через их поверхностные рецепторы Fc . Рецепторы Fc обнаружены на многих клетках иммунной системы, включая NK-клетки. Когда NK-клетки сталкиваются с клетками, покрытыми антителами, Fc-области последних взаимодействуют с их Fc-рецепторами, высвобождая перфорин и гранзим B, чтобы убить опухолевую клетку. Примеры включают ритуксимаб , офатумумаб , элотузумаб и алемтузумаб . Разрабатываемые антитела изменили регионы Fc, которые имеют более высокое сродство к определенному типу рецептора Fc, FcγRIIIA, что может значительно повысить эффективность. [40] [41]
Многие опухолевые клетки сверхэкспрессируют CD47 , чтобы избежать иммунонадзора иммунной системы хозяина. CD47 связывается со своим рецепторным сигнально-регуляторным белком альфа (SIRPα) и подавляет фагоцитоз опухолевых клеток. [42] Таким образом, анти-CD47-терапия направлена на восстановление клиренса опухолевых клеток. Кроме того, все больше данных подтверждают использование Т-клеточного ответа , специфичного для опухолевого антигена , в ответ на терапию анти-CD47. [43] [44] В настоящее время разрабатывается ряд терапевтических средств, в том числе антитела против CD47 , сконструированные рецепторы-ловушки , антитела против SIRPα и биспецифические агенты. [43] По состоянию на 2017 год в клинических испытаниях проходил широкий спектр солидных и гематологических злокачественных новообразований. [43] [45]

Углеводные антигены на поверхности клеток могут быть использованы в качестве мишеней для иммунотерапии. GD2 представляет собой ганглиозид , обнаруженный на поверхности многих типов раковых клеток, включая нейробластому , ретинобластому , меланому , мелкоклеточный рак легких , опухоли головного мозга , остеосаркому , рабдомиосаркому , саркому Юинга , липосаркому , фибросаркому , лейомиосаркому и другие саркомы мягких тканей . Обычно он не экспрессируется на поверхности нормальных тканей, что делает его хорошей мишенью для иммунотерапии. По состоянию на 2014 год клинические испытания продолжались. [46]
В систему комплемента входят белки крови, которые могут вызывать гибель клеток после связывания антитела с поверхностью клетки ( классический путь комплемента , среди способов активации комплемента). Обычно система имеет дело с чужеродными патогенами, но при раке ее можно активировать с помощью терапевтических антител. Система может быть активирована, если антитело является химерным, гуманизированным или человеческим; при условии, что он содержит Fc-область IgG1 . Комплемент может привести к гибели клеток за счет активации мембраноатакующего комплекса , известного как комплементзависимая цитотоксичность ; усиление антителозависимой клеточно-опосредованной цитотоксичности ; и CR3-зависимая клеточная цитотоксичность. Комплементзависимая цитотоксичность возникает, когда антитела связываются с поверхностью раковой клетки, комплекс C1 связывается с этими антителами, и впоследствии в мембране раковой клетки образуются белковые поры . [47]
Блокировка
Терапия антителами также может действовать, связываясь с белками и физически блокируя их взаимодействие с другими белками. Ингибиторы контрольных точек (CTLA-4, PD-1 и PD-L1) действуют по этому механизму. Короче говоря, ингибиторы контрольных точек — это белки, которые обычно помогают замедлить иммунные реакции и предотвратить атаку иммунной системы на нормальные клетки. Ингибиторы контрольных точек связывают эти белки и мешают им нормально функционировать, что повышает активность иммунной системы. Примеры включают дурвалумаб , ипилимумаб , ниволумаб и пембролизумаб .
Алемтузумаб (Campath-1H) представляет собой гуманизированное моноклональное антитело IgG1 против CD52, предназначенное для лечения резистентного к флударабину хронического лимфоцитарного лейкоза (ХЛЛ), кожной Т-клеточной лимфомы , периферической Т-клеточной лимфомы и Т-клеточного пролимфоцитарного лейкоза . CD52 обнаруживается на >95% лимфоцитов периферической крови (как Т-клеток, так и В-клеток) и моноцитов , но его функция в лимфоцитах неизвестна. Он связывается с CD52 и инициирует его цитотоксический эффект за счет фиксации комплемента и механизмов ADCC. Из-за мишени антител (клеток иммунной системы) частыми осложнениями терапии алемтузумабом являются инфекция, токсичность и миелосупрессия . [65] [66] [67]
Дурвалумаб (Имфинзи) представляет собой моноклональное антитело человеческого иммуноглобулина G1 каппа (IgG1κ), которое блокирует взаимодействие лиганда 1 запрограммированной гибели клеток (PD-L1) с молекулами PD-1 и CD80 (B7.1). Дурвалумаб одобрен для лечения пациентов с местно-распространенным или метастатическим уротелиальным раком, у которых:
16 февраля 2018 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов одобрило дурвалумаб для пациентов с неоперабельным немелкоклеточным раком легких III стадии (НМРЛ), у которых заболевание не прогрессировало после одновременной химиотерапии на основе платины и лучевой терапии. [68]
Ипилимумаб («Ервой») представляет собой человеческое антитело IgG1 , связывающее поверхностный белок CTLA4 . В нормальной физиологии Т-клетки активируются двумя сигналами: связыванием рецептора Т-клетки с комплексом антиген - MHC и связыванием поверхностного рецептора Т-клетки CD28 с белками CD80 или CD86 . CTLA4 связывается с CD80 или CD86, предотвращая связывание CD28 с этими поверхностными белками и, следовательно, отрицательно регулируя активацию Т-клеток. [69] [70] [71] [72]
Активные цитотоксические Т-клетки необходимы иммунной системе для атаки клеток меланомы. Обычно ингибированные активные цитотоксические Т-клетки, специфичные для меланомы, могут вызывать эффективный противоопухолевый ответ. Ипилимумаб может вызывать сдвиг соотношения регуляторных Т-клеток к цитотоксическим Т-клеткам, усиливая противоопухолевый ответ. Регуляторные Т-клетки ингибируют другие Т-клетки, что может принести пользу опухоли. [69] [70] [71] [72]
Ниволумаб представляет собой человеческое антитело IgG4 , которое предотвращает инактивацию Т-клеток путем блокирования связывания лиганда 1 запрограммированной гибели клеток 1 или лиганда 2 запрограммированной гибели клеток 1 (PD-L1 или PD-L2), белка, экспрессируемого раковыми клетками, с PD- 1 , белок, обнаруженный на поверхности активированных Т-клеток. [73] [74] Ниволумаб используется при распространенной меланоме, метастатическом почечно-клеточном раке, распространенном раке легких, распространенном раке головы и шеи и лимфоме Ходжкина. [75]
Офатумумаб представляет собой человеческое антитело IgG1 второго поколения , которое связывается с CD20 . Он используется при лечении хронического лимфоцитарного лейкоза (ХЛЛ), поскольку раковые клетки ХЛЛ обычно представляют собой B-клетки, экспрессирующие CD20. В отличие от ритуксимаба , который связывается с большой петлей белка CD20, офатумумаб связывается с отдельной маленькой петлей. Это может объяснить их различные характеристики. По сравнению с ритуксимабом офатумумаб индуцирует комплементзависимую цитотоксичность в более низких дозах и с меньшей иммуногенностью . [76] [77]
По состоянию на 2019 год пембролизумаб , который блокирует PD-1 , белок 1 запрограммированной гибели клеток, использовался посредством внутривенной инфузии для лечения неоперабельной или метастатической меланомы , метастатического немелкоклеточного рака легких (НМРЛ) в определенных ситуациях в качестве препарата второй линии. лечение плоскоклеточного рака головы и шеи (HNSCC), после химиотерапии на основе платины , а также для лечения взрослых и детей с рефрактерной классической лимфомой Ходжкина (кЛХ). [78] [79] Он также показан некоторым пациентам с уротелиальной карциномой , раком желудка и раком шейки матки . [80]
Ритуксимаб представляет собой химерное моноклональное антитело IgG1, специфичное к CD20, разработанное на основе исходного антитела ибритумомаба . Как и ибритумомаб, ритуксимаб воздействует на CD20, что делает его эффективным при лечении некоторых В-клеточных злокачественных новообразований. К ним относятся агрессивные и индолентные лимфомы, такие как диффузная крупноклеточная В-клеточная лимфома и фолликулярная лимфома, а также лейкозы , такие как В-клеточный хронический лимфоцитарный лейкоз . Хотя функция CD20 относительно неизвестна, CD20 может быть кальциевым каналом , участвующим в активации B-клеток. Механизм действия антитела заключается в первую очередь в индукции ADCC и цитотоксичности, опосредованной комплементом. Другие механизмы включают апоптоз [ необходимы разъяснения ] и остановку клеточного роста. Ритуксимаб также повышает чувствительность раковых B-клеток к химиотерапии. [81] [82] [83] [84] [85]

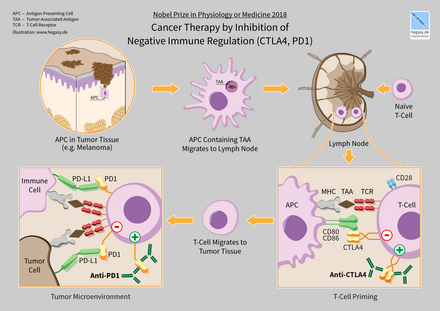
Контрольные точки иммунитета влияют на функцию иммунной системы. Контрольные точки иммунитета могут быть стимулирующими или тормозящими. Опухоли могут использовать эти контрольные точки для защиты от атак иммунной системы. Терапия контрольных точек, одобренная в 2012 году, блокирует ингибирующие рецепторы контрольных точек. Таким образом, блокада передачи сигналов отрицательной обратной связи иммунным клеткам приводит к усилению иммунного ответа против опухолей. [74] По состоянию на 2020 год методы блокады иммунных контрольных точек имеют различную эффективность. При лимфоме Ходжкина и Т-клеточной лимфоме естественных киллеров уровень ответа высок – 50–60%. Однако уровень ответа на лечение рака молочной железы и простаты довольно низок. [86] Основной проблемой являются большие различия в ответах на ингибиторы иммуноконтрольных точек: у некоторых пациентов наблюдаются впечатляющие клинические ответы, в то время как у других не наблюдается никаких положительных эффектов. Было предложено множество возможных причин отсутствия эффективности у многих пациентов, но биомедицинскому сообществу еще предстоит найти консенсус в этом отношении. Например, в недавней статье документально подтверждено, что инфекция Helicobacter pylori может отрицательно влиять на действие ингибиторов иммуноконтрольных точек при раке желудка [87] , но это мнение было быстро оспорено другими. [88]
Одним из исследуемых взаимодействий лиганд-рецептор является взаимодействие между трансмембранным белком запрограммированной гибели клеток 1 (PDCD1, PD-1; также известным как CD279) и его лигандом, лигандом 1 PD-1 (PD-L1, CD274). PD-L1 на поверхности клетки связывается с PD1 на поверхности иммунных клеток, что ингибирует активность иммунных клеток. Среди функций PD-L1 ключевая регуляторная роль в активности Т-клеток. Похоже, что (опосредованная раком) активация PD-L1 на поверхности клеток может ингибировать Т-клетки, которые в противном случае могли бы атаковать. PD-L1 на раковых клетках также ингибирует FAS- и интерферон-зависимый апоптоз, защищая клетки от цитотоксических молекул, продуцируемых Т-клетками. Антитела, которые связываются либо с PD-1, либо с PD-L1 и, следовательно, блокируют взаимодействие, могут позволить Т-клеткам атаковать опухоль. [89]
Первым антителом контрольной точки, одобренным FDA, был ипилимумаб , одобренный в 2011 году для лечения меланомы. [90] Он блокирует молекулу иммунного контрольного пункта CTLA-4 . По состоянию на 2012 год клинические испытания также показали некоторые преимущества терапии анти-CTLA-4 при раке легких или раке поджелудочной железы , особенно в сочетании с другими препаратами. [91] [92] В текущих исследованиях комбинация блокады CTLA-4 с ингибиторами PD-1 или PD-L1 тестируется на различных типах рака. [93]
Однако по состоянию на 2015 год известно, что пациенты, получающие блокаду контрольных точек (в частности, антитела, блокирующие контрольные точки) или комбинацию антител, блокирующих контрольные точки, подвергаются высокому риску возникновения нежелательных явлений, связанных с иммунной системой, таких как дерматологические, желудочно-кишечные, эндокринные или печеночные аутоиммунные реакции. [73] Это, скорее всего, связано с широтой индуцированной активации Т-клеток при введении антител против CTLA-4 путем инъекции в кровоток.
Интересно, что когортное исследование использования ICI во время беременности в 2024 году не выявило завышенных данных о специфических побочных эффектах на беременность, плод и/или новорожденного. [94]
Используя мышиную модель рака мочевого пузыря, исследователи обнаружили, что местная инъекция низкой дозы анти-CTLA-4 в область опухоли имела такую же способность ингибировать опухоль, как и при доставке антитела в кровь. [95] В то же время уровни циркулирующих антител были ниже, что позволяет предположить, что местное применение терапии анти-CTLA-4 может привести к меньшему количеству побочных эффектов. [95]
Первоначальные результаты клинических испытаний ниволумаба с антителом IgG4 PD1 были опубликованы в 2010 году. [74] Он был одобрен в 2014 году. Ниволумаб одобрен для лечения меланомы, рака легких, рака почки, рака мочевого пузыря, рака головы и шеи и лимфомы Ходжкина . [96] Клиническое исследование немелкоклеточного рака легких, проведенное в 2016 году, не достигло основной конечной точки для лечения в первой линии, но одобрено FDA для последующих линий терапии. [97]
Пембролизумаб (Кейтруда) — еще один ингибитор PD1, одобренный FDA в 2014 году. Пембролизумаб одобрен для лечения меланомы и рака легких. [96]
Антитело BGB-A317 является ингибитором PD-1 (разработанным для того, чтобы не связываться с гамма-рецептором Fc I) на ранних клинических испытаниях. [98]
В мае 2016 г. ингибитор PD-L1 атезолизумаб [99] был одобрен для лечения рака мочевого пузыря.
Антитела против PD-L1, находящиеся в настоящее время в разработке, включают авелумаб [100] и дурвалумаб [101] в дополнение к ингибирующему аффимеру . [102]
Многие онкологические больные не реагируют на блокаду иммунных контрольных точек. Частоту ответа можно повысить, сочетая это с дополнительными методами лечения, в том числе теми, которые стимулируют инфильтрацию Т-клеток. Например, таргетная терапия, такая как лучевая терапия, агенты, воздействующие на сосуды, и иммуногенная химиотерапия [107] могут улучшить реакцию блокады иммунных контрольных точек на животных моделях.
Сочетание иммунотерапии, такой как ингибиторы PD1 и CTLA4, может привести к устойчивому ответу. [108] [109]
Комбинаторная абляция и иммунотерапия усиливают иммуностимулирующий ответ и оказывают синергетический эффект при лечении метастатического рака. [110]
Сочетание иммунотерапии контрольных точек с фармацевтическими агентами может улучшить ответ и по состоянию на 2018 год являлось целью клинических исследований. [111] Иммуностимулирующие препараты, такие как ингибиторы CSF-1R и агонисты TLR , оказались эффективными. [112] [113]
Два независимых клинических исследования 2024 года показали, что комбинации ингибиторов JAK с иммунотерапией против PD-1 могут повысить эффективность. В ходе исследования фазы 2 эта комбинация изучалась в качестве терапии первой линии при метастатическом немелкоклеточном раке легких. Назначение итацитиниба после лечения пембролизумабом улучшило терапевтический ответ. В отдельном исследовании фазы 1/2 с участием пациентов с рецидивирующей/рефрактерной лимфомой Ходжкина сочетали руксолитиниб и ниволумаб , что дало улучшенную клиническую эффективность у пациентов, у которых ранее не удалась иммунотерапия с блокадой контрольных точек. [114]
Цитокины — это белки, продуцируемые многими типами клеток, присутствующих в опухоли. Они могут модулировать иммунные реакции. Опухоль часто использует их, чтобы позволить себе расти и снижать иммунный ответ. Эти иммуномодулирующие эффекты позволяют использовать их в качестве лекарств, вызывающих иммунный ответ. Двумя наиболее часто используемыми цитокинами являются интерфероны и интерлейкины. [115]
Интерлейкин-2 и интерферон -α представляют собой цитокины, белки, которые регулируют и координируют поведение иммунной системы. Они обладают способностью усиливать противоопухолевую активность и, таким образом, могут использоваться в качестве пассивного лечения рака. Интерферон-α используется при лечении волосатоклеточного лейкоза , саркомы Капоши, связанной со СПИДом , фолликулярной лимфомы , хронического миелолейкоза и злокачественной меланомы . Интерлейкин-2 используется при лечении злокачественной меланомы и почечно-клеточного рака . [116]
Интерфероны вырабатываются иммунной системой. Они обычно участвуют в противовирусной реакции, но также могут использоваться при раке. Они делятся на три группы: тип I (IFNα и IFNβ), тип II (IFNγ) и тип III (IFNλ). IFNα был одобрен для использования при волосатоклеточном лейкозе , саркоме Капоши, связанной со СПИДом, фолликулярной лимфоме, хроническом миелолейкозе и меланоме. Интерфероны I и II типов были широко исследованы, и хотя оба типа способствуют противоопухолевому воздействию на иммунную систему, клинически эффективны только IFN I типа. IFNλ демонстрирует многообещающие противоопухолевые эффекты на животных моделях . [117] [118]
В отличие от IFN типа I, гамма-интерферон еще не одобрен для лечения рака. Однако улучшение выживаемости наблюдалось при назначении гамма-интерферона пациентам с раком мочевого пузыря и меланомой . Наиболее многообещающий результат достигнут у пациенток со 2 и 3 стадией рака яичников . Исследование IFN-гамма in vitro в раковых клетках является более обширным, и результаты указывают на антипролиферативную активность IFN-gamma, приводящую к ингибированию роста или гибели клеток, обычно индуцируемой апоптозом , но иногда и аутофагией . [119]
Интерлейкины оказывают множество эффектов на иммунную систему. Интерлейкин-2 используется при лечении злокачественной меланомы и почечно-клеточного рака . В нормальной физиологии он стимулирует как эффекторные Т-клетки, так и Т-регуляторные клетки, но точный механизм его действия неизвестен. [115] [120]
Из-за высокой стоимости многих иммунотерапевтических препаратов и нежелания медицинских страховых компаний вносить предоплату за их рецепты были предложены различные методы тестирования, чтобы попытаться спрогнозировать эффективность этих препаратов. В некоторых случаях FDA одобрило генетические тесты для лекарств, специфичных для определенных генетических маркеров. Например, FDA одобрило лекарство, связанное с BRAF, для лечения метастатической меланомы, которое будет назначаться пациентам после тестирования на генетическую мутацию BRAF. [121]
По состоянию на 2018 год обнаружение белка PD-L1 казалось признаком рака, чувствительного к нескольким иммунотерапевтическим препаратам, но исследования показали, что как отсутствие этого белка, так и его включение в раковую ткань были неубедительными из-за малоизученной различные количества белка в разное время и в разных местах внутри инфицированных клеток и тканей. [122] [123] [124]
В 2018 году были обнаружены некоторые генетические признаки, такие как мутационная нагрузка опухоли (TMB, количество мутаций в целевой генетической области ДНК раковой клетки) и микросателлитная нестабильность (MSI, количество нарушенных несоответствий ДНК, приводящих к вероятным мутациям). одобрен FDA как хороший индикатор вероятности эффективного лечения некоторых видов рака иммунотерапевтическими препаратами, но исследования все еще продолжаются. [125] [126] По состоянию на 2020 год приоритетность иммунотерапии на основе ТМВ для пациентов все еще оставалась весьма спорной. [127] [128]
Тесты такого типа широко рекламируются для общего лечения рака и являются дорогостоящими. В прошлом некоторые генетические тесты для лечения рака использовались в мошенничествах, таких как скандал с мошенничеством с раком в Университете Дьюка , или назывались мистификациями. [129] [130] [131]
Онколитический вирус – это вирус, который преимущественно заражает и убивает раковые клетки. Поскольку инфицированные раковые клетки разрушаются в результате онколиза , они выделяют новые инфекционные вирусные частицы или вирионы, которые помогают уничтожить оставшуюся опухоль. Считается, что онколитические вирусы не только вызывают прямое разрушение опухолевых клеток, но и стимулируют противоопухолевые иммунные реакции хозяина для долгосрочной иммунотерапии. [132] [133] [134]
Потенциал вирусов как противораковых агентов был впервые осознан в начале двадцатого века, хотя скоординированные исследовательские усилия начались только в 1960-х годах. Ряд вирусов, включая аденовирус , реовирус , корь , вирус простого герпеса , вирус болезни Ньюкасла и вакцину, в настоящее время прошли клинические испытания в качестве онколитических агентов. T-Vec — первый онколитический вирус , одобренный FDA для лечения меланомы. Ряд других онколитических вирусов находится на стадии разработки II-III. [135]
Определенные соединения, содержащиеся в грибах , в первую очередь полисахариды , могут стимулировать иммунную систему и обладать противораковыми свойствами. Например, в лабораторных исследованиях было показано, что бета-глюканы , такие как лентинан, стимулируют макрофаги , NK-клетки , Т-клетки и цитокины иммунной системы , а также исследовались в клинических испытаниях в качестве иммунологических адъювантов . [136]
Многие опухоли экспрессируют мутации. Эти мутации потенциально создают новые целевые антигены (неоантигены) для использования в Т-клеточной иммунотерапии. Присутствие CD8+ Т-клеток в раковых поражениях, выявленное с помощью данных секвенирования РНК, выше в опухолях с высокой мутационной нагрузкой. Уровень транскриптов, связанных с цитолитической активностью естественных клеток-киллеров и Т-клеток, положительно коррелирует с мутационной нагрузкой во многих опухолях человека. У пациентов с немелкоклеточным раком легкого, получавших ламбролизумаб, мутационная нагрузка демонстрирует сильную корреляцию с клиническим ответом. У пациентов с меланомой, получавших ипилимумаб, долгосрочный эффект также связан с более высокой мутационной нагрузкой, хотя и менее значимо. Предсказанные MHC-связывающие неоантигены у пациентов с долгосрочной клинической пользой были обогащены рядом тетрапептидных мотивов, которые не были обнаружены в опухолях пациентов с отсутствием или минимальной клинической пользой. [137] Однако неоантигены человека, идентифицированные в других исследованиях, не демонстрируют смещения в сторону тетрапептидных сигнатур. [138]
В 1980-х годах Министерство здравоохранения, труда и социального обеспечения Японии одобрило полисахарид К, извлеченный из гриба Coriolus versicolor , для стимуляции иммунной системы пациентов, проходящих химиотерапию. Это пищевая добавка в США и других юрисдикциях. [139]
Здесь мы впервые демонстрируем успешную конъюгацию низкомолекулярного агониста TLR7 с противоопухолевым моноклональным антителом (ритуксимаб против hCD20) без ущерба для специфичности антигена.