Общие анестетики (или анестетики ) часто определяют как соединения, вызывающие потерю сознания у людей или потерю рефлекса выпрямления у животных. Клинические определения также расширены и теперь включают индуцированную кому, вызывающую неосведомленность о болевых раздражителях, достаточную для облегчения хирургического применения в клинической и ветеринарной практике. Общие анестетики не действуют как анальгетики , и их также не следует путать с седативными средствами . Общие анестетики представляют собой структурно разнообразную группу соединений, механизмы действия которых охватывают множество биологических мишеней, участвующих в контроле нейрональных путей. Точная работа является предметом некоторых дискуссий и продолжающихся исследований. [1]
Общие анестетики вызывают состояние общей анестезии . Остается несколько спорным вопрос о том, как следует определять это состояние. [2] Однако общие анестетики обычно вызывают несколько ключевых обратимых эффектов: обездвиженность, анальгезия, амнезия , потеря сознания и снижение вегетативной реакции на вредные раздражители. [2] [3] [4]
Общие анестетики могут вводиться либо в виде газов или паров ( ингаляционные анестетики ), либо в виде инъекций ( внутривенные или даже внутримышечные ). Все эти агенты обладают свойством быть весьма гидрофобными (т.е. в жидком виде они не смешиваются свободно (или смешиваются) с водой, а в виде газов они растворяются в маслах лучше, чем в воде). [3] [5] Анестезия возможна исключительно путем ингаляции или инъекции, но чаще всего эти две формы комбинируются: инъекция вводится для индукции анестезии, а газ используется для ее поддержания. [5]
.jpg/440px-thumbnail.jpg)
Ингаляционные анестетики представляют собой летучие жидкости или газы и обычно вводятся с помощью наркозного аппарата . Наркозный аппарат позволяет составить смесь кислорода, анестетиков и окружающего воздуха, доставить ее пациенту и контролировать параметры пациента и аппарата. Жидкие анестетики испаряются в аппарате. [5]
Многие соединения использовались для ингаляционной анестезии, но лишь некоторые из них до сих пор широко используются. Десфлюран , изофлюран и севофлуран являются наиболее широко используемыми на сегодняшний день летучими анестетиками . Их часто комбинируют с закисью азота . Старые, менее популярные летучие анестетики включают галотан , энфлюран и метоксифлуран . Исследователи также активно изучают возможность использования ксенона в качестве анестетика. [5]
Инъекционные анестетики используются для индукции и поддержания бессознательного состояния. Анестезиологи предпочитают использовать внутривенные инъекции , поскольку они быстрее, менее болезненны и надежнее, чем внутримышечные или подкожные инъекции . Среди наиболее широко используемых препаратов можно выделить:
Бензодиазепины являются седативными средствами и используются в сочетании с другими общими анестетиками. [2] [5]
Индукция и поддержание общей анестезии, а также контроль различных физиологических побочных эффектов обычно достигаются с помощью комбинаторного лекарственного подхода. Отдельные общие анестетики различаются в зависимости от их конкретных физиологических и когнитивных эффектов. Хотя индукцию общей анестезии можно облегчить с помощью одного общего анестетика, другие могут использоваться параллельно или впоследствии для достижения и поддержания желаемого состояния анестезии. Используемый лекарственный подход зависит от процедуры и потребностей медицинских работников. [2]
Предполагается, что общие анестетики оказывают свое действие путем активации тормозных рецепторов центральной нервной системы (ЦНС) и инактивации возбуждающих рецепторов ЦНС . Относительная роль различных рецепторов все еще обсуждается, но существуют доказательства того, что определенные мишени связаны с действием определенных анестетиков и лекарств. [2] [6] [7]
Ниже приведены несколько ключевых целей общих анестетиков, которые, вероятно, опосредуют их эффекты:
Во время введения анестетика получатель проходит различные стадии поведения, в конечном итоге приводящие к потере сознания . Этот процесс ускоряется при внутривенном введении анестетиков настолько, что его нельзя учитывать при их применении. Четыре стадии анестезии описываются с помощью знаков Геделя, обозначающих глубину анестезии. Эти этапы описывают влияние анестезии главным образом на когнитивные функции, мышечную активность и дыхание. [4]
Получатель анестезии сначала чувствует аналгезию , за которой следует амнезия и чувство спутанности сознания, перешедшее на следующую стадию. [4]
Стадия II часто характеризуется бредом, спутанностью сознания и тяжелой амнезией. На этом этапе анестезии часто наблюдаются нарушения в характере дыхания. Тошнота и рвота также являются индикаторами анестезии II стадии. Иногда в результате бреда могут возникать борьба и паника. [4]
Нормальное дыхание возобновляется в начале III стадии. Ближе к концу этапа дыхание полностью прекращается. Показателями III стадии анестезии являются потеря ресничного рефлекса, а также регулярное дыхание. Глубину анестезии III стадии часто можно оценить по движению глаз и размеру зрачка. [4]
На стадии IV дыхание отсутствует. Вскоре за этим следует недостаточность кровообращения и угнетение сосудодвигательных центров . На этой стадии анестезии часто случается смерть, если отсутствует поддержка дыхания и кровообращения. [4]
Помимо клинически выгодных эффектов общих анестетиков, существует ряд других физиологических последствий, опосредованных этим классом препаратов. Примечательно, что снижению артериального давления могут способствовать различные механизмы, включая снижение сократимости сердца и расширение сосудистой сети. Это падение артериального давления может активировать рефлекторное увеличение частоты сердечных сокращений благодаря механизму обратной связи, опосредованному барорецепторами . Однако некоторые анестетики нарушают этот рефлекс. [3] [4]
Пациенты, находящиеся под общей анестезией, подвергаются большему риску развития гипотермии , поскольку вышеупомянутая вазодилатация увеличивает потерю тепла через периферический кровоток. В целом эти препараты снижают порог внутренней температуры тела, при котором запускаются вегетативные механизмы терморегуляции в ответ на холод. (С другой стороны, порог, при котором запускаются механизмы терморегуляции в ответ на тепло, обычно увеличивается.) [9]
Анестетики обычно влияют на дыхание. Ингаляционные анестетики вызывают расширение бронхов , увеличение частоты дыхания и уменьшение дыхательного объема . Конечным эффектом является снижение дыхания, которое должны контролировать медицинские работники, пока пациент находится под общей анестезией. [4] Рефлексы, которые помогают облегчить обструкцию дыхательных путей, также ослабляются (например, рвота и кашель). В сочетании со снижением тонуса нижнего пищеводного сфинктера , что увеличивает частоту срыгиваний, пациенты особенно склонны к асфиксии во время наркоза. Медицинские работники внимательно наблюдают за людьми, находящимися под общим наркозом, и используют ряд устройств, таких как эндотрахеальная трубка , для обеспечения безопасности пациентов. [3]
Общие анестетики также влияют на триггерную зону хеморецепторов и рвотный центр ствола мозга , вызывая тошноту и рвоту после лечения. [3]
Общие анестетики, вводимые внутривенно, обычно представляют собой небольшие и высоко липофильные молекулы. Эти характеристики способствуют их быстрому преимущественному распространению в головном и спинном мозге, которые обладают высокой васкуляризацией и липофильностью. Именно здесь действие этих препаратов приводит к индукции общей анестезии. [3]
После распределения в центральной нервной системе (ЦНС) анестетик диффундирует из ЦНС в мышцы и внутренние органы, а затем в жировую ткань . У пациентов, получивших однократную инъекцию препарата, такое перераспределение приводит к прекращению общей анестезии. Таким образом, после однократного болюсного введения анестетика продолжительность действия препарата зависит исключительно от кинетики перераспределения. [3]
Однако период полувыведения анестезирующего препарата после длительной инфузии зависит как от кинетики перераспределения препарата, метаболизма препарата в печени, так и от существующей концентрации препарата в жире. Когда большие количества анестетика уже растворены в жировых запасах организма, это может замедлить его перераспределение из головного и спинного мозга, продлевая его действие на ЦНС. По этой причине период полураспада этих введенных препаратов считается зависящим от контекста . Как правило, длительные инфузии анестетиков приводят к увеличению периода полувыведения препарата, замедлению выведения из головного и спинного мозга и задержке прекращения общей анестезии. [3]
Минимальная альвеолярная концентрация (МАК) — это концентрация ингаляционного анестетика в легких, которая предотвращает реакцию 50% пациентов на хирургический разрез. Это значение используется для сравнения эффективности различных ингаляционных общих анестетиков и влияет на парциальное давление препарата, используемого медицинскими работниками во время индукции и/или поддержания общей анестезии. [3] [4]
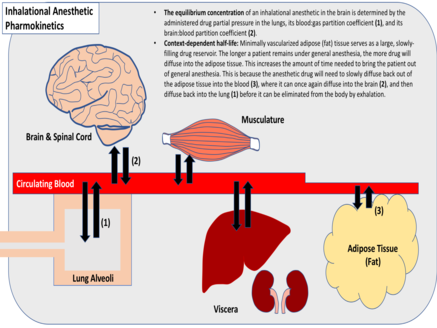
Вводу анестезии способствует диффузия ингаляционного анестетика в головной и спинной мозг. Диффузия по организму продолжается до тех пор, пока парциальное давление лекарства в различных тканях не станет эквивалентным парциальному давлению лекарства в легких. [3] Медицинские работники могут контролировать скорость индукции анестезии и конечную концентрацию анестетика в тканях, изменяя парциальное давление вдыхаемого анестетика. Более высокое парциальное давление лекарства в легких приведет к более быстрой диффузии по всему организму и приведет к более высокой максимальной концентрации в тканях. Частота дыхания и объем вдоха также влияют на скорость начала анестезии, как и степень легочного кровотока. [4]
Коэффициент распределения газообразного лекарственного средства свидетельствует о его относительной растворимости в различных тканях. Этот показатель представляет собой относительную концентрацию лекарства между двумя тканями, когда их парциальные давления равны (газ:кровь, жир:кровь и т. д.). Ингаляционные анестетики широко различаются по растворимости в тканях и коэффициентам распределения. [3] Хорошо растворимые анестетики требуют большого количества молекул лекарственного средства для повышения парциального давления внутри данной ткани, в отличие от минимально растворимых анестетиков, для которых требуется относительно мало молекул. [4] Обычно ингаляционные анестетики с минимальной растворимостью достигают равновесия быстрее. Однако ингаляционные анестетики с высоким коэффициентом распределения жир:кровь достигают равновесия медленнее из-за минимальной васкуляризации жировой ткани, которая служит большим, медленно заполняющимся резервуаром для препарата. [3]
Ингаляционные анестетики выводятся с выдохом после диффузии в легкие. Этот процесс во многом зависит от коэффициента разделения кровь: газ анестетика , растворимости тканей, притока крови к легким, а также частоты дыхания пациента и объема вдоха. [4] Для газов с минимальной растворимостью в тканях прекращение анестезии обычно происходит так же быстро, как и начало анестезии. Однако для газов с высокой растворимостью в тканях прекращение анестезии обычно зависит от контекста . Как и при внутривенных инфузиях анестетиков, длительная доставка хорошо растворимых анестетиков обычно приводит к более длительному периоду полувыведения препарата, замедлению выведения из головного и спинного мозга и задержке прекращения анестезии. [3]
Метаболизм ингаляционных анестетиков обычно не является основным путем выведения препарата. [4]
{{cite book}}: CS1 maint: другие ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )