

Клеточный цикл или цикл клеточного деления — это серия событий, происходящих в клетке , которые заставляют ее делиться на две дочерние клетки. Эти события включают в себя дупликацию его ДНК ( репликация ДНК ) и некоторых его органелл , а затем разделение его цитоплазмы, хромосом и других компонентов на две дочерние клетки в процессе, называемом клеточным делением .
В эукариотических клетках (имеющих клеточное ядро ), включая клетки животных , растений , грибов и простейших , клеточный цикл делится на две основные стадии: интерфазу и митоз в фазе М , который также включает цитокинез . [1] Во время интерфазы клетка растет, накапливая питательные вещества, необходимые для митоза, и реплицирует свою ДНК и некоторые из своих органелл. Во время фазы М реплицированные хромосомы, органеллы и цитоплазма разделяются на две новые дочерние клетки. Чтобы обеспечить правильную репликацию клеточных компонентов и деление, существуют механизмы контроля, известные как контрольные точки клеточного цикла, после каждого из ключевых этапов цикла, которые определяют, может ли клетка перейти к следующей фазе.
В безъядерных клетках прокариотов , бактерий и архей клеточный цикл делится на периоды В, С и D. Период B простирается от окончания деления клетки до начала репликации ДНК. Репликация ДНК происходит в период C. Период D относится к этапу между окончанием репликации ДНК и разделением бактериальной клетки на две дочерние клетки. [2]
В одноклеточных организмах организм воспроизводит себя за один цикл деления клеток. В многоклеточных организмах, таких как растения и животные, серия циклов деления клеток — это то, как организм развивается из одноклеточной оплодотворенной яйцеклетки в зрелый организм, а также процесс, посредством которого волосы , кожа , клетки крови и некоторые внутренние клетки органы регенерируются и излечиваются (за исключением нервов ; см. повреждение нервов ). После деления клеток каждая из дочерних клеток начинает интерфазу нового клеточного цикла. Хотя различные стадии интерфазы обычно не различимы морфологически, каждая фаза клеточного цикла имеет особый набор специализированных биохимических процессов, которые подготавливают клетку к началу клеточного деления.
Эукариотический клеточный цикл состоит из четырех отдельных фаз: фаза G1 , фаза S ( синтез ), фаза G2 (вместе известная как интерфаза ) и фаза М (митоз и цитокинез). Фаза М сама по себе состоит из двух тесно связанных процессов: митоза, при котором делится ядро клетки, и цитокинеза , при котором цитоплазма клетки делится , образуя две дочерние клетки. Активация каждой фазы зависит от правильного развития и завершения предыдущей. Говорят, что клетки, которые временно или обратимо прекратили деление, вошли в состояние покоя, называемое фазой G0 .
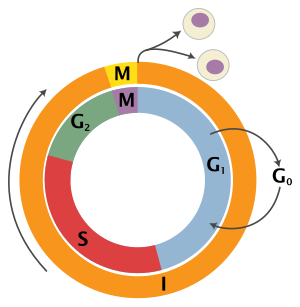
После деления клеток каждая из дочерних клеток начинает интерфазу нового цикла. Хотя различные стадии интерфазы обычно не различимы морфологически, каждая фаза клеточного цикла имеет особый набор специализированных биохимических процессов, которые подготавливают клетку к инициации клеточного деления.

G 0 — фаза покоя, когда клетка вышла из цикла и прекратила делиться. Клеточный цикл начинается с этой фазы. Непролиферативные (неделящиеся) клетки у многоклеточных эукариот обычно переходят в состояние покоя G0 из G1 и могут оставаться в состоянии покоя в течение длительных периодов времени, возможно, бесконечно (как это часто бывает для нейронов ). Это очень характерно для клеток, которые полностью дифференцированы . Некоторые клетки переходят в фазу G0 полупостоянно и считаются постмитотическими, например, некоторые клетки печени, почек и желудка. Многие клетки не входят в G 0 и продолжают делиться на протяжении всей жизни организма, например эпителиальные клетки.
Слово «постмитотический» иногда используется для обозначения как покоящихся , так и стареющих клеток. Клеточное старение происходит в ответ на повреждение ДНК и внешний стресс и обычно представляет собой остановку G1 . Клеточное старение может сделать потомство клетки нежизнеспособным; часто это биохимическая альтернатива самоуничтожению такой поврежденной клетки путем апоптоза .
Интерфаза представляет собой фазу между двумя последовательными фазами М. Интерфаза — это серия изменений, происходящих во вновь образовавшейся клетке и ее ядре, прежде чем она снова станет способна делиться. Его еще называют подготовительной фазой или интермитозом. Обычно интерфаза длится не менее 91% от общего времени, необходимого для клеточного цикла.
Интерфаза протекает в три стадии: G 1 , S и G 2 , за которыми следует цикл митоза и цитокинеза. Содержимое ядерной ДНК клетки дублируется во время S-фазы.

Первая фаза интерфазы, от конца предыдущей М-фазы до начала синтеза ДНК, называется G1 ( G указывает на разрыв ). Ее еще называют фазой роста. Во время этой фазы биосинтетическая деятельность клетки, которая значительно замедляется во время М-фазы, возобновляется с высокой скоростью. Продолжительность G 1 сильно варьирует даже среди разных клеток одного и того же вида. [4] На этом этапе клетка увеличивает запас белков, увеличивает количество органелл (таких как митохондрии, рибосомы) и увеличивается в размерах. В фазе G 1 у клетки есть три варианта.
Решающая точка называется контрольной точкой ( Restriction Point ). Эта контрольная точка называется точкой ограничения или СТАРТ и регулируется циклинами G 1 /S, которые вызывают переход от фазы G 1 к фазе S. Прохождение через контрольную точку G 1 приводит к делению клетки.
Последующая S-фаза начинается, когда начинается синтез ДНК ; когда он завершен, все хромосомы реплицированы , т. е. каждая хромосома состоит из двух сестринских хроматид . Таким образом, во время этой фазы количество ДНК в клетке увеличивается вдвое, хотя плоидность и число хромосом не изменяются. Скорость транскрипции РНК и синтеза белка на этой фазе очень низкая. Исключением является производство гистонов , большая часть которого происходит во время S-фазы. [5] [6] [7]
Фаза G 2 наступает после репликации ДНК и представляет собой период синтеза белка и быстрого роста клеток для подготовки клетки к митозу. Во время этой фазы микротрубочки начинают реорганизовываться в веретено (препрофаза). Прежде чем перейти к митотической фазе , клетки необходимо проверить в контрольной точке G2 на наличие повреждений ДНК внутри хромосом. Контрольная точка G2 в основном регулируется опухолевым белком р53 . Если ДНК повреждена, р53 либо восстановит ДНК, либо вызовет апоптоз клетки. Если р53 дисфункционален или мутировал, клетки с поврежденной ДНК могут продолжать клеточный цикл, что приводит к развитию рака.
Относительно короткая фаза М состоит из деления ядра ( кариокинез ). Это относительно короткий период клеточного цикла. Фаза М сложна и строго регулируется. Последовательность событий разделена на фазы, соответствующие завершению одного набора действий и началу следующего. Эти фазы последовательно называются:

Митоз — это процесс, посредством которого эукариотическая клетка разделяет хромосомы в ядре клетки на два идентичных набора в двух ядрах. [8] В процессе митоза пары хромосом конденсируются и прикрепляются к микротрубочкам , которые тянут сестринские хроматиды к противоположным сторонам клетки. [9]
Митоз происходит исключительно в эукариотических клетках, но у разных видов происходит по-разному. Например, клетки животных подвергаются «открытому» митозу, при котором ядерная оболочка разрушается до разделения хромосом, тогда как грибы , такие как Aspergillus nidulans и Saccharomyces cerevisiae ( дрожжи ), подвергаются «закрытому» митозу, при котором хромосомы делятся внутри неповрежденного ядра клетки . . [10]
Сразу за митозом следует цитокинез , который делит ядра, цитоплазму , органеллы и клеточную мембрану на две клетки, содержащие примерно равные доли этих клеточных компонентов. Митоз и цитокинез вместе определяют деление материнской клетки на две дочерние клетки, генетически идентичные друг другу и родительской клетке. Это составляет примерно 10% клеточного цикла.
Поскольку цитокинез обычно происходит в сочетании с митозом, «митоз» часто используется как синоним «М-фазы». Однако во многих клетках митоз и цитокинез происходят отдельно, образуя отдельные клетки с множеством ядер в процессе, называемом эндорепликацией . Это чаще всего встречается среди грибов и слизевиков , но встречается и в различных группах. Даже у животных цитокинез и митоз могут происходить независимо, например, на определенных стадиях эмбрионального развития плодовых мух . [11] Ошибки в митозе могут привести к гибели клеток в результате апоптоза или вызвать мутации , которые могут привести к раку .

Регуляция клеточного цикла включает процессы, имеющие решающее значение для выживания клетки, включая обнаружение и восстановление генетических повреждений, а также предотвращение неконтролируемого деления клеток. Молекулярные события, контролирующие клеточный цикл, упорядочены и направлены; то есть каждый процесс происходит последовательно, и «обратить» цикл невозможно.
Два ключевых класса регуляторных молекул, циклины и циклин-зависимые киназы (CDK), определяют продвижение клетки в клеточном цикле. [12] Леланд Х. Хартвелл , Р. Тимоти Хант и Пол М. Нерс получили в 2001 году Нобелевскую премию по физиологии и медицине за открытие этих центральных молекул. [13] Многие гены, кодирующие циклины и CDK, консервативны среди всех эукариот, но в целом более сложные организмы имеют более сложные системы контроля клеточного цикла, которые включают больше отдельных компонентов. Многие из соответствующих генов были впервые идентифицированы при изучении дрожжей, особенно Saccharomyces cerevisiae ; [14] генетическая номенклатура дрожжей называет многие из этих генов cdc (от «цикла деления клеток»), за которым следует идентификационный номер, например, cdc25 или cdc20 .
Циклины образуют регуляторные субъединицы, а CDK — каталитические субъединицы активированного гетеродимера ; циклины не обладают каталитической активностью, а CDK неактивны в отсутствие партнерского циклина. При активации связанным циклином CDK выполняют общую биохимическую реакцию, называемую фосфорилированием , которая активирует или инактивирует целевые белки для организации скоординированного перехода в следующую фазу клеточного цикла. Различные комбинации циклин-CDK определяют целевые нижестоящие белки. CDK конститутивно экспрессируются в клетках, тогда как циклины синтезируются на определенных стадиях клеточного цикла в ответ на различные молекулярные сигналы. [15]
При получении промитотического внеклеточного сигнала комплексы G1 циклин -CDK становятся активными, подготавливая клетку к S-фазе, способствуя экспрессии факторов транскрипции , которые, в свою очередь, способствуют экспрессии S-циклинов и ферментов, необходимых для репликации ДНК . Комплексы G1 циклин-CDK также способствуют деградации молекул, которые действуют как ингибиторы S-фазы, направляя их на убиквитинирование . После убиквитинирования белка он подвергается протеолитической деградации с помощью протеасомы . Однако результаты недавнего исследования динамики транскрипции E2F на уровне отдельных клеток показывают, что роль активности G1 циклин-CDK, в частности циклина D-CDK4/6, заключается в настройке времени, а не в обеспечении вступления в клеточный цикл. . [16]
Активные комплексы S-циклин-CDK фосфорилируют белки, которые составляют пререпликационные комплексы , собранные во время фазы G 1 в точках начала репликации ДНК . Фосфорилирование служит двум целям: активировать каждый уже собранный пререпликационный комплекс и предотвратить образование новых комплексов. Это гарантирует, что каждая часть генома клетки будет реплицирована один и только один раз. Причина предотвращения пробелов в репликации довольно ясна: дочерние клетки, в которых отсутствуют все или часть важнейших генов, погибнут. Однако по причинам, связанным с эффектом количества копий генов , наличие дополнительных копий определенных генов также вредно для дочерних клеток.
Митотические комплексы циклин-CDK, которые синтезируются, но инактивируются во время фаз S и G2 , способствуют инициации митоза путем стимуляции нижестоящих белков, участвующих в конденсации хромосом и сборке митотического веретена . Критическим комплексом, активируемым во время этого процесса, является убиквитинлигаза, известная как комплекс, способствующий анафазе (APC), который способствует деградации структурных белков, связанных с хромосомными кинетохорами . APC также нацелен на деградацию митотических циклинов, обеспечивая возможность продолжения телофазы и цитокинеза. [17]
Циклин D — это первый циклин, вырабатываемый в клетках, которые вступают в клеточный цикл в ответ на внеклеточные сигналы (например, факторы роста ). Уровни циклина D остаются низкими в покоящихся клетках, которые не пролиферируют. Кроме того, CDK4/6 и CDK2 также неактивны, поскольку CDK4/6 связываются членами семейства INK4 (например, p16), ограничивая киназную активность. Между тем, комплексы CDK2 ингибируются белками CIP/KIP, такими как p21 и p27. [18] Когда приходит время клетке войти в клеточный цикл, который запускается митогенными митогенными стимулами, уровни циклина D увеличиваются. В ответ на этот триггер циклин D связывается с существующим CDK4 /6, образуя активный комплекс циклин D-CDK4/6. Комплексы циклин D-CDK4/6, в свою очередь, монофосфорилируют белок восприимчивости ретинобластомы ( Rb ) до pRb. Нефосфорилированный опухолевый супрессор Rb вызывает выход клеточного цикла и поддерживает арест G0 (старение). [19]
В последние несколько десятилетий получила широкое признание модель, согласно которой белки pRB инактивируются посредством фосфорилирования, опосредованного циклином D-Cdk4/6. Rb имеет более 14 потенциальных сайтов фосфорилирования. Циклин D-Cdk 4/6 постепенно фосфорилирует Rb до гиперфосфорилированного состояния, что запускает диссоциацию комплексов pRB- E2F , тем самым индуцируя экспрессию генов клеточного цикла G1/S и переход в S-фазу. [20]
Однако научные наблюдения недавнего исследования показывают, что Rb присутствует в трех типах изоформ: (1) нефосфорилированный Rb в состоянии G0; (2) монофосфорилированный Rb, также называемый «гипофосфорилированным» или «частично» фосфорилированным Rb в раннем состоянии G1; и (3) неактивный гиперфосфорилированный Rb в позднем состоянии G1. [21] [22] [23 ] ] В ранних клетках G1 монофосфорилированный Rb выходит в виде 14 различных изоформ, каждая из которых имеет различное сродство к связыванию E2F . [23] Было обнаружено, что Rb связывается с сотнями различных белков [24] и идея о том, что разные монофосфорилированные Rb Изоформы Rb имеют разные партнерские белки. [25] Недавний отчет подтвердил, что монофосфорилирование контролирует ассоциацию Rb с другими белками и генерирует функциональные различные формы Rb. [26] Все различные монофосфорилированные изоформы Rb ингибируют транскрипционную программу E2F и способны арестовывать клетки в G1-фазе.Важно, что различные монофосфорилированные формы Rb имеют разные транскрипционные выходы, выходящие за рамки регуляции E2F. [26]
В общем, связывание pRb с E2F ингибирует экспрессию гена-мишени E2F некоторых генов перехода G1/S и S, включая циклины E-типа . Частичное фосфорилирование Rb де-репрессирует Rb-опосредованное подавление экспрессии гена-мишени E2F, начинает экспрессию циклина E. Молекулярный механизм, который вызывает переключение клетки на активацию циклина E, в настоящее время неизвестен, но по мере повышения уровня циклина E образуется активный комплекс циклин E-CDK2, в результате чего Rb инактивируется путем гиперфосфорилирования. [23] Гиперфосфорилированный Rb полностью диссоциирует от E2F, что обеспечивает дальнейшую экспрессию широкого спектра генов-мишеней E2F, необходимых для перехода клеток в S-фазу [1]. Недавно было идентифицировано, что циклин D-Cdk4/6 связывается с C-концевой областью альфа-спирали Rb, которая отличима только от циклина D, а не от других циклинов, циклинов E , A и B. [27] Это наблюдение, основанное на структурном анализе фосфорилирования Rb, подтверждает, что Rb фосфорилируется на разных уровнях посредством множества комплексов Cyclin-Cdk. Это также делает возможной текущую модель одновременной переключающей инактивации всех монофосфорилированных изоформ Rb посредством одного типа механизма гиперфосфорилирования Rb. Кроме того, мутационный анализ специфичной для циклина D-Cdk 4/6 С-концевой спирали Rb показывает, что нарушение связывания циклина D-Cdk 4/6 с Rb предотвращает фосфорилирование Rb, останавливает клетки в G1 и усиливает функции Rb в качестве супрессора опухоли. . [27] Этот переходный механизм клеточного цикла, управляемый циклином-Cdk, управляет клеткой, вступающей в клеточный цикл, который обеспечивает клеточную пролиферацию. Рост раковых клеток часто сопровождается нарушением регуляции активности Cyclin D-Cdk 4/6.
Гиперфосфорилированный Rb диссоциирует от комплекса E2F/DP1/Rb (который был связан с генами, чувствительными к E2F , эффективно «блокируя» их транскрипцию), активируя E2F. Активация E2F приводит к транскрипции различных генов, таких как циклин E , циклин A , ДНК-полимераза , тимидинкиназа и т. д. Полученный таким образом циклин E связывается с CDK2 , образуя комплекс циклин E-CDK2, который переводит клетку из G 1 в S-фазу. (G 1 /S, который инициирует переход G 2 /M). [28] Активация комплекса циклин B -cdk1 вызывает разрушение ядерной оболочки и инициацию профазы , а затем его дезактивация приводит к выходу клетки из митоза. [15] Количественное исследование динамики транскрипции E2F на уровне отдельных клеток с использованием сконструированных флуоресцентных репортерных клеток обеспечило количественную основу для понимания логики контроля входа в клеточный цикл, бросив вызов канонической модели учебника. Гены, которые регулируют амплитуду накопления E2F, такие как Myc, определяют участие в клеточном цикле и вход в S-фазу. Активность G1-циклина-CDK не является движущей силой входа в клеточный цикл. Вместо этого они в первую очередь регулируют время увеличения E2F, тем самым модулируя темп прогрессирования клеточного цикла. [16]

Два семейства генов, семейство cip /kip ( белок , взаимодействующий с CDK/белок, ингибирующий киназу ) и семейство INK4a/ARF ( ингибитор киназы 4/ альтернативная рамка чтения ) , предотвращают прогрессирование клеточного цикла . Поскольку эти гены играют важную роль в предотвращении образования опухолей , они известны как опухолевые супрессоры .
Семейство cip / kip включает гены p21 , p27 и p57 . Они останавливают клеточный цикл в фазе G1 путем связывания и инактивации комплексов циклин-CDK. p21 активируется p53 (который, в свою очередь, запускается повреждением ДНК, например, вследствие радиации). p27 активируется трансформирующим фактором роста β ( TGF β ), ингибитором роста.
Семейство INK4a/ARF включает p16 INK4a , который связывается с CDK4 и останавливает клеточный цикл в фазе G1 , и p14 ARF , который предотвращает деградацию p53.
Синтетические ингибиторы Cdc25 также могут быть полезны для остановки клеточного цикла и, следовательно, в качестве противоопухолевых и противораковых средств. [29]
Многие виды рака человека обладают гиперактивированной активностью Cdk 4/6. [30] Учитывая наблюдения за функциями циклина D-Cdk 4/6, ингибирование Cdk 4/6 должно привести к предотвращению пролиферации злокачественной опухоли. Следовательно, ученые попытались изобрести синтетический ингибитор Cdk4/6, поскольку Cdk4/6 считается терапевтической мишенью для достижения противоопухолевой эффективности. Три ингибитора Cdk4/6 — палбоциклиб , рибоциклиб и абемациклиб — в настоящее время получили одобрение FDA для клинического применения для лечения поздней стадии или метастатического гормон -рецептор-положительного (HR-положительного, HR+) и HER2-негативного (HER2-) рака молочной железы. . [31] [32] Например, палбоциклиб является перорально активным ингибитором CDK4/6, который продемонстрировал улучшение результатов при ER-положительном/HER2-негативном распространенном раке молочной железы. Основным побочным эффектом является нейтропения , которую можно купировать путем снижения дозы. [33]
Таргетная терапия Cdk4/6 будет лечить только те виды рака, где экспрессируется Rb. Раковые клетки с потерей Rb обладают первичной устойчивостью к ингибиторам Cdk4/6.
Имеющиеся данные свидетельствуют о том, что полуавтономная транскрипционная сеть действует совместно с механизмом CDK-циклина, регулируя клеточный цикл. Несколько исследований экспрессии генов у Saccharomyces cerevisiae выявили 800–1200 генов, экспрессия которых меняет экспрессию в течение клеточного цикла. [14] [34] [35] Они транскрибируются на высоких уровнях в определенные моменты клеточного цикла и остаются на более низких уровнях на протяжении остальной части цикла. Хотя набор выявленных генов различается в разных исследованиях из-за вычислительных методов и критериев, используемых для их идентификации, каждое исследование показывает, что большая часть генов дрожжей регулируется во времени. [36]
Многие периодически экспрессируемые гены управляются транскрипционными факторами , которые также периодически экспрессируются. Один скрининг нокаутов одного гена выявил 48 факторов транскрипции (около 20% всех несущественных факторов транскрипции), которые демонстрируют дефекты прогрессирования клеточного цикла. [37] Полногеномные исследования с использованием высокопроизводительных технологий выявили факторы транскрипции, которые связываются с промоторами генов дрожжей, а корреляция этих результатов с временными паттернами экспрессии позволила идентифицировать факторы транскрипции, которые управляют фазоспецифической экспрессией генов. [34] [38] Профили экспрессии этих факторов транскрипции определяются факторами транскрипции, пик которых приходится на предыдущую фазу, а вычислительные модели показали, что CDK-автономная сеть этих факторов транскрипции достаточна для создания устойчивых колебаний в экспрессия генов). [35] [39]
Экспериментальные данные также свидетельствуют о том, что экспрессия генов может колебаться в зависимости от периода, наблюдаемого при делении клеток дикого типа, независимо от механизма CDK. Орландо и др. использовали микрочипы для измерения экспрессии набора из 1271 гена, который они идентифицировали как периодический как в клетках дикого типа, так и в клетках, лишенных всех S-фазы и митотических циклинов ( clb1,2,3,4,5,6 ). Из 1271 проанализированного гена 882 продолжали экспрессироваться в клетках с дефицитом циклина в то же время, что и в клетках дикого типа, несмотря на то, что клетки с дефицитом циклина арестовываются на границе между G 1 и S фазой . Однако 833 из исследованных генов изменили поведение клеток дикого типа и мутантных клеток, что указывает на то, что эти гены, вероятно, прямо или косвенно регулируются механизмом CDK-циклин. Некоторые гены, которые продолжали вовремя экспрессироваться в мутантных клетках, также экспрессировались на разных уровнях в мутантных клетках и клетках дикого типа. Эти данные свидетельствуют о том, что, хотя транскрипционная сеть может колебаться независимо от осциллятора CDK-циклин, они связаны таким образом, что требуется и то, и другое, чтобы гарантировать правильное время событий клеточного цикла. [35] Другая работа показывает, что фосфорилирование , посттрансляционная модификация факторов транскрипции клеточного цикла с помощью Cdk1 , может изменить локализацию или активность факторов транскрипции, чтобы жестко контролировать время срабатывания генов-мишеней. [37] [40] [41]
Хотя осциллирующая транскрипция играет ключевую роль в развитии дрожжевого клеточного цикла, механизм CDK-циклина работает независимо на раннем эмбриональном клеточном цикле. До перехода мидбластулы зиготическая транскрипция не происходит , и все необходимые белки, такие как циклины B-типа, транслируются с материнской мРНК . [42]
Анализ синхронизированных культур Saccharomyces cerevisiae в условиях, которые предотвращают инициацию репликации ДНК без задержки прогрессирования клеточного цикла, показал, что лицензирование происхождения снижает экспрессию генов с происхождением вблизи их 3'-концов, показывая, что нижестоящие источники происхождения могут регулировать экспрессию вышестоящих генов. [43] Это подтверждает предыдущие предсказания математического моделирования глобальной причинной координации между активностью начала репликации ДНК и экспрессией мРНК, [44] [45] [46] и показывает, что математическое моделирование данных микрочипов ДНК можно использовать для правильного предсказания ранее неизвестных биологические способы регуляции.
Контрольные точки клеточного цикла используются клеткой для мониторинга и регулирования хода клеточного цикла. [47] Контрольные точки предотвращают развитие клеточного цикла в определенных точках, позволяя проверять необходимые фазовые процессы и восстанавливать повреждения ДНК . Ячейка не может перейти к следующему этапу, пока не будут выполнены требования контрольной точки. Контрольные точки обычно состоят из сети регуляторных белков, которые контролируют и определяют продвижение клетки на различных стадиях клеточного цикла.
Подсчитано, что в нормальных клетках человека около 1% одноцепочечных повреждений ДНК преобразуются примерно в 50 эндогенных двухцепочечных разрывов ДНК на клетку за клеточный цикл. [48] Хотя такие двухцепочечные разрывы обычно восстанавливаются с высокой точностью, считается, что ошибки в их восстановлении вносят значительный вклад в уровень заболеваемости раком у людей. [48]
Существует несколько контрольных точек, гарантирующих, что поврежденная или неполная ДНК не перейдет в дочерние клетки. Существуют три основные контрольные точки: контрольная точка G 1 /S, контрольная точка G 2 /M и контрольная точка метафазы (митотическая). Еще одна контрольная точка — это контрольная точка Go, в которой ячейки проверяются на зрелость. Если клетки не смогут пройти эту контрольную точку, поскольку еще не готовы, они будут исключены из деления.
Переход G 1 /S является этапом, ограничивающим скорость клеточного цикла, и также известен как точка ограничения . [15] Здесь клетка проверяет, достаточно ли у нее сырья для полной репликации своей ДНК (нуклеотидных оснований, ДНК-синтазы, хроматина и т. д.). Нездоровая или истощенная клетка застрянет на этом контрольно-пропускном пункте.
Контрольная точка G 2 /M — это точка, где клетка гарантирует, что у нее достаточно цитоплазмы и фосфолипидов для двух дочерних клеток. Но иногда, что более важно, он проверяет, подходящее ли сейчас время для репликации. В некоторых ситуациях всем клеткам необходимо реплицироваться одновременно (например, растущий эмбрион должен иметь симметричное распределение клеток, пока он не достигнет перехода средней бластулы). Это осуществляется путем управления контрольной точкой G 2 /M.
Контрольная точка метафазы является довольно незначительной контрольной точкой: как только клетка находится в метафазе, она начинает митоз. Однако это не значит, что это не важно. В этой контрольной точке клетка проверяет, сформировалось ли веретено и что все хромосомы выровнены по экватору веретена, прежде чем начнется анафаза. [49]
Хотя это три «основные» контрольные точки, не все клетки должны проходить через каждую из этих контрольных точек в указанном порядке для репликации. Многие виды рака вызваны мутациями, которые позволяют клеткам проходить через различные контрольные точки или даже вообще их пропускать. Переход от фазы S к фазе M к фазе S почти последовательно. Поскольку эти клетки потеряли свои контрольные точки, любые мутации ДНК, которые могли возникнуть, игнорируются и передаются дочерним клеткам. Это одна из причин, почему раковые клетки имеют тенденцию экспоненциально приобретать мутации. За исключением раковых клеток, многие полностью дифференцированные типы клеток больше не размножаются, поэтому они покидают клеточный цикл и остаются в G0 до своей смерти. Таким образом устраняется необходимость в сотовых контрольно-пропускных пунктах. Также была предложена альтернативная модель ответа клеточного цикла на повреждение ДНК, известная как контрольная точка пострепликации .
Регуляция контрольных точек играет важную роль в развитии организма. При половом размножении, когда происходит оплодотворение яйцеклетки, когда сперматозоид связывается с яйцеклеткой, он высвобождает сигнальные факторы, которые уведомляют яйцеклетку о том, что она оплодотворена. Среди прочего, это заставляет оплодотворенный ооцит вернуться из своего ранее дремлющего состояния G 0 обратно в клеточный цикл и перейти к митотической репликации и делению.
p53 играет важную роль в запуске механизмов контроля как в G1 / S, так и в G2 / M контрольных точках. Помимо р53, активно исследуются регуляторы контрольных точек на предмет их роли в росте и распространении рака.

Новаторская работа Ацуши Мияваки и его коллег разработала флуоресцентный индикатор клеточного цикла на основе убиквитинирования (FUCCI), который позволяет флуоресцентно визуализировать клеточный цикл. Первоначально зеленый флуоресцентный белок mAG был слит с hGem (1/110), а оранжевый флуоресцентный белок (mKO 2 ) был слит с hCdt1 (30/120). Обратите внимание, что эти слияния представляют собой фрагменты, которые содержат сигнал ядерной локализации и сайты убиквитинирования для деградации , но не являются функциональными белками. Зеленый флуоресцентный белок образуется во время фазы S, G2 или M и разлагается во время фазы G0 или G1 , тогда как оранжевый флуоресцентный белок образуется во время фазы G0 или G1 и разрушается во время S, G2 . , или М-фаза. [50] FUCCI в дальнем красном и ближнем инфракрасном диапазоне был разработан с использованием флуоресцентного белка , полученного из цианобактерий ( smURFP ), и флуоресцентного белка, полученного из бактериофитохрома (фильм можно найти по этой ссылке). [51]
Нарушение регуляции компонентов клеточного цикла может привести к образованию опухоли . [52] Как упоминалось выше, когда некоторые гены, такие как ингибиторы клеточного цикла, RB , p53 и т. д., мутируют, они могут вызвать бесконтрольное размножение клеток, образуя опухоль. Хотя продолжительность клеточного цикла в опухолевых клетках равна или превышает продолжительность нормального клеточного цикла, доля клеток, находящихся в активном клеточном делении (по сравнению с покоящимися клетками в фазе G0 ) , в опухолях намного выше, чем в нормальной ткани. . [53] Таким образом, наблюдается чистое увеличение количества клеток, поскольку количество клеток, умирающих в результате апоптоза или старения, остается прежним.
Клетки, которые активно проходят клеточный цикл, являются целью терапии рака, поскольку ДНК относительно открыта во время клеточного деления и, следовательно, восприимчива к повреждению лекарствами или радиацией . Этот факт используется при лечении рака; с помощью процесса, известного как уменьшение объема , удаляется значительная масса опухоли, что вытесняет значительное количество оставшихся опухолевых клеток из фазы G 0 в фазу G 1 (из-за увеличения доступности питательных веществ, кислорода, факторов роста и т. д.). Лучевая или химиотерапия после процедуры уменьшения объема убивает эти клетки, которые недавно вступили в клеточный цикл. [15]
Самые быстрые циклические клетки млекопитающих в культуре — клетки крипт кишечного эпителия — имеют продолжительность цикла всего от 9 до 10 часов. Стволовые клетки в покоящейся коже мыши могут иметь продолжительность цикла более 200 часов. Большая часть этой разницы обусловлена различной длиной G 1 , наиболее изменчивой фазы цикла. М и S не сильно различаются.
В целом клетки наиболее радиочувствительны в поздних фазах M и G2 и наиболее устойчивы в поздней S-фазе. Для клеток с более длительным временем клеточного цикла и значительно продолжительной фазой G1 имеется второй пик устойчивости в конце G1 . Характер резистентности и чувствительности коррелирует с уровнем сульфгидрильных соединений в клетке. Сульфгидрилы — это природные вещества, которые защищают клетки от радиационного повреждения и имеют тенденцию иметь самые высокие уровни в S и самые низкие вблизи митоза.
Гомологичная рекомбинация (HR) — это точный процесс восстановления двухцепочечных разрывов ДНК . ЧСС практически отсутствует в фазе G1 , наиболее активна в фазе S и снижается в фазе G2 / M. [54] Негомологичное соединение концов , менее точный и более мутагенный процесс восстановления двухцепочечных разрывов, активен на протяжении всего клеточного цикла.
Клеточный цикл должен дублировать все клеточные компоненты и в равной степени разделять их на две дочерние клетки. Многие компоненты, такие как белки и рибосомы , производятся непрерывно на протяжении всего клеточного цикла (за исключением М-фазы ). Однако хромосомы и другие связанные элементы, такие как MTOC , дублируются только один раз в течение клеточного цикла. Центральным компонентом клеточного цикла является его способность координировать непрерывные и периодические дупликации различных клеточных элементов, которые развивались при формировании генома.
Доклеточная среда содержала функциональные и самореплицирующиеся РНК . [55] Все концентрации РНК зависели от концентраций других РНК, которые могли помогать или препятствовать сбору ресурсов. В этой среде рост был просто непрерывным производством РНК. Этим доклеточным структурам пришлось бы бороться с паразитическими РНК, проблемами наследственности и контролем количества копий специфических РНК. [55] [56]
Разделение «геномной» РНК на «функциональную» РНК помогло решить эти проблемы. [57] Слияние нескольких РНК в геном дало матрицу, от которой были отщеплены функциональные РНК. Теперь, чтобы выжить, паразитическим РНК придется внедриться в геном, что является гораздо более серьезным барьером. Контроль количества копий геномной РНК также позволил определять концентрацию РНК через скорость синтеза и период полураспада РНК, а не через конкуренцию. [55] Отделение дупликации геномных РНК от генерации функциональных РНК позволило добиться гораздо большей точности дублирования геномных РНК без ущерба для производства функциональных РНК. Наконец, замена геномной РНК ДНК , которая является более стабильной молекулой, позволила увеличить геномы. Переход от самокаталитического синтеза ферментов к геном-направленному синтезу ферментов стал критическим шагом в эволюции клеток и имел долгосрочные последствия для клеточного цикла, который должен регулировать функциональный синтез и дупликацию генома самыми разными способами. [55]
Развитие клеточного цикла контролируется колебательными концентрациями различных циклинов и возникающими в результате молекулярными взаимодействиями различных циклин-зависимых киназ (CDK). У дрожжей только один CDK (Cdc28 у S. cerevisiae и Cdc2 у S. pombe ) контролирует клеточный цикл. [58] Однако у животных развились целые семейства CDK. [59] [60] Cdk1 контролирует вход в митоз, а Cdk2, Cdk4 и Cdk6 регулируют вход в S-фазу. Несмотря на эволюцию семейства CDK у животных, эти белки имеют родственные или дублирующие функции. [61] [62] [63] Например, клетки мышей с тройным нокаутом cdk2, cdk4, cdk6 все еще могут проходить основной клеточный цикл. [64] Нокаут cdk1 является летальным, что предполагает, что наследственная киназа типа CDK1 в конечном итоге контролирует клеточный цикл. [64]
Arabidopsis thaliana имеет гомолог Cdk1, называемый CDKA;1, однако мутанты cdka;1 A. thaliana все еще жизнеспособны, [65] что противоречит опистоконтному паттерну киназ типа CDK1 как важных регуляторов, контролирующих клеточный цикл. [66] Растения также имеют уникальную группу CDK B-типа, функции которых могут варьироваться от функций, специфичных для развития, до основных участников митотической регуляции. [67] [68]

Контрольная точка G1/S — это точка, в которой клетка совершает деление в течение клеточного цикла. Сложные регуляторные сети приводят к принятию решения о переходе G1/S. У опистоконтов наблюдаются как сильно дивергентные белковые последовательности, так и поразительно схожие топологии сетей. [66] [69]
Вход в S-фазу как у дрожжей, так и у животных контролируется уровнями двух противоположных регуляторов. [66] Сети, регулирующие эти факторы транскрипции , представляют собой петли двойной отрицательной обратной связи и петли положительной обратной связи как у дрожжей, так и у животных. [66] [69] [70] Дополнительная регуляция регуляторной сети контрольной точки G1/S у дрожжей и животных включает фосфорилирование / дефосфорилирование комплексов CDK-циклин. Сумма этих регуляторных сетей создает гистерезисную и бистабильную схему, несмотря на то, что конкретные белки сильно дивергентны. [71] [72] Для дрожжей Whi5 должен быть подавлен фосфорилированием Cln3 для экспрессии SBF, [73] в то время как у животных Rb должен быть подавлен комплексом Cdk4/6-циклин D для экспрессии E2F . [74] И Rb, и Whi5 ингибируют транскрипт посредством привлечения белков гистондеацетилазы к промоторам. [75] [76] Оба белка дополнительно имеют несколько сайтов фосфорилирования CDK, посредством которых они ингибируются. [77] [74] Однако эти белки не имеют сходства последовательностей.
Исследования A. thaliana расширяют наши знания о переходе G1/S у эукариот в целом. Растения также имеют ряд консервативных сетевых особенностей с опистоконтами, и многие растительные регуляторы имеют прямых гомологов животных. [78] Например, растениям также необходимо подавлять Rb для трансляции E2F в сети. [79] Эти консервативные элементы растительных и животных клеточных циклов могут быть предковыми у эукариот. Хотя дрожжи имеют консервативную топологию сети с растениями и животными, сильно различающаяся природа дрожжевых регуляторов предполагает возможную быструю эволюцию по линии дрожжей. [66]